Какие анализы нужно сдать для выявления паразитов в печени
Обновлено: 07.05.2024
Считается, что есть безопасные дозы алкоголя и в интернете можно найти нормы, как будто рекомендуемые всемирной организацией здравоохранения. На самом деле ВОЗ предупреждает, что безопасной дозы алкоголя не существует.
Мы знаем, что есть уровень употребления алкоголя, при котором риск различных недомоганий низкий, однако ВОЗ не устанавливает четких значений для таких доз, медицинские данные свидетельствуют о том, что для здоровья безопаснее не пить. Чем больше человек выпивает, тем выше риск заболеть. Одним из серьезных, но незаметно развивающихся заболеваний печени может стать .алкогольная болезнь печени, которая приводит к циррозу.
Нередко человек просто не догадывается о проблемах с печенью, поскольку этот орган весьма терпелив – и пока основательно не пострадает, старается ничем не выдать имеющихся проблем. Поэтому лучше периодически проверять состояние печени.
Будет ли печень болеть, если превышать безопасную норму употребления алкоголя?
Как не упустить болезнь печени? Какие анализы надо сдавать регулярно?
Лучшее, что мы можем сделать для своей печени, это, не ожидая симптомов, регулярно раз в год сдавать биохимический анализ крови из вены, проверяя уровень билирубина (прямого и общего) и 4-х печеночных ферментов (АСТ, АЛТ, ЩТ и ГГТ). Этот тест - Обследование печени, базовый - позволит оценить токсическое действие вредных веществ на клетки органа. Данное обследование необходимо при подозрении на текущее заболевание печени или при состояниях, связанных как с повреждением самих клеток печени, так и с нарушением оттока желчи.
Расширенный комплекс Обследование печени наиболее целесообразен пациентам с уже имеющимися заболеваниями печени как для оценки текущего состояния, так и для оценки эффективности проводимого лечения. В этот комплекс помимо выше названных анализов входят тест на протромбин, определяется уровень общего белка и белковые фракций, а также оценивается способность печени к синтезу необходимых организму веществ - холинэстеразы и холестерина.
Различных тестов на болезни печени много. Какой анализ самый точный?
Анализы крови на общий, прямой и непрямой билирубин служат важным маркером оценки функции печени. Их обычно назначают при появлении желтухи, а также при подозрении на заболевания печени (например, гепатит).
Аланинаминотрансфераза (АЛТ) – это фермент печеночных клеток. При повреждении клеток печени, уровень АЛТ в крови поднимается. Причем, это происходит задолго до появления желтухи. Существенное (более, чем в 10 раз) повышение уровня АЛТ обычно связано либо с острым вирусным гепатитом, либо с острым токсическим поражением печени. Умеренный рост АЛТ (в несколько раз) характерен для хронических вирусных гепатитов, нарушения оттока желчи и хронических заболеваний гепато-билиарной зоны, а также злоупотребления алкоголем и поражений печени при инфекционных заболеваниях.
Второй фермент–аспартатаминотрансфераза (АСТ) – менее показателен, но важен в комплексной диагностике функции печени. Его обычно назначают вместе с анализом на АЛТ.
Повышение щелочной фосфатазы (ЩФ) может наблюдаться при нарушении оттока желчи и других заболеваниях печени, а также при любых формах холестаза (затруднения желчеотделения).
ГГТ (гамма-глутамилтрансфераза) — фермент, участвующий в метаболизме аминокислот. Его повышенная концентрация в сыворотке крови чаще всего является маркером затруднения оттока желчи, а также интоксикации, вызванной алкоголем или лекарственными препаратами. Анализ крови на ГГТ важен для диагностики многих заболеваний печени.
Почему нет одного теста, для оценки функции печени всегда предлагают сдать комплекс анализов?
На самом деле, очень важно сдавать все анализы в комплексе, потому что важно изменение каждого из показателей в сочетании друг с другом. Например, высокий уровень АСТ может указывать не только на проблемы с печенью, но и на повреждение сердечной мышцы. Или, скажем, одновременное повышение ГГТ и ЩФ позволяет предположить холестаз, но если ГГТ повышается изолированно от ЩФ, то можно заподозрить, что все дело - в длительном употреблении алкоголя. Повышение же ЩФ при нормальных значениях ГГТ скорее говорит не о болезнях печени, а о наличии заболеваний костной ткани.

Диагностика заболеваний почек — довольно сложная задача, поскольку большая часть нефрологических болезней долгое время протекает бессимптомно. Специфические лабораторные тесты позволяют вовремя выявить нарушения работы почек и назначить эффективное лечение.
Какие анализы покажут заболевания почек? Как расшифровать результаты исследований? Читайте об этом в нашей статье!
Для чего нужно обследовать почки?
Почки — орган мочевыделительной системы, который выполняет много важных функций:
- выводит из организма избыток жидкости, органических и неорганических веществ, вредные и токсические соединения;
- секретирует фермент ренин, необходимый для поддержания нормального артериального давления;
- вырабатывает гормон эритропоэтин, контролирующий эритропоэз — процесс образования эритроцитов;
- поддерживает постоянство состава и pH крови;
- участвует в обмене веществ.
Однако при заболеваниях почек функциональность органа снижается, что приводит к изменению нормального состава крови, интоксикации организма и другим патологическим состояниям. Без своевременной диагностики многие нефрологические заболевания приводят к терминальной хронической почечной недостаточности — угрожающему жизни состоянию, при котором требуется заместительная терапия в виде гемодиализа или пересадки почки.
Для диагностики нарушения работы почек существуют специальные лабораторные тесты:
-
на определенные показатели, которые отражают функциональное состояние почек;
- определение скорости клубочковой фильтрации (СКФ), проба Реберга;
- анализы мочи — общий анализ мочи, исследование на микроальбуминурию, проба Зимницкого, анализ мочи по Нечипоренко.
В каких ситуациях назначаются анализы?
Врач может назначить скрининг состояния почек при наличии у пациента симптомов, характерных для почечных патологий. Например, к таким признакам относятся отеки на лице и теле, высокое артериальное давление, тошнота, сниженный диурез. Также поводом для назначения скрининга могут стать сомнительные результаты общего анализа крови, общего анализа мочи и других базовых исследований.
Скрининг показан людям с высокой вероятностью развития заболеваний почек. К ним относятся пациенты с диабетом, системной красной волчанкой, гипертонической болезнью. Также скрининг может быть назначен после приема нефротоксичных препаратов.
Кроме этого, регулярный мониторинг необходим людям с хроническими заболеваниями почек для оценки течения болезни и эффективности лечения.
Почечные показатели биохимического исследования крови
Некоторых показатели биохимического исследования крови позволяют врачу сделать вывод о состоянии почек. Анализ проводится в утренние часы натощак. Подготовка к исследованию заключается в следующем:
- за сутки до забора биологического материала исключается прием алкоголя;
- между взятием крови и последним приемом пищи должно пройти не менее 12 часов;
- за час до сдачи анализа нужно отказаться от курения;
- перед исследованием можно употреблять только воду.
Рассмотрим основные показатели исследования, которые помогают обнаружить заболевания почек.
Креатинин
Вещество, которое образуется в мышечной ткани, далее поступает в кровь и выводится из организма почками. Первостепенной задачей креатинина является обеспечение организма энергией, необходимой для сокращения мышц. Уровень вещества в крови во многом зависит от мышечной массы. Именно поэтому его концентрация в крови у мужчин больше, чем у женщин и детей.
Креатинин относится к беспороговым веществам, которые не подвергаются процессу реабсорбции в почечных канальцах и полностью выводятся мочевыделительной системой при любой их концентрации в крови. При стабильной мышечной нагрузке и хорошей работе почек концентрация его в крови у человека достаточно постоянна. Поэтому уровень креатинина в крови напрямую отражает функциональное состояние почек.
Референсные значения показателя представлены в таблице ⇓⇓⇓
Уровень креатинина, мкмоль/л
Высокий уровень вещества в крови может указывать на следующие заболевания почек:
- острая почечная недостаточность — стремительно развивающееся нарушение функционирования почек;
- хроническая почечная недостаточность — постепенное угасание почечных функций;
- гломерулонефрит — поражение почечных клубочков, которое может быть следствием инфекции или аутоиммунного процесса;
- пиелонефрит — воспалительный процесс в почечных канальцах.
Также причиной высокого показателя может стать обструкция мочеточника, вызванная воспалительным процессом или механическим фактором. Например, обструкция может наблюдаться при мочекаменной болезни. Если камень попадает в мочеточник, то нарушается отток мочи, соответственно уровень креатинина в крови растет.
Высокий уровень показателя не всегда указывает на проблемы с почками. Концентрация вещества в крови повышается при лихорадке, травмах с разрушением тканей, обезвоживании, сильных физических нагрузках, преобладании мясных продуктов в рационе. Также повышенные значения креатинина могут наблюдаться при гипертиреозе, акромегалии, гигантизме.
Низкие значения наблюдаются на ранних сроках беременности, при длительном голодании или отсутствии в рационе мясных продуктов, избыточном содержании воды в организме.
Мочевина
Образование мочевины проходит в несколько этапов:
- При распаде белков образуется аммиак — токсичное для организма вещество.
- Аммиак нейтрализуется клетками печени, превращаясь в мочевину, которая выводится из организма почками.
Данное химическое соединение организм никак не использует, а только избавляется от него. Так как процесс образования мочевины непрерывный, небольшое количество вещества постоянно находится в крови. Референсные значения показателя представлены ниже ⇓⇓⇓

Как правило, повышение уровня мочевины в крови вызывают те же факторы, что и повышение уровня креатинина. А вот низкие показатели чаще всего указывают на патологии печени. Также показатель снижается при нефротическом синдроме, низкобелковой диете, гипергидратации, на ранних сроках беременности.
Мочевая кислота
Образуется в результате обмена пуринов — азотсодержащих веществ, входящих в состав нуклеиновых кислот. Кроме этого, мочевая кислота является результатом переваривания продуктов с высоким содержание пуринов. Большая часть вещества выводится из организма почками, меньшая — желудочно-кишечным трактом. Референсные значения содержания мочевой кислоты в крови представлены в таблице ⇓⇓⇓
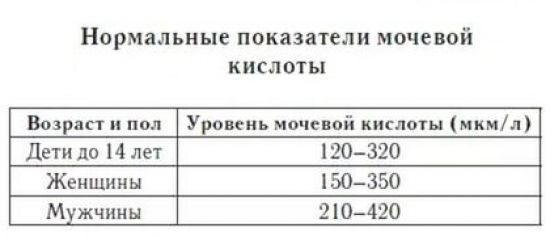
Повышение показателя может быть признаком почечной недостаточности, а также:
- подагры — отложения в тканях кристаллов уратов;
- синдрома Леша-Нихена — наследственной патологии, при которой увеличен синтез мочевой кислоты;
- злокачественных заболеваний кроветворной системы;
- алкогольной интоксикации организма;
- приема мочегонных препаратов;
- преобладания в рационе продуктов, богатых пуринами — рыбы, телятины, субпродуктов, бобовых;
- избыточной физической нагрузки.
Низкий показатель наблюдается при дисфункции почечных канальцев. Например, уровень мочевой кислоты в крови снижается при синдроме Фанкони — наследственном заболевании, которое характеризуется общим нарушением проксимального канальцевого транспорта.
Другие причины низкого показателя — нарушения пуринового обмена, низкопуриновая диета.
Общий белок
Показатель отражает концентрацию всех белков в крови и служит маркером не только почечных патологий, но также заболеваний печени, щитовидной железы и других органов. Референсные значения показателя выглядят следующим образом ⇓⇓⇓
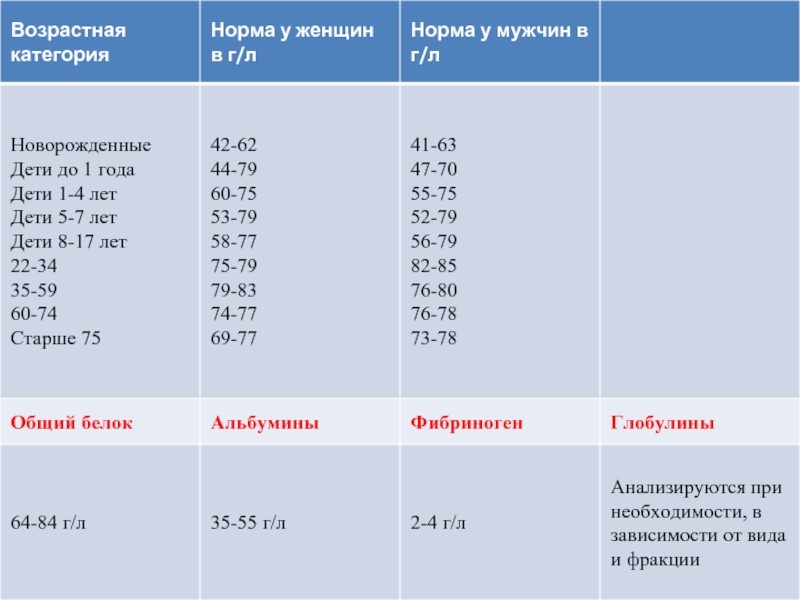
Высокое содержание общего белка в крови наблюдаются при:
- обезвоживании организма;
- острых и хронических инфекционных патологиях;
- аутоиммунных процессах;
- злокачественных образованиях.
Низкие значения показателя могут указывать на гломерулонефрит, нефротический синдром. Кроме этого, концентрация белка в крови снижается при заболеваниях печени, кровотечениях, гиперфункции щитовидной железы, голодании, во время беременности, в период грудного вскармливания.
Скорость клубочковой фильтрации (СКФ), проба Реберга
Нефроны (структурные единицы почки) состоят из почечных клубочков и канальцев. В почечных клубочках происходит первый этап мочеобразования — фильтрация практически всех составляющих плазмы, кроме высокомолекулярных белков и форменных элементов крови. В почечных канальцах происходит обратная реабсорбция некоторых веществ, т.е. канальцевая реабсорбция отражает состояние концентрационной функции почек.
При некоторых патологиях почек этот процесс нарушается.
Для оценки функционального состояния различных отделов нефрона пользуются несколькими методиками: определение СКФ и проведение пробы Реберга. СКФ рассчитывается по специальной формуле, в которой отражаются возраст, пол, масса тела, рост, раса пациента и уровень креатинина в крови конкретного человека.
Проба Реберга — тест отражает несколько показателей: СКФ, канальцевую реабсорбцию и минутный диурез. Существуют несколько вариантов проведения пробы:
Референсные значения клиренса креатинина представлены в таблице, единицы измерения — мл/мин/1,7 м².
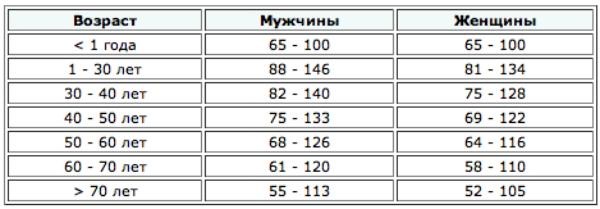
Точность результатов исследования во многом зависит от правильной подготовки. В связи с этим за несколько дней до начала сбора урины нужно исключить:
- сильные физические нагрузки;
- употребление алкогольных напитков, кофеина;
- прием диуретиков, препаратов с содержанием аскорбиновой кислоты.
Также стоит ограничить употребление мясных продуктов.
Какие заболевания позволяет выявить исследование?
- Исследование клубочковой фильтрации имеет важное практическое значение, так как при ряде почечных патологий (хронический гломерулонефрит, волчаночный нефрит, диабетический гломерулосклероз) снижение СКФ является наиболее ранним признаком начинающейся хронической почечной недостаточности.
- Высокие значения СКФ — признак нефротического синдрома, начала развития сахарного диабета, артериальной гипертензии.
- Также показатель может отклоняться от референтных значений по физиологическим причинам. Например, повышение СКФ наблюдается при избытке белков в рационе, приеме диуретиков, обильном употреблении жидкости; снижение — при обезвоживании, при бессолевой диете.
- Снижение канальцевой реабсорбции рано наступает у больных поликистозом почек, при гидронефрозе, пиелонефрите. При заболеваниях почек, сопровождающимися преимущественным поражением клубочков (гломерулонефрит и др.), канальцевая реабсорбция снижается значительно позже, чем клубочковая фильтрация.
Другие лабораторные методы обследования почек
Также для диагностики заболеваний почек применяют такие методы исследования, как анализ мочи на микроальбуминурию, проба Зимницкого, анализ мочи по Нечипоренко.
Анализ на микроальбуминурию проводится для определения наличия в моче альбуминов — простых растворимых в воде белков. При отсутствии заболеваний почек альбумин может попасть в мочу только в следовых количествах.
Повышенная концентрация вещества в моче наблюдается при диабетической, токсической, лекарственной нефропатии, гломерулонефрите, воспалительных процессах в почках. Также альбумин в моче повышается при непереносимости фруктозы, высоком артериальном давлении, некоторых аутоиммунных заболеваниях, сердечной недостаточности, тяжелой физической работе.
Микроальбуминурия может определяться как в утренней, так и в суточной моче. Референсные значения представлены ниже ⇓⇓⇓
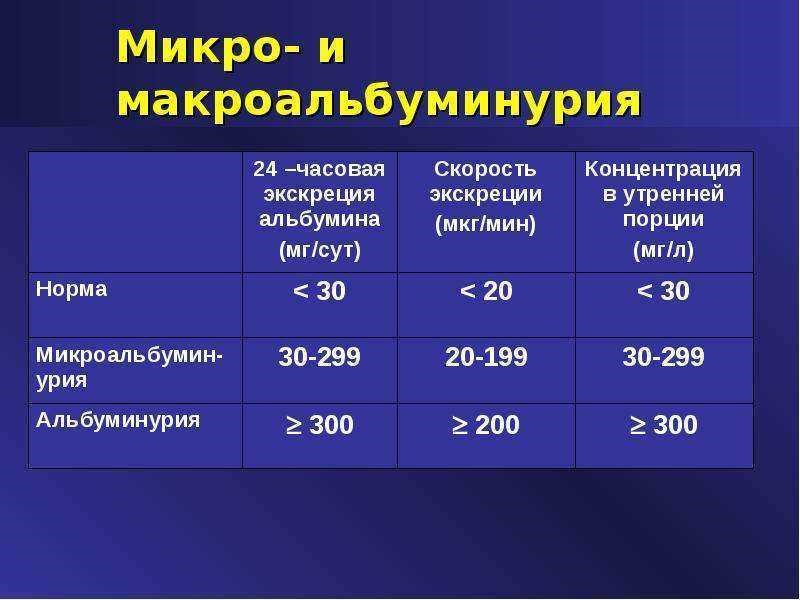
Анализ мочи по Нечипоренко чаще всего назначается, если в общем анализе мочи обнаружены отклонения от референтных значений. Во время исследования определяется количество форменных элементов в 1 мл осадка мочи.
Проба Зимницкого позволяет оценить работу почек в динамике. Биоматериал собирается каждые три часа на протяжении суток.
Более подробную информацию об анализе мочи по Нечипоренко и пробе Зимницкого вы найдете в нашей статье.
Как происходит заражение?
До попадания в организм человека, гельминты и простейшие проходят цикл развития в других средах или живых организмах.
- В почве при определённых условиях температуры и влажности сохраняются яйца и личинки аскарид, стронгилоид, анкилостом Человек заражается при попадании зараженной почвы через грязные руки, воду, непромытые фрукты и овощи, непосредственно с землёй.
- В живых организмах проходят циклы развития следующие гельминты: описторхи (кошачья двуустка), клонорхи, трихинеллы, токсокары, эхинококки, свиной и бычий цепень. До достижения зрелости, чтобы паразитировать в человеке, возможна смена одного или двух промежуточных хозяев. Это моллюски, ракообразные, рыба, насекомые. Употребление термически недостаточно обработанной рыбы и мяса, сырой воды приводит к заражению.
Ещё один путь заражения - при непосредственном контакте людей через рукопожатия, общие предметы гигиены и быта или путем самозаражения. Речь идёт о контагиозных гельминтах: энтеробиоз, стронгилоидоз, цистицеркоз, лямблиоз.
Как можно заподозрить паразитарное заболевание?
Проявления могут быть разнообразными, течение от легкого до тяжёлого. Редко возникают типичные признаки, выдающие конкретного возбудителя. Зачастую признаков нет, или они маскируются под другие заболевания, или исчезают по мере окончания одного цикла развития паразита и начала другого. Например, личинки аскарид сначала попадают в лёгкие человека, где дозревают и мигрируют в кишечник. Ребёнка может беспокоить недолгий кашель (похоже на простуду), не настораживающий родителя.
Тем не менее, обычно выделяют острую и хроническую фазы течения паразитарного заболевания.
Острые проявления возникают вследствие общего воздействия на организм:
- Влияния токсинов – повышение температуры до 37 – 37,5 градусов, слабость, головные боли, снижение настроения и работоспособности, нарушения сна;
- Аллергических реакций – кожный зуд, крапивница, бронхоспазм, одышка, реже отёк Квинке;
- Активации иммунной системы– боли в мышцах и суставах; увеличение лимфоузлов, печени и селезенки
- Механического воздействия – если посмотреть под микроскопом, у каждого гельминта можно увидеть приспособления для закрепления в организме, травмирующие слизистую: зубья, крючья, присоски. В результате возникают боли в животе, частый стул, диспепсия.
Хроническая фаза характеризуется поражением определённых органов и систем. Чаще всего страдает кишечник, длительное механическое воздействие приводит к его воспалению, нарушениям всасывания и переваривания пищи. Развивается анемия, недостаток витаминов и микроэлементов, а у маленьких детей отмечается задержка роста и набора веса. Могут поражаться желчный пузырь и желчевыводящие пути (лямблиоз); сердечно-сосудистая система, лёгкие, нервная система (чаще трихинеллез); лёгкие и печень (эхинококкоз) и так далее. При длительном течении подавляется иммунитет и присоединяются вторичные инфекции.
Если Вы обнаружили любой из перечисленных признаков, сдайте клинический анализ крови с лейкоцитарной формулой. Повышение эозинофилов до 7-10% и более станет ещё одним подозрительным критерием.
Как выявить паразитарное заболевание?
-
, предпочтительнее обогащающий метод – PARASEP Определяет яйца всех видов гельминтов и простейших, обитающих в кишечнике
Следует обратить внимание на следующие моменты:
На что нужно обратить внимание?
- Наличие проявлений и одновременное обнаружение IgG могут свидетельствовать о хронической фазе гельминтоза
- В сомнительных случаях рекомендовано повторное исследование IgG через 2 недели. Нарастание уровня антител в 2 раза и более говорит об активности гельминта
- При трихинеллезе, эхинококкозе, цистицеркозе определение антител – единственный возможный метод лабораторной диагностики, поскольку человек – промежуточный хозяин для данных гельминтов.
Паразитарные заболевания печени – группа разнородных болезней, вызываемых паразитами и гельминтами. Самые распространенные паразитозы печени: аскаридоз, эхинококкоз, амебиаз, описторхоз и др. К общим симптомам относят истощение, дистрофические изменения кожи и волос, повышенную утомляемость, нарушения сна, неприятный запах изо рта. В диагностике используют дуоденальное зондирование, исследование дуоденального содержимого, анализ кала на яйца гельминтов, УЗИ, КТ, сцинтиграфию печени. Лечение консервативное, заключающееся в назначении антипаразитарного препарата (специфического либо широкого спектра действия), либо оперативное.
Общие сведения
Паразитарные заболевания печени вызываются протозоозами и глистными инвазиями. Всемирная организация здравоохранения считает, что не менее 25% населения Земли заражено теми или иными паразитами. Паразитозы и гельминтозы занимают четвертое место среди заболеваний, приносящих наибольший вред здоровью человека. На данный момент не существует исследований, которые бы отражали истинную заболеваемость паразитарными болезнями и гельминтозами в России. По мнению экспертов в области инфекционных заболеваний и гастроэнтерологии, паразитарные инвазии могут быть выявлены не менее чем у двадцати миллионов россиян. Учитывая тот факт, что паразиты и глисты могут персистировать в организме долгие годы, заболевание нередко накладывает отпечаток на всю жизнь: вызывает задержку роста и развития в детском возрасте, ухудшает умственные способности школьников, провоцирует снижение работоспособности и активности взрослого населения.
Причины паразитарных заболеваний печени
Все паразитарные заболевания печени возникают либо при протозойном инфицировании, либо в результате глистной инвазии. Поражение печени в этой ситуации выступает одним из проявлений генерализованной инфекции. Среди протозойных инфекций печень чаще всего поражается при токсоплазмозе, амебиазе, лейшманиозе, малярии. Гельминтозы представлены нематодозами, цестодозами, трематодозами. Нематодозы вызываются круглыми червями (аскаридоз, стронгилоидоз, токсокароз, трихинеллез); трематодозы – сосальщиками (фасциолез, клонорхоз, описторхоз); цестодозы – ленточными глистами (альвеококкоз, эхинококкоз).
Разнообразие клинических проявлений паразитарных заболеваний печени обусловлены не только видом паразита либо гельминта, но и их жизненным циклом, местом внедрения в организм, локализацией различных жизненных форм, реакцией иммунитета на возбудителя.
Сосальщики обычно локализуются в желчевыводящих протоках, желчном пузыре. Присосками сосальщиков повреждается эпителий протоков, в которых образуются кисты, воспалительная реакция, формируется холангит и холестаз. При фасциолезе личинки с током крови проникают в ткань печени, затем мигрируют в желчевыводящие пути и там превращаются в половозрелого паразита. В дальнейшем гельминты повреждают ткань печени, формируя микроскопические гнойники в паренхиме и желчных ходах. Схожий патогенез заболевания имеет и аскаридоз.
При эхинококкозе и амебиазе в печени формируются объемные образования. Шистосомозы приводят к фиброзированию паренхимы печени. Заражение малярийным плазмодием, трипаносомами, шистосомами приводит к значительному увеличению размеров печени, воспалительному процессу, печеночной недостаточности.
Главную роль в поражении печеночной паренхимы играют патологические иммунные реакции. Паразиты и гельминты выделяют антигены, которые провоцируют избыточные иммунные реакции, приводящие к значительному поражению клеток и микрососудов печени. Личинки и взрослые особи глистов, находящиеся в ткани печени, выделяют ряд ферментов, повреждающих гепатоциты и стимулирующих синтез фибрина. Хроническое персистирование паразитов рано или поздно приводит к фиброзированию печени, хронической печеночной недостаточности. Ниже рассмотрены основные виды паразитарных заболеваний печени, встречающиеся в России.
Виды паразитарных заболеваний печени
Эхинококкоз печени
Эхинококкоз занимает ведущее место среди всех паразитарных заболеваний печени. В подавляющем большинстве случаев поражается правая половина печени, практически у половины пациентов эхинококковых кист несколько. У людей эхинококкоз печени может быть гидатидным (личиночная стадия, кистозная форма, человек является промежуточным хозяином) и альвеококковым. Основным хозяином являются псовые, в организме которых эхинококк созревает, а его терминальные членики с огромным количеством яиц попадают в окружающую среду, вызывая заражение человека фекально-оральным либо контактным путем. Попадая в желудок, оболочка яиц растворяется и гельминты проникают через стенку желудка или кишечника в кровь. С током крови возбудители мигрируют в печень, а затем и в другие органы, формируя в них кисты (изначально – около 1 мм диаметром). Эхинококковая киста печени имеет две оболочки, внутренняя продуцирует жидкую составляющую кисты, образует дочерние пузыри. Наружная оболочка может кальцифицироваться, содержимое ее может нагнаиваться. Кисты огромных размеров сдавливают паренхиму печени и сосуды, желчевыводящие пути.
Гидатидный эхинококкоз. В первые годы после заражения эхинококкоз может никак не проявляться. Первые клинические проявления обычно возникают по достижению кистой больших размеров – боли в правом боку, тошнота и рвота, слабость, исхудание, хроническая диарея, аллергические высыпания на коже, ломкость волос. Размеры печени увеличиваются, при поверхностном расположении кисты ее можно даже пропальпировать. Желтуха развивается только при сдавлении кистой протоков печени. Возможен прорыв кистозного образования в брюшную или грудную полость, сопровождающийся сильной болью, анафилактическим шоком (реакция на всасывание содержимого кисты). Нагнаивание содержимого кисты сопровождается болезненностью печени, лихорадкой, ухудшением общего состояния.
Диагностика эхинококкоза включает сбор анамнеза (контакт с собакой), пальпацию печени и выявление эхинококковой кисты. Специфическим методом диагностики является реакция Казони (положительна в 85% случаев), латекс-агглютинации (90%). Визуализировать паразита помогут УЗИ печени и желчного пузыря, ангиография чревного ствола, МРТ печени и желчевыводящих путей, статическая сцинтиграфия печени, диагностическая лапароскопия.
Лечение только оперативное. Производится иссечение эхинококковых кист печени, предварительно в кисту вводят формалин и отсасывают ее содержимое. Полость кисты ушивают наглухо. В последующем может сформироваться непаразитарная киста, гнойник. При маленьких размерах и краевом положении кисты возможна резекция печени вместе с кистой.
Альвеолярный эхинококкоз. Является более редкой формой паразитарного заболевания печени, вызываемого эхинококком. Возбудитель альвеококкоза отличается своей личиночной стадией. Заражение происходит при обработке шкур основного хозяина (лисы и др.), употреблении зараженных продуктов. Особенностью альвеококкоза является образование множества мелких кист, которые инфильтрируют паренхиму печени, плотно прилегая друг к другу и образуя опухолевидный узел в ткани печени. Пузырьки паразита способны прорастать в паренхиму печени, сосуды, желчные пути, соседние органы. В центре очага альвеококкоза формируется некроз, в дальнейшем альвеококковый очаг может обызвествляться. Дифференцировать заболевание следует с раком печени, циррозом печени.
Клиническая картина альвеококкоза сходна с гидатидной формой заболевания, однако имеет большую частоту механической желтухи. Лечение альвеококкоза печени имеет определенные особенности. Проведение операции затруднено инфильтративным ростом паразитов, прорастанием сосудов, желчных путей, круглой связки печени. Обычно операция назначается при значительном поражении печени, нагноении и прорыве кист. Чаще всего производится частичная резекция печени, оставшиеся кисты обрабатываются химиопрепаратами или формалином, подвергаются криодеструкции.
Аскаридоз печени и желчных путей
На сегодняшний день аскаридоз печени встречается достаточно редко. Человек заражается при употреблении в пищу зараженных яйцами аскарид продуктов. Попадая в кишечник, возбудители через кишечную стенку проникают в кровеносное русло, с током крови попадают в печень. В печени из-за персистирования паразитов формируются некрозы, микроабсцессы. В дальнейшем возбудители могут мигрировать по организму, попадая в другие органы и системы, а в кишечнике превращаясь в половозрелые формы.
Основными проявлениями аскаридоза являются холангиты, холестаз, абсцессы печени. Специфических симптомов аскаридоза не существует. Диагноз аскаридоза печени устанавливается на основании обнаружения аскарид и их яиц в рвотных массах, кале; также возможна визуализация гельминтов при УЗИ, КТ печени.
Лечение аскаридоза желчевыводящих путей только хирургическое. Применение противоаскаридозных средств при закупорке желчных путей противопоказано, так как приводит к кратковременной активизации паразитов и их дальнейшему проникновению в желчные пути и паренхиму печени. Для уточнения степени поражения протоков во время операции проводят РХПГ. Для профилактики персистирования аскаридоза, образования конкрементов желательно провести холецистэктомию. В послеоперационном периоде по дренажам вводят антиаскаридозные препараты для уничтожения оставшихся гельминтов.
Описторхоз печени
Данное паразитарное заболевание печени встречается достаточно редко, заражение человека происходит через сырую рыбу, зараженные водоемы. Размножение гельминта в желчных путях приводит к их расширению. Ткань печени становится очень плотной, расширенные внутрипеченочные протоки видны сквозь капсулу печени. Персистирование инвазии приводит к утолщению стенок желчных путей, формированию грубых рубцовых изменений вокруг них, которые напоминают цирроз печени, часто приводят к перфорации желчных протоков и перитониту. Закупорка желчных ходов благоприятствует застою и воспалительным изменениям в них. У пациентов с описторхозом часто в будущем развивает рак печени.
Описторхоз, как и другие паразитарные заболевания печени, не имеет специфической клиники. Частыми проявлениями являются увеличение и уплотнение печени, боли в правом подреберье, жидкий стул. В случае присоединения инфекции пациента беспокоят лихорадка, озноб, липкий пот.
Диагноз ставится на основании выявления особей и яиц гельминтов в кале и дуоденальном соке, полученном при зондировании. Лечение описторхоза печени хирургическое, заключается в дренировании протоков, введении антипаразитарных препаратов в дренажи.
Амебиаз печени
Заболевание часто встречается в тропических странах. Характеризуется преимущественным поражением толстого кишечника, диссеминацией возбудителя в паренхиматозные органы. Цисты амеб попадают в организм человека с зараженной водой, фруктами и овощами, зеленью.
Амебы вызывают образование язв в кишечнике, через которые возбудители попадают в кровоток, а затем в печень, приводя к формированию абсцессов печени примерно в 10% случаев. Особенность амебных абсцессов в том, что они не имеют капсулы, содержат в себе расплавленные ткани, кофейного цвета гной. Состояние пациентов обычно очень тяжелое, печень увеличена и болезненна. Кожные покровы иктерично-серые, сухие.
В диагностике абсцесса печени используют УЗИ гепатобилиарной системы, сцинтиграфию печени, КТ, пункционную биопсию печени (с целью выявления амеб). Лечение амебиаза обычно комплексное: антиамебные, антибактериальные и дезинтоксикационные препараты. Хирургическое лечение проводится при неэффективности консервативных мероприятий, возникновении осложнений.
Прогноз и профилактика паразитарных заболеваний печени
Прогноз при паразитарных заболеваниях печени зависит от многих факторов: длительности паразитарной инвазии, обширности поражения печени, наличия осложнений. При длительном течении паразитарного поражения печени с формированием фиброза, развитием печеночной недостаточности прогноз неблагоприятный.
Профилактика всех паразитарных заболеваний печени заключается в соблюдении правил личной гигиены (мыть руки после контакта с животными, пить только кипяченую воду, тщательно мыть овощи и фрукты перед употреблением в пищу, проводить термическую обработку мяса и рыбы), контроле за состоянием водоемов, из которых производится забор питьевой воды.
Читайте также:

