Кипферон при отравлениях у деток
Обновлено: 10.05.2024
Представлены результаты клинико-лабораторной оценки применения отечественного иммунобиологического препарата,при лечении острых респираторных вирусных инфекций у 120 детей от 6 месяцев до 14 лет. Результаты исследования свидетельствуют о клинико-лабораторной эффективности препарата в отсутствие побочных и аллергических реакций.
Острые респираторные вирусные инфекции (ОРВИ) в педиатрической практике имеют самый большой удельный вес [1, 2]. С учетом частоты распространения вирусных инфекций, тяжести заболевания, возникновения бактериальных осложнений тактика лечения острых респираторных заболеваний у детей систематически совершенствуется. Сложность решения проблемы профилактики и лечения острых респираторных заболеваний связана с множеством инфекционных агентов с преобладающей ролью вирусов [3, 4]. В большинстве наблюдений доказана способность вирусов поражать все отделы органов дыхания с течением заболевания от легких форм до тяжелых и неотложных состояний, к числу последних относят стенозирующий ларинготрахеит и обструктивный бронхит, особенно у детей раннего возраста [5, 6].
В настоящее время в терапии острых респираторных заболеваний перспективным остается применение иммунобиологических препаратов, которые позитивно влияют на специфические механизмы, не только возникающие в ответ на инфекционные агенты, но и обладающие противовирусным и иммуномодулирующим действиями. С учетом частоты распространения вирусных инфекций, возможности затяжного течения и возникновения бактериальных осложнений у детей одним из перспективных направлений в терапии следует признать использование готовых лекарственных форм человеческого рекомбинантного альфа-2b-интерферона, обладающего противовирусным, антибактериальным, иммуномодулирующим и антипролиферативным эффектами [7, 8]. К одним из таких средств относится препарат в форме суппозиториев для вагинального или ректального введения, содержащий достаточно изученные компоненты: человеческий рекомбинантный альфа-2b-интерферон и комплексный иммунобиологический препарат с высоким содержанием специфических иммуноглобулинов (Ig) IgA и IgM – до 15–25 % и IgG – 50 %).
Подобная композиция препарата позволяет одновременно сочетать противовирусное, антибактериальное, иммуномодулирующее воздействие на организм, дополненное введением Ig и антитоксическим влиянием. Оба компонента разрешены к медицинскому применению. Суппозитории имеют цилиндрическую форму белого или светло-бежевого цвета однородной консистенции.
В одной свече содержится не менее 500 тыс. МЕ человеческого рекомбинантного альфа-2β-интерферона и 60 мг комплексного иммунобиологического препарата с содержанием специфических Ig. Показано, что ректальный метод введения препарата по фармакокинетике интерферона сопоставим с внутримышечным [9, 10], а побочные эффекты при этом практически отсутствуют [11].
Суппозитории вводят ректально (преимущественно после акта дефекации): детям до года – по одному суппозиторию в день, от года до 12 лет – по 1 суппозиторию 2 раза в день и детям старше 12 лет – по 1 суппозиторию 3 раза в день. При выраженных клинических проявлениях заболевания и тяжести состояния суточная доза может быть увеличена на один суппозиторий (но не более трех суппозиториев в сутки).
Наиболее эффективно и целесообразно назначение суппозиториев в остром периоде заболевания (желательно в первые 3 дня). Лечение совместимо с общепринятыми средствами патогенетической и этиотропной терапии инфекционных заболеваний у детей.
Длительность курса лечения определяется этиологией, формой тяжести инфекционного заболевания, наличием сопутствующих осложнений и патологических состояний, обычно не превышает 5–10 дней.
Целью настоящего исследования стала оценка клинико-лабораторной эффективности иммунобиологического препарата в комплексном лечении острых респираторных заболеваний у детей.
Проведено исследование 120 детей в возрасте от 6 месяцев до 14 лет с диагнозом ОРВИ, течение которой в 55,8 % случаев сопровождалось острым стенозирующим ларинготрахеитом 1–2-й степени, в 37,5 % – обструктивным бронхитом и в 6,7 % – пневмонией. Отягощенный преморбидный статус отмечен у большинства наблюдавшихся детей: анте- и постнатальный факторы риска (патология беременности и родов) – в 20 % случаев, раннее искусственное вскармливание – в 34 %, пищевая и лекарственная аллергия – в 15 %, частые ОРВИ – в 71,7 %.
Иммунобиологический был назначен 60 больным (основная группа), остальные 60 детей составили группу сравнения. Обе группы были репрезентативны по возрасту, преморбидному статусу, нозологии, степени тяжести и срокам начала терапии. Препарат был включен в комплекс общепринятого лечения, в т.ч. при наличии показаний применялась антибактериальные средства. Препарат вводили ректально в возрастной дозировке курсом 5–7 дней.
Наряду с клиническим наблюдением, детальной регистрацией всех клинических симптомов заболевания в комплекс исследований включили лабораторное исследование крови и мочи, определение биохимических параметров крови, проведение ЭКГ и рентгенографии органов грудной клетки по показаниям.
Этиологическая расшифровка респираторной вирусной инфекции проведена методом люминесцентной микроскопии слизистой носа. Методом иммуноферментного анализа в сыворотке крови определены общие антитела к респираторному синцитиальному вирусу и Pneumocystis carinii, методом реакции иммунофлюоресценции слизистой носа и трахеального секрета обнаружен антиген респираторного синцитиального вируса и антиген P. carinii.
Исследованы уровни интерферона в слюне и сыворотке крови, содержание Ig классов А, М и G в сыворотке крови, качественный и количественный состав аспирата трахеи в динамике.
Статистическая обработка данных выполнена с использованием программ Microsoft оffiсe, еxcel-2003 с определением критериев Стьюдента, Шапиро–Уилка, Фишера.
Вирусная природа острых респираторных заболеваний у 120 детей доказана в 42,5 % случаев, Р. carini выявлена у 6,7 % больных. В целом в этиологии острых респираторных заболеваний принимают участие все известные респираторные вирусы, но при распределении удельного веса возбудителей доминировало участие вирусов парагриппа. Этиологическая расшифровка ОРВИ представлена в таблице.
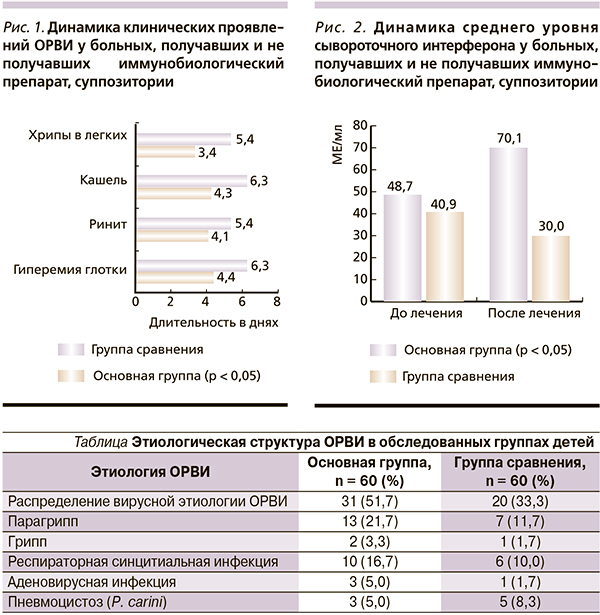
Сопоставление клиники обратного развития признаков ОРВИ свидетельствовало о том, что применение иммунобиологического препарата в комплексной терапии способствовало уменьшению продолжительности основных симптомов заболевания, особенно местных проявлений болезни (рис. 1). У детей, получавших препарат, достоверно раньше исчезали ринит, гиперемия слизистой оболочки ротоглотки, кашель, аускультативные изменения в легких (4,06 ± 0,15 против 5,43 ± 0,33 дня; 4,4 ± 0,15 против 6,3 ± 0,35 дня; 4,31 ± 0,23 против 6,33 ± 0,38 дня; 3,58 ± 0,53 против 5,36 ± 0,53 дня в основной группе и группе сравнения соответственно, р < 0,05).
Повторное вирусологическое исследование свидетельствовало о том, что у больных острыми респираторными заболеваниями, получавших препарат, к моменту выздоровления в 93,5 % случаев произошла элиминация возбудителей, в группе сравнения – в 65,0 %.
В начале заболевания уровень сывороточного интерферона у обследованных детей колебался в широких пределах (от 2 до 256 МЕ/мл). В динамике средний уровень сывороточного интерферона достоверно повысился у больных, лечившихся с использованием иммунобиологического препарата (от 48,73 ± 9,78 до 70,13 ± 13,55 МЕ/мл, р < 0,05; рис. 2).
При этом повышение уровня интерферона в 2–32 раза выявлено у 53,3 % детей. В группе сравнения средний уровень сывороточного интерферона уменьшился (от 40,93 ± 9,49 до 30,0 ± 4,83 МЕ/мл, р > 0,05), а его повышение (не более чем в 2–4 раза) отмечено лишь у 36,6 % детей.
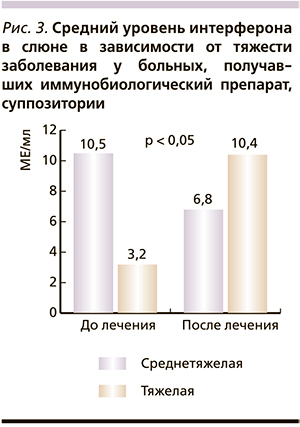
Немаловажным фактором местной противоинфекционной резистентности служит способность слизистых к продукции интерферона. У больных с поражением носо- и ротоглотки при исследовании уровня интерферона в слюне было выявлено, что интерферон определялся в 96,7 % случаев. Более отчетливая динамика уровня интерферона в слюне наблюдалась среди детей, получавших препарат в зависимости от тяжести процесса (рис. 3). Так, уровень интерферона достоверно повысился после лечения больных тяжелой формой ОРВИ, осложненной пневмонией (пациенты имели низкий исходный уровень по сравнению с больными иной степени тяжести заболевания).
При изучении показателей гуморального иммунитета в периоде разгара клинических проявлений заболевания наибольшие отклонения выявлены в отношении содержания классов сывороточных IgM и IgА, уровень которых оказался сниженным в 20–80 % случаев. За короткий период наблюдения у пациентов, получавших иммунобиологический препарат, имелась отчетливая тенденция к нарастанию IgG и IgA.
Микробиоценоз верхних дыхательных путей у детей с острой респираторной патологией при поступлении в стационар характеризовался высокой частотой обнаружения стрептококков в ассоциации из 2–3 культур (76 %), реже – из 4–5 культур. Грамположительные кокки определялись в 53,3 и 50,0 %, золотистый стафилококк – в 43,3 и 43,0 % случаев (в основной группе и группе сравнения соответственно). Редко обнаруживали грамотрицательные палочки, энтеробактерии и другие аэробы.
Таким образом, включение отечественного комбинированного иммунобиологического препарата, суппозитории для вагинального или ректального введения, в терапию ОРВИ с осложненным течением (стенозирующий ларинготрахеит, обструктивный бронхит, пневмония) у детей с отягощенным преморбидным фоном положительно влияло на сроки исчезновения клинических симптомов заболевания, элиминацию вирусов, уровень интерферона и состояние микрофлоры верхних дыхательных путей. При использовании препарата со стороны больных не наблюдалось побочных и аллергических реакций, а также отсутствовали рецидивы и повторные эпизоды заболевания в катамнезе в течение 1–3 месяцев.
Литература
- Шарапова О.В. Корсунский А.А. Инфекционные болезни у детей: прошлое, настоящее и будущее. Детские инфекции. 2003;1:4–6.
- Учайкин В.Ф. Решенные и нерешенные проблемы инфекционной патологии у детей. Детские инфекции. 2003;4:3–7.
- Лыкова Е.А. Антибактериальная терапия сочетанных бактериальных осложнений ОРВИ у детей / Материалы научно-практической конференции, посвященной 50-летию детского инфекционного отделения МОНИКИ, 2008. С. 109–13.
- Самсыгина Г.А. Часто болеющие дети: проблемы патогенеза, диагностики и терапии. Педиатрия. Consilium medicum. 2004;2:3–10.
- Заплатников А.Л. Принципы рациональной терапии острых респираторных вирусных инфекций у детей раннего возраста. РМЖ. 2004;12(13):10–6.
- Афанасьева О.И., Суховецкая В.Ф., Осидак Л.В. Клинико-лабораторная характеристика и терапия ОРВИ со стенозирующим ларинготрахеитом у детей.Детские инфекции. 2005;1:32–6.
- Самсыгина Г.А. Инфекции респираторного тракта у детей раннего возраста. М., 2006. С. 279.
- Интерфероновый статус, препараты интерферона в лечении и профилактике инфекционных заболеваний и реабилитации больных / Под ред. С.С. Афанасьева, Г.Г. Онищенко, В.А. Алешкина и др. М., 2005. 767 с.
- Попов В.Ф. Лекарственные формы интер-феронов. М., 2001.
- Сенцова Т.Б. Использование иммуно-моду-ляторов в педиатрии. Педиатрия. 2005;4(2).
- Препараты интерферона в лечении острых кишечных инфекций у детей. Пособие для врачей МЗ РФ. Составители: Л.В. Феклисова, Е.Р. Мескина, С.С. Афанасьев, В.А. Алешкин. М., 2005. 22 с.
Об авторах / Для корреспонденции
Феклисова Л.В., Мескина Е.Р., Галкина Л.А., Целипанова Е.Е., Казакова С.П., Савицкая Н.А.
Инфекционные заболевания - наиболее широко распространенная патология детского возраста. Ведущее место в структуре детской инфекционной заболеваемости занимают респираторные и кишечные инфекции, на долю которых приходится более 90% всех регистрируемых инфекций, причем уровень показателей не имеет тенденции к снижению 1. Вместе с тем вопросы лечения и профилактики респираторных и кишечных инфекций по-прежнему остаются нерешенными проблемами 2. Это обусловлено чрезвычайным разнообразием респираторных и кишечных патогенов, отсутствием широкого внедрения в практику современных диагностических методик, позволяющих своевременно идентифицировать возбудителя заболевания, а также высоким уровнем регистрации неблагоприятных состояний и факторов, отягощающих течение инфекционного процесса у современных детей 3.
Достижения и успехи в лечении основаны на применении современных иммунобиологических препаратов, клиническая эффективность которых определяется модуляцией базисной иммунореактивности больного ребенка, что позволяет улучшить исходы и снизить дальнейшее распространение инфекций 8.
Наиболее перспективным и патогенетически оправданным направлением представляется использование готовых лекарственных форм человеческого рекомбинантного a-2b-интерферона, обладающего противовирусным, антибактериальным, иммуномодулирующим и антипролиферативным действием 12. Ректальный метод введения, при котором фармакокинетика интерферона сравнима с внутримышечным применением [13,14], а побочные эффекты интерферонотерапии практически отсутствуют [10,11,15], наиболее приемлем в педиатрической практике. А создание комплексных препаратов на его основе, сочетающих положительные свойства монопрепаратов различного механизма действия, позволяют расширить спектр применения.
В результате проведенных научных исследований и десятилетнего опыта использования нами разработан алгоритм применения комбинированного иммунобиологического препарата "Кипферон® суппозитории для вагинального или ректального введения" (Регистрационное удостоверение Р N000126/01 от 31.03.2006, ООО "Алфарм", г. Москва), содержащего человеческий рекомбинантный a-2b-интерферон (в одной свече содержится не менее 500 000 МЕ) и КИП (комплексный иммуноглобулиновый препарат с высоким содержанием специфических IgG, IgA и IgM, 60 мг) в лечении и профилактике острых вирусно-бактериальных инфекций у детей. Использование препарата позволяет одномоментно сочетать противовирусный, антибактериальный, иммуномодулирующий эффекты интерферона с пассивной иммунотерапией, введением готовых антител и антитоксическим влиянием.
Алгоритм применения суппозиториев Кипферона® разработан в результате рандомизированных плацебо-контролируемых исследований по Государственной программе клинических испытаний ФГУН ГНИИСК медицинских и биологических препаратов им. Л.А. Тарасевича, результаты которых опубликованы и защищены в качестве диссертационных работ 16. В исследования были включены 375 детей. В том числе 282 ребенка (66 - острые кишечные инфекции (ОКИ), 60 - ангины, 120 - ОРВИ, 36 - инфекционный мононуклеоз Эпштейна-Барр вирусной и смешанной этиологии) были госпитализированы для стационарного лечения, 19 (с тяжелой соматической патологией) находились для лечения и реабилитации в специализированном стационаре, 74 ребенка - в детских закрытых коллективах с круглосуточным пребыванием (детские санатории, дом ребенка). Наблюдения охватывали все возрастные группы детей.
Комплекс исследований состоял из клинического наблюдения с регистрацией всех клинических симптомов заболевания, рутинным лабораторным исследованием крови и мочи, определением биохимических параметров, характеризующих функцию печени, почек, поджелудочной железы, проведением ЭКГ. Одновременно оценивались клинические и лабораторные признаки возможных негативных влияний проводимого лечения. Для расшифровки этиологии заболевания использовались бактериологические посевы фекалий и смывов из ротоглотки, серологические методы (РПГА) для диагностики группы бактериальных кишечных инфекций, ротавирусный гастроэнтерит диагностировался на основании обнаружения антигенов в фекалиях методом РНГА. Для подтверждения диагноза мононуклеоза использовались ПЦР и определение специфических антител классов IgM, IgG в ИФА. Кроме того, были исследованы уровни интерферона в слюне, сыворотке крови и копрофильтратах (при ОКИ), иммуноглобулинов различных классов в тех же средах, качественного и количественного состава микрофлоры кишечника, аспирата трахеи и ротоглотки у детей с ОКИ, ОРВИ, ангинами, инфекци-онным мононуклеозом. Профилактический эффект использования Кипферона® оценивался по клиническим параметрам состояния здоровья детей, находившихся в закрытых коллективах, с регистрацией всех случаев острых заболеваний в течение 2 месяцев наблюдения.
В исследование включались пациенты с тяжелыми и среднетяжелыми формами болезни. У 60-80% отмечено отягощение преморбидного статуса, у половины выявлена сочетанная вирусно-бактериальная инфекция. Каждая группа больных была рандомизирована на равные по возрасту, преморбидному статусу, нозологической форме, степени тяжести процесса и срокам начала лечения подгруппы - получавших и не получавших Кипферон®. Препарат включался в комплекс общепринятого лечения, в том числе с антибактериальной терапией при наличии показаний. Обоснованием эффективности метода служили полученные результаты.
Динамика клинических проявлений. Сравнительный анализ обратного развития признаков ОРВИ свидетельствовал о том, что использование Кипферона® в комплексной терапии способствовало уменьшению продолжительности основных симптомов инфекции, особенно местных проявлений. У получавших препарат достоверно раньше исчезали гиперемия слизистой оболочки ротоглотки, ринит (4,06±0,15 против 5,43±0,33 дней, р<0,05) кашель (4,31±0,236 против 3,3±0,38 дней, р<0,05), аускультативные изменения в легких (3,38±0,53 против 5,36±0,53 дней, р<0,05), быстрее купировался стеноз гортани.
Установлено достоверно значимое положительное влияние Кипферона® на сокращение продолжительности клинических симптомов инфекционного мононуклеоза на 1-2 дня: лихорадки, интоксикации, гиперемии слизистой ротоглотки, увеличения размеров миндалин, боли при глотании, налетов на миндалинах, гепатомегалии (p<0,05-0,001).
Таким образом, сравнительный анализ динамики клинических проявлений ОРВИ, ангины, инфекционного мононуклеоза и ОКИ у наблюдавшихся пациентов выявил убедительные преимущества включения суппозиториев Кипферона® в терапевтическую схему лечения.
Препарат хорошо переносился больными: ни у одного ребенка, в том числе с отягощенным аллергоанамнезом, не отмечено побочных реакций. Данные общепринятого лабораторного обследования свидетельствовали об отсутствии отрицательной динамики показателей.
Динамика лабораторных показателей. Микробиологический пейзаж верхних дыхательных путей больных ОРВИ характеризовался высокой частотой обнаружения стрептококка в ассоциации из 2-3 культур, реже - из 4-5. У 37,5% больных выделялись энтеробактерии или другие несвойственные для данного локуса микробы, что в 2,8 раза чаще, чем у здоровых.
У детей, получавших Кипферон®, после лечения не отмечалось расширения видового состава и угнетения облигатной ассоциации микробов, в 2 раза реже встречались монокультуры микроорганизмов при одновременном снижении в 3 раза частоты высева золотистого стафилококка. В группе сравнения в динамике лечения возросло число несвойственных для данного биотопа микробов, в том числе обнаруживались ранее отсутствовавшие гемолизирующая кишечная палочка и грибы рода Candida.
Микрофлора слизистой ротоглотки у больных ангинами в основном была представлена ассоциациями из 2-3 микробов (78,3%). Ассоциации микробов из 4-5 культур высевались у единичных пациентов. Энтеробактерии, золотистый стафилококк, грибы рода Candida обнаруживались у детей с осложненным течением болезни, хроническими воспалительными очагами. Динамика микробиологических показателей у детей с ангинами была сравнима с таковой при ОРВИ: у получавших Кипферон® в 6 раз уменьшилась частота высева золотистого стафилококка (p<0,05), отмечено более редкое (9,9% против 24,2%, p<0,05) обнаружение грамотрицательных энтеробактерий после лечения.
Группа детей, больных инфекционным мононуклеозом, характеризовалась высокой частотой обнаружения α-, β- и γ-гемолитических стрептококков (94,5%), а также ассоциаций различных культур (87,8%) с числом ассоциантов - 3 и более (до 26%) с большим видовым разнообразием микроорганизмов. Удельный вес пролиферации грибов рода Candida у больных мононуклеозом оказался наивысшим - 30%. Последнее с определенной долей вероятности может служить признаком иммунологических и выраженных дисбиотических нарушений.
Лечение Кипфероном® способствовало улучшению микробиологических показателей: снижению числа детей с высоким числом (3-6) микробных ассоциантов на слизистой ротоглотки и грибов рода Candida, более высокой (в 3 раза) элиминации β-гемолитического стрептококка группы А.
В группе детей с ОКИ отмечена высокая частота обнаружения (59-63%) ротавирусного антигена в фекалиях в титрах 1:320-1:640. К 5-му дню терапии Кипфероном® зафиксировано снижение титров у 89,5% больных (контроль - 71,4%), с элиминацией ротавирусов в 36,8% и 28,6% наблюдений соответственно. Использование суппозиториев Кипферона® в отличие от контроля позволило достичь достоверного снижения среднегеометрических титров ротавирусных антигенов в копрофильтратах (от 2,24±0,07 до 1,94±0,07 lg МЕ/мл, p< 0,01).
Уровень сывороточного интерферона у обследованных детей колебался в широких пределах (от 2 до 256 МЕ/мл) вне зависимости от этиологии инфекции. При индивидуальной разнонаправленной динамике средний его уровень в процессе лечения повысился у больных ОРВИ и ангинами, если они лечились с использованием Кипферона® (ОРВИ от 40,9±9,5 до 70,1±13,55 МЕ/мл, p
Немаловажным фактором местной противоинфекционной резистентности является способность слизистых к продукции интерферона. Нарастание титров интерферона в копрофильтратах у детей с ОКИ наблюдалось в 3,3 раза чаще, если дети лечились с использованием Кипферона®. У них частота обнаружения интерферона в копрофильтратах при повторном обследовании выросла более чем в два раза, достоверно превысив таковую в группе сравнения (34,4 против 12,51%). Назначение Кипферона® способствовало также достоверному нарастанию среднегеометрических титров интерферона в копрофильтратах (0,34±0,03 против 0,55±0,07 lg МЕ/мл, p<0,05).
При изучении показателей гуморального иммунитета в периоде разгара клинических проявлений инфекции наибольшие отклонения выявлены в отношении содержания сывороточных иммуноглобулинов M и А, уровень которых оказался сниженным в 20-80% случаев. За короткий период наблюдения у получавших Кипферон® имело место достоверное нарастание сывороточных титров IgM у больных ангинами и ОКИ, а также секреторного IgA в слюне и копрофильтратах у детей первого года жизни и при тяжелых формах инфекции, имевших наиболее низкие показатели. Именно у данной категории больных имело место существенное (в 2-3 раза) нарастание sIgA.
Суммируя результаты лабораторного обследования больных, можно судить о положительном влиянии комплексного иммунобиологического препарата Кипферон®, обусловленном иммуномодулирующим воздействием, главным образом на местное звено иммунитета.
В детском стационаре Московской области, предназначенном для лечения и реабилитации детей раннего возраста с тяжелой неврологической патологией, недоношенностью II-III ст, внутриутробными инфекциями, гипотрофией I-II ст. и др., в связи с подозрением на нозокомиальную ротавирусную инфекцию было проведено вирусологическое обследование фекалий всех детей, выявившее упорное бессимптомное носительство ротавирусов у 13 из 19 пациентов. Клинические и эпидемиологические показания послужили основанием для назначения Кипферона®. Контрольное вирусологическое обследование, проведенное сразу после 10-дневного курса лечения, имело желаемый результат. Прибавка массы тела за период наблюдения соответствовала средним возрастным показателям. Таким образом, Кипферон® оказался эффективным и безопасным санирующим средством в отношении ротавирусов, длительно персистирующих в кишечнике ослабленных детей, в том числе и при безуспешных предварительных курсах лечения.
Включение Кипферона® в комплекс оздоровительных мероприятий в закрытых детских коллективах способствовал снижению частоты, либо тяжести респираторных инфекций. В отличие от групп, в которых Кипферон® не использовался, детям в 2 раза реже понадобилось назначение антибактериальной терапии и не потребовалась госпитализация.
Показания к назначению суппозиториев Кипферона® следующие:
среднетяжелые и тяжелые формы ОРВИ, в том числе протекающие с синдромом стеноза гортани и обструкции бронхов;
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем и подготовлено для печатного издания справочника Видаль 2021 года.
Владелец регистрационного удостоверения:
Произведено:
Вторичная упаковка и выпускающий контроль качества:
Контакты для обращений:
Активные вещества
- интерферон альфа-2b (interferon alfa-2b) USAN принятое к употреблению в США
- иммуноглобулин человека нормальный [IgG+IgA+IgM] (human normal immunoglobulin [IgG+IgA+IgM]) Group Группировочное наименование
Лекарственная форма
Форма выпуска, упаковка и состав препарата Кипферон ®
Суппозитории вагинальные и ректальные белого, белого с желтоватым оттенком или светло-бежевого цвета, цилиндрической формы с заостренным концом, на продольном срезе однородны; на срезе допускается наличие воздушного стержня или воронкообразного углубления; допускается неоднородность окраски в виде мраморности; с характерным запахом.
| 1 супп. | |
| иммуноглобулиновый комплексный препарат* | 200 мг |
| интерферон альфа-2b человеческий рекомбинантный | 500000 МЕ |
* иммуноглобулин человека нормальный, содержащий IgG, IgA, IgM.
Вспомогательные вещества: жир специального назначения "СолПро" кондитерский для шоколадных изделий и конфет - 838 мг, парафин нефтяной твердый П-2 - 85 мг, эмульгатор "Твердый" (Т-2) - 85 мг, натрия гидрофосфата додекагидрат - 0.055 мг, натрия дигидрофосфата дигидрат - 0.018 мг, натрия хлорид - 0.11 мг, вода очищенная - 12 мг.
5 шт. - упаковки ячейковые контурные (1) - пачки картонные.
5 шт. - упаковки ячейковые контурные (2) - пачки картонные.
Фармакологическое действие
Кипферон ® представляет собой комплексную лекарственную форму, содержащую человеческий рекомбинантный интерферон-α2 и комплексный иммуноглобулиновый препарат (КИП). Обладает иммуномодулирующим, противовирусным, противохламидийным действием.
Интерферон-α2 является активатором врожденного и приобретенного иммунитета, обладает выраженной противовирусной активностью, усиливает защиту от вирусных, хламидийных, микоплазменных и бактериальных инфекций, оказывает иммуномодулирующий эффект в развитии иммунологических реакций, способствует росту и сохранению нормофлоры кишечника и влагалища. Биологическая активность интерферона-α2 реализуется посредством взаимодействия с рецепторным аппаратом иммунокомпетентных и других клеток, приводящим к усилению экспрессии молекул HLA I и HLA II на поверхности всех типов клеток и регуляции кооперации клеток, повышению активности естественных киллеров, а также приданию интактным клеткам устойчивости против их цитолитического действия, пролиферации CD8 Т-клеток. Повышает выработку гамма-интерферона естественными киллерами.
Комплексный иммуноглобулиновый препарат содержит специфические и неспецифические иммуноглобулины классов G, М, А. Сочетание антивирусных, антихламидийных, антибактериальных и антитоксических антител, принадлежащих к различным классам иммуноглобулинов, обеспечивает агглютинацию, нейтрализацию и преципитацию этиотропных патогенных агентов. В месте аппликации обеспечивает стабилизацию интерферона от секретов слизистых оболочек, нормализует местный иммунитет за счет поступления IgA и IgM с суппозиториями (заместительный эффект), повышает активность местно образуемых цитокинов.
Показания препарата Кипферон ®
Препарат применяют в комплексной терапии заболеваний, сопровождающихся вторичными иммунодефицитными состояниями:
- острые респираторные заболевания, воспалительные заболевания ротоглотки бактериальной и вирусной этиологии у детей и взрослых;
- острые вирусные (ротавирусные) и бактериальные (сальмонеллез, дизентерия, коли-инфекция) кишечные инфекции, в т.ч. с проявлениями дисбактериоза кишечника различной выраженности у детей;
- урогенитальный хламидиоз у женщин (в т.ч. у беременных во II-III триместрах беременности), в т.ч. с проявлениями дисбактериоза влагалища, вульвовагинита, цервицита, эрозии шейки матки.
| Код МКБ-10 | Показание |
| A02 | Другие сальмонеллезные инфекции |
| A03 | Шигеллез |
| A04.4 | Другие кишечные инфекции, вызванные Escherichia coli |
| A04.9 | Бактериальная кишечная инфекция неуточненная |
| A08.0 | Ротавирусный энтерит |
| A56.0 | Хламидийные инфекции нижних отделов мочеполового тракта |
| A56.1 | Хламидийные инфекции органов малого таза и других мочеполовых органов |
| J02 | Острый фарингит |
| J06.9 | Острая инфекция верхних отделов дыхательных путей неуточненная |
| K63.8 | Другие уточненные болезни кишечника |
| N72 | Воспалительная болезнь шейки матки (в т.ч. цервицит, эндоцервицит, экзоцервицит) |
| N77.1 | Вагинит, вульвит и вульвовагинит при инфекционных и паразитарных болезнях, классифицированных в других рубриках |
| N86 | Эрозия и эктропион шейки матки |
| N89.8 | Другие невоспалительные болезни влагалища |
| O23 | Инфекция мочеполовых путей при беременности |
Режим дозирования
Препарат применяют ректально и вагинально.
Кипферон ® используется в комплексе с общепринятыми средствами патогенетической терапии инфекционных заболеваний, а также антибиотиками по показаниям. Способ и режим дозирования, а так же применение в комплексном лечении определяется врачом в зависимости от диагноза, остроты и тяжести заболевания.
Острые респираторные заболевания, воспалительные заболевания ротоглотки бактериальной и вирусной этиологии: суппозитории вводят ректально (преимущественно после акта дефекации) детям в возрасте до 1 года - по 1 супп./сут, детям в возрасте до 12 лет – по 1 супп. 2 раза/сут, взрослым и детям старше 12 лет – по 1 супп. 3 раза/сут. Наиболее эффективно и целесообразно назначение препарата Кипферон ® в остром периоде заболевания (желательно в первые 3 дня). Длительность курса лечения определяется этиологией, формой тяжести заболевания, наличием сопутствующих осложнений, патологических состояний и составляет 5-7 дней.
Острые вирусные (ротавирусные) и бактериальные (сальмонеллез, дизентерия, коли-инфекция) кишечные инфекции, в т.ч. с проявлениями дисбактериоза кишечника различной выраженности у детей : суппозитории вводят ректально (преимущественно после акта дефекации) детям в возрасте до 1 года - по 1 супп./сут, детям в возрасте до 12 лет – по 1 супп. 2 раза/сут, взрослым и детям старше 12 лет – по 1 супп. 3 раза/сут. Наиболее эффективно и целесообразно назначение препарата в остром периоде заболевания (желательно в первые 3 дня). Длительность курса лечения определяется этиологией, формой тяжести заболевания, наличием сопутствующих осложнений, патологических состояний и составляет 5-7 дней.
Урогенитальный хламидиоз у женщин (в т.ч. у беременных во II-III триместрах беременности), в т.ч. с проявлениями дисбактериоза влагалища, вульвовагинита, цервицита, эрозии шейки матки: суппозитории вводят глубоко интравагинально (до контакта с задним сводом влагалища и шейкой матки). Назначают по 1-2 супп., в зависимости от выраженности заболевания, 2 раза/сут. Курс лечения составляет в среднем 10 дней; при наличии эрозии шейки матки применение препарата продолжают до ее эпителизации. По показаниям курс лечения может быть повторен через 1 месяц. Лечение следует начинать в первые дни после окончания менструации. Перед введением рекомендуется удалить слизь со слизистых оболочек влагалища и шейки матки.
Для цитирования: Феклисова Л.В., Мескина Е.Р., Галкина Л.А. и др. Оптимизация результатов лечения вирусно–бактериальных инфекций у детей: алгоритм применения суппозиториев Кипферона®. РМЖ. 2009;7:468.
Инфекционные заболевания – наиболее широко распространенная патология детского возраста. Ведущее место в структуре детской инфекционной заболеваемости занимают респираторные и кишечные инфекции, на долю которых приходится более 90% всех регистрируемых инфекций, причем уровень показателей не имеет тенденции к снижению [1–3]. Вместе с тем вопросы лечения и профилактики респираторных и кишечных инфекций по–прежнему остаются нерешенными проблемами [1–3]. Это обусловлено чрезвычайным разнообразием респираторных и кишечных патогенов, отсутствием широкого внедрения в практику современных диагностических методик, позволяющих своевременно идентифицировать возбудителя заболевания, а также высоким уровнем регистрации неблагоприятных состояний и факторов, отягощающих течение инфекционного процесса у современных детей [3–5].
Инфекционные заболевания – наиболее широко распространенная патология детского возраста. Ведущее место в структуре детской инфекционной заболеваемости занимают респираторные и кишечные инфекции, на долю которых приходится более 90% всех регистрируемых инфекций, причем уровень показателей не имеет тенденции к снижению [1–3]. Вместе с тем вопросы лечения и профилактики респираторных и кишечных инфекций по–прежнему остаются нерешенными проблемами [1–3]. Это обусловлено чрезвычайным разнообразием респираторных и кишечных патогенов, отсутствием широкого внедрения в практику современных диагностических методик, позволяющих своевременно идентифицировать возбудителя заболевания, а также высоким уровнем регистрации неблагоприятных состояний и факторов, отягощающих течение инфекционного процесса у современных детей [3–5].
Достижения и успехи в лечении основаны на применении современных иммунобиологических препаратов, клиническая эффективность которых определяется модуляцией базисной иммунореактивности больного ребенка, что позволяет улучшить исходы и снизить дальнейшее распространение инфекций [6–9].
Наиболее перспективным и патогенетически оправданным направлением представляется использование готовых лекарственных форм человеческого рекомбинантного a –2b–интерферона, обладающего противовирусным, антибактериальным, иммуномодулирующим и антипролиферативным действием [10–12]. Ректальный метод введения, при котором фармакокинетика интерферона сравнима с внутримышечным применением [13,14], а побочные эффекты интерферонотерапии практически отсутствуют [10,11,15], наиболее приемлем в педиатрической практике. А создание комплексных препаратов на его основе, сочетающих положительные свойства монопрепаратов различного механизма действия, позволяют расширить спектр применения.
Алгоритм применения суппозиториев Кипферона ® разработан в результате рандомизированных плацебо–контролируемых исследований по Государственной программе клинических испытаний ФГУН ГНИИСК медицинских и биологических препаратов им. Л.А. Тарасевича, результаты которых опубликованы и защищены в качестве диссертационных работ [15–19]. В исследования были включены 375 детей. В том числе 282 ребенка (66 – острые кишечные инфекции (ОКИ), 60 – ангины, 120 – ОРВИ, 36 – инфекционный мононуклеоз Эпштейна–Барр вирусной и смешанной этиологии) были госпитализированы для стационарного лечения, 19 (с тяжелой соматической патологией) находились для лечения и реабилитации в специализированном стационаре, 74 ребенка – в детских закрытых коллективах с круглосуточным пребыванием (детские санатории, дом ребенка). Наблюдения охватывали все возрастные группы детей.
Комплекс исследований состоял из клинического наблюдения с регистрацией всех клинических симптомов заболевания, рутинным лабораторным исследованием крови и мочи, определением биохимических параметров, характеризующих функцию печени, почек, поджелудочной железы, проведением ЭКГ. Одновременно оценивались клинические и лабораторные признаки возможных негативных влияний проводимого лечения. Для расшифровки этиологии заболевания использовались бактериологические посевы фекалий и смывов из ротоглотки, серологические методы (РПГА) для диагностики группы бактериальных кишечных инфекций, ротавирусный гастроэнтерит диагностировался на основании обнаружения антигенов в фекалиях методом РНГА. Для подтверждения диагноза мононуклеоза использовались ПЦР и определение специфических антител классов IgM, IgG в ИФА. Кроме того, были исследованы уровни интерферона в слюне, сыворотке крови и копрофильтратах (при ОКИ), иммуноглобулинов различных классов в тех же средах, качественного и количественного состава микрофлоры кишечника, аспирата трахеи и ротоглотки у детей с ОКИ, ОРВИ, ангинами, инфекци-онным мононуклеозом. Профилактический эффект использования Кипферона ® оценивался по клиническим параметрам состояния здоровья детей, находившихся в закрытых коллективах, с регистрацией всех случаев острых заболеваний в течение 2 месяцев наблюдения.
В исследование включались пациенты с тяжелыми и среднетяжелыми формами болезни. У 60–80% отмечено отягощение преморбидного статуса, у половины выявлена сочетанная вирусно–бактериальная инфекция. Каждая группа больных была рандомизирована на равные по возрасту, преморбидному статусу, нозологической форме, степени тяжести процесса и срокам начала лечения подгруппы – получавших и не получавших Кипферон ® . Препарат включался в комплекс общепринятого лечения, в том числе с антибактериальной терапией при наличии показаний. Обоснованием эффективности метода служили полученные результаты.
Динамика клинических проявлений . Сравнительный анализ обратного развития признаков ОРВИ свидетельствовал о том, что использование Кипферона ® в комплексной терапии способствовало уменьшению продолжительности основных симптомов инфекции, особенно местных проявлений. У получавших препарат достоверно раньше исчезали гиперемия слизистой оболочки ротоглотки, ринит (4,06±0,15 против 5,43±0,33 дней, р<0,05) кашель (4,31±0,236 против 3,3±0,38 дней, р<0,05), аускультативные изменения в легких (3,38±0,53 против 5,36±0,53 дней, р<0,05), быстрее купировался стеноз гортани.
Установлено достоверно значимое положительное влияние Кипферона ® на сокращение продолжительности клинических симптомов инфекционного мононуклеоза на 1–2 дня: лихорадки, интоксикации, гиперемии слизистой ротоглотки, увеличения размеров миндалин, боли при глотании, налетов на миндалинах, гепатомегалии (p<0,05–0,001).
Таким образом, сравнительный анализ динамики клинических проявлений ОРВИ, ангины, инфекционного мононуклеоза и ОКИ у наблюдавшихся пациентов выявил убедительные преимущества включения суппозиториев Кипферона ® в терапевтическую схему лечения.
Препарат хорошо переносился больными: ни у одного ребенка, в том числе с отягощенным аллергоанамнезом, не отмечено побочных реакций. Данные общепринятого лабораторного обследования свидетельствовали об отсутствии отрицательной динамики показателей.
Динамика лабораторных показателей . Микробиологический пейзаж верхних дыхательных путей больных ОРВИ характеризовался высокой частотой обнаружения стрептококка в ассоциации из 2–3 культур, реже – из 4–5. У 37,5% больных выделялись энтеробактерии или другие несвойственные для данного локуса микробы, что в 2,8 раза чаще, чем у здоровых.
У детей, получавших Кипферон ® , после лечения не отмечалось расширения видового состава и угнетения облигатной ассоциации микробов, в 2 раза реже встречались монокультуры микроорганизмов при одновременном снижении в 3 раза частоты высева золотистого стафилококка. В группе сравнения в динамике лечения возросло число несвойственных для данного биотопа микробов, в том числе обнаруживались ранее отсутствовавшие гемолизирующая кишечная палочка и грибы рода Candida.
Микрофлора слизистой ротоглотки у больных ангинами в основном была представлена ассоциациями из 2–3 микробов (78,3%). Ассоциации микробов из 4–5 культур высевались у единичных пациентов. Энтеробактерии, золотистый стафилококк, грибы рода Candida обнаруживались у детей с осложненным течением болезни, хроническими воспалительными очагами. Динамика микробиологических показателей у детей с ангинами была сравнима с таковой при ОРВИ: у получавших Кипферон ® в 6 раз уменьшилась частота высева золотистого стафилококка (p<0,05), отмечено более редкое (9,9% против 24,2%, p<0,05) обнаружение грамотрицательных энтеробактерий после лечения.
Группа детей, больных инфекционным мононуклеозом, характеризовалась высокой частотой обнаружения α –, β – и γ –гемолитических стрептококков (94,5%), а также ассоциаций различных культур (87,8%) с числом ассоциантов – 3 и более (до 26%) с большим видовым разнообразием микроорганизмов. Удельный вес пролиферации грибов рода Candida у больных мононуклеозом оказался наивысшим – 30%. Последнее с определенной долей вероятности может служить признаком иммунологических и выраженных дисбиотических нарушений.
Лечение Кипфероном ® способствовало улучшению микробиологических показателей: снижению числа детей с высоким числом (3–6) микробных ассоциантов на слизистой ротоглотки и грибов рода Candida, более высокой (в 3 раза) элиминации β –гемолитического стрептококка группы А.
В группе детей с ОКИ отмечена высокая частота обнаружения (59–63%) ротавирусного антигена в фекалиях в титрах 1:320–1:640. К 5–му дню терапии Кипфероном ® зафиксировано снижение титров у 89,5% больных (контроль – 71,4%), с элиминацией ротавирусов в 36,8% и 28,6% наблюдений соответственно. Использование суппозиториев Кипферона ® в отличие от контроля позволило достичь достоверного снижения среднегеометрических титров ротавирусных антигенов в копрофильтратах (от 2,24±0,07 до 1,94±0,07 lg МЕ/мл, p< 0,01).
Уровень сывороточного интерферона у обследованных детей колебался в широких пределах (от 2 до 256 МЕ/мл) вне зависимости от этиологии инфекции. При индивидуальной разнонаправленной динамике средний его уровень в процессе лечения повысился у больных ОРВИ и ангинами, если они лечились с использованием Кипферона ® (ОРВИ от 40,9±9,5 до 70,1±13,55 МЕ/мл, p
Немаловажным фактором местной противоинфекционной резистентности является способность слизистых к продукции интерферона. Нарастание титров интерферона в копрофильтратах у детей с ОКИ наблюдалось в 3,3 раза чаще, если дети лечились с использованием Кипферона ® . У них частота обнаружения интерферона в копрофильтратах при повторном обследовании выросла более чем в два раза, достоверно превысив таковую в группе сравнения (34,4 против 12,51%). Назначение Кипферона ® способствовало также достоверному нарастанию среднегеометрических титров интерферона в копрофильтратах (0,34±0,03 против 0,55±0,07 lg МЕ/мл, p<0,05).
При изучении показателей гуморального иммунитета в периоде разгара клинических проявлений инфекции наибольшие отклонения выявлены в отношении содержания сывороточных иммуноглобулинов M и А, уровень которых оказался сниженным в 20–80% случаев. За короткий период наблюдения у получавших Кипферон ® имело место достоверное нарастание сывороточных титров IgM у больных ангинами и ОКИ, а также секреторного IgA в слюне и копрофильтратах у детей первого года жизни и при тяжелых формах инфекции, имевших наиболее низкие показатели. Именно у данной категории больных имело место существенное (в 2–3 раза) нарастание sIgA.
Суммируя результаты лабораторного обследования больных, можно судить о положительном влиянии комплексного иммунобиологического препарата Кипферон ® , обусловленном иммуномодулирующим воздействием, главным образом на местное звено иммунитета.
В детском стационаре Московской области, предназначенном для лечения и реабилитации детей раннего возраста с тяжелой неврологической патологией, недоношенностью II–III ст, внутриутробными инфекциями, гипотрофией I–II ст. и др., в связи с подозрением на нозокомиальную ротавирусную инфекцию было проведено вирусологическое обследование фекалий всех детей, выявившее упорное бессимптомное носительство ротавирусов у 13 из 19 пациентов. Клинические и эпидемиологические показания послужили основанием для назначения Кипферона ® . Контрольное вирусологическое обследование, проведенное сразу после 10–дневного курса лечения, имело желаемый результат. Прибавка массы тела за период наблюдения соответствовала средним возрастным показателям. Таким образом, Кипферон ® оказался эффективным и безопасным санирующим средством в отношении ротавирусов, длительно персистирующих в кишечнике ослабленных детей, в том числе и при безуспешных предварительных курсах лечения.
Включение Кипферона ® в комплекс оздоровительных мероприятий в закрытых детских коллективах способствовал снижению частоты, либо тяжести респираторных инфекций. В отличие от групп, в которых Кипферон ® не использовался, детям в 2 раза реже понадобилось назначение антибактериальной терапии и не потребовалась госпитализация.
Показания к назначению суппозиториев Кипферона ® следующие:
• стартовая монотерапия ротавирусных гастроэнтеритов;
• тяжелые и среднетяжелые формы вирусно–бактериальных и бактериальных кишечных инфекций;
• нозокомиальные кишечные инфекции (вирусные и бактериальные);
• среднетяжелые и тяжелые формы ОРВИ, в том числе протекающие с синдромом стеноза гортани и обструкции бронхов;
• повторные эпизоды ОРВИ у часто болеющих детей;
• инфекционный мононуклеоз, в том числе с бактериальными осложнениями;
• ангина у детей с хронической патологией ЛОР– органов, осложненное течение ангины (паратонзиллит, паратонзиллярный абсцесс, лимфаденит);
• сочетанная инфекция различных органов и систем;
• респираторные и кишечные инфекции у детей раннего возраста с отягощенным преморбидным статусом, у детей любого возраста с выявленными дефектами фагоцитоза и местного секреторного иммунитета;
• длительное и упорное выделение возбудителей заболевания;
• в составе реабилитационных мероприятий у детей с повторными инфекционными заболеваниями органов дыхания.
Суппозитории Кипферона ® вводятся ректально (преимущественно после акта дефекации) детям до 1 года по одному суппозиторию в сутки (можно разделить пополам на 2 приема), детям до 12 лет по 1 суппозиторию 2 раза в сутки и детям старше 12 лет – по 1 суппозиторию трижды в сутки. При выраженных клинических проявлениях заболевания и тяжести состояния суточная доза может быть увеличена на 1 суппозиторий (но не более 3 суппозиториев в сутки детям старше одного года).
Наиболее эффективно и целесообразно назначение Кипферона ® в остром периоде заболевания (желательно в первые 3 дня).
В зависимости от этиологии и формы тяжести заболевания препарат может быть использован либо как единственное средство этиопатогенетического лечения, либо в составе общепринятой комбинированной терапии. Лечение Кипфероном ® совместимо с общепринятыми средствами патогенетической терапии инфекционных заболеваний у детей. Длительность курса лечения определяется этиологией, формой тяжести инфекционного заболевания, наличием сопутствующих осложнений и патологических состояний.
При ротавирусной инфекции Кипферон ® может быть единственным этиопатогенетическим средством лечения на фоне общепринятой комплексной терапии (оральная или инфузионная регидратация при необходимости, дозированное лечебное питание). Курс лечения при легких и среднетяжелых формах заболевания составляет до 5 дней. При тяжелых формах с целью достижения эффективной вирусологической санации он может быть продлен до 7 дней.
При вирусно–бактериальных кишечных инфекциях длительность курса составляет 7 дней. В случае среднетяжелых форм у детей без отягощенного преморбидного статуса и сопутствующей патологии Кипферон ® может быть единственным средством этиопатогенетической терапии. При тяжелых формах лечение Кипфероном ® проводят на фоне общепринятой, в том числе антибактериальной терапии.
Длительность курса лечения среднетяжелых и тяжелых форм бактериальных кишечных инфекций в комплексе общепринятой терапии составляет до 7 дней.
Курс терапии, проведенный с целью достижения вирусологической и бактериологической санации при длительном и упорном выделении возбудителей инфекции из кишечника, составляет 7–10 дней.
Курс лечения Кипфероном ® ОРВИ на фоне базисной симптоматической терапии составляет 3 дня. У детей с отягощенным преморбидным состоянием при частых повторных эпизодах инфекции курс лечения продлевается до 5 дней. В случае развития вирусно–бактериального стенозирующего ларинготрахеита лечение целесообразно продолжать в течение 5 дней, а для лечения обструктивного бронхита или бактериальных осложнений ОРВИ (отит, синусит, пневмония) – не менее 7 дней. Лечение Кипфероном ® проводят в комплексе с патогенетической терапией, а также антибиотиками по показаниям.
Лечение ангины проводят Кипфероном ® в течение 5 дней на фоне общепринятой терапии. При ангине у детей с хронической патологией ЛОР–органов курс лечения Кипфероном ® продлевается до 7 дней. У детей с осложненным течением ангины (паратонзиллит, паратонзиллярный абсцесс) Кипферон ® целесообразно назначать в течение 10 дней: 5 дней – в возрастных дозировках, затем еще 5 дней по одному суппозиторию в день.
Кипферон ® может быть препаратом выбора этиопатогенетической терапии инфекционного мононуклеоза (моноинфекция, легкие и среднетяжелые формы). При тяжелом течении заболевания и осложненных формах Кипферон ® включают в комплексную терапию. Курс лечения инфекционного мононуклеоза – 10 дней: 5 дней в соответствующих возрастных дозировках, затем еще 5 дней – по одному суппозиторию в сутки.
Часто болеющим детям в периоде ремиссии в комплекс реабилитационных мероприятий включают Кипферон ® в соответствующих возрастных дозировках в течение 5 дней, затем целесообразно продлить лечение еще на 5 дней, назначая по одному суппозиторию в день. Таким образом, общий курс составляет 10 дней. Для профилактики распространения ОРВИ в детских закрытых коллективах Кипферон ® назначают по одной свече 1 раз в сутки в течение 10 дней.
Алгоритм лечения Кипфероном ® представлен на рисунке 1.
Таким образом, включение препарата Кипферон ® в терапию наиболее распространенных инфекционных заболеваний дыхательных путей и желудочно–кишечного тракта у детей повышает эффективность лечения на 20–25% и способствует сокращению сроков болезни на 25–35%. Полученный позитивный эффект может быть результатом расширения спектра этиотропного воздействия, активации локальных механизмов защиты в местах проникновения патогенов, иммуномодулирующего влияния, что в целом улучшает противоинфекционную резистентность и приводит к элиминации возбудителей.
Метод отличают простота воспроизведения, возможность применения у детей любого возраста и отсутствие побочных эффектов и осложнений.
На сервисе СпросиВрача доступна консультация педиатра онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте, вопрос "Можно" или "нужно" всё таки? Если Вам назначено, в связи с тем, что до этого были перенесы бронхит и пневмония, думаю, назначение оправдано. Любые интерфероны в сечах (Виферон, Кипферон, Генферон). Помимо противовирусного эффекту, у них есть другие не менее полезные , вспомогательные лечебные эффекты.
Лариса, спасибо! Назначения не было .Я только что смерила температуру .В поликлинику ещё не обращалась .Поэтому и спрашиваю ,чтобы хоть как то предотвратить последствия.


Здравствуйте
Поставить свечу кипферон можно, но не нужно- препарат не имеет доказанной эффективности, не сократит время болезни и никак не облегчит симптомы.
Дарья, спасибо! А можно хоть как то предотвратить последствия заболевания? У нас любое ОРВИ заканчивается либо обструктивным бронхитом ,либо пневмонией. В анамнезе бронхиальная астма

Так как у ребенка бронхиальная астма то соответственно это и отягощает любое орви
Базисную терапию принимаете?

Чтобы снизить риск последствий и затяжного течения, необходимо принимать базисную терапию, особенно во время орви
По мере роста и взросления ребёнка боонхиолы будут менее реактивны и обструкции будут происходить реже. Сейчас это связано с возрастными особенностями - реактивные стенки бронхов, большое образование вязкой слизи, узость просвета бронхов.
Подрастёт и станет легче
Дарья, понятно ! Если вдруг начнется кашель ,есть ли необходимость в базисной терапии,если при кашле у нас схема : Пульмикорт 2 р/д + Беродуал 3р/д
Не будет передозировки гормонов?

Да, базисная терапия применяется для профилактики обострения бронх астмы.
А пульмикорт и беродуал непосредственно при присоединении симптомов (кашля)
Передозировки не будет


Добрый вечер. Кипферон не имеет доказательной базы эффективности. Я не вижу смысла в его использовании

Елена, добрый вечер. Кипферон хороший препарат, раньше им пользовалась сама. Но на сегодня нет доказательной базы его результата.
Первый день болезни, обильное питье, промывание носа и зева Мирамистин.
Выздоравливайте.

Здравствуйте, поставить можно, никакого вреда не будет.
Если начинать с первого дня, возможно поможет сократить период болезни.

Здравствуйте! Судя по всему ребенок уже заразился и уже вирусный процесс запущен,так что смысла в профилактике уже, к сожалению, нет. Ну и к тому же препараты этой группы не доказали своей эффективности как профилактика ОРВИ. Сейчас лучшее что вы можете сделать это уже обильное питье ребенку из расчета 30 мл/кг, увлажнение воздуха в помещении где ребёнок проводит большую часть времени и обязательно на сон тоже. При желании гулять и купаться )

Добрый день. Препараты интерыероноаого рчда при легких ОРЗ не показаны. Эти препараты являются иммуномодуляторами и лишний паз стимулировать имунную систему не нужно. Бесконтрольное применение приводит к снижению нейтрофилов и приводит к усиоению частоты заболевания.
Читайте также:

