Когда появится лечение вич с помощью инъекции
Обновлено: 25.04.2024
Китайские двойняшки
Хе Цзянькуй (He Jiankui), китайский ученый из Южного университета науки и технологий в Шэньчжэне, рассказал в середине ноября о рождении девочек-близняшек с измененным геномом. Геном был отредактирован на стадии эмбрионального развития для защиты детей от ВИЧ.
Китайский ученый-генетик Хе Цзянькуй
Около 1% населения Северной Европы, в том числе в России, имеют иммунитет к ВИЧ с рождения.
Попытки научиться переносить эту невосприимчивость от одного человека к другому ученые предпринимают уже давно. На этой идее основывался и эксперимент Хе Цзянькуя. Но несмотря на окрыляющие результаты, к истории с редактированием генома эмбрионов много вопросов.
Во-первых, ни одной статьи в рецензируемом научном журнале с деталями работы пока не опубликовано. А раздел, посвященный работе с детьми, на сайте лаборатории Хе в Южном университете недоступен. И все сведения об успехе эксперимента основаны на выступлении ученого на Международной конференции по редактированию генома в Гонконге и его интервью Associated Press.
Из-за отсутствия доказательств безопасности редактирования генома подсаживать измененные эмбрионы женщинам запрещено в большинстве стран. Поэтому выпускник Стэнфорда и университета Райса Хе Цзянькуй и поставил эксперимент в Китае. Кстати, в этом ему помогал профессор биоинженерии Майкл Дим, с которым Хе познакомился во время обучения.
Более того, китайский ученый не смог или отказался ответить на несколько важных вопросов, в том числе о том, кто финансировал исследование и как он удостоверился, что подопытные знали о возможных последствиях. Смутило ученых и то, что данные о начале эксперимента в государственный реестр клинических испытаний были внесены лишь 8 ноября 2018 года — почти через год после его начала.
Берлинский пациент
Говорить об излечении Рея от ВИЧ специалисты не спешат: сколько еще 52-летний пациент сможет продержаться без терапии, неизвестно.
Испанские больные
В результате у 10 из 13 пациентов количество вирусов в крови увеличилось, и они стали проходить антиретровирусную терапию. Но у остальных вирус либо не обнаружился вообще, либо — в незначительном объеме. И в таком состоянии без терапии они провели до 30 недель. Отчитались ученые о работе с 13 пациентами, но на самом деле их было больше — не все вошли в финальную выборку по разным причинами.
После публикации результатов многие СМИ писали о создании вакцины от ВИЧ, однако говорить об этом было преждевременно. Тем более что новых заявлений испанских ученых по поводу состояния подопытных найти не удалось.
Российские инфицированные
Подобные случаи, когда зараженные ВИЧ не нуждаются в замедляющей развитие вируса терапии, встречаются не только в Германии и Испании. По крайней мере об одном ВИЧ-положительном с 20-летним стажем, который без проблем для здоровья отказался от терапии, известно в России. Однако экстраполировать этот опыт на других пациентов так, чтобы состояние улучшалось в 100% случаев, пока не удается.
Поэтому люди с ВИЧ-положительным статусом постоянно принимают лекарства. Антиретровирусная терапия — единственный способ борьбы с вирусом, чья эффективность, пусть и временная, доказана. Кроме того, она исключает возможность передачи вируса от человека к человеку, в том числе от ВИЧ-положительных матерей детям.
Во-вторых, терапия дорогая. В России за счет бюджета в прошлом году удалось обеспечить лекарствами 340 тыс. пациентов, в этом — 412 тыс.
По данным Министерства здравоохранения РФ на ноябрь 2018 года, у 808 тыс. россиян ВИЧ.
Пусть это меньше, чем 1,2 или 1,5 млн, о которых говорят другие организации, в том числе негосударственные, которые ведут свою статистику. В любом случае, количество людей, которых удается лечить за счет бюджета, существенно меньше количества больных. В прошлом году Россия стала первой страной в Европе по числу новых случаев заражения — 71,1 случай на 100 тыс. населения.
Инфицированным остается ждать попадания в бюджетную программу или лечиться самостоятельно. Ко второму варианту подталкивает и то, что некоторые новые зарубежные препараты запрещено покупать за государственный счет.
Дело нескольких лет
И хотя испытания российского препарата были удачными, о выпуске его на рынок речь пойдет, только когда медики получат доказательства отсутствия непредсказуемых последствий вмешательства в геном клеток. Тех самых доказательств, которых не стал дожидаться Хе Цзянькуй.
На сегодняшний день лечение от ВИЧ-инфекции предполагает ежедневный прием таблеток. Ситуация может измениться уже в этом году вместе с появлением инъекционных препаратов. Это революционное решение может значительно упростить жизнь людям с ВИЧ, повысить приверженность к лечению, решить проблему с приемом большого количества таблеток, ежедневно напоминающих о диагнозе.
Несколько исследований третьей фазы, в которых участники получали инъекционный режим каботегравир + рилпивирин один раз в месяц, а в другом исследовании — раз в два месяца, доказали высокую эффективность и безопасность этого режима терапии.
И несмотря на встречающиеся побочные эффекты в виде реакций в месте инъекции, результаты опроса участников показали бо́льшую удовлетворенность лечением среди пациентов, получавших инъекционные препараты.
Другим ожидаемым препаратом пролонгированного действия станет ленакапавир от компании Gilead. Согласно данным исследований, достаточно будет всего одной инъекции раз в полгода, в отличие от ежедневного перорального лечения.
В случае регистрации ленакапавир станет первым препаратом из нового класса ингибиторов капсида и совершенной новой опцией для пациентов, имеющих резистентность к другим препаратам антиретровирусной терапии.
В компании заявляют, что ожидают возможности поделиться данными долгосрочного наблюдения за участниками исследования с множественной резистентностью к АРТ в этом или в следующем году и представить эти данные на утверждение регуляторным органам.
Инъекционные препараты в качестве доконтактной профилактики (PrEP)
Согласно результатам исследования HPTN 083, инъекционные препараты продемонстрировали свои перспективы для применения в качестве профилактики инфицирования ВИЧ. Каботегравир, вводимый инъекционно один раз в два месяца, оказался на 69 % эффективнее ежедневного приема традиционного варианта доконтактной профилактики с таблетками для мужчин, практикующих секс с мужчинами, и трансгендерных женщин.
Кроме того, исследование HPTN 084 продемонстрировало, что доконтактную профилактику в виде инъекций можно будет применять для женщин, которые раньше были практически не вовлечены в использование PrEP.
И несмотря на то, что на сегодняшний день Россия не может похвастаться большой доступностью доконтактной профилактики, появление новых, еще более эффективных опций в виде инъекционных препаратов может способствовать распространению этого метода.
FDA уже присвоило каботегравиру пролонгированного действия для доконтактной профилактики статус прорывной терапии, а значит, регистрация и начало использования этого препарата будут максимально ускорены. Пусть это еще и не вакцина от ВИЧ, но это большой шаг к длительному и эффективному снижению риска инфицирования.
Перспективные вакцины
Несмотря на огромный прогресс в лечении ВИЧ-инфекции, разработка эффективной вакцины против ВИЧ остается труднодостижимой. Исследования вакцин продолжаются, а наиболее перспективным на сегодняшний день является кандидат в вакцины от Janssen. По задумке исследователей, мозаичная вакцина, введенная 6 раз за 12 месяцев, обеспечит ВИЧ-отрицательных людей антителами к ВИЧ, которые позволят избежать инфицирования. Ожидается, что в 2021 году будут опубликованы результаты фазы IIb исследования Imbokodo, куда были включены 2600 человек.
Британская компания ViiV Healthcare проводит клинические исследования по всему миру под названием ATLAS-2M. В них изучается эффективность инъекционной антиретровирусной терапии. Испытуемым вводят раз в 4 или 8 недель препараты Каботегравир и Рилпивирин.
Эту процедуру участники исследования должны проходить не менее 100 недель, если сами не захотят раньше выйти из программы из-за побочных эффектов. Ожидается, что первые отчетные данные будут опубликованы уже в 2019 году.
СПИД.ЦЕНТР связался с участником исследования в России, чтобы узнать, насколько программа эффективнее привычной таблеточной схемы, а также расспросил его обо всех плюсах и минусах такого лечения.
Михаил (попросил называть его этим именем) живет с ВИЧ с 2015 года, до лета 2018 года принимал АРВТ-препараты привычным способом — в виде таблеток.
Я попал в исследование ATLAS-M2 совершенно случайно. У меня есть друг, которому один врач сказал, что в экспериментальной группе есть несколько мест, и он позвал меня с собой на тестирование.
В Федеральном научно-методическом центре по профилактике и борьбе со СПИДом на Соколиной горе у меня и других испытуемых взяли кровь на скрининг. Я в программу попал, а друг — нет. Он не прошел из-за условия, что схема терапии пациента не должна меняться ни разу. Также на протяжении года вирусная нагрузка должна быть меньше 50 клеток. У меня все время, до июня этого года, была одна и та же схема.

Фотография памятки, которую выдают участникам исследования.
До начала терапии моя вирусная нагрузка была меньше 50 копий/мл и 483 CD4-лимфоцитов. После первой инъекции нагрузка тоже была меньше 50, но иммунный статус упал до 380.
На сегодняшний день у меня было уже 3 инъекции. Физических изменений я никаких не чувствую. Неприятно было только в самом начале — после первого укола, надо было привыкнуть к препарату, потом становилось все легче и легче. Побочек почти нет.
Резистентности я не боюсь. Знал, на что шел: до эксперимента мне дали подписать договор, в котором указаны возможные побочные эффекты: от головокружений, тошноты и ухудшения настроения вплоть до летального исхода. Наверное, это может быть связано с неправильным смешиванием терапии с другими лекарствами.
У меня были побочные эффекты от таблеток моей старой схемы. Если их вечером выпить и сразу не уснуть, то потом начинает кружиться голова, и уже ничего не можешь сделать. Но без серьезных последствий.
Фотография памятки, которую выдают участникам исследования. Фотография памятки, которую выдают участникам исследования.
Перед началом инъекционной схемы необходимо принимать месяц таблетки Каботегравира и Рилпивирина. Затем эти же лекарства начинают колоть в ягодицы: по препарату в каждую. Соблюдать приверженность уколам очень легко. Я записан на программу длительного действия препаратов, которые вводятся 1 раз в 8 недель. Каждый сеанс обсуждаем с врачом по WhatsApp. Хожу обычно по вторникам перед работой.
Уколов я не боюсь. Есть дискомфорт, но нет никакого страха. Хотя, конечно, в первый раз было страшновато. После укола (где-то через 5—6 часов), обычно к вечеру, когда уже больше двигаешься после работы, немного поднимается температура и ощущается боль в ягодицах.
Врачи рассказывали, что были случаи, когда люди отказывались из-за дискомфорта: кому-то больно делать уколы из-за низкого болевого порога. Такое чаще встречаются у парней, девушки более стойкие. Есть и те, кто бросают схему из-за сильных побочек, но я их не испытывал.
За полгода на инъекционной терапии могу сказать, что никаких проблем нет, я очень доволен, что смог попасть в исследование. Я не могу ответить, лучше уколы или хуже таблеток, но точно намного удобнее — не надо принимать таблетки строго по расписанию. К тому же в путешествия нет необходимости брать с собой запасы препаратов. Планирование отпуска надо обсудить с врачом, он, конечно, нехотя может дать с собой препараты для укола, но в принципе можно и опоздать с уколом на несколько дней — от двух до пяти.
Также с врачом необходимо обсуждать, если собираешься пить какие-то таблетки или витамины. Нельзя есть грейпфрут, помело, зверобой и их компоненты.
Также к исследованию мне дали календарь, расписанный до сотой недели терапии. В нем указано, что в какой день надо делать и какие анализы сдавать. Существует и дополнительная фаза исследования — до тех пор, пока спонсор не завершит его или пока терапия не перестанет быть эффективной. Посещения не будут отличаться, но будут проводить и другие анализы: например, измерение веса, частоты сердечных сокращений и другие обследования.
К сожалению, мест на исследования больше нет. Не знаю, как сюда остальные люди попали, но я нигде не слышал про терапию — это вроде закрытого клуба. Мой друг жалеет, что не попал, потому что у него 22 будильника стоят на телефоне с напоминанием вовремя выпить таблетку.
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
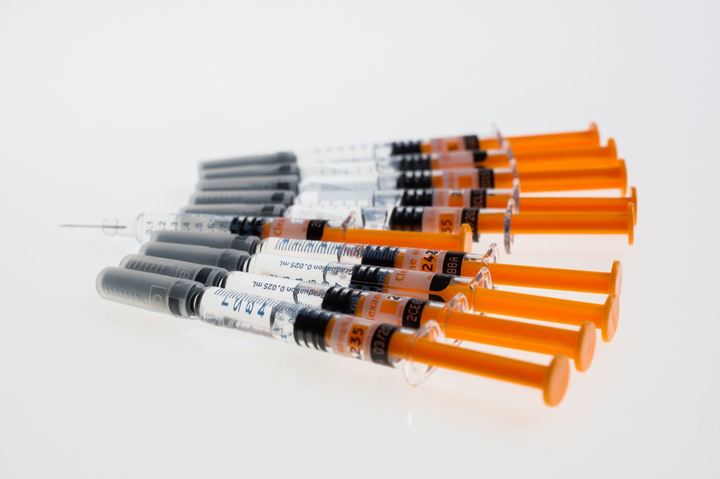
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
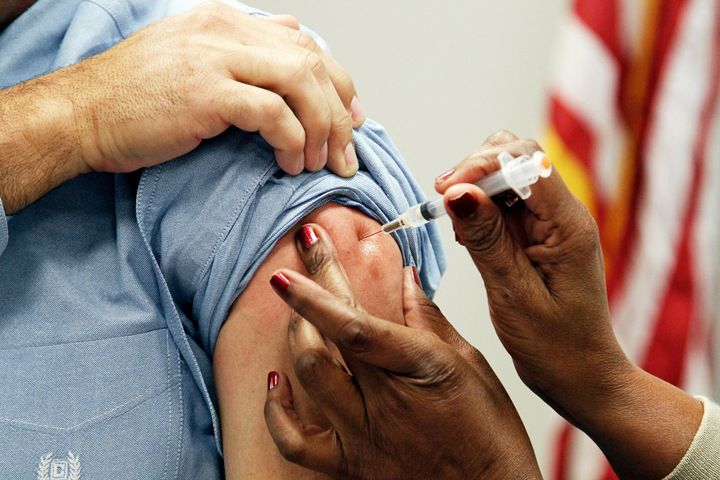
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
EMA рекомендовало выдачу регистрационного удостоверения двум новым антиретровирусным лекарствам, которые будут использоваться для лечения пациентов с инфекцией вируса иммунодефицита человека 1 типа (ВИЧ-1). Эти препараты будут первыми в своем классе – поставляться в форме инъекций длительного действия.

Комбинация инъекций Rekambys и Vocabria предназначена для поддерживающего лечения взрослых с неопределяемым уровнем ВИЧ в крови (вирусная нагрузка менее 50 копий/мл). Она также применима в случае, когда вирус не развил резистентность к определенному классу антител против ВИЧ (ненуклеозидным ингибиторам обратной транскриптазы и ингибиторам переноса цепи интегразы).
Стандартная терапия против инфекции ВИЧ-1 представляет собой комбинацию антиретровирусных препаратов, по крайней мере, двух разных классов. Их необходимо принимать ежедневно для подавления репликации вируса и увеличения количества клеток CD4 (лейкоцитов, которые важны для борьбы с инфекциями), что препятствует прогрессированию болезни.
Для некоторых ВИЧ-инфицированных доступность АРВ-препаратов длительного действия может оказаться большим преимуществом. Такие лекарства сокращают частоту приемов дозы и увеличивают общую удовлетворенность лечением.
Мнение Комитета EMA по лекарствам для человека основано на данных трех рандомизированных открытых клинических испытаний III фазы. В них приняли участие ВИЧ-инфицированные обоего пола, никогда не принимавшими АРВ-терапию или получавшие эффективное лечение от ВИЧ, в возрасте 18 лет или старше. Эти исследования продемонстрировали безопасность и эффективность схемы лечения с использованием Rekambys и Vocabria при назначении каждые четыре или восемь недель.
По данным ВОЗ, в 2019 году во всем мире насчитывалось 38 млн человек с ВИЧ. Хотя лекарства от ВИЧ-инфекции не существует, АРВ-терапия может сдерживать вирус, предотвращать его передачу и продлевать выживаемость пациентов.
Читайте также:

