Критерии характеризующие упб как возбудителя инфекционного процесса
Обновлено: 25.04.2024
Лабораторные исследования при инфекционных заболеваниях. Методы
Отбор проб для анализа при инфекционных заболеваниях. Для микробиологического исследования может быть отобрана любая ткань или физиологическая жидкость организма.
Выделение чистой культуры способствует увеличению количества бактерий и их точной идентификации. Для этого используют питательные среды. Если в образце присутствует нормальная микрофлора, то применяют избирательные (селективные) среды, позволяющие создать условия, неблагоприятные для роста непатогенных микроорганизмов и способствующие росту патогенной микрофлоры.
Для получения точных результатов следует выбрать оптимальный метод отбора проб и подойти к этому процессу с должной аккуратностью. При несоблюдении правил асептики контаминация проб крови микроорганизмами извне может привести к назначению неправильного лечения.
Большинство бактерий не способны существовать вне организма хозяина: облигатные анаэробы погибают под действием кислорода воздуха, а некоторые возбудители очень чувствительны к высыханию (Neisseria gonorrhoeae). Именно поэтому анализируемые образцы сразу после отбора должны быть помещены на подходящие среды или посеяны на среды для транспортировки.
Лабораторные методы исследования при инфекционных заболеваниях
Образцы могут быть проанализированы невооружённым глазом (например, для определения взрослых гельминтов в фекалиях или крови в мокроте). Микроскопия — быстрый и недорогой метод исследования, но требует высокого технического мастерства, характеризуется низкой чувствительностью: для точного определения необходимо присутствие большого количества возбудителей.
Кроме того, очень часто условно-патогенные микроорганизмы принимают за патогенные, что связано с недостаточной специфичностью метода.
Для определения возбудителя могут быть использованы различные красители (например, аурамин или окрашивание по Цилю—Нильсену для идентификации микобактерий). Уротропиновый серебряный окрашивает хитин клеточной стенки грибов и Pneumocystis jiroveci. Краситель Гимза применяют для окрашивания возбудителей малярии, лейшманий и других паразитов.
В основе иммунофлюоресцентного метода лежит применение специфических антител, помеченных флюоресцентными маркёрами. Микроскопию осуществляют в ультрафиолетовом свете, при этом возбудитель и связанные с ним антитела светятся ярко-зелёным цветом.
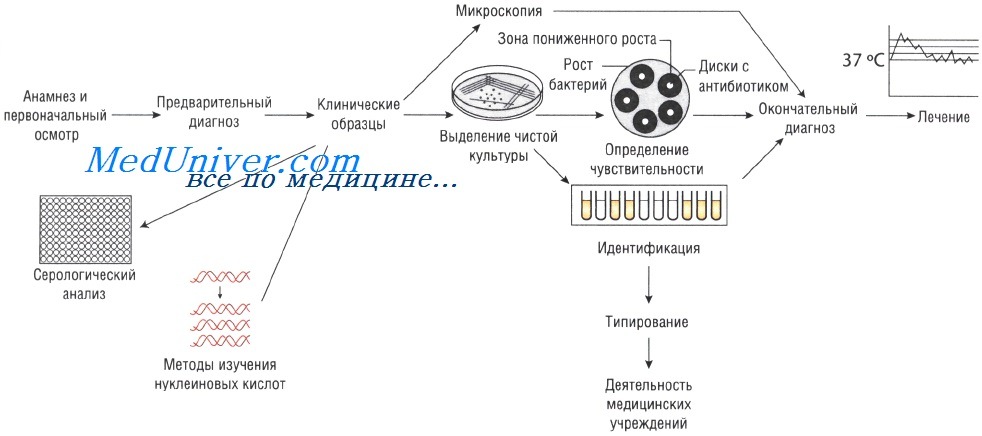
Лабораторные исследования при инфекционных заболеваниях
Выделение чистой культуры возбудителя при инфекционных заболеваниях
Иногда, даже при выраженных клинических симптомах, возбудитель может присутствовать в очаге инфекции в количестве, недостаточном для микроскопического определения. В этом случае выделение чистой культуры позволяет увеличить численность микроорганизмов в исследуемом субстрате.
Существует два способа выращивания микроорганизмов: на жидких (увеличивается количество возбудителей) и твёрдых (исследуют отдельные колонии, в том числе и на чувствительность к антибиотикам) питательных средах. Большинство возбудителей инфекций человека достаточно требовательны к условиям культивирования. Именно поэтому питательные среды для их выращивания должны содержать белки, сахарозу и нуклеиновые кислоты (присутствующие в крови и сыворотке).
Кроме того, необходимо поддерживать соответствующий газовый состав: для культивирования анаэробов необходимо отсутствие кислорода, в то время как для облигатных аэробов (Bordetella pertussis) — наоборот. Оптимальная температура выращивания большинства патогенных микроорганизмов составляет 37 °С; культивирование некоторых фибов осуществляют при 30 С.
Идентификация возбудителя инфекционного заболевания
Симптомы заболеваний зависят от вида возбудителей, вызвавших их. Именно поэтому идентификация микроорганизма позволяет предположить клиническую картину вызываемого им заболевания (например, симптомы инфекции, вызванной Vibrio cholerae, отличны от таковых при заражении Shigella sonnei). Большое значение имеет выделение Neisseria meningitidis именно из спинномозговой жидкости. Идентификация микроорганизмов основана на:
• изучении морфологических свойств их колоний в агаре;
• различной окраске по Граму;
• способности возбудителей к образованию спор;
• изучении биохимических свойств (каталазный или коагулазный тесты).
Точное определение штамма обычно зависит от результатов биохимического анализа (например, уреазный тест) или обнаружения продуктов жизнедеятельности бактерий (индол). Возбудителей, которые не могут быть выращены на питательных средах, идентифицируют при помощи молекулярно-генетического метода ДНК и секвенирования (например, Trophyrema whippelii).

Определение чувствительности возбудителя инфекционного заболевания к антибиотикам
Если для эрадикации микроорганизмов достаточно стандартной дозы антимикробного препарата, то их считают чувствительными, если необходимо увеличение дозы лекарственного средства — относительно устойчивыми. Абсолютно устойчивыми (резистентными) называют возбудителей, в отношении которых антибиотикотерапия неэффективна. Существует широкий спектр различных методов определения чувствительности к антимикробным препаратам.
Методы Британской ассоциации антимикробной химиотерапии (British Society of Antimicrobial Chemotherapy — BSAQ и Института клинических лабораторных стандартов (Clinical Laboratory Standards Institute — С LSI) основаны на определении диаметра зоны слабого роста микроорганизмов на твёрдой питательной среде при применении антимикробного препарата.
Минимальную подавляющую концентрацию антибиотика измеряют с помощью Е-теста, растворения препарата в питательном бульоне или нанесения его на плотный агар. В последнем случае на засеянный исследуемыми микроорганизмами агар наносят бумажные диски, пропитанные различными антибиотиками (метод бумажных дисков).
Уровень чувствительности зависит от диаметра зоны пониженного роста бактерий. Однако тестирование in vitro предоставляет лишь приблизительные данные, так как в клинической практике многое зависит от состояния больного.

Серологический анализ при инфекционном заболевании
Различные виды инфекций можно идентифицировать с помощью определения иммунного ответа, возникающего при внедрении возбудителя. Для этого существует большое количество различных методов: реакция агглютинации (РА), реакция связывания комплемента (РСК), реакция нейтрализации (РН) и иммуноферментный анализ (ИФА). Диагноз устанавливают на основании:
• определения уровня антител (IgM) в ответ на попадание в организм чужеродного белка (антигена);
• определения антигена.
Молекулярный анализ при инфекционном заболевании
Южный блоттинг и метод гибридизации нуклеиновых кислот. Методы основаны на связывании меченой ДНК с анализируемым образцом, при условии, что он имеет определённую последовательность аминокислот. Связанный комплекс определяют по активности метки. Это достаточно быстрый и надёжный способ, который, тем не менее, уступает по чувствительности молекулярно-генетическим методам.

Метод молекулярно-генетический (NAAT)
Для диагностики инфекционных заболеваний используют несколько молекулярно-генетических методов. Механизм выделения патогенной ДНК или РНК в количестве, достаточном для постановки диагноза, для каждого метода индивидуален. Так, при молекулярно-генетическом методе ДНК возбудителя разделяют на отдельные цепи, затем синтезируют праймеры для связывания с целевыми последовательностями. Образование новой ДНК катализирует полимераза.
Основное преимущество — достижение результата даже при наличии всего лишь одной копии ДНК. Благодаря автоматизированным системам и большому выбору специальных наборов эти методы стали доступны большинству диагностических лабораторий. Новые аппараты способны выдавать результат в режиме реального времени. Генетические методы позволяют идентифицировать микроорганизмы, выращивание которых отличается сложностью или сопряжено с риском для человека (например, Mycobacterium tuberculosis и Chlamydia trachomatis).
Кроме того, их можно использовать для определения генов, кодирующих устойчивость к действию антибиотиков (например, мутационный ген rpoВ, обеспечивающий устойчивость М. tuberculosis к рифампицину). Это позволяет заранее выбрать альтернативный путь лечения инфекционных заболеваний.
Иногда необходимо проводить типирование микроорганизмов в случае их распространения в больницах или в окружающей (внебольничной) среде.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Типы патогенных микроорганизмов. Токсины
В норме организм человека населён различными бактериями и простейшими, которые не вызывают инфекционных заболеваний. Инфекционный процесс возникает при поражении патогенной микрофлорой тканей и слизистых оболочек организма хозяина. Патоген — агент, способный вызвать инфекционный процесс.
Представителей нормальной микрофлоры считают условно-патогенными (комменсалами). Патогенность — способность микроорганизма вызывать заболевание макроорганизма. Вирулентность — степень патогенности (способность вызвать тяжёлое течение заболевания).
Например, основной фактор, определяющий патогенность Streptococcus pneumoniae, — капсула, без которой этот микроорганизм не может вызвать инфекцию. В роли возбудителей могут выступать простейшие и некоторые многоклеточные организмы. Они также могут быть патогенными и условно-патогенными.
Типы патогенных микроорганизмов
Облигатные патогены практически всегда вызывают заболевание (например, Treponema pallidum, ВИЧ). Условно-патогенные микроорганизмы вызывают заболевание только при определённых условиях.
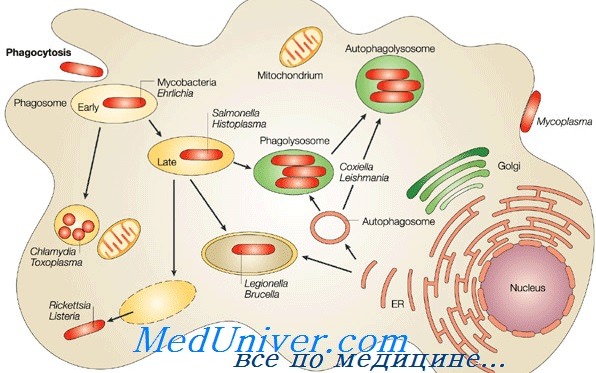
Например, Bacteroides fragilis (комменсал) — представитель нормальной микрофлоры кишечника, но при попадании в брюшную полость (особенно вместе с Е. coli) он может стать причиной абсцесса; Staphylococcus aureus является комменсалом бактериальной флоры передних отделов носовых проходов, он может быть причиной заболевания только при попадании на раневую поверхность.
Другие микроорганизмы считают оппортунистическими патогенами. Они обычно поражают людей со слабой иммунной системой. Например, Pneumocystis jiroveci может быть причиной пневмонии только у пациентов со сниженным Т-клеточным иммунитетом.
Токсины патогенных микроорганизмов
Эндотоксины — стимуляторы выработки ИЛ-1 и ФНО-а макрофагами, вызывающие развитие лихорадки и шока.
Экзотоксины — вещества белковой структуры, оказывающие местное или системное повреждающее воздействие на макроорганизм. Большинство из них состоит из нескольких субъединиц, одна из которых способствует прикреплению или проникновению в клетки-мишени, а вторая обусловливает физиологический эффект.
Классический пример — холерный токсин, В-субъединица которого связывается с эпителиальными клетками, а А-субъединица активирует аденилатциклазу и усиливает отток ионов натрия и хлора из клетки, способствуя возникновению диареи.
Некоторые экзотоксины выступают в роли суперантигенов, вызывая неспецифическую активацию Т-клеток, усиливая выработку медиаторов воспаления — цитокинов, что приводит к развитию ярко выраженных физиологических эффектов (лихорадки, шока, желудочно-кишечных расстройств, сыпи).
Некоторые экзотоксины влияют на синтез белка (например, дифтерийный токсин и синегнойный экзотоксин А), в то время как другие нарушают нервно-мышечную передачу (столбнячный и ботулиновый токсины).
В большинстве случаев антитела к токсинам нейтрализуют их эффекты и обладают протективным действием.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Лабораторные исследования при инфекционных заболеваниях. Методы
Отбор проб для анализа при инфекционных заболеваниях. Для микробиологического исследования может быть отобрана любая ткань или физиологическая жидкость организма.
Выделение чистой культуры способствует увеличению количества бактерий и их точной идентификации. Для этого используют питательные среды. Если в образце присутствует нормальная микрофлора, то применяют избирательные (селективные) среды, позволяющие создать условия, неблагоприятные для роста непатогенных микроорганизмов и способствующие росту патогенной микрофлоры.
Для получения точных результатов следует выбрать оптимальный метод отбора проб и подойти к этому процессу с должной аккуратностью. При несоблюдении правил асептики контаминация проб крови микроорганизмами извне может привести к назначению неправильного лечения.
Большинство бактерий не способны существовать вне организма хозяина: облигатные анаэробы погибают под действием кислорода воздуха, а некоторые возбудители очень чувствительны к высыханию (Neisseria gonorrhoeae). Именно поэтому анализируемые образцы сразу после отбора должны быть помещены на подходящие среды или посеяны на среды для транспортировки.
Лабораторные методы исследования при инфекционных заболеваниях
Образцы могут быть проанализированы невооружённым глазом (например, для определения взрослых гельминтов в фекалиях или крови в мокроте). Микроскопия — быстрый и недорогой метод исследования, но требует высокого технического мастерства, характеризуется низкой чувствительностью: для точного определения необходимо присутствие большого количества возбудителей.
Кроме того, очень часто условно-патогенные микроорганизмы принимают за патогенные, что связано с недостаточной специфичностью метода.
Для определения возбудителя могут быть использованы различные красители (например, аурамин или окрашивание по Цилю—Нильсену для идентификации микобактерий). Уротропиновый серебряный окрашивает хитин клеточной стенки грибов и Pneumocystis jiroveci. Краситель Гимза применяют для окрашивания возбудителей малярии, лейшманий и других паразитов.
В основе иммунофлюоресцентного метода лежит применение специфических антител, помеченных флюоресцентными маркёрами. Микроскопию осуществляют в ультрафиолетовом свете, при этом возбудитель и связанные с ним антитела светятся ярко-зелёным цветом.

Лабораторные исследования при инфекционных заболеваниях
Выделение чистой культуры возбудителя при инфекционных заболеваниях
Иногда, даже при выраженных клинических симптомах, возбудитель может присутствовать в очаге инфекции в количестве, недостаточном для микроскопического определения. В этом случае выделение чистой культуры позволяет увеличить численность микроорганизмов в исследуемом субстрате.
Существует два способа выращивания микроорганизмов: на жидких (увеличивается количество возбудителей) и твёрдых (исследуют отдельные колонии, в том числе и на чувствительность к антибиотикам) питательных средах. Большинство возбудителей инфекций человека достаточно требовательны к условиям культивирования. Именно поэтому питательные среды для их выращивания должны содержать белки, сахарозу и нуклеиновые кислоты (присутствующие в крови и сыворотке).
Кроме того, необходимо поддерживать соответствующий газовый состав: для культивирования анаэробов необходимо отсутствие кислорода, в то время как для облигатных аэробов (Bordetella pertussis) — наоборот. Оптимальная температура выращивания большинства патогенных микроорганизмов составляет 37 °С; культивирование некоторых фибов осуществляют при 30 С.
Идентификация возбудителя инфекционного заболевания
Симптомы заболеваний зависят от вида возбудителей, вызвавших их. Именно поэтому идентификация микроорганизма позволяет предположить клиническую картину вызываемого им заболевания (например, симптомы инфекции, вызванной Vibrio cholerae, отличны от таковых при заражении Shigella sonnei). Большое значение имеет выделение Neisseria meningitidis именно из спинномозговой жидкости. Идентификация микроорганизмов основана на:
• изучении морфологических свойств их колоний в агаре;
• различной окраске по Граму;
• способности возбудителей к образованию спор;
• изучении биохимических свойств (каталазный или коагулазный тесты).
Точное определение штамма обычно зависит от результатов биохимического анализа (например, уреазный тест) или обнаружения продуктов жизнедеятельности бактерий (индол). Возбудителей, которые не могут быть выращены на питательных средах, идентифицируют при помощи молекулярно-генетического метода ДНК и секвенирования (например, Trophyrema whippelii).

Определение чувствительности возбудителя инфекционного заболевания к антибиотикам
Если для эрадикации микроорганизмов достаточно стандартной дозы антимикробного препарата, то их считают чувствительными, если необходимо увеличение дозы лекарственного средства — относительно устойчивыми. Абсолютно устойчивыми (резистентными) называют возбудителей, в отношении которых антибиотикотерапия неэффективна. Существует широкий спектр различных методов определения чувствительности к антимикробным препаратам.
Методы Британской ассоциации антимикробной химиотерапии (British Society of Antimicrobial Chemotherapy — BSAQ и Института клинических лабораторных стандартов (Clinical Laboratory Standards Institute — С LSI) основаны на определении диаметра зоны слабого роста микроорганизмов на твёрдой питательной среде при применении антимикробного препарата.
Минимальную подавляющую концентрацию антибиотика измеряют с помощью Е-теста, растворения препарата в питательном бульоне или нанесения его на плотный агар. В последнем случае на засеянный исследуемыми микроорганизмами агар наносят бумажные диски, пропитанные различными антибиотиками (метод бумажных дисков).
Уровень чувствительности зависит от диаметра зоны пониженного роста бактерий. Однако тестирование in vitro предоставляет лишь приблизительные данные, так как в клинической практике многое зависит от состояния больного.

Серологический анализ при инфекционном заболевании
Различные виды инфекций можно идентифицировать с помощью определения иммунного ответа, возникающего при внедрении возбудителя. Для этого существует большое количество различных методов: реакция агглютинации (РА), реакция связывания комплемента (РСК), реакция нейтрализации (РН) и иммуноферментный анализ (ИФА). Диагноз устанавливают на основании:
• определения уровня антител (IgM) в ответ на попадание в организм чужеродного белка (антигена);
• определения антигена.
Молекулярный анализ при инфекционном заболевании
Южный блоттинг и метод гибридизации нуклеиновых кислот. Методы основаны на связывании меченой ДНК с анализируемым образцом, при условии, что он имеет определённую последовательность аминокислот. Связанный комплекс определяют по активности метки. Это достаточно быстрый и надёжный способ, который, тем не менее, уступает по чувствительности молекулярно-генетическим методам.

Метод молекулярно-генетический (NAAT)
Для диагностики инфекционных заболеваний используют несколько молекулярно-генетических методов. Механизм выделения патогенной ДНК или РНК в количестве, достаточном для постановки диагноза, для каждого метода индивидуален. Так, при молекулярно-генетическом методе ДНК возбудителя разделяют на отдельные цепи, затем синтезируют праймеры для связывания с целевыми последовательностями. Образование новой ДНК катализирует полимераза.
Основное преимущество — достижение результата даже при наличии всего лишь одной копии ДНК. Благодаря автоматизированным системам и большому выбору специальных наборов эти методы стали доступны большинству диагностических лабораторий. Новые аппараты способны выдавать результат в режиме реального времени. Генетические методы позволяют идентифицировать микроорганизмы, выращивание которых отличается сложностью или сопряжено с риском для человека (например, Mycobacterium tuberculosis и Chlamydia trachomatis).
Кроме того, их можно использовать для определения генов, кодирующих устойчивость к действию антибиотиков (например, мутационный ген rpoВ, обеспечивающий устойчивость М. tuberculosis к рифампицину). Это позволяет заранее выбрать альтернативный путь лечения инфекционных заболеваний.
Иногда необходимо проводить типирование микроорганизмов в случае их распространения в больницах или в окружающей (внебольничной) среде.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ВБИ - это любое клинически распознаваемое инфекционное заболевание, которое поражает больного в результате его поступления в больницу или обращения в нее за лечебной помощью, или инфекционное заболевание сотрудника больницы вследствие его работы в данном учреждении вне зависимости от появления симптомов заболевания до или во время пребывания в больнице ( по определению ВОЗ, 1979г.).
Факторы, влияющие на рост ИСМП:
- тесное общение пациентов и персонала крупных больничных комплексов;
- длительность пребывания пациентов в стационаре;
- нарушение правил асептики и антисептики и любые отклонения от санитарно-гигиенических норм;
- широкое использование для диагностики и лечения инвазивных технологий;
- применение лекарственных средств, подавляющих иммунитет пациента;
- появление резистентных (устойчивых) штаммов микроорганизмов.
Инфекционный процесс
Инфекционный процесс – сложный многокомпонентный процесс (цепочка событий) взаимодействия инфекционных патогенных агентов с макроорганизмом, с развитием в последующем комплекса морфологических и иммунологических изменений. Знание элементов (звеньев) инфекционного процесса помогает предотвратить ВБИ.
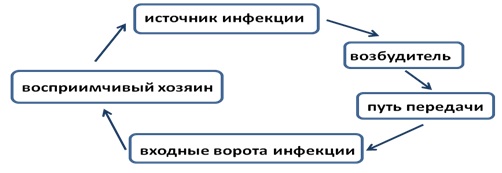
Элементы инфекционного процесса
Возбудитель
- вирусы (СПИД, гепатит, грипп…);
- бактерии (патогенные, условно патогенные);
- простейшие;
- грибки (кандида…);
- многоклеточные паразиты (гельминты, чесоточный зудень, вши).
- Вирулентность – степень, мера патогенности, индивидуально присущая каждому штамму патогенного возбудителя
- Инвазивность – способность к проникновению в ткани и органы макроорганизма и распространению в них
- Токсигенность – способность к выработке и выделению различных токсинов
- Патогенность (болезнетворность) – способность вызывать заболевание. Виды микроорганизмов по типу действия:
- патогенные – вызывающие развитие инфекционного процесса
- условно-патогенные – вызывают развитие инфекционного заболевания только при определенных условиях
- непатогенные – никогда не вызывают заболевание
Источник (резервуар)
- пациенты;
- персонал;
- посетители;
- больные и носители
Основные резервуары микроорганизмов во внешней среде
- дыхательная аппаратура;
- медицинское оборудование и инструментарий;
- поверхности, находящиеся вблизи пациентов;
- предметы ухода;
- дезинфицирующие растворы пониженной концентрации;
- медикаменты;
- емкости для воды;
- системы кондиционирования.
Восприимчивый хозяин
Восприимчивый хозяин - организм, имеющий слабую сопротивляемость. Факторы риска для заражения являются:
Типы патогенных микроорганизмов. Токсины
В норме организм человека населён различными бактериями и простейшими, которые не вызывают инфекционных заболеваний. Инфекционный процесс возникает при поражении патогенной микрофлорой тканей и слизистых оболочек организма хозяина. Патоген — агент, способный вызвать инфекционный процесс.
Представителей нормальной микрофлоры считают условно-патогенными (комменсалами). Патогенность — способность микроорганизма вызывать заболевание макроорганизма. Вирулентность — степень патогенности (способность вызвать тяжёлое течение заболевания).
Например, основной фактор, определяющий патогенность Streptococcus pneumoniae, — капсула, без которой этот микроорганизм не может вызвать инфекцию. В роли возбудителей могут выступать простейшие и некоторые многоклеточные организмы. Они также могут быть патогенными и условно-патогенными.
Типы патогенных микроорганизмов
Облигатные патогены практически всегда вызывают заболевание (например, Treponema pallidum, ВИЧ). Условно-патогенные микроорганизмы вызывают заболевание только при определённых условиях.
![патогенные микроорганизмы]()
Например, Bacteroides fragilis (комменсал) — представитель нормальной микрофлоры кишечника, но при попадании в брюшную полость (особенно вместе с Е. coli) он может стать причиной абсцесса; Staphylococcus aureus является комменсалом бактериальной флоры передних отделов носовых проходов, он может быть причиной заболевания только при попадании на раневую поверхность.
Другие микроорганизмы считают оппортунистическими патогенами. Они обычно поражают людей со слабой иммунной системой. Например, Pneumocystis jiroveci может быть причиной пневмонии только у пациентов со сниженным Т-клеточным иммунитетом.
Токсины патогенных микроорганизмов
Эндотоксины — стимуляторы выработки ИЛ-1 и ФНО-а макрофагами, вызывающие развитие лихорадки и шока.
Экзотоксины — вещества белковой структуры, оказывающие местное или системное повреждающее воздействие на макроорганизм. Большинство из них состоит из нескольких субъединиц, одна из которых способствует прикреплению или проникновению в клетки-мишени, а вторая обусловливает физиологический эффект.
Классический пример — холерный токсин, В-субъединица которого связывается с эпителиальными клетками, а А-субъединица активирует аденилатциклазу и усиливает отток ионов натрия и хлора из клетки, способствуя возникновению диареи.
Некоторые экзотоксины выступают в роли суперантигенов, вызывая неспецифическую активацию Т-клеток, усиливая выработку медиаторов воспаления — цитокинов, что приводит к развитию ярко выраженных физиологических эффектов (лихорадки, шока, желудочно-кишечных расстройств, сыпи).
Некоторые экзотоксины влияют на синтез белка (например, дифтерийный токсин и синегнойный экзотоксин А), в то время как другие нарушают нервно-мышечную передачу (столбнячный и ботулиновый токсины).
В большинстве случаев антитела к токсинам нейтрализуют их эффекты и обладают протективным действием.Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.Читайте также:

