Лечение описторхоза в белокурихе
Обновлено: 25.04.2024
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Описторхоз – паразитарное заболевание, в основе которого - поражение организма человека гельминтами - описторхами.
В России более двух миллионов человек, у которых диагностировано заболевание - описторхоз. Наибольшее распространение данное заболевание получило в Западной Сибири и в Приднепровье. Новосибирская область входит в тройку лидеров по данной патологии.


Преимущества
По данным Всемирной организации здравоохранения (ВОЗ), описторхоз – одна из причин возникновения злокачественных новообразований печени
Заражение происходит при употреблении недостаточно термически обработанной рыбы (сырой, копченой, сушёной, мороженой, жареной…), с мясом которой личинки гельминтов попадают в кишечник человека, затем проникают в желчевыводящие протоки печени, где и дозревают. Спустя около 40 дней, достигнув половой зрелости, они начинают яйцевыделение. Описторхи, вопреки распространенному мнению, не размножаются. Новые паразиты могут появиться в организме человека только с повторными порциями рыбы.
Описторхоз оказывает выраженное негативное воздействие на организм заболевшего непосредственно повреждаются желчные протоки и протоки поджелудочной железы, что вызывает нарушение тока желчи и сока поджелудочной железы, появляются кисты и новообразования в ткани этих органов. Часто повышается уровень аллергизации организма в целом, снижаются общий тонус организма и работоспособность.
Симптомы
Клиническая картина болезни от момента попадания паразита в организм человека развивается в течение нескольких недель.
При остром течении болезни отмечаются повышенная температура, боли как в мышцах, так и в суставах, расстройство стула, рвота, боли в области печени и ее увеличение, необоснованные аллергические высыпания на коже. С развитием болезни все симптомы могут значительно усилиться. Также при описторхозе могут беспокоить бессонница и раздражительность. Возможно и легкое, почти бессимптомное, течение описторхоза.
При длительном хроническом течении возможно присоединение вторичной бактериальной инфекции с развитием холецистита, холангита, панкреатита.
Наличие описторхоза в организме человека ухудшает течение всех уже имеющихся у него заболеваний.
Диагностика
Наиболее достоверной диагностикой описторхоза считается нахождение яиц описторхов при микроскопии кала. Вероятность их выявления повышается при исследовании кала методом обогащения различными способами и микроскопии желчи, полученной при дуоденальном зондировании. Для качественной диагностики крайне важна высокая квалификация врача-лаборанта, проводящего исследование.
Способы лечения
Для лечения описторхоза проводится комплексная терапия, которая включает в себя противогельминтные средства, а также препараты, направленные на нормализацию функции желудочно-кишечного тракта, детоксикацию (очищение от токсических, ядовитых веществ), десенсибилизацию (уменьшение повышенной чувствительности организма к аллергену).
Предварительно врач-гастроэнтеролог назначает обследование, по результатам которого корректирует диету больного и назначает подготовительную терапию, которая включает в себя целый комплекс медикаментов, фитопрепаратов и физиопроцедуры. Данный период длится не менее 2 недель. В последующем, при отсутствии отклонений в результатах обследований и эффективности подготовительной терапии, врач назначает антигельминтный препарат.
На данный момент единственным препаратом с доказанным противоописторхозным эффектом является Бильтрицид (Празиквантел). Применение этого лекарства должно производиться под обязательным контролем врача, суточная доза для каждого пациента рассчитывается индивидуально, поскольку гибель паразитов может вызвать непредвиденную реакцию организма (аллергическую, токсическую).
После приема данного препарата проводится восстановительный курс лечения, который также планируется в индивидуальном порядке. Через 3 и 6 месяцев после начала лечения контролируется его эффективность – проводится дуоденальное зондирование и/или исследование кал.
В клинике “Евромед” подготовительный и восстановительный этапы терапии описторхоза, проводятся амбулаторно, а прием препарата Бильтрицид (Празиквантел) - в комфортных условиях стационара, под круглосуточным врачебным контролем, в течение одной ночи.
Эффективность правильно проводимой антипаразитарной терапии составляет около 95-97%.
Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ? С чем связаны возможны
 |
| Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания |
Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ?
С чем связаны возможные ошибки в диагностике?
Какова основная роль b-агонистов в терапии бронхиальной астмы?
Как назначаются кортикостероиды?
Несмотря на возросшую компетентность врачей и доступность эффективных методов лечения, смертность от бронхиальной астмы остается высокой. Предотвратить многие смертельные исходы и даже избежать большинства случаев госпитализации можно было бы при проведении правильного лечения.
Необходимо помнить, что ведение больных астмой — процесс сложный и длительный.
Недооценка степени несостоятельности дыхания. Тяжесть состояния пациента и степень несостоятельности его дыхательной системы можно не распознать, если пренебречь тщательным выяснением всех проявлений болезни и построением диаграммы измерений максимальной скорости потока (МСП) выдыхаемого воздуха.
Зачастую у больных астмой снижены виды на будущее, хотя некоторые и склонны недооценивать серьезность симптомов своего заболевания. Чтобы выявить такую недооценку, нужно подробно расспросить пациента, бывает ли у него кашель или хриплое дыхание ночью или при физической нагрузке.
Если пациентам не удается достичь наилучшей возможной функции легких, то для коррекции этого состояния необходимо для начала вычислить нормальную МСП выдыхаемого воздуха для данного пациента, пользуясь диаграммой, прилагаемой к пикфлуометру.
Если измеренная МСП более чем на 20% меньше вычисленной, стоит провести исследование обратимости этого состояния, что делается путем сопоставления МСП или жизненной емкости легких (ЖЕЛ) до и после лечения.
Необходимая терапия может состоять всего лишь в однократном приеме бронходилятатора, но если это не увеличивает МСП на 20%, то есть до вычисленного уровня, могут понадобиться более серьезные меры, например трехнедельный курс системных кортикостероидов (30 мг преднизолона в день для взрослых). Таким образом выясняется наилучший достижимый уровень МСП, на который ориентируются в последующем лечении.
Иногда пациенты сообщают об уменьшении одышки, но при этом значения МСП не изменяются. В таких случаях необходимо провести измерение ЖЕЛ с помощью спирометра, которое может подтвердить улучшение, не определяемое по МСП (рис. 2). Спирометрами в настоящее время укомплектованы все врачебные приемные.
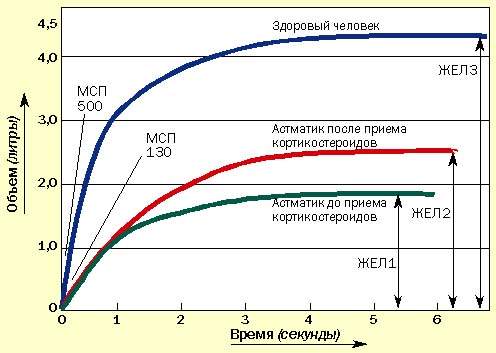 |
| Рисунок 2. Изменение ЖЕЛ под влиянием курса кортикостероидов. МСП может не измениться, но увеличение ЖЕЛ свидетельствует об улучшении состояния |
Бронхиальная астма, замаскированная под хроническое обструктивное заболевание легких (ХОЗЛ). Страдающие одышкой пациенты, которым поставлен диагноз ХОЗЛ или эмфизема, могут иметь скрытый бронхоспастический элемент, обусловленный бронхиальной астмой.
Таким пациентам необходимо провести исследование обратимости процесса, как описано выше. Любое улучшение функции легких можно поддержать, проводя адекватное лечение бронхиальной астмы. При отсутствии улучшения легочной функции назначение кортикостероидов ничем не оправдано, а только приводит к нежелательным побочным эффектам, таким как остеопороз.
Что должен помнить врач, наблюдающий больных с бронхиальной астмой
- Сказал ли я, что нужно применять спейсер при ингалировании кортикостероидов?
- Проверил ли я навыки ингаляции?
- Осмотрел ли я всех пациентов, недавно перенесших тяжелые приступы или госпитализацию?
- Все ли пациенты с повторными назначениями регулярно приходят на прием?
- Все ли я сделал, чтобы исключить астму у пациентов с ХОЗЛ?
- Проводятся ли регулярные проверки для достижения единообразного подхода к ведению астматиков?
Постоянный прием b-агонистов короткого действия. Показано, что лечение астмы постоянным приемом b-агонистов увеличивает гиперреактивность легких и утяжеляет бронхиальную астму [1]. Если пациент использует b-агонисты скорее регулярно, чем случайно, их применение должно сопровождаться назначением ингаляционных кортикостероидов или, если кортикостероиды уже применяются, увеличением их дозы до достаточной, чтобы контролировать астму. Таким образом, b-агонисты оставляют на случаи одышки и хрипов.
Последние методические указания по лечению бронхиальной астмы в Британии рекомендуют начинать с высокой дозы ингаляционных или системных кортикостероидов для достижения быстрого контроля, затем постепенно снижать дозу до минимальной, обеспечивающей нормальное самочувствие пациента и оптимальные значения МСП или ЖЕЛ на фоне минимального применения бронходилятатора (рис. 3). Быстрое облегчение состояния, достигаемое при применении кортикостероидов, улучшает настроение пациента и увеличивает его доверие к лечению.
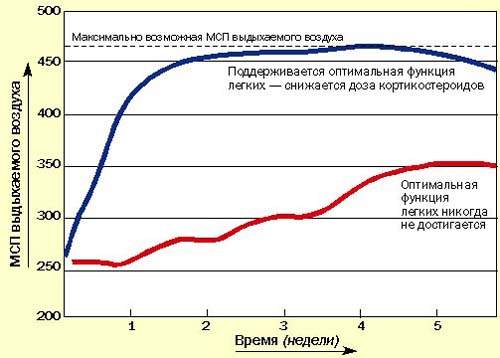 |
| Рисунок 3. Рекомендуется начинать с высоких доз кортикостероидов, а затем постепенно снижать дозу до минимальной (оптимальные значения МСП или ЖЕЛ) |
Последние данные свидетельствуют о том, что назначать кортикостероиды нужно как можно раньше всем астматикам, и не только для контролирования симптомов, но и для предотвращения прогрессирующих структурных повреждений легких, обусловленных хроническим воспалением [2,3]. Это означает, что кортикостероиды следует предпочесть b-агонистам, как только диагноз подтверждается МСП-диаграммой. b-агонисты остаются препаратами резерва на крайний случай.
Возможность альтернативного лечения. Хотя ингалируемые кортикостероиды должны быть краеугольным камнем в лечении астмы, в случаях, трудно поддающихся лечению, можно использовать и некоторые другие препараты. Доказано, что противовоспалительным эффектом обладают теофиллины в достаточно небольших дозах, но надо учитывать в каждом индивидуальном случае их возможное взаимодействие с другими препаратами.
Пожилым пациентам целесообразно назначать ипратропиум. Иногда оказываются эффективными недокромил и кромогликат.
Бронходилятаторы длительного действия, такие как сальметерол, могут облегчать состояние, особенно ночью, блокируя бронхоконстрикторные механизмы. Однако необходимо, чтобы все вышеперечисленные препараты сопровождались применением адекватных доз кортикостероидов.
Техника ингаляции. Нужно добиться, чтобы у пациентов выработались правильные навыки обращения с ингалятором. Врач должен помочь подобрать тот тип ингалятора, который наиболее удобен пациенту, и проверить его работоспособность. Для этого в кабинете врача должен быть полный набор ингаляторов.
Спейсеры. Применяемые вместе с аэрозольными ингаляторами, спейсеры облегчают проникновение препарата в легкие и снижают как накопление его в глотке, так и системное всасывание за счет проглатывания.
Спейсеры помогают координировать выброс препарата со вдохом. Это особенно важно при ингалировании кортикостероидов. Так как кортикостероиды применяются только дважды в день, громоздкий спейсер можно хранить дома.
Спейсеры обеспечивают лучшее накопление препарата в легких, чем распылители. Необходимо правильно их применять: встряхнуть ингалятор, чтобы лекарство смешалось с носителем, и однократно впрыснуть смесь с последующим скорейшим вдохом [4].
Триггерные факторы. Нераспознанные триггерные факторы могут быть и дома, и на работе, и на отдыхе, то есть практически в любом месте. Выявить источник поможет анамнез. Например, при профессиональной бронхиальной астме состояние улучшается во время отпуска и в выходные дни. Отсутствие раздражителя уменьшает или устраняет проявления болезни и снижает необходимость в лекарствах.
Проблемой, которую часто не принимают во внимание, может быть пассивное курение. Такие препараты, как b-блокаторы и нестероидные противовоспалительные средства (НПВС), также могут вызывать астму.
Использование распылителей (небулайзеров) без фоновой кортикостероидной терапии. При лечении острого астматического приступа без назначения пероральных кортикостероидов все еще используют распылители, которые обеспечивают проникновение более высокой дозы b-агонистов. Это действительно снимает бронхоспазм, но поскольку высокая доза b-агонистов не воздействует на сопутствующий воспалительный процесс, необходимо сразу же дать больному кортикостероиды внутрь, чтобы предотвратить нарастание приступа; эффект бронходилятаторов снижается по мере увеличения отека слизистой.
Если тяжесть приступа такова, что требуется небулайзер, необходимо назначить системные кортикостероиды. Даже при умеренном приступе бронходилятаторы сами по себе приносят лишь временное облегчение и есть опасность повторения приступа — возможно, глубокой ночью!
Несвоевременное назначение оральных кортикостероидов. Если не проводить противовоспалительной терапии, у больных нарастает отек слизистой, что приводит к повторению приступов. Такие пациенты часто нуждаются в госпитализации и назначении высоких доз кортикостероидов в течение нескольких дней, прежде чем у них наступит стабилизация состояния.
Пациенты, подверженные быстроразвивающимся приступам, нуждаются в как можно более раннем назначении кортикостероидов и бронходилятаторов. Они должны уметь распознавать ухудшение состояния, всегда иметь под рукой кортикостероиды и знать, как их использовать. Не следует заставлять этих пациентов дожидаться прихода к ним врача (рис. 4).
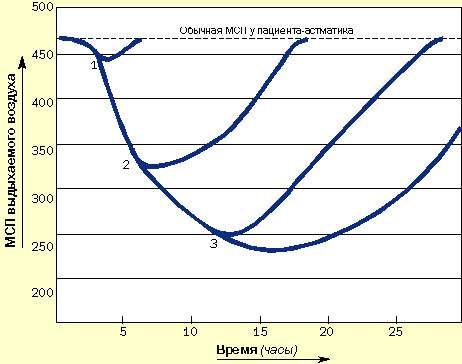 |
| Рисунок 4. Зависимость развития острых приступов от времени назначения кортикостероидов и как результат применения длительных курсов системной кортикостероидной терапии. (1) Кортикостероиды назначены сразу после возникновения приступа: выздоровление наступает быстро. (2) Кортикостероиды назначены через 6 часов: выздоровление замедлено. (3) Кортикостероиды назначены позже чем через 12 часов: приступ тяжелый и длительный, выздоровление наступает медленно |
Пациенты с постепенным развитием приступов могут подождать и посмотреть, помогает ли увеличенная доза ингаляционных кортикостероидов в сочетании с бронходилятаторами.
Неадекватный курс системных кортикостероидов. Иногда назначенные кортикостероиды отменяют до полного купирования приступа, что ведет к сохранению гиперреактивности бронхов и очередному приступу.
Подобная цепь событий может привести пациента к ложному заключению, что у него бронхиальная астма, трудно поддающаяся лечению.
Прекращение наблюдения за пациентом после острого приступа или госпитализации. Трудности возникают при отмене системного кортикостероида и назначении ингаляционного. В этот переходный период необходимо тщательное наблюдение; по достижении стабилизации состояния дозу ингалируемого кортикостероида постепенно снижают до минимально необходимой, чтобы заболевание никак себя не проявляло и функция легких была оптимальной.
Целью последующего лечения становится поддержание наивысшей МСП, достигнутой в больнице после курса системных кортикостероидов.
Консультация, проведенная через некоторое время после выписки, дает хорошую возможность проверить план ведения пациента, выяснить, что не так, и внести соответствующие поправки.
Кашель и хрипы с гнойной мокротой иногда принимают за легочную инфекцию. Однако мокрота больных астмой содержит гораздо больше эозинофилов, чем полиморфных клеток и бактерий. В пожилом возрасте левожелудочковая недостаточность и сердечная астма должны наводить на мысль о предшествующей бронхиальной астме. Будьте осторожны с b-блокаторами!
Внезапная одышка может быть обусловлена пневмотораксом или легочной эмболией. Хрипы встречаются при туберкулезе легких, бронхиальной карциноме или инородном теле и могут быть четко локализованы. Следовательно, у любого пациента с астмой, развившейся во взрослом возрасте, необходимо провести рентгенологическое исследование органов грудной клетки.
После установления диагноза основная цель врача — освободить пациента от проявлений болезни и оптимизировать функцию легких, а также установить контроль за болезнью. Для этого специально обученный медперсонал должен обучать больных и проверять правильность выполнения ими всех назначений.
Конечно, в некоторых случаях это может оказаться затруднительным, однако план предписанных действий способно усвоить абсолютное большинство больных.
Все пациенты должны:
- уметь распознать начало приступа
- знать, как применять высокие дозы b-агонистов;
- самостоятельно начать прием преднизолона внутрь;
- знать, когда звонить врачу или отправляться в больницу;
- все страдающие от приступов, должны быть обеспечены кортикостероидами.
Литература
1. Sears M. R., Taylor D. R. et al. Regular inhaled b-agonist treatment in bronchial asthma. Lancet 1990;336:1491–1396.
2. Tari Haahtela et al. Comparinson of terbutaline with budesonide in newly detected asthma. N Engl J Med 1991;325:388–392.
3. Redingon A. K., Howarth P. H. Airway remodelling in asthma. Thorax 1997;52:310–312.
4. O'Callaghan C., Barry P. Spacer devices in the treatment of asthma. BMJ 1997;314:1061–1062.
Спирометрия при хронической бронхиальной астме
Бочкообразная грудная клетка при хронической бронхиальной астме возникает из-за задержки воздуха в периферических отделах легких, что приводит к постоянному поддержанию грудной клетки в состоянии вдоха. Задержанный воздух не выдыхается и бесполезно занимает большую часть легких (остаточный объем). Это снижает объем воздуха (жизненную емкость легких), входящего в легкое.
Воздух задерживается из-за хронического воспаления, вызывающего отек слизистой периферических бронхиол. При лечении кортикостероидами отек спадает и воздух высвобождается. Это доказывается увеличением ЖЕЛ, определенной спирометрически. МСП может не изменяться (см. рис. 2.)
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Летом часто обостряются заболевания желудочно-кишечного тракта. Одна из неприятных болезней – описторхоз. Её симптомы можно легко принять за гастрит. Но точный диагноз могут поставить только в медицинских центрах. Что такое описторхоз, как он себя проявляет и куда обращаться с первыми неприятными симптомами, рассказываем в этой статье.
Что такое описторхоз?

Трематодоз, вызванный плоскими червями. Возбудитель описторхоза, попадая в организм человека, концентрируется в печени и желчевыводящей системе. Паразит попадает в организм человека из плохо термически обработанных морепродуктов – сырой, вяленой, копченой рыбы или представителей семейства карповых.
Чем опасен описторхоз?
Возбудитель заболевания двуустка кошачья паразитирует в желчном пузыре и желчных протоках и пожирает слизистую оболочку органов. Постепенно ухудшается нормальный пищеварительный процесс. Возникает дисбактериоз, появляется аллергическая реакция непонятного происхождения, воспаляются ближайшие к желчному пузырю внутренние органы, формируются камни.
Если патология появляется во время беременности, паразит оказывает угнетающее действие на развитие плода, физическое и умственное развитие. Одно из самых страшных последствий – рак печени, желчного пузыря, поджелудочной железы.
Помимо органов желудочно-кишечного тракта, у больного страдают сердце и сосуды, обмен веществ, нервная система. Как следствие, может возникать вегетососудистая дистония, бессонница, нервозность, появляется тремор конечностей, снижается аппетит, изменяется менструальный цикл.
Первые симптомы описторхоза
Первые признаки появляются при снижении защитной функции иммунитета. На ранних стадиях пациент сталкивается с появлением общей слабости, усиливается потоотделение. Острая форма описторхоза проявляется следующим образом:
появление бессонницы и нервозности;
боль в правом подреберье;
болевые ощущения в спине и животе;
наличие астматического бронхита;
ощущение ломоты в теле и повышение температуры;
появление на коже аллергических высыпаний;
присутствие метеоризма, тошноты, рвоты, болей в животе, общего дискомфорта;
резкое снижение аппетита, слишком жидкая консистенция стула.
При обследовании организма врач может обнаружить увеличенную печень, повышенное количество эозинофилов в общем анализе крови.
Симптомы описторхоза у взрослых несколько отличаются от первых признаков детей. У маленьких непосед заболевание выражается в проявлении устойчивого аллергоза, интоксикации всего организма и иммунодепрессивном состоянии. Также может повышаться температура и держаться до 2-3 недель.
Симптомы у женщин проявляются наиболее ярко во время менструального цикла. Если в печени женщины есть паразит, то менструации становятся очень болезненными, а цикл становится нестабильным.
Как быстро проявляется патология?
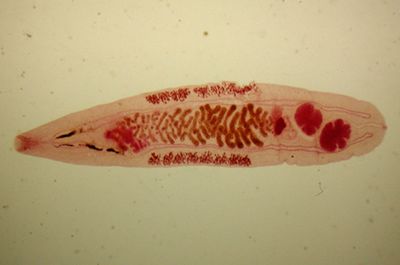
Когда паразиты попадают в организм человека, начинают снижаться защитные функции иммунитета. После этого в течение 20 дней могут проявляться первые признаки. Человек испытывает общую слабость, недомогание, учащенное сердцебиение, повышение температуры тела, сильное потоотделение.
Примерно через 30 дней заболевание переходит в хроническую стадию и его симптомы становятся похожи на хронический холецистит, гастродуоденит, панкреатит, гепатит. Беспокоят приступы боли в правом подреберье, схожие с желчными коликами. Появляется нервозность, нарушения сна, хроническая усталость, частые аллергические высыпания на коже, дрожат руки, веки.
Период острого этапа заболевания – от нескольких дней до 3 месяцев, иногда дольше. К симптомам присоединяются признаки лёгочных заболеваний, увеличивается печень, могут выявиться эрозии и язвы слизистых оболочек и тканей желудка, двенадцатиперстной кишки во время проведения исследования.
Стадии острого описторхоза
Когда же речь идет об описторхозе острой формы, то ее разделяют на 4 класса.
Тифоподобное протекание – присутствуют симптомы панкреатита, желтухи и гепатита, увеличенная печень, есть гастрит, эозинофилы в крови до 90%.
Гепатохолангетический тип – панкреатит, ноющие боли в животе, поражается печень, нарушается функция поджелудочной железы.
Гастроэнтерологический – наличие энтероколита, язвы желудка, эрозивного гастрита, наблюдаются нарушения стула.
Поражение дыхательных путей – присутствие бронхита астматического типа, плеврита и пневмонии.
Как проводится диагностика заболевания?
Первое, что нужно сделать, если обнаружили у себя признаки описторхоза, - это не заниматься самолечением, а обратиться за консультацией гастроэнтеролога. Врач проведет визуальный осмотр, соберет анамнез и направит на анализы и дуоденальное зондирование. Это метод обследования пациента, который проводится при заболеваниях желчевыводящих путей и желчного пузыря для забора желчи на лабораторное исследование.
Другие виды диагностики:
общий анализ крови;
исследование внутренних органов с помощью УЗИ;
анализ кала на яйца глистов;
полимеразная цепная реакция (ПЦР).
После проведения диагностики, врач изучает результаты всех анализов и исследований, ставит пациенту точный диагноз. После постановки точного диагноза пациенту назначается лечение. Оно проходит под строгим наблюдением.
Лечение описторхоза
Лечение патологии должно проводиться независимо от стадии и вида описторхоза. Чем быстрее начато лечение, тем меньше вероятность того, что паразит нанесет сильные увечья вашему организму.
Для того, чтобы начать лечение, необходимо иметь свежие результаты общего анализа крови и мочи, биохимический анализ крови, ФГДС, УЗИ органов брюшной полости, для пациентов старше 40 лет также ЭКГ.
Использование медикаментозных препаратов снимает воспаление. Если есть аллергические реакции, интоксикация, то эту проблему устраняют за счет использования антигистаминных средств. Назначаются желчегонные препараты, которые принимаются в назначенные врачом сроки, прописывают антибиотики. Препараты чаще всего принимаются сроком до 14 дней. Для больного устанавливается специальная диета, которую он обязан соблюдать.
После курса лечения будет сделано контрольное дуоденальное зондирование, вы получите полное медицинское заключение и рекомендации врача, которых нужно придерживаться в течение всей жизни.
После проведения противопаразитарной терапии наступает период реабилитации. Он может длиться на протяжении 3-4 месяцев, основными его задачами являются:
восстановление нормальной работы органов пищеварительной системы;
полное избавление от мертвых гельминтов, которые остались в организме;
устранение последствий жизнедеятельности гельминтов в человеческом организме.
Лечение описторхоза в Красноярске

Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Язва желудка – одно из самых распространенных заболеваний желудочно-кишечного тракта. Это хроническая патология, при которой возникают дефекты в слизистой оболочке желудка. При несвоевременном лечении или полном его отсутствии может стать причиной инвалидности человека или даже гибели.
Язвой желудка и двенадцатиперстной кишки страдают люди в возрасте от 20 до 65 лет. Мужчины от 25 до 40 лет болеют в 5-6 раз чаще женщин по той причине, что мужские половые гормоны косвенно повышают кислотность и агрессивность желудочного сока, а женские — понижают.
Строение человеческого желудка
Желудок – это орган пищеварительной системы, в котором скапливается пища, и под действием желудочного сока, подвергается первичному перевариванию с образованием кашицеобразной смеси.
Желудок по большей части располагается в верхней левой области брюшной полости. Определённой формой и размером желудок не обладает, так как они зависят от степени его наполнения, состояния его мышечной стенки (сокращённая или расслабленная) и возраста. Вместительность органа около 3 литров, длиной 21-25 см.
Желудок обладает двумя основными функциями:
- Секреторной. Выведение желудочного сока, который содержит необходимые компоненты для начальных этапов пищеварения и образования химуса (пищевого комка). За сутки примерно выделяется около 2 литров желудочного сока. При расстройстве секреторной функции желудка, у человека повышается кислотность, т.е. усиливается выделение соляной кислоты, либо снижается кислотность, сопровождаясь уменьшением выделение соляной кислоты.
- Моторной. Мышечный слой желудка сокращается, в результате чего происходит перемешивание пищи с желудочным соком, первичное переваривание и продвижение по двенадцатиперстной кишке.
Нарушения моторики желудка из-за нарушения тонуса его мышечной стенки приводит к нарушению пищеварения и эвакуации желудочного содержимого в кишечник. Это проявляется различными диспепсическими нарушениями (тошнота, рвота, вздутие, изжога и другие).
Механизм образования язвы желудка
Язва желудка, представляет собой дефект слизистой оболочки желудка, редко меньше 1см (иногда подслизистой), окружённый воспалительной зоной.
Наиболее частой причиной образования язв желудка и двенадцатиперстной кишки является инфекция Helicobacter Pylori. Различные факторы приводят к дисбалансу между защитными факторами (желудочная слизь, гастрит, секретин, гидрокарбонаты, слизисто-эпителиальный барьер желудка и другие) слизистой желудка и факторами агрессии (Helicobacter Pylori, соляная кислота и пепсин).
Под действием лечения, дефект зарастает соединительной тканью (образуется рубец). Участок, на котором образовался рубец, не обладает функциональной способностью (секреторной функцией).
Причины развития патологии
Бактерия Helicobacter Pylori (возбудитель язвы) – оказывает разрушающее действие на клетки слизистой желудка, разрушает местные факторы защиты. В результате чего образуется такой дефект, как язва. Заражение бактерией через слюну инфицированного человека (несоблюдение правил личной гигиены, использование немытой посуды после инфицированного человека).
Повышенная кислотность – развивается в результате усиленного выделения соляной кислоты, которая оказывает разъедающее действие на слизистую оболочку желудка, с последующим образованием дефекта.
Что влияет на образование язвы желудка?
- Нервно-эмоциональное перенапряжение приводит к повышению выделения желудочного сока (соляной кислоты).
- Генетическая предрасположенность к образованию язвы желудка.
- Курение, употребление алкогольных напитков, потребление кофе в больших количествах, никотин и этиловый спирт стимулируют образование желудочного сока, тем самым повышая кислотность.
- Наличие предъязвенного состояния: хронический гастрит, хроническое воспаление слизистой желудка.
- Нарушенный режим питания: еда в сухомятку, длительные перерывы между приёмами пищи приводят к нарушению выделения желудочного сока.
- Злоупотребление кислой, острой и грубой пищи.
- Длительный приём медикаментов, которые оказывают разрушительное действие на слизистую желудка.
Симптомы язвы желудка
- Болезненные ощущения. Боль при язве может беспокоить днём и ночью. Чаще всего боль при патологии проявляется во время голода. Она локализуется в верхних отделах живота, может уменьшаться или усиливаться сразу, или через время после приёма пищи в зависимости от места расположения язвенного дефекта.
Неприятные признаки язвы желудка могут быть настолько ярко выраженными, что появляется тошнотой или даже рвотой, которая усиливается с утра и проходит после приема пищи. Язва проявляет себя чаще в осенне-весенние периоды.
- Чувство тяжести в желудке. Человек часто начинает уменьшать порции еды, так как поглощение даже небольшого количества пищи, которая попадает на воспалённые участки слизистой желудка и язвы, может вызывать эти неприятные ощущения.
- Запах изо рта, налет на языке. Частые спутники любых воспалительных заболеваний верхних отделов желудочно-кишечного тракта, в том числе и гастрита (воспаления желудка), на фоне которого язвы чаще всего и появляются.
Диагностика язвы желудка
Диагностика типичной язвы желудка достаточно проста, проводится терапевтом или гастроэнтерологом. При осмотре врач определяет общее состояние пациента, выясняет жалобы, характер и особенности течения болезни, при пальпации уточняет границы болезненных зон и их характер.
Чтобы сформировать точное представление о состоянии здоровья пациента, врач может назначить общий анализ крови и инструментальное обследование. Чаще всего это эндоскопическое исследование (ЭГДС).
Процедура безопасна, длится несколько минут, сопровождается неприятными, но вполне переносимыми ощущениями. Позволяет обследовать верхние отделы желудочно-кишечного тракта, установить наличие и характер воспалительных и эрозивно-язвенных процессов, а также появление новообразований.
Лечение язвы желудка
Лечением язвенной болезни занимается терапевт или гастроэнтеролог. Оно направлено на устранение симптомов, заживление язв и ликвидацию причины этого заболевания с помощью диеты, изменения образа жизни и назначения медикаментов.
Медикаментозная терапия
Для избавления от инфекции Хеликобактер Пилори врач назначает антибиотики, а для снижения кислотности желудочного сока — кислотоснижающие препараты и др. Если язва желудка вызвана приёмом обезболивающих препаратов (НПВС) или иных медикаментов, которые могут спровоцировать развитие язвы, то врач подбирает пациенту другие препараты, у которых нет язвообразующего действия.
Сначала снимается боль с помощью обезболивающих. Принимаются препараты только при ощущении дискомфорта в желудке. Также прописываются энтеросорбенты, которые нейтрализуют негативное действие токсинов. Кроме того, больному необходимо пропить курс витаминов.
Питание
Важно при язве желудка не обострять симптомы при помощи вредных привычек. Нужно перестать курить и употреблять спиртные напитки. А также следить за своим питанием. При язве желудка должна быть назначена специальная диета.
Она предполагает полноценное питание, разделённое на 5-6 приёмов пищи в день. Ограничивается употребление сильных раздражителей желудочной секреции (кетчупов, острых специй), грубых продуктов и блюд. Пища готовится в основном протёртой, варится на пару или в воде, рыба и негрубые сорта мяса подаются кусками. Из рациона исключаются очень холодные и горячие блюда. Ограничивается приём поваренной соли.
Появление избыточного количества соляной кислоты в желудке ведет к тому, что возникают боли, пациента мучает изжога. Необходима вода, которая обладает ощелачивающим эффектом – при ее применении вредное воздействие соляной кислоты нейтрализуется.
Противоположная проблема – пониженная кислотность. В этом случае желудочного сока вырабатывается мало. Итог: пища плохо переваривается, возникает ощущение переполнения желудка.
Щелочные минеральные воды ускоряют обработку пищи и способствуют быстрому продвижению ее по желудочно-кишечному тракту.
Профилактика язвы желудка
При здоровом образе жизни, правильном питании, бережном отношении к своему здоровью вероятность появления язвы желудка крайне низкая. Как мы уже выяснили, к развитию язвы желудка приводят нарушения сна и питания, чрезмерно активный образ жизни, а также несоблюдение правил личной гигиены.
Если у родственников была язвенная болезнь, то независимо от жалоб рекомендована ЭГДС с определением кислотности желудочного сока, уточняющими биопсиями для определения инфекции H. Pylori и гистологическим изучением подозрительных участков хотя бы раз в 2 года.
Также нужно придерживаться здорового образа жизни: отказаться от вредных привычек, быть физически активным, спать ночью не менее 7 часов. Избегать стрессовых ситуаций, учиться правильно их воспринимать.
Регулярно посещать врача в рамках диспансеризации и устранять очаги хронической инфекции. Начиная с 25 лет раз в два года проходить плановое комплексное эндоскопическое обследование — ЭГДС с определением H. Pylori.
Где пройти диагностику и лечение язвенной болезни желудка в Красноярске?
Для записи заполните онлайн-форму обратной связи, указанную на сайте, или позвоните и уточните информацию по номеру телефона клиники 201-03-03.
Читайте также:

