Лечение вэб инфекции ацикловиром
Обновлено: 25.04.2024
Рак желудка и носоглотки, паркинсонизм, болезни органов дыхания, ряд аутоиммунных заболеваний и распространенный среди современных людей синдром хронической усталости – все это следствие воздействия на организм мельчайшего вируса Эпштейна-Барр (ВЭБ). Патологическая роль этого возбудителя доказана при развитии множества недугов, в том числе таких редких, как синдром Алисы в стране чудес (синдром Тодда), когда у человека нарушено визуальное восприятие собственного тела и он кажется себе значительно более крупным или маленьким, чем есть на самом деле.
История названия вируса
Вирус Эпштейна-Барр, относящийся к самым распространенным вирусам в человеческой популяции, был открыт и описан не так давно, в средине прошлого столетия. Свое название он получил в честь английского вирусолога Майкла Эпштейна и его аспирантки Ивонны Барр, которые обнаружили этот вирус и исследовали его при помощи редкого в то время устройства – электронного микроскопа, который давал ученым значительно больше возможностей, чем обычный.
До появления электронных микроскопов биолог Илья Мечников предполагал, что онкологические и другие заболевания вызывают мельчайшие вирусы, которые при помощи увеличительных линз увидеть невозможно.
Вирус Эпштейна-Барр (ВЭБ): что это такое?
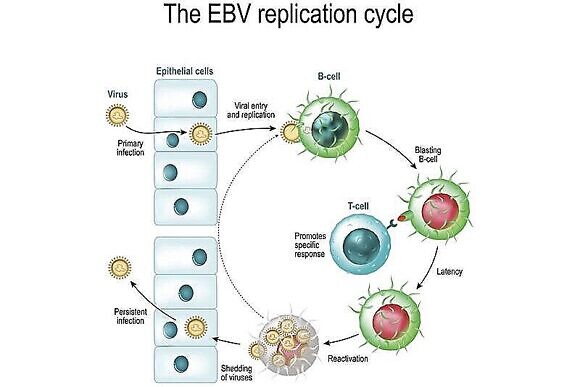
ВЭБ (или ЭБВ – аббревиатура названия вируса на английском языке: Epstein Barr Virus) входит в семейство Herpesviridae и подсемейство гамма-Herpesviridae. Это вирус герпеса 4 типа. Он способен поражать даже самых маленьких детей. Согласно статистике, более 10% детей в возрасте до года уже инфицированы этим вирусом. С течением времени и по мере взросления ребенка и его взаимодействия с окружающими людьми значительно увеличивается риск заражения. К 18 годам ВЭБ обнаруживается почти у 65% юношей и девушек вне зависимости от их образа жизни, социально-экономического статуса и отсутствия или наличия половых связей. Этот вирус встречается на всех континентах нашей планеты.
Источником заражения является инфицированный человек с типичными или стертыми, т.е. практически незаметными формами болезни. Наиболее распространенный путь передачи – воздушно-капельный. Вирус передается с частицами слюны во время разговора, при чихании и кашле, при употреблении пищи и напитков из одной посуды, при использовании общих средств гигиены и предметов обихода, в том числе игрушек у детей. Как уже упоминалось, возможна передача ВЭБ через поцелуи, а также через кровь, сперму, влагалищные и уретральные выделения. При трансплантации органов и переливании крови также может произойти заражение.
В отличие от многих других вирусов герпеса, ВЭБ при попадании в организм в первую очередь локализуется в области ротовой полости, глотки, миндалин и слюнных желез. Практически сразу же начинается активное размножение клеток вируса, после чего они распространяются по всем органам и системам. Инфицируется лимфатическая система, практически все внутренние органы, включая ЖКТ, а также кровь. Уже через несколько дней после заражения инфицированный человек начинает активно выделять вирус в окружающее пространство.
ВЭБ – персистирующая инфекция?
Обосновавшись в организме, ВЭБ у части людей приводит к развитию неверифицированной респираторной инфекции, что чаще всего все принимают за обычную простуду. Беспокоят слабость, повышается температура тела, дискомфорт в области носоглотки, увеличиваются лимфатические узлы.
Классификация заболеваний при ЭБВ
При ослабленной иммунной системе ВЭБ способен стать причиной развития следующих заболеваний:
- инфекционный мононуклеоз – острое инфекционное заболевание, которое вызывает повышение температуры тела, увеличение лимфатических узлов, поражение гортани, глотки, а также увеличение печени, селезенки и нарушение работы кровеносной системы. В ряде случаев заболевание становится хроническим и трудно поддающимся лечению.
- заболевания нервной системы. Вирусные частицы с током крови проникают в головной и спинной мозг, локализуются в периферических нервах. Возможно развитие таких заболеваний, как менингит, энцефалит и миелит. У некоторых пациентов развиваются тяжелые синдромы, параличи, острые нарушения моторики и психозы. Некоторые состояния могут требовать помощи не только невролога, но и психиатра.
- заболевания кроветворных органов. При ЭБВ нарушается функционирование кроветворного аппарата вследствие изменения состава крови, регуляции иммунного ответа и развития некоторых видов первичного иммунодефицита, вызванного влиянием ВЭБ.
- опухолевые заболевания. Вирус герпеса 4 типа может стать причиной появления ходжскинских и не-ходжскинских лимфом, лейомиосарком, а также рака носоглотки, ЖКТ и ряда других видов злокачественных новообразований.
- другие болезни. ВЭБ можно назвать одним из самых непредсказуемых вирусов, который может вызвать заболевания любых органов. Например, этот вирус способен привести к пневмониям и другим заболеваниям легких, панкреатиту, а также к такой распространенной болезни сердечно-сосудистой системы, как миокардит.
ЭБВ инфекция у детей

Вирус Эпштейна-Барр у детей нередко приводит к развитию такого заболевания, как инфекционный мононуклеоз. Инкубационный период инфекции составляет от четырех до семи недель. Развитие заболевания начинается с появления симптомов интоксикации, лихорадки, повышенной потливости, болей в горле. Поражаются ротоглотка и лимфатические узлы, печень, селезенка, наблюдаются изменения в составе крови. i
Лечение инфекционного мононуклеоза у детей проводят как амбулаторно, так и в условиях стационара, в зависимости от состояния ребенка. Методы медикаментозного лечения включают средства этиотропной и симптоматической терапии, а также средства иммунотерапии и иммунокоррекции.
Препараты интерферона альфа входят в клинические рекомендации оказания медицинской помощи детям больным инфекционным мононуклеозом, разработанные научно-исследовательским центром по лечению инфекционно-воспалительных заболеваний у детей ФГБУ НИИДИ ФМБА России.
Какой сдать анализ, как провести диагностирование и как лечиться при ВЭБ
Для диагностики применяются физикальные данные и лабораторные исследования, в том числе метод ПЦР. Обнаружение антител к ЭБВ проводится путем ИФА. По показаниям также проводятся инструментальные методы диагностики, включающие рентгенографию, биопсию, КТ, МРТ и УЗИ и ряд других анализов.
При развитии инфекционного мононуклеоза для лечения взрослых так же, как и для лечения детей, применяются препараты для проведения этиотропного и симптоматического лечения, а также противовирусные препараты с содержанием интерферонов. ii
Как уже упоминалось выше, ВЭБ является вирусом герпеса 4 типа. Одним из препаратов, применяемых для лечения заболеваний, вызванных вирусами герпеса, является ВИФЕРОН – противовирусный и иммуномодулирующий препарат, который обладает рядом уникальных фармакологических свойств.

В составе препарата содержится интерферон альфа-2b, который помогает блокировать размножение вирусов, а также помогает корректировать показатели собственного иммунитета организма. ВИФЕРОН выпускается в форме свечей (суппозиториев), мази и геля. Научно доказано, что форма выпуска обеспечивает препарату уникальные фармакодинамические характеристики, а наличие высокоактивных антиоксидантов, витаминов Е и С, позволяет усилить противовирусную активность интерферона. Для лечения герпесвирусных инфекций у взрослых применяются свечи в дозировке 1 000 000 МЕ, у беременных женщин – 500 000 МЕ, у детей – 150 000 МЕ 1 раз в 12 часов в течение пяти дней.
Эпштейна-Барр вирусная инфекция (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям человека. Антитела (Ат) к вирусу Эпштейна-Барр (ВЭБ) обнаруживают у 60% детей первых двух лет жизни и у 80–100% взрослых [3, 13]. Заболеваемость острой формой ЭБВИ (ОЭБВИ) в различных регионах мира колеблется от 40 до 80 случаев на 100 тыс. населения [2]. Хроническая форма ЭБВИ (ХЭБВИ) развивается у 15–25% лиц после ОЭБВИ [1, 5, 15]. Установлена роль ВЭБ в развитии злокачественных новообразований, аутоиммунных заболеваний и синдрома хронической усталости [3, 5, 14, 15]. Все это свидетельствует об актуальности проблемы ЭБВИ.
ВЭБ, открытый в 1964 г. M. Epstein и Y. Barr, относится к γ-герпес-вирусам [3]. ВЭБ имеет в своем составе 3 антигена: капсидный (VCA), ранний (EA) и ядерный (EBNA). Своеобразие патологического процесса при ЭБВИ определяется способностью ВЭБ к трансформации В-лимфоцитов, пожизненной персистенции в организме человека, индукции вторичного иммунодефицитного состояния (ИДС), аутоиммунных реакций, злокачественных опухолей [1, 3, 5, 12].
Источник заражения ВЭБ — больные манифестными и бессимптомными формами. 70–90% лиц, перенесших ОЭБВИ, выделяют вирус в последующие 1–18 мес. Пути передачи ВЭБ: воздушно-капельный, контактно-бытовой, парентеральный, половой, вертикальный. ОЭБВИ характеризуется эпидемическими подъемами 1 раз в 6–7 лет, чаще регистрируется в возрасте от 1 до 5 лет, в организованных коллективах [4, 7, 9].
Иммунный статус 109 больных ОЭБВИ в возрасте от 5 до 14 лет в нашей работе выявил признаки активации Т-клеточного звена иммунной системы — повышение количества Т-лимфоцитов (CD3), цитотоксических Т-лимфоцитов (CD8), клеток с маркерами поздней активации (HLA-DR); поликлональную активацию В-лимфоцитов — увеличение количества CD20-клеток, иммуноглобулинов (Ig) IgA, IgM, IgG, циркулирующих иммунных комплексов (ЦИК). Обнаружены признаки угнетения иммунной системы: нормальное содержание Т-хелперов (CD4), снижение иммунорегуляторного индекса CD4/CD8, количества естественных киллерных клеток NK (CD16), повышение готовности иммунокомпетентных клеток к апоптозу (CD95). Наблюдалась активация кислородзависимого метаболизма нейтрофилов и редукция его адаптационных возможностей.
У трети обследованных детей (33,9%) ОЭБВИ протекала в форме микст-инфекции с цитомегаловирусами (ЦМВ), вирусами простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2). При бактериологическом исследовании мазков из ротоглотки у 41,3% пациентов выделены Streptococcus (S.) viridans, у 11,9% — Candida albicans, у 8,2% — Staphilococcus (Staph.) epidermidis, у 6,4% — S. pyogenes, у 2,7% — Klebsiella (Kl.) pneumoniae, у 41,3% — ассоциация бактерий. У 43,1% пациентов — серологические маркеры активной формы хламидийной инфекции, у 30,3% — микоплазмоза.
Возможны следующие исходы ОЭБВИ: латентная инфекция, ХЭБВИ, ИДС, онкологические, аутоиммунные заболевания, синдром хронической усталости [5, 8, 10, 11]. Переход в ХЭБВИ связан с комплексом неблагоприятных факторов в анте-, интра- и постнатальном периодах, нарушением нейроиммунноэндокринной регуляции, генетической предрасположенностью.
Проведенное нами обследование 60 детей в возрасте от 5 до 14 лет с ХЭБВИ показало, что в этой группе у 86,7% матерей имел место отягощенный акушерский анамнез; у 83,3% детей обнаружены перинатальная и постнатальная патология ЦНС, ЛОР-органов и др.
Нарушения иммунного статуса приводили к активации условно-патогенной микрофлоры, вирусных и грибковых инфекций. В микробном спектре слизистой ротоглотки пациентов с ХЭБВИ выделены S. Viridans (30%), Candida albicans (28,3%), Staph. Epidermidis (25%), S. Pyogenes (20%), Kl. Pneumoniae (8,4%), ассоциация бактерий (41,7%); у 28,3% — серологические маркеры активной формы хламидиоза, у 26,7% — микоплазмоза. У 90% пациентов заболевание протекало в форме микст-инфекции с участием герпес-вирусов: ВЭБ + ЦМВ, ВЭБ + ВПГ-1, ВПГ-2.
Классификация. Общепринятая классификация заболевания отсутствует; рекомендуем использовать разработанную нами рабочую классификацию ЭБВИ.
- По периоду возникновения: врожденная, приобретенная.
- По форме: типичная (инфекционный мононуклеоз), атипичная: стертая, бессимптомная, висцеральная.
- По тяжести: легкая, среднетяжелая, тяжелая.
- По течению: острая, затяжная, хроническая.
- По фазе: активная, неактивная.
- Осложнения: гепатит, разрыв селезенки, менингоэнцефалит, полирадикулонейропатия, миокардит, синусит, отит, гемолитическая анемия, тромбоцитопения, нейтропения, панкреатит и др.
- Микст-инфекция.
Примеры оформления диагноза:
- Осн.: Приобретенная ЭБВИ, типичная тяжелая форма (инфекционный мононуклеоз), острое течение, активная фаза. Осл.: Острый гепатит.
- Осн.: Приобретенная ЭБВИ, висцеральная форма (менингоэнцефалит, гепатит, нефрит), тяжелое хроническое течение, активная фаза. Осл.: острая печеночно-почечная недостаточность. Сопp.: Респираторный хламидиоз (ринофарингит, бронхит, пневмония).
Клиническая картина острой ЭБВИ впервые была описана Н. Ф. Филатовым (1885) и Е. Пфейфером (1889). Инкубационный период длится от 4-х дней до 7 нед. Полный симптомокомплекс формируется к 4–10-му дням болезни [4, 7].
Нами обследованы 109 детей с ОЭБВИ. У большинства пациентов заболевание начинается остро, с повышения температуры тела и появления симптомов интоксикации; реже отмечается постепенное начало: несколько дней наблюдается недомогание, слабость, вялость, снижение аппетита. Температура тела субфебрильная или нормальная. Ко 2–4-му дням болезни температура достигает 39–40 °С; лихорадка и симптомы интоксикации могут сохраняться в течение 2–3 и более недель.
Тонзиллит — наиболее частый и ранний симптом ОЭБВИ, сопровождается увеличением миндалин до II-III степени. Лакунарный рисунок подчеркнут за счет инфильтрации ткани миндалин или сглажен из-за лимфостаза. На миндалинах — налеты желтовато-белого или грязно-серого цвета в виде островков, полосок. Они исходят из лакун, имеют шероховатую поверхность (напоминают кружево), легко снимаются без кровоточивости, растираются, не тонут в воде. Характерно несоответствие размера налета и степени увеличения регионарных ЛУ. При фибринозно-некротическом характере налетов в случае их распространения за пределы миндалин необходим дифференциальный диагноз с дифтерией. Налеты на миндалинах исчезают, как правило, через 5–10 дней.
Гепатомегалия может быть обнаружена с первых дней болезни, однако чаще выявляется на второй неделе. Нормализация размеров печени происходит в течение полугода. У 15–20% больных в качестве осложнения развивается гепатит.
Спленомегалия относится к поздним симптомам, встречается у большинства больных. Нормализация размеров селезенки происходит в течение 1–3 нед.
Экзантема при ОЭБВИ появляется на 3–14-й дни болезни, имеет полиморфный характер — пятнистая, папулезная, пятнисто-папулезная, розеолезная, мелкоточечная, геморрагическая. Определенной локализации нет. Сыпь наблюдается в течение 4–10 дней, иногда оставляет пигментацию. У детей, получавших ампициллин или амоксициллин, сыпь появляется чаще (90–100%).
Гематологические изменения включают лейкоцитоз (10–30 х 10 9 /л), нейтропению с палочкоядерным сдвигом влево, увеличение количества лимфоцитов, моноцитов, атипичных мононуклеаров до 50–80%, повышение СОЭ до 20–30 мм/час. Характерный гематологический признак — атипичные мононуклеары в количестве 10–50%: они появляются к концу первой недели заболевания, сохраняются в течение 1–3 нед.
Хроническая ЭБВИ является исходом ОЭБВИ или развивается как первично-хроническая форма [2, 5, 8, 10, 11, 15]. Нами обследовано 60 детей с ХЭБВИ, клиника которой включала хронический мононуклеозоподобный синдром и полиорганную патологию. У всех пациентов обнаружены лимфопролиферативный синдром (генерализованная лимфаденопатия, гипертрофия небных и глоточной миндалин, увеличение печени и селезенки) и признаки хронической интоксикации (длительный субфебрилитет, слабость, снижение аппетита и др.). Вследствие развития ИДС наблюдались острые инфекции респираторного тракта и ЛОР-органов с обострениями до 6–11 раз в год: ринофарингиты (28,3%), фаринготонзиллиты (91,7%), аденоидиты (56,7%), отиты (11,7%), синуситы (20%), ларинготрахеиты (18,3%), бронхиты (38,3%), пневмонии (25%). Обращала внимание высокая частота полиорганной патологии, обусловленная длительной репликацией ВЭБ, вторичным ИДС, аутоиммунными реакциями (патология ЦНС; хронический гастрит, дискинезия желчевыводящих путей; кардиальный синдром, артралгии).
В последние годы описана врожденная ЭБВИ. Установлено, что риск ее при первичной ЭБВИ во время беременности составляет 67%, при реактивации — 22%. Клиника врожденной ЭБВИ сходна с ЦМВИ.
Установлена роль ВЭБ в развитии онкологических заболеваний и паранеопластических процессов — лимфомы Беркетта, назофарингеальной карциномы, лимфогранулематоза, опухолей желудка, кишечника, слюнных желез, матки, лейкоплакии языка и слизистой ротовой полости, а также ряда аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена, лимфоидного интерстициального пневмонита, хронического гепатита, увеита и др. [3, 5, 14, 15]. ВЭБ, наряду с вирусами герпеса человека 6 и 7 типов, является этиологическим фактором синдрома хронической усталости и наиболее частой причиной (15%) развития длительной лихорадки неясного генеза.
Диагностика ЭБВИ основана на учете групп риска, ведущих клинических синдромов и данных лабораторного исследования [8–11]. К группам риска у матери относят отягощенный анамнез, маркеры герпес-вирусных инфекций и др., у ребенка — перинатальное поражение ЦНС, аллергический фенотип, ИДС, маркеры герпес-вирусных инфекций и др. Ведущими клиническими синдромами ЭБВИ являются мононуклеозоподобный, общеинфекционный синдромы, экзантема, синдром полиорганной патологии.
В обязательный стандарт диагностики ЭБВИ входят клинический анализ крови, общий анализ мочи, биохимическое исследование крови, бактериологическое исследование слизи ротоглотки и носа, серологические маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм, УЗИ органов брюшной полости, консультация ЛОР-врача, по показаниям — рентгенография придаточных пазух носа, органов грудной клетки, ЭКГ. Дополнительный стандарт диагностики (в специализированном лечебно-профилактическом учреждении): маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм методом полимеразной цепной реакции (ПЦР), иммунограмма второго уровня, консультация иммунолога, по показаниям — коагулограмма, морфологическая картина стернальной пункции, консультация гематолога, онколога.
Методом иммуноферментного анализа (ИФА) определяют Ат к антигенам ВЭБ, что позволяет осуществить лабораторную диагностику ЭБВИ и определить период инфекционного процесса.
Ат класса IgM к VCA появляются одновременно с клиникой ОЭБВИ, сохраняются в течение 2–3 мес, повторно синтезируются при реактивации ВЭБ. Длительная персистенция высоких титров этих Ат характерна для ХЭБВИ, ВЭБ-индуцированных опухолей, аутоиммунных заболеваний, ИДС.
Ат класса IgG к EA достигают высокого титра на 3–4-й нед ОЭБВИ, исчезают через 2–6 мес. Они появляются при реактивации, отсутствуют при атипичной форме ЭБВИ. Высокие титры Ат данного класса выявляют при ХЭБВИ, ВЭБ-индуцированных онкологических и аутоиммунных заболеваниях, ИДС.
Ат класса IgG к EBNA появляются через 1–6 мес после первичной инфекции. Затем их титр уменьшается и сохраняется в течение всей жизни. При реактивации ЭБВИ происходит повторное увеличение их титра.
Большое значение имеет исследование авидности Ат класса IgG (прочности связывания антигена с Ат). При первичной инфекции сначала синтезируются Ат с низкой авидностью (индекс авидности (ИА) менее 30%). Для поздней стадии первичной инфекции характерны Ат со средней авидностью (ИА — 30–49%). Высокоавидные Ат (ИА — более 50%) образуются через 1–7 мес после инфицирования ВЭБ.
Серологическими маркерами активной фазы ЭБВИ являются Ат IgM к VCA и Ат IgG к EA, низкая и средняя авидность Ат IgG к маркерам неактивной фазы, Ат IgG к EBNA.
Материалом для ПЦР служат кровь, ликвор, слюна, мазки со слизистой ротоглотки, биоптаты органов и др. Чувствительность ПЦР при ЭБВИ (70–75%) ниже, чем при других герпесвирусных инфекциях (95–100%). Это связано с появлением ВЭБ в биологических жидкостях лишь при иммуноопосредованном лизисе инфицированных В-лимфоцитов.
На основании опыта лечения 169 детей с ЭБВИ нами разработан стандарт лечения этого заболевания.
Базисная терапия: охранительный режим; лечебное питание; противовирусные препараты: вироцидные препараты — инозин пранобекс (Изопринозин), аномальные нуклеозиды (Валтрекс, Ацикловир), Арбидол; препараты ИФН — рекомбинантный ИФН α-2β (Виферон), Кипферон, Реаферон-ЕС-Липинт, интерфероны для в/м введения (Реаферон-EC, Реальдирон, Интрон А, Роферон А и др.); индукторы ИФН — Амиксин, сверхмалые дозы антител к γ-ИФН (Анаферон), Циклоферон, Неовир. По показаниям: локальные антибактериальные препараты (Биопарокс, Лизобакт, Стопангин и др.); системные антибактериальные препараты (цефалоспорины, макролиды, карбапенемы); иммуноглобулины для внутривенного введения (Иммуновенин, Габриглобин, Интраглобин, Пентаглобин и др.); витаминно-минеральные комплексы — Мульти-табс, Вибовит, Санасол, Киндер Биовиталь гель и др.
Интенсификация базисной терапии по показаниям:
Симптоматическая терапия.
При лихорадке — жаропонижающие препараты (парацетамол, ибупрофен и др.); при затруднении носового дыхания — назальные препараты (Изофра, Полидекса, Називин, Виброцил, Адрианол и др.); при сухом кашле — противокашлевые препараты (Глаувент, Либексин), при влажном кашле — отхаркивающие и муколитические препараты (АмброГЕКСАЛ, бромгексин, ацетилцистеин и др.).
Эффективность этиотропной терапии ОЭБВИ оценена в двух группах больных. Пациенты 1-й группы (52 человека) получали инозин пранобекс (Изопринозин) в сочетании с рекомбинантным ИФН α-2β (Вифероном), больные 2-й группы (57 детей) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Клинико-серологические показатели до начала лечения и через 3 мес терапии представлены в табл. 1. У пациентов обеих групп в динамике отмечалось достоверное уменьшение таких симптомов, как генерализованная лимфаденопатия, тонзиллит, аденоидит, гепатомегалия и спленомегалия. Вместе с тем на фоне комбинированной терапии, положительная динамика клинических показателей была более значительной; острые респираторные инфекции (ОРИ) лишь у 19,2% больных 1-й группы и у 40,3% больных 2-й группы (p < 0,05). На фоне комбинированной терапии наблюдалось более быстрое исчезновение серологических маркеров репликации.
Эффективность этиотропной терапии исследована у 60 больных ХЭБВИ. Пациенты 1-й группы (30 детей) получали инозина пранобекс (Изопринозин) и рекомбинантный ИФН α-2β (Виферон), 2-я группа (30 человек) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Независимо от схемы лечения через 3 мес после начала терапии отмечалось достоверное уменьшение частоты генерализованной лимфаденопатии, гипертрофии небных и глоточной миндалин, спленомегалии, интоксикационного, инфекционного и вегето-висцерального синдромов (табл. 2). Комбинация инозина пранобекса (Изопринозина) с рекомбинантным ИФН α-2β (Вифероном) способствовало более существенной динамике клинических показателей. Количество эпизодов ОРИ снизилось с 6–11 (7,9 ± 1,1) до 4–6 (5,2 ± 1,2) в год на фоне монотерапии рекомбинантным ИФН α-2β (Вифероном), и до 2–4 (2,5 ± 1,4) в год на фоне комбинированной терапии (p < 0,05). В обеих группах уменьшалась частота репликации ВЭБ, однако при сочетанном применении противовирусных препаратов этот эффект был более выраженным.
Побочных эффектов при использовании инозина пранобекса (Изопринозина) и рекомбинантного ИФН α-2β (Виферона) не было.
Результаты проведенного исследования свидетельствуют о потенцировании эффектов при комбинации инозина пранобекса (Изопринозина) с рекомбинантным ИФН a-2b (Вифероном) у больных ЭБВИ.
Потенцирование противовирусных, иммуномодулирующих и цитопротекторных эффектов этих препаратов приводит к более существенной, чем при монотерапии, положительной динамике проявлений клинических симптомов ЭБВИ, к исчезновению серологических маркеров активности инфекционного процесса. Следует отметить высокую эффективность и безопасность комбинированной терапии с использованием инозина пранобекса (Изопринозина) и рекомбинантного ИФН α-2β (Виферона).
Реабилитация. Ребенок наблюдается участковым врачом и инфекционистом, снимается с учета через 6–12 мес после исчезновения клинико-лабораторных показателей активности инфекционного процесса. Кратность осмотров — 1 раз в месяц. По показаниям рекомендуют консультацию ЛОР-врача, иммунолога, гематолога, онколога и др. Лабораторные и инструментальные исследования пациентов включают: клинический анализ крови 1 раз в месяц в течение 3 мес, затем 1 раз в 3 месяца, по показаниям — чаще; серологические маркеры ВЭБ методом ИФА один раз в три месяца, по показаниям — чаще; ПЦР крови, мазков из ротоглотки 1 раз в 3 месяца, по показаниям — чаще; иммунограмма — 1 раз в 3–6 мес; биохимическое и инструментальное исследования — по показаниям.
Реабилитационная терапия включает: охранительный режим, лечебное питание, противовирусные препараты по пролонгированным схемам. Под контролем иммунограммы осуществляют иммунокоррекцию. По показаниям назначают локальные антибактериальные препараты, курсы витаминно-минеральных комплексов, про- и пребиотиков, препаратов метаболической реабилитации, энтеросорбентов, антигистаминные препараты, гепато-, нейро- и ангиопротекторы, кардиотропные препараты, ферменты, гомеопатические средства, немедикаментозные методы лечения.
Таким образом, ЭБВИ характеризуется широким распространением, длительным течением с периодической реактивацией инфекционного процесса у части пациентов, возможностью развития осложнений и неблагоприятных исходов (онкозаболеваний, аутоиммунной патологии). Важную роль при ЭБВИ играет формирование вторичного ИДС. Ведущими клиническими синдромами ЭБВИ являются острый и хронический мононуклеозоподобный синдромы, интоксикационный, инфекционный, церебральный, гастроинтестинальный, кардиальный и артралгический синдромы. Диагностика ЭБВИ основана на анализе групп риска, выделении ведущих клинических синдромов и лабораторном исследовании. Лечение ЭБВИ является комплексным и включает этиотропные средства (виростатические препараты, интерферон и его индукторы), препараты патогенетической, иммуномодулирующей, симптоматической терапии. Сочетанное пролонгированное использование инозина пранобекс (Изопринозина) и рекомбинантного ИФН α-2β (Виферона), потенцирующих свои иммунокорригирующие и цитопротекторные эффекты, существенно повышает эффективность лечения. Больные ЭБВИ нуждаются в длительной реабилитации с обязательным контролем клинико-лабораторных показателей активности инфекционного процесса.
По вопросам литературы обращайтесь в редакцию.
Э. Н. Симованьян, доктор медицинских наук, профессор
В. Б. Денисенко, кандидат медицинских наук
Л. Ф. Бовтало, кандидат медицинских наук
А. В. Григорян
Ростовский ГМУ, Ростов-на-Дону
Герпесвирусы широко распространены в человеческой популяции. После первичного инфицирования вирусы герпесгруппы переходят в латентное состояние и пожизненно персистируют в организме. При неблагоприятных условиях и снижении местного или системного иммунитета может происходить реактивация инфекции, что обусловливает развитие воспаления чаще всего на местном уровне. Разнообразие клинических форм герпесвирусных инфекций постоянно поддерживает научный интерес как в области изучения их патофизиологии, так и в области поиска эффективной противовирусной терапии. Особенно актуально это для β- и γ-герпесвирусов, т. к. группа α-герпесвирусов изучена достаточно хорошо.
Цель исследования: определить эффективность валацикловира в отношении репликации вируса Эпштейна – Барр (ВЭБ), вируса герпеса человека 6 типа (ВГЧ-6), цитомегаловируса (ЦМВ) в ротоглотке у часто болеющих взрослых с хроническими воспалительными заболеваниями верхних дыхательных путей (ВДП).
Материал и методы: нами амбулаторно обследованы 80 пациентов с частыми рецидивами хронических воспалительных заболеваний ВДП. Всем пациентам проводились микробиологическое исследование мазков из ротоглотки и оценка вирусной нагрузки в смешанной слюне и цельной крови вне периода обострения. Пациенты получали терапию валацикловиром по схеме 500 мг 3 р./сут в течение 14 дней. Контроль вирусной нагрузки в биоматериале проводился после окончания лечения.
Результаты и обсуждение: микробный пейзаж ротоглотки часто болеющих взрослых вне периода обострения представлен преимущественно нормальной или условно-патогенной микрофлорой. В смешанной слюне обнаруживалась ДНК ВЭБ, ВГЧ-6, но не ЦМВ. При этом в образцах крови указанных пациентов ДНК вирусов герпесгруппы не выявлялась. Применение валацикловира в дозе 500 мг 3 р./сут достоверно снижает репликацию ВЭБ в ротоглотке у часто болеющих взрослых.
Выводы: целесообразно провести дальнейшие исследования по определению режима дозирования и оценке клинической эффективности ациклических нуклеозидов в лечении ВЭБ-инфекции.
Ключевые слова: герпесвирусы, вирус Эпштейна – Барр, вирус герпеса человека, цитомегаловирус, часто болеющие взрослые, вирусная нагрузка, валацикловир.
Human herpesviruses infections: clinical features and opportunities of therapy
R.V. Shubelko 1 , I.N. Zuykova 2 , A.E. Shulzhenko 2
1 JSC "K+31", Moscow
2 “National Research Center — Institute of Immunology” Federal Medical-Biological Agency of Russia, Moscow
Herpesviruses are widely spread among the human population. After the primary infection, the herpesviruses become latent and persistent in the human body for life. Adverse conditions and a low local or systemic immunity may reactivate the infection, which causes the inflammation, usually at the local level. The variety of clinical forms of herpesviruses infections constantly supports scientific interest both in the field of studying their pathophysiology and in the search for effective antiviral therapy. This is especially important for β- and γ-herpesviruses, since the α-herpesvirus group has been studied rather well.
Aim: to determine the efficacy of valacyclovir for replication of the Epstein-Barr virus (EBV), human herpesvirus type 6 (HHV-6), cytomegalovirus (CMV) in the oropharynx in frequently ill adults with chronic inflammatory diseases of the upper respiratory tract.
Patients and Methods: 80 patients with frequent recurrences of chronic inflammatory diseases of the upper respiratory tract were examined outpatiently. All patients underwent microbiological examination of swabs from the oropharynx and the viral load in mixed saliva and whole blood not in exacerbation period was assessed. Patients received valacyclovir therapy according to the scheme 500 mg x 3 times a day for 14 days. Control of viral load in the biomaterial was carried out after the end of treatment.
Results and Discussion: out of the period of exacerbation the oropharynx microflora in frequently ill adults is represented mainly by a normal or conditionally pathogenic microflora. EBV DNA, HHV-6, but not CMV DNA, were detected in the mixed saliva. The DNA of the herpesvirus was not detected in the blood samples of these patients. The use of valacyclovir in a dose
of 500 mg 3 times a day significantly reduces the replication of EBV in the oropharynx in frequently ill adults.
Conclusions: it is advisable to conduct further studies to determine the dosage regimen and evaluate the clinical efficacy of acyclic nucleosides in the treatment of EBV infection.
В статье рассмотрены клинические особенности и возможности терапии герпесвирусных инфекции человека. Определена эффективность валацикловира в отношении репликации вируса Эпштейна – Барр, вируса герпеса человека 6 типа, цитомегаловируса.
Введение
Герпесвирусы широко распространены в человеческой популяции и обладают большим разнообразием клинических проявлений, поражая различные органы и ткани. В настоящее время известно 8 видов герпесвирусов человека, разделенных на 3 группы: α-герпесвирусы — вирусы простого герпеса 1 и 2 типа (ВПГ-1, -2), вирус ветряной оспы (ВВО), β-герпесвирусы: цитомегаловирус (ЦМВ), вирус герпеса человека 6 типа (ВГЧ-6), ВГЧ-7 и γ-герпесвирусы: вирус Эпштейна – Барр (ВЭБ) и ВГЧ-8 [1, 2].
По данным ВОЗ, около 90% населения земного шара инфицированы одним или несколькими видами герпесвирусов. Первичное инфицирование, как правило, происходит в детском возрасте, после чего вирусы герпесгруппы переходят в латентное состояние, которое характеризуется отсутствием вирусной репликации и экспрессией вирусных белков. Реактивация герпесвирусов из латентной формы происходит на фоне транзиторных (инфекция, неблагоприятные факторы внешней среды, психоэмоциональные перегрузки, эндокринные нарушения и др.) или стойких (первичные или вторичные иммунодефициты, иммуносупрессивная терапия) иммунодефицитных состояний.
Распространенность герпесвирусов в мире и широкий клинический полиморфизм потенцируют проведение большого количества исследований в области изучения патофизиологии и иммунобиологии этой инфекции, а также поиск эффективной противовирусной терапии [1–3].
В своей практической деятельности врачи многих специальностей, в т. ч. и иммунологи, встречаются с заболеваниями, вызванными ВПГ 1 и 2 типа (лабиальный и генитальный герпес), ВВО (ветряная оспа, опоясывающий лишай), для которых разработаны и стандартизированы методы диагностики и терапии. Однако патофизиология и патоморфология хронических герпесвирусных инфекций, обусловленных β- и γ-герпесвирусами, недостаточно изучены, не разработаны четкие методы и стандарты их лечения, что создает определенные трудности в ведении таких пациентов.
Вирус Эпштейна – Барр
Цитомегаловирус
ЦМВ относится к семейству β-герпесвирусов. Для постнатальной цитомегаловирусной инфекции (ЦМВИ) входными воротами служат чаще всего слизистые оболочки ротоглотки и слюнные железы, где и происходит первичная репродукция вируса. Первичное инфицирование ЦМВ иммунокомпетентных лиц обычно протекает бессимптомно, лишь в 5% случаев — в виде мононуклеозоподобного синдрома (цитомегаловирусный мононуклеоз). Отличительными признаками острого процесса являются высокая лихорадка, интоксикационный синдром, сиалоаденит (чаще околоушных слюнных желез), фарингит, гепатомегалия, спленомегалия, выраженный и длительный астенический синдром. При этом для острого процесса поражение миндалин нехарактерно, увеличение регионарных лимфатических узлов отмечается редко. После разрешения первичной ЦМВИ вирус персистирует в латентном состоянии в моноцитах, эпителиальных клетках и клетках слюнных желез, которые являются резервуаром вирусных частиц.
ЦМВИ у взрослых протекает в латентной (локализованной) и генерализованной формах. Латентная форма обычно не проявляется четкими клиническими симптомами. Иногда наблюдаются легкие гриппоподобные состояния, субфебрилитет. У женщин латентно протекающая ЦМВИ может проявляться в виде повторного невынашивания беременности и мертворождения, а также в виде вульвовагинита, кольпита, цервицита, эндометрита, сальпингоофорита.
Генерализованная форма приобретенной ЦМВИ у взрослых наблюдается редко, чаще на фоне иммуносупрессии, и, безусловно, является прерогативой наблюдения инфекционистов. При этом могут поражаться желудочно-кишечный тракт (гепатит, сиалоаденит, эзофагит, гастрит, энтероколит), надпочечники (адреналит), бронхолегочная система (интерстициальная пневмония, бронхит, фиброзирующий бронхиолит, альвеолит), нервная система (энцефаловентрикулит, миелит, полирадикулопатия, полинейропатия), почки, глаза, миокард [1–3].
У иммунокомпетентных взрослых ЦМВ не поражает лимфоидную ткань, а его локальная реактивация проявляется репликацией в клетках эпителия слюнных желез, поэтому, вероятнее всего, он не играет какой-либо роли в развитии хронических воспалительных заболеваний ВДП у взрослых, характеризующихся в первую очередь поражением лимфоидных структур ротоглотки.
Вирус герпеса человека 6 типа
Еще один представитель семейства β-герпесвирусов — ВГЧ-6. Ведущий путь передачи герпесвирусной инфекции, вызванной ВГЧ-6, — воздушно-капельный. В таких случаях первичная репликация происходит в слюнных железах, лимфоидной ткани ротоглотки и шейных лимфатических узлах. Генерализация инфекции может происходить гематогенным или лимфогенным путем. Около 90% инфицированных клеток представлено Т-лимфоцитами (преимущественно CD4+), оставшаяся часть включает В-лимфоциты, моноцитарно-макрофагальные, глиальные клетки и мегакариоциты. Первичная ВГЧ-6-инфекция может протекать бессимптомно, в виде внезапной экзантемы, фебрильных или нефебрильных судорог.
На сегодняшний день считается доказанной роль ВГЧ-6 в формировании инфекционного мононуклеоза (или мононуклеозоподобного синдрома), который характеризуется непродолжительной фебрильной лихорадкой, умеренно выраженными симптомами интоксикации, умеренной лимфоаденопатией, поражением лимфоидной ткани ротоглотки (острый тонзиллит), умеренной гепатомегалией и, в половине случаев, спленомегалией, розеолоподобными высыпаниями (внезапная экзантема). В дальнейшем ВГЧ-6 переходит в латентную или персистирующую форму. Системная реактивация ВГЧ-6 чаще наблюдается у иммунокомпрометированных лиц и может приводить к развитию тяжелых органных поражений (энцефалит, пневмонит, миокардит и др.) и потенциально летальных системных поражений (вирусный сепсис) [1–3, 5].
К числу основных зон персистенции ВГЧ-6 относятся моноциты слюнных желез и лимфоидная ткань ротоглотки [2, 3, 5], поэтому реактивация хронической инфекции у иммунокомпетентных взрослых может происходить по типу мононуклеозоподобного синдрома, с воспалением слизистых оболочек и лимфоидных структур ротоглотки (тонзиллит, фарингиты). Не исключено также, что ВГЧ-6 играет определенную роль в снижении мукозального иммунитета ротоглотки и поддержании хронического воспалительного процесса на местном уровне.
Лечение герпесвирусных инфекций
Материал и методы
Результаты
Первичная герпесвирусная инфекция, обусловленная ВЭБ, ЦМВ, ВГЧ-6, протекает в большинстве случаев в виде инфекционного мононуклеоза. В дальнейшем герпесвирусы пожизненно персистируют в макроорганизме, в т. ч. и в области входных ворот инфекции (лимфоидная ткань ротоглотки). При неблагоприятных условиях и снижении местного или системного иммунитета может происходить локальная реактивация герпесвирусов, провоцируя развитие воспаления на местном уровне.
Микробный пейзаж ротоглотки у часто болеющих взрослых вне периода обострения представлен преимущественно нормальной или условно-патогенной микрофлорой.
В смешанной слюне часто болеющих взрослых вне периода обострения с высокой частотой достоверности обнаруживается ДНК ВЭБ, ВГЧ-6, и не обнаруживается ДНК ЦМВ. При этом в образцах крови указанных пациентов ДНК вирусов герпесгруппы не выявлена, что свидетельствует не о системной, а о преимущественно местной реактивации герпесвирусной инфекции. Учитывая, что титры вирусной нагрузки ВЭБ при микст-инфекции выше (4,47 Lg, копий/10 5 клеток), чем при моноинфекции
(3,99 Lg, копий/105 клеток), можно предположить стимулирующее влияние ВГЧ-6 на активность ВЭБ.
Стандартная антибактериальная терапия без учета вирусной репликации зачастую неэффективна или недостаточно эффективна. Применение противовирусной терапии ациклическими нуклеозидами в комплексном лечении пациентов с частыми рецидивами хронических воспалительных заболеваний ВДП позволяет повысить целенаправленность этиотропной терапии текущего воспалительного процесса.
Из ациклических нуклеозидов наиболее оптимальным и исследованным в лечении герпесвирусов является валацикловир, обладающий высокой биодоступностью и хорошим профилем безопасности. В нашей работе мы применяли дозу валацикловира в 2 раза меньшую, чем та, которая ранее апробировалась разными исследователями, главным образом потому, что мы воздействовали не на острый системный процесс, а на локальную реактивацию герпесвирусной инфекции. Выяснилось, что применение валацикловира в дозе 500 мг 3 р./сут достоверно снижает репликацию ВЭБ в ротоглотке у пациентов с микст-инфекцией (ВЭБ + ВГЧ-6) — на 75%, в большей степени у пациентов с моноинфекцией (ДНК ВЭБ) — на 86%. В отношении инфекции, вызванной ВГЧ-6, не получено достоверных данных о снижении вирусной нагрузки.
Выводы
У часто болеющих взрослых микробный пейзаж вне периода обострения представлен сочетанной бактериально-вирусной микрофлорой: нормальной и/или условно-патогенной бактериальной флорой и представителями герпесгруппы (ВЭБ, ВГЧ-6), что может играть роль в хронизации воспаления в ротоглотке, способствовать снижению местного иммунитета и приводить к частым обострениям патологии ВДП.
Применение валацикловира в дозе 500 мг 3 р./сут в течение 14 дней оказалось эффективным в отношении ВЭБ — на фоне терапии вирусная нагрузка снижалась до нулевых или клинически незначимых титров.
Валацикловир обладает хорошей переносимостью и безопасностью как у молодых пациентов, так и у пациентов старшего возраста.
Дальнейшие исследования должны быть направлены на оценку клинической эффективности валацикловира в лечении реактивации ВЭБ-инфекции у часто болеющих взрослых.
1. Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis / Eds A. Arvin, G. Campadelli-Fiume et al. Cambridge: Cambridge University Press, 2007. 1432 p.
2. Исаков В. А., Архипова Е. И., Исаков Д. В. Герпесвирусные инфекции человека. СПб.: СпецЛит., 2013. 670 с. [Isakov V.A., Arkhipova Ye.I., Isakov D. V. Gerpesvirusnyye infektsii cheloveka. SPb.: SpetsLit., 2013. 670 s. (in Russian)].
3. Иммунотерапия: Руководство для врачей / под ред. Хаитова Р. М., Атауллаханова Р. И., Шульженко А. Е. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа, 2018. 768 с. [Immunoterapiya: Rukovodstvo dlya vrachey / pod red. Khaitova R. M., Ataullakhanova R. I., Shul’zhenko A. Ye. 2-ye izd., pererab. i dop. M.: GEOTAR-Media, 2018. 768 s. (in Russian)].
4. Lennon P., Crotty M., Fenton J. E. Infectious mononucleosis // British Medical Journal. 2015. Vol. 350. P. 1–7.
5. Agut H., Bonnafous P., Gautheret-Dejean A. Laboratory and Clinical Aspects of Human Herpesvirus 6 Infection // Clinical Microbiology Reviews. 2015. Vol. 28 (2).
P. 313–335. doi: 10.1128/CMR.00122–14.
6. Andersson J., Britton S., Ernberg I. et al. Effect of acyclovir on infectious mononucleosis: a double-blind, placebo-controlled study // J Infect Dis. 1986. Vol. 153. P. 283–290.
7. Andersson J., Sköldenberg B., Henle W. et al. Acyclovir treatment in infectious mononucleosis: a clinical and virological study // Infection. 1987. Vol. 15. P. 14–20.
8. Pagano J. S., Sixbey J. W., Lin J. C. Acyclovir and Epstein-Barr virus infection // J Antimicrob Chemother. 1983. Vol. 12 (Suppl B). P. 113–121.
9. Tynell E., Aurelius E., Brandell A. et al. Acyclovir and prednisolone treatment of acute infectious mononucleosis: a multicenter, double-blind, placebo-controlled study // J Infect Dis. 1996. Vol. 174. P. 324–331.
10. Van der Horst C., Joncas J., Ahronheim G. et al. Lack of effect of peroral acyclovir for the treatment of acute infectious mononucleosis // J Infect Dis. 1991. Vol. 164. P. 788–792.
11. Vouloumanou E. K., Rafailidis P. I., Falagas M. E. Current diagnosis and management of infectious mononucleosis // Current Opinion in Hematology. 2012. Vol. 19 (1). P. 14–20. doi: 10.1097/MOH.0b013e32834daa08.
12. Balfour Jr.H., Hokanson K. M., Schacherer R. M. et al. A virologic pilot study of valacyclovir in infectious mononucleosis // Journal of Clinical Virology. 2007. Vol. 39. P. 16–21.
13. Walling D. M., Flaitz C. M., Nichols C. M. Epstein-Barr Virus Replication in Oral Hairy Leukoplakia: Response, Persistence, and Resistance to Treatment with Valacyclovir // Journal of Infectious Diseases. 2003. Vol. 188. P. 883–890.
14. Cox A. J., Gleeson M., Pyne D. B. et al. Valtrex therapy for Epstein-Barr virus reactivation and upper respiratory symptoms in elite runners // Med. Sci. Sports Exerc. 2004. Vol. 36 (7). P. 1104–1110.
15. Vezina H. E., Balfour Jr. H., Weller D. R. et al. Valacyclovir pharmacokinetics and exploratory pharmacodynamics in young adults with Epstein-Barr virus infectious mononucleosis // J Clin Pharmacol. 2010. Vol. 50. P. 734–742.
16. Hoshino Y., Katano H., Zou P. et al. Long-Term Administration of Valacyclovir Reduces the Number of Epstein-Barr Virus (EBV) -Infected B Cells but Not the Number of EBV DNA Copies per B Cell in Healthy Volunteers // Journal of virology. 2009. Vol. 83 (22). P. 11857–11861.
17. De Paor M., O’Brien K., Fahey T., Smith S. M. Antiviral agents for infectious mononucleosis (glandular fever) // The Cochrane Database of Systematic Reviews. 2016. Issue 12. CD011487. doi: 10.1002/14651858.

Вирус Эпштейна-Барр (ВЭБ) – причина хронической персистирующей инфекции из группы герпесвирусных возбудителей (вирус герпеса 4-го типа). Источником заражения ВЭБ является больной человек или вирусоноситель. Передача вируса может происходить воздушно-капельным, половым и контактно-бытовым путем через слюну, мокроту, влагалищные и уретральные выделения, кровь. По имеющимся данным около 80% населения инфицированы ВЭБ.
Заболевания, вызванные ВЭБ
Эпштейна-Барр вирусная инфекция, как правило, встречается у детей и молодых людей. Однако могут наблюдаться в любом возрасте. Клинические проявления инфекции крайне разнообразны и отличаются пестрой симптоматикой, что значительно затрудняет диагностику. Как правило, проявления ВЭБ развиваются на фоне снижения иммунитета, что свойственно всем герпесвирусным инфекциям. Первичные формы заболевания и его рецидивы всегда связаны с врожденным или приобретенным иммунодефицитом. У людей с выраженным иммунодефицитом наблюдаются генерализованные формы инфекции с поражением центральной нервной системы, печени, легких и почек. Нередко тяжелые формы инфекции ВЭБ, могут ассоциироваться с ВИЧ-инфекцией.
Внимание!
В настоящее время установлено, что ВЭБ также ассоциирован с целым рядом онкологических, преимущественно лимфопролиферативных и аутоиммунных заболеваний (классические ревматические болезни, васкулиты, неспецифический язвенный колит и др.). Кроме того, ВЭБ вызывает манифестные и стертые формы заболевания, протекающие по типу острого и хронического мононуклеоза.
Течение ВЭБ-инфекции
У людей с нормальным иммунитетом после заражения ВЭБ возможны два варианта. Инфекция может протекать бессимптомно либо проявляться в виде незначительных признаков, напоминающих грипп или острое респираторное вирусное заболевание (ОРВИ). Однако в случае заражения на фоне уже имеющегося иммунодефицита у пациента может развиться картина инфекционного мононуклеоза.
В случае развития острого инфекционного процесса возможны несколько вариантов исхода заболевания:
– выздоровление (ДНК вируса можно выявить только при специальном исследовании в единичных В-лимфоцитах или эпителиальных клетках);
– бессимптомное вирусоносительство или латентная инфекция (вирус определяется в слюне или лимфоцитах лабораторно);
– развитие хронического рецидивирующего процесса:
а) хроническая активная ВЭБ-инфекция по типу хронического инфекционного мононуклеоза;
б) генерализованная форма хронической активной ВЭБ-инфекции с поражением ЦНС, миокарда, почек и др.;
в) стертые или атипичные формы ВЭБ-инфекции: длительный субфебрилитет неясного генеза, рецидивирующие бактериальные, грибковые, часто микст-инфекции респираторного и желудочно-кишечного тракта, фурункулез;
г) развитие онкологических заболеваний (лимфома Беркитта, назофарингеальная карцинома и др.);
д) развитие аутоиммунных заболеваний;
е) ВЭБ-ассоциированный синдром хронической усталости.
Исход острой инфекции, вызванной ВЭБ, зависит от наличия и степени выраженности иммунного дефицита, а также от наличия ряда внешних факторов (стрессы, сопутствующие инфекции, операционные вмешательства, гиперинсоляция, переохлаждения и др.), способных нарушать работу иммунной системы.
Клинические проявления ВЭБ-инфекции
Клинические проявления заболеваний, вызванных ВЭБ, во многом зависят от остроты процесса. Также имеет значение первичность инфекционного процесса или возникновение клинической симптоматики хронической инфекции. В случае развития острого инфекционного процесса при заражении ВЭБ наблюдается картина инфекционного мононуклеоза. Он, как правило, возникает у детей и молодых людей.
Развитие данного заболевания приводит к появлению следующих клинических признаков:
– повышение температуры,
– увеличение различных групп лимфоузлов,
– поражение миндалин и гиперемии зева.
Достаточно часто наблюдается отечность лица и шеи, а также увеличение печени и селезенки.
В случае развития хронически активной ВЭБ-инфекция наблюдается длительное рецидивирующее течение заболевания. Пациентов беспокоят: слабость, потливость, нередко боли в мышцах и суставах, наличие различных кожных высыпаний, кашель, дискомфорт в горле, боли и тяжесть в правом подреберье, головные боли, головокружение, эмоциональная лабильность, депрессивные расстройства, нарушение сна, снижение памяти, внимания, интеллекта. Часто наблюдаются субфебрильная температура, увеличение лимфоузлов и гепатоспленомегалия различной степени выраженности. Обычно эта симптоматика имеет волнообразный характер.
У пациентов с выраженной иммунной недостаточностью возможно возникновение генерализованных форм ВЭБ-инфекции с поражением центральной и периферической нервной систем (развитие менингита, энцефалита, мозжечковой атаксии, полирадикулоневритов), а также с поражением других внутренних органов (развитие миокардита, гломерулонефрита, лимфоцитарного интерстициального пневмонита, тяжелых форм гепатита). Генерализованные формы ВЭБ-инфекции могут привести к летальному исходу.
Достаточно часто хроническая ВЭБ инфекция протекает стерто или может напоминать другие хронические заболевания. При стертых формах инфекции пациента может беспокоить волнообразно возникающие субфебрильная температура, боли в мышцах и лимфоузлах, слабость, нарушение сна. В случае течения инфекционного процесса под маской другого заболевания наиболее важными признаками являются: длительность симптоматики и устойчивость к терапии.
Лабораторные исследования
Их можно разделить на две группы скрининговые и уточняющие:
1. К скрининговым можно отнести те, которые наряду с клинической симптоматикой позволяют заподозрить ВЭБ-инфекцию. В клиническом анализе крови: могут наблюдаться: незначительный лейкоцитоз, лимфомоноцитоз, возможно, тромбоцитопения. В биохимическом анализе крови выявляются: повышение уровня трансаминаз и других ферментов, белков острой фазы – С-реактивный белок, фибриноген и др. Однако эти изменения не являются строго специфичными для ВЭБ-инфекции (их можно обнаружить и при других вирусных инфекциях).
2. Важным исследованием, позволяющим установить наличие возбудителя в организме, является серологическое обследование: повышение титров антител к ВЭБ, является критерием наличия инфекционного процесса в настоящее время или свидетельством контакта с инфекцией в прошлом. Однако наличие антител не позволяет однозначно говорить о том, что клинические проявления заболевания вызваны ВЭБ.
3. Для получения наиболее достоверных результатов используется ДНК-диагностика. С помощью метода полимеразной цепной реакции (ПЦР) определение ДНК ВЭБ проводят в различных биологических материалах: слюне, сыворотке крови, лейкоцитах и лимфоцитах периферической крови. При необходимости проводят исследование в биоптатах печени, лимфоузлов, слизистой кишечника и т. д. Таким образом, для постановки диагноза ВЭБ-инфекции, помимо проведения общеклинических обследований, необходимы серологические исследования (ИФА) и ДНК диагностика инфекции в различных материалах в динамике.
Лечение ВЭБ-инфекции
В настоящее время общепринятых схем лечения ВЭБ-инфекции не существует. Объем терапии больных, как с острой, так и с хронической активной ВЭБ-инфекцией может быть различным, в зависимости от длительности заболевания, тяжести состояния и иммунных расстройств. В комплексном лечении данного заболевания используются различные группы препаратов, в том числе рекомбинантные интерфероны, которые подавляют размножение вируса, защищают незараженные клетки, укрепляют иммунитет. Кроме того, применяются ациклические синтетические нуклеозиды и другие противовирусные препараты, обеспечивающие остновку репликации вируса в пораженных клетках, а также глюкокортикоиды, действие которых направлено на купирование воспалительных процессов в органах и тканях. В зависимости от выраженности тех или иных симптомов заболевания назначается различная симптоматическая терапия (анальгетики, антиоксиданты, нестероидные противовоспалительные средства, муколитики и др.).
Интерферон в лечении болезни
Препаратом выбора при лечении ВЭБ-инфекции может стать интерферон-альфа, в среднетяжелых случаях назначаемый в виде монотерапии. Обоснованием включением в терапевтический комплекс противовирусных средств иммунного действия (интерферонов) является то, что клинические проявления инфекции обычно связаны с иммунодефицитными состояниями различной степени выраженности. При ВЭБ-инфекции всегда наблюдается сниженная выработка собственного интерферона. Учитывая, что ВЭБ-инфекция является хроническим, персистирующим заболеванием, интерферонотерапия может быть рекомендована и в качестве профилактики обострений. В этом случае назначается курсовое лечение, длительность которого зависит от тяжести течения заболевания.
Из группы рекомбинантных интерферонов может назначаться препарат ВИФЕРОН® Суппозитории. Сочетание основного действующего вещества интерферона альфа-2b и высокоактивных антиоксидантов: альфа-токоферола ацетата и аскорбиновой кислоты (в составе лекарственной формы представлена в виде смеси аскорбиновая кислота/натрия аскорбат) позволяет снизить терапевтически эффективную концентрацию интерферона альфа-2b и избежать проявления побочных эффектов интерферонотерапии. В присутствии аскорбиновой кислоты и ее соли и альфа-токоферола ацетата возрастает специфическая противовирусная активность интерферона, усиливается его иммуномодулирующее действие и нормализуются показатели интерферона.
Лечение ВЭБ-инфекции необходимо проводить под контролем клинического анализа крови (один раз в 7—14 дней), биохимического анализа (один раз в месяц, при необходимости чаще), иммунологического исследования — через один-два месяца.
Справочно-информационный материал
Автор статьи
Врач дерматовенеролог, клинический иммунолог, д.м.н., профессор
Читайте также:

