Микоплазменная и хламидийная инфекция дыхательных путей
Обновлено: 25.04.2024
Диагностика инфекций, вызванных Mycoplasma pneumonia.
Возбудителем респираторного микоплазмоза является Mycoplasma pneumoniae - представитель класса Mollicutes, объединяющего бесстеночные, способные к автономному существованию бактерии, по уровню структурной организации занимающие промежуточное положение между бактериями и вирусами. Респираторный микоплазмоз - распространенное антропогенное заболевание. Особенностью респираторного микоплазмоза является периодичность эпидемий с интервалами, по данным разных источников, варьирующими от 3 до 7 лет. Распространению инфекции способствует частота и длительность контактов среди лиц, пребывающих в закрытых и полузакрытых коллективах (военнослужащие, школы-интернаты), особенно при их формировании. В 3-10% случаев микоплазменной инфекции рентгенологически диагностируется пневмония. В 1-5% случаев заболеваний респираторным микоплазмозом требуется госпитализация. Микоплазменная пневмония сопровождается частым мучительным и продолжительным кашлем со скудной вязкой мокротой, которая плохо эвакуируется, отмечаются боли в грудной клетке, может развиться обструкция бронхов. Диагностика микоплазменной пневмонии только на основании клинических или рентгенологических данных невозможна, поскольку не имеет патогномонических черт. Основная роль в подтверждении микоплазменной этиологии пневмонии отводится лабораторной этиологической диагностике. Для этиологической диагностики микоплазменной пневмонии применяют: обнаружение ДНК М. pneumoniae методом полимеразной цепной реакции (ПЦР) в режиме реального времени (ПЦР-РВ); выявление антигена микоплазм в реакции прямой иммунофлуоресценции (РИФ); серологические исследования по обнаружению специфических антител класса IgM и IgG к M. pneumoniae в сыворотках крови методом иммуноферментного анализа (ИФА). Mycoplasma pneumoniae относится к трудно культивируемым микроорганизмам.
С целью быстрой этиологической диагностики пневмонии рекомендуется использовать ПЦР при исследовании биологического материала, полученного из нижних дыхательных путей (мокрота при глубоком откашливании, аспираты из трахеи, мокрота, полученная в результате индукции посредством ингаляции гипертонического раствора натрия хлорида, жидкость бронхоальвеолярного лаважа (БАЛ), получаемая с помощью фибробронхоскопии. При получении положительного результата ПЦР при исследовании биологического материала, полученного из нижних дыхательных путей, этиология пневмонии считается установленной. При невозможности получения биологического материала из нижних дыхательных путей для ПЦР допустимо использовать мазки из верхних дыхательных путей (объединенный мазок из носоглотки и задней стенки глотки), и при получении положительного результата следует считать этиологию пневмонии предположительно установленной.
Диагностика инфекций, вызванных Chlamydophila pneumoniae.
Chlamydophila pneumoniae- патогенная для человека грамотрицательная бактерия с облигатным внутриклеточным типом паразитирования, обладает тропизмом к клеткам столбчатого цилиндрического эпителия слизистых оболочек человека, в частности, к эпителию бронхиол, бронхов, а также к альвеолярным макрофагам, моноцитам. Для C. pneumoniae-инфекции характерна генерализация процесса, вследствие чего возбудитель может инфицировать эндотелиальные клетки сосудов, синовиальные клетки, гепатоциты и ткани нервной системы.
С. pneumoniae вызывает пневмонии различной тяжести, длительно протекающие бронхиты, фарингиты, синуситы. Пневмония, вызванная С. pneumoniae обычно имеет благоприятное течение, в редких случаях течение очень тяжелое. Микст-инфекция, например сочетание с пневмококком или наличие тяжелых сопутствующих заболеваний, особенно у пожилых лиц, осложняет течение заболевания и увеличивает риск летального исхода. Нередко инфекция протекает малосимптомно. В группу риска попадают все возраста, но частота заболеваемости хламидийной пневмонией выше у детей школьного возраста. Заболеваемость среди мужчин выше, чем среди женщин. Эпидемические вспышки происходят каждые 4-10 лет.
Наиболее специфичным и чувствительным методом выявления возбудителя является ПЦР- диагностика в реальном времени (ПЦР-РВ). Высокая чувствительность и отсутствие ложноположительных результатов могут быть обеспечены использованием только лицензированных наборов для эффективного выделения ДНК из клинического материала и наборов для постановки ПЦР современного поколения на основе ПЦР в реальном времени (ПЦР-РВ).
При получении положительного результата ПЦР при исследовании биологического материала, полученного из нижних дыхательных путей, этиология пневмонии считается установленной. Однако при пневмониях, вызванных Chlamydophila pneumoniae, кашель часто бывает непродуктивным, в таких случаях для ПЦР рекомендуется использовать мазки из верхних дыхательных путей (объединенный мазок из носоглотки и задней стенки глотки), и при получении положительного результата следует считать этиологию пневмонии предположительно установленной.
Материалом для проведения ПЦР служат пробы ДНК, полученные из образцов следующего материала: мокроты (либо аспиратов из трахеи), промывных вод бронхов, бронхо-альвеолярного лаважа, мазков со слизистой нижнего носового хода и задней стенки ротоглотки, секционного материала, цельной крови.
Взятие мазков со слизистой нижнего носового хода
Мазки берут сухим стерильным назофарингеальным велюр-тампоном на пластиковом аппликаторе. Если полость носа заполнена слизью, перед процедурой рекомендуется провести высмаркивание. Зонд вводят легким движением по наружной стенке носа на глубину 2-3 см до нижней раковины. Затем зонд слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину до носоглотки, делают вращательное движение и удаляют вдоль наружной стенки носа.
После взятия материала тампон (рабочую часть зонда с тампоном) помещают до места слома в стерильную одноразовую пробирку с 500 мкл транспортной среды для хранения и транспортировки респираторных мазков. Конец зонда отламывают с расчетом, чтобы он позволил плотно закрыть крышку пробирки. Пробирку с раствором и рабочей частью зонда закрывают и маркируют.
Взятие мазков из ротоглотки
Мазки из ротоглотки берут сухими стерильными зондами с вискозными тампонами вращательными движениями с поверхности миндалин, небных дужек и задней стенки ротоглотки.
После взятия материала тампон (рабочую часть зонда с вискозным тампоном) помещают в стерильную одноразовую пробирку с 500 мкл транспортной среды для хранения и транспортировки респираторных мазков. Конец зонда отламывают, придерживая крышкой пробирки с расчетом, чтобы он позволил плотно закрыть пробирку. Пробирку с раствором и рабочей частью зонда закрывают и маркируют.
Допускается хранение клинического материала до проведения исследования в течение 3 суток при температуре от 2 до 8 °С или 1 неделю при температуре не выше минус 16 °С.
Мокрота или аспират из трахеи
Мокроту собирают в стерильные герметичные одноразовые пластиковые контейнеры, после предварительного полоскания полости рта водой. Аспираты из трахеи получают традиционным способом и помещают в стерильные герметичные одноразовые пластиковые контейнеры.
Бронхо-альвеолярный лаваж (БАЛ) или промывные воды бронхов (ПВБ) собирают в одноразовые плотно завинчивающиеся емкости из полипропилена (во избежание адгезии клеток на внутренней поверхности емкости) объемом не менее 5 мл.
Допускается хранение вышеперечисленного материала до проведения исследования в течение 1 суток при температуре от 2 до 8 °С или 1 неделю при температуре не выше минус 16 °С.
Секционный материал помещают в стерильные одноразовые контейнеры и замораживают сразу после взятия либо исследуют в течение 1 ч. Дальнейшее хранение материала возможно в течение года при температуре не выше минус 68 °С. Допускается однократное замораживание-оттаивание материала.
Цельную кровь собирают в пробирки типа Vacuette с раствором или напылением ЭДТА. Закрытую пробирку с материалом несколько раз переворачивают, чтобы перемешать консервант. Для анализа используют цельную кровь, собранную у пациента утром натощак, без предварительной подготовки.
Внимание! Данный материал не используется для диагностики ОРЗ.
Cреди всех видов пневмоний практическому врачу наиболее часто приходится сталкиваться с внебольничной пневмонией. По данным официальной статистики МЗ РФ, заболеваемость внебольничной пневмонией в России среди лиц старше 18 лет составляет
Cреди всех видов пневмоний практическому врачу наиболее часто приходится сталкиваться с внебольничной пневмонией. По данным официальной статистики МЗ РФ, заболеваемость внебольничной пневмонией в России среди лиц старше 18 лет составляет 3,9%. Зарубежные исследователи установили, что заболеваемость внебольничной пневмонией среди лиц молодого и среднего возраста варьирует от 1 до 11,6%, а в старшей возрастной группе достигает 25–44% [11, 13].
Наиболее распространенной причиной внебольничных пневмоний является Streptococcus pneumoniae (30–50%) [5, 11, 13]. Однако все большее значение среди этиологических факторов внебольничной пневмонии в последние годы придается так называемым атипичным микроорганизмам, прежде всего Mycoplasma pneumoniae и Chlamydophila (Chlamidia) pneumoniae, на долю которых приходится от 8 до 25% случаев заболевания [5, 9, 12].
Mycoplasma pneumoniae в структуре внебольничных пневмоний варьирует в пределах 5–50% [7, 11, 13]. Наиболее часто микоплазменная пневмония диагностируется у детей старше 5 лет и лиц молодого возраста (до 25 лет) [3, 4, 7, 10]. Каждые 3–5 лет наблюдаются эпидемиологические подъемы заболеваемости, которые длятся несколько месяцев. Вспышки заболевания характерны для изолированных и полуизолированных групп населения (военнослужащие, студенты, школьники и др., семейные вспышки) [10, 11]. Признается наличие сезонных колебаний, а именно большая распространенность инфекции в осенне-зимний период [6, 10, 13]. Источником инфекции являются как больные, так и носители. Механизм передачи инфекции — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период длится 2–3 нед. Летальность при микоплазменной пневмонии составляет 1,4% [4, 11].
Mycoplasma pneumoniae занимает промежуточное положение между вирусами, бактериями и простейшими и является мембрано-ассоциированным (но может быть и внутриклеточным) анаэробом, имеет трехслойную цитоплазматическую мембрану вместо клеточной стенки, что обусловливает резистентность к различным агентам, подавляющим синтез клеточной стенки, прежде всего к пенициллину и другим β-лактамам [6, 10]. С помощью терминальной структуры микоплазма прикрепляется к клеткам хозяина (эритроцитам, клеткам реснитчатого эпителия бронхов и др.) [6]. Микоплазма также обладает механизмом мимикрии под антигенный состав клетки-хозяина, что способствует длительной персистенции возбудителя и вызывает образование аутоантител и развитие аутоиммунных процессов при микоплазменной инфекции [6, 10]. Предполагается, что именно с формированием аутоантител связано развитие нереспираторных проявлений Mycoplasma pneumoniae-инфекции.
Считается, что от 5 до 15% внебольничных пневмоний вызываются хламидиями, а в период эпидемии эти показатели могут увеличиваться до 25% [4, 5, 10]. Наиболее часто хламидийная пневмония встречается у взрослых, особенно у лиц среднего и пожилого возраста [2, 10]. Описаны эпидемиологические вспышки в изолированных и полуизолированных коллективах, случаи внутрисемейной передачи хламидийной инфекции [7, 10, 13]. Сезонной закономерности распространения этой инфекции не выявлено. Единственным известным резервуаром инфекции является человек. Механизм передачи — аэрогенный, путь передачи — воздушно-капельный. Инкубационный период составляет 2–4 нед. Летальность при хламидийных пневмониях достигает 9,8% [4, 5, 13].
Chlamydophila pneumoniae — это патогенные облигатные внутриклеточные грамотрицательные бактерии, способные к латентному существованию или персистенции в организме хозяина. Характеризуются двухфазным циклом развития, состоящим из чередования функционально и морфологически различных форм — элементарных и ретикулярных телец [2, 4, 7, 10].
Клинические проявления микоплазменнойи хламидийной пневмоний
У 30–40% пациентов, заболевших микоплазменной и/или хламидийной пневмонией, диагноз ставится лишь в конце первой недели болезни; первоначально у них чаще всего ошибочно диагностируются бронхит, трахеит или ОРЗ. Это связано с тем, что, в отличие от бактериальных пневмоний, микоплазменная и хламидийная не имеют отчетливых физикальных и рентгенологических признаков инфильтрации, а культуральная диагностика их невозможна, так как микоплазмы и хламидии являются внутриклеточными возбудителями. Поэтому диагностика микоплазменной и хламидийной пневмоний основывается в первую очередь на выявлении особенностей клинико-рентгенологических данных и подтверждается серологически или с помощью полимеразно-цепной реакции (ПЦР).
Обычно микоплазменная и хламидийная пневмонии начинаются с респираторного синдрома, проявляющегося трахеобронхитом, назофарингитом, ларингитом; протекают с субфебрильной температурой, малопродуктивным, мучительным кашлем, скудными аускультативными данными; характеризуются наличием внелегочных проявлений — кожных, суставных, гематологических, гастроэнтерологических, неврологических и других, а также нетипичными лабораторными показателями — отсутствием лейкоцитоза и нейтрофильного сдвига в периферической крови [3, 4, 7, 10, 11]. Рентгенологические изменения в легких отмечаются усилением легочного рисунка, перибронхиальной или субсегментарной инфильтрацией [5, 10, 11, 13].
Нами были обследованы 60 пациентов: 44 — с микоплазменной пневмонией и 16 — с хламидийной пневмонией. Анализ клинического материала показал, что начало заболевания при микоплазменной и хламидийной пневмониях может быть как острым, так и постепенным (табл. 1). При подостром течении пневмония начинается с поражения верхних дыхательных путей, ухудшения общего состояния и познабливания. Температура тела может быть нормальной или субфебрильной в течение 6–10 дней и лишь потом повышается до 38–39,9°С при микоплазменной и до 38–38,9°С при хламидийной пневмонии. При остром начале симптомы интоксикации появляются уже в первый день и достигают максимума к 3-му дню болезни. У пациентов с постепенным началом болезни интоксикация наиболее выражена на 7–12-й день от начала заболевания. Характерными признаками интоксикации для микоплазменной и хламидийной пневмоний являются умеренная головная боль, миалгия, общая слабость.
Одним из постоянных признаков микоплазменной и хламидийной пневмоний, по нашим данным, является кашель, который возникает одновременно с лихорадкой. У больных микоплазменной пневмонией, в отличие от хламидийной, наблюдается частый, преимущественно непродуктивный, навязчивый, мучительный, приступообразный кашель (см. табл. 1). Наряду с кашлем, у пациентов с хламидийной и микоплазменной пневмониями наблюдаются умеренные признаки поражения верхних дыхательных путей — ринит, фарингит, ларингит. Ринит чаще всего встречается у больных хламидийной пневмонией (75,0 ± 10,8%, р < 0,001) и проявляется заложенностью носа и нарушением носового дыхания, у части больных наблюдаются небольшие либо умеренные слизисто-серозные или слизисто-гнойные выделения из носа. У пациентов же с микоплазменной пневмонией чаще регистрируются явления фарингита и ларингита, проявляющиеся гиперемией ротоглотки и осиплостью голоса (77,3 ± 6,3%, р < 0,05).
Из внелегочных проявлений при микоплазменной пневмонии чаще отмечались миалгия (63,6%), макуло-папулезная сыпь (22,7%), явления желудочно-кишечного дискомфорта (25%), при хламидийной — артралгия (18,8%) и миалгия (31,3%).
Изменения в легких, характерные для уплотнения легочной ткани, при физикальном обследовании пациентов с пневмониями, вызванными атипичными возбудителями (в отличие от больных с бактериальными пневмониями), определялись не всегда. В частности, укорочение перкуторного звука у больных микоплазменной и хламидийной пневмониями наблюдалось в 68,2 и 68,8% случаев соответственно (табл. 1). Этот признак всегда выявлялся у больных с сегментарной, полисегментарной, долевой пневмонией и лишь у 1/3 пациентов с перибронхиальной инфильтрацией. У больных микоплазменной пневмонией над зоной поражения чаще выслушивались ослабленное дыхание (40,9%), сухие и влажные хрипы (47,7%), у пациентов с хламидийной пневмонией — как ослабленное (37,5%), так и бронхиальное дыхание (31,2%) и влажные хрипы (62,5%).
При рентгенографии органов грудной клетки у больных микоплазменной и хламидийной пневмониями выявлялись и типичные пневмонические инфильтрации и интерстициальные изменения. При микоплазменной пневмонии чаще наблюдается двустороннее поражение легких (40,9%) с усилением легочного рисунка (22,7%) и перибронхиальной инфильтрацией (50%), при хламидийной пневмонии — наоборот, чаще полисегментарная инфильтрация (43,7%) и реже интерстициальные изменения (31,3%).
В общем анализе крови у больных микоплазменной и хламидийной пневмониями чаще отмечается нормальное количество лейкоцитов и умеренное повышение СОЭ (в среднем 37,1 ± 1,9 мм/ч).
По нашим наблюдениям, для микоплазменной и хламидийной пневмоний характерно затяжное рецидивирующее течение.
Таким образом, согласно клинико-рентгенологическим данным и с учетом эпидемиологической ситуации, из общего числа пациентов с внебольничными пневмониями можно выделить больных с микоплазменной и/или хламидийной пневмониями. В нашем исследовании таких больных оказалось 80, из них у 60 (75%) в дальнейшем лабораторным методом была установлена микоплазменная или хламидийная этиология пневмонии.
Диагностика микоплазменной и хламидийной пневмоний
Решающая роль в выявлении микоплазменной и хламидийной инфекции отводится лабораторной диагностике.
Также в последнее время для этиологической диагностики микоплазменной и хламидийной инфекции используется ПЦР, основанная на определении ДНК возбудителя с применением метода генных зондов [3, 4, 5, 7, 10]. С помощью ПЦР возможна быстрая диагностика микоплазменной и хламидийной инфекции, но этот метод не позволяет отличить активную инфекцию от персистирующей [1, 7, 10, 11].
Таким образом, для достоверной этиологической идентификации микоплазменной и хламидийной пневмоний необходимо проведение серологических тестов в комплексе с методами, основанными на выявлении ДНК микроорганизма.
Лечение микоплазменной и хламидийной пневмоний
Рассмотренные выше микробиологические особенности Mycoplasma pneumoniae и Chlamydophila pneumoniae (главным образом внутриклеточный цикл развития) объясняют неэффективность широко используемых в клинической практике β-лактамных антибиотиков (пенициллины и цефалоспорины) и обусловливают необходимость применения антимикробных препаратов, способных проникать и накапливаться в пораженных клетках, а также блокировать внутриклеточный синтез белка. Такими свойствами обладают макролиды, фторхинолоны и тетрациклины, которые и являются средствами эрадикационной терапии при Mycoplasma pneumoniae- и Chlamydophila pneumoniae-инфекции [3, 4, 7, 10, 11].
В России макролиды представлены широким спектром препаратов (см. табл. 3). Среди них наиболее активным в отношении Mycoplasma pneumoniae признан азитромицин, имеющий ряд преимуществ перед эритромицином и кларитромицином [4, 10, 11]. В отношении Chlamydophila pneumoniae наиболее активным средством признается кларитромицин [10]. Также эффективны в отношении этих внутриклеточных патогенов и некоторые другие представители макролидов: джозамицин, спирамицин. Старый антимикробный препарат из этой группы — эритромицин — также обладает антимикоплазменной и антихламидийной активностью, но, несомненно, уступает в этом отношении вышеперечисленным антибиотикам, обладая при этом целым рядом побочных эффектов [5, 10, 11].
Значительной активностью по отношению к Mycoplasma pneumoniae и Chlamydophila pneumoniae обладают фторхинолоны — офлоксацин (заноцин, таривид, офло), ципрофлоксацин (ципробай, ципролет, цифран, сифлокс, медоциприн, цифлоксинал), в связи с чем эти антимикробные препараты рассматриваются в качестве альтернативы макролидам при данной инфекции. Высокую активность проявляют новые фторхинолоны — левофлоксацин (таваник) и моксифлоксацин (авелокс). Моксифлоксацин и левофлоксацин успешно подавляют практически любую флору, вызывающую пневмонии.
При лечении микоплазменных и хламидийных пневмоний эффективны и тетрациклины, однако антибиотики этой группы не применяются при беременности, а также печеночной недостаточности. Вероятность проявления побочных эффектов при их применении может быть выше. Из тетрациклинов активны в отношении атипичных микроорганизмов доксициклин и моноциклин (см. табл. 3).
Продолжительность антимикробной терапии неосложненных бактериальных внебольничных пневмоний составляет 5–10 дней. Для лечения микоплазменной и хламидийной пневмоний рекомендуется применять антимикробные средства не менее 2–3 нед [4, 5, 10, 11]. Сокращение сроков лечения чревато развитием рецидива инфекции [4, 10].
При нетяжелом течении микоплазменной и хламидийной пневмоний антимикробные препараты назначаются внутрь в среднетерапевтических дозах. Естественно, при тяжелых пневмониях предпочтение следует отдавать внутривенному применению антибиотика. Эритромицин фосфат назначается до 1–2 г/сут в 2–3 введения (максимально по 1 г каждые 6 ч). Спирамицин используется внутривенно по 1,5 млн МЕ 3 раза в сутки, а кларитромицин — по 250 мг 2 раза в сутки с равными интервалами. Для разведения спирамицина и кларитромицина следует применять 5%-ный раствор глюкозы.
Стоимость внутривенного лечения антибиотиками (в частности, макролидами) весьма высока, поэтому используют ступенчатую терапию, при которой лечение начинается с внутривенного применения антибиотиков, а по достижении клинического эффекта (обычно через 2–3 дня) пациент переводится на пероральную терапию тем же препаратом или другим макролидом. Ступенчатая монотерапия макролидами может проводиться эритромицином, кларитромицином, спирамицином, т. е. препаратами, которые выпускаются в двух формах: для внутривенного введения и для приема внутрь.
Несмотря на большой спектр противомикробных препаратов, эффективное лечение микоплазменных и хламидийных пневмоний представляет до настоящего времени большую проблему [2, 6, 10, 11]. Это связано с тем, что их развитие, как правило, происходит на фоне снижения антиинфекционной резистентности организма, обусловленного угнетением иммунитета [8, 9, 10, 12]. Проведенное нами исследование показателей иммунограммы у пациентов с внебольничной пневмонией микоплазменной и хламидийной этиологии выявило снижение абсолютного числа лимфоцитов, зрелых Т-лимфоцитов (CD3+), Т-хелперов (CD4+), абсолютного числа Т-супрессоров (CD8+), угнетение функциональной активности Т-системы, проявляющееся снижением плотности рецепторов к IL-2 (CD25+), способности к бласттрансформации (CD71+ — лимфоциты) и апоптозу (CD95+), а также активацию гуморального иммунитета, что проявлялось повышением числа В-лимфоцитов (CD20+), уровня IgM и ЦИК.
Микоплазмы и хламидии на разных стадиях развития располагаются как внутриклеточно, так и внеклеточно, что требует для их элиминации участия гуморальных и клеточных механизмов иммунитета [8, 9, 10, 12]. Большинство антимикробных средств действует преимущественно на внеклеточную форму возбудителей. Это приводит к персистенции возбудителей, диссеминации ее в организме, хронизации процесса, формированию осложнений. Применение лишь антимикробных средств означает лишь временное подавление возбудителей, так как на фоне такой терапии происходит сохранение и даже усугубление иммунологических расстройств, что повышает риск рецидива заболеваний [14]. Так, по результатам наших исследований, к концу курса традиционной терапии происходило усугубление Т-клеточной депрессии: снижалось относительное и абсолютное количество Т-лимфоцитов (CD3+), Т-хелперов (CD4+), Т-супрессоров (CD8+) на фоне повышения уровня IgG, ЦИК, фагоцитарного индекса и уменьшения IgA.
В связи с этим хотелось бы подчеркнуть, что терапия микоплазменной и хламидийной пневмоний должна быть комплексной и включать, помимо антимикробных средств, препараты, действие которых направлено на коррекцию иммунного ответа.
С этой целью у больных микоплазменной и хламидийной пневмониями нами применяются иммуномодуляторы (ронколейкин, ликопид, тималин, тимоген).
Включение иммуномодуляторов в комплексное лечение микоплазменных и хламидийных пневмоний позволяет добиться ярко выраженного иммунологического эффекта. Последний сочетается с выраженным клиническим воздействием, проявляющимся сокращением сроков достижения клинико-лабораторной ремиссии в среднем на 3 койко-дня, уменьшением интоксикационных симптомов через 1–3 сут после начала лечения, сокращением лихорадочного периода в 2 раза, четкой положительной рентгенологической динамикой к 12-му дню лечения у 76,7% больных; значительным уменьшением вероятности развития повторных рецидивов и хронизации процесса.
Литература
- Бочкарев Е. Г. Лабораторная диагностика хламидийной инфекции // Иммунопатология, аллергология, инфектология. — 2000. — № 4. — С. 65–72.
- Гранитов В. М. Хламидиозы. — М., 2000. — 48 с.
- Новиков Ю. К. Атипичные пневмонии // Русский медицинский журнал. — 2002. — Т. 10. — № 20. — С. 915–918.
- Ноников В. Е. Диагностика и лечение атипичных пневмоний // CONSILIUM medicum. — 2001. — T. 3. — № 12. — C. 569–574.
- Проект практических рекомендаций МЗ РФ. Внебольничная пневмония у взрослых: диагностика, лечение, профилактика. — М., 2002. — 51 с.
- Прозоровский С. В., Раковская И. В., Вульфович Ю. В. Медицинская микоплазмология. — М.: Медицина, 1995. — 285 с.
- Синопальников А. И. Атипичная пневмония // Русский медицинский журнал. — 2002. — Т. 10. — № 23. — С. 1080–1085.
- Справочник по иммунотерапии для практического врача / Под ред. А. С. Симбирцева. — СПб.: Диалог, 2002. — 480 с.
- Хаитов Р. М., Игнатьева Г. А., Сидорович И. Г. Иммунология. — М.: Медицина, 2000. — 432 с.
- Хаитов Р. Ф., Пальмова Л. Ю. Mycoplasma pneumoniae и Chlamydophila pneumoniae инфекции в пульмонологии: актуальные вопросы клиники, диагностики и лечения. — Казань, 2001. — 64 с.
- Чучалин А. Г., Синопальников А. И, Чернеховская Н. Е. Пневмония. — М.: Экономика и информатика, 2002. — 480 с.
- Boym A. Separation of leucocytes from blood und bone marrow // Scand J Clin. Lad. Jnvest. — 1968. — V. 21. — Suppl. 87. — P. 77–82.
- Guidelines for management of adult community-acquired lower respiratory tract infections. European Study in Community-acquired Pneumonia (ESOCAP) Committee // Eur Resp J. — 1998. — № 11. — Р. 986–991.
- Kawamoto M., Oshita Y., Yoshida H. et al. Two cases hypoxemic acute broncholitis due to Mycoplasma pneumoniae // Kansenshogaku Zasshi. — 2000. — V. 74. — № 3. — P. 259–263.
Г. Г. Мусалимова, кандидат медицинских наук
В. Н. Саперов, доктор медицинских наук, профессор
Т. А. Никонорова
Чувашский ГМУ, г. Чебоксары

- Streptococcus pneumoniae - грамположительные кокки, самые частые возбудители пневмонии во всех возрастных группах (30% и более всех случаев);
- Haemophilus influenzae - грамотрицательные палочки, ответственные за развитие пневмонии у 5-18% взрослых, чаще у курильщиков и больных хроническим обструктивным бронхитом;
- Moraxella (Branhamella) catarrhalis - грамотрицательные коккобациллы, неактуальный возбудитель пневмонии (у 1-2% больных), имеет этиологическое значение, как правило, у больных с сопутствующим хроническим обструктивным бронхитом.
Другие часто выявляемые этиологические агенты ВП отличаются от перечисленных выше микроорганизмов несколько иной патогенностью и биологическими свойствами. Бессимптомная колонизация верхних дыхательных путей этими микроорганизмами маловероятна.
Основными способами заражения микроорганизмами при ВП, вызванной атипичными возбудителями, являются аспирация содержимого ротоглотки и ингаляция микробного аэрозоля — в случае легионеллезной пневмонии. В нормальных условиях ряд микроорганизмов, например S. pneumoniae, могут колонизировать ротоглотку, но нижние дыхательные пути при этом остаются стерильными. Микроаспирация секрета ротоглотки — физиологический феномен, наблюдающийся у 70% здоровых лиц, преимущественно во время сна. Однако слаженная работа мукоцилиарного клиренса, наряду с бактерицидным действием находящихся в бронхиальном секрете лактоферрина, лизоцима, интерферона и секреторного иммуноглобулина класса А, препятствует адгезии и колонизации микроорганизмов и последующему развитию ВП.
Частота микоплазменных пневмоний возрастает во время эпидемических вспышек, повторяющихся каждые 4–5 лет, и может достигать в среднем 20% от общего числа ВП в осенне-зимний период. Этот возбудитель чаще вызывает заболевания у молодых людей, клиническая картина обычно включает лихорадку, фарингит, миалгии, астению и внелегочные осложнения. Заболевание может излечиваться спонтанно в течение 1–2 нед, но нередко продолжается на протяжении 4–6 нед и сопровождается всеми характерными для него проявлениями, включая кашель со слизистой мокротой. Культуральная диагностика микоплазменной инфекции затруднительна. Диагноз может быть подтвержден выявлением 4-кратной сероконверсии специфических антител класса IgM к микоплазме с помощью теста Elisa.
Пневмонии, вызванные хламидиями, стали известны сравнительно недавно. Cl. pneumoniae вызывает инфекцию по крайней мере у 10% больных молодого возраста. Клиническая картина этой инфекции, кроме проявлений собственно бронхита и пневмонии, включает фарингит и ларингит. Обычными признаками являются осиплость голоса, небольшая лихорадка и постоянный кашель, который часто остается сухим, а отделяемая мокрота обычно слизистая и не бывает гнойной. У больных бронхиальной астмой хламидийная инфекция нередко провоцирует учащение приступов удушья. Воспаление бронхов, вызванное хламидией, как правило, встречается у молодых больных и практически не наблюдается в старческом возрасте. Диагноз может быть подтвержден данными сероконверсии, наиболее современным считается тест Elisa. В настоящее время для диагностики микоплазменной и хламидийной инфекции стали использовать полимеразную цепную реакцию (ПЦР).
Пневмония, вызванная L. Pneumophila, не является частым возбудителем ВП, но обычно характеризуется тяжелым течением и развитием системной воспалительной реакции и экстрапульмональной симптоматикой. Наиболее высокой природной активностью против легионелл обладает рифампицин, который часто используют в комбинации с эритромицином. Также эффективны другие макролиды (особенно кларитромицин и азитромицин, создающие высокие концентрации в бронхиальном секрете), новые и ранние фторхинолоны.
Клинико-рентгенологические симптомы атипичных ВП
Крупные мультицентровые исследования, основанные на принципах доказательной медицины, убедительно показали, что в большинстве случаев, основываясь на анализе клинико-рентгенологической картины заболевания, не удается с достаточной степенью определенности высказаться о вероятной этиологии ВП.
В частности, разделение ВП на типичную (например, пневмококковую) и атипичную (микоплазменную или хламидийную) лишено особого клинического значения, так как не влияет на выбор стартового антибиотика для эмпирической терапии. Однако были отмечены некоторые особенности атипичной ВП: образование полостей деструкции в легких не характерно для пневмококковой, микоплазменной и хламидийной пневмоний, а скорее свидетельствует в пользу стафилококковой инфекции, аэробных грамотрицательных энтеробактерий и анаэробов; ретикулонодулярная инфильтрация в базальных отделах легких характерна для микоплазменной ВП (в 20% случаев микоплазменная пневмония может сопровождаться очагово-сливной инфильтрацией в проекции нескольких сегментов или даже доли).
Лабораторная диагностика атипичных ВП
Серологическая диагностика инфекций, вызванных M. pneumoniae, C. pneumoniae и Legionella spp., не рассматривается в ряду обязательных методов исследования, поскольку с учетом необходимости повторного забора сыворотки крови в острый период болезни и в период реконвалесценции (через несколько недель от начала заболевания) это не клинический, эпидемиологический уровень диагностики. В последнее время получил распространение иммуноферментный тест — с определением в моче специфичного растворимого антигена L. pneumophila (1-й серотип), однако в нашей стране использование этих методов экспресс-диагностики практикуется лишь в отдельных клинических центрах.
Лечение атипичных ВП
Распространенную в некоторых регионах Российской Федерации практику широкого использования аминогликозидов (гентамицин и др.) при лечении ВП следует признать ошибочной, так как они не активны в отношении пневмококка и атипичных возбудителей.
M. pneumoniae обладают природной устойчивостью к β-лактамным антибиотикам, так как лишены клеточной стенки и ее составной части — пептидогликана, который является мишенью действия β-лактамов. Наибольшей природной активностью характеризуются макролиды и тетрациклины, а новые фторхинолоны по активности превосходят ранние фторхинолоны.
Cl. pneumoniae тоже устойчивы к β-лактамам, аминогликозидам, а препаратами выбора для лечения хламидийных ВП являются макролидные антибиотики и тетрациклины. Эритромицин или доксициклин являются препаратами выбора при пневмониях, вызванных распространенными возбудителями. У больных с непереносимостью указанных препаратов, выражающейся в виде желудочно-кишечных нарушений, рекомендуется другой макролид, например азитромицин или кларитромицин.
Эритромицин или доксициклин должны обеспечивать адекватное лечение пневмоний, вызванных большинством штаммов S. pneumoniae, а также атипичными возбудителями: Mycoplasma, Chlamydia pneumoniae и Legionella. Эритромицин может оказаться неэффективным при постгриппозной пневмонии, которую чаще вызывают более резистентные возбудители, такие, как Staphylococcus aureus и Haemophilus influenzae. Необходимо принимать во внимание частоту побочных эффектов в отношении желудочно-кишечного тракта (ЖКТ) и вероятность лекарственного взаимодействия. Доксициклин противопоказан при беременности.
Среди макролидов особого внимания заслуживает азитромицин (азитрал и сумамед), который быстро абсорбируется из ЖКТ, что обусловлено его устойчивостью в кислой среде и липофильностью, а также хорошо проникает в дыхательные пути. Высокая концентрация в тканях (в 10–50 раз выше, чем в плазме крови) и длительный TЅ обусловлены низким связыванием азитромицина с белками плазмы крови. Способность азитромицина накапливаться преимущественно в лизосомах особенно важна для элиминации внутриклеточных возбудителей. Доказано, что фагоциты доставляют азитромицин в места локализации инфекции, где он высвобождается в процессе фагоцитоза. Концентрация азитромицина в очагах инфекции достоверно выше, чем в здоровых тканях (в среднем на 24–34%), и коррелирует со степенью воспалительного отека. Несмотря на высокую концентрацию в фагоцитах, азитромицин не оказывает существенного влияния на их функцию. Азитромицин сохраняется в бактерицидных концентрациях в очаге воспаления в течение 5–7 дней после приема последней дозы, что позволило разработать короткие (3-дневные и 5-дневные) курсы лечения и применять препарат 1 раз в сутки.
Высокой активностью характеризуются новые фторхинолоны, а из ранних фторхинолонов наиболее активным против хламидий признан офлоксацин. Левофлоксацин рекомендуется у больных, которые не переносят препаратов первой линии. Этот фторхинолон имеет расширенный спектр активности, позволяющий использовать его при инфекциях дыхательных путей. Он удобен тем, что вводится однократно в сутки.
Литература
Г. И. Сторожаков, доктор медицинских наук, профессор, академик РАМН
Д. Б. Утешев, доктор медицинских наук, профессор
РГМУ, Москва
Хламидийная пневмония – это инфекционно-воспалительный процесс в легких, вызванный облигатными внутриклеточными бактериями рода Chlamydia и Chlamydophila. Для хламидийной пневмонии характерны респираторные проявления (ринит, трахеобронхит), малопродуктивный кашель, субфебрильная и фебрильная температура, внелегочные симптомы (артралгия, миалгия). При постановке диагноза учитываются аускультативные и рентгенологические данные, однако решающая роль принадлежит лабораторной диагностике (ИФА, МИФ, ПЦР и др.). Для терапии хламидийной пневмонии применяются антимикробные средства (макролиды, тетрациклины, фторхинолоны), иммуномодуляторы, физиопроцедуры.
МКБ-10
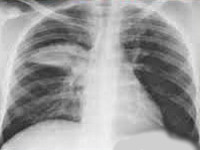
Общие сведения
Хламидийная пневмония – этиологическая разновидность атипичной пневмонии, возникающая при инфицировании дыхательных путей различными видами хламидий - Ch. рneumoniae, Ch. psittaci и Ch. trachomatis. Считается, что ежегодно среди внебольничных пневмоний от 5 до 15% случаев вызываются хламидиями; во время эпидемических вспышек этот показатель может составлять 25%. Чаще всего заболевают взрослые, случаи хламидийной пневмонии у новорожденных связаны с заражением от матерей, больных урогенитальным хламидиозом.
Бессимптомное носительство хламидий в носоглотке определяется более чем у половины взрослых и 5-7% детей, поэтому вероятность передачи инфекции с респираторными секретами очень высока. Описаны внутрисемейные вспышки хламидийной пневмонии, а также случаи массовой заболеваемости в изолированных коллективах.

Причины
Характеристика возбудителя
Из всего многообразия представителей семейства Chlamydiaceae в этиологическом отношении практический интерес для пульмонологии представляют три типа хламидий: Chlamydophila pneumoniae, Сhlamydia trachomatis и Chlamydophila psittaci.
- Ch. pneumoniae служит самым частым возбудителем респираторных хламидиозов (в том числе хламидийного фарингита, синусита, бронхита, пневмонии) у пациентов всех возрастов.
- С Сh. trachomatis связана заболеваемость трахомой, мочеполовым хламидиозом, венерической лимфогранулемой, а также хламидийной пневмонией среди новорожденных и грудничков до 6 месяцев. Также с этим типом хламидий ассоциированы пневмонии у иммунокомпрометированных лиц и сотрудников лабораторий.
- Ch. psittaci рассматривается как возбудитель орнитоза (пситтакоза), часто протекающего в форме тяжелой интерстициальной пневмонии.
Механизм передачи
Пути заражения каждой разновидностью хламидий отличаются, однако все типы могут распространяться гематогенным путем. Передача Ch. pneumoniae от человека к человеку осуществляется преимущественно воздушно-капельным и контактно-бытовым путями. Инфицирование штаммом Ch. psittaci происходит воздушно-пылевым или фекально-оральным путем при вдыхании пыли или употреблении пищи, содержащей биологические секреты птиц-переносчиков инфекции (попугаев, канареек, кур, уток, голубей, воробьев и др.).
Инфицирование новорожденных Ch. trachomatis происходит в процессе родов от матерей с урогенитальной хламидийной инфекцией. При интранатальном заражении у 15-25% младенцев возникает хламидийный назофарингит и конъюнктивит, которые часто осложняются пневмонией.
Патогенез
Все хламидии являются облигатными грамотрицательными микроорганизмами, паразитирующими внутри клеток хозяина. В макроорганизме хламидии могут существовать в инфекционной форме (элементарные тельца) и вегетативной форме (ретикулярные тельца). Элементарные тельца проникают внутрь клетки путем стимуляции эндоцитоза, где преобразуются в ретикулярные тельца. Последние обладают высокой метаболической активностью и способностью к внутриклеточному бинарному делению.
Цикл размножения длится около 48 часов, после чего ретикулярные тельца вновь превращаются в элементарные, происходит разрыв мембраны клетки хозяина с выходом элементарных телец новой генерации во внеклеточную среду. Далее цикл инфицирования новых клеток повторяется.
Симптомы хламидийной пневмонии
Пневмония, вызванная Chlamydophila pneumoniae
Хламидийной пневмонией, вызванной Ch. pneumoniae, чаще болеют дети и молодые люди в возрасте от 5 до 35 лет. Среди причин внебольничной пневмонии в этой возрастной группе хламидии уступают только Mycoplasma pneumoniae.
Начало болезни острое или постепенное. В первом случае симптомы интоксикации и поражения дыхательных путей достигают максимальной выраженности уже на 3-и сутки. При подостром течении хламидийная пневмония манифестирует с респираторного синдрома (ринита, назофарингита, ларингита), познабливания, субфебрилитета, в связи с чем в первую неделю болезни у пациентов ошибочно диагностируется ОРЗ. Главным образом, больных беспокоит заложенность носа, нарушением носового дыхания, умеренные слизистые выделения из носа, осиплость голоса.
Пневмония, вызванная Сhlamydia trachomatis
Начало часто постепенное; у детей хламидийной пневмонии нередко предшествует конъюнктивит, острый средний отит или бронхит этой же этиологии. Ранним признаком становится сухой кашель, который, усиливаясь, приобретает приступообразный характер. На фоне кашлевых приступов у ребенка возникает тахипноэ, цианоз и рвота, однако репризы отсутствуют. Постепенно отмечается усугубление одышки, увеличение ЧД до 50-70 в минуту, дыхание становится кряхтящим. Вместе с тем, общее состояние обычно остается удовлетворительным, симптомы интоксикации и дыхательная недостаточность выражены слабо.
Аускультативная и рентгенологическая картина двусторонней хламидийной пневмонии разворачивается к исходу первой – в начале второй недели. В разгар заболевания могут появиться симптомы энтероколита, гепатоспленомегалия. Выздоровление часто затягивается на многие недели и месяцы. При тяжелых формах хламидийной пневмонии может возникать пневмоторакс, плеврит, абсцедирование. Из внелегочных осложнений встречаются миокардиты, эндокардиты, менингоэнцефалиты. Дети, перенесшие хламидийную пневмонию, вызванную Ch. trachomatis, в дальнейшем чаще страдают бронхиальной астмой и другими хроническими обструктивными заболеваниями легких.
Пневмония, вызванная Chlamydophila psittaci (Орнитоз)
Варианты клинического течения орнитоза различны – от бессимптомного до тяжелого. Самым ярким симптомом выступает высокая (до 39,5-40°С и выше) температура тела, сопровождающаяся ознобами и сильнейшей интоксикацией (резкой слабостью, головной болью, артралгиями, миалгиями). В отсутствие других симптомов данное состояние нередко расценивается как лихорадка неясного генеза.
В дальнейшем более чем в половине случаев возникает малопродуктивный кашель, боль в груди, увеличение печени и селезенки. Характерными признаками, указывающими на хламидийную этиологию пневмонии, служат признаки нейротоксикоза, пятнистая сыпь на коже, носовые кровотечения. Часто возникают расстройства пищеварения: тошнота, рвота, абдоминальные боли, поносы или запоры.
Клинико-рентгенологические изменения могут сохраняться в течение 4-6 недель. Типичными осложнениями орнитоза выступают гепатит, ДВС-синдром, венозные тромбозы, гемолитическая анемия, полиневропатии, миокардит.
Диагностика
Затруднения при установлении этиологического диагноза связаны с тем, что в отличие от бактериальных пневмоний, при хламидийной пневмонии отсутствуют отчетливые физикальные и рентгенологические признаки, а также характерные изменения в периферической крови. В этих условиях терапевтам и пульмонологам приходится ориентироваться, главным образом, на указания анамнеза, особенности клинической картины и подтверждать свои подозрения лабораторными методами (ИФА, ПЦР и др.).
- Физикальный осмотр. Аускультативные данные вариабельны: дыхание может быть жестким, бронхиальным или ослабленным везикулярным; хрипы в разгар заболевания чаще влажные или крепитирующие. Перкуторный звук обычно притуплен.
- Рентгенография. При рентгенографии легких выявляется очаговая, сегментарная или долевая инфильтрация либо интерстициальные изменения.
- Лабораторная диагностика. Наиболее специфичным и чувствительным является культуральный метод выделение возбудителя, однако из-за длительности и трудоемкости диагностики на практике обычно ограничиваются серотипированием. Стандартом на сегодняшний день служат ИФА и МИФ (реакция микроиммунофлюоресценции). При проведении ИФА на активность хламидийной инфекции указывает повышение титра специфических IgМ, IgG и IgА более 1:16, 1:512 и 1:256 соответственно; МИФ - повышение титра IgG/IgА в парных сыворотках крови в 4 и более раз. ПЦР-анализ позволяет быстро и безошибочно идентифицирвоать ДНК возбудителя, однако не позволяет отличить персистирующую инфекцию от активной.
Дифференциальную диагностику хламидийной пневмонии следует проводить с гриппом, коклюшем; вирусной, микоплазменной, легионеллезной, грибковой пневмонией и другими атипичными легочными инфекциями.
Лечение хламидийной пневмонии
Сложность эффективного лечения хламидийной пневмонии сопряжена с тем, что хламидии присутствуют в организме одновременно как во внеклеточных, так и внутриклеточных формах, поэтому необходимо воздействовать на оба этих звена. Кроме этого, активизация инфекции, как правило, происходит на фоне угнетения иммунитета, что также требует коррекции иммунного ответа.
Средствами эрадикационной терапии при хламидийной пневмонии признаны антимикробные препараты из групп макролидов, фторхинолонов и тетрациклинов. Наиболее предпочтительны среди них макролиды, т. к. могут применяться для терапии новорожденных, детей и беременных. Из препаратов этой группы наибольшей активностью в отношении хламидий обладают кларитромицин, джозамицин, эритромицин, спирамицин.
Также успешно справляются с хламидийной инфекцией фторхинолоны (ципрофлоксацин, офлоксацин, левофлоксацин) и тетрациклины (доксициклин, моноциклин), однако прием последних исключается при беременности и печеночной недостаточности. Длительность курса противомикробного лечения хламидийной пневмонии составляет не менее 2–3 недель.
С целью коррекции иммунологических расстройств, а также предупреждения рецидива инфекции, помимо антимикробных средств, назначаются иммуномодуляторы, витамины, пробиотики. В период реконвалесценции большое внимание уделяется физиотерапии, дыхательной гимнастике.
Прогноз
У пациентов молодого возраста с отсутствием сопутствующей патологии хламидийная пневмония обычно оканчивается выздоровлением. Среди пожилых летальные исходы возникают в 6-10% случаев. Наблюдения специалистов указывают на возможную этиологическую роль Ch. pneumoniae в развитии атеросклероза, саркоидоза легких, ишемического инсульта, болезни Альцгеймера, поэтому перенесенная хламидийная пневмония может иметь далеко идущие последствия. Однозначно доказано отрицательное влияние респираторного хламидиоза на течение бронхиальной астмы и частоту ее обострений.
Микоплазменная респираторная инфекция представляет собой острую инфекцию дыхательных путей, характеризующуюся развитием бронхопневмонии. Респираторный микоплазмоз представляет собой весьма распространенное заболевание. Отмечается волнообразный подъем заболеваемости с частотой 1 раз в 2-4 года. Имеет место сезонность: пик заболеваемости приходится на холодное время года. Микоплазмозы составляют 6-22% всех острых пневмоний и 5-6% заболеваний дыхательных путей. В периоды эпидемических вспышек доля микоплазменных инфекций среди респираторных заболеваний может достигать 50%.
Общие сведения
Микоплазменная респираторная инфекция представляет собой острую инфекцию дыхательных путей, характеризующуюся развитием бронхопневмонии. Респираторный микоплазмоз представляет собой весьма распространенное заболевание. Отмечается волнообразный подъем заболеваемости с частотой 1 раз в 2-4 года. Имеет место сезонность: пик заболеваемости приходится на холодное время года. Микоплазмозы составляют 6-22% всех острых пневмоний и 5-6% заболеваний дыхательных путей. В периоды эпидемических вспышек доля микоплазменных инфекций среди респираторных заболеваний может достигать 50%.

Характеристика возбудителя
Возбудителем микоплазменной респираторной инфекции является Mycoplasma pneumoniae. Микоплазмы представляют собой микроорганизмы, не имеющие клеточной стенки, внедряющиеся в клеточную структуру ткани организма хозяина. Микоплазмы различных видов выделяются из растений, тканей человека и животных. Для 14 видов микоплазм человек является естественным хозяином. Mycoplasma pneumoniae выделяется своей способностью продуцировать гемолизин и гемаглютинины, ферментировать углеводы. Микоплазма в аэрозоли внутри помещения может сохранять жизнеспособность до получаса, при 4 °С - 37 часов, при 37 °С – 5 часов. Микроорганизмы чувствительны к облучению УФ и рентгеновскими лучами, ультразвуковым колебаниям, вибрации, реагируют на изменение кислотно-основного состояния среды, температурные условия.
Источником и резервуаром микоплазменной респираторной инфекции является человек. Больные выделяют возбудителя около 7-10 дней после начала заболевания, в некоторых случаях этот период удлиняется. Носительство без клинический проявлений вне эпидемического очага практически не встречается, но транзиторно может отмечаться у лиц, длительно и тесно общающихся с больным. Пневмонийная микоплазма передается с помощью аэрозольного механизма воздушно-капельным и воздушно-пылевым путем, в некоторых случаях может реализоваться контактно-бытовой путь передачи (через загрязненные руки, предметы быта).
Естественная восприимчивость человека к микоплазменной инфекции умеренная, чаще поражаются лица, страдающие иммунодефицитными состояниями, вызванными различного рода тяжелыми системными заболеваниями, больные с синдромом Дауна, серповидно-клеточной анемией. Отмечается генетическая склонность к развитию микоплазменной респираторной инфекции. Постинфекционный иммунитет стойкий, продолжительность может достигать 5-11 лет. При перенесении латентной формы инфекции напряженность иммунитета ниже.
Пневмонийные микоплазмы имеют сродство к клеткам эпителия, выстилающего слизистые оболочки всей дыхательной системы, что позволяет микроорганизму поражать любые ее отделы, вызывая инфильтративный воспалительный процесс. Продуцирование микоплазмой супероксиданта способствует отмиранию эпителиальных клеток дыхательных путей, что вызывает воспаление как в бронхах, так и в прилегающих тканях. При распространении процесса поражаются альвеолы, их стенки при этом уплотняются.
Диссеминация микоплазмы вызывает воспаления других органов и систем: суставов (артрит), мозговых оболочек (менингит), может вызывать гемолиз, кожные высыпания. Чаще всего микоплазменная респираторная инфекция протекает в виде пневмонии или бронхита, ларингита. Может проявляться как ОРВИ, или осложнять течение какой-либо вирусной респираторной инфекции.
Симптомы респираторного микоплазмоза
Инкубационный период микоплазменной инфекции может составлять от нескольких дней до месяца. У лиц с синдромом иммунодефицита может проявиться клинически спустя длительное время латентного носительства возбудителя. Респираторный микоплазмоз нередко протекает в форме разнообразных заболеваний верхних дыхательнах путей (ринофарингит, ларингофарингит, трахеит, бронхит), показывая характерную для них клиническую картину. Явления общей интоксикации и температурная реакция, как правило, умеренная, выраженный токсикоз и лихорадка, в основном, развиваются у детей.
При микоплазменных поражениях верхних дыхательных путей отмечается сухой мучительный кашель, боль в горле, ринорея. Осмотр может выявить конъюнктивит, инъецированность склер, умеренное увеличение лимфатических узлов: подчелюстных, шейных. Слизистая оболочка глотки, миндалины, небные дужки гиперемированы, иногда отмечается зернистость. При аускультации легких дыхание жесткое, сухие хрипы.
Чаще всего заболевание непродолжительно, клиническая симптоматика стихает через неделю, иногда затягивается на срок до двух недель. В большинстве случаев микоплазменная респираторная инфекция протекает по типу пневмонии, которая может начаться как остро, с специфических симптомов поражения легких, так и на фоне клиники ОРВИ спустя несколько дней после появления катаральной симптоматики.
Для микоплазменной пневмонии характерна интоксикация (головная боль, озноб, мышечные и суставные боли), лихорадка, достигающая 39 градусов. Кашель из сухого прогрессирует во влажный, с отделением скудной, вязкой мокроты прозрачного или беловатого цвета, позднее – с гнойными вкраплениями. Для микоплазменной пневмонии затруднения дыхания, сердечно-сосудистые нарушения не характерны, цианоз не отмечается.
Иногда интоксикацию могут сопровождать тошнота, рвота и диарея. Кожные покровы больных бледные, склеры инъецированы, выслушивание легких может вовсе не выявить нарушений, либо обнаружить жесткое дыхание и локализованные сухие или мелкопузырчатые хрипы. Результатом микоплазменной пневмонии могут стать бронхоэктазы, деформирующий бронхит, пневмосклероз.
Микоплазменная респираторная инфекция может осложняться экссудативным плевритом, воспалением сердечной мышцы (миокардит), мозговых оболочек.
Диагностика
Возбудителя микоплазменной респираторной инфекции выделяют из мокроты, крови, мазка носоглотки, после чего проводят бактериологическое исследование. Серологические методы (выявление антител к возбудителю) включают РНГА, РСКА, РН, ИФА. Общий анализ крови показывает лимфоцитоз при нормальном количестве лейкоцитов или умеренном повышении их концентрации.
Важным диагностическим методом выявления пневмонии является рентгенография легких. При этом в легких отмечаются зоны инфильтративного воспаления, как сегментов легких, так и интерстициальной ткани. Рентгенологические признаки пневмонии могут сохраняться некоторое время после клинического выздоровления. Пациенты с респираторным микоплазмозом нуждаются в консультации отоларинголога и пульмонолога.
Лечение респираторного микоплазмоза
Этиотропная терапия микоплазменной респираторной инфекции заключается в назначении антибиотиков: эритромицина, азитромицина, кларитромицина. Препараты назначаются 10-14-дневным курсом в среднетерапевтических дозировках. При невозможности применения вышеуказанных средств можно назначить доксициклин. Если инфекция ограничивается верхними дыхательными путями, можно не прибегать к антибиотикотерапии, ограничившись симптоматическими средствами: отхаркивающими препаратами, сосудосуживающими средствами местного применения при рините, дезинфицирующими препаратами для полоскания горла, физиотерапевтическими методиками.
Хороший эффект при микоплазменных ларингофарингитах и ринофарингитах дает применение местного УФ-облучения, ингаляций с фитосоставами, бактерицидами. Пневмония, а также осложненные, тяжело протекающие формы микоплазменной инфекции лечатся в стационаре. Полиморфная эритема, миелиты, энцефалит являются показанием к назначению препаратов группы кортикостероидных гормонов.
Прогноз и профилактика
Как правило, прогноз благоприятный, в особенности в случаях протекания микоплазменной инфекции по типу ОРВИ. Пневмонии могут оставлять после себя участки склерозирования легочной ткани, бронхоэктазы. Заметно ухудшаться может прогноз при развитии тяжелых осложнений, угрожающих жизни состояний.
Общая профилактика микоплазменной респираторной инфекции соответствует таковой при других респираторных заболеваниях, подразумевает осуществление карантинных мероприятий в очаге инфекции, изоляцию больных на дому либо в стационаре вплоть до исчезновения клиники, соблюдение санитарно-гигиенических норм в лечебных учреждениях и коллективах. Личная профилактика подразумевает избегание тесного контакта с больными лицами, применение средств индивидуальной защиты (марлевые маски для защиты дыхательных путей), соблюдение личной гигиены. Мер специфической профилактики данного заболевания нет.
Читайте также:

