Можно при биопсии выявить вич
Обновлено: 12.05.2024
Инфекционная клиническая больница №2, Москва
Московский областной НИИ акушерства и гинекологии;
кафедра акушерства и гинекологии ФУВ МОНИКИ им. М.Ф. Владимирского
Кафедра акушерства, гинекологии, перинатологии и репродуктологии факультета последипломного профессионального обучения врачей Московской медицинской академии им. И.М. Сеченова;
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова
Инфекционная клиническая больница №2, Москва
Особенности патологии шейки матки у больных c ВИЧ-инфекцией
Журнал: Российский вестник акушера-гинеколога. 2013;13(1): 17‑22
Гафуров Ю.Т., Краснопольская К.В., Назаренко Т.А., Сундуков А.В. Особенности патологии шейки матки у больных c ВИЧ-инфекцией. Российский вестник акушера-гинеколога. 2013;13(1):17‑22.
Gafurov IuT, Krasnopol'skaia KV, Nazarenko TA, Sundukov AV. The specific features of abnormalities of the cervix uteri in HIV-infected patients. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(1):17‑22. (In Russ.).
Инфекционная клиническая больница №2, Москва
В обзоре отражены частота, особенности этиологии, патогенеза предраковых заболеваний и рака шейки матки у ВИЧ-инфицированных пациенток. Описаны методы обследования и лечения данной категории больных. Собраны разные мнения об эффективности стандартных методов терапии, приведены данные о положительной роли применения высокоактивной антиретровирусной терапии в комплексе лечебных мероприятий.
Инфекционная клиническая больница №2, Москва
Московский областной НИИ акушерства и гинекологии;
кафедра акушерства и гинекологии ФУВ МОНИКИ им. М.Ф. Владимирского
Кафедра акушерства, гинекологии, перинатологии и репродуктологии факультета последипломного профессионального обучения врачей Московской медицинской академии им. И.М. Сеченова;
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова
Инфекционная клиническая больница №2, Москва
Рак шейки матки (РШМ) занимает второе место в структуре смертности от онкологических заболеваний у женщин [3]. Диагностика и лечение патологии шейки матки остается одной из актуальных проблем гинекологии и, несмотря на успехи современной медицины, уровень заболеваемости имеет устойчивый восходящий тренд. Этиологическим фактором в развитии дисплазии шейки матки признано поражение вирусом папилломы человека (ВПЧ), а длительная персистенция ВПЧ способствует возникновению рецидивов и/или злокачественной трансформации поражений [4]. Особую актуальность представляет проблема заболеваний шейки матки у больных, пораженных вирусом иммунодефицита человека (ВИЧ). Это обусловлено тем, что повреждения шейки матки ВПЧ развиваются на фоне дисфункции иммунитета с нарушением противовирусного ответа [2], а наблюдение и обследование больных ВИЧ-инфекцией могут помочь смоделировать развитие интраэпителиальных повреждений в условиях иммунодефицита и разработать методы профилактики и лечения.
Накопленные данные исследователей всего мира показывают, что ВИЧ-инфицированные женщины отличаются более высоким уровнем хронического поражения ВПЧ, многообразием типов онкогенных вирусов, более частыми патологическими изменениями мазков по Папаниколау, агрессивностью течения РШМ по сравнению с этими данными у ВИЧ-отрицательных пациенток [64]. Выявлена прямая зависимость между продолжительностью заражения ВИЧ-инфекцией и возникновением патологии шейки матки [41]. Несмотря на успехи применения высокоактивной антиретровирусной терапии (ВААРТ), уровень поражения РШМ у ВИЧ-инфицированных остается выше, чем в популяции [13]. Длительное применение ВААРТ продлевает жизнь ВИЧ-инфицированных пациенток, следовательно, растет удельный вес ВПЧ-индуцированных заболеваний у этой категории больных [64].
ВИЧ-инфекция повышает риск поражения наружных половых органов ВПЧ [66], способствует более раннему [17] и более частому [37, 43] развитию тяжелой формы дисплазии и РШМ. При этом, чем выше степень иммунносупрессии и ниже уровень клеток СD4+, тем чаще выявляются высокоонкогенные штаммы ВПЧ и интраэпителиальные заболевания шейки матки, вплоть до рака [6, 18, 24, 45, 63].
Повреждения шейки матки способствуют гетеросексуальной и перинатальной передаче ВИЧ-инфекции [74]. У юных беременных, перинатально зараженных ВИЧ-инфекцией, при обследовании во время беременности чаще, чем в популяции, выявляли патологию шейки матки методом Папаниколау [15].
Мониторинг больных с дисплазией шейки матки показал значимое прогрессирование процесса у ВИЧ-инфицированных больных по сравнению с его течением у здоровых женщин [59, 63]. При обследовании больных с дисплазией шейки матки II-III степени выявлено, что у ВИЧ-инфицированных снижены показатели местного иммунного ответа [5]. ВПЧ высокого онкогенного риска, выявленный методом полимеразной цепной реакции из отделяемого цервикального канала, низкий уровень СD4+ и высокая вирусная нагрузка, являются факторами, способствующими возникновению дисплазии шейки матки, интраэпителиальной неоплазии [30, 37, 50, 73]. Напротив, при уровне СД4+ более 500 клеток/мл частота диагностики внутриэпителиальных повреждений у больных с ВИЧ-инфекцией не отличается от таковой у здоровых пациенток [81].
Частота выявления ВПЧ-инфекции быстро возрастает в течение первых лет после сероконверсии ВИЧ, по всей видимости, вследствие иммунной дисфункции слизистой оболочки шейки матки, характерной для ВИЧ-инфекции [79]. Хотя ВПЧ-инфицирование связано с передачей половым путем, у 22% ВИЧ-инфицированных больных с уровнем СD4+ менее 200 клеток/мл, не живущих половой жизнью, выявляли, по крайней мере, один тип ВПЧ [75].
В образцах, полученных при биопсии шейки матки, с нормальным эпителием и особенно с цервикальной интраэпителиальной неоплазией (CIN) у ВИЧ-инфицированных больных значительно чаще выявляли маркеры апоптоза [78].
ВИЧ-инфекция запускает патогенез плоскоклеточного РШМ у ВПЧ-пораженных больных [8, 38]. Уровень заболеваемости РШМ у лиц с ВИЧ или СПИДом имел стойкую тенденцию к увеличению в США за период с 1980 по 2007 г. [72]. В некоторых странах Африки РШМ является причиной самой высокой смертности [54]. Этот факт объясняется большим количеством ВИЧ-инфицированных женщин и отсутствием возможности цитологического исследования шейки матки [20]. Замечено, что РШМ чаще поражает больных, заразившихся половым путем [28], причем количество больных РШМ растет вместе с ростом числа ВИЧ-инфицированных [62].
У ВИЧ-инфицированных спектр ВПЧ более многообразен, чем у ВИЧ-негативных больных [24]. ВИЧ-инфицированные больные, пораженные РШМ, в среднем на 13 лет моложе ВИЧ-негативных [61]. Одни авторы указывают, что ВПЧ 16-го типа выявлялся у больных с ВИЧ-инфекцией, повреждениями шейки матки высокой степени тяжести и РШМ значительно чаще, чем у женщин с нормальными цитологическими мазками [24, 30, 44, 70]. Другие получили противоположный результат - ВПЧ
В настоящее время обязательным является ежегодный осмотр пациентки, включающий цитологическое исследование (РАР-тест), кольпоскопию, типирование ВПЧ у ВИЧ-инфицированных больных [19, 46]. Часто ВИЧ-инфицированные пациентки не знают, что использование РАР-теста может помочь в предотвращении РШМ [65], поэтому цитологическое исследование шейки матки должно быть включено в стандарт оказания помощи ВИЧ-инфицированным больным [65, 73]. Обязательному цитологическому обследованию должны быть подвергнуты ВИЧ-инфицированные пациентки старше 30 лет, так как у них вероятность диагностики повреждений шейки матки высокой степени тяжести достигает более 70% [9], и пациентки с уровнем СD4+ менее 200 клеток/мл [31].
Помимо РАР-теста в настоящее время для скрининга применяют цитологическое исследование вагинальных смывов, типирование ВПЧ, методы прямой визуализации [42]. Тестирование ВПЧ может способствовать сокращению числа случаев прогрессирующего РШМ [71]. Цитологическое исследование вагинальных смывов может быть альтернативой РАР-тесту [36], но не имеет преимуществ перед тестом Папаниколау [76]. Использование количественной оценки уровня вирусной нагрузки ВПЧ как маркера повреждения шейки матки у ВИЧ-инфицированных пациенток [51] и уровня СD4+ может быть полезным в качестве индикатора риска прогрессирования процесса [63].
ВПЧ проявляет наибольшую активность при уровне СD4+ менее 200 клеток/мл и вирусной нагрузке более чем 100 000 копий/мл [31, 75]. Любой подозрительный участок должен быть подвергнут биопсии и гистологической экспертизе [27], так как у 14,3% ВИЧ-инфицированных с нормальной цитологической картиной шейки матки выявляли CIN [7]. Эта группа больных характеризовалась уровнем СD4+ менее 500 клеток/мкл и поражением ВПЧ. Биопсия шейки матки должна сочетаться с выскабливанием цервикального канала, так как при этом значительно чаще выявляется патология у серопозитивных женщин [16].
Чаще всего для лечения повреждения шейки матки используется петлевая эксцизия, так как данная процедура может быть выполнена амбулаторно, позволяет исключить инвазивную неоплазию, оценить края резекции, сохранить репродуктивную функцию, сопровождается минимальной кровопотерей и низким процентом послеоперационных осложнений [68]. Однако данное вмешательство у ВИЧ-инфицированных больных менее эффективно, чем у ВИЧ-негативных пациенток [9, 52]. Петлевая эксцизия, выполненная больным с HSIL, несмотря на свою эффективность в 15% случаев дает рецидив процесса [53]. Рецидивы CIN после конизации составляют от 20 до 75% [77]. Описаны случаи развития рака через 2 года после петлевой эксцизии, выполненной по поводу LSIL [36]. Одной из причин неудачи считается низкий иммунный статус: при уровне СD4+ меньше 200 клеток/мл и CIN II-III степени [56]. Напротив, при уровне СD4+ более 500 клеток/мл, 5-летний мониторинг после конизации или петлевой эксцизии, выполненной по поводу HSIL, не выявил различий в группах ВИЧ-позитивных и ВИЧ-негативных пациенток [33]. Еще одна причина рецидива в том, что дооперационная кольпоскопия не всегда в состоянии визуализировать всю зону преобразования, и у части больных было эндоцервикальное распространение поражения [32].
ВИЧ-инфицированные больные хуже поддаются лучевой терапии РШМ [35]. В результате применения сочетанного (дистанционное + внутриполостное) лучевого лечения больных РШМ IIB-III стадии 4-летняя выживаемость у ВИЧ-негативных и ВИЧ-инфицированных составила 46% и 0 соответственно [47]. Поэтому есть мнение, что более предпочтительны радикальные методы лечения, например, экстирпация матки с верхней третью влагалища при дисплазии шейки матки [1].
Профилактика РШМ у ВИЧ-инфицированных больных остается важной задачей [40]. Среди женщин с ВИЧ-инфекцией в проспективном исследовании, которое включало меры по профилактике РШМ, уровень последнего не превышал такового в группе сравнения ВИЧ-негативных женщин [57].
Многие исследователи утверждают, что ВААРТ способствует снижению частоты, регрессу ВПЧ-повреждений шейки матки [60], предотвращению рецидива повреждений и РШМ [21, 39]. К примеру, ингибитор протеазы ВИЧ индинавир способен воздействовать на клетки, пораженные РШМ [48]. Следовательно, применение ВААРТ может быть приоритетом в профилактике РШМ по сравнению с вакциной.
Таким образом, большинство исследователей указывают на более высокую заболеваемость РШМ у ВИЧ-инфицированных больных по сравнению с таковой в общей популяции. Многие авторы обращают внимание на большую распространенность ВПЧ у этой категории больных.
В то же время существуют противоположные публикации, утверждающие, что вероятность более частого возникновения CIN и РШМ у больных ВИЧ-инфекцией не доказана [19], уровень клеток СD4+ у пораженных ВПЧ и ВПЧ-отрицательных не различается [19] и не влияет на возникновение интраэпителиальных повреждений [61]. Уровень повреждения эпителия шейки матки не зависит от продолжительности ВИЧ-инфекции, использования ВААРТ, вирусной нагрузки [30, 49, 59]. Уровень СD4+ до ВААРТ и после нее не имеет значения для прогнозирования течения РШМ [10]. Применение ВААРТ, увеличивая выживаемость за счет сокращения случаев смерти от оппортунистических инфекций, не влияет на продолжительность жизни больных раком шейки матки [14].
Таким образом, в мировой литературе нет единого мнения об особенностях патогенеза, терапии и профилактики интраэпителиальных повреждений у ВИЧ-инфицированных больных, и, следовательно, данная проблема ждет своего разрешения.
Балтийский федеральный университет им. Иммануила Канта, Калининград
Московский городской центр по профилактике и борьбе со СПИДом, Москва, Россия
ФГБУ "Российский центр судебно-медицинской экспертизы" Минздрава России
ВИЧ-ассоциированные заболевания в практике судебно-медицинских вскрытий
Журнал: Судебно-медицинская экспертиза. 2018;61(4): 28‑31
Балтийский федеральный университет им. Иммануила Канта, Калининград
Рассмотрены вопросы, связанные с судебно-медицинской диагностикой ВИЧ-ассоциированных заболеваний с учетом сведений, предоставленных из Московского городского центра профилактики и борьбы со СПИДом. Изучены количество и структура диагностированных ВИЧ-ассоциированных заболеваний. Проведен анализ коморбидных ВИЧ/СПИД причин насильственной и скоропостижной смерти, установленных в Бюро судебно-медицинской экспертизы Департамента здравоохранения Москвы за период с 2013 по 2016 г. Выявлена тенденция к увеличению числа случаев смерти от ВИЧ-ассоциированных инфекций: туберкулеза, пневмонии, резистентных к лечению хронических иммунодефицитных состояний, а также от злокачественных новообразований. Изученный период характеризовался увеличением возраста умерших. При насильственной смерти ВИЧ-ассоциированные болезни диагностировались как сопутствующие заболевания, среди которых существенно преобладали случаи острых отравлений наркотиками и алкоголем, травмы, самоубийства. Полученные результаты демонстрируют актуальность и значимость сотрудничества специалистов данных учреждений для судебно-медицинской диагностики и мониторинга ВИЧ-ассоциированных заболеваний.
Балтийский федеральный университет им. Иммануила Канта, Калининград
Московский городской центр по профилактике и борьбе со СПИДом, Москва, Россия
ФГБУ "Российский центр судебно-медицинской экспертизы" Минздрава России
Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ-инфекция) — медленно прогрессирующее антропонозное заболевание с контактным механизмом передачи. Характеризуется специфическим поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИД), приводящего к смерти от вторичных оппортунистических инфекций, злокачественных новообразований, аутоиммунных процессов. В течение последних 10 лет из различных ВИЧ-ассоциированных инфекций наиболее часто встречается туберкулез. ВИЧ-инфекция часто сочетается с иными сопутствующими заболеваниями, в том числе вирусными гепатитами, наркозависимостью. После широкого внедрения антиретровирусной терапии (АРТ) ВИЧ-инфекция перестала быть фатальной и приняла характер управляемого хронического заболевания, при котором возможно сохранить продолжительность и качество жизни, социальную активность. Продолжительность жизни ВИЧ-инфицированного, принимающего эффективную схему АРТ, вполне сопоставима с таковой у человека, не инфицированного ВИЧ. По данным объединенных программ ООН по ВИЧ/СПИДу (ЮНЭЙДС), общее число умерших от причин, связанных со СПИДом, с момента начала эпидемии составляет около 35 млн. В настоящее время наблюдается общемировой тренд на снижение числа случаев смерти от причин, связанных со СПИДом: в 2016 г. умерли около 1 млн человек, в 2005 г. — 1,9 млн. Наиболее значительно (от 1,1 млн в 2004 г. до 420 000 тыс. в 2016 г.) число случаев смерти больных ВИЧ-инфекцией снизилось в Восточной и Южной Африке, что объясняется широким внедрением АРТ в данных регионах [1, 2].
В частности, предполагать ВИЧ-инфекцию следует при выявлении персистирующей генерализованной лимфаденопатии (увеличение двух и более лимфатических узлов до 1 см в диаметре на протяжении 3 мес); кандидозе, кокцидиоидомикозе, криптококкозе; длительной диарее (более 1 мес); цитомегаловирусной инфекции; вирусе простого герпеса; деменции, истощении с потерей более 10% массы тела, лихорадке продолжительностью более 1 мес; гистоплазмозе, изоспориазе продолжительностью более 1 мес, а также при саркоме Капоши, лимфоме Беркитта, иммунобластной саркоме, лимфомах; микобактериозе, вызванном атипичными микобактериями; внелегочном туберкулезе; сальмонеллезе, септицемии; пневмоцистной пневмонии; лейкоэнцефалопатии; токсоплазмозе и других иммунодефицитных состояниях [5—7].

Для повышения качества информации о структуре летальности целесообразно сопоставление персональных данных умерших с реестрами центров СПИДа. Данное исследование, посвященное посмертной диагностике ВИЧ-ассоциированных заболеваний, демонстрирует эффективность взаимодействия судебно-медицинской службы с территориальными центрами профилактики и борьбы со СПИДом. Провели анализ ВИЧ-ассоциированных заболеваний, диагностированных в Бюро судебно-медицинской экспертизы Департамента здравоохранения Москвы (далее Бюро) в период 2013—2017 гг. с учетом сведений, полученных из Московского городского центра профилактики и борьбы со СПИДом (МГЦ СПИД). За указанный период в ответ на 32 359 запросов из танатологических отделений Бюро с информацией о поступивших в морг трупах из МГЦ СПИД пришло 3016 извещений о прижизненной регистрации ВИЧ-инфекции, установленной методом иммуноблоттинга. Количество ежегодно направляемых в Бюро извещений, а также их доля в общем числе запросов из Бюро в МГЦ СПИД представлены в табл. 1. Таблица 1. Количество извещений о регистрации ВИЧ-инфекции в МГЦ СПИД
В изученных наблюдениях не имелось существенных различий по полу и возрасту. Возраст мужчин составлял от 21 года до 60 лет, женщин — от 20 до 55 лет. В динамике за 6 лет с 2012 по 2017 г. средний возраст мужчин увеличился на 5,7 года (с 36,2±19,5 до 41,9±18,9 года), женщин — на 5,2 года (с 33,6±18,1 до 38,5±18,4 года).
Согласно классификации, утвержденной Приказом Минздравсоцразвития России № 166 от 17.03.06, при диагностировании ВИЧ-инфекции следует устанавливать стадии, фазы и варианты течения [8].

Среди изученных случаев судебно-медицинских вскрытий преобладала IVБ стадия ВИЧ-инфекции (табл. 2). Таблица 2. Количество случаев ВИЧ-инфекции с учетом стадии болезни
Во всех наблюдениях проводился химико-токсикологический анализ для обнаружения наркотиков, сильнодействующих и психотропных веществ. Из общего количества наблюдений выделены случаи, в которых ВИЧ-инфекция была диагностирована как основное или сопутствующее заболевание. Оказалось, что почти в ¼ всех наблюдений (3016 случаев, или 24,7%) ВИЧ-инфекция диагностирована как основное заболевание, в остальных — как сопутствующее, а частично — как фоновое. Среди ВИЧ-ассоциированных болезней, диагностированных как первоначальная причина смерти, чаще других встречались туберкулез легких и внутригрудных лимфатических узлов (37,2%), пневмония (29,5%), орофарингеальный кандидоз и кандидоз пищевода (24,9%).
В динамике за изученный период установлена выраженная тенденция к увеличению числа случаев смерти от таких ВИЧ-ассоциированных заболеваний, как туберкулез, злокачественные новообразования, хронические резистентные и иммунодефицитные состояния. Выявили тенденцию к увеличению возраста умерших, у которых указанные заболевания были диагностированы в качестве основной причины смерти.
Редко определялись или были единичными случаи таких ВИЧ-ассоциированных заболеваний, как лимфома Беркитта, криптококкоз, злокачественная лимфома кардиального отдела желудка с распадом и прорастанием в нижнюю треть пищевода, плазмобластная лимфома внутрибрюшных лимфатических узлов, саркома Капоши.
При наличии ассоциированных с ВИЧ-инфекцией заболеваний и состояний ведущая роль в патогенезе отводится ВИЧ-инфекции, что соответствует блоку B20—B24 в МКБ-10. При анализе наблюдений в 7,6% от всех изученных случаев выявили ошибки кодирования причин смерти, не отвечающие требованиям МКБ-10.

Патоморфологическая картина ВИЧ-ассоциированных заболеваний имеет характерные секционные и гистологические отличия: утрата черт специфичности воспалительного процесса; воспаление без признаков волнообразного течения; мономорфность гнойно-некротических фокусов в легких; отсутствие элементов продуктивного воспаления по периферии очагов; перифокально выраженная экссудативная реакция; преимущественно периваскулярное расположение очагов воспаления. Иммуносупрессивный характер ВИЧ-инфекции проявляется в прогрессировании вторичных оппортунистических инфекций, а микроскопическая картина — в некоторой стертости границ перифокальной воспалительной реакции (см. рисунок). Микроскопическая картина ВИЧ-ассоциированных заболеваний. a — туберкулезный очаг в легком. Окраска по методу Ван-Гизона. Ув. 400; б — микобактерии туберкулеза. Окраска по методу Циля—Нильсена. Ув. 600; в — пневмоцистная пневмония. ШИК-реакции (реактив Шиффа). Ув. 400; г — (головной мозг) цитомегаловирусная инфекция. Окраска гематоксилином и эозином. Ув. 800.

В случаях насильственной смерти установленную ВИЧ-инфекцию диагностировали как сопутствующее заболевание. Частота таких случаев в зависимости от вида насильственной смерти отражена в табл. 3. Таблица 3. Виды насильственной смерти, при которых ВИЧ-инфекция диагностирована как сопутствующее заболевание
ВИЧ-инфекция как сопутствующее заболевание диагностирована при вторичной кардиомиопатии (8,7%), циррозе печени в исходе хронического вирусного и алкогольного гепатита (3,4%). Таким образом, ВИЧ-инфекция в качестве сопутствующего заболевания преобладала при острых отравлениях наркотиками, алкоголем, механической травме, в том числе при суицидах, а также при смерти от вторичной кардиомиопатии.
Заключение
Анализ ВИЧ-ассоциированных заболеваний, диагностированных в Бюро, с учетом сведений из МГЦ СПИД за период 2013—2017 гг. отражает увеличение случаев смерти от таких ВИЧ-ассоциированных заболеваний, как туберкулез, злокачественные новообразования, хронические резистентные и иммунодефицитные состояния. Отметили также увеличение возраста умерших, у которых указанные патологии диагностированы как основная причина смерти.
Наиболее часто ВИЧ-инфекция отмечалась в качестве основной причины смерти в сочетании с туберкулезом легких, пневмонией, кандидозом, а в качестве сопутствующего заболевания — с отравлением наркотиками, алкоголем и механическими травмами, что согласуется с результатами исследований, изложенных в современных публикациях [9—11].
Авторы выражают благодарность Юлии Рашидовне Зюзе, к.м.н., заведующей централизованным патологоанатомическим отделом Инфекционной клинической больницы № 2 Москвы, за возможность использования гистологических препаратов.
Диагностика заболеваний органов грудной клетки у больных ВИЧ-инфекцией с помощью видеоэндохирургических технологий
Журнал: Эндоскопическая хирургия. 2017;23(2): 17‑22
Проведен анализ результатов видеоэндоскопических методов диагностики заболеваний органов грудной клетки у ВИЧ-инфицированных пациентов. Выполнены следующие видеоэндохирургические и видеоассистированные оперативные вмешательства: видеоторакоскопия, биопсия плевры/легкого/лимфоузла — 55 (70,5%); видеомедиастиноскопия, биопсия лимфатических узлов средостения — 17 (21,7%); резекция легкого (сегментарная или лобэктомия) — 5 (6,5%); пневмонэктомия — 1 (1,3%). Из 78 оперированных пациентов диагноз туберкулеза был установлен у 56 (71,8%), нетуберкулезную этиологию имели 22 (28,2%) пациента, наиболее часто встречаются неспецифические плевриты —11 (14,1%), лимфомы — 5 (6,4%) и доброкачественные образования легких — 3 (3,8%). Использование видеоэндохирургических методов в диагностике заболеваний органов грудной клетки является безопасным, эффективным и не приводит к значительному числу осложнений и летальности среди больных ВИЧ-инфекцией вне зависимости от исходного иммунного статуса.
В настоящее время в мире продолжает увеличиваться число больных ВИЧ-инфекцией, связано это как с регистрацией новых случаев заболевания, так и с продлением срока жизни пациентов в результате широкого применения антиретровирусной терапии (АРТ) [1]. Прогрессирование ВИЧ-инфекции, связанное со снижением иммунологической реактивности, сопровождается присоединением вторичных заболеваний, которые определяют тяжесть состояния больных и исход. Своевременная диагностика и лечение ВИЧ-ассоциированных заболеваний позволяет значительно продлить жизнь ВИЧ-инфицированным лицам и улучшить ее качество [2]. Одним их наиболее часто встречающихся вторичных заболеваний является туберкулез, больные ВИЧ-инфекцией в 20—37 раз более подвержены риску развития туберкулеза в сравнении с ВИЧ-негативными лицами [3]. По оценке ВОЗ, около 10,4 млн человек заболели туберкулезом в мире, из них не менее 1,2 млн (11,6%) составили больные ВИЧ-инфекцией. За 2015 г. от туберкулеза умерли порядка 1,8 млн человек, из них сочетанная ВИЧ/туберкулез инфекция имелась у 390 тыс. — около 22% от всех умерших от туберкулеза и не менее 30% от 1,1 млн человек, умерших в 2015 г., ВИЧ-позитивных жителей [4].
Эпидемиологическая обстановка по туберкулезу в России существенно улучшилась за последние годы, а уровень заболеваемости в Москве сопоставим с показателями наиболее экономически развитых стран Европы, постоянные жители болеют туберкулезом все реже, происходит замещение контингентов на представителей групп риска. В Москве за период с 2010 по 2014 г. отмечено увеличение доли больных ВИЧ-инфекцией с впервые выявленным туберкулезом с 14,6 до 20,3%. В то же время абсолютное число впервые выявленных больных ВИЧ/туберкулезом не увеличилось, а, наоборот, имело тенденцию к уменьшению с 419 до 400 (с выявленными посмертно). За последние 5 лет доля больных ВИЧ/туберкулез инфекцией среди больных, стоящих на учете в противотуберкулезной службе города Москвы, возросла с 11,2 до 16,3%, а в абсолютных цифрах число больных уменьшилось с 812 до 795. Распространенность ВИЧ/туберкулез-инфекции в Москве снижается, в 2013 г. этот показатель составлял 6,8 на 100 000 населения, а в 2014 г. — 6,5 на 100 000. В Москве увеличение доли больных сочетанной ВИЧ/ТБ-инфекцией связано не с увеличением ВИЧ-инфицированных лиц, а со снижением числа больных туберкулезом в городе [5].
Для выявления и диагностики туберкулеза разработаны алгоритмы обследования с включением лучевых методов (цифровая флюорография или рентгенография, мультиспиральная компьютерная томография), различных иммунологических тестов, в первую очередь это туберкулиновая кожная проба и тесты, основанные на фиксации освобождаемого гамма-интерферона (IGRA-тесты). Проведенные исследования не установили преимущества того или иного теста с позиций доказательной медицины [6, 7]. В то же время многие авторы высказывают мнение о большей чувствительности тестов IGRA в сравнении с туберкулиновой пробой [8—10]. В России у ВИЧ-инфицированных лиц наряду с кожной туберкулиновой пробой и IGRA-тестами нашел свое применение тест с аллергеном туберкулезным рекомбинантным [7, 11]. Основным диагностическим критерием установления диагноза туберкулеза является выявление возбудителя (микобактерий туберкулезного комплекса, наиболее часто — Mycobacterium tuberculosis) бактериологическим или молекулярно-генетическим методом, а также морфологическая верификация. Кроме туберкулеза у больных ВИЧ-инфекцией могут встречаться заболевания иной этиологии с поражением органов дыхания, плевры, внутригрудных лимфатических узлов, требующие проведения дифференциальной диагностики, в том числе с применением хирургических методов [12—15]. При снижении уровня CD4 + лимфоцитов ниже 50 кл/мкл присоединяется нетуберкулезная микобактериальная инфекция, вызванная Mycobacterium avium-intracellulare (MAC-инфекция). Это заболевание среди ВИЧ-негативных лиц встречается крайне редко, передача от человека к человеку инфекционного агента не доказана [16]. Лечение МАС-инфекции отличается от лечения туберкулеза, и поэтому необходимо проводить видовую идентификацию возбудителя с определением лекарственной чувствительности.
ВИЧ-инфекция является фактором риска развития злокачественных заболеваний, по сравнению с общей популяцией риск заболевания саркомой Капоши у ВИЧ-инфицированных выше в 3640 раз, лимфомами в 200—600 раз [17]. Применение АРТ привело к определенному снижению опухолевых заболеваний, однако отмечается постоянный рост других новообразований, таких как рак легких, молочной железы, печени, лимфогранулематоз. Частота рака легкого у ВИЧ-инфицированных в 2—3 раза превышает общепопуляционные показатели даже после проведения коррекции показателя с учетом курения. Полученные результаты комплексного лечения рака легкого показали отсутствие негативного влияния ВИЧ-инфекции на его результат, который определялся в основном стадией онкологического заболевания при выявлении [18, 19]. Указанные особенности эпидемиологии онкологических заболеваний среди больных ВИЧ-инфекцией определяют необходимость тщательного скрининга и диагностики новообразований в этой группе населения [20].
В связи с этим проблема дифференциальной диагностики заболеваний грудной клетки у ВИЧ-инфицированных пациентов является весьма актуальной. При неинформативности методов детекции возбудителя зачастую единственно возможным способом установления диагноза остается биопсия легочной ткани, плевры, внутригрудных лимфоузлов с морфологическим исследованием. Бесспорное преимущество среди хирургических методов принадлежит малоинвазивным операциям, к которым можно отнести видеоэндохирургические вмешательства: торакоскопию с биопсией легкого, плевры, лимфоузлов, медиастиноскопию с биопсией лимфоузлов. Сокращение сроков госпитализации, уменьшение болевого синдрома, малое число осложнений и ранняя послеоперационная реабилитация — основные достоинства указанных методик [11, 21, 22].
Цель исследования — изучение возможности и эффективности применения видеоэндоскопических методов в диагностике заболеваний органов грудной клетки у ВИЧ-инфицированных пациентов, а также особенностей течения послеоперационного периода.
Материал и методы
В исследование включены 78 больных ВИЧ-инфекцией, которым были выполнены диагностические торакальные операции с применением видеоэндохирургических методов в Клинике № 2 ГБУЗ МНПЦ борьбы с туберкулезом ДЗМ за период 2013—2016 гг. Изучена структура оперированных больных с сочетанием ВИЧ-инфекции и заболеваний органов грудной клетки, этиологию которых невозможно было определить с помощью рентгенологического исследования (мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки с внутривенным контрастированием), микробиологических методов, иммунологических проб. Выполнена оценка послеоперационных результатов диагностических операций. Для этого были проанализированы медицинские карты, протоколы операций, результаты бактериологического, молекулярно-генетического и морфологического обследования. Использованы аналитический, экспертный и статистический методы для оценки результатов.
В общем числе пациентов мужчин было — 56 (71,8%), женщин — 22 (28,2%). Средний возраст пациентов — 31,7±7,0 года (от 19 до 62 лет), большинство — лица молодого возраста от 20 до 40 лет — 69 (88,5%) человек (табл. 1). Преобладали постоянные жители города Москвы — 63 (80,8%) человека, представителей Московской области и других регионов Российской Федерации было 7 (9%) и 3 (3,8%) соответственно, лиц БОМЖ — 3 (3,8%), иностранных граждан — 2 (2,6%). Больные ВИЧ-инфекцией на момент выполнения им хирургического вмешательства находились на разных стадиях заболевания. Стадии вторичных заболеваний отмечены у 52 больных: IVБ у 36 (46,7%) и IVВ у 16 (19,4%), стадия III (субклиническая) у 26 (33,3%). У наибольшего числа больных диагноз ВИЧ-инфекции был установлен в течение последних 5 лет — у 41 (51,9%), у 25 (32,5%) пациентов — от 5 до 10 лет, у 12 (15,6%) — более 10 лет. АРТ на момент госпитализации получали 55 (70,5%), никогда не получали или прервали ее 23 (29,5%) пациента. Все больные ВИЧ-инфекцией имели различный уровень иммуносупрессии. Выраженный иммунодефицит со снижением уровня CD4 + лимфоцитов ниже 400 кл/мкл имели 60 (76,7%) больных, причем предельно низкие показатели, ниже 200 кл/мкл, наблюдались у 34 (42,9%) пациентов. Только у 18 (23,4%) иммунный статус был относительно сохранен и уровень Т-хелперов был выше 400 кл/мкл. Большинство пациентов имели сопутствующие заболевания, среди которых первое место принадлежало хроническому вирусному гепатиту С, который диагностирован у 46 (59,0%) пациентов. Хронический вирусный гепатит С и В выявлен у 5 (6,4%) пациентов, кроме того, 42 (53,8%) пациента являлись активными потребителями психоактивных веществ.

Таблица 1. Распределение оперированных больных по возрасту
Выполнены следующие видеоэндохирургические и видеоассистированные оперативные вмешательства: видеоторакоскопия, биопсия плевры/легкого/лимфоузла — 55 (70,5%); видеомедиастиноскопия, биопсия лимфатических узлов средостения — 17 (21,7%); резекция легкого (сегментарная или лобэктомия) — 5 (6,5%), пневмонэктомия — 1 (1,3%). Полученный при операциях диагностический материал был подвергнут морфологическому, молекулярно-генетическому и бактериологическому анализу.
Результаты и обсуждение
В результате комплексного исследования операционно-биопсийного материала диагноз туберкулеза был установлен у 56 (71,8%) больных, нетуберкулезная этиология заболевания выявлена у 22 (28,2%). Среди больных туберкулезом преобладали пациенты с плевритом, эмпиемой плевры — 41 (52,6%), значительную группу составили пациенты с туберкулезом внутригрудных лимфатических узлов — 12 (15,4%), у 3 (3,8%) выявлена туберкулема легкого. У больных ВИЧ-инфекцией без туберкулеза большую группу составили пациенты с неспецифическим плевритом 11 (14,1%), далее распределение по нозологическим единицам было следующим: 5 (6,4%) пациентов с лимфопролиферативными заболеваниями (лимфома, лимфогранулематоз), 3 (3,8%) — с доброкачественными заболеваниями легких и средостения, 2 (2,6%) — с легочной формой саркомы Капоши, 1 (1,3%) — с нетуберкулезным микобактериозом (табл. 2). Интраоперационных осложнений не было, в послеоперационном периоде наблюдались осложнения: у 2 (2,6%) больных нагноение послеоперационной раны (торакопорт); у 6 (7,7%) — замедленное расправление легкого, потребовавшее длительного (до 8 суток) дренирования плевральной полости; у 4 (5,1%) больных после удаления дренажа из плевральной полости и выполнения на следующий день рентгенологического контроля выявлен пневмоторакс, что потребовало повторного дренирования плевральной полости. Все осложнения были ликвидированы. Послеоперационной летальности не было. У 14 (17,9%) пациентов после операции отмечено увеличение уровня СD4 + лимфоцитов, у 9 (11,5%) — снижение уровня СD4 + лимфоцитов, у 55 (70,6%) — значимых изменений не выявлено. Послеоперационные болевые ощущения были незначительными, и обезболивание проводилось только ненаркотическими анальгетиками.

Таблица 2. Характер выявленной патологии
Больной В., 33 года. ВИЧ-инфекция выявлена в 2013 г., получал АРТ. Генерализованный туберкулез с поражением внутригрудных, внутрибрюшных и периферических лимфоузлов также выявлен в 2013 г. Проведена противотуберкулезная химиотерапия с хорошим эффектом, достигнуто клиническое излечение. В 2016 г. при контрольной рентгенографии вновь выявлено увеличение внутригрудных лимфоузлов и заподозрен рецидив туберкулеза. МСКТ органов грудной клетки с внутривенным контрастированием (мягкотканное окно) показала: на уровне дуги аорты в верхнем центральном средостении конгломерат правых паратрахеальных лимфоузлов, сдавливающих просвет трахеи наполовину, смещающий сосудистые структуры кпереди; жидкость в плевральной полости (рис. 1). При фибробронхоскопии отмечены признаки сдавления трахеи, бронхов правого легкого — главного, верхнедолевого и среднедолевого. Учитывая клинико-рентгенологическую картину, решено провести морфологическую верификацию заболевания. Перед операцией уровень CD4 + лимфоцитов составлял 79 (13%) клеток, вирусная нагрузка не определялась. Произведена видеомедиастиноскопия, выполнена биопсия лимфоузлов. Послеоперационный период протекал без осложнений. Получено морфологическое заключение: лимфома Ходжкина, вариант нодулярного склероза. Больной для дальнейшего лечения переведен в гематологический стационар.

Рис. 1. КТ органов грудной клетки. В верхнем центральном средостении конгломерат правых паратрахеальных лимфоузлов.
Больная Ф., 64 года. ВИЧ-инфекция выявлена в 2008 г., АРТ получала в течение последних трех лет. В 2016 г. проходила обследование для планового оперативного лечения по поводу хронического калькулезного холецистита. Иммунный статус снижен умеренно: CD4 + лимфоциты — 579 (18%) клеток; определялась невысокая вирусная нагрузка — 128 копий/мл. Фибробронхоскопия патологических изменений не выявила. МСКТ органов грудной клетки показала: в S6 левого легкого определяется субплеврально расположенное округлое мягкотканное образование до 1,5 см в диаметре, с четкими контурами. Окружающая легочная паренхима не изменена (рис. 2 и 3). Установлен предварительный диагноз: туберкулема S6 левого легкого без бактериовыделения МБТ (–). Планировалось проведение курса противотуберкулезной химиотерапии в течение 2 мес. Однако появление новообразования в легком, c учетом возраста больной, является серьезным основанием для проведения дифференциальной диагностики между неспецифическими воспалительными изменениями, туберкулезом, первичной опухолью или метастатическим поражением легкого. Проведенное обследование не выявило патологических образований в других органах, и больная была оперирована одномоментно: выполнены видеоторакоскопическая резекция S6 левого легкого (срочное морфологическое исследование не показало данных за злокачественное новообразование) и лапароскопическая холецистэктомия. Плановое морфологическое заключение показало, что образование в легком являлось хондроматозной гамартомой. Послеоперационный период протекал без особенностей, больная выписана из противотуберкулезного учреждения под наблюдение специалистов Центра СПИДа. С учетом контакта с больными туберкулезом ей была назначена химиопрофилактика туберкулеза.

Рис. 2. КТ органов грудной клетки. В S6 левого легкого определяется периферическое округлое мягкотканное образование 1,5 см в диаметре (легочная реконструкция).

Рис. 3. КТ органов грудной клетки. В S6 левого легкого определяется периферическое округлое мягкотканное образование 1,5 см в диаметре (мягкотканное окно).
Приведенное клиническое наблюдение демонстрирует необходимость верификации изменений в легочной паренхиме у больных ВИЧ-инфекцией, так как лечебная тактика после установления морфологического диагноза может кардинально отличаться от ранее предложенной. Применение в торакальной хирургии эндохирургических методов у ВИЧ-инфицированных пациентов оправданно и безопасно.
Заключение
Использование малоинвазивных эндохирургических методов у больных ВИЧ-инфекцией торакального профиля не только безопасны и высокоэффективны, но и существенно снижают риск инфицирования ВИЧ медицинских работников при выполнении операции. Довольно часто хирургическая диагностика заболеваний органов грудной клетки проводится в учреждениях противотуберкулезной службы, что не является оптимальным по эпидемиологическим причинам в связи с риском инфицирования туберкулезом больных ВИЧ-инфекцией без туберкулеза, а это около трети направляемых пациентов.
Вывод
Проведенное исследование показало, что наиболее часто поражение органов грудной клетки у больных ВИЧ-инфекцией связано с туберкулезной инфекцией. Из 78 оперированных диагностических пациентов диагноз туберкулеза установлен у 56 (71,8%), инфекцию нетуберкулезной этиологии имели 22 (28,2%) пациента, наиболее частой патологией были неспецифические плевриты — в 11 (14,1%) случаях, лимфомы — в 5 (6,4%) и доброкачественные образования легких — в 3 (3,8%) случаях.
Использование видеоэндохирургических методов в диагностике заболеваний органов грудной клетки является безопасным, эффективным и не приводит к значительному числу осложнений и летальности среди больных ВИЧ-инфекцией независимо от исходного иммунного статуса.
При туберкулезе морфологическая верификация патологических изменений в сочетании с бактериологическим исследованием операционного материала позволяет назначить адекватный режим противотуберкулезной химиотерапии в соответствии с чувствительностью возбудителя. При установлении нетуберкулезной этиологии выявленных изменений ВИЧ-инфицированные пациенты из противотуберкулезного учреждения направляются в специализированные медицинские учреждения соответствующего профиля.
Тем не менее, в последние десятилетия адекватная противовирусная терапия позволила не только улучшить результаты противоракового воздействия, но и в разы уменьшить вероятность развития злокачественного процесса у ответственного пациента.
Когда при ВИЧ появляются злокачественные опухоли
Рак и другие злокачественные опухоли развиваются при переходе ВИЧ-инфекции в позднюю стадию болезни, когда концентрация иммунных клеток устремляется к минимальной, позволяя активно и почти беспрепятственно размножаться разнообразной микрофлоре — от простейший и грибов до бактерий и вирусов.
Всё, что происходило в организме инфицированного пациента ранее, было обычной ВИЧ-инфекцией, появление рака или других опухолей, а также тяжёлых распространённых инфекций — это уже СПИД.
Благодаря лечению период от заражения вирусом иммунодефицита до последней стадии болезни растянулся почти на три десятилетия, тогда как в конце 1980-х годов занимал несколько лет.
Какие раки развиваются при ВИЧ-инфекции
В конце ХХ века выявление определённых, практически не встречающихся при нормальном иммунитете заболеваний и злокачественных процессов, позволяло ставить диагноз ВИЧ/СПИД без сложных лабораторных исследований. Такие процессы обозначили как ассоциированные с вирусом иммунодефицита или, по-современному, СПИД-индикаторные. В этот список наряду с необычными инфекциями включены инвазивный рак шейки матки, саркома Капоши и злокачественные лимфомы, вероятность которых у инфицированного пациента возрастает в сотни раз.
Значительно чаще, но не в сотни раз, при ВИЧ-инфекции вероятно развитие плоскоклеточного рака анального канала и рака вульвы, карциномы лёгкого и злокачественных опухолей яичка, плоскоклеточного рака головы и шеи, меланомы и рака кожи.
Для большинства злокачественных процессов доказана основополагающая патогенетическая роль вирусов, в первую очередь, папилломы человека (ВПЧ) и гепатита В, С и D. Способствует раннему развитию злокачественных новообразований носительство вирусов герпеса, особенно 4 типа — вируса Эпштейна-Барр. Традиционно значимы у ВИЧ-инфицированных факторы риска злокачественного перерождения клеток бронхолегочной системы — курение и наследственная предрасположенность.
Как ВИЧ-инфекция влияет на течение рака
Однозначно — очень неблагоприятно, усугубляя скорость прогрессирования и увеличивая массив опухолевого поражения. И хотя рак у ВИЧ-инфицированного пациента возникает много раньше, чем в общей популяции, практически в молодом возрасте, пациенты не могут похвастать исходным хорошим здоровьем.

Как ВИЧ сказывается на переносимости химиотерапии
В большинстве случаев злокачественный процесс на фоне ВИЧ-инфекции течёт агрессивнее, поэтому на первом этапе требует системного лечения с использованием противоопухолевых препаратов, гарантирующих разнообразный спектр токсических реакций. При этом ни в коем случае нельзя отказываться от специфической противовирусной терапии, также изобилующей неблагоприятными проявлениями.
В итоге переносимость противоракового лечения, проводимого на фоне ВААРТ, ухудшается, а продолжительность жизни пациентов не в пример короче, чем это могло быть в отсутствии ВИЧ. При активной противоопухолевой и противовирусной терапии больше года после выявления опухоли живёт только каждый четвёртый, пятилетку — всего 19%.
Существует ещё одна серьёзная проблема — клинического изучения эффективности противоопухолевой терапии у ВИЧ-инфицированных не проводится из-за малочисленности групп пациентов и, следовательно, сомнительной достоверности результатов. Поэтому очень важно в этот тяжёлый период найти клинику и специалистов одинаково высоко компетентных в вопросах лечения ВИЧ и противораковой химиотерапии.
Как лечат рак у ВИЧ-инфицированных
В большинстве случаев терапия рака не должна отличаться от таковой у пациентов с нормальными показателями иммунитета.
При технической возможности хирургической операции ВИЧ-пациенту от неё нельзя отказываться, поскольку излечение возможно только при удалении всех очагов рака. Если для злокачественной опухоли лимфатической системы признана необходимость высокодозной химиотерапии с трансплантацией стволовых клеток, то и инфицированный вирусом пациент должен получить программное лечение. При раке шейки матки практически невозможно обойтись без лучевой терапии.
ВИЧ-компрометированному пациенту потребуется ВААРТ и гораздо более серьёзное сопроводительное лечение. Чтобы провести химиотерапию без сокращения доз и интервалов необходима индивидуальная программа реабилитационного воздействия. Кроме того, пациент должен получать множество препаратов для лечения грибковых поражений и сдерживания вирусов герпеса, разнообразные антибактериальные средства, каждое из которых имеет собственную токсичность.

Такое комплексное воздействие способна осуществить только команда врачей разных специальностей, блестяще ориентированная как в потребностях онкологического пациента, так и в возможностях организма инфицированного.
а) Терминология:
1. Аббревиатуры:
• Синдром приобретенного иммунного дефицита (СПИД)
• Вирус иммунодефицита человека (ВИЧ)
2. Определения:
• Внутрибрюшные оппортунистические инфекции и опухоли, возникающие на фоне ВИЧ-обусловленного иммунодефицита
б) Визуализация брюшной полости при ВИЧ/СПИД:
1. Общая характеристика:
• Локализация:
о Могут поражаться висцеральные органы, желудочно-кишечный тракт, мочевыделительная система, лимфатические узлы
• Размеры:
о Могут быть различными: от микроабсцесса (
2. Рекомендации по визуализации:
• Лучший метод визуализации:
о КТ с внутривенным контрастным усилением
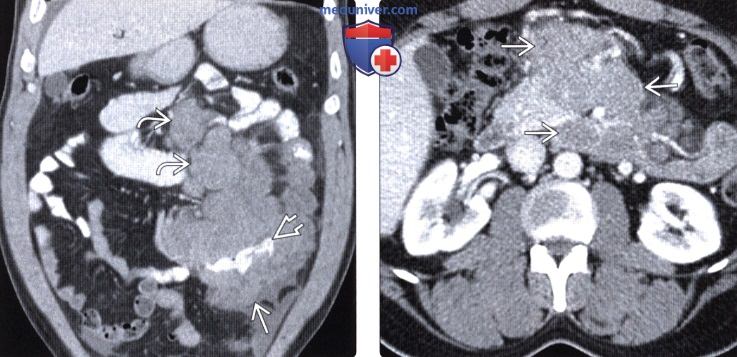
(Слева) На изображении в коро-нальной плоскости при КТ с контрастным усилением определяется диффузное опухолевидное утолщение стенки и расширение тонкого кишечника в левом нижнем квадранте, видно также контрастное вещество в просвете кишки. Чуть выше обратите внимание на выраженную лим фаденопатию. Эти изменения обусловлены подтвержденной биопсией СПИД-детерминированной неходжкинской лимфомой.
(Справа) На аксиальном срезе при КТ с контрастом определяется выраженная мезентериальная лимфаденопатия, обусловленная СПИД-детерминированной неходжкинской лимфомой.
3. КТ брюшной полости при ВИЧ/СПИД:
• Печень:
о В печени могут быть выявлены узловые образования и цирротические изменения, т. к. ВИЧ часто сопровождается хроническими вирусными гепатитами
о Маленькие гиподенсные диффузные очаги в паренхиме печени могут быть обусловлены микроабсцессами (часто при авиум-микобактериальной инфекции, туберкулезе, гистоплазмозе, поражении кандидами, пневмоцистами и др.)
о Могут наблюдаться диффузно-инфильтративные изменения печени, вызванные инфекциями, например авиум-туберкулезом
о Пневмоцисты (реже, чем при авиум-туберкулезе или цитомегаловирусной инфекции) могут приводить к появлению множественных диффузных кальцинатов
- Появление кальцинатов не означает снижение активности заболевания
о у 1/4 пациентов со СПИД-ассоциированной лимфомой печени выявляются гиподенсные узлы различного размера
• Билиарный тракт:
о Холангит, обусловленный оппортунистическими инфекциями:
- Экстра- и интрапеченочные билиарные стриктуры и сосочковый стеноз: желчные протоки могут выглядеть утолщенными и расширенными
- Внешний вид желчных протоков симулирует изменения при первичном склерозирующем холангите
о Акалькулезный холецистит в результате оппортунистических инфекций (цитомегаловирус, криптоспоридии):
- Утолщение и деформация желчного пузыря с наличием жидкости в окружающих тканях
• Селезенка:
о Спленомегалия выявляется у 3/4 пациентов со СПИДом, даже без наличия инфекции или опухоли
о Множественные мелкие гиподенсные очаги (микроабсцессы) обычно обусловлены диссеминированной инфекцией (например, грибками Candida, авиум-микобактериальной инфекцией, кокцидиоидомикозом, пневмоцистами и др.)
о Распространенные гиподенсные поражения могут возникать в результате инфильтративных инфекций, однако нельзя исключать и СПИД-ассоциированную лимфому
о Мелкие кальцинаты, похожие на таковые в печени, при пневмоцистной инфекции
• Желудок, тонкий и толстый кишечник:
о Утолщение стенки кишки, полнокровие слизистой и изменения жировой клетчатки вокруг кишечника всегда подозрительны в плане инфекций (включая оппортунистические)
- Язвообразование в кишечнике на фоне цитамегаловирусной инфекции может привести к перфорации (одна из наиболее частых причин экстренных оперативных вмешательств в брюшной полости у пациентов со СПИДом)
о Многие оппортунистические инфекции могут поражать любой отдел ЖКТ (криптоспоридии, ЦМВ, микобактериальная авиум-инфекция, туберкулез, микромпоридии, Clostridium difficile, амебиаз и др.):
- Предугадать вид возбудителя на основе только его локализации - очень сложная задача, однако некоторые возбудители имеют склонность к определенным отделам ЖКТ:
ЦМВ и туберкулез поражают преимущественно подвздошную кишку
Кандиды, микроспоридии - преимущественно начальные отделы тонкого кишечника
Инфекционные заболевания толстого кишечника чаще всего обусловлены ЦМВ, С. difficle, Campylobacter, амебной инфекцией, сальмонеллами и шигеллами
о Утолщение стенки пищевода говорит об эзофагите, чаще всего обусловленном кандидами, ЦМВ или вирусом простого герпеса
о Проктит у гомосексуалистов, связанный с сексуальной активностью, может быть вызван гонококками Нейссера, хламидиями или вирусом простого герпеса
о Местное утолщение стенки кишки, похожее на объемное образование, подозрительно на злокачественную опухоль (лимфома, саркома Капоши):
- Лимфома, связанная с инвагинацией
• Лимфатические узлы:
о Умеренно выраженная генерализованная лимфаденопатия (размер узла обычно менее 1,5 см) может быть реактивной и означать первую стадию ВИЧ-инфекции:
- Может сохраняться годами при отсутствии каких-либо симптомов (персистирующая генерализованная лимфаденопатия)
о Более выраженная лимфаденопатия (более 1,5 см) характерна для оппортунистических инфекций (авиум-микобактериальная инфекция, туберкулез) или СПИД-ассоциированной лимфомы/саркомы Капоши:
- Некроз мезентериальных лимфоузлов вследствие авиум-микобактериальной инфекции или туберкулеза
- Значительное увеличение лимфоузлов при саркоме Капоши о СПИД-ассоциированная лимфома может быть связана с дискретными очагами поражения в печени/селезенке или с фокальными объемными образованиями ЖКТ:
- ЖКТ, особенно толстая кишка, подвздошная кишка и желудок - наиболее частая экстранодальная локализация поражений при лимфоме (75%)
• Почки:
о Двухстороннее увеличение почек с утолщением уротелия может быть следствием ВИЧ-нефропатии
о Фокальные гиподенсные очаги поражения могут быть проявлением инфекции (туберкулез, авиум-микобактериоз, грибковые) или СПИД-ассоциированной лимфомы
о Кальцинаты могут обнаруживаться при пневмоцистной инфекции (сходные изменения в печени и в селезенке) или реже при МАИ/ЦМВ
• Поджелудочная железа:
о Оппортунистические инфекции могут стать причиной острого панкреатита и стриктур панкреатического протока (например, ЦМВ, Cryptococcus и др.)
(Слева) На аксиальном срезе при КТ с контрастом визуализируются множественные объемные образования в печени, в т. ч. с кровоизлияниями,, у пациента со СПИДом. Данные очаги обусловлены неходжкинской лимфомой. Не совсем типичной находкой в этом случае является легкая обструкция внутрипеченочных желчных протоков.
(Справа) При УЗИ в продольной плоскости выявлено большое гипоэхогенное объемное образование у пациента со СПИДом. При биопсии была подтверждена СПИД-ассоциированная В-клеточная неходжкинекая лимфома. (Слева) При УЗИ в продольной плоскости визуализируется правая почка обычных размеров с выраженной гиперэхогенностью у пациента с ВИЧ-нефропатией в анамнезе. В отличие от остальных хронических заболеваний, почки при ВИЧ-нефропатии часто имеют нормальные размеры или несколько увеличены.
(Справа) При УЗИ в поперечной плоскости выявлены множественные небольшие кальцинаты в селезенке у ВИЧ-инфицированного пациента. Это проявления первичной пневмоцистной инфекции.
4. УЗИ брюшной полости при ВИЧ/СПИД:
• Желчный пузырь:
о Утолщение стенки желчного пузыря может быть реактивным при гепатите или вторичным при остром акалькулезном холецистите, обусловленном оппортунистической флорой
о Утолщение стенки и расширение внепеченочных и/или внутрипеченочных желчных протоков обусловлено холангиопатией на фоне СПИД
• Печень:
о Оппортунистические инфекции проявляются небольшими гипоэхогенными узелками (микроабсцессы) с диффузным распределением в печени
о Пневмоцистная инфекция дает картину небольших гипоэхогенных узлов/мелких очагов с неизмененной эхогенностью
• Лимфатические узлы:
о Некроз лимфоузлов чаще всего возникает в результате авиум-микобактериальной инфекции или туберкулеза
в) Дифференциальная диагностика поражений брюшной полости при ВИЧ/СПИД:
1. Лимфома, не обусловленная ВИЧ/СПИД:
• Более выраженное поражение лимфоузлов, в отличие от СПИД, при котором преобладают экстранодальные поражения
• СПИД-обусловленная лимфома протекает агрессивно, имеет склонность к метастазированию, в то время как лимфома, не обусловленная СПИД, на ранних стадиях ограничивается поражением лимфоузлов
2. Билиарные гамартомы:
• Множественные мелкие кистозные поражения с диффузным распределением в печени
• Могут симулировать микроабсцессы печени, но у пациентов нет каких-либо симптомов инфекции
3. Саркоидоз:
• Может проявляться множественными мелкими гиподенсными поражениями в печени и селезенке (похожими на микроабсцессы)
• Характерна верхняя внутрибрюшная лимфаденопатия, которая ошибочно может быть принята за лимфаденопатию при ВИЧ
• Медиастинальная и воротная лимфаденопатия, характерное поражение легких и отсутствие симптоматики поможет в дифференциальной диагностике
г) Патология. Общая характеристика:
• Этиология:
о При инфицировании ВИЧ приводит к разрушению CD4(+) Т-лимфоцитов и иммунному дефициту о У ВИЧ-инфицированных пациентов повышается риск развития новообразований, особенно при одновременном инфицировании вирусом Эпштейна-Барр, герпеса или папилломавирусом:
- Частота СПИД-ассоциированных опухолей (неходжкинская лимфома, саркома Капоши) существенно снижается при ВААРТ
- Риск других опухолей, протекающих более агрессивно и появляющихся в нетипично молодом возрасте, намного выше у ВИЧ-инфицированных
- Неходжкинская лимфома:
СПИД-ассоциированное новообразование (обычно при CD4 ниже 100), объединяющее несколько типов лимфом, в т.ч. диффузную В-клеточную лимфому и лимфому Беркитта
Выраженная тенденция к экстранодальному распространению (особенно в ЖКТ), поражению нетипичных мест и появлению при прогрессировании основного заболевания
- Саркома Капоши:
Низкодифференцированная саркома мягких тканей сосудистой природы, ассоциированная с ВПГ-8
о Инфекционные осложнения чаще возникают у ВИЧ-инфицированных пациентов с CD4> 200, в то же время, риск значительно возрастает при снижении уровня CD4:
- Множество различных СПИД-детерминированных инфекций, включая распространенную авиум-микобактериальную инфекцию, туберкулез, пневмоцистную инфекцию, рецидивирующие бактериальные пневмонии, персистирующую криптоспоридиальную инфекцию, хроническую герпес-вирусную инфекцию (ВПГ):
Большая часть инфекций возникают при CD4
д) Клинические особенности:
1. Проявления поражений брюшной полости при ВИЧ/СПИД:
• Самые частые признаки/симптомы:
о Острая ВИЧ-инфекция может напоминать мононукпеоз, проявляясь лихорадкой, головными болями и болями во всем теле
о У пациентов с хронической ВИЧ-инфекцией нет клинической симптоматики на фоне эффективной ВААРТ:
- Кожные проявления и легкая общая симптоматика возможны даже без иммуносупрессии
о Пациенты с выраженным СПИДом на фоне ВИЧ и с иммуносупрессией могут иметь симптоматику, обусловленную оппортунистическими инфекционными агентами (диарея, кашель/одышка, боли в животе и др.):
- У некоторых пациентов может возникать синдром кахексии со значительной потерей веса и постоянной диареей
• Другие признаки/симптомы:
о Для пациентов с низким уровнем CD4 характерна панцитопения (анемия, тромбоцитопения, лимфопения)
о Генерализованная лимфаденопатия и спленомегалия могут быть даже при отсутствии активной инфекции
• Клинический профиль:
о Клинический профиль варьирует в зависимости от страны проживания:
- ВИЧ в развивающихся странах распространяется преимущественно при вагинальных половых контактах (другие пути-при введении наркотиков и перинатальный-распространены значительно меньше)
- ВИЧ в США передается преимущественно при внутривенном применении наркотиков и при гомосексуальных половых контактах
2. Демография:
• Возраст:
о Преимущественно взрослое население, однако возможен и перинатальный путь заражения
• Пол:
о По мировой статистике большинство случаев у гетеросексуальных пар, Ж>М
• Эпидемиология:
о Больше 35 млн инфицированных по всему миру
3. Течение и прогноз:
• Разнообразные оппортунистические инфекции и СПИД-обусловленные опухоли без ВААРТ с целью подавления ВИЧ
• СПИД определяется при CD4
4. Лечение поражений брюшной полости при ВИЧ/СПИД:
• Антиретровирусные препараты для поддержания иммунного статуса
• Антибиотики при бактериальных инфекциях и антивирусные препараты при ЦМВ-инфекции
е) Список использованной литературы:
1. Tonolini М et al: Mesenterial, omental, and peritoneal disorders in antiretroviral-treated HIV/AIDS patients: spectrum of cross-sectional imaging findings. Clin Imaging. 37(3):427-39, 2013
Читайте также:

