Неврологические нарушения при интоксикациях
Обновлено: 25.04.2024
Наша клиника специализируется в неврологии и иммунологии. У нас работают неврологи с дополнительной подготовкой по иммунологии. Мы используем комплексный подход к лечению заболеваний нервной системы, в том числе занимаемся диагностикой и лечением демиелинизирующих заболеваний.
Инфекция. Инфекционное и постинфекционное поражение нервной системы
Инфекционное поражение нервной системы – это воспаление различных ее отделов:
- Оболочек головного и/или спинного мозга (менингит, арахноидит);
- Вещества головного мозга (энцефалит) или спинного мозга (миелит);
- Периферических нервов (неврит, полиневрит);
- Нервных корешков спинного мозга (радикулит);
- Нервных сплетений (плексит);
- Нервных узлов (ганглионит).
Как инфекция повреждает нервную систему? Возможны два варианта:
В норме с большинством потенциально опасных инфекций каждый из нас встречается периодически или постоянно. При этом заболевание не наступает, пока иммунная система в состоянии защитить организм. Опасность поджидает при снижении иммунной защиты. Микробы, не встречая должного сопротивления, внедряются в организм и часто сами еще больше блокируют работу иммунной системы (вторичное иммунодефицитное состояние).
Лечение только инфекции, без коррекции иммунного ответа, почти всегда неэффективно из-за повторного заражения. Поэтому, планируя лечение, мы подробно исследуем Ваш иммунный статус и антитела к ряду инфекций. Когда картина иммунитета и инфекционного фона ясна, составляется план лечения, охватывающий две задачи:
- Подавить инфекцию;
- Отрегулировать работу иммунной системы.
Онкология и поражение нервной системы
Многие злокачественные опухоли способствуют образованию в организме большого количества токсинов и иммунных факторов, агрессивных к собственным тканям организма, в т.ч. к головному и спинному мозгу, к периферическим нервам, мышцам. Паранеопластическое заболевание нервной системы – это повреждение нервной системы не опухолью, а иммунной системой под влиянием опухоли. У нас есть специалисты и современные лабораторные тесты для диагностики паранеопластических заболеваний нервной системы и опыт их лечения.
Интоксикация и аутоиммунная агрессия могут стать причиной паранеопластических синдромов и повреждения:
- мышц,
- периферических нервов,
- головного и спинного мозга.
Симптомы паранеопластических процессов могут быть самыми разнообразными:
Какие ткани нервной системы могут пострадать при паранеопластических синдромах?
- Периферические нервы – полинейропатия и полиневрит.
- Мышцы – миопатия и полимиозит.
- Головной мозг – энцефалопатия, энцефалит.
- Спинной мозг – миелопатия.
Аутоиммунная агрессия. Аутоиммунный процесс
Некоторые заболевания нервной системы связаны с агрессией организма против самого себя, а именно, с атакой иммунной системы на ткани собственной же нервной системы (демиелинизация). Некоторые аутоиммунные заболевания провоцируются инфекцией. Прежде чем составить план лечения, мы подробно исследуем Ваш иммунный статус и инфекционный фон.
Наша основная задача – найти причину аутоиммунной агрессии и предотвратить ее дальнейшее развитие. Во многих случаях реально ввести аутоиммунный процесс в длительную ремиссию или остановить его совсем.
Примеры аутоиммунных болезней нервной системы:
Аналогичные явления наблюдаются при ревматических болезнях, когда иммунная агрессия направлена против суставов, связок, мышц, кровеносных сосудов.
Причины аутоиммунных процессов
Почему появляются аутоиммунные болезни? Обычно этому способствует неудачное совпадение трех основных факторов:
Известен “феномен декомпактизации миелина”, когда в результате инфекционного или аутоиммунного повреждения обнажаются глубоко залегающие антигены миелина, с которыми иммунная система в норме вообще не контактирует. Эти антигены воспринимаются иммунной системой как чужеродные, к ним образуются аутореактивные иммунокомпетентные клетки и антитела (аутоантитела), запускающие дальнейшую иммунную агрессию.

Молекулярная мимикрия и аутоиммунная реакция. Антигены некоторых микробов похожи на аутоантигены здоровых клеток организма. 1-Клетка иммунитета; 2-Инфекционный агент; 3-Нерв; 4-Одинаковые рецепторы.
Образовавшиеся агрессивные аутоантитела могут участвовать в перекрестной аутоиммунной агрессии и к другим тканям организма. Поэтому пациентов с демиелинизирущими заболеваниями мы часто обнаруживаем и другие аутоиммунные процессы:
-
(воспаление щитовидной железы); ; ;
- Антитела к инсулину и бета-клеткам поджелудочной железы (риск сахарного диабета и ожирения).
Лечение аутоиммунных заболеваний
Лечение любого аутоиммунного заболевания предполагает снижение аутоиммунной агрессии.
Наиболее убедительные результаты лечения мы получаем от воздействия сразу на три звена аутоиммунного процесса:
Стресс. Психический стресс. Снятие психического стресса
Природа стресса. Стресс – это сверхсильный ответ организма на опасные обстоятельства. Стрессовый ответ на опасность обеспечивают эволюционно древние нижние отделы мозга, доставшиеся нам еще от рыбы (вегетативная нервная система).
Стресс у человека, как и у любого животного, приводит к повышению физических возможностей тела (быстро бегать, драться и др.), за счет ранее накопленных ресурсов. Все это происходит независимо от сознания.
Например, на Вас кто-то накричал. В ответ Ваше сердце забилось, накачивая кровь в мышцы, мышцы напряглись, зрачок расширился для улучшения зрения, дыхание активизировалось, насыщая мышцы кислородом, хотя физическая опасность Вам не угрожает и силовой ответ не требуется.

Стрессорная реакция в процессе эволюции изменилась не сильно – при стрессе организм готовится к отражению физической угрозы, даже, если физически никто не угрожает.
У социального человека подобные реакции обычно не реализуются в поведении, а значит, длительно сохраняются в виде нереализованной поведенческой реакции. А если Вы эмоциональны, но очень хорошо контролируете свое поведение? Это означает, что нервная система будет длительно держать тело в переактивированном состоянии, расходуя при этом огромное количество ресурсов.
При этом происходит постепенное истощение нервной системы и разлад обмена веществ.
Стресс и иммунитет. В хроническом стрессе иммунитет становится более агрессивным, но быстро истощается, теряя целенаправленность иммунного ответа.
В ответ на внедрение инфекции возможен очень сильный, но недостаточно целенаправленный ответ, с иммунной атакой против собственных тканей организма:
Поэтому в лечении аутоиммунных заболеваний нервной системы:
Уменьшение стрессового напряжения в нервной системе приводит к значительным изменениям в лабораторных показателях иммунного статуса и в самочувствии.
Нарушение обмена веществ
Самые разные обменные нарушения в организме могут стать причиной страдания нервной системы т.к. она очень требовательна к обеспечению питанием и очень чувствительна к токсическому воздействию продуктов нарушенного обмена веществ. В нашей клинике неврологи работают в тесном сотрудничестве с эндокринологом, при необходимости мы предложим Вам совместную консультацию.
Чаще всего мы обнаруживаем два варианта обменного поражения нервной системы:
-
– это страдание волокон периферических нервов (нервов конечностей, зрительных и слуховых нервов);
- Энцефалопатия – это страдание вещества головного мозга.
Возможно сочетание полинейропатии и энцефалопатии.
Лечение в нашей клинике включает в себя:
- коррекцию нарушений обмена веществ,
- восстановительное лечение для нервной системы (детоксикация, ноотропы, витамины, магнитная стимуляция, гимнастика и др.).

Лечение нарушения обмена веществ в клинике “Эхинацея”
Некоторые заболевания, при которых происходят нарушения обмена веществ, пагубное для нервной системы:
-
– одна из частых причин полинейпропатии. Подробнее здесь
- Гипоталамический синдром часто сопровождается инсулинорезистентностью, т.е. невосприимчивостью клеток к действию гормона инсулина. Нервная система при этом не в состоянии усвоить достаточное количество глюкозы. Это возможная причина развития полинейропатии и энцефалопатии. Подробнее здесь.
- Гипотиреоз, Тиреотоксикоз и Тиреоидит – это заболевания щитовидной железы и частая причина страдания нервной системы. Подробнее здесь.
- Нарушение функции паращитовидных желез приводит к нарушению кальциево-фосфорного обмена и отложению кальция в подкорковых ядрах головного мозга. Это возможная причина мышечных судорог, гиперкинезов и вторичного паркинсонизма. Подробнее здесь.
- Печеночная и почечная недостаточность – возможные причины страдания головного мозга и периферических нервов. Характерно повышенное содержание мочевины, креатинина, АЛТ, АСТ. ГГТ в биохимическом анализе крови.
- Дефицит витаминов, особенно витаминов группы В может быть причиной полинейропатии. Типичный случай – дефицит витаминов группы В при регулярном употреблении алкоголя.
- Болезни накопления приводят к отложению в тканях нервной системы каких-либо веществ (медь, марганец, кальций и др.), и гибели ее клеток.
Дисциркуляторная энцефалопатия, нарушение кровообращения
Нервная система человека расходует огромное количество энергии, и поэтому очень зависима от обеспечения питанием. Доставка кислорода, глюкозы и других необходимых веществ обеспечивается артериальной кровью. С венозной кровью эвакуируются подлежащие утилизации продукты обмена веществ. При дефиците кровоснабжения мозговое вещество или постепенно атрофируется (энцефалопатия) или гибнет в течение нескольких часов (инсульт).
Нарушение мозгового кровообращения может быть связано с сужением и закупоркой кровеносных сосудов по различным причинам:
- Васкулит (воспаление кровеносных сосудов из-за иммунной атаки или инфекции). Это довольно опасное заболевание приводит обычно к постепенной мелкоочаговой гибели вещества головного мозга. При МР-томографии васкулит часто путают с различного рода энцефалопатиями, рассеянным склерозом. Подробнее здесь
- Атеросклероз – это отложение жира (холестерина) между слоями внутренних стенок кровеносных сосудов. Отложение происходит в виде бляшек. Бляшки выбухают внутрь артерий и препятствуют току крови, вызывая хронический дефицит кровообращения, с постепенной атрофией мозгового вещества. Наибольшую опасность представляют разорвавшиеся бляшки, жировые массы из которых попадают в кровь и закупоривают меньшие по диаметру артерии (инсульт, острое нарушение мозгового кровообращения, инфаркт мозга).
- Повышение свертываемости и вязкости крови препятствует похождению крови по самым мелким кровеносным сосудам (капиллярам) и вызывает хронический дефицит кровоснабжения мозга. Кроме того, возможно внутрисосудистое свертывание крови с закупоркой сосуда (инсульт, острое нарушение мозгового кровообращения, инфаркт мозга).
- Сдавление или извитость кровеносного сосуда. Обычно страдают артерии, проходящие через шейные позвонки (позвоночные артерии), что является причиной головокружения, потери равновесия, зрительных и слуховых расстройств.
Лечение нарушения мозгового кровообращения в нашей клинике начинается с точного обнаружения его причины. Так мы подбираем метод лечения, реально эффективный именно в данном случае. Для диагностики мы используем:
-
на жиры, маркеры васкулита и свертываемость;
- УЗДГ и/или МР-ангиографию для уточнения места сужения кровеносного сосуда;
- Рентгенографию, КТ или МР-томографию для поиска опасных для сосудов деформаций шейных позвонков.
Интоксикация организма. Снятие интоксикации. Как снять интоксикацию?
Интоксикация – это болезненное состояние, связанное с отравлением каким-либо вредным веществом (токсином), пагубно влияющее на состояние нервной системы, печени и т.д. Интоксикация может быть связана с попаданием токсина из внешней среды (употребление внутрь, вдыхание паров и др.) или образование его внутри организма при различных заболеваниях. Многие токсины приводят к гибели: периферических нервов (токсическая полинейропатия); вещества головного мозга (токсическая энцефалопатия); спинного мозга (токсическая миелопатия). Лечение токсических поражений (интоксикации) нервной системы в нашей клинике предполагает детоксикацию и лечение, направленное на восстановление работоспособности нервной системы. Часто используемые для детоксикации препараты:
-
, , , (при интоксикации алкоголем, свинцом, марганцем и т.д. бывает показано введение витаминов через капельницу),
- восстановительное лечение после интоксикации.

Детоксикация – выведение из организма вещества, вызвавшего токсическую энцефалопатию и введение лекарственных препаратов
Интоксикация различными веществами может приводить к различным симптомам со стороны центральной нервной системы:
- Алкоголь при регулярном употреблении приводит к страданию периферических нервов рук и ног (алкогольная полинейропатия) и головного мозга (алкогольная энцефалопатия). Подробнее про интоксикацию алкоголем.
- Свинец вызывает психическое возбуждение, нарушение памяти и интеллекта, боли в мышцах и суставах, повреждение нервных клеток спинного мозга с параличами и другие нарушения. Отравление характерно при контакте с некоторыми сортами бензина, парами, содержащими свинец (испарения аккумуляторов и расплавов свинца). развивается обычно после употребления эфедрона – кустарно изготовленного наркотического препарата, содержащего большое количество марганца. Характерен паркинсонизм, с нарушением координации движений, тремором конечностей, затруднениями при изменении положения тела, вплоть до полного обездвиживания.
- Длительное воздействие металлической ртути приводит к характерному сочетанию мозжечковых симптомов со ртутным эретизмом (раздражительность, снижение памяти, бессонница, патологическая пугливость и конфузливость). Иногда развивается психоз с психическим возбуждением (делирий). Он был впервые описан у рабочих, занятых на производстве фетровых шляп, и даже получил название “болезнь сумасшедшего шляпника”. У лиц с некоторыми особенностями иммунитета низкие дозы ртути из зубных пломб могут вызывать патологические иммунные реакции, но данных на этот счет пока недостаточно.
- Интоксикация приболезнях почек и печени связана с повышенным образованием и/или недостаточным выведением продуктов обмена веществ. Накопившиеся вредные продукты обмена могут причиной повреждения периферических нервов и головного мозга.
- Интоксикация при инфекционных болезнях обусловлена образованием токсинов в результате деятельности болезнетворных микробов и разрушения клеток организма.
Демиелинизация. Очаги демиелинизации
Миелин – это оболочка нервных волокон. Демиелинизация – это разрушение оболочек нервов, а затем и самих нервных волокон. Демиелинизация головного мозга, спинного мозга и периферических нервов может происходить по множеству причин. Наиболее опасна демиелинизация из-за агрессии иммунной системы в отношении белков миелина. Лечение демиелинизирующих заболеваний в нашей клинике (ДМЗ) предполагает поиск и лечение причин демиелинизации, стимуляцию процессов ремиелинизации.
Возможные причины демиелинизации:
-
на белки, входящие в состав миелина. Это происходит по ошибке иммунной системы, под влиянием инфекции, врожденных особенностей иммунитета. Иммунная система воспринимает белки миелина как чужеродные и разрушает их. Это характерно для рассеянного склероза, рассеянного энцефаломиелита, хронической воспалительной демиелинизирующей полинейропатии (ХВДП),синдрома Гийена-Барре, ревматических болезней, хронических инфекций. может приводить к нарушению питания и гибели миелина. Это характерно для сахарного диабета, болезней щитовидной железы. . Миелин может быть мишенью атаки некоторых инфекций, в первую очередь, вирусных.
- Паранеопластические процессы – осложнения онкологических заболеваний.
- Интоксикация химическими веществами или агрессивными продуктами жизнедеятельности самого организма (свободные радикалы, перекиси).
Ремиелинизация – это процесс восстановления миелиновых оболочек. Процесс ремиелинизации можно стимулировать разными путями – подробнее на этой странице
Токсическая энцефалопатия – это сочетание неврологических расстройств, обусловленных воздействием токсинов, ядов или производственных химикатов. Клинические проявления многообразны, зависят от этиологического фактора, могут включать в себя атактический и судорожный синдром, галлюцинации, расстройства речи, зрения, слуха и когнитивной сферы, поражения черепно-мозговых нервов, специфические кожные проявления. При диагностике используются данные анамнеза, результаты общего осмотра, лабораторных и инструментальных тестов. Лечение включает антидотную, дезинтоксикационную, патогенетическую и симптоматическую терапию.
МКБ-10
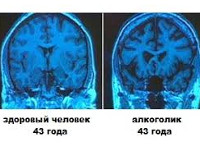
Общие сведения

Причины
Все токсические энцефалопатии возникают на фоне отравления организма токсичным для центральной нервной системы веществом. Причиной может быть как однократный контакт или прием (острые ТЭ), так и продолжительное насыщение токсином (хронические ТЭ). К наиболее распространенным причинам этой группы патологий относятся:
- Злоупотребление алкоголем, наркотики. Включает хроническое употребление больших доз алкоголя с последующим дефицитом витамина В1. Также токсическое влияние на ЦНС оказывают наркотические вещества – героин, кокаин, амфетамин и др.
- Работа на вредных производствах. Причиной энцефалопатии может стать продолжительный контакт с такими веществами как метанол, этиленгликоль, свинец, марганец, ртуть, фосфорорганические соединения, угарный газ при работе на заводе или в шахте. Возможно одномоментное получение большой дозы химиката при техногенных катастрофах, ошибочном употреблении в пищу.
- Бесконтрольный прием медикаментов. Чрезмерно высокие дозы или сочетание большого количества фармакотерапевтических средств могут оказывать пагубное воздействие на центральную нервную систему. Развитие ТЭ способны вызывать бензодиазепиновые производные, барбитураты, антидепрессанты, холинолитики и нестероидные противовоспалительные препараты (в первую очередь – салицилаты).
- Патологии печени и почек. Печень и почки – органы, отвечающие за утилизацию токсичных продуктов метаболизма. При выраженной почечной или печеночной недостаточности усиливается негативное воздействие экзогенных ядов, накапливаются естественные метаболиты, токсичные для ЦНС – аммиак, органические кислоты.
Патогенез
Механизмы развития различных форм токсических энцефалопатий досконально не изучены. Также не установлена четкая взаимосвязь между клиническими проявлениями и морфологическими изменениями в нервной системе. Принято считать, что в основе ТЭ лежит как прямое воздействие токсичного вещества, так и нарушение кровоснабжения головного мозга вследствие повреждения церебральных сосудов. Это, в свою очередь, приводит к дегенеративно-дистрофическим изменениям в тканях и отеку мозговых оболочек.
Возникают гемодинамические и ликвородинамические нарушения, что еще больше усугубляет токсическое и гипоксическое воздействие на ЦНС. В результате формируются диссеминированные участки некроза коры и подкорковых структур, фрагментации миелиновых оболочек. С учетом конкретного вещества могут выявляться определенные особенности, связанные с повышенной восприимчивостью некоторых структур нервной системы и способностью соединений накаливаться в различных органах.
Тетраэтилсвинец и ртуть могут депонироваться в паренхиматозных органах и нервной системе. При сатурнизме наблюдается повреждение нейронов в ЦНС, сегментарная демиелинизация с последующим аксональным поражением периферических нервов. Ртуть оказывает токсическое действие на нейроны коры затылочных долей и гранулярные клетки мозжечка, патология сопровождается аксональной дегенерацией и демиелинизацией периферических нервов. Угарный газ вызывает острую гипоксию головного мозга, взаимодействуя с гемоглобином и создавая стойкое соединение – карбоксигемоглобин.
ФОС вызывают нарушение функции ацетилхолинэстеразы, фермента одного из основных медиаторов ЦНС – ацетилхолина, что ведет к перевозбуждению М- и N-холинорецепторов. Сероводород оказывает негативное влияние путем связывания активных аминокислот, блокирования медьсодержащих энзимов, нарушения метаболизма серотонина, триптофана, никотиновой кислоты и витамина В6. При отравлении салицилатами и этиленгликолем ведущую роль играет формирующийся метаболический ацидоз.
Симптомы токсической энцефалопатии
Клинические проявления напрямую зависят от токсина, вызвавшего заболевание. При передозировке салицилатов вначале возникает общее недомогание, тошнота с рвотой, звон или шум в ушах, нарушение речи, звуковые и зрительные галлюцинации. Иногда наблюдается судорожный синдром, когнитивные расстройства, коматозное состояние. Отравление угарным газом сопровождается общемозговыми симптомами, нарушением памяти, галлюцинациями, атаксией, гипертонусом скелетных мышц, хореическими гиперкинезами и угнетением сознания.
Свинцовая ТЭ характеризуется сильной разлитой головной болью, общей слабостью, недомоганием, ухудшением памяти, статическим тремором, выраженным ухудшением зрения, центральными парезами и параличами. В некоторых случаях определяется поражение двигательных и смешанных черепных нервов, эпилептические приступы. Типичное проявление – лилово-серая кайма, возникающая вдоль зубного ряда (симптом Брутона). При отравлении этиленгликолем отмечается горизонтальный нистагм и общее состояние, имитирующее алкогольную интоксикацию. При тяжелом отравлении возникает судорожный синдром, сопорозное состояние или кома.
Острая алкогольная энцефалопатия характеризуется ярко выраженными общемозговыми симптомами, офтальмоплегией, страбизмом, нистагмом, выпадением сухожильных и периостальных рефлексов, гиперкинезами, мозжечковым нарушением координации движений, вегетососудистой дисфункцией и психическими расстройствами. При хронической форме алкогольной ТЭ возникают вегетативные и нейроэндокринные нарушения, бессонница или тревожные сны, тремор, деменция.
Диагностика
В процессе диагностики врач-невролог руководствуется анамнестическими сведениями, жалобами больного, результатами физикального, лабораторного и инструментального методов исследований. С учетом формы токсической энцефалопатии решающую роль в постановке заключительного диагноза могут играть различные диагностические методики. Общая программа обследования пациента с подозрением на ТЭ состоит из следующих пунктов:
- Сбор жалоб и анамнеза. Зачастую позволяет выявить токсическое вещество, спровоцировавшее нарушение состояния пациента. На вероятную этиологию могут указывать установленные в ходе беседы поражения других органов и систем. Акцентируется внимание на характере речи – наличии дизартрий, бессвязности сказанного.
- Внешний осмотр. При физикальном обследовании оценивается пульс, уровень артериального давления, состояние кожных покровов и видимых слизистых оболочек, объем активных и пассивных движений с целью поиска парезов, параличей и самопроизвольных мышечных подергиваний, тонус надкостных и сухожильных рефлексов. Исследуются функции черепных нервов, острота зрения и слуха на предмет быстро развивающейся слепоты и глухоты, нистагма и других симптомов.
- Общеклинические лабораторные тесты. В ОАК может определяться анемический синдром, лейкопения, нейтрофильный лейкоцитоз, панцитопения, базофильная зернистость эритроцитов и повышение СОЭ. В ОАМ могут выявляться свежие эритроциты, оксалаты, гиалиновые цилиндры, протеинурия, гематопорфирин и остатки тяжелых металлов. В биохимическом анализе крови отмечаются изменения водно-электролитного и кислотно-основного баланса, признаки нарушения порфиринового обмена.
- Электроэнцефалография.ЭЭГ применяется при наличии судорожного синдрома, глубокого нарушения сознания. На электроэнцефалограмме могут присутствовать медленные волны высокой амплитуды, угнетение α-ритма, общее подавление биоэлектрической активности или проявления судорожных очагов.
- Дополнительные методы диагностики. С учетом клинической ситуации и необходимости дифференциальной диагностики с другими патологиями дополнительно назначается электромиография, спинномозговая пункция, компьютерная или магнитно-резонансная томография головного мозга, токсикологические исследование волос и ногтей.
Лечение токсической энцефалопатии
Целью лечения патологии является выведение из организма химического вещества, минимизация поражений головного мозга, коррекция неврологического дефицита. В зависимости от тяжести общего состояния пациента терапия проводится в отделении клинической неврологии или блока реанимации и интенсивной терапии, включает в себя следующие мероприятия:
- Эвакуация токсина из организма. При острых интоксикациях, спровоцированных попаданием химиката внутрь через ЖКТ, производится промывание желудка дистиллированной водой или специфическими реагентами, после чего применяются энтеросорбенты.
- Дезинтоксикационная терапия. Направлена на связывание или выведение токсина, циркулирующего в крови. Представлена внутривенной инфузией плазмозаменителей и специфических антидотов, хелатной терапией, гемодиализом.
- Симптоматическая и патогенетическая терапия. Может состоять из масочной ингаляции кислорода, искусственной вентиляции легких, назначения противоэпилептических и мочегонных препаратов, транквилизаторов, нестероидных противовоспалительных средств, кортикостероидов.
Прогноз и профилактика
Исход токсической энцефалопатии зависит от степени поражения ЦНС и свойств вещества. Выраженные интоксикации тяжелыми металлами, ФОС и этиленгликолем зачастую приводят к летальному исходу. Клинические проявления при отравлениях органическими растворителями могут самостоятельно регрессировать спустя несколько дней либо недель после прекращения контакта. Профилактика ТЭ основывается на соблюдении правил техники безопасности, использовании средств индивидуальной защиты при работе с токсическими веществами в быту и в условиях вредных производств, четком соблюдении рекомендаций врача при проведении медикаментозной терапии, отказе от вредных привычек.
3. Неврологические симптомы, синдромы и болезни. Энциклопедический справочник / Гусев Е.И., Никифоров А.С., Камчатнов П.Р. – 1999.
Нейротоксикоз у детей – это патологическое состояние, которое возникает у ребенка раннего возраста при генерализации вирусных и/или бактериальных заболеваний и преимущественно проявляется нарушениями функций ЦНС. Клинически данное состояние характеризуется нарушением сознания ребенка, повышением температуры, гипертонусом мышц, увеличением ЧСС и ЧД. Диагностика нейротоксикоза у детей подразумевает сопоставление клинической картины, клинических анализов и результатов исследования ликвора. Лечение включает в себя этиотропные препараты, дезинтоксикацию и симптоматическую терапию, зависящую от клиники.
Общие сведения

Причины нейротоксикоза у детей
Нейротоксикоз у детей – это полиэтиологическое явление. Он может возникать на фоне большого количества заболеваний вирусного (ОРВИ, аденовирусная инфекция и т. д.) и бактериального (шигеллез, сальмонеллез, пищевая токсикоинфекция и др.) генеза или их сочетания. Также нейротоксикоз является первым симптом нейроинфекций (менингиты и энцефалиты).
Нейротоксикоз чаще всего развивается у детей раннего возраста благодаря их анатомо-физиологическим особенностям. Для ребенка характерен высокий уровень обмена веществ, который значительно выше такового у взрослых. Строение ЦНС и ее функционирование также отличается. У детей есть склонность к массивным воспалительным реакциям тканей головного мозга. Ткани гипоталамуса более чувствительные к гипоксии и поражаются быстрее, чем у взрослых. В возрасте до 3 лет ГЭБ функционально незрелый, из-за чего он пропускает токсины через себя. Это проявляется повышением внутричерепного давления и отеком головного мозга.
Патогенетически нейротоксикоз у детей обусловлен нарушением микроциркуляторного русла центральной и автономной нервной системы. Экзотоксины, которые выделяют бактерии в процессе жизнедеятельности, и эндотоксины, что попадают в кровь после их гибели, повреждают сосудистую стенку, повышают ее проницаемость для патогенных агентов и провоцируют гипоксию тканей. Вирусы вызывают аналогичный эффект, но другими путями. Они разрушают клетки организма, в результате чего в кровь попадают агрессивные протеолитические ферменты. Также вирусы способны самостоятельно вызывать деструкцию клеток эндотелия сосуда. Благодаря АФО ребенка такие изменения происходят диффузно по всей ЦНС. В развитии нейротоксикоза ведущую роль играет нарушение работы гипоталамуса, т. к. он является высшим вегетативным центром человека и отвечает за терморегуляцию, контролирует работу всех систем и эндокринных желез.
Классификация нейротоксикоза у детей
Различают 3 степени тяжести нейротоксикоза у детей:
Также нейротоксикоз у детей классифицируется согласно вариантам его протекания и ведущим симптомам:
Симптомы нейротоксикоза у детей
Нейротоксикоз у детей возникает остро, клинические проявления развиваются быстро. Токсическая энцефалопатия протекает в 3 периода: продромальный, развернутой клинической симптоматики и восстановления. Для каждого из них характерны свои симптомы.
Продромальный период кратковременный – от 2 до 6 часов. Проявляется ранними симптомами нарушения ЦНС: тошнота, рвота, которая не приносит облегчения и не зависит от приема пищи; нарастание головной боли; чрезмерное беспокойство и капризность; беспокойство, вздрагивания во время сна; сонливость днем; постепенное нарастание температуры тела до 38,5-39°С. Без медицинского вмешательства развивается нарушение сознания (от ступора до комы), дыхательной (повышение ЧД, одышка) и сердечно-сосудистой (повышение ЧСС) систем.
Развернутый нейротоксикоз у детей может иметь различные проявления, которые зависят от степени поражения ЦНС и микроциркуляторного русла. Длительность варьирует от 12 до 72 часов. При интенсивном нарушении кровообращения нейротоксикоз у детей развивается молниеносно. За несколько часов возникает декомпенсация работы сердечно-сосудистой системы, появляются геморрагии, развивается дыхательная недостаточность и отек легких. Нарушения ЦНС выражены в меньшей степени.
При непосредственном поражении ЦНС течение нейротоксикоза у детей более медленное. Нарастает интенсивность симптомов продромального периода, возникают судороги. Сознание ребенка нарушается постепенно – от сонливости до комы, продолжительность которой может составлять до 2 суток. Могут развиваться гипервентиляционный и гипертермический синдромы. Гипервентиляция проявляется увеличением ЧД до 80/мин. без структурных изменений легких или дыхательных путей. Гипертермия при нейротоксикозе достигает 40° С и не снимается обычными жаропонижающими средствами. Без экстренного медицинского вмешательства может возникнуть остановка сердца и дыхания, которые переходят в клиническую и биологическую смерть.
Период восстановления начинается после купирования острого состояния. Восстановление напрямую зависит от тяжести нейротоксикоза, адекватности и своевременности лечения. При легкой степени симптомы нарушения ЦНС исчезают за 12-24 часа. При тяжелых случаях неврологическая симптоматика может сохраняться на протяжении 2-4 суток.
Диагностика нейротоксикоза у детей
При подозрении на нейротоксикоз проводится дифференциальная диагностика с нейроинфекциями, которые сопровождаются синкопе и судорожным синдромом. Для этого выполняется спинномозговая пункция с исследованием ликвора.
Лечение нейротоксикоза у детей
Терапия нейротоксикоза у детей проводится исключительно в условиях реанимационного отделения. Если ребенок на момент развития патологии находится дома – его немедленно госпитализируют. На догоспитальном этапе проводится лечение жизнеугрожающих проявлений: судорожного синдрома и гипертермии.
Этиотропное лечение включает назначение антибиотиков широкого спектра действия, после получения результатов антибиотикограммы – противомикробных препаратов, к которым чувствительна высеянная микрофлора. Допускается использование иммуностимуляторов. При проведении дезинтоксикационной терапии используются 0,9% раствор NaCl, 5% глюкоза, раствор Рингера-лактат. Важно соблюдать небольшой объем и низкую скорость введения растворов, т. к. инфузионная терапия может спровоцировать отек головного мозга.
Прогноз
Прогноз при нейротокискозе зависит от степени тяжести и своевременности лечения. I и II степени при адекватном лечении имеют благоприятный прогноз. При тяжелой (III) степени прогноз для жизни при полноценной терапии благоприятный, для здоровья – сомнительный. При несвоевременном оказании квалифицированной помощи при I-II степени прогноз сомнительный, III степени – неблагоприятный. Без соответствующего лечения – неблагоприятный прогноз нейротоксикоза любой степени тяжести.
Профилактика
Профилактика нейротоксикоза у детей заключается в полноценном лечении основного заболевания по рекомендациям педиатра, соблюдении рациональной диеты и укреплении иммунитета. Лечение инфекционных заболеваний у детей с наличием неврологических нарушений в анамнезе должно проводиться под строгим наблюдением в условиях стационара.
Нейроковид – это неофициальное название поражений центральной и периферической нервной системы при COVID-19. Состояние вызвано как прямым повреждающим действием коронавируса, так и опосредованными системными нарушениями работы организма. Патология имеет полиморфные проявления: астенический синдром, психоэмоциональные нарушения, когнитивный дефицит. Тяжелые формы нейроковида характеризуются расстройствами церебрального кровообращения. Диагностика требует проведения нейровизуализации (КТ, МРТ), ЭЭГ, УЗДГ сосудов головы и шеи. Для лечения неврологических последствий COVID-19 используют методы фармакотерапии, физиотерапии, психотерапии, коррекцию образа жизни.
МКБ-10



Общие сведения
По данным зарубежных исследований, с неврологическими последствиями новой коронавирусной инфекции сталкиваются 49% пациентов в США, 50% в Великобритании, 35-45% в Германии. В среднем более трети больных, перенесших COVID-19, предъявляют жалобы, типичные для поражения головного мозга и периферических нервов. Ситуация осложняется тем, что симптоматика накладывается на другие проявления острого периода коронавируса и постковидного синдрома. Неврологические аспекты коронавирусной пандемии требуют дальнейшего изучения и подбора оптимальных схем медицинской помощи, включая длительную реабилитацию.

Причины нейроковида
Поражение нервной системы возникает при любой клинической форме COVID-19, в том числе при бессимптомном или малосимптомном течении. Поскольку повреждение ЦНС и периферических нервных структур не всегда имеет непосредственную связь с коронавирусной болезнью, требуются дальнейшие масштабные исследования и метаанализы. При этом установление точных причинно-следственных связей затруднительно, особенно у пациентов с сопутствующими заболеваниями.
Предрасполагающие факторы
Важный фактор риска позднего нейроковида – длительное и массивное медикаментозное лечение. Применение высоких доз системных кортикостероидов, моноклональных антител и сосудистых препаратов негативно влияет на церебральный кровоток. Ситуация ухудшается при полипрагмазии и у пациентов с коморбидными состояниями, требующими поддерживающей терапии. Прослеживается тенденция к увеличению частоты и тяжести нейроковида среди пожилых больных.
Патогенез
Последние исследования показывают, что SARS-CoV-2 способен преодолевать гематоэнцефалический барьер (ГЭБ). Это реализуется по трем основным механизмам. Во-первых, вирус взаимодействует с рецепторами ангиотензинпревращающего фермента, которые активно экспрессируются на эндотелии церебральных сосудов. Во-вторых, вирусный протеин S напрямую повреждает ГЭБ. В-третьих, возбудитель активизирует сосудистую воспалительную реакцию и нарушает микроциркуляцию.
Инфекция SARS-CoV-2 вызывает прямое повреждение нервных клеток. Вирусный геном встраивается в митохондриальный матрикс нейронов, после чего активизируется репликация возбудителя. В инфицированных клетках развивается окислительный стресс, активизируется приток ионов кальция и нарастает дисфункция митохондрий. Такие изменения результируют некрозом или апоптозом нейронов в разных участках головного мозга.

Симптомы нейроковида
Головная боль – самое распространенное неврологическое проявление коронавирусной инфекции, которое возникает у большинства больных в остром периоде и беспокоит более 13% пациентов во время постковида. Симптом зачастую сопровождается головокружением, мышечными болями, повышенной утомляемостью. Аносмия и дисгевзия возникают у 85-88% людей в начальном периоде болезни, в 10% случаев сохраняются более 6 месяцев после перенесенного COVID-19.
Серьезную проблему представляет астенический синдром при нейроковиде, который проявляется снижением работоспособности, быстрой утомляемостью после незначительных нагрузок, отсутствием бодрости даже после длительного отдыха. Ситуация усугубляется когнитивными нарушениями: ухудшением краткосрочной и долгосрочной памяти, снижением концентрации внимания, расстройствами мышления.
Неврологические осложнения коронавирусной инфекции включают нарушения работы вегетативной нервной системы, контролирующей деятельность внутренних органов. Характерны колебания артериального давления и пульса, особенно при вертикализации и физических нагрузках. Возникают ортостатические и рефлекторные обмороки, несистемное головокружение. Развивается постуральная гипоксемия, которая проявляется одышкой при вставании с постели.
Осложнения
У пожилых людей и пациентов с другими факторами риска возможно развитие цереброваскулярных последствий: ишемического инсульта, тромбоза венозного синуса, кровоизлияния в ткани головного мозга. Риск развития инсульта в остром периоде коронавирусной инфекции варьирует от 2,8% до 8,7%. Смертность при ОНМК в группе пациентов с COVID-19 в 5-6 раз выше, чем в среднем в популяции.
В периоде нейроковида возможен дебют аутоиммунных полирадикулоневропатий (синдромов Гийена-Барре и Миллера-Фишера), лейкоэнцефалопатии, рассеянного склероза. К тяжелым осложнениям относят менингоэнцефалит, острую некротизирующую энцефалопатию. Около 50% людей с гипертермией и снижением сатурации имеют признаки энцефалопатии: атаксию, спутанность сознания, психические симптомы.
Диагностика
Обследование больных с острыми проявлениями нейроковида требует участия невролога, инфекциониста, врачей-реаниматологов. При хронических последствиях COVID-19 пациенты проходят диагностику и терапию в неврологическом отделении. Важную роль играет сбор жалоб, выяснение инфекционного и эпидемиологического анамнеза, статуса вакцинации против коронавирусной инфекции. Полная диагностическая программа включает следующие методы:
- Осмотр у невролога. Оценка неврологического статуса – базовый метод исследования при нейроковиде. При физикальном исследовании определяют уровень сознания, сохранность поверхностной и глубокой чувствительности, состояние моторных и высших психических функций. По показаниям диагностику дополняют консультацией психиатра.
- МРТ головного мозга. На снимках обнаруживаются мультифокальные очаги поражения в белом веществе, признаки точечных кровоизлияний. При острых нарушениях мозгового кровообращения в 80-90% случаев видны участки гиперинтенсивности, которые появляются в первые часы и позволяют быстро провести дифференциальную диагностику.
- Ультразвуковая допплерография. Исследование быстро выявляет нарушения кровотока в экстра- и интракраниальных сосудах, указывает на локализацию и протяженность патологических изменений. УЗДГ также показывает параметры венозного оттока, состояние коллатерального кровообращения, наличие артериовенозных мальформаций.
- ЭЭГ. Исследование электрической активности головного мозга проводится при когнитивных нарушениях, судорожных пароксизмах, инсомнии. По форме и соотношению разных типов волн удается судить о функциональном состоянии нервных структур, определить локализацию и степень патологических изменений.
- Лабораторная диагностика. Анализы клеточного и биохимического состава крови необходимы для оценки общего состояния здоровья. Дополнительно проводится исследование острофазовых показателей, аутоиммунных маркеров. При сохраняющейся одышке требуется анализ газов крови.
Основная задача дифференциальной диагностики – разграничить проявления нейроковида и неврологические проблемы, возникающие по другим причинам. Для этого пациенты проходят полную лабораторную диагностику с ПЦР-исследованием, анализом на антитела классов M и G. Также больным требуется консультация кардиолога, пульмонолога, иммунолога, чтобы исключить прочие проявления постковидного синдрома.

Лечение нейроковида
Терапевтическая программа подбирается с учетом нозологической формы нейроковида, тяжести состояния больного и наличия сопутствующих заболеваний. При критических неврологических осложнениях лечение проводится в реанимационном или неврологическом стационаре. Хронические симптомы требуют длительной амбулаторной терапии с последующей нейрореабилитацией.
Медикаментозное лечение нейроковида включает вазоактивные препараты, нейропротекторы и ноотропы, витаминные комплексы. Для стабилизации психического состояния используются седативные средства, антидепрессанты и легкие транквилизаторы. При ОНМК необходима тромболитическая, антикоагулянтная и антиагрегантная терапия. Манифестация аутоиммунных процессов требует приема стероидных гормонов и иммуносупрессоров.
Для восстановления здоровья большую роль играют немедикаментозные методы: изменение образа жизни, постепенное расширение физической активности, сбалансированное и витаминизированное питание. После улучшения самочувствия рекомендовано санаторно-курортное лечение, талассотерапия, спелеотерапия и бальнеотерапия. Пациентам оказывают помощь на сеансах индивидуальной и групповой психотерапии, применяют методы арт-терапии, музыкотерапии.
Прогноз и профилактика
При проведении комплексной терапевтической программы удается полностью восстановить неврологические функции у большинства пациентов. Однако выздоровление и реабилитация требуют времени: у 20% людей патологические симптомы сохраняются более 5 недель, у 10% – дольше 3 месяцев. Менее благоприятный прогноз при развитии ишемического или геморрагического инсульта при нейроковиде, после чего остаются резидуальные неврологические изменения.
Основу профилактики нейроковида составляют противоэпидемические меры, направленные на борьбу с распространением COVID-19. При отсутствии противопоказаний настоятельно рекомендовано пройти полный курс вакцинации против SARS-CoV-2, что является самой надежной защитой от заражения и развития тяжелых осложнений. Также важны неспецифические меры: физическое дистанцирование, ношение средств индивидуальной защиты, ограничение социальных контактов.
1. Неврологические последствия COVID-19 у пожилых/ А.Ю. Никитина, А.Ш. Чимагомедова, О.С. Левин// Журнал неврологии и психиатрии им С.С. Корсакова. – 2021. – №10.
2. Неврологические нарушение у пациентов с long COVID синдромом и методы клеточной терапии для их коррекции: обзор литературы/ И.С. Долгополов, Г.Л. Менткевич, М.Ю. Рыков, Л.В. Чичановская// Сеченовский вестник. – 2021. – №3.
3. Неврологические аспекты COVID-19. Тактика ведения пациентов неврологом с учетом эпидемиологической ситуации/ Демьяновская Е. Г., Крыжановский С. М., Васильев А. С., Шмырев В. И.// Лечащий врач. – 2021. – №2.
4. Неврологические проявления и осложнения у пациентов с COVID-19/ И.К. Терновых, М.П. Топузова, А.Д. Чайковская, П.Ш. Исабекова, Т.М. Алексеева// Трансляционная медицина. – 2020. – №7.
Читайте также:

