Общий ответ на инфекцию
Обновлено: 13.05.2024
Типы гуморального иммунного ответа при вирусной инфекции. Иммуноглобулин A.
Иммунная система организма на вирусные инфекции или иммунизацию вирусными вакцинами отвечает выработкой антител, обладающих специфичностью к различным вирусным компонентам и принадлежащих к разным классам иммуноглобулинов.
Важнейшая биологическая функция иммуноглобулинов - специфическое связывание с антигеном. Антитела против некоторых эпитопов на поверхности вирионов нейтрализуют инфекционность, они могут также действовать как опсонины, облегчая поглощение и разрушение макрофагами. Кроме того, антитела могут прикрепляться к вирусным антигенам на поверхности инфицированных клеток, вызывая их разрушение вследствие активации классического или альтернативного действия комплемента или с помощью активации Fc-рецепторсвязывающих клеток, таких как NK-клетки, полиморфноядерные лейкоциты и макрофаги (антителозависимая цитотоксичность).
Различают четыре основных класса антител: два мономера IgG и IgE и два полимера IgM и IgA. Все иммуноглобулины имеют подобную структуру, но широко варьируют по аминокислотной последовательности антигенсвязывающего сайта, который определяет их специфичность для данной антигенной детерминанты. N-концевая последовательность L- и Н-цепей образует антигенсвязывающий центр, то есть антидетерминанту. Чем больше антидетерминант на поверхности иммуноглобулина, тем выше его активность.
Авидность характеризует прочность связи антитела с соответствующим антигеном. Афинность - прочность связи между отдельными антидетерминантами и детерминантами.
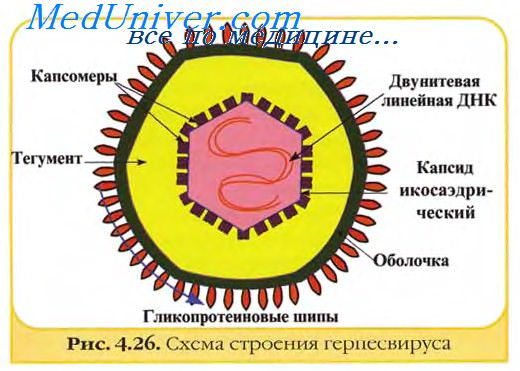
IgG является основным классом антител в крови. Он состоит из двух Н- и L-цепей, каждая из которых содержит постоянные и вариабельные участки. Молекулы IgG содержат два идентичных антигенсвязывающих Fab-фрагмента и Fc-фрагмент, выполняющий эффекторные функции (связывание комплемента, прикрепление к фагоцитам и плацентарному или колостральному трансферу).
В результате системной вирусной инфекции IgG синтезируется в течение длительного периода и является главным фактором защиты от реинфекции. Субклассы IgG отличаются константной областью их V-цепей и, соответственно, биологическими свойствами, такими как фиксация комплемента и прикрепление к фагоцитам.
Первоначально антитела относятся к классу IgM, но соматические рекомбинации (транслокации) затем рождают класс, обусловленный связыванием V-генных сегментов различными постоянными участками Н-цепей. В изменении изотипов (переход изотипов на другой путь) важная роль принадлежит различным цитокинам. Таким образом, через несколько дней IgG , IgA и иногда IgE-антите-ла той же самой специфичности становятся доминантными в иммунном ответе.
Тц-клетки достигают своего пика обычно через неделю после инфекции, а антитела — через 2—3 недели. NK-клетки максимально активируются через два дня, а активность интерферона совпадает с пиком концентрации вируса.
Динамика гуморального иммунного ответа проявляется, в первую очередь, в смене синтеза антител различных классов. В начальной фазе иммунного ответа синтезируется преимущественно IgM с относительно слабым сродством к антигену (авидный класс антител). IgM является пентамером с 10 Fab-фрагментами. Синтез IgM сменяется синтезом IgG, а затем IgA. IgM-антитела находятся в большинстве случаев в плазме крови и лимфе, обладая способностью преципитировать, агглютинировать и лизировать антигены.
Устойчиво высокие титры антител могут отражать также персистенцию вирусной инфекции (например, вирусов герпеса, кори) или повторную стимуляцию вирусным антигеном, однако антитела к некоторым вирусам могут персистировать и без явных признаков заболевания. IgG -антитела содержатся в сыворотке крови в наиболее высокой концентрации (~12г/л), откуда они поступают в тканевую жидкость. В отличие от других иммуноглобулинов, у человека и приматов они способны проникать через плаценту и снабжать плод материнскими антителами. Период полураспада их равен 10-35 дням.
Иммуноглобулин A (IgA) является димером с 4 Fab-фрагментами. Проходя через эпителиальные клетки, IgA приобретает J-фрагмент (секреторный фрагмент), становясь секреторным slgA, который секретируется через эпителий респираторного, кишечного и урогенитального трактов. Секреторный IgA более устойчив к протеазам, чем другие иммуноглобулины, и является основным иммуноглобулином на слизистых поверхностях, в молозиве и молоке многих видов млекопитающих. Поэтому IgA-антитела играют важную роль в защите от инфекции респираторного, кишечного и урогенитального трактов. Иммунизация через слизистые при некоторых инфекциях является более эффективной, чем системное введение вакцины.
Секреторные антитела появляются на 4-7-й день после инфицирования и представлены в основном IgA, IgG и IgM. Они считаются менее специфичными, чем сывороточные. Динамика накопления антител в сыворотке крови и секретах практически одинакова.
В отличие от сывороточного IgA, большая часть которого является мономером, молекула секреторного IgA представляет собой димер. Мономерный IgA синтезируется плазматическими клетками костного мозга, периферических лимфатических узлов, селезенки и других органов. Димерные формы sIgA с соединительной j-цепью синтезируются лимфоидной тканью желудочно-кишечного, респираторного и урогенитального трактов.
Добавочный структурный компонент секреторного IgA, вероятно, функционирует как поверхностный рецептор клеток секреторного эпителия и придает устойчивость sIgA к действию протеаз. Биологическая функция sIgA состоит в основном в местной защите слизистых оболочек от инфекции. Формирование местных секреторных IgA на поверхности слизистых оболочек имеет особое значение для формирования устойчивости организма к вирусам, обычно проникающим через дыхательный, кишечный или урогенитальный эпителий. Для индукции секреторных IgA в кишечнике вирус должен вступить в контакт с лимфоидной тканью кишечника. После формирования местного ответа В-клетки памяти, образующие IgA, мигрируют в другие участки кишечника. Аналогичный механизм индукции IgA функционирует в респираторном тракте.
Система секреторного иммунитета функционирует и регулируется иначе, чем иммунная система в целом. Она может коррелировать с общей иммунной реакцией или быть независимой от нее. Кроме секреторного IgA, существенное значение для иммунитета слизистых оболочек имеют содержащиеся в секретах у человека IgM и IgG. IgM также представляет секреторный иммуноглобулин, однако он не так прочно, как sIgA, связывает секреторный компонент. В пищеварительном тракте IgM играет более важную роль, чем IgG, а в носоглотке - наоборот.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

У РНК-содержащих ретровирусов сначала происходит обратная транскрипция генома в ДНК, затем ее интеграция в клеточные хромосомы и лишь после этого транскрипция генов.
Цитопатические эффекты при вирусных инфекциях разнообразны, они определяются как вирусом, так и клеткой и сводятся к разрушению клетки (цитолитический эффект), сосуществованию вируса и клетки без гибели последней (латентная и персистирующая инфекция) и трансформации клетки.
Вовлеченность организма в инфекционный процесс зависит от ряда обстоятельств - количества погибших клеток, токсичности вирусов и продуктов распада клеток, от реакций организма, начиная от рефлекторных и заканчивая иммунными. Количество погибших клеток влияет на тяжесть инфекционного процесса. Например, будут ли поражены при гриппе только клетки носа и трахеи или вирус поразит клетки эпителия альвеол, зависит тяжесть и исход болезни.
Хотя вирусы и не образуют типичных токсинов, однако и вирионы, и вирусные компоненты, накапливающиеся в пораженных тканях, выходя в кровоток, оказывают токсическое действие. Неменьшее токсическое действие оказывают и продукты распада клеток. В этом случае действие вирусной инфекции столь же неспецифично, как и действие патогенных организмов, убивающих клетки и вызывающих их аутолиз. Поступление токсинов в кровь вызывает ответную реакцию - лихорадку, воспаление, иммунный ответ. Лихорадка является преимущественно рефлекторным ответом на поступление в кровь и воздействие на ЦНС токсичных веществ.
Если лихорадка - общий ответ организма на вирусную инфекцию, то воспаление - это местная многокомпонентная реакция. При воспалении происходят инфильтрация пораженных тканей макрофагами, утилизация продуктов распада, репарация и регенерация. Одновременно развиваются реакции клеточного и гуморального иммунитета. На ранних стадиях инфекции действуют неспецифические киллеры и антитела класса IgM. Затем вступают в действие основные факторы гуморального и клеточного иммунитета. Однако гораздо раньше, уже в первые часы после заражения, начинает действовать система интерферона, представляющая семейство секреторных белков, вырабатываемых клетками организма в ответ на вирусы и другие стимулы. Описанные явления относятся к так называемой острой репродуктивной вирусной инфекции. Взаимодействие вируса и клеток может происходить, как отмечалось выше, без гибели последних. В этом случае говорят о латентной, т.е. бессимптомной или персистирующей хронической вирусной инфекции. Дальнейшая экспрессия вируса, образование вирусспецифических белков и вирионов вызывает синтез антител, на этой стадии латентная инфекция переходит в персистирующую и появляются первые признаки болезни.
Репродукция вируса в клетках сопровождается развитием цитопатических процессов, специфичных для разных вирусов и для разных типов инфекционных процессов. Цитопатические процессы при вирусных инфекциях разнообразны, они определяются как вирусом, так и клетками, причем специфика их больше "задается" клеткой, нежели вирусом, и сводится в основном к разрушению клеток, сосуществованию вируса и клеток без гибели последних и трансформация клеток. Несмотря на значительные различия цитоцидного действия разных вирусов, в общем, они сходны. Подавление синтеза клеточных макромолекул - нуклеиновых кислот и белков, а также истощение энергетических ресурсов клетки ведут к необратимым процессам, заканчивающимся гибелью пораженной клетки. Повреждение клеток вирусами, их отмирание и распад переносят вирусную инфекцию с клеточного уровня на уровень организма в целом.
При встрече организма с вирусной инфекцией продукция интерферона (растворимого фактора, вырабатываемого вирус-инфицированными клетками, способного индуцировать антивирусный статус в неинфицированных клетках) становится наиболее быстрой реакцией на заражение, формируя защитный барьер на пути вирусов намного раньше специфических защитных реакций иммунитета, стимулируя клеточную резистентность, - делая клетки непригодными для размножения вирусов.
Продукция и секреция цитокинов относятся к самым ранним событиям, сопутствующим взаимодействию микроорганизмов с макрофагами. Этот ранний неспецифический ответ на инфекцию важен по нескольким причинам: он развивается очень быстро, поскольку не связан с необходимостью накопления клона клеток, отвечающих на конкретный антиген; ранний цитокиновый ответ влияет на последующий специфический иммунный ответ.
Интерферон активирует макрофаги, которые затем синтезируют интерферон-гамма, ИЛ-1, 2, 4, 6, ФНО, в результате макрофаги приобретают способность лизировать вирус-инфицированные клетки.
Интерферон-гамма является специализированным индуктором активации макрофагов, который способен индуцировать экспрессию более 100 разных генов в геноме макрофага.
Продуцентами этой молекулы являются активированные Т-лимфоциты (Тh1-тип) и естественные киллеры (NK-клетки). Интерферон-гамма индуцирует и стимулирует продукцию провоспалительных цитокинов (ФНО, ИЛ-1, 6), экспрессию на мембранах макрофагов, антигенов МНС II; гамма-интерферон резко усиливает антимикробную и противовоспалительную активность путем повышения продукции клетками супероксидных радикалов, а усиление иммунного фагоцитоза и антителоопосредованной цитотоксичности макрофагов под влиянием гамма-интерферона связано с усилением экспрессии Fc-рецепторов для JgG. Активирующее действие интерферона-гамма на макрофаги опосредовано индукцией секреции этими клетками ФНО -альфа. Этот пик наблюдается совместно с ФНО-альфа. Максимум продукции ИЛ-4 наступает через 24-48 ч с момента активации клеток. При этом ИЛ-4 рассматривается как цитокин, ограничивающий иммуновоспалительные реакции и снижающий ответ организма на инфекцию, угнетая при этом экспрессию гамма-интерферона. Интерферон-гамма ин витро усиливает фагоцитарную активность нейтрофилов, что обусловлено усилением экспрессии Fc-рецепторов и поверхностных белков семейства интегринов на нейтрофилы. Это позволяет нейтрофилам осуществлять цитотоксические функции и фагоцитоз. В качестве основных эффекторных клеток воспалительного процесса, они обеспечивают элиминацию инфекта из организма.
Взаимодействие цитокина с клеткой определяется универсальной биологической системой, специфическим механизмом которой является рецепторный аппарат, связанный с восприятием метаболического кода. Для проявления биологической активности цитокина необходимо присутствие на поверхности чувствительных клеток специфических рецепторов, которые могут экспрессироваться параллельно с синтезом цитокина. Рецепторы цитокинов представляют собой комплексы, состоящие из двух и более рецепторных молекул, которые объединяются на мембране клетки-мишени и образуют высокоаффинный рецепторный комплекс. Большинство рецепторов состоит из отдельных молекул, связывающих цитокины, которые ассоциируются после связывания лиганда с сигналпередающим рецепторным компонентом; часть рецепторов существует как растворимые изоформы, способные связывать и растворять цитокины, а часть функционирует как многокомпонентные блоки; механизм комплексирования субъединиц рецепторов объясняет плейотропные и дублирующие эффекты цитокинов, имеющих большое структурное сходство. Рецепторы ИЛ-10 имеют гомологию рецепторов интерферона, и подобно ИЛ-10 индуцирует экспрессию в моноцитах гена Fc- рецептора. Для полного функционирования цитокиновой системы необходимы повышение уровня цитокина в ответ на инфект и экспрессия нормального количества рецепторов к ним на клетках. Изменение рецепторов после их связывания с цитокином заключается в интернализации комплексов цитокин - рецептор внутрь клетки. На поверхности клеток рецептор появляется заново, постепенно синтезируясь в течение 24-36 ч (время появления рецепторов интерферон-альфа). В этот период клетки остаются чувствительными к последующим дозам цитокина, чем объясняется эффективность введения препаратов интерферона и их индукторов три раза в неделю.
При антигенной стимуляции клеток трансдукция сигнала с активированного рецептора на генетический аппарат осуществляется с помощью внутриклеточных регуляторных систем, компоненты которых (белки мембран, ферментов, хроматина) связываются с чувствительными к ним последовательностями ДНК. После связывания цитокина (интерферон) с поверхностными клеточными мембранными рецепторами происходит активация ферментов протеинкиназы-С (ПКС), тирозинкиназы, ц-АМФзависимой протеинкиназы, серин-треонинкиназы. Интерферон-альфа активирует tyk 2 и jak 1-киназы, а интерферон-гамма активирует jak 1 и 2-киназы. Далее факторы транскрипции перемещаются в ядро клетки и связывают гены раннего ответа.
Первый ответ клеток на цитокин - это быстрая индукция генов раннего ответа ("immediate early" генов), в число которых и входит ген интерферон-гамма. Стимуляция экспрессии этих генов важна для выхода клеток из Go-стадии и перехода в Gi-стадию и дальнейшей прогрессии клеточного цикла. Их индукция происходит после активации рецепторов роста на клеточной мембране и активации протеин-киназной системы. Гены раннего ответа являются ключевыми регуляторами клеточной пролиферации и дифференцировки, кодируют белки, регулирующие репликацию ДНК.
Таким образом, при активации клеток происходит стимуляция генов раннего ответа, что ассоциируется с изменением фаз клеточного цикла. Основная протективная роль в иммунном ответе, направленном против внутриклеточных паразитов (грибы, простейшие, вирусы, микобактерии туберкулеза), принадлежит клеточным механизмам. Способность перечисленных возбудителей переживать и размножаться внутри клеток делает их защищенными от действия антител и системы комплемента. Резистентность к антимикробным факторам макрофагов позволяет им длительно переживать внутри этих клеток. Для элиминации возбудителя необходим специфический клеточно-опосредованный ответ. Его специфичность определяется антигенраспознающими СД8+-Т-лимфоцитами, которые пролиферируют, активируются и формируют клон эффекторных цитотоксических лимфоцитов. Решающий момент специфического иммунного ответа - это ответ СД4+Т-лимфоцитов с хелперной направленностью на распознавание антигена. На этом этапе определяется форма иммунного ответа: либо с преобладанием гуморального иммунитета, либо с преобладанием клеточных реакций (ГЗТ). Направление дифференцировки СД4 + -лимфоцитов, от которого зависит форма специфического иммунного ответа, контролируется цитокинами, образующимися в ходе воспалительной реакции. Так, в присутствии ИЛ-12 и интерферон-гамма СД4 + -лимфоциты дифференцируются в воспалительные Тh1-клетки, начинают продуцировать и секретировать интерлейкин-2, интерферон-гамма, ФНО и определяют клеточный характер специфического иммунного ответа. Присутствие ИЛ-12 обеспечивается его продукцией макрофагами, а интерферон-гамма - естественными киллерами, активированными в раннюю фазу ответа на внутриклеточно паразитирующие бактерии и вирусы. В отличие от этого, в присутствии ИЛ-4 СД4 + -лимфоциты дифференцируются в хелперы Тh 2, которые начинают продуцировать и секретировать ИЛ-4, ИЛ-5, ИЛ-6 и запускают гуморальный иммунный ответ, т.е. синтез специфических антител - иммуноглобулинов. Воспалительные Тh 1-лимфоциты нужны для борьбы с внутриклеточными паразитами, а Тh 2 хелперы нужны для элективной защиты от внеклеточных паразитов.
Вирусная инфекция может вызывать быстрое подавление экспрессии ряда клеточных генов (из которых наиболее изучены интерфероновые гены и гены, кодирующие дс-РНК-зависимые ферменты -2,5-ОАС и ПК-дс), принимающих участие в антивирусном действии. Специальные исследования механизма антивирусного действия интерферонов и дс-РНК в клеточных и бесклеточных системах показали ключевую роль в этом процессе вышеуказанных ферментов. ПК-дс, взаимодействуя с дс-РНК, фосфорилируется и в активной форме фосфорилирует регуляторные факторы транскрипции и трансляции, из которых наиболее изучен инициирующий фактор трансляции (eIF2).
ПК-дс выполняет регуляторную роль в системе клеточной пролиферации на уровне факторов трансляции и активации ряда генов цитокинов. Вероятно, существует связь между подавлением транскрипции мРНК и ПК-дс, угнетением общего синтеза клеточного белка при вирусных инфекциях и накоплением в ядрах клеток белка нуклеокапсида и белка NSP2. Фрагментация клеточных хромосом, наблюдающаяся на ранних сроках вирусной инфекции, может быть одной из причин подавления экспрессии генов, участвующих в противовирусном ответе.
Есть основания предполагать участие белков NSP2 в регуляции активности генов цитокинов - низкомолекулярных белковых регуляторных веществ, продуцируемых клетками и способных модулировать их функциональную активность. Нарушения в системе цитокинов приводят к нарушению кооперативных взаимодействий иммунокомпетентных клеток и нарушению иммунного гомеостаза.
В последние годы показано, что ИЛ- 12, относящийся к провоспалительным цитокинам, является ключевым для усиления клеточно-опосредованного иммунного ответа и инициации эффективной защиты против вирусов.
Средства терапии гриппа и ОРЗ можно разделить на этиотропные, иммунокорригирующие, патогенетические и симптоматические. Приоритет принадлежит этиотропным препаратам, действие которых направлено непосредственно на возбудитель инфекции. Все препараты этиотропного действия целесообразно рассматривать с учетом их точек приложения в цикле репродукции вирусов гриппа и других ОРЗ.
Применение химиопрепаратов для профилактики и лечения гриппа и ОРЗ относится к базовой терапии и является общепризнанным мировым стандартом. Многолетние клинические исследования достоверно выявили их высокую лечебно-профилактическую значимость. Химиотерапевтические средства представлены тремя основными группами: это блокаторы М2-каналов (амантадин, ремантадин); ингибиторы нейраминидазы (занамивир, озельтамивир) и ингибиторы протеаз (амбен, аминокапроновая кислота, трасилол). Препараты оказывают прямое антивирусное действие, нарушая различные фазы репликативного цикла вирусов. Несколько особняком стоит группа вирулицидных препаратов, применяемых местно для предотвращения адсорбции и проникновения вирионов в клетки.
В онлайн-лаборатории Lab4U мы хотим, чтобы каждый из вас мог заботиться о своем здоровье. Для этого мы просто и понятно рассказываем о показателях организма.
Что такое антитела? И как расшифровать результаты анализа?
Антитела — это белки, которые иммунная система вырабатывает в ответ на проникновение инфекции. В лабораторной диагностике именно антитела служат маркером проникновения инфекции. Общим правилом подготовки к анализу на антитела является сдавать кровь из вены натощак (после приема пищи должно пройти не менее четырех часов). В современной лаборатории сыворотку крови исследуют на автоматическом анализаторе с использованием соответствующих реагентов. Иногда серологический анализ на антитела является единственным способом диагностики инфекционных заболеваний.
Анализы на инфекции могут быть качественными (дают ответ, есть ли инфекция в крови) и количественными (показывают уровень содержания антител в крови). Норма антител для каждой инфекции своя (для некоторых их не должно быть совсем). Референсные значения (показатели нормы) антител можно получить с результатом анализа.
В онлайн-лаборатории Lab4U можно сдатькомплекс анализов на все TORCH-инфекции за один раз и со скидкой 50%!
Различные классы антител IgG, IgM, IgA
Иммуноферментный анализ определяет антитела инфекций относящиеся к различным классам Ig (G, A, M). Антитела к вирусу, при наличии инфекции, определяются на очень ранней стадии, что обеспечивает эффективную диагностику и контроль течения заболеваний. Самые распространенные методы диагностики инфекций — это тесты на антитела класса IgM (острая фаза течения инфекции) и антитела класса IgG (устойчивый иммунитет к инфекции). Эти антитела определяют для большинства инфекций.
Однако, один из самых распространенных анализов — госпитальный скрининг (анализы на ВИЧ, сифилис и гепатиты B и С) не дифференцирует тип антител, поскольку наличие антител к вирусам данных инфекций автоматически предполагает хроническое течение заболеваний и является противопоказанием, например, для серьезных хирургических вмешательств. Поэтому важно опровергнуть или подтвердить диагноз.
Детальную диагностику типа и количества антител при диагностированном заболевании можно сделать, сдав анализ на каждую конкретную инфекцию и тип антител. Первичная инфекция выявляется при обнаружении диагностически значимого уровня антител IgM в образце крови или значимым ростом числа антител IgA или IgG в парных сыворотках, взятых с интервалом 1-4 недели.
Реинфекция, или повторная инфекция, выявляется быстрым подъемом уровня антител IgA или IgG. Антитела IgA имеют более высокую концентрацию у пациентов старшего возраста и более точно диагностируют текущую инфекцию у взрослых.
Перенесенная инфекция в крови определяется как повышенные антитела IgG без роста их концентрации в парных образцах, взятых с интервалом 2 недели. При этом отсутствуют антитела классов IgM и А.
Антитела IgM
Их концентрация повышается вскоре после заболевания. Антитела IgM определяются уже через 5 дней после его начала и достигают пика в промежутке от одной до четырех недель, затем снижаются до диагностически незначительных уровней в течение нескольких месяцев даже без проведенного лечения. Однако, для полной диагностики недостаточно определения только антител класса М: отсутствие этого класса антител еще не говорит об отсутствии заболевания. Острой формы заболевания нет, но может быть хроническая.
Антитела IgM имеют большое значение в диагностике гепатита А и детских инфекций (краснуха, коклюш, ветрянка), легко передающихся воздушно-капельным путем, так как важно как можно раньше выявить заболевание и изолировать заболевшего.
Антитела IgG
Основная роль антител IgG — это длительная защита организма от большинства бактерий и вирусов — хотя их выработка происходит более медленно, но ответ на антигенный раздражитель сохраняется более устойчивым, чем у антител класса IgM.
Уровни антител IgG повышаются медленнее (через 15-20 дней после начала заболевания), чем IgM, но остаются повышенными дольше, поэтому могут показывать давно текущую инфекцию при отсутствии IgM АТ. IgG могут находиться на низком уровне в течение многих лет, но, при повторном воздействии того же антигена, уровень антител IgG быстро повышается.
Антитела IgG, в частности, используются для диагностики Helicobacter pylori — одной из причин язвы и гастрита.
Антитела IgA
В сыворотке появляются через 10-14 дней после начала заболевания, и вначале их даже можно обнаружить в семенной и вагинальной жидкостях. Уровень антител IgA обычно снижается к 2-4 месяцу после инфицирования в случае успешного лечения. При повторном инфицировании уровень антител IgA вновь возрастает. Если уровень IgA не падает после проведенного лечения, то это — признак хронической формы инфекции.
Анализ на антитела в диагностике TORCH-инфекций
Аббревиатура TORCH появилась в 70-х годах прошлого столетия, и состоит из заглавных букв латинских названий группы инфекций, отличительной особенностью которых является то, что при относительной безопасности для детей и взрослых, TORCH инфекции при беременности представляют чрезвычайную опасность.
Анализ крови на TORCH инфекции является комплексным исследованием, в его состав входит 8 тестов:
Нередко, заражение женщины инфекциями TORCH-комплекса во время беременности (наличие в крови только антител IgM) является показанием для ее прерывания.
В заключение
Иногда, обнаружив в результатах анализа антитела IgG, например, токсоплазмоза или герпеса, пациенты приходят в панику, не посмотрев на то, что антитела IgM, которые показывают наличие текущей инфекции, могут отсутствовать вовсе. В этом случае анализ говорит о перенесенной ранее инфекции, к которой выработался иммунитет.
В любом случае, интерпретацию результатов анализа лучше доверить врачу, и с ним же в случае необходимости определиться с тактикой лечения. А сдать анализы вы можете доверить нам.
Почему быстрее, удобнее и выгоднее сдавать анализы в Lab4U?
Вам не нужно долго ждать в регистратуре
Все оформление и оплата заказа происходит онлайн за 2 минуты.
Путь до медцентра не займет более 20 минут
Наша сеть вторая по величине в Москве, а еще мы есть в 23 городах России.
Сумма чека не шокирует вас
Постоянная скидка в 50% действует на большинство наших анализов.
Вам не придется приходить минута-в-минуту или ждать в очереди
Сдача анализа происходит по записи в удобный промежуток времени, например с 19 до 20.
Вам не придется долго ждать результатов или ходить за ними в лабораторию
В онлайн-лаборатории Lab4U мы хотим, чтобы каждый из вас мог заботиться о своем здоровье. Для этого мы просто и понятно рассказываем вам о показателях здоровья!
Как правило, самый распространенный вопрос на этапе диагностики болезни, который возникает у педиатра или терапевта - бактериальная или вирусная инфекция у пациента? Оказывается, при вирусных и бактериальных инфекциях в организме происходят два разных процесса. Поэтому от ответа на этот вопрос зависит стратегия дальнейшего лечения.
Содержание:
Как делается общий анализ крови
Самый информативный способ узнать вид инфекции — сдать общий анализ крови. Кровь человека состоит из плазмы и клеток лейкоцитов, эритроцитов и тромбоцитов. Лаборант берет кровь из вены, размазывает ее по стеклышку, кладет под микроскоп и смотрит, сколько каких лейкоцитов. Они бывают разные: нейтрофилы, эозинофилы, базофилы, моноциты и лимфоциты. В итоге он получает лейкограмму— процентное соотношение различных видов лейкоцитов в окрашенном мазке крови под микроскопом. Если в крови много лимфоцитов, то заболевание вирусное, а если много нейтрофилов - бактериальная.
| Наименование теста | Результат | Единицы измерения | Референсные значения |
| Общий анализ крови (свс) | |||
| Гемоглобин | 129 | г/л | 120 – 158 |
| Эритроциты | 4.69 | 10^12/л | 3.90 – 5.20 |
| Средний объем эритроцитов | 82.9 | фл | 81.00 – 100.00 |
| Среднее содержание hb в эритроците | 27.5 | пг | 26.00 – 34.00 |
| Средняя концентрация hb в эритроците | 332 | г/л | 310 – 370 |
| Гетерогенность эритроцитов по объему | 13.0 | % | 11.9 – 15.5 |
| Гематокрит | 38.9 | % | 34.9 – 44.5 |
| Тромбоциты | 248 | 10^9/л | 150 – 400 |
| Средний объем тромбоцитов | 11.7 | фл | 6.0 – 13.0 |
| Гетерогенность тромбоцитов по объему | 15.5 | % | 9.0 – 20.0 |
| Тромбокрит | 0.29 | % | 0.12 – 0.36 |
| Лейкоциты | 5.31 | 10^9/л | 4.00 – 10.50 |
| Лейкоцитарная формула (микроскопия) | |||
| Палочкоядерные нейтрофилы | 6 | % | 1 – 6 |
| Сегментоядерные нейтрофилы | 34 ↓ | % | 41 – 72 |
| Эозинофилы | 2 | % | 0 – 6 |
| Базофилы | 0 | % | 0 – 1 |
| Моноциты | 9 | % | 4 – 12 |
| Лимфоциты | 49 ↑ | % | 19 – 48 |
Как и зачем отличать палочкоядерный нейтрофил от сегментоядерного?
Оказывается, это очень просто сделать глазами, но почти невозможно определить с помощью машины. Именно поэтому стоит делать не просто общий анализ крови, а общий анализ крови с микроскопией, т.е. с ручным исследованием. Представим ситуацию, у вас или ребенка пятый день держится температура, вы сделали общий анализ крови с микроскопией. По результатам - завышен уровень палочкоядерных нейтрофилов. Это значит, что болезнь не вирусная, а уже бактериальное осложнение. И в этому случае педиатр или терапевт понимает, что пора давать антибиотики. Если начать пить их раньше — когда болезнь вирусная — антибиотики не только не помогут бороться с инфекцией, но и будут способствовать ослаблению иммунитета. Это ослабит организм и риск бактериального осложнения вырастет в несколько раз.
Когда сдавать общий анализ крови с микроскопией
К сожалению, не всегда врачи назначают анализы. При постановке диагноза многие обращают внимание только на симптоматику: сопли, горло, температура, кашель и т.д. И это иногда чревато серьезными последствиями.
Наши клиенты часто звонят нам и рассказывают истории, связанные с диагностикой и лечением. И вот одна из них. Месяц назад у Виталия заболела дочь. У нее держалась высокая температура, были сопли. Попытки сбить температуру не дали результата: она держалась от +37,5 до +39. Виталий обратился к педиатру. Тот осмотрел ребенка и принял решение наблюдать за ним в течение четырех дней. На пятый день улучшений не было, о проявился еще один симптом — начали болеть уши. Педиатр отправил Виталия с дочерью к отоларингологу. ЛОР при первом же осмотре поставила девочке диагноз: двусторонний гнойный отит. Ребенка ждало хирургическое лечение, курс антибиотиков и физиотерапии. А всего этого можно было избежать, если бы Виталий перед приемом педиатра отвел дочь на сдачу общего анализа крови с микроскопией или педиатр назначил бы его на первом приеме. Он стоит всего 310 рублей, делается за один день.
Расшифровка общего (клинического) анализа крови
Для каждого показателя в общем анализе крови существует диапазон референсных (нормальных) значений. Эти нормы зависят от пола и возраста. Так, нормы анализа крови у взрослых и детей значительно отличаются. Расшифровка анализа крови у детей варьируется в зависимости от возраста. Чем младше ребенок, тем больше его нормальные показатели крови будут отличаться от показателей взрослого человека. Например, количество лейкоцитов в первые дни жизни ребенка может в 2-3 раза превышать концентрации этих клеток в крови взрослого человека. И это не будет отклонением от нормы.
- Cегментоядерные формы 47 –72%
- Палочкоядерные формы 1 –6%
Эозинофилы 0.5 – 5%
Лимфоциты 19 – 37%
- Мужчины
- Женщины
- 3 – 10 мм/ч
- 5 – 15 мм/ч
Отклонения от нормы тех или иных показателей еще не говорят о наличии патологических состояний. На результаты анализа крови может влиять сильная физическая нагрузка, перенесенная накануне забора крови, а у женщин – еще и фаза менструального цикла. Известно, например, что за день до начала менструации уровень лейкоцитов может подняться почти в 2 раза, следовательно, показатели нормы будут отличаться от стандартных. Поэтому за интерпретацией лучше обратиться к терапевту или педиатру. Если вы хотите сами понимать, что происходит в организме, можно воспользоваться сервисом Расшифровка анализов онлайн, где можно ввести показатели своего общего анализа крови и получить предварительное заключение бесплатно.
Разные лаборатории могут использоваться разные единицы измерения показателей крови. Если они отличаются от заявленных в сервисе Расшифровка анализов онлайн, то вы можете перевести их с помощью калькулятора пересчета единиц измерения.

Выводы:
Если подытожить все вышесказанное, то по анализу крови с микроскопией можно определить - о какой инфекции (вирусной или бактериальной) идет речь, как организм на нее реагирует, нуждается ли он в активной помощи антибиотиков. Без результатов анализа при осмотре врач не сможет сразу определить вид инфекции и назначить адекватное лечение.
При необходимости сдайте общий анализ крови с микроскопиейи принесите результаты своему лечащему врачу. Так он сможет назначить вам правильное лечение.
Вы можете сдать общий анализ крови с микроскопиейсо скидкой 50%. Анализ будет готов в течение 1 дня. Вы получите результаты на электронную почту сразу по готовности.
Читайте еще по теме:
Почему быстрее, удобнее и выгоднее сдавать анализы в Lab4U?
-
Вам не нужно долго ждать в регистратуре
Все оформление и оплата заказа происходит онлайн за 2 минуты.
Наша сеть вторая по величине в Москве, а еще мы есть в 23 городах России.
Постоянная скидка в 50% действует на большинство наших анализов.
Сдача анализа происходит по записи в удобный промежуток времени, например с 19 до 20.
С инфекцией мочевыводящих путей (ИМП) сталкиваются и дети, и мужчины, и женщины. Вы можете услышать этот диагноз, если придете к врачу с жалобами на болезненное и частое мочеиспускание. Попробуем разобраться, какие анализы помогут при этом недуге.
Мочевыделительные пути включают путь от почек наружу. Это мочеточники (трубки, которые идут от почек к мочевому пузырю), мочевой пузырь и уретра (трубка, которая выводит мочу из мочевого пузыря наружу).
Чем проявляются ИМП
- Боль или жжение при мочеиспускании
- Боль в нижней части живота, над мочевым пузырем (над лобковой костью)
- Частые позывы (желание мочиться)
- Небольшие порции мочи за раз
- Моча мутная, темная, с неприятным запахом, с кровью.
- У мужчин может быть болезненное семяизвержение
- Лихорадка, озноб, тошнота и боль пояснице больше свидетельствуют о поражении почек.
Кто виновник ИМП
Большинство ИМП происходит из-за бактерий, которые обычно находятся в кишечнике. Это так называемая кишечная палочка E.coli. Но и другие бактерии, такие как стафилококк, протей, клебсиелла, энтерококк и псевдомонада, могут вызывать инфекцию. На фоне проблем с иммунной системой, аутоиммунных заболеваний и сахарного диабета, больше шансов получить ИМП от самых разных возбудителей.
Особой группой являются инфекции, передающиеся половым путем, включая хламидии и микоплазмы.
Анатомия важна
Если инфекция в почках, врачи называют это пиелонефрит. Если она в мочевом пузыре — цистит. Если воспаление в уретре – уретрит. Инфекция почек это серьезное заболевание. Его часто провоцируют врожденные нарушения строения мочевого тракта и иммунодефицитные состояния. Пиелонефрит может осложнять течение беременности, повторные случаи нарушать работу почек.
Гораздо чаще встречаются инфекции нижних отделов мочевого тракта. Женщины чаще страдают от ИМП, потому что уретра у них намного короче. Уретральное отверстие располагается ближе к анусу и кишечные бактерии легче проникают в уретру. Влажный контакт во время секса также облегчает проникновение бактерий из влагалища и заднего прохода в уретру.
У мужчин ИМП часто связана с проблемами в предстательной железе, инфекциями, передающимися половым путем.
Что может провоцировать ИМП
- Предшествующие эпизоды ИМП
- Заболевания, нарушающие иннервацию мочевого пузыря (сахарный диабет, рассеянный склероз, болезнь Паркинсона и травмы спинного мозга)
- Период менопаузы у женщин или использование местных противозачаточных средств
- Избыточный вес
- Состояния, блокирующие отток мочи (камень в почках, увеличенная простата у мужчин)
- Преимущественно анальный секс
Что можно увидеть в анализах
При указанных выше жалобах, первым делом врачи просят сдать общий анализ мочи. Он собирается утром, после подмывания чистой водой. Желательно собрать всю порцию мочи в чистую емкость, перемешать и отлить часть в стерильный контейнер. Общий анализ мочи покажет наличие лейкоцитов, крови и бактерий.
Если нужно более прицельно посмотреть содержание лейкоцитов и крови (эритроцитов), собирают только среднюю порцию мочи и сдают анализ по Нечипоренко. В этом случае, начинают мочиться в унитаз, собирают среднюю порцию мочи в контейнер и заканчивают мочеиспускание также в унитаз.
Посев мочи позволяет определить тип бактерий, вызвавших инфекцию. Также он поможет врачу выбрать антибиотик для лечения.
У сексуально активных девушек и молодых людей оправдано проводить ПЦР исследования мазков из урогенитального тракта на инфекции, передающиеся половым путем. Поскольку эти возбудители не выявляются в обычном посеве мочи.
Читайте также:

