Пневмоцистоз легких что это такое
Обновлено: 12.05.2024
Гистоплазмоз (Histoplasmosis; Histoplasmose - нем.; histoplasmose - франц.) - глубокий микоз, который характеризуется полиморфизмом клинических проявлений от легких и латентных форм до прогрессирующих заболеваний, заканчивающихся смертью больного. Преобладают легочные формы гистоплазмоза.
Что провоцирует / Причины Гистоплазмоза легких:
Возбудитель - Histoplasma capsulatum - диморфный гриб, существующий в тканевой и культуральной формах. Тканевая форма располагается в клетках органов ретикулоэндотелиальной системы (печень, селезенка, лимфатические узлы). По форме и размерам (2-4 мкм) этот микроорганизм напоминает лейшмании или токсоплазмы. Мицелиальная форма гриба никогда не встречается в тканях. Она хорошо развивается на питательных средах при температуре ниже 30С. Гистоплазмы в обеих фазах являются патогенными для белых мышей, крыс, морских свинок, золотистых хомячков, собак. Гриб длительно сохраняется во влажной почве (6 нед) и в воде. Быстро погибает под влиянием различных дезинфицирующих препаратов.
Возбудитель болезни сохраняется в почве. В загрязнении (заражении) почвы имеет определенное значение выделение гриба инфицированными животными и птицами (летучие мыши, кошки, собаки, куры, скворцы и др.). Инфицирование людей происходит воздушно-пылевым путем. Случаев заражения человека от больных людей и животных не наблюдалось. Гистоплазмоз широко распространен в различных странах Африки и Америки, встречается также в Европе и Азии, единичные случаи гистоплазмоза описаны в нашей стране, возможны и завозные случаи. Наиболее инфицированными являются области, расположенные от 45° до 30° к северу. Важную роль в эпидемиологии гистоплазмоза играет почва. В период дождей гистоплазма размножается в почве. Одна колония гриба диаметром 2,5 см может нести миллионы спор. После окончания периода дождей споры рассеиваются во внешней среде. Заражение происходит при вдыхании спор, в частности при проведении разного рода земляных работ (рытье траншей, строительство и т. д.). Инфекция от больных людей здоровым не передается даже при длительных тесных контактах.
Патогенез (что происходит?) во время Гистоплазмоза легких:
Воротами инфекции чаще являются органы дыхания. Споры гриба с пылью попадают в бронхи и альвеолы, там они превращаются в паразитические дрожжеподобные формы, внедряются в ткани и обусловливают возникновение первичного легочного очага. С током лимфы возбудитель проникает в регионарные лимфатические узлы, вызывая в них воспалительный процесс. Наличие гриба в ткани приводит к формированию гранулематозного процесса, который разрешается некрозом, изъязвлением или петрификацией легочной ткани и лимфатических узлов, реже абсцедированием. Эта форма напоминает первичный туберкулез легких. Антигены гистоплазм проникают в общий круг кровообращения и приводят к аллергической перестройке организма (что выявляется внутрикожной пробой с гистоплазмином) и выработке специфических антител. На этом процесс может закончиться, не давая выраженной симптоматики, иногда процесс протекает в виде инаппарантной формы. В других же случаях наступает гематогенная диссеминация гриба по всему организму с поражением многих органов. Процесс быстро прогрессирует и часто приводит к летальному исходу. В возникновении подобной формы большое значение имеет состояние иммунной системы. Такое течение, как правило, наблюдается у ВИЧ-инфицированных лиц.
Симптомы Гистоплазмоза легких:
Инкубационный период длится от 4 до 30 дней (чаще 7-14 дней). Чем короче инкубационный период, тем тяжелее протекает заболевание.
По клиническому течению выделяют следующие формы гистоплазмоза:
1. Острый гистоплазмоз легких:
а) бессимптомная (инаппарантная) форма;
б) клинически выраженные формы (легкая, средней тяжести, тяжелая).
2. Хронический прогрессирующий (кавернозный) гистоплазмоз легких.
3. Острый диссеминированный гистоплазмоз (доброкачественный, прогрессирующий).
4. Хронический диссеминированный гистоплазмоз (с поражением слизистых оболочек и кожи).
Чаще всего встречается острый гистоплазмоз легких, что обусловлено аэрогенным инфицированием. Острые формы легочного гистоплазмоза могут протекать бессимптомно и обнаруживаться лишь при постановке внутрикожной пробы с гистоплазмином, по положительным результатам серологических реакций, иногда по петрификатам в легких и прикорневых лимфатических узлах. При легких формах, которые преобладают, самочувствие больных остается хорошим, нередко они продолжают работать, лихорадка отсутствует или бывает кратковременной (3-4 дня), а общая длительность лечения 2-3 нед. При рентгенологическом исследовании выявляют усиление рисунка и увеличение тени корней легких, лишь у отдельных больных наблюдаются мелкоочаговые тени, преимущественно в нижних отделах легких.
Тяжелые формы острого гистоплазмоза легких характеризуются внезапным началом, быстрым повышением температуры тела до 40-41С. Температурная кривая неправильного типа с большим суточным размахом. Потрясающие ознобы сменяются диффузным потоотделением. Больные жалуются на сильную головную боль, слабость, боли в мышцах и костях, кашель, боли в груди. У некоторых больных отмечаются тошнота, рвота, понос, боли в животе. Длительность лихорадки 2-6 нед. В периоде реконвалесценции длительно наблюдается субфебрилитет, астенизация, резкое снижение трудоспособности, потливость. Эти явления сохраняются до 1 года. При перкуссии легких можно отметить некоторое укорочение звука, при аускультации - мелкопузырчатые влажные хрипы, преимущественно в нижних отделах легких. Рентгенологически выявляют крупно- и среднеочаговые тени в виде "ватных хлопьев", которые могут сливаться. В дальнейшем инфильтраты полностью исчезают или на их месте образуются очаги фиброза и кальцинации.
При среднетяжелых формах клинические и рентгенологические проявления выражены не так резко, лихорадка сохраняется около 2 нед, а продолжительность стационарного лечения составляет около месяца.
Хронический гистоплазмоз легких протекает в виде длительной прогрессирующей болезни, периодически дающей обострения. Наблюдают умеренную лихорадку, кашель с мокротой, при рентгенологическом исследовании выявляются каверны, фиброз и множественные кальцинированные очаги.
Острая форма диссеминированного гистоплазмоза проявляется высокой лихорадкой гектического или неправильного типа, повторными ознобами и потоотделением, выраженными симптомами общей интоксикации (головная боль, мышечные и суставные боли, тошнота, рвота, боли в животе, нарастающая слабость). На этом фоне появляются множественные вторичные очаги как результат диссеминации: различного рода экзантемы (макулопапулезная, фурункулоподобная, геморрагическая, типа многоформной или узловатой эритемы), лимфаденопатия, мезаденит, увеличение печени и селезенки, энцефалит или менингоэнцефалит, септический эндокардит, язвенный колит, перитонит. Клинические и рентгенологические изменения могут напоминать милиарный туберкулез (при аэрогенном инфицировании).
Хронический диссеминированный гистоплазмоз характеризуется вялым течением, самочувствие больных вначале удовлетворительное, лихорадка не выражена, типично вовлечение в процесс кожи и слизистых оболочек. Образуются характерные язвы на языке, слизистых оболочках глотки и гортани. В дальнейшем состояние ухудшается, появляется лихорадка неправильного типа (септического), наблюдается увеличение печени, селезенки, всех групп лимфатических узлов, поражение желудка, глаз (хорио-ретиниты) и т. д.
Гистоплазмоз у ВИЧ-инфицированных лиц.
Снижение иммунитета существенно повышает риск инфицирования гистоплазмами. Эта проблема особенно актуальна в регионах, эндемичных по гистоплазмозу. По сравнению с аспергиллезом и кандидозом, гистоплазмоз встречается реже (у 0,5% больных СПИДом). В эндемичных районах США этот процент значительно выше. Гистоплазмоз у ВИЧ-инфицированных протекает как гематогенно диссеминированный процесс и характеризуется высокой лихорадкой, лимфаденопатией, значительным увеличением печени и селезенки, постоянными проявлениями служат кашель и инфильтраты в легких. При исследовании крови отмечается лейкопения и анемия. Протекает тяжело, даже в начальных стадиях
При ВИЧ-инфекции летальность свыше 80% (при отсутствии терапии), при раннем назначении противомикозных препаратов летальность снижается до 15%. У больных СПИДом летальность достигает 100%, и даже большие дозы амфотерицина В не предупреждают рецидивов болезни.
Диагностика затрудняется отрицательными результатами как внутрикожной пробы с гистоплазмином, так и серологических реакций. При наличии гистоплазмоза (особенно диссеминированных форм) больной должен обязательно проверяться на ВИЧ-инфекцию.
Диагностика Гистоплазмоза легких:
Распознавание гистоплазмоза представляет значительные трудности, особенно в районах, не эндемичных для данного заболевания. Для подтверждения диагноза используют выделение возбудителя из мокроты, соскобов со слизистой оболочки, из крови, пунктатов абсцессов, лимфатических узлов, печени, селезенки, костного мозга, микроскопию мазка, выделение культуры гриба, биопробы на животных. Для подтверждения диагноза гистоплазмоза у детей раннего возраста и у ВИЧ-инфицированных наиболее информативными оказались выделения культуры из костного мозга, крови и легких. Значительно реже гистоплазмы удавалось обнаружить в тканях лимфатических узлов, кожи, головного мозга, кишечника. При диагностике гистоплазмоза у лиц с нормальной иммунной системой можно использовать серологические реакции и внутрикожную пробу с гистоплазмином. Для обнаружения специфических антител в сыворотке крови ставят РСК, реакции преципитации и агглютинации частиц латекса, нагруженных гистоплазмином. Диагностическими титрами являются 1:16-1:32. Лучше проводить исследование в динамике, особенно при острых формах гистоплазмоза, так как реакция становится положительной лишь со 2-4-й недели болезни. Очень проста кожная проба с гистоплазмином. Вводят 0,1 мл аллергена, разведенного в соотношении 1:1000, результаты учитывают через 24 и 48 ч. Реакция становится положительной через 3-4 нед от начала заболевания. Следовательно, наиболее быстрым и достоверным способом лабораторного подтверждения диагноза является выделение культуры гриба.
Острые формы гистоплазмоза необходимо дифференцировать от орнитоза, острых бактериальных пневмоний, лихорадки Ку, микоплазмоза, туберкулеза. Хронические формы гистоплазмоза дифференцируют от туберкулеза и легочных форм глубоких микозов (нокардиоз, аспергиллез, кокцидиоидомикоз). Диссеминированные формы гистоплазмоза дифференцируют от сепсиса и милиарного туберкулеза.
Лечение Гистоплазмоза легких:
Больные легкой и среднетяжелой формами гистоплазмоза не нуждаются в назначении противомикозных (довольно токсичных) препаратов. Можно ограничиться лечебным режимом, полноценным питанием и симптоматической терапией. При гистоплазмозе глаз показаны местное применение кортикостероидных препаратов, десенсибилизирующая терапия с помощью гистоплазмина, а также фотокоагуляция. Назначают антигистаминные препараты, витамины и другие патогенетические средства.
При лечении гистоплазмоза применяют азоловые препараты (кетоконазол, итраконазол) либо амфотерицин В. Дозы лекарственных препаратов зависят от клинической формы заболевания.
Больные легкой и среднетяжелой формами гистоплазмоза не нуждаются в назначении противомикозных (довольно токсичных) препаратов. Можно ограничиться лечебным режимом, полноценным питанием и симптоматической терапией. При тяжелых формах острого гистоплазмоза назначают амфотерицин В из расчета 1000 ЕД/кг массы тела в сутки. Препарат вводят внутривенно капельно в течение 4 ч в 5% растворе глюкозы. Для определения индивидуальной переносимости первое введение делают из расчета 100 ЕД/кг массы тела. При отсутствии побочных реакций и удовлетворительной переносимости антибиотика вводят препарат из расчета 250 ЕД/кг и затем постепенно повышают дозу до 1000 ЕД/кг. Антибиотик вводят через день или 2 раза в неделю. Продолжительность лечения 4-8 нед. При введении амфотерицина В наблюдаются побочные явления: тромбофлебиты, тошнота, рвота, мышечные боли, судороги, кишечные кровотечения, анемия, токсические поражения почек.
При хронических формах лучшие результаты дает длительное назначение амфотерицина В повторными 6-7-дневными курсами в сочетании с хирургическим лечением.
Можно использовать также амфоглюкамин (Amphoglucaminum) - водорастворимый препарат амфотерицина В, предназначенный для приема внутрь. Он менее токсичен, из побочных реакций отмечается лишь нарушение функций почек. Выпускается в таблетках по 100 000 ЕД (в упаковке 10 или 40 штук). Лечение назначают с 200 000 ЕД 2 раза в сутки после еды. При хорошей переносимости дозу повышают до 500 000 ЕД 2 раза в сутки. Курс лечения 3-4 нед. Следить за состоянием почек! При появлении белка в моче или повышения уровня остаточного азота выше 30 ммоль/л амфоглюкамин отменяют. При гистоплазмозе глаз показаны местное применение кортикостероидных препаратов, десенсибилизирующая терапия с помощью гистоплазмина, а также фотокоагуляция.
Из зарубежных препаратов можно использовать кетоконазол (Ketoconazole). Препарат можно использовать при лечении гистоплазмоза у ВИЧ-инфицированных изолированно или в сочетании с амфотерицином В. Из других препаратов, которые используют при терапии ВИЧ-инфицированных, - флукондзол (fluconazole), который назначают по 50-100 мг в день. Назначают антигистаминные препараты, витамины и другие патогенетические средства.
При бессимптомных формах гистоплазмоза этиотропную терапию не проводят.
Прогноз
При остром гистоплазмозе легких прогноз благоприятный, лишь при относительно редко встречающихся тяжелых формах процесс может переходить в хронический и давать рецидивы. При хроническом легочном гистоплазмозе летальность достигала 60% (без лечения противомикозными антибиотиками). Гистоплазмоз у ВИЧ-инфицированных протекает тяжело и даже при лечении обычно заканчивается гибелью больного.
Профилактика Гистоплазмоза легких:
Специфическая профилактика только еще разрабатывается. Рекомендуется всемерное предотвращение запыления воздуха в местах распространения в почве гистоплазм, предохранение от вдыхания зараженного грибами воздуха в помещениях, на земляных работах, в микологических лабораториях, тщательное обеззараживание воздуха в этих лабораториях. Контроль за растительными материалами, фруктами, овощами, соответствующая обработка запыленных предметов и материалов, прибывших из зон, где распространено это заболевание. Больной гистоплазмозом опасности для других людей не представляет.
К каким докторам следует обращаться если у Вас Гистоплазмоз легких:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Гистоплазмоза легких, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Пневмоцистоз – оппортунистическая инфекция дыхательных путей, чаще поражающая детей раннего возраста, а также лиц с ослабленным иммунитетом. Пневмоцистоз может протекать в форме ОРЗ, ларингита, обструктивного бронхита, обострения ХЗЛ, интерстициальной пневмонии. Диагностика пневмоцистоза основана на обнаружении пневмоцист в мокроте и бронхиальном секрете с помощью микроскопии и ПЦР; данных гистологического исследования биоптатов бронхов; рентгенографии и КТ легких, сцинтиграфии, спирографии. Для проведения противопневмоцистной терапии используются препараты сульфаметоксазол+триметоприм, пентамидин, комбинация триметоприма с дапсоном и другие схемы лечения.
МКБ-10
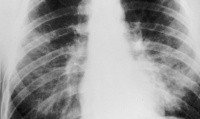
Общие сведения
Пневмоцистоз – легочная инвазия, вызываемая пневмоцистами и протекающая преимущественно в виде пневмоцистной пневмонии. Пневмоцистоз является иммунодефицит-ассоциированным инфекционным заболеванием, которым чаще всего болеют недоношенные дети, а также пациенты с первичными и вторичными иммунодефицитами. Смертельную опасность пневмоцистоз представляет для больных ВИЧ/СПИДом: при отсутствии лечения заболевание неизбежно заканчивается летальным исходом. Пневмоцистоз может возникать как спорадическая или внутрибольничная инфекция в отделениях педиатрии, гемобластозов, пульмонологии, противотуберкулезных инфекционных стационарах.

Причины пневмоцистоза
На сегодняшний день вопрос с видовой принадлежностью возбудителя пневмоцистоза окончательно не решен. В течение длительного времени микроорганизм Pneumocystis Carinii относили к простейшим класса споровиков. Однако в настоящее время доминирует точка зрения, что пневмоцисты занимают промежуточное положение между низшими и высшими грибами. В своем развитии пневмоцисты претерпевают 4 стадии: трофозоита, предцисты, цисты и спорозоита, протекающие на альвеоцитах. При разрыве оболочки созревшей цисты из нее выходят спорозоиты, которые проникают в легочные альвеолы, запуская очередной цикл стадийного развития пневмоцист новой генерации.
Источником эпидемиологической опасности выступает инвазированный человек (больной или носитель), выделяющий спорозоиты с частицами слизи во внешнюю среду при кашле или чихании. Передача возбудителей пневмоцистоза происходит по аспирационному механизму, воздушно-капельным, воздушно-пылевым, ингаляционным или аэрогенным путями. Считается, что среди клинически здоровых лиц до 10% являются носителями пневмоцист, однако у людей с нормально функционирующей иммунной системой инвазия протекает бессимптомно. Риску заболеваемости манифестными формами пневмоцистоза, главным образом, подвержены недоношенные новорожденные; дети с гипогаммаглобулинемией, гипотрофией, рахитом; больные ВИЧ/СПИДом и туберкулезом; пациенты, получающие иммуносупрессивную терапию по поводу коллагенозов, злокачественных новообразований, гематологических и лимфопролиферативных заболеваний, трансплантации органов и пр.
Пневмоцистоз развивается при снижении количества СД4+ клеток (Т-хелперов) в 4 и более раз по сравнению с нормой и достижении уровня менее 200 клеток в 1 мкл. При нарушении клеточного и гуморального иммунитета пневмоцисты начинают активно размножаться в альвеолах, вызывая развитие реактивного альвеолита, образование пенистого альвеолярного экссудата, содержащего пневмоцисты, лейкоциты, клеточный детрит и фибрин. При прогрессировании патологического процесса возникают участки ателектазов в легких, буллезное вздутии легочной ткани, что сопровождается нарушением вентиляции и газообмена, развитием дыхательной недостаточности.
Симптомы пневмоцистоза
В клиническом течении пневмоцистоза выделяют отечную (1-7 недель), ателектатическую (около 4-х недель) и эмфизематозную стадии. У части больных пневмоцистоз может протекать в виде ларингита, обструктивного или астматического бронхита, бронхиолита; в остальных случаях развивается пневмоцистная пневмония.
Инкубационный период пневмоцистоза занимает от 10 дней до 2-5 недель. Проявления отечной стадии развиваются постепенно и на ранних этапах включают в себя субфебрилитет, слабость, вялость. В конце первого периода присоединяется сухой кашель, тахипноэ, одышка. Признаками развивающегося пневмоцистоза у грудных детей может служить вялое сосание, отказ от кормления, плохая прибавка в массе тела, цианоз носогубного треугольника. Рентгенологические изменения в легких в отечной стадии пневмоцистоза отсутствуют; аускультативно определяется жестковатое дыхание, мелко- и среднепузырчатые хрипы; перкуторно - тимпанит в верхних отделах грудной клетки.
В ателектатической стадии пневмоцистоз может осложниться развитием пневмоторакса, экссудативного плеврита, легочного сердца, отека легких, а в случае присоединения бактериальной или грибковой инфекции – абсцессом легких. Летальные исходы в этот период обычно обусловлены дыхательной и сердечной недостаточностью. Третья, эмфизематозная стадия пневмоцистоза характеризуется уменьшением одышки и улучшением общего состояния больных. В исходе пневмоцистоза развивается эмфизема легких, сопровождающаяся значительным снижением показателей функции внешнего дыхания.
Диагностика
Клинические, физикальные и рентгенологические данные при пневмоцистозе не являются патогномоничными, что затрудняет своевременную диагностику заболевания. Между тем, пневмоцистную пневмонию всегда следует исключать у иммунокомпрометированных пациентов. С целью верификации пневмоцистоза проводится комплекс лабораторных и инструментальных исследований.
Для подтверждения диагноза пневмоцистоза выполняется бронхоскопия с забором бронхиального секрета, трансбронхиальная биопсия легкого, сцинтиграфия легких с галлием-67. Для лабораторной детекции P.carinii микроскопически исследуются окрашенные мазки мокроты, бронхиальный и трахеальный аспират; выполняется гистологическое исследование биоптатов, исследование мокроты методом ПЦР. Проводится иммунологическая диагностика: определение титра противопневмоцистных IgG и IgM в сыворотке крови с помощью РИФ и ИФА. Дифференциальную диагностику пневмоцистоза необходимо проводить с цитомегаловирусной, хламидийной, уреаплазменной, бактериальной пневмонией, туберкулезом легких, саркомой Капоши и др.
Лечение пневмоцистоза
Лечение пневмоцистоза проводится в стационаре. Лица с иммунодефицитом и недоношенные дети должны быть помещены в отдельные стерильные палаты с ламинарным воздушным потоком. В большинстве случаев для проведения специфической фармакотерапии пневмоцистоза используется комбинированные препараты (сульфаметоксазол+триметоприм, триметоприм+дапсон), пентамидин, эфлорнитин, атоваквон в течение 2-3 недель. Для устранения побочных эффектов терапии назначают фолиевую кислоту, глюкокортикоиды. Проводится инфузионная терапия (введение гамма-глобулина, солевых растворов, глюкозы, плазмы крови, альбумина и др.), кислородотерапия. У больных ВИЧ-инфекцией этиотропная терапия пневмоцистной пневмонии сочетается с высокоактивной антиретровирусной терапией.
Прогноз
Выживаемость при пневмоцистозе составляет 75-90%, а при повторном развитии пневмоцистной пневмонии – 60%. У 25-60% ВИЧ-инфицированных в течение года отмечаются рецидивы заболевания, поэтому больные нуждаются в проведении противорецидивного курса химиотерапии.
Пневмоцистная пневмония – это тяжелая форма интерстициального легочного воспаления, вызываемая пневмоцистами и развивающаяся на фоне выраженных иммунодефицитных состояний. Клиническое течение характеризуется нарастающей одышкой, непродуктивным кашлем, фебрильной лихорадкой, болями в груди, развитием сердечно-легочной недостаточности. Диагноз ставится на основании рентгенологических признаков, состояния иммунного статуса, лабораторной идентификации патогена в крови, БАЛ, мокроте, биоптате (ПЦР, серологические тесты, РНИФ). Для этиотропной терапии используются сульфаниламидные, противопротозойные, иммуномодулирующие средства.
МКБ-10
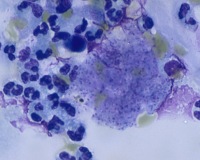


Общие сведения
Пневмоцистная пневмония (ПП) относится к оппортунистическим инфекциям, поражающим лиц с иммунодефицитом и иммуносупрессией. При этом большинство людей с нормальным уровнем иммунитета переносит пневмоцистную инфекцию в виде ОРВИ. Антитела к возбудителю имеют около 90% взрослого населения, около 10% являются бессимптомными носителями пневмоцист – именно они представляют наибольшую угрозу для иммунокомпрометированных пациентов. Пневмоцистная пневмония является самой тяжелой клинической формой пневмоцистоза.

Причины
Характеристика возбудителя
Pneumocystis jirovecii – микроорганизм, вызывающий пневмоцистную пневмонию и другие виды пневмоцистоза у человека. До недавнего времени пневмоцисты считались простейшими, однако в 1988 г. на основании ряда характерных генетических, морфологических и биохимических признаков были отнесены к грибам семейства актиномицетов. Пневмоцисты обладают тропизмом к легочной ткани, весь их жизненный цикл протекает внутри альвеол и проходит 4 стадии:
- Трофозоит. Представляет собой вегетативную стадию P. Jirovecii. Имеет амебоидную форму, диаметр 1-5 мкм, одно ядро и тонкую двухслойную мембрану. Прикрепляется к альвеолоцитам, где увеличивается в размерах и делится.
- Прециста. Имеет овальную форму, диаметр 5 мкм. В ранней стадии содержит одно ядро, окруженное митохондриями, на поздней – 2-6 ядер с мембранами.
- Циста. Зрелая циста округлой формы, с 3-слойной стенкой, диаметром 7-8 мкм. Внутри цисты содержится четное количество (обычно 8 шт.) внутрицистных телец ‒ спорозоитов.
- Спорозоит. При разрыве зрелых цист из них высвобождаются спорозоиты, часть которых обладает одинарным набором хромосом (являются гаплоидными). Сливаясь, они вновь образуют трофозоиты, и жизненный цикл патогена повторяется.
В описанном цикле различают две фазы: неполовую, или асексуальную (деление трофозоита), и половую, или сексуальную (спорозоит-трофозоит-прециста-циста).
Пути передачи
Источниками P. jirovecii являются носители (бессимптомные или больные ОРЗ) и больные пневмоцистной инфекцией. В 30% случаев выявляется вовлеченность в эпидемический процесс медицинских работников. При кашле и чихании носители выделяют мелкодисперсный аэрозоль, содержащий патогены. Заражение восприимчивого макроорганизма происходит при вдыхании контаминированного воздуха (воздушно-капельным, воздушно-пылевым путем). Воротами для входящей инфекции служат дыхательные пути. Редко реализуется трансплацентарный путь передачи.
Характерны внутрисемейные и внутрибольничные эпидемические вспышки пневмоцистной пневмонии. Последние чаще происходят в отделениях недоношенных, домах престарелых, инфекционных стационарах. Пик детской заболеваемости пневмоцистной пневмонией приходится на конец лета – начало осени, взрослые болеют круглогодично.
Группы риска
Пневмоцисты являются типичными оппортунистами, поскольку вызывают манифестную инфекцию только при выраженном дефиците клеточного и гуморального иммунитета у определенного контингента пациентов. К группам риска по заболеваемости пневмоцистной пневмонией относятся:
- ВИЧ-инфицированные и больные СПИДом;
- пациенты с ЦМВ-инфекцией;
- недоношенные дети и младенцы с ЗВУР;
- дети, страдающие гипотрофией, рахитом;
- больные, получающие иммуносупрессивную терапию (по поводу лейкозов, миеломной болезни, других видов рака, трансплантации органов, коллагенозов);
- пациенты с первичными иммунодефицитами, болезнями крови (анемией, полицитемией), туберкулезом, патологией почек.

Патогенез
Пневмоцисты присутствуют в дыхательных путях здоровых людей, но вызывают пневмоцистную пневмонию только у лиц с нарушением гуморального и клеточного звена иммунитета. Экспериментально доказано, что ведущую роль в механизме пневмоцистоза играет снижение Т-хелперов (критическим является снижение СД4+ лимфоцитов ˂300-200 клеток/мкл), увеличение количества цитотоксических лимфоцитов СД8+.
P. Jirovecii с помощью особых выростов – филоподий – прикрепляется к альвеолоцитам первого порядка и альвеолярным макрофагам. Клеточной адгезии также способствуют гликопротеины пневмоцистов, которые взаимодействуют с фосфолипидами, апопротеинами, мукополисахаридами, сурфактантом альвеолярного эпителия. В условиях иммунокомпрометации цисты размножаются, используя сурфактант-ассоциированные белки, выделяют токсические метаболиты.
Происходит разрушение альвеолоцитов, заполнение альвеол пенистым экссудатом, содержащим большое количество пневмоцист на разных стадиях развития, воспалительные клетки, детрит. Интерстициальная ткань инфильтрируется плазматическими клетками. Развивается интерстициальная плазмоклеточная пневмония. Межальвеолярные перегородки гипертрофируются, что приводит к резкому снижению диффузии газов (альвеолярно-капиллярный блок), формированию дыхательной недостаточности и тяжелой гипоксии.
Классификация
В соответствии с патоморфологическими критериями в современной пульмонологии выделяют три стадии пневмоцистной пневмонии:
- I стадия. Происходит прикрепление пневмоцист к альвеолярной стенке. Воспалительная реакция и клинические проявления отсутствуют.
- II стадия. Отмечается десквамация альвеолоцитов, увеличение числа возбудителей в форме цист в макрофагах. В эту стадию появляются начальные клинические проявления пневмоцистной пневмонии.
- III стадия. Развивается альвеолит, плазмоцитарная инфильтрация интерстиция, гигантские скопления пневмоцист в макрофагах и альвеолах. Соответствует разгару заболевания.
Этапы развития пневмоцистной пневмонии:
- отечная фаза ‒ длится 7-10 дней, характеризуется нарастанием симптоматики;
- ателектатическая фаза ‒ продолжается в течение 4-х недель, сопровождается выраженной легочной недостаточностью;
- эмфизематозная фаза – имеет различную длительность, знаменуется обратным развитием симптоматики.
Симптомы пневмоцистной пневмонии
Инкубационный период вариабелен – от 7-10 дней до 2-4 недель (у больных СПИДом – до 10 недель). В отечную стадию клинические признаки пневмоцистной пневмонии легко спутать с обычной респираторной инфекцией. Симптомы нарастают постепенно: вначале беспокоит слабость, недомогание, субфебрилитет. Затем появляется одышка при умеренной нагрузке, боли в грудной клетке, сухой кашель.
В ателектатической стадии лихорадка принимает фебрильный характер, усиливается интоксикационный синдром (отсутствие аппетита, снижение веса, потливость по ночам). Кашель становится коклюшеподобным, постоянным, особенно беспокоит в ночное время суток. Одышка до 30-50 дыхательных движений в минуту выражена в покое. Отмечаются бледность кожных покровов с носогубным цианозом, тахикардия. В этот период пациент может погибнуть от сердечно-легочной недостаточности (СЛН).
У выживших пациентов наступает эмфизематозная стадия. Температура тела снижается, дыхательные расстройства исчезают. В исходе пневмоцистной пневмонии формируется эмфизема легких, легочное сердце. Пневмоцистная пневмония часто протекает в ассоциации с туберкулезом легких.
Четкая стадийность при пневмоцистозе прослеживается в основном у детей раннего возраста. У ВИЧ-инфицированных болезнь имеет стертое затяжное течение, у ВИЧ-негативных лиц с иммунодефицитом – более активное, с быстрым нарастанием СЛН.
Осложнения
Типичными осложнениями, развивающимися в разгар болезни, являются пневмоторакс, подкожная эмфизема, пневмомедиастинум, возникающие вследствие разрыва мелких кистозных образований. Возможно развитие абсцедирующей пневмонии. Эти состояния еще более усугубляют дыхательную недостаточность, повышают летальность. При значительном подавлении иммунитета может произойти генерализация пневмоцистной инфекции с мультиорганным поражением печени, селезенки, ЖКТ, щитовидной железы, органов зрения и слуха, лимфоузлов, костного мозга.

Диагностика
Из-за неспецифичности и стертости симптоматики существенной проблемой является гиподиагностика пневмоцистной пневмонии. Иногда патология диагностируется только посмертно. Все больные с подозрением на ПП должны быть в срочном порядке проконсультированы врачом-пульмонологом, инфекционистом. При выставлении диагноза опираются на следующие данные:
Дифференциальная диагностика
Комплексное клинико-лабораторное, рентгенологическое и бронхологическое обследование позволяет отличить пневмоцистную пневмонию от других поражений легких:
- легочного кандидоза;
- криптококковой пневмонии;
- цитомегаловирусной пневмонии;
- микоплазменной пневмонии;
- хламидийной пневмонии;
- туберкулеза легких;
- респираторного криптоспоридиоза;
- саркомы Капоши;
- бактериальной пневмонии.
Лечение пневмоцистной пневмонии
Стандартные антибактериальные средства при ПП неэффективны. В настоящее время препаратами первой линии считаются комбинированные сульфаниламиды, оказывающие противомикробное, бактерицидное и противопротозойное действие. Могут назначаться как перорально, так и внутривенно. Курс лечения составляет 1-3 недели.
При выраженных токсических эффектах и резистентности подбираются другие антибиотики, активные в отношении пневмоцист (линкозамиды, противолепрозные, противомалярийные, антипротозойные препараты). Из-за массовой гибели патогенов в первые дни терапии состояние пациентов с пневмоцистной пневмонией может ухудшиться, в связи с чем целесообразно назначение кортикостероидов.
Прогноз и профилактика
Смертность от пневмоцистной пневмонии достигает 50% среди недоношенных детей, 25-40% ‒ среди больных СПИДом. У 10-30% иммунокомпрометированных пациентов через несколько месяцев после излечения возникают рецидивы ПП. При отсутствии лечения летальность 100%.
Профилактическая работа реализуется в двух направлениях: эпидемиологическом и медикаментозном. Первый аспект предполагает широкое тестирование на пневмоцистную инфекцию представителей групп риска: пациентов с ВИЧ, онкопатологией, иммунодефицитами, недоношенных детей, сотрудников роддомов и стационаров. Второе направление – это фармакопрофилактика пневмоцистной пневмонии у лиц с количеством СД4+ клеток ˂200. Она заключается в приеме сульфаниламидов в профилактических дозах длительными курсами.
1. Пневмоцистная пневмония. Этиология, патогенез, клиника, дифференциальная диагностика, лечение (лекция)/ Боровицкий В.С.// Проблемы медицинской микологии. – 2012.
2. Пневмоцистная пневмония: исторические, эпидемиологические, клинико-морфологические аспекты/ Марковский В. Д., Плитень О. Н., Мирошниченко М. С., Мирошниченко А. А.// Annals of Mechnikov Institute, - 2012. - №3.
3. Особенности пневмоцистной пневмонии у ВИЧ-инфицированных лиц/ Пузырёва Л.В., Сафонов А.Д., Мордык А.В.// Медицинский вестник Северного Кавказа. – 2016. – Т.11, №3.
4. Пневмоцистоз. Современное состояние проблемы/ Каражас Н.В.// Альманах клинической медицины. – 2010.
Пневмосклероз – патологическое замещение легочной ткани соединительной, как следствие воспалительных или дистрофических процессов в легких, сопровождающееся нарушением эластичности и газообмена в пораженных участках. Локальные изменения протекают бессимптомно, диффузные – сопровождаются прогрессирующей одышкой, кашлем, болями в груди, быстрой утомляемостью. Для выявления и оценки поражения применяется рентгенография и компьютерная/мультиспиральная КТ легких, спирография, биопсия легкого с морфологической верификацией диагноза. В лечении пневмосклероза используются ГКС, цитостатики, антифибротические препараты, кислородотерапия, дыхательная гимнастика; при необходимости ставится вопрос о трансплантации легких.
МКБ-10
Общие сведения
Пневмосклероз – патологический процесс, характеризующийся замещением легочной паренхимы нефункционирующей соединительной тканью. Пневмофиброз обычно развивается в исходе воспалительных или дистрофических процессов в легких. Разрастание в легких соединительной ткани вызывает деформацию бронхов, резкое уплотнение и сморщивание легочной ткани. Легкие становятся безвоздушными и уменьшаются в размерах. Пневмосклероз может развиваться в любом возрасте, чаще эта патология легких наблюдается у мужчин старше 50 лет. Поскольку склеротические изменения в легочной ткани необратимы, заболевание носит неуклонно прогрессирующее течение, может привести к глубокой инвалидности и даже смерти пациента.
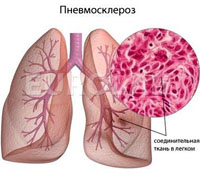
Классификация пневмосклероза
По степени выраженности замещения легочной паренхимы соединительной тканью выделяют:
- пневмофиброз - тяжистые ограниченные изменения паренхимы легких, чередующиеся с воздушной легочной тканью;
- пневмосклероз (собственно пневмосклероз) – уплотнение и замещение паренхимы легких соединительной тканью;
- пневмоцирроз – крайний случай пневмосклероза, характеризующийся полным замещением альвеол, сосудов и бронхов соединительной тканью, уплотнением плевры, смещением в пораженную сторону органов средостения.
По распространенности в легких пневмосклероз может быть ограниченным (локальным, очаговым) и диффузным. Ограниченный пневмосклероз бывает мелко- и крупноочаговым. Ограниченный пневмосклероз макроскопически представляет участок уплотненной легочной паренхимы с уменьшением объема этой части легкого. Особой формой очагового пневмосклероза является карнификация (постпневмонический склероз, при котором в очаге воспаления легочная ткань по виду и консистенции напоминает сырое мясо). При микроскопическом исследовании в легком могут определяться склерозированные нагноительные очаги, фиброателектаз, фибринозный экссудат и т. д.
Диффузный пневмосклероз поражает целое легкое, а иногда оба легких. Легочная ткань уплотнена, объем легких уменьшен, их нормальная структура утрачена. Ограниченный пневмосклероз не оказывает существенного влияния на газообменную функцию и эластичность легких. При диффузном поражении легких пневмосклерозом наблюдается картина ригидного легкого и снижения его вентиляции.
По преимущественному поражению тех или иных структур легких различают альвеолярный, интерстициальный, периваскулярный, перилобулярвый и перибронхиальный пневмосклероз. По этиологическим факторам выделяют постнекротический, дисциркуляторный пневмосклерозы, а также склероз легочной ткани, развившийся вследствие воспалительных и дистрофических процессов.
Причины и механизм развития пневмосклероза
Обычно пневмосклероз сопровождает течение или служит исходом некоторых заболеваний легких:
- неразрешившихся инфекционных, вирусных и аспирационных пневмоний, туберкулеза, микозов;
- ХОБЛ, хронического бронхита и перибронхита;
- ателектаза легкого, длительных массивных плевритов;
- пневмокониозов, вызванных вдыханием промышленных газов и пыли, лучевых поражений;
- альвеолитов (фиброзирующего, аллергического);
- саркоидоза легких;
- инородных тел бронхов;
- травм и ранений грудной клетки и легочной паренхимы;
- наследственных заболеваний легких.
К развитию пневмосклероза может приводить недостаточный объем и эффективность противовоспалительной терапии данных заболеваний.
Также пневмосклероз может развиваться в результате гемодинамических нарушений в системе малого круга кровообращения (как следствие митрального стеноза, левожелудочковой сердечной недостаточности, тромбоэмболии легочной артерии), в результате ионизирующего излучения, приема токсических пневмотропных лекарственных средств, у пациентов со сниженной иммунной реактивностью.
Постпневмонический пневмосклероз развивается в результате неполного разрешения воспаления в легких, приводящего к разрастанию соединительной рубцовой ткани и облитерации просвета альвеол. Особенно часто пневмосклероз возникает после стафилококковых пневмоний, сопровождающихся образованием некроза легочной паренхимы и формированием абсцесса, заживление которого сопровождается разрастанием фиброзной ткани. Посттуберкулезный пневмосклероз характеризуется разрастанием в легких соединительной ткани и развитием околорубцовой эмфиземы.
Механизмы развития и формы пневмосклероза обусловлены его причинами. Однако, общими для всех этиологических форм пневмосклероза служат нарушения вентиляционной функции легких, дренажной способности бронхов, циркуляции крови и лимфы в легких. Нарушение строения и деструкция альвеол ведет к замещению морфофункциональных структур легочной паренхимы соединительной тканью. Нарушение лимфо- и кровообращения, сопровождающие бронхолегочную и сосудистую патологию, также способствуют возникновению пневмосклероза.
Симптомы пневмосклероза
Ограниченный пневмосклероз обычно не беспокоит пациентов, иногда отмечается незначительный кашель со скудной мокротой. При осмотре на стороне поражения может обнаруживаться западение грудной клетки.
Диффузный пневмосклероз симптоматически проявляется одышкой - на первых порах при физической нагрузке, а в дальнейшем – в покое. Кожные покровы с цианотичным оттенком вследствие снижения вентиляции альвеолярной ткани легких. Характерным признаком дыхательной недостаточности при пневмосклерозе служит симптом пальцев Гиппократа (в форме барабанных палочек). Диффузный пневмосклероз сопровождается явлениями хронического бронхита. Пациентов беспокоит кашель – сначала редкий, затем навязчивый с выделением гнойной мокроты. Утяжеляет течение пневмосклероза основное заболевание: бронхоэктатическая болезнь, хроническая пневмония. Возможны ноющие боли в груди, слабость, похудание, повышенная утомляемость.
Нередко появляются признаки цирроза легкого: грубая деформация грудной клетки, атрофия межреберных мышц, смещение сердца, крупных сосудов и трахеи в сторону поражения. При диффузных формах пневмосклероза развивается гипертензия малого круга кровообращения и симптомы легочного сердца. Тяжесть течения пневмосклероза определяется объемом пораженной легочной ткани.
Морфологические изменения альвеол, бронхов и сосудов при пневмосклерозе ведут к нарушениям вентиляционной функции легких, артериальной гипоксемии, редукции сосудистого русла и осложняются развитием легочного сердца, хронической дыхательной недостаточностью, присоединением воспалительных заболеваний легких. Постоянным спутником пневмосклероза служит эмфизема легких.
Диагностика пневмосклероза
Физикальные данные при пневмосклерозе зависят от локализации патологических изменений. Над зоной поражения или диффузно выслушивается резко ослабленное дыхание, влажные и сухие хрипы, перкуторный звук – тупой.
Достоверно выявить пневмосклероз позволяет рентгенография легких. С помощью рентгенографии обнаруживаются изменения в легочной ткани при бессимптомном течении пневмосклероза, их распространенность, характер и степень выраженности. Для детализации состояния пораженных пневмосклерозом участков проводят бронхографию, КТ легких и МРТ.
При проведении бронхоскопии нередко выявляются бронхоэктазы, признаки хронического бронхита. Анализ клеточного состава смыва с бронхов позволяет уточнить этиологию и степень активности патологических процессов в бронхах. При исследовании функции внешнего дыхания (спирометрия, пикфлоуметрия) выявляются снижение жизненной емкости легких и показателя проходимости бронхов (индекса Тиффно). Изменения крови при пневмосклерозе неспецифичны.
Лечение пневмосклероза
Лечение пневмосклероза проводит пульмонолог или терапевт. Острый воспалительный процесс в легких или развитие осложнений могут стать показанием к стационарному лечению в отделении пульмонологии. В терапии пневмосклероза основной упор делается на устранение этиологического фактора.
Ограниченные формы пневмосклероза, не проявляющие себя клинически, не требуют активной терапии. Если пневмосклероз протекает с обострениями воспалительного процесса (частыми пневмониями и бронхитами), назначают антимикробные, отхаркивающие, муколитические, бронхолитические средства, проводят лечебные бронхоскопии для улучшения дренажа бронхиального дерева (бронхоальвеолярный лаваж). При явлениях сердечной недостаточности применяют сердечные гликозиды и препараты калия, при наличии аллергического компонента и диффузного пневмосклероза – глюкокортикоиды.
Хорошие результаты при пневмосклерозе дает использование лечебно-физкультурного комплекса, массажа грудной клетки, оксигенотерапии и физиотерапии. Ограниченные пневмосклерозы, фиброзы и циррозы, деструкция и нагноение легочной ткани требуют хирургического лечения (резекция пораженной части легкого). Новой методикой в лечении пневмосклероза является использование стволовых клеток, позволяющих восстанавливать нормальную структуру легких и их газообменную функцию. При грубых диффузных изменениях единственным методом лечения становится трансплантация легких.
Прогноз и профилактика пневмосклероза
Меры профилактики пневмосклероза предусматривают предупреждение заболеваний органов дыхания, своевременное лечение простудных заболеваний, инфекций, бронхитов, пневмоний, туберкулеза легких. Необходимо также соблюдение предосторожности при взаимодействии с пневмотоксичными веществами, приеме пневмотоксичных препаратов. На вредных производствах, связанных с вдыханием газов и пыли, необходимо использование респираторов, установка вытяжной вентиляции в шахтах и на рабочих местах резчиков по стеклу, шлифовальщиков и др. При выявлении у работника признаков пневмосклероза необходим перевод на другое место работы, не связанное с контактом с пневмотоксичными веществами. Улучшают состояние пациентов с пневмосклерозом прекращение курения, закаливание, легкие физические упражнения.
1. Механизмы формирования пневмосклероза при хроническом эндотоксикозе: Автореферат диссертации/Ахмад, М.А. Итмези – 2006.
Пневмоцистоз - оппортунистическая инфекция с преимущественным поражением легких, у больных с иммунодефицитом способная к генерализации. Относится к числу наиболее распространенных СПИД-индикаторных болезней.
Возбудитель пневмоцистоза - Pneumocystis carina (Delanoe M., Delanoe P., 1912) - одноклеточный микроорганизм. По морфологическим признакам и чувствительности к антипротозойным препаратам их длительное время относили к типу простейших. Постепенно у пневмоцист начали выявлять черты, характерные для грибов. Попытки отнести их к грибам или простейшим наталкивались на нечеткость систематических критериев. По некоторым показателям они близки к Protozoa: по морфологии, наличию мейоза, присутствию в составе клеточной оболочки холестерола (а не эргостерола, как у грибов, что делает их чувствительными к антипаразитарным препаратам и нечувствительными к противогрибковому средству амфотерицину В), невозможности их культивирования на питательных средах для грибов. С грибами их сближает то, что пневмоцисты содержат структуры, подобные аскоспорам у грибов, а также фитостеролы, которых лишены животные клетки.
Метаболизм у P. carinii (синтез ароматических аминокислот, тимидина и др.) происходит, как у грибов; кроме того, у пневмоцист отсутствует спорогония, характерная для простейших. В 1988 г. Edman и Stringer, применив методы молекулярной генетики, показали, что последовательность нуклеотидов в т-РНК пневмоцист имеет высоую степень гомологии с последовательностью нуклеотидов т-РНК грибов, относящихся к дрожжам ( Saccharomycetes serevisiae). Для сравненения - аналогичные последовательности изучались также у разных видов простейших: токсоплазм, плазмодиев, акантамеб и др. По генетическим признакам пневмоцисты были ближе всего к грибам. Но это грибы, которые имеют ряд черт, сближающих их с простейшими. Так, м-ДНК P. carinii содержит гены дегидрогеназы и цитохромоксидазы, которые на 60% подобны генам грибов и только на 20% генам простейших. Аналогичные свойства были установлены и у других видое грибов.
По последним данным пневмоцисты относят к грибам возможно, к актиномицетам или высшим грибам - аско- или базидомицетам. Одновременно некоторые исследователи считают P. carinii филогенетически древним возбудителем неопределенного систематического положения, который в процессе эволюции утратил характерные таксономические признаки (Т. В. Бейер, 1989 г.). Современный молекулярно-биологический и молекулярно-генетический анализ не может окончательно определить их видовую принадлежность. Для решения этого вопроса необходимо ультраструктурное исследование возбудителя, изучение его филогенеза и усовершенствование техники культивирования пневмоцист.
P. carinii - внеклеточный паразит, тропный к легочной ткани. В цикле развития пневмоцисты выделяют вегетативную форму (трофозоит), предцисту и цисту с внутрицистными тельцами.
Трофозоиты - клетки размером 1-8 мкм, покрытые тонкой оболочкой. Их форма разнообразная и мобильная (овальная, амебоподобная и др.). Она зависит от формы структур, к которым они прилегают. От поверхности трофозоита отходят микровыросты и длинные отростки в виде филоподий. За их счет пневмоцисты соединяются между собой и прикрепляются к клеткам хозяина. Ядро ограничено двумя мембранами. В цитоплазме выявляются митохондрии, свободные рибосомы, мелкие и крупные вакуоли, полисахариды, капли липидов. Иногда встречаются сдвоенные клетки, что может свидетельствовать о делении или копуляции. По данным электронно-микроскопических исследований, трофозоиты плотно прилегают к альвеолоцитам первого порядка. Филоподий могут углубляться в клетку легкого хозяина, не разрывая ее оболочку. Одновременно мембрана альвеолоцита может входить в тело трофозоита, не повреждая его. Физиологический контакт возбудителя с хозяином осуществляется через систему микропиноцитарных пузырьков.
Предцисты - овальные клетки диаметром 2-5 мкм, лишенные пелликулярных выростов. В них происходит деление ядер. Цисты P. carinii округлой или овальной формы размером 3,5 - 10 мкм, иногда до 30 мкм (рис. 20). Они покрыты плотной трехслойной оболочкой и внешней мембраной. В цитоплазме содержится от 1 до 8 внутрицистных телец, которые выходят в просвет альвеолы после разрыва оболочки цисты. Пустые цисты имеют неправильную форму, чаще в виде полумесяца, иногда в них выявляются внутрицистные тельца. Размер последних 1-2 мкм. Пелликула внутрицистных телец вновь образуется после выхода из разрушенной цисты. Они становятся внеклеточными трофозоитами и начинают новый раунд жизненного цикла.
Патогенез пневмоцистоза определяется биологическими свойствами возбудителя и состоянием иммунной системы хозяина. Пропагативные формы пневмоцист, которые до настоящего времени не описаны, минуют верхние дыхательные пути, достигают альвеол и начинают жизненный цикл в организме нового хозяина. Прикрепление трофозоитов к альвеолоцитам первого порядка опосредуется многими механизмами, в частности большим количеством поверхностных гликопротеинов у P. carinii, которые взаимодействуют с протеинами легочной ткани через маннозные рецепторы на клетках хозяина, особенно макрофагах. Поверхностные гликопротеины пневмоцист высоко иммунногенные. Прикрепление пневмоцист сопровождается пролиферацией возбудителя, его взаимодействием с сурфактантом, освобождением токсических метаболитов. Защиту организма хозяина от P. carinii осуществляют Т-лимфоциты, альвеолярные макрофаги, специфические AT. Взаимодействие микро- и макроорганизма остается на субклиническом уровне, пока иммунная система не нарушена. Компроментация иммунной системы стимулирует рост численности пневмоцист.
При СПИДе число паразитов в альвеолах и бронхах настолько большое, что нарушается альвеолярная вентиляция, и больной умирает от нарастающей легочной недостаточности. Разрушение альвеолярно-капиллярной мембраны может приводить к диссеминации пневмоцист с основного места локализации.
На гистологических срезах легких, пораженных пневмоцистами, возникает картина, характерная только для пневмоцистоза. Расширенные бронхиолы, альвеолы и мелкие бронхи заполнены эозинофильной пенистой массой. Альвеолярный эпителий, контактирующий с возбудителем, гипертрофирован, стенки альвеол утолщены за счет расширения капилляров и инфильтрации лимфоидно-гистиоцитарными элементами. Вокруг сосудов наблюдаются обильные скопления плазмоцитов. На стенках бронхов и альвеол видны отдельные круглые формы и пласты пневмоцист, стелящиеся по стенкам альвеол. Выявляются разорванные цисты P. carinii с выбросом в окружающее пространство внутрицистных телец, которые наращивают цитоплазму и превращаются в трофозоиты, а потом дозревают до цист. Гистологическая картина легких напоминает альвеолярный липопротеиноз с явлениями экссудации, лейкоцитоза и сетчатого склероза. Заполненные пенистой массой группы альвеол и альвеолярные ходы чередуются с участками компресионного ателектаза и эмфиземы.
Для построения собственной клеточной оболочки P. carinii использует фосфолипиды (ненасыщенный фосфатидилхолин) сурфактанта хозяина. Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта. Выраженное размножение и созревание P. carinii прямо коррелирует с пиком активности сурфактантной системы. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Механическое разрушение и инактивация сурфактанта белками экссудата усугубляют гипоксическое состояние тканей, активируют фиброзирование межальвеолярных перегородок. Происходит снижение секреторной функции альвеолоцитов второго порядка и возрастание их пролиферативной активности. Плоский альвеолярный эпителий замещается кубическим. У больных СПИДом размножение в альвеолах P.carinii часто происходит в составе смешанной инфекции (бактериальная флора, грибы). Это создает патоморфологическую картину пневмоцистоза.
После проведенного лечения и выздоровления полного восстановления сурфактантной системы легких не происходит. Это является причиной колонизации дыхательной системы больных СПИДом нозокомиальными, стойкими к антибиотикам широкого спектра действия штаммами микроорганизмов. Поэтому рецидивирующие пневмонии у больных СПИДом - нередкое явление.
Читайте также:

