Почему нельзя принимать лактобактерии при кандидозе
Обновлено: 12.05.2024
Проблема вагинальных инфекций знакома практически каждой женщине. Одно из первых мест в структуре заболеваний женских половых органов в настоящее время занимает бактериальный вагиноз, который, по данным литературы, диагностируется у 30–57,6% женщин репродуктивного возраста [1].
Особое коварство данного патологического процесса состоит в том, что он может спровоцировать различные осложнения при планировании ребенка и во время беременности, да и просто причиняет женщине ежедневные бытовые неудобства. Поэтому вопрос эффективного лечения данной патологии весьма актуален. Сегодня на рынке представлен широкий спектр препаратов для лечения вагинальных инфекций. Но далеко не все из них одинаково эффективны [3].
В терапии вагинальных инфекций традиционно применяют две группы препаратов: антибактериальные и антисептические. Антибиотики влияют только на бактерии, не включая вирусы (герпес, вирус папилломы человека) и других представителей патогенной флоры. К тому же антибиотики не создают условий для развития лактобактерий – типичных представителей нормального биоценоза влагалища (рис. 1). Кроме того, залогом успешного лечения является нормализация pH среды влагалища.
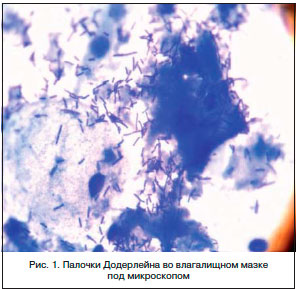
Бетадин ® выпускается в виде вагинальных свечей и содержит 200 мг поливинилпирролидона йода, который давно известен своим бактерицидным действием. Высвобождаясь из комплекса с поливинилпирролидоном при контакте с кожей и слизистыми, йод образует с белками клетки бактерий йодамины, коагулирует их и вызывает гибель микроорганизмов. Оказывает бактерицидное действие на грамположительные и грамотрицательные бактерии (за исключением Mycobacterium tuberculosis), анаэробы. Также активен в отношении грибов, вирусов, простейших. Суппозитории изготовлены на водорастворимой основе и при соприкосновении с кожей и слизистыми не оказывают раздражающего действия. Кроме того, находящийся в комплексе с поливинилпирролидоном йод высвобождается постепенно и равномерно.
По сравнению с другими антисептиками Бетадин ® обладает рядом существенных преимуществ:
- эффективнее подавляет размножение микроорганизмов даже в большом разведении;
- физико-химические условия в очаге воспаления мало влияют на действие препарата Бетадин ® ;
- активен в отношении вирусов герпеса и папилломавирусной инфекции;
- нормализует кислотность вагинальной среды и создает условия для быстрого восстановления нормальной микрофлоры влагалища, что является важным фактором для отсутствия рецидивов вагинальной инфекции после лечения.
Препарат отлично зарекомендовал себя в лечении и профилактике инфекций женской половой сферы. Причем начать лечение можно сразу после визита к врачу, не дожидаясь результатов анализов, т. к. Бетадин ® эффективен практически при всех вагинальных инфекциях. А в повседневной жизни женщины препарат обеспечивает профилактику инфекций, передающихся половым путем.
Более того, данный препарат достаточно удобен, поскольку его можно использовать и во время менструации, и в первом триместре беременности, когда лечение воспалений приобретает особую актуальность.
С целью оценки эффективности и переносимости препарата Бетадин ® при лечении бактериального вагиноза нами было проведено специальное исследование.
Бактериальный вагиноз (другие названия: вагинальный дисбиоз (дисбактериоз)) – это инфекционный невоспалительный синдром, характеризующийся резким снижением или отсутствием лактофлоры и ее заменой на полимикробные ассоциации анаэробов и Gardnerella vaginalis (рис. 2), концентрация которых достигает 109–1011 КОЕ/мл вагинального отделяемого [1, 2, 4].
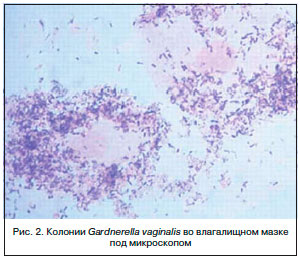
Особенностью микрофлоры влагалища является ее изменчивость под действием как экзогенных, так и эндогенных факторов. На микроценоз оказывают влияние физиологические и гормональные изменения (пубертатный период, беременность, менопауза), фазы менструального цикла, различные нарушения менструальной функции, снижение активности иммунных факторов вследствие перенесенных заболеваний, нерегулярного и несбалансированного питания, дисбактериоза кишечника, гиповитаминоза, хронического стресса. Большое значение имеют степень половой активности, использование антибактериальных препаратов, гормонотерапия, хирургические вмешательства. При бактериальном вагинозе, развившемся в результате действия одного или сочетания перечисленных факторов, происходит элиминация лактобацилл, сопровождающаяся колонизацией влагалища строгими анаэробами: Fusobacterium, Mobiluncus, Peptostreptococcus и Gardnerella vaginalis [3, 5].
Факторами риска развития бактериального вагиноза являются:
- ранее перенесенные заболевания половых органов инфекционно-воспалительного характера;
- длительный и бесконтрольный прием антибактериальных препаратов;
- наличие различных нарушений менструального цикла;
- наличие фоновых процессов шейки матки;
- длительное применение внутриматочной контрацепции;
- применение комбинированных оральных контрацептивов.
Нами были обследованы 142 пациентки в возрасте от 18 до 47 лет с клиническими признаками бактериального вагиноза. Диагноз был установлен при помощи микроскопии влагалищных мазков, бактериологического исследования цервикальной слизи, определения количества лактобактерий, обследования на инфекции, передающиеся половым путем, методами полимеразной цепной реакции (ПЦР), реакции иммунной флюоресценции (РИФ).
В качестве основного симптома при бактериальном вагинозе выступали обильные выделения из половых путей белого или серого цвета (93%), иногда пенящиеся (38%), часто с неприятным запахом (76%). Выделения усиливались перед менструацией или после полового акта. Пациентки с длительным существованием процесса (16%) отмечали желто-зеленую окраску влагалищных выделений, а также их густую, тягучую, липкую консистенцию. При осмотре в зеркалах выделения равномерно распределялись по стенкам влагалища и влагалищной части шейки матки и легко удалялись со слизистой марлевым тампоном.
Другие жалобы – на зуд (46%), нарушения мочеиспускания (18%), боли во время полового акта (7%) – встречались гораздо реже. У 14% женщин с бактериальным вагинозом жалобы отсутствовали. Диагноз у последних был поставлен на основании данных микроскопии влагалищных мазков и результатов бактериологического исследования цервикальной слизи.
Таким образом, в зависимости от наличия жалоб бактериальный вагиноз подразделяется на два варианта: бессимптомный и с клиническими проявлениями.
- При бессимптомном течении заболевания отмечается отсутствие клинических проявлений наряду с положительными результатами лабораторных анализов.
- При варианте с выраженными клиническими проявлениями отмечаются длительно существующие (в течение 2–3 лет) выделения – обильные, жидкие, белого или сероватого цвета, с неприятным запахом гнилой рыбы. Характерно частое сочетание с патологическими процессами шейки матки (псевдоэрозией, лейкоплакией, эндоцервицитом, эндометриозом) и рецидивирующее течение. Нередко возникают нарушения менструального цикла по типу олигоменореи или неполноценной второй фазы цикла.
Лечение бактериального вагиноза проводится в два этапа и сводится к:
- селективной деконтаминации (выборочное устранение возбудителей заболевания), для чего назначаются препараты с антимикробным действием, направленные на снижение количества анаэробных микроорганизмов;
- восстановлению нормального или максимально приближенного к норме микробиоценоза влагалища с помощью эубиотиков. Микробиоценоз – микроорганизмы и продукты их жизнедеятельности, которые в нормальном состоянии находятся на слизистых влагалища [6].
Лечение бактериального вагиноза в настоящем наблюдении проводилось согласно протоколу, представленному фармацевтической компанией Egis. Всем пациенткам назначался Бетадин ® по 1 свече в сутки во влагалище в течение 14 дней. Эффективность терапии оценивали на основании клинических данных и результатов лабораторных исследований.
До лечения при микроскопии влагалищного мазка количество лейкоцитов колебалось от 8 до 22 в поле зрения, что соответствовало второй (43%) и третьей (57%) степени чистоты влагалищного содержимого. На этом фоне в бактериальных посевах у 37% женщин была выявлена Candida albicans, у 19% – Staphylococcus epidermidis в концентрации 106 КОЕ, у 17% – Enterococcus fecalis и у 23% – Staphylococcus saprophyticus (104 КОЕ). В 67% наблюдений в большом количестве были выявлены ключевые клетки (гарднереллы), в 11% определялись условно-патогенные штаммы уреаплазмы, а в 6% – микоплазмы, выявленные методами ПЦР и РИФ. Лактобактерии отсутствовали у 27%, в концентрации 102 КОЕ обнаружены у 22%, 103 КОЕ – у 36%, 104 КОЕ – у 13% и только у 2% пациенток лактобактерии были выявлены в концентрации 105 КОЕ.
После проведенного лечения при первом и втором контрольных обследованиях методом РИФ мы не выявили условно-патогенные микроорганизмы.
После проведенной терапии уже на втором визите жалоб не предъявляла ни одна пациентка. Анализ лабораторных данных показал, что через 1 нед. после проведенной терапии только у 2 пациенток был высеян Staphylococcus epidermidis, а при втором контрольном визите у всех женщин отсутствовала условно-патогенная флора и был отмечен рост титра лактобактерий.
После курса лечения препаратом Бетадин ® проводили терапию эубиотиками, на фоне которых нормализовался биоценоз влагалища, титр лактобактерий при повторном исследовании был в пределах нормы.
Через 4 нед. после проведенной терапии у 96% пациенток пейзаж влагалищного мазка нормализовался: количество лейкоцитов было 2–6 в поле зрения. В бактериальных посевах после лечения условно-патогенная флора не выявлялась.
До лечения ни в одном наблюдении не был выявлен нормальный титр лактобактерий. Независимо от схемы лечения, с применением эубиотиков или без них, при контрольном исследовании у 69% женщин титр лактобактерий был в пределах нормы.
Через 1 мес. после терапии жалобы на умеренные выделения из половых путей, не сопровождавшиеся зудом и неприятным запахом, предъявляли лишь 5% женщин. Кроме того, в процессе терапии препаратом Бетадин ® пациентки в подавляющем большинстве наблюдений не отмечали каких-либо побочных реакций, связанных с применением свечей, в виде неприятных ощущений в области наружных половых органов и влагалища (жжения, зуда, отека и т. д.).
Таким образом, проведенные нами исследования показали высокую эффективность препарата Бетадин ® при лечении бактериального вагиноза и смешанной урогенитальной инфекции. У 100% пациенток через 1 мес. после терапии полностью исчезли клинические симптомы бактериального вагиноза и у 96% нормализовался микробный пейзаж влагалища.
Успешное лечение бактериального вагиноза зависит от правильной диагностики и патогенетически обоснованной терапии (т. е. лечения, воздействующего на все звенья процесса развития дисбактериоза влагалища) [7]. Для предупреждения возникновения новых эпизодов бактериального вагиноза рекомендуется использование вагинальных антисептиков (свечи Бетадин ® ) и пробиотиков.
Ключевые слова: кандидозный вульвовагинит, микробиоценоз влагалища, лактобактерии.
Combination of antifungal agent and prebiotic for acute vulvovaginal candidiasis
P.N. Krotin, O.V. Kirilenko
City Consultative Diagnostic Center “Juventa”, St. Petersburg, Russian Federation
Aim: To assess efficacy and safety of Ecofucin ® vaginal suppositories based on the time to clinical and microbiological remission in women with acute vaginal or vulvovaginal candidiasis.
Patients and Methods: The study enrolled women aged 18–45 with acute vaginal or vulvovaginal candidiasis. All patients were subdivided into 2 groups. Study group included 36 patients who received Ecofucin ® vaginal suppositories (natamycin 100 mg plus lactulose 300 mg) once a day for 6 days. Control group included 36 patients who received Pimafucin ® vaginal suppositories (natamycin 100 mg) once a day for 6 days. Efficacy and safety of medications were assessed by gynecological examination, laboratory tests, and patient diaries. Follow-up examinations were performed at days 4, 7, and 37 (±2 days) after treatment begins (30±2 days after treatment finishes).
Results: Combination of antifungal medication (natamycin) and prebiotic in a vaginal suppository provides more rapid clinical remission and complete elimination of VVC causative agent thus resulting in active growth of lactobacilli, principal competitors of yeasts in vaginal microbiocoenosis.
Conclusions: Good tolerability of Ecofucin ® was demonstrated, no adverse reactions were reported.
Keywords: vulvovaginal candidiasis, vaginal microbiocoenosis, lactobacilli.
For citation: Krotin P.N., Kirilenko O.V. Combination of antifungal agent and prebiotic for acute vulvovaginal candidiasis. Russian Journal of Woman and Child Health. 2019;2(2):120–125.
Статья посвящена оценки эффективности комбинации противогрибкового препарата и пребиотика в терапии острого кандидозного вульвовагинита.
Материал и методы
Результаты и обсуждение
В ходе исследования были отобраны и рандомизированы 72 пациентки, у которых обнаруживались дрожжеподобные грибы и почкующийся мицелий. При этом у 71 пациентки в бактериологических посевах образцов обнаружены Candida albicans и только у одной — Candida glabrata. Пациентки были разделены на 2 группы: основная группа — 36 человек — получала интравагинально Экофуцин ® (натамицин 100 мг с лактулозой 300 мг); контрольная группа — 36 пациенток — получала свечи Пимафуцин ® (натамицин 100 мг).
Поскольку одним из важных параметров эффективности лечения КВВ является срок наступления клинической ремиссии, первоначально была проведена оценка частоты жалоб в группах на 4, 7 и 37-й день наблюдения, результаты представлены в таблице 1.
Стоит заметить, что до начала терапии достоверных различий среди пациенток в группах по частоте встречаемости жалоб не отмечено. При этом уже через 4 дня после начала терапии исследуемыми препаратами в обеих группах у пациенток наблюдалось значимое уменьшение практически всех жалоб в сравнении с их частотой до начала терапии. В то же время не отмечено различий в частоте жалоб между группами на 4, 7 и 37-й день от начала терапии, что указывает на схожую эффективность обоих исследуемых препаратов. По всей видимости, это связано с наличием в их составе одинаковых дозировок натамицина. Как известно из данных литературы, натамицин проявляет высокую противогрибковую активность в отношении Candida albicans и Candida glabrata, которые были обнаружены у пациенток [20]. Действие натамицина привело к снижению численности грибов Candida во влагалище, что отразилось в уменьшении воспаления слизистой и соответственно уменьшении жалоб пациенток. Положительный эффект натамицина подтвержден результатами клинического осмотра. Результаты исследования представлены в таблице 2. Значение уровня значимости (p) оценивали при сравнении двух групп по двустороннему критерию Фишера.
Как видно из результатов, представленных в таблице 2, уже на 4-е сут от начала терапии наблюдалась высокая эффективность Экофуцина и Пимафуцина, которая выражалась в исчезновении клинических проявлений КВВ у 75 и 64% пациенток соответственно. Обращает также на себя внимание бóльшая эффективность препарата Экофуцин ® по сравнению с Пимафуцином на 7-е сут после начала терапии, поскольку в группе Экофуцина пациенток без клинических проявлений КВВ было на 25% достоверно больше, чем в группе Пимафуцина (p=0,022). По всей видимости, превосходство препарата Экофуцин ® над Пимафуцином на 7-е сут после начала терапии связано с тем, что лактулозе, содержащейся в составе препарата Экофуцин ® , для восстановления естественной микрофлоры влагалища 4 сут недостаточно, чтобы препарат мог проявить более выраженные лечебные свойства у большинства пациенток [19]. Вероятно, за 7 сут лактулоза более эффективно повлияла на восстановление микрофлоры и подавление роста болезнетворных грибов у большинства пациенток, что отразилось в преобладающем числе пациенток без клинических признаков КВВ в группе Экофуцина. На 37-е сут от начала терапии такой разницы между группами уже не наблюдали. Вероятно, это было связано с одновременным прекращением действия натамицина в обеих группах после его отмены на 7-й день от начала лечения, что подтверждает его основную роль в лечении КВВ. Такое предположение согласуется с данными других исследований, в которых изучалась частота наступления микробиологической ремиссии (табл. 3). Значение уровня значимости (p) оценивали при сравнении обеих групп по двустороннему критерию χ 2 Пирсона.
Как следует из таблицы 3, уже на 4-е сут от начала терапии наблюдалась высокая частота микробиологической ремиссии у пациенток, получавших Экофуцин ® и Пимафуцин ® , что выражалось в исчезновении возбудителя у 75 и 72% пациенток соответственно. При этом значимых отличий между группами по частоте элиминации Candida albicans не выявлено, что, по всей видимости, свидетельствует об отсутствии прямой противогрибковой активности лактулозы. Полученные результаты соответствуют данным других исследователей, которые оценивали эффективность интравагинально применяемого натамицина в схожей дозировке [20]. В целом в клинической практике лечения КВВ установленная в исследовании эффективность препаратов, содержащих натамицин, оценивается как высокая [20, 21].
При исследовании усредненного срока наступления клинической ремиссии в группах, получавших Экофуцин ® и Пимафуцин ® , наблюдается более выраженная эффективность Экофуцина (рис. 1).
В группе, получавшей Экофуцин ® , клиническая ремиссия наступала на 0,7 сут раньше, чем в группе Пимафуцина. Такая разница в скорости наступления ремиссии, вероятнее всего, связана с процессом восстановления микрофлоры влагалища за счет действия лактулозы в составе Экофуцина. Известно, что лактулоза способна стимулировать рост различных пробиотических бактерий, например тех, которые играют приоритетную роль в микробиоценозе влагалища и обеспечивают защиту от различных патогенов [19].
Содержание лактобактерий в мазках пациенток обеих групп показало существенное увеличение численности Lactobacillus spp. в группе, получавшей Экофуцин ® (рис. 2).
Как видно из рисунка 2, уровни Lactobacillus spp. у пациенток до начала терапии в обеих группах значимо не различались между собой. Тем не менее на 37-е сут после начала лечения в группе, получавшей Экофуцин ® , наблюдали достоверное увеличение числа Lactobacillus spp. практически в 100 раз по сравнению с группой пациенток, получавших Пимафуцин ® . Такое увеличение числа Lactobacillus spp., вероятно, связано с прямым действием лактулозы, которая, как известно, является предпочтительным субстратом для этих бактерий и усиливает их рост [19]. Также можно отметить тенденцию к увеличению числа Lactobacillus spp. в группе Пимафуцина, сопряженную, скорее всего, с естественным восстановлением микрофлоры, что подтверждается исследованиями других авторов [21]. Учитывая, что к 37-му дню после начала терапии лактулоза не поступала во влагалище пациенток вместе с препаратом более 30 дней, можно судить о стойком и длительном эффекте лактулозы. Уровни Lactobacillus spp., которые были выявлены в ходе исследования, не являются достаточными и соответствующими нормальному составу микрофлоры влагалища. Так, считается, что в норме содержание лактобактерий должно быть не менее 10 9 КОЕ/мл, т. е. в 1000–10000 раз больше, чем наблюдали в данном исследовании (в пересчете с количества КОЕ в мазке). По всей видимости, недостаточно высокий уровень лактобактерий во влагалище после терапии, который не может обеспечить надлежащую защиту от патогенов, может оказаться причиной развития рецидивов КВВ, обычно возникающих в 10% случаев [1]. Учитывая полученный в ходе данного исследования опыт интравагинального применения препарата Экофуцин ® , можно предположить, что местное применение препаратов, содержащих лактулозу, сразу после терапии КВВ противогрибковыми средствами, такими как натамицин, в течение дополнительных 7 дней позволит более существенно восстановить нормальную микрофлору влагалища и обеспечить значимое снижение риска развития рецидивов КВВ. Применение лактулозы с натамицином при КВВ также перспективно, поскольку дает более высокую эффективность и способствует более интенсивному восстановлению микрофлоры влагалища уже на этапе лечения.
Обращает на себя внимание хорошая переносимость препарата Экофуцин ® пациентками в течение всего курса терапии КВВ. В результате исследования не было отмечено ни одного случая нежелательных реакций на данный препарат, а также каких-либо местных или общих отклонений в здоровье пациенток, которые могли бы быть связаны с его использованием.
Заключение
Для цитирования: Бурова С.А. Комплексный подход к терапии больных с кандидозом органов пищеварительного тракта. РМЖ. 2015;13:760.
Грибы Candida – условно-патогенные микроорганизмы, заселяют пищеварительный тракт в норме, участвуют в процессе брожения, переваривания пищи и др. Этот феномен, называемый колонизацией, клинически протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует у них в орофарингеальной зоне в 20–30%, в тонком кишечнике – в 50–54%, в толстом кишечнике – в 55–70%, в фекалиях – в 65–70% случаев.
Итак, при физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, с другой – факторы патогенности грибов. Устойчивость организма зависит от принадлежности к группам риска и компетентности его иммунной системы. Для защиты важен также макрофагальный и нейтрофильный фагоцитоз, препятствующий диссеминации грибковой, особенно кандидозной инфекции.
По мнению большинства исследователей, бессимптомное пребывание грибов в желудочно-кишечном тракте (ЖКТ) может прекратиться, когда они приобретают патогенные свойства, а у пациента обнаруживается несостоятельность иммунной системы.
Наиболее частыми микозами пищеварительного тракта являются кандидоз пищевода и кандидоз кишечника, которые встречаются как у иммунокомпетентных, так и (гораздо чаще) у иммуносупрессированных лиц. Первичные микозы желудка, в т. ч. и кандидоз, диагностируют редко, что связано с физиологической кислотной средой желудка, где грибковые клетки погибают.
Факторами риска развития кандидоза пищевода и кишечника являются:
1. Заболевания ЖКТ:
- заболевания слизистых оболочек полости рта;
- гастроэзофагеальная рефлюксная болезнь;
- обсемененность желудка Helicobacter pylori;
- атрофический гастрит, гипоацидность желудка, ахалазия, бульбит;
- эрозивно-язвенные заболевания пищевода и кишечника;
- микст-инфекция кишки, дисбиоз;
- дивертикулез, полипоз;
- энтероколит, болезнь Крона, синдром раздраженного кишечника и др.
2. Другие заболевания:
- онкологические;
- гематологические;
- эндокринологические;
- аллергические;
- СПИД и ВИЧ-инфицированность.
3. Травмирование слизистой оболочки ЖКТ:
- пищеводно-желудочным зондом;
- ожоги пищевода;
- оперативные вмешательства.
4. Прием лекарственных препаратов:
- антибиотиков;
- цитостатиков;
- гормонов и других химиопрепаратов.
Нарушение питания, голодание, алкоголизм, курение, наркомания способствуют развитию кандидоза. К факторам риска относится также пожилой возраст, когда происходит старение иммунной системы, присоединяются многочисленные соматические заболевания, уменьшаются амплитуда продольных сокращений пищевода и сила сокращений сфинктеров, нарушаются процессы всасывания и т. д.
Клинически кандидоз пищеварительного тракта подразделяется на:
- орофарингеальный кандидоз (псевдомембранозный, атрофический, эритроматозный, ромбовидный глоссит, ангулярный хейлит);
- кандидозный эзофагит (эрозивный и без эрозий);
- кандидоз желудка (эрозивно-фибринозный и вторичный на фоне язвенной болезни);
- кандидоз кишечника (псевдомембранозный, коллагеновый, лимфоцитарный);
- кандидозный проктосигмоидит;
- перианальный кандидоз;
- секреторную диарею, ассоциированную с кандидозом.
Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации – до 4%, при диссеминированном карциноматозе – от 2,8 до 6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при исследованиях населения в 1–7% случаев. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют 4 типа: от легкого отека, гиперемии, единичных белых налетов
Кандидоз желудка, как правило, развивается вторично на фоне язвенной и гастроэзофагеальной рефлюксной болезни. Ахлоргидрия в свою очередь способствует колонизации грибов на слизистой с последующей инвазией, особенно в зонах дефекта (язвы, эрозии), что замедляет репарацию (заживление), появляется болевой синдром, иногда кровоточивость язвы.
В большинстве случаев грибковые поражения ЖКТ сопровождаются изменением микробиоценоза и снижением колонизационной резистентности организма. Для лечения кандидоза ЖКТ применяют самые разнообразные антимикотики как системного, так и местного действия. Также одной из задач терапии является создание условий для роста и функционирования нормальной микрофлоры.
В современной научной литературе препараты для коррекции дисбиозов делят на 3 основные группы: пробиотики – содержат жизнеспособные микроорганизмы; пребиотики – содержат стимуляторы роста микрофлоры; синбиотики – содержат живые микроорганизмы и пребиотики. Существуют пробиотические комплексы, представляющие собой комбинацию из перечисленных выше компонентов, а также сорбентов, витаминов и микроэлементов. Средств коррекции нарушений микрофлоры кишечника достаточно много, постоянно появляются новые варианты и разновидности.
В состав комплекса Бактистатин включены дополняющие друг друга природные компоненты: сорбент, пробиотик, пребиотик. Одним из преимуществ комплекса Бактистатин является отсутствие живых бактерий, чужеродных для ЖКТ человека, длительное присутствие которых в больших количествах нежелательно. Вместо живых бактерий в состав комплекса Бактистатин включены продукты их жизнедеятельности – активные метаболиты. Поэтому Бактистатин начинает работать сразу, и его действие направлено на восстановление собственной нормальной микрофлоры, которая уникальна у каждого человека.
Нами проведено исследование по оценке эффективности и безопасности пробиотического комплекса Бактистатин в схемах терапии больных с кандидозным эзофагитом и энтероколитом.
В ходе исследования оценивались эффективность и безопасность 2-х схем лечения кандидоза пищевода и кишечника в 2-х группах: 1-я группа – контрольная, в которой пациенты получали этиотропную противогрибковую терапию; 2-я – основная группа пациентов, у которых в схему вышеназванной терапии включен комплекс Бактистатин.
В обеих группах больных проводили селективную деконтаминацию современными эффективными противогрибковыми препаратами направленного действия в течение 7–14 дней. Пациенты основной группы дополнительно получали Бактистатин по 2 капсулы 2 р./сут 20 дней.
Для изучения клинических, эндоскопических и лабораторных показателей в динамике на фоне лечения больных кандидозным эзофагитом и энтероколитом была разработана специальная анкета, включающая физикальное обследование, гастроскопию, колоноскопию, бактериологическое исследование кала.
Результаты сравнения балльной оценки клинической симптоматики показали, что на фоне приема комплекса Бактистатин быстрее уходили проявления кандидоза пищевода и кишечника. Так, до лечения общий балл выраженности симптоматики кандидозного эзофагита был 355, после лечения этот показатель снизился до 123 в контрольной группе и до 60 у пациентов основной группы, принимающих Бактистатин (рис. 1). В отношении кандидозного энтероколита до лечения общий балл выраженности симптоматики составлял 645, после лечения – 317 в контрольной группе и 120 в основной группе (рис. 2).
Кроме того, применение комплекса Бактистатин в лечении кандидоза ЖКТ существенно влияло на восстановление микробиоценоза толстой кишки за счет увеличения числа бифидо- и лактобактерий и уменьшения количества энтеробактерий, неферментирующих бактерий и грибов.
Полученные данные свидетельствуют, что использование метабиотика Бактистатин позволяет избежать побочного действия системных антимикотиков на микрофлору кишечника, улучшить состояние пищевода и кишечника в короткие сроки за счет более выраженного снижения степени тяжести заболевания.
Таким образом, применение комплекса Бактистатин в схемах терапии грибковых поражений ЖКТ способствует быстрому созданию условий для роста и функционирования нормальной микрофлоры и уменьшению побочных эффектов системных антимикотиков.
Аполихина И. А. 1,2 , Гасанова Г. Ф. 1 , Додова Е. Г. 1 , Горбунова Е.А. 1
1 – Федеральное государственное бюджетное учреждение Научный Центр акушерства, гинекологии и перинатологии им. академика В. И. Кулакова Минздрава России.
2 – Институт профессионального образования Первый Московский Государственный медицинский университет имени И.М. Сеченова, кафедра акушерства, гинекологии, перинатологии и репродуктологии.
Сведения об авторах:
Цель исследования: оценить клиническую эффективность и безопасность противорецидивной терапии бактериального вагиноза (БВ) и вульвовагинального кандидоза (ВВК), включающей интравагинальное применение живых ацидофильных лактобактерий после проведения этиотропного лечения.
Ключевые слова: бактериальный вагиноз, вульвовагинальный кандидоз, дисбиоз влагалища, лактобактерии.
Нарушение микроэкологии влагалища – бактериальный вагиноз (БВ) и вульвовагинальный кандидоз (ВВК) – наиболее широко распространенные состояния у женщин репродуктивного возраста. Согласно данным современных публикаций, в структуре вульвовагинальных инфекций частота БВ достигает 30–65%, ВВК - от 20-45%. В патогенезе БВ и ВВК существенную роль играет снижение лактобациллярного пула микрофлоры [13].
Несмотря на разную этиологию, факторы риска БВ и ВВК аналогичны. Это применение антибактериальных препаратов широкого спектра действия, хронические воспалительные заболевания органов малого таза (ХВЗОМТ), эндокринные заболевания (сахарный диабет, заболевания щитовидной железы и др.). В развитии данных состояний имеет значение злоупотребление химическими спермицидами, применение комбинированных оральных контрацептивов с высоким содержанием эстрогенов, длительное ношение внутриматочных контрацептивов, а также нарушение иммунологических взаимодействий на уровне влагалищного эпителия [9,11]. Несмотря на то, что вульвовагинальный кандидоз и бактериальный вагиноз исключены из числа заболеваний, передаваемых половым путем, частая смена половых партнеров и их количество являются ведущими факторами риска развития этих заболеваний, так как эти состояния приводят к нарушению вагинальной микрофлоры. Известно, что в части клинических наблюдений отмечается сочетание кандидоза гениталий и бактериального вагиноза [2,3,6,7,10], при котором дрожжеподобные грибы участвуют в полимикробных ассоциациях, как возбудители заболевания. В этих случаях дрожжеподобные грибы (чаще в высоком титре) обнаруживают на фоне большого количества (более 10 9 КОЕ/мл) облигатных анаэробных бактерий и гарднерелл при резком снижении концентрации или отсутствии лактобацилл. Вульвовагинальный кандидоз, как и бактериальный вагиноз, часто носит рецидивирующий характер. Известно, что рецидивирующее течение ВВК отмечается у 75% у женщин репродуктивного возраста [8,12].
Традиционные схемы лечения позволяют достаточно быстро купировать симптомы БВ и ВВК. При этом дисмикробиоценоз влагалища усугубляется за счет подавления пула лактобацилл и одновременного потенцирования процессов дисбактериоза, вследствие чего у 25-72% пациенток наблюдаются рецидивы заболевания в среднем через 6 месяцев после окончания курса лечения [4].
Результаты многочисленных исследований по применению препаратов, содержащих лактобактерии в лечении и профилактике рецидивов бактериального вагиноза и вульвовагинального кандидоза, свидетельствуют о позитивном эффекте данного метода коррекции вагинальной микрофлоры [4,5,6]. Опыт применения пробиотиков, содержащих лактобактерии показывает, что наиболее эффективным является двухэтапный метод лечения БВ и ВВК: первым этапом является антибактериальная и/или противогрибковая терапия, вторым - восстановление биоценоза влагалища за счет применения пробиотических препаратов [5].
Терапевтическая эффективность пробиотиков заключается наряду с прямым воздействием на микрофлору в стимуляции репаративных процессов в слизистой оболочке влагалища, повышении иммунологической реактивности и общей неспецифической резистентности организма. Назначение при бактериальном вагинозе пробиотиков без предварительного этапа антибактериальной терапии нецелесообразно ввиду выраженной конкурентности между БВ- ассоциированными микроорганизмами и штаммами лактобацилл, содержащихся в препаратах в пользу первых [1].
Таким образом, имеющиеся данные о применении лактобактерий как при лечении рецидивирующего БВ, так и ВВК, явились предпосылкой для проведения данного исследования.
Материал и методы.
Проведено клинико-лабораторное обследование 80 женщин в возрасте от 20 до 50 лет (cредний возраст обследуемых составил 25,3±5,6 лет), обратившихся в гинекологическое отделение восстановительного лечения и стационар дневного пребывания ФГБУ Научный Центр Акушерства, Гинекологии и Перинатологии им. В. И. Кулакова Минздрава России. Все пациентки имели в анамнезе 4 и более обострений ВВК или БВ в течение 1 года, прошли основной курс терапии в соответствии с общепризнанными рекомендованными схемами. Терапия обострения бактериального вагиноза проводилась одним из препаратов: метронидазол 500 мг внутрь 3 раза в день – 7-10 дней, клиндамицин 300 мг внутрь 3 раза в день – 7 дней, интравагинальное применение метронидазола 500 мг 1 раз в день -10 дней, клиндамицина 100 мг 1 раз в день - 6 дней. Лечение обострений вульвовагинального кандидоза проводилась одним из следующих препаратов: миконазол крем 2% (5г) интравагинально 7дней; миконазол крем 4% (5г) интравагинально 3 дня; терконазол крем 0,4% (5г) однократно интравагинально; флуконазол перорально 150 мг 1 раз в день на 1, 4 и 7 дни лечения.
Противорецидивная терапия вульвовагинального кандидоза проводилась с применением одного из следующих препаратов: флуконазола 150 мг 1 раз в неделю перорально на протяжении 6 месяцев, кетоконазола 100 мг 1 раз в сутки 3 дня 1 раз в месяц, интраконазола 200-400 мг внутрь 1 раз в месяц, клотримазола 500 мг интравагинально 1 раз в месяц.
Критериями исключения являлись: беременность или лактация; использование комбинированных оральных контрацептивов, наличие признаков воспаления и бактериального вагиноза, а также наличие в контрольных мазках (бактериоскопия, ПЦР, посев на Candida и Gardnerella vaginalis) грибов рода Candida и Gardnerella vaginalis после основного курса терапии; эпизоды ВВК, вызванные Candida non-albicans (по результатам лабораторных методов исследования) в анамнезе; злокачественные новообразования различных локализаций. Всем пациенткам, включенным в исследование, проводилось общее клинико-анамнестическое обследование, гинекологический осмотр с оценкой критериев Амселя, измерением рН вагинального секрета, бактериоскопическое исследование мазков из заднего свода влагалища и цервикального канала, определение ДНК Gardnerella vaginalis методом ПЦР в образцах эпителиальных клеток влагалища. Проводилось бактериологическое исследование мазков из заднего свода влагалища на определение грибов рода Candida и Gardnerella vaginalis, на количественное определение Lact. acidophillus. Исследования проводились трижды: в начале лечения и через 3 и 6 месяцев после завершения основного курса терапии.
Результаты исследования и обсуждение.
Результаты клинического наблюдения коррелировали с данными бактериологического исследования: на протяжении шести месяцев результаты посевов на грибы рода Candida указывали на низкий их титр у всех пациенток 1 и 2 групп. В то же время, титр грибов рода Candida, выявленный у пациенток в 1-й группе, был статистически значимо ниже такового в группе сравнения (2 группа) и составил 0,2±0,001 против 1,1±0,01 lg КОЕ/мл на шестой месяц наблюдения (p<0,05) (Таблица №2).
Оценка наличия воспалительной реакции в микроскопических мазках проводилась с определением числа лейкоцитов (Ед в поле зрения), которое было статистически значимо ниже в 1 группе, чем во второй на третий и шестой месяцы наблюдения (Таблица № 2).
Таблица № 1. Оценка лабораторных показателей у пациенток в течение шести месяцев наблюдения.
Выявление в мазках
Candida albicans/
Gardnerella vaginalis
методом ПЦР
Группа 1 (n=22)
Группа 2 (n=18)
Группа 3 (n=20)
Группа 4 (n=20)
Лактонорм
при ВВК
Контроль
при ВВК
Лактонорм
при БВ
Контроль
при БВ
Частоты
% в
группе
Часто
ты
% в
группе
Частоты
% в группе
часто
ты
% в группе
Визит 2
(3 мес. наблюдения)
Да
4
18,2%
5
27,7%
5
25 % *
6
30 % *
Нет
18
81,8 %
13
72,2% **
15
75 %
14
70 %
Визит 3
(6 мес. наблюдения)
Да
2
9 %
8
44,5%
0
11
55%
Нет
20
91 %
10
55,5% ***
20
100%
9
45% ***
Таблица № 2. Динамика показателей бактериологического исследования и микроскопии мазков в группах с рецидивирующим ВВК.
Candida (Lg КОЕ/мл)
Лактобактерии (Lg КОЕ/мл)
вспомогательные вещества: компоненты защитной среды высушивания (желатин; сахароза (сахар); молоко).
Состав защитной среды высушивания (на 1 л среды): желатин пищевой - от 3 до 8,5%; сахар белый кусковой или сахароза - от 8 до 28%; молоко сухое обезжиренное или молоко питьевое пастеризованное обезжиренное, или молоко обезжиренное, или молоко натуральное коровье - сырье (в пересчете на сухое вещество) - от 6 до 14%.
Содержание компонентов защитной среды высушивания в готовом препарате не определяют.
Описание
Кристаллическая или пористая масса желтовато-бежевого или беловато-серого цвета, со специфическим запахом.
Фармакотерапевтическая группа
Код АТХ
Фармакодинамика:
Препарат представляет собой микробную массу живого антагонистически активного штамма лактобактерий (Lactobacillus plantarum 8Р-А3 или Lactobacillus fermentum 90Т-С4) лиофилизированную в среде культивирования с добавлением защитной сахарозо-желатино-молочной среды высушивания.
Лактобактерин обладает высокой антагонистической активностью в отношении патогенных и условно-патогенных микробов включая стафилококки энтеропатогенные кишечные палочки протеи шигеллы что определяет коррегирующее действие препарата при нарушениях бактериоценоза. Препарат улучшает обменные процессы препятствует формированию затяжных форм кишечных заболеваний повышает неспецифическую резистентность организма.
Показания:
Лечение заболеваний желудочно-кишечного тракта и женских гениталий сопровождающихся нарушениями нормальной микрофлоры.
Препарат применяют взрослым и детям независимо от возраста.
При заболеваниях желудочно-кишечного тракта :
- реконвалесценты перенесшие острые кишечные инфекции при наличии дисфункций кишечника или выделении патогенных и условно-патогенных бактерий;
- соматические заболевания сопровождающиеся дисбактериозами возникшими в результате применения антибиотиков химиотерапии и других причин;
- комплексное лечение ослабленных детей с заболеваниями инфекционной и неинфекционной этиологии сопровождающимися дисбактериозами атопическим дерматитом;
- хронические колиты различной этиологии в том числе неспецифические язвенные колиты.
При заболеваниях женской половой сферы :
- для санации половых путей при неспецифических воспалительных заболеваниях гениталий и предродовой подготовке беременных "группы риска" с нарушениями чистоты вагинального секрета до III-IV степени.
В связи с отсутствием возрастных ограничений для назначения препарата возможность применения у подростков и детей младшего возраста оценивает врач с учетом возможной пользы риска и возрастных особенностей пациента.
Противопоказания:
Повышенная чувствительность к компонентам препарата.
Дефицит сахаразы/изомальтазы непереносимость фруктозы глюкозо-галактозная мальабсорбция.
Противопоказано местное применение при вульвовагинальных кандидозах.
Безопасность и терапевтическая эффективность перорального применения препарата при вульвовагинальных кандидозах клинически не исследовалась.
Беременность и лактация:
Способ применения и дозы:
Лактобактерин при кишечных заболеваниях применяют внутрь а в акушерско-гинекологической практике - интравагинально.
Содержимое флакона растворить кипяченой водой комнатной температуры из расчета 5 мл (чайная ложка) воды на 1 дозу препарата.
Растворение осуществить следующим образом: в стакан налить необходимое количество воды (в соответствии с количеством доз указанных на флаконе); вскрыть флакон удалив колпачок и пробку; из стакана перенести во флакон небольшое количество воды; после растворения (препарат растворяется не более 5 мин с образованием гомогенной суспензии желтовато-бежевого или беловато-серого цвета) содержимое флакона перенести в тот же стакан и перемешать. Одна чайная ложка растворенного таким образом препарата составляет 1 дозу. Детям содержимое флакона растворяют из расчета 1 мл на 1 дозу препарата.
При кишечных заболеваниях препарат следует принимать за 40-60 мин до еды и желательно запивать молоком. Лечение рекомендуется сопровождать применением витаминов.
Суточную дозу и продолжительность курса лечения определяет врач в зависимости от клинической формы заболевания и выраженности дисбактериоза.
При кишечных заболеваниях Лактобактерин применяют в следующих суточных дозах:
Возраст
Доза
3 дозы 2 раза в день
От 6 мес до 1 года
3 дозы 3 раза в день
5 доз 2 раза в день
Старше 3 лет и взрослые
5 доз 2-3 раза в день
Курс лечения Лактобактерином при различных заболеваниях составляет:
а) при затяжном и хроническом течении дизентерии постдизентерийном колите долечивании реконвалесцентов после ОКИ а также при длительной кишечной дисфункции неустановленной этиологии - не менее 4 недель;
б) при неспецифическом язвенном колите а также хронических колитах и энтероколитах - до 2 мес;
в) при дисбактериозах различной этиологии - 3-4 недели.
При отсутствии эффекта от применения препарата на протяжении 2 недель необходимо повторное исследование микрофлоры желудочно-кишечного тракта и коррекция ее другими препаратами в зависимости от полученного результата.
Для закрепления полученного клинического эффекта или при отсутствии полной нормализации микрофлоры после окончания курса лечения при заболеваниях протекающих с рецидивами целесообразны повторные курсы лечения. В этих случаях перед назначением препарата необходимо повторное исследование микрофлоры.
При воспалительных заболеваниях гениталий Лактобактерин назначают по 5 доз 2 раза в день интравагинально в течение 10-12 дней начиная с 10-12 дня менструального цикла.
Для предродовой подготовки беременных "групп риска" Лактобактерин назначают по 5 доз 1 раз в день в течение 5-8 дней.
При интравагинальном применении содержимое флакона растворить в 5 -10 мл кипяченой воды комнатной температуры стерильный тампон пропитать растворенным препаратом ввести тампон во влагалище и оставить на 2-3 часа. У подростков и детей младшего возраста можно использовать спринцевания (орошения).
Лечение проводить под контролем восстановления чистоты вагинального секрета до I-II степени появления лактофлоры и исчезновения клинических симптомов заболевания.
Побочные эффекты:
Побочное действие препарата не установлено.
У отдельных людей с измененной реактивностью могут развиваться аллергические реакции на компоненты препарата.
При появлении побочных действий не упомянутых в инструкции необходимо обратиться к лечащему врачу.
Передозировка:
Взаимодействие:
Ввиду высокой антибиотикоустойчивости лактобактерий допускается применение Лактобактерина при антибиотикотерапии.
Особые указания:
Перед применением препарата необходимо проконсультироваться с врачом.
Непригоден для применения препарат целостность упаковки которого нарушена (треснувшие флаконы) препарат с измененным внешним видом биомассы при наличии посторонних включений препарат без маркировки.
Не рекомендуется растворение препарата в горячей воде (выше 40 °С). Растворенный препарат хранению не подлежит.
Влияние на способность управлять трансп. ср. и мех.:
Форма выпуска/дозировка:
Упаковка:
По 3 или 5 доз во флаконе.
По 10 флаконов в пачке (коробке) с инструкцией по применению.
Условия хранения:
При температуре от 2 до 8 °С. Хранить в недоступном для детей месте.
Условия транспортирования. При температуре от 2 до 8 °С.
Срок годности:
Препарат с истекшим сроком годности использованию не подлежит.
Условия отпуска
Производитель
Федеральное государственное унитарное предприятие "Научно-производственное объединение по медицинским иммунобиологическим препаратам "Микроген" Министерства здравоохранения и социального развития Российской Федерации (ФГУП "НПО "Микроген" Минздравсоцразвития России), 634040, Томская область, г. Томск, ул. Ивановского, д. 8, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ФГУП "НПО "Микроген" Минздравсоцразвития России
Лактобактерин - цена, наличие в аптеках
Указана цена, по которой можно купить Лактобактерин в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
Читайте также:

