Природа и происхождение инфекции
Обновлено: 25.04.2024
Источники инфекций. Распространение инфекционных болезней
Источники инфекции. Инфекционный процесс может быть вызван как представителями нормальной микрофлоры организма хозяина (эндогенные инфекции), так и микроорганизмами извне (экзогенные инфекции).
Условно-патогенные бактерии нормальной микрофлоры кишечника становятся источниками инфекции только при определённых условиях (например, при перфорации кишечника). Энтеробактерии и неспорообразующие анаэробы (например, Bacteroides fragilis) вызывают внутрибрюшинные абсцессы. При попадании в лёгкие содержимого желудочного и ротоглотки, в котором присутствуют представители нормальной микрофлоры (факультативные и облигатные анаэробы), развивается пневмония или абсцесс лёгкого.
Обитающий на слизистой оболочке передних отделов носовых ходов Staphylococcus aureus может вызвать раневую инфекцию после хирургического вмешательства. Нейтропенический сепсис (бактериемия) возникает, когда бактериям удаётся преодолеть внутренние защитные механизмы слизистой оболочки кишечника или при снижении функции нейтрофилов во время химиотерапевтического лечения лейкемии. Различные изменения в организме хозяина повышают риск развития заболеваний: хирургическое вмешательство и катетеризация сосудов способствуют развитию инфекций, вызываемых представителями нормальной микрофлоры; применение иммунодепрессантов увеличивает риск возникновения оппортунистических инфекций, вызываемых возбудителями с низкой вирулентностью.
Источником экзогенных инфекций могут стать различные животные (зоонозныс инфекции). В этом случае заражение происходит контактно-бытовым и пищевым путями. Кроме того, инфекции могут быть вызваны микроорганизмами, обитающими в окружающей среде (например, Legionella или Clostridium).
Изменение условий окружающей среды ведёт к выраженному повышению риска заражения. Так, распространению зоонозных инфекций способствовало активное развитие сельского хозяйства и земледелия. Например, скармливание крупному рогатому скоту белков животного происхождения привело к возникновению эпидемии губчатой энцефалопатии, которая затем распространилась среди людей (вариантная болезнь Крейцфельдта—Якоба).
Развитие птицеводства способствовало распространению сальмонеллёза (факторы передачи — пух и перо домашней птицы), а механизация пищевой промышленности — повышению риска перекрёстной контаминации. Избежать подобных проблем позволяет совершенствование методов ведения сельского хозяйства и соблюдение санитарно-гигиенических норм.
Недостаточный контроль систем вентиляции в зданиях приводит к возникновению заболеваний, вызываемых Legionella pneumophila.
Сложный жизненный цикл некоторых микроорганизмов помогает им выжить в неблагоприятных условиях и способствует их распространению. Например, возбудители, выделяющиеся из организма хозяина с экскрементами, как правило, передаются посредством фекально-орального механизма. Многие возбудители часть своего жизненного цикла проводят в организме переносчика, и в этом случае заражение происходит во время укуса. Иногда в качестве промежуточного хозяина паразиты могут использовать не животных, а человека (например, при эхинококкозе).

Выживание и распространение возбудителей инфекций
Каждый микроорганизм по-своему приспосабливается к условиям окружающей среды. Так, бактерии способны долгое время выживать в неблагоприятных условиях в виде спор — покоящихся клеток со сниженным метаболизмом, снабжённых твёрдой многослойной оболочкой. Яйца гельминтов также снабжены твёрдой оболочкой, помогающей им выживать в окружающей среде. Распространению возбудителей способствует их длительное персистирование в организме хозяина, который в этом случае становится резервуаром инфекции.
Микроорганизмы, выделяющиеся в окружающую среду при чихании, могут долгое время находиться в воздухе в составе микроскопических капель (5 мкм). Инфекционный процесс возникает при их попадании в лёгкие здорового человека (воздушно-капельный путь передачи). Этим способом происходит распространение как возбудителей респираторных заболеваний (вирусы гриппа и др.), так и микроорганизмов, поражающих другие органы (например, Neisseria meningitides).
Возбудителей желудочно-кишечных расстройств (Salmonella) можно обнаружить в воде и пище (алиментарный путь передачи). Такое распространение инфекции наблюдают при токсоплазмозе и цистицеркозе, поражающих различные органы.
Через неповреждённый кожный покров проникают Leptospira, Treponema и Schistosoma. Передача ВИЧ происходит во время инъекций и переливаний крови (при нарушении кожного барьера). Представители нормальной микрофлоры кожного покрова (Staphylococcus epidermidis) могут проникать в организм через венозный катетер. Переносчиками некоторых инфекций служат насекомые, питающиеся кровью (например, малярию переносят самки комара рода Anopheles).
При половом контакте происходит передача микроорганизмов, не способных к жизни вне организма человека (например, Neisseria gonorrhoeae или Treponema pallidum). При этом заражению способствуют изъязвления слизистой оболочки половых органов.
Факторы распространения инфекций
Улучшение социальной обстановки и условий окружающей среды способствует снижению риска заражения и распространения инфекционных болезней. Например, соблюдение санитарно-гигиенических норм ведёт к уменьшению риска возникновения диареи, а улучшение жилищных условий препятствует распространению туберкулёза. Кроме того, полноценное питание уменьшает восприимчивость человека к инфекционным заболеваниям.
Однако как ни парадоксально, с увеличением уровня жизни возрастает и смертность от некоторых инфекционных заболеваний. Тяжесть осложнений инфекционного процесса прямо пропорциональна возрасту пациента, например при паралитическом полиомиелите или ветряной оспе.
Просвещение населения и распространение инфекций. Существует большое количество программ медицинского просвещения населения, охватывающих такие проблемы, как половое воспитание, рекомендации для беременных, соблюдение правил личной гигиены (гигиенические нормы при приёме пищи, рекомендации для путешественников и др.), использование одноразовых игл и шприцев.
Безопасность пищевых продуктов и распространение инфекций. В Европейском союзе существуют общепринятые стандарты безопасности пищевых продуктов. Контроль за их соблюдением осуществляют специалисты по вопросам гигиены окружающей среды, а также представители Министерства окружающей среды, продовольствия и сельского хозяйства. Пастеризация молока помогает снизить риск возникновения заболеваний, вызываемых Mycobacterium bovis и бактериями рода Campylobacter.
Борьба с переносчиками инфекций. Борьбе с переносчиками инфекций придают огромное значение в регионах, где промежуточными хозяевами возбудителей могут быть насекомые. Лица, посещающие тропические страны, могут существенно снизить риск развития заболевания, приняв меры, предотвращающие нападение и укусы насекомых. Попытки контролировать популяции насекомых с помощью инсектицидов могут быть неудачными вследствие наличия резистентности к этим препаратам.
Профилактика инфекционных заболеваний
Для профилактики некоторых заболеваний (например, дифтерия, менингококковая инфекция) применяют лекарственные препараты. Цель — уничтожение возбудителей заболевания в организме носителя для предупреждения развития острого состояния или распространения инфекции.
Например, для профилактики менингококковой инфекции применяют рифампицин или ципрофлоксацин, приём изониазида рекомендован пациентам с риском обострения туберкулёза при снижении иммунитета.
Значение эпидемиологии в распространении инфекций
Значение организации здравоохранения в распространении инфекционных заболеваний
В большинстве стран существует департамент здравоохранения, занимающийся изучением, профилактикой и лечением инфекционных заболеваний. Обязанности департамента:
• контроль за инфекционной заболеваемостью;
• эпидемиологическое обследование в очаге инфекционного заболевания;
• контроль за вакцинопрофилактикой;
• научные эпидемиологические исследования и обучение медицинского персонала.
Для предотвращения вспышек зоонозных инфекционных заболеваний необходимо тесное сотрудничество между учреждениями (министерствами) пищевой и сельскохозяйственной промышленности и органами санитарно-эпидемиологического надзора. В некоторых странах функции всех этих организаций выполняет одна из них, например Департамент здравоохранения в Великобритании и СДС — Центр по контролю и предупреждению распространения заболеваний — в США. Кроме того, в ведении этих организаций находится решение проблемы биологического терроризма. При этом особую важность приобретает быстрое определение вида возбудителя и своевременное оповещение населения о применении биологического оружия.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Вернуться в раздел "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.

Обзор
Автор
Редактор
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Исследования в области происхождения злокачественных опухолей, ежегодно уносящих миллионы человеческих жизней, ведутся с XIX века. Работая в области молекулярной вирусологии, Вармус совместно с Дж. М. Бишопом в исследованиях 1970-х гг. сделали открытие, которое по-новому осветило долго остававшуюся дискуссионной проблему этиологии опухолей у человека и животных. Согласно полученным результатам, неконтролируемый рост клеток, образующих опухоль, вызывается не только проникающим в клетку извне онковирусом, но и внутренними процессами в самой клетке. Вармус доказал, что нормальные гены роста клетки вследствие случайных спонтанных мутаций под воздействием химических канцерогенов или, порой, процесса старения могут изменять свою молекулярную структуру и таким образом превращаться в протовирусы онкогенной природы. За открытие клеточного происхождения онкогенных протовирусов Вармус совместно с Дж. М. Бишопом в 1989 г. были удостоены Нобелевской премии по физиологии и медицине [1].
Один из самых распространённых вирусов в человеческой популяции — вирус Эпштейна-Барр (рис. 1) — был открыт и описан в 1964 году двумя английскими вирусологами: Майклом Эпштейном и Ивонной Барр. Вирус Эпштейна-Барр (ВЭБ) — член семейства герпесвирусов [6, 7]. В инфицированных клетках вирусная ДНК, как правило, не встроена в клеточный геном, а находится в ядре в виде замкнутого кольца (эписомы). Биологическое значение интеграции ВЭБ в геном клетки остается неясным. Высказываются предположения, что эписомная ДНК необходима для реализации полноценной репликации ВЭБ, завершающейся формированием вирусных частиц [8].

В отличие от многих других герпесвирусов, вирус Эпштейна-Барр поражает в первую очередь эпителиальные клетки ротовой полости, глотки, миндалин. Здесь он размножается наиболее активно, и поэтому главным путём заражения вирусом являются поцелуи (вот и приехали). Наибольшее количество вирусных частиц находится в клетках эпителия около слюнных желез, и со слюной выделяется большое количество их. Не удивительно, что инфекционный мононуклеоз — самое распространённое заболевание, вызываемое вирусом Эпштейна-Барр, — называют ещё болезнью поцелуев [9].
После первой встречи человека с ВЭБ вирус в незначительном количестве сохраняется в организме хозяина в течение всей жизни. Однако если любой элемент иммунного ответа нарушен, даже незначительное количество ВЭБ-инфицированных клеток может преумножиться колоссально [12].
Инфицированные В-клетки могут значительное время находиться в миндалинах, что позволяет вирусу выделяться во внешнюю среду со слюной. С зараженными клетками ВЭБ распространяется по другим органам. В пораженных вирусом клетках возможно два вида развития: литический, приводящий к разрушению клетки-хозяина, и латентный (клетка заражена, но ничего не выдает нахождения вируса), когда число вирусных копий небольшое и клетка не разрушается. ВЭБ может длительно находиться в В-лимфоцитах, эпителии носоглотки и слюнных железах. Кроме того, он способен проникать и в другие клетки: Т-лимфоциты, NK-клетки, макрофаги, нейтрофилы, эпителиоциты сосудов (рис. 2а, 2б) [13].

Злокачественные лимфомы (например, увеличение лимфоузлов), согласно данным Международного агентства по изучению рака, составляют 3–4% среди всех регистрируемых в мире злокачественных новообразований [14]. Лимфомы делят на две основные группы: лимфома Ходжкина (20–30 % всех лимфом) и неходжкинские лимфомы (около 70%) [14, 15].
Неходжикинские лимфомы — это совокупность новообразований, в возникновении которых принимают участие различные агенты [18]. Первая группа — это вирусы, трансформирующие лимфоциты и другие клетки (ВЭБ, HHV-8). Вторая группа представлена факторами различной природы, вызывающими иммунодефицитные состояния. К таким факторам в первую очередь относится ВИЧ (вирус иммунодефицита человека), вызывающий у инфицированного лица подавление иммунитета в результате истощения пула Т-лимфоцитов CD4+ и возникновение СПИДа. В третью группу входят некоторые инфекции, (например, H. pylori), которые увеличивают риск возникновения лимфом на фоне вызываемой ими хронической стимуляции иммунной системы и постоянной активации лимфоцитов [17].
Исследования последних лет свидетельствуют о том, что в патогенезе ВЭБ-ассоциированных патологий чрезвычайно важную роль играет вредный LMP1 — латентный мембранный белок 1, кодируемый одноименным геном (LMP1). Он обладает свойствами онкобелка и функционирует как постоянно активный псевдорецептор. Он способен изменять В-лимфоциты человека [19].
Есть предположение, что аминокислотные замены, накапливающиеся в LMP1, по-видимому, также вносят свой вклад в возникновение опухолей. Механизм этого процесса окончательно не установлен, но предполагается, что усиленный трансформирующий эффект мутированных LMP1 может представлять важную составляющую этого процесса. При этом показано, что различия в последовательности гена LMP1 могут определять агрессивный географически локализованный генотип ВЭБ [21].
Из известных механизмов действия LMP-2 (второй из братьев семейства LMP), расположенного на противоположном конце линейного генома, упоминается лишь способность этих белков совместно повышать сигнальную трансдукцию в ВЭБ (+) клетках [19].
По данным Харальда цур Хаузена, связь между вирусом и раковым заболеванием считается установленной при определении следующих критериев:
- эпидемиологические доказательства того, что вирусная инфекция является фактором риска для развития специфической опухоли;
- присутствие и сохранение генома вируса в клетках опухоли;
- стимуляция пролиферации клеток после введения генома (или его части) вируса в ткани культуры клеток;
- демонстрация того, что геном возбудителя индуцирует пролиферацию и злокачественный фенотип опухоли [19].
Однако канцерогенность ВЭБ далеко не однозначна. Несмотря на то, что кодируемые вирусом продукты способны вызывать пролиферацию инфицированных клеток, ведущую к возникновению лимфом у больных с иммунодефицитом, эти клинически агрессивные опухоли довольно часто поликлональны и подвергаются регрессии при восстановлении иммунного ответа на ВЭБ. Такие опухоли как лимфома Беркитта (ЛБ) и лимфома Ходжкина (ЛХ) встречаются не только в ВЭБ-ассоциированных, но и в ВЭБ-неассоциированных вариантах, что говорит о том, что патогенез этих новообразований связан не только с ВЭБ. Кроме того, злокачественные клетки больных ЛБ и ЛХ отличаются фенотипически от клеток ЛКЛ, полученных под воздействием ВЭБ in vitro, и не экспрессируют ряд белков, необходимых для трансформирующего роста. Эти находки позволяют предположить, что опухолевые клетки могут возникать и под воздействием факторов невирусного происхождения, а также зависеть от различных усиливающих рост клеток стимулов [17].
Лабораторная диагностика ВЭБ-инфекции базируется на цитологическом исследовании крови или костного мозга, серологических исследованиях и ПЦР. С помощью метода ПЦР можно определить ДНК вируса в плазме до клинических проявлений болезни, а репликация вируса в организме является показанием к противовирусной терапии и критерием эффективности проведенного лечения. Материалом для исследования служат слюна или рото- и носоглоточная слизь, соскоб эпителиальных клеток урогенитального тракта, кровь, спинномозговая жидкость, ткани опухоли и костный мозг. Как у больных ВЭБ, так и у носителей может быть получен положительный результат в ПЦР. Поэтому для их дифференцировки проводится количественный ПЦР-анализ для определения количества копий вирусного генома. У маленьких детей (до 1–3-х лет) по причине недостаточно сформированного иммунитета диагностика по антителам затруднительна, поэтому в данной группе пациентов в помощь приходит именно ПЦР. Однако в силу того, что ПЦР-анализ информативен только при размножении (репликации) вируса, то существует и определенный процент ложноотрицательных результатов (до 30%), связанный именно с отсутствием репликации в момент исследования. При этом важно сопоставление результатов клинических, серологических и молекулярных обследований в определении ВЭБ-инфекции, как причины имеющегося заболевания [1].
Специфическая профилактика (вакцинация) против ВЭБ не разработана, но проводятся клинические испытания. Основной проблемой при разработке вакцины является большое отличие в белковом составе вируса на разных фазах его существования. Впрочем, в настоящее время разрабатывается вакцина, которая содержит рекомбинантный поверхностный антиген gp350. После вакцинации первичная инфекция протекает субклинически, но собственно инфицирование человека не предупреждается. Кроме того, вырабатывающиеся нейтрализующие антитела не влияют на течение различных форм латентной инфекции, в том числе опухолей. Профилактические меры сводятся к укреплению иммунитета, закаливанию детей, мерам предосторожности при появлении больного в окружении, соблюдение правил личной гигиены.
Заключение
Широкое распространение ВЭБ с выраженным трансформирующим потенциалом среди населения планеты и редкого возникновения в инфицированной популяции связанных с этим вирусом опухолей с преимущественной их локализацией в определенных географических регионах позволяет сделать важный вывод. Подобно большинству опухолей иной вирусной природы, в патогенезе ВЭБ-ассоциированных новообразований важную роль играют дополнительные факторы, и одного ВЭБ недостаточно для возникновения опухоли. ВЭБ лишь инициирует пролиферацию инфицированных им клеток, а последующие события влияют на гистопатологический спектр возникающих неоплазий. Одним из важнейших факторов, в значительной степени определяющих возникновение ВЭБ-ассоциированных опухолей, служит выраженная иммуносупрессия (врожденная, ятрогенная или индуцированная любой вирусной инфекцией, и в первую очередь ВИЧ), приводящая к утрате функции иммунного распознавания клеток, инфицированных ВЭБ.
Таким образом, несмотря на многолетнее изучение связи ВЭБ с опухолями человека, вопрос о роли вируса в их возникновении до конца не изучен. Раскрытие механизма злокачественной трансформации вирусом, персистирующим в латентном состоянии более чем у 90% населения планеты, — задача чрезвычайно сложная. Однако технические достижения последних лет, существенно повысившие специфичность исследований, позволяют надеяться, что детали ВЭБ-ассоциированного канцерогенеза будут выяснены.

Новость
Путь прионов
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
Биологическая сущность прионов
Рисунок 1. Метафора нейродегенеративного поражения мозга — это губка, в которую превращается нервная ткань в результате массовой гибели нейронов.
И тогда происходит удивительное событие: нормальные молекулы белка, контактируя с патологическими, сами превращаются в них, изменяя свою пространственную структуру (механизм трансформации остаётся загадкой и по сей день) [1]. Таким образом прион, как самый настоящий инфекционный агент, заражает нормальные молекулы, запуская цепную реакцию, разрушительную для клетки.
Некоторые сведения о прионах
Условия возникновения заболеваний
Условия возникновения прионовых болезней уникальны. Они могут формироваться по трём сценариям: как инфекционные, спорадические и наследственные поражения. В последнем варианте главную роль играет генетическая предрасположенность [2].
В последнее десятилетие интерес к этой теме возобновился в связи с возможностью развития диагностики и эффективной терапии [5]. Появилось множество различных объяснений для возрастных нейродегенеративных болезней, — например, окислительная модификация ДНК, липидов и/или белков; соматические мутации; измененный врождённый иммунитет; экзогенные токсины; несоответствия ДНК—РНК; нарушение работы шаперонов; отсутствие одного из аллелей гена [5]. Альтернативным комплексным разъяснением служит то, что различные группы белков могут формировать прионы. Несмотря на то, что небольшое количество прионов может быть удалено посредством путей белковой деградации, их чрезмерное накопление с течением времени позволяет прионам самостоятельно распространяться в организме (рис. 2), что приводит к нарушению деятельности центральной нервной системы [5].

Группы риска прионных заболеваний
Вот кого прионные заболевания могут настичь с наибольшей вероятностью:
- работники пищевой промышленности;
- ветеринары;
- патологоанатомы;
- хирурги;
- пациенты трансплантолога;
- каннибалы;
- лица, в семье которых были замечены синдромы Герстманна—Штрейслера—Шейнклера или фатальной инсомнии.
Лабораторная диагностика и лечение
Диагностика базируется на внутримозговом заражении мышат или хомяков, у которых медленно (до 150 дней) развивается соответствующее заболевание, если пациент был болен [2]. Часто проводится гистологическое исследование головного мозга погибших животных [2].
К сожалению, до настоящего времени еще не разработаны эффективные методы лечения прионовых болезней, хотя попытки предотвратить конформационный переход нормального белка в аномальный производятся. Поэтому самым надёжным способом предупреждения развития инфекционных форм является профилактика [2].
Перспективы
По-видимому, интерес к прионам не угаснет до тех пор, пока предположения на их счёт полностью не подтвердятся и не будут найдены эффективные способы лечения прионных заболеваний. В статье [6] говорится о необходимости современного исследования, которое требует тщательного рассмотрения чужеродных прионов в экстраневрональных тканях.
В качестве модельных объектов авторы использовали мышей: две линии, которые трансгенно экспрессировали овечий прионный белок, и одну линию, которая экспрессировала человеческий прионный белок (рис. 3). Задачей было сравнить эффективность межвидовой передачи инфекции посредством тканей мозга и селезёнки. Внутримозговое заражение чужеродным прионным белком выражалось в отсутствии или небольшом количестве инфекционного агента в мозгах этих мышей. Однако инфекционные чужеродные прионы обнаруживались в селезёнке на более ранних этапах заражения в сравнении с моментом, когда были использованы нейротропные прионы, тем самым определяя, что лимфатическая ткань может быть более пермиссивной к распространению чужеродных прионов по сравнению с мозгом.

Рисунок 3. Способность приона хомяков Sc237 заражать и передаваться при введении в мозг или селезенку трансгенным мышам, имеющим прионный белок PrP овцы (tg338; белые мыши) или человека (tg7; серые мыши). Число заболевших/инъецированных мышей показано в скобках; ниже приведено среднее время жизни (в днях).
Чем вызвана эта предпочтительная репликация прионов в лимфатических тканях, пока неизвестно. Однако полученные данные показывают, что человек может быть более чувствительным к чужеродным прионам, чем предполагалось ранее на основании присутствия прионов в мозгу, и по этой причине бессимптомный переносчик прионной болезни может быть не распознан. Это ещё раз подтверждает, что такая могущественная биомолекула как прион таит в себе немало загадок, раскрытие которых, возможно, поможет в понимании ряда неразрешимых проблем человечества.
Патогенность — видовой признак. Таким образом, всегда возможны внутривидовые вариации. Это означает, что патогенность может быть по-разному выражена у различных штаммов. Вероятность развития инфекционной болезни в значительной степени определяют видовые свойства возбудителя, количество возбудителя, пути и место проникновения в организм, скорость размножения.
Инфицирующая доза
При попадании в организм незначительного числа патогенных микроорганизмов (что бывает наиболее часто) их обычно эффективно элиминируют защитные факторы организма. Для развития заболевания необходимо, чтобы патоген обладал достаточной вирулентностью, а его количество (инфицирующая доза) превышало некоторый порог, определяемый в каждом конкретном случае вирулентностью возбудителя и состоянием резистентности организма. В контексте патогенных свойств инфицирующую дозу можно рассматривать как определённое количество микроорганизмов, обеспечивающее возможность адгезии, колонизации и инвазии в ткани.
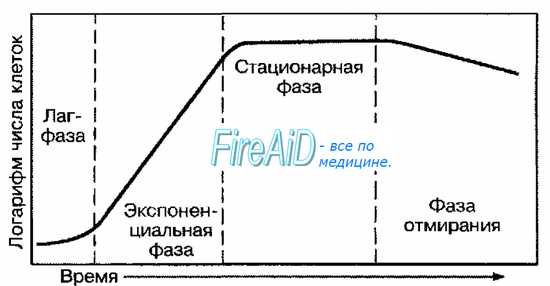
Скорость размножения
На вероятность развития инфекционного процесса и его тяжесть существенно влияет скорость размножения возбудителя. Например, чумная палочка настолько быстро размножается в организме, что иммунная система практически не успевает ответить на её проникновение формированием защитных реакций.
Не менее значимо проникновение возбудителя. Многих возбудителей отличает тропизм [от греч. trope, направление] к определённым тканям. Например, гонококк вызывает типичные поражения после попадания на слизистые оболочки половых органов или глаз, а дизентерийная амёба — на слизистую оболочку кишечника. С другой стороны, туберкулёзная или чумная палочки способны, вызвать заболевание вне зависимости от пути проникновения, приводя к развитию полиморфных поражений, варьирующих в зависимости от места проникновения. Для таких патогенов характерен пантропизм. Проникнув в организм, возбудитель начинает размножаться в месте внедрения, формируя первичный очаг поражения (первичный аффект), либо распространяется (диссеминирует) в другие органы и ткани.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

