Профилактика катетер-ассоциированных инфекций мочевыводящих путей
Обновлено: 05.05.2024
Катетер-ассоциированная инфекция мочевыводящих путей (ИМП) является ИМП, при которой была получена положительная культура тогда, когда постоянный мочевой катетер находился в месте введения в течение > 2 календарных дней. У пациентов с постоянно стоящими мочепузырными дренажами имеется предрасположенность к бактериурии и инфекций мочевыводящих путей. Симптомы могут быть стертыми или указывать на сепсис. Диагностика зависит от наличия симптомов. Лабораторная диагностика включает общий анализ и посев мочи, после того как катетер удален и установлен новый. Наиболее эффективные профилактические меры включают исключение катетеризаций без необходимости и как можно более быстрое удаление катетеров.
Бактерии могут попадать в мочевой пузырь во время установки катетера Катетеризация мочевого пузыря Катетеризацию мочевого пузыря используют для следующих целей: Получение образца мочи для исследования Измерение объема остаточной мочи Разрешения задержки мочи или недержания мочи Доставки рентгеноконтрастных. Прочитайте дополнительные сведения по его просвету или из внешней среды, окружающей его наружную часть. На ней и уротелии формируется биопленка. Бактерии проникают в эту биопленку, которая защищает их от смывания мочой, действия иммунных факторов организма и антибиотиков, что делает уничтожение бактерий сложным. Даже при тщательном асептическом уходе за катетером и его установке вероятность развития значительной бактериурии составляет 3–10%, возрастая с каждым днем присутствия катетера. У 10–25% больных с бактериурией развиваются симптомы инфекции мочевыводящих путей. Реже развивается сепсис Сепсис и септический шок Сепсис представляет собой клинический синдром с развитием жизнеугрожающей органной дисфункции, вызванный нарушением регуляции ответа на инфекцию. При септическом шоке происходит критическое. Прочитайте дополнительные сведения .
ИМП могут также развиться у женщин в течение нескольких дней после удаления катетера.
Клинические проявления
Диагностика
Анализ и посев мочи у больных с симптомами или высоким риском развития сепсиса
Пациенты с нейтропенией
Больные с трансплантацией органов, принимающие иммунодепрессанты
Пациенты, перенесшие урологическую операцию

Диагностические исследования включают общий анализ мочи Общий анализ мочи У пациентов с нефрологической патологией симптомы и признаки заболевания могут быть неспецифическими и/или отсутствовать до поздних стадий болезни. Симптомы могут быть местными (например, отражающими. Прочитайте дополнительные сведения и посев мочи. Если подозревают бактериемию, производят посев крови. Следует провести культуральное исследование мочи, предпочтительно после замены катетера (чтобы избежать культивирования колонизирующих бактерий), а затем путем прямого укола иглой из катетера получить мочу; все проводят при соблюдении правил асептики, чтобы контаминация образца сводилось к минимуму.
У женщин, которым производят удаление катетера, рекомендовано провести посев мочи в пределах 48 часов вне зависимости от появления симптомов.
Лечение
Бессимптомные пациенты с низким риском лечения не требуют. Пациентов высокого риска и с наличием симптомов следует лечить с использованием антибиотиков и симптоматического лечения. Катетер должен быть заменен в начале лечения. Выбор эмпирического антибиотика, как при остром пиелонефрите Острый пиелонефрит Бактериальные инфекции мочевыводящих путей могут затрагивать уретру, предстательную железу, мочевой пузырь и почки. Симптомы могут отсутствовать или включать поллакиурию, императивные позывы. Прочитайте дополнительные сведения . Иногда к режиму лечения добавляют ванкомицин. Впоследствии следует использовать антибиотики с активностью узкого спектра, основанные на результатах культурального исследования и исследования на чувствительность. Оптимальная продолжительность лечения не установлена, но длительность 7–14 дней является обоснованной для пациентов с удовлетворительным клиническим ответом, включая разрешение системных проявлений.
Мужчин и женщин с недавним удалением уретрального катетера, отсутствием симптомов и подтверждением инфекцией мочевыводящих путей при посеве мочи следует лечить согласно результатам посева. Оптимальная продолжительность лечения неизвестна.
Профилактика
Наиболее эффективными профилактическими мерами является сведение к минимуму частоты катетеризаций и удаление катетеров при первой возможности. Оптимизация методик асептики и использование закрытых дренажных систем также уменьшает риск. Неизвестно насколько часто, и вообще стоит ли планировать замену постоянного катетера. Периодическая катетеризация несет меньший риск, чем использование постоянного катетера, и должна использоваться вместо него при возможности. Антибиотикопрофилактика и катетеры, покрытие антибиотиками, больше не рекомендуются для пациентов, которые требуют долгосрочного установления постоянных катетеров.
Ключевые моменты
Долгосрочное использование катетеров мочевого пузыря увеличивает риск развития бактериурии, хотя бактериурия обычно бессимптомная.
Инфекция мочевыводящих путей с наличием симптомов может проявляться системными симптомами (например, лихорадка, изменения психического состояния, снижение артериального давления), незначительными симптомами или отсутствием симптомов, характерных для инфекции мочевыводящих путей.
Следует провести анализа мочи и бактериологическое исследование мочи, если у пациентов есть симптомы или высокий риск развития сепсиса (например, из-за снижения иммунитета).
Лечить следует аналогично другим осложненным инфекцией мочевыводящих путей.
Всякий раз, когда это возможно, следует избегать использования катетеров или удалять их при первой же возможности.
Инфекция мочевыводящих путей является одной из самых распространенных внутрибольничных инфекций и в большинстве случаев наблюдается на фоне катетеризации мо¬чевого пузыря. Основной причиной развития инфекций мочевых путей считаю патогенную и условно-патогенную микрофлору толстого кишечника пациента. Возбудителями катетер-ассоциированной инфекции в более, чем 40% случаев являются грамотрицательные микроорганизмы, реже — энтерококки, стафилококки и грибы. Из госпитальных штаммов микроорганизмов следует выделить Pseudomonas aeruginosa, Enterobacter agglomerans, Klebsiella spp., E. coli, Staphylococcus spp., Enterococcus faecalis, Proteus mirabilis, Candida albicans и др. Важным фактором риска развития бактериурии при катетеризации являет¬ся продолжительность нахождения катетера в мочевом пузыре. Если катетер находится там незначительное время, то большинство периодов бактериурии про¬текают бессимптомно или же краткосрочно. В большинстве случаев, они вызваны моно¬инфекцией. Другие патогенные и условно-патогенные микроорганизмы чаще всего проникают в организм человека при нахождении катетера в мочевом пузыре более 30 дней или же при нарушении правил катетеризации пациентов в случае однократной установки катетера. Аннотация: в данной статье рассматриваются основные факторы и причины развития катетер-ассоциированной инфекции мочеполовых путей. На основе современных статистических данных выявлена взаимосвязь между длительностью катетеризации и течением бактериемии, между нарушениями в процессе постановки мочевого катетера и вероятностью развития КАИМП.

2.Шуб Г.М., Швиденко И.Г., Корженевич В.И., Лунева И.О., Турковская О.В. Основы медицинской бактериологии, вирусологии и иммунологии/Под ред. Шуба Г.М.: Учебное пособие. – М.: Логос, 2001. – 264 с.
3. Коза, Н. М. Факторы риска и профилактика внутрибольничных инфекций мочевыводящих путей / Н. М. Коза // Пермский медицинский журнал. — 2015. — Т.32, № 1. — С. 135–140.
4. Эпидемиологическая безопасность — важнейшая составляющая обеспечения качества и безопасности медицинской помощи / Н. И. Брико, Е. Б. Брусина, Л. П. Зуева, Г. Е. Ефимов, О. В. Ковалишена, В. Л. Стасенко, И. В. Фельдблюм, В. В. Шкарин // Вестник РОСЗДРАВНАДЗОРА. — 2014. — № 4 — С. 8–13.
5. Васильев А.О., Говоров А.В., Пушкарь Д.Ю. Роль уретрального катетера в развитии катетер-ассоциированной инфекции. Урологические ведомости. 2017;7:19–20.
Европейско-Азиатские рекомендации по ведению пациентов с инфекциями, связанными с уретральным катетером, и по профилактике катетер-ассоциированных инфекций / П.Тенке, Б.Ковач, T. E. Бьерклунд Йохансен, T. Мацумото, П. А. Тамбья, К. Г. Набер // Клиническая микробиология и антимикробная химиотерапия. — 2008. — Т.10, № 3. — С.201–216.
Инфекции мочевыводящих путей это одна из наиболее актуальных проблем современной урологии. Эти инфекции зачастую приводят к развитию тяжелых гнойно-септических осложнений, бактериемии, сепсиса. Существует множество факторов, осложняющих течение инфекций мочевыводящих путей, такие как: нарушение уродинамики по обструктивному типу, наличие инородных тел в мочевыводящих путях.
Основной источник распространения патогенных микроорганизмов — катетеризация мочевого пузыря. В ходе оценки лечебно-диагностического процесса установлено, что доля катетеризаций мочевого пузыря среди всех госпитализированных пациентов составила 49,6 %, причем большая часть, примерно 69%, из них представлена мужчинами. [1, стр. 51]
Отдельной группой выделяют катетер-ассоциированные инфекции, при которых происходит инфицирование антибиотикорезистентными госпитальными штаммами или же представителями собственной кишечной микрофлоры пациента. По данным Клинических рекомендаций Европейской ассоциации урологов, опубликованных в 2007 г., более 5% пациентов ежегодно колонизируются патогенными микроорганизмами [6, стр. 202].
Мочевыводящие пути представляют собой один из главных источников нозокомиальных инфекций, в частности при наличии катетера в мочевом пузыре.. По данным ВОЗ, среди взрослых пациентов отделений реанимации и интенсивной терапии (ОРИТ) в странах с высоким уровнем дохода плотность инцидентности ИМП составляет 4,1 на 1000 катетеро-дней (95 % ДИ 3,7–4,6), в странах со средним и низким уровнем доходов (в том числе и в Российской Федерации) данный показатель выше — 8,8 на 1000 катетеро-дней (95 % ДИ 7,4–10,3) [1, стр. 52].
Ведущим фактором риска развития катетер-ассоциированной бактериурии является длительность катетеризации. Именно поэтому целью моей работы является на основе современных статистических данных проследить зависимость между вероятностью развития КАИМП и длительностью катетеризации.
Материал исследования: современные литературные исследования, статьи и публикации, касающиеся данной темы, и статистика заболеваемости КАИМП за последние 10 лет.
Методы исследования: статистический анализ данных.
Нормальная микрофлора человека как совокупность множества микробиоценозов, характеризующихся определенным составом, представлена в виде биопленки. Биопленка это скопление микроколоний микроорганизмов на полисахаридном каркасе, построенном из микробных полисахаридов и муцина, которые вместе образуют структурную популяцию на какой-либо твердой поверхности. Биопленки распространенны повсеместно, исключая отдельные стерильные органы человека. Так, нормальная микрофлора наружной части уретры и у мужчин, и у женщин представлена коринебактериями, микобактериями, грамотрицательными бактериями фекального происхождения и неспорообразующими анаэробами: пептококки, пептосптрептококки, бактероиды. Эти микроорганизмы обычно определяются в количестве 10 2 -10 4 в 1 мл мочи. [2, стр. 36]
Однако биопленка можно образовываться и на катетерах, мочеприемниках и других инородных телах. Такая биопленка состоит из 3х слоев: связующей, базальной прослойки, непосредственно прикрепляющейся к ткани; основного слоя и поверхностного, от которого отщепляются свободно плавающие микроорганизмы. Микроорганизмы, оказавшиеся внутри биопленки, защищены от агрессивных факторов окружающей среды и организма человека, свободно размножаются и заполняют весь основной слой биопленки. [3, стр. 137]
Уретральные катетеры могут принимать участие в подавлении некоторых защитных механизмов микроорганизмов (например, гликозаминогликановый слой на поверхности эпителия уретры), которые в норме сводят к минимуму контакт бактерий с эпителием и препятствуют образованию биопленок. [4, стр. 11]
Помимо этого, следует обратить внимание на характер поверхности катетера, от этого зависят скорость и характер роста микробной пленки. По данным последних исследований, риск возникновения ИМП на фоне уретрального катетера возрастает на 4-7,5% в зависимости от материала, из которого изготовлен катетер и особенности его поверхности.[5, стр.19]
Однако, патогенные и условно-патогенные штаммы микроогранизмов, несмотря на защитную роль катетеров, способны проникать в мочевыводящие пути человека. Например, во время постановки катетера вследствие недостаточной обработки места введения катетера может развиться бактериурия даже при интермитирующей катетеризации. Вопрос преимущественной обработки непосредственного места постановки катетера остается открытым, однако у госпитализированных пациентов попадание бактерий именно во время катетеризации остается ведущим.
Что же касается длительной катетеризации, она способствует образованию слизистой муфты, свободно располагающейся между стенкой катетера и слизистой оболочкой уретры, создавая благоприятную среду для инвазии и проникновения бактерий. В связи с этим ведущим фактором развития катетер-ассоциированной инфекции является длительность катетеризации.
Способы катетеризации и риски КАИМП
В зависимости от способа катетеризации выделяют однократную, кратковременную и длительную катетеризацию.
Так, при однократной катетеризации риск развития КАИМП повышен у женщин (вследствие высокой вероятности ретроградного направления развития инфекции), пациентов с задержкой мочи, при катетеризации в родах и послеродовом периоде (70-80%), при обструкции мочевыводящих путей увеличенной предстательной железой, при сахарном диабете, у ослабленных лежачих больных и пожилых людей (20-30%). [1, стр. 49]
Кратковременная катетеризация, проводимая у пациентов с нарушением произвольного мочеиспускания и недержанием мочи, может являться следствием развития бактериемий. Большинство эпизодов не сопровождается клиническими симптомами и вызывается, как правило, одним возбудителем. Согласно данным Азиатской ассоциации урологов, более 25% пациентов катетеризированы на 2-4 сутки госпитализации; у 10-30% из них развивается бактериурия. [4, стр.9] По современным данным, наиболее часто выделяют E. coli, P. aeruginosa, Klebsiella pneumoniae, Proteus mirabilis, Staphylococcus epidermidis, Enterococcus spp. и Candida spp.
Однако, многие современные исследования подтверждают корреляцию между полом пациента и преобладающим возбудителем ИМП [5стр.19]. При проведении бактериологических исследований посевов мочи от катетеризированных пациентов были сделаны выводы о том, что на посевах мочи мужчин и женщин были выявлены разные спектры возбудителей. Так, у пациентов урологического отделения мужского пола с КАИМП можно обнаружить грамположительные микроорганизмы S.epidermidis (50,0 %), у женщин чаще инфекцию вызывали грамотрицательные — E.coli (33,2 %), A. calcoaceticus (16,7 %).[3, стр.8]
Частота развития бактериемии значительно у пациентов с длительно установленными катетерами, подвергающихся эндоскопическим вмешательствам.
Несмотря на то, что вероятность развития КАИМП выше у пациентов с длительно установленным катетером, клинические проявления как следствие восходящей инфекции или бактериемии, наблюдаются редко. В длительных исследованиях показано, что ИМП являются причиной лихорадки менее чем в 10% случаев.[6, стр. 203] Именно поэтому, у катетеризированного пациента крайне важно исключить другие возможные причины развития бактериурии.
Важно отметить, что риск развития бактериемии при первичной установке катетера соответствует риску развития бактериемии при замене катетера у длительно катетеризированных пациентов. Относительно низкая частота развития ИМП с лихорадкой и бактериемии может быть обусловлена колонизацией менее вирулентными микроорганизмами. Например, при катетер-ассоциированных инфекциях, вызванных E. coli, у штаммов E. coli могут отсутствовать Р-фимбрии. По данным ВОЗ, до 20% пациентов колонизируются сразу после катетеризации.[1, стр. 51]
Доказательства того, что наличие постоянного катетера является фактором риска выраженной заболеваемости являются спорными.
Однако очевиден факт, что длительное персистирование патогенных возбудителей в организме человека значительно повышает вероятность развития КАИМП. При длительно катетеризировании нередко выделяются Pseudomonas, Proteus, Morganella и Acinetobacter spp. Приблизительно в 95% случаев бактериурия имеет полимикробный характер.[1, стр. 51]
Важно отметить, что в большинстве случаев микроорганизмы при длительной катетеризации населяют только катетер, что подтверждают результаты мочи, взятые путем надлобковой пункции.
Очевидно, что длительная катетеризация приводит к развитию различных осложнений: образованию мочевых камней, развитию простатита и абсцессу мошонки. Ряд данных подтверждает прямую зависимость риска развития данных заболеваний и длительностью катетеризации. Но, данные, касающиеся вероятности развития КАИМП остаются неоднозначными.
Таким образом, однозначное утверждение о том, что ведущим фактором развития КАБ является длительность катетеризации нельзя считать достоверным. Современные исследования не выявляют зависимости между длительностью катетеризации и вероятностью развития бактериурии, результаты их исследования считаются спорными.
Однако подтверждены данные о том, что бактериурии, связанные с кратковременной катетеризацией, в большинстве случаев протекают бессимптомно и вызываются, как правило, одним возбудителем. При увеличении времени катетеризации бактериурии становятся полимикробными. По региональным данным показатель заболеваемости ИМП в общей структуре ИСМП колеблется в пределах 0,004–0,02 на 1000 пролеченных пациентов.[1, стр. 50]
Следует сделать вывод о том, что для снижения риска развития КАИМП врачу прежде всего важно следить за тем, чтобы дренажная система оставалась закрытой, снизить риск перекрестной передачи инфекции между катетеризированными пациентами, рассматривать альтернативы постоянным уретральным катетерам и стремиться к снижению длительности катетеризации, в том числе и для снижения риска развития других сопутствующих заболеваний. [4, стр.12]
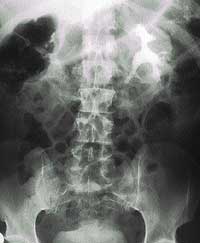
Инфекции мочевыводящих путей (ИМП) в большинстве стран мира — одна из наиболее актуальных проблем. Так, в США ИМП становятся причиной обращения к врачу 7 миллионов пациентов в год, а для миллиона пациентов являются причиной госпитализации [9]. Особую категорию ИМП составляют осложненные инфекции. Согласно современной классификации, к осложненным инфекциям мочевыводящих путей (ОИМП) относятся заболевания, объединенные наличием функциональных или анатомических аномалий верхних или нижних мочевых путей или протекающие на фоне заболеваний, снижающих общий иммунный статус.
Необходимо отметить, что группа ОИМП представлена крайне разнородными заболеваниями: от тяжелого пиелонефрита с явлениями обструкции и угрозой развития уросепсиса до катетер-ассоциированных инфекций МВП, которые могут исчезнуть самостоятельно после извлечения катетера.
Причины возникновения осложненных ИМП
Наиболее часто встречающиеся причины возникновения ОИМП приведены в табл. 1 [5].
Нарушения уродинамики вследствие обструкции МВП
На основании данных можно сделать вывод, что в большинстве случаев причиной осложненного течения ИМП становятся нарушения уродинамики по обструктивному типу при камнях различной локализации, стриктурах мочеточника и лоханочно-мочеточникового сегмента, инфравезикальной обструкции. Восстановление нормальной уродинамики является краеугольным камнем лечения любой мочевой инфекции. В тех случаях, когда причина возникновения обструкции не может быть ликвидирована немедленно, следует прибегать к дренированию верхних мочевых путей нефростомическим дренажем, а в случае инфравезикальной обструкции — к дренированию мочевого пузыря цистостомическим дренажем. Обе операции предпочтительно выполнять чрезкожно под ультразвуковым контролем.
Инородные тела МВП
Часто причиной осложнений при ИМП становятся инородные тела в мочевыводящих путях: конкременты почек и мочевого пузыря, различные дренажи. Лечение подобных инфекций длительное и подчас малоэффективное. Причина кроется в образовании на поверхности инородных тел микробной пленки, которая состоит из связанных между собой и с какой-либо поверхностью микроорганизмов, находящихся в различных фазах роста, их внеклеточных продуктов, соматических клеток, органического и неорганического материала [1].
Биопленка может быть ассоциирована не только с поверхностью дренажных трубок и конкрементов, но и с рубцово-измененными и некротизированными тканями, присутствующими в просвете мочевыводящих путей после предшествующих оперативных вмешательств. Так или иначе, но большинство осложняющих факторов благоприятствуют образованию биопленок. Бактерии, формирующие биопленку, значительно отличаются от планктонных свободно плавающих микробных клеток, не говоря уже о культуре микроорганизмов, использующейся для лабораторных тестов. Доза антибиотика, бактерицидная в отношении возбудителя в лабораторных условиях, зачастую не оказывает на биопленку никакого воздействия; кроме того, бактерии в биопленке более устойчивы к факторам окружающей среды. Вышесказанное свидетельствует о том, что именно биопленка в итоге является основной причиной возникновения трудностей, которые часто сопровождают лечение осложненной хронической персистирующей инфекции мочевыводящих путей.
Нейрогенные нарушения мочеиспускания
К заболеваниям, нарушающим нормальную уродинамику и осложняющим течение ИМП, относятся и нейрогенные нарушения мочеиспускания. Рассчитывать на успех лечения ИМП можно только после коррекции нейрогенных нарушений и восстановления нормальной уродинамики.
Сопутствующие заболевания
Особую группу составляют осложняющие факторы, связанные с наличием сопутствующих тяжелых заболеваний. Список этих заболеваний является предметом обсуждения, однако некоторые нозологии могут быть внесены в него без колебаний. Это заболевания, обусловливающие общее снижение иммунологической реактивности организма: сахарный диабет, иммунодефицитные состояния. К фоновым заболеваниям, значительно осложняющим течение ИМП, относятся также серповидно-клеточная анемия, почечная и печеночно-почечная недостаточность.
Катетер-ассоциированные ИМП
Факторы риска развития ОИМП
Помимо причин, обусловливающих возникновение ОИМП, существует ряд факторов риска развития этого состояния (табл. 3) [5].
Серьезную проблему для выбора эффективной терапии представляет сочетание ОИМП с хроническим простатитом. Хронический простатит — одно из самых трудных для диагностики и лечения заболеваний в урологии. Любое повышение внутриуретрального давления приводит к рефлюксу мочи и содержащихся в ней микроорганизмов в протоки периферической зоны в обход протоков центральной зоны предстательной железы, соустье которых с уретрой по своей природе почти клапанное. При несостоятельности внутреннего сфинктера нейрогенного происхождения или резекции шейки мочевого пузыря ткань простаты подвергается постоянному риску инфицирования и реинфицирования. Хронический бактериальный простатит характеризуется персистированием преимущественно грамотрицательных бактерий в секрете простаты и рецидивирующими ИМП [1, 3].
Этиология ОИМП
В табл. 2 приведены возбудители, наиболее часто являющиеся причиной возникновения ИМП [7]. Обращает на себя внимание, что на втором и третьем местах после наиболее распространенного возбудителя ИМП — кишечной палочки — при осложненных ИМП находятся Enterococcus spp. и Pseudomonas spp., а при катетер-ассоциированных инфекциях — дрожжевые грибки, отсутствующие при неосложненных ИМП.
Микробиологические особенности осложненных ИМП учитываются при выборе препарата для их лечения.
Лечение ОИМП
Лечение инфекции мочевых путей подразумевает проведение эффективной антибактериальной терапии при условии восстановления нормальной уродинамики и направлено на профилактику уросепсиса и возникновения рецидивов. Исключения составляют катетер-ассоциированные инфекции, в большинстве случаев исчезающие после удаления катетера. Открытым остается вопрос о необходимости антибактериальной терапии у пациентов с асимптоматической бактериурией. Большинство урологов считают, что лечение в подобных ситуациях не показано.
Дополнительной проблемой, значительно усложняющей лечение ОИМП, является высокая устойчивость микроорганизмов к большинству антибактериальных препаратов, длительно применяющихся в урологической практике. Госпитализация, неадекватные по длительности курсы лечения и некорректное назначение лекарственных препаратов приводят зачастую к возникновению антибиотико-устойчивых штаммов.
В нашей клинике в случае тяжелых инфекций мочевыводящих путей, а также в послеоперационном периоде после масштабных оперативных вмешательств мы в последнее время применяем новый антимикробный препарат группы фторхинолонов — L-изомер офлоксацина — левофлоксацин (таваник). Подобный выбор при назначении антибактериальной терапии объясняется доказанной способностью препаратов этой группы лучше проникать в биопленку [2, 9].
Поскольку на левофлоксацин приходится практически вся противомикробная активность в рацемической смеси изомеров, его активность in vitro в два раза превышает активность офлоксацина. Биодоступность препарата равняется 99 %, а особенности его фармакокинетики таковы, что 87 % препарата экскретируется с мочой в неизмененном виде [4]. Несмотря на наличие перекрестной устойчивости между левофлоксацином и другими фторхинолонами, некоторые микроорганизмы, устойчивые к хинолонам, могут проявлять чувствительность к левофлоксацину.
В исследованиях in vitro левофлоксацин доказал свою эффективность в отношении E.coli, Enterobacter, Klebsiella, Proteus Mirabilis, Pseudomonas aurugenosa, являющихся наиболее частыми возбудителями осложненной и неосложеннной форм урогенитальной инфекции (табл. 2).
Курс лечения таваником в дозе 250 мг однократно в течение суток на протяжении 10 дней проведен нами у 20 больных. Согласно полученным данным, эффективность и безопасность лечения были признаны хорошими и очень хорошими у 95% пациентов. Сходные результаты приводят в своих работах G. Richard, C. DeAbate et al., применявшие препарат по аналогичной схеме и добившиеся клинического эффекта у 98,1% пациентов [8]. Столь высокие показатели объясняются непродолжительностью применения левофлоксацина в урологической практике, чем и обусловлено отсутствие устойчивых к его действию штаммов микроорганизмов. Надо отметить, что устойчивость к препаратам этой фармакологической группы, связанная со спонтанными мутациями in vitro, встречается крайне редко [9].
Наряду с фторхинолонами в лечении ИМП широко применяются цефалоспорины II поколения (цефуроксим) и особенно III поколения (цефотаксим, цефтазидим и др.), а также карбапенемные антибиотики (имипенем/циластатин, меропенем).
При осложненных инфекциях МВП иногда назначают полусинтетические пенициллины (ампициллин, пиперациллин) и их комбинации с ингибиторами b-лактамаз (ампициллин/сульбактам, пиперациллин/тазобактам), ко-тримоксазол, аминогликозиды (обычно в комбинации с b-лактамами). Однако эффективность этих препаратов при ОИМП прогнозировать достаточно сложно из-за существенных различий в чувствительности возбудителей в зависимости от региона, стационара и источника развития инфекции (внебольничные или госпитальные). Таким образом, при назначении указанных препаратов в ходе терапии ОИМП следует опираться на данные бактериологического исследования мочи и учитывать чувствительность выделенных микроорганизмов.
Препараты нитрофуранового ряда — нефторированные хинолоны (налидиксовая кислота), оксихинолины (5-НОК) — не должны применяться для терапии ОИМП, так как они являются уроантисептиками, то есть создают терапевтическую концентрацию в моче, но не в паренхиме почек.
Длительность курса антибактериальной терапии ОИМП должна составлять не менее 14 дней. Более короткие курсы (7-10 дней) допустимы при назначении фторхинолоновых антибиотиков, выделении высокочувствительного возбудителя и устранении факторов, осложняющих течение ИМП [5].
В заключение хочется подчеркнуть, что лечение инфекций мочевыводящих путей — процесс сложный, длительный и зачастую малоэффективный, поскольку из всего многообразия существующих на сегодня антибактериальных препаратов ни один не обладает достаточно высокой эффективностью в отношении биопленок. Поэтому усилия врачей должны быть направлены преимущественно на профилактику возникновения подобных инфекций.
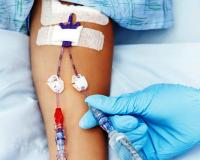
Катетер-ассоциированные инфекции кровотока (КАИК) – это нозокомиальные инфекционные осложнения, связанные с использованием внутрисосудистых катетеров. Клинически проявляются местными воспалительными изменениями (отек, болезненность, гиперемия в области катетера) или генерализованной инфекцией (фебрильная лихорадка, озноб, бактериемия). Для лабораторного подтверждения КАИК осуществляется посев крови на гемокультуру и микробиологическое исследование сосудистого катетера. При первых признаках КАИК производится удаление катетера, назначается антибактериальная, инфузионная терапия.
МКБ-10
Общие сведения

Причины
Установка внутрисосудистого устройства (ВСУ) – инвазивная манипуляция, сопряженная с нарушением целостности кожных покровов и сосудистой стенки, внедрением и оставлением в просвете сосуда инородного предмета. Катетерные инфекции кровотока в большинстве случаев ассоциированы с установкой центрального венозного катетера (ЦВК), инфузионной порт-системы, периферической венозной канюли. Чаще КАИК развиваются при катетеризации бедренной вены, реже – подключичной и внутренней яремной.
Развитию ангиогенных инфекций предшествует контаминация сосудистого устройства патогенными или условно-патогенными микроорганизмами. Источниками и причинами обсеменения могут стать:
- инфекции кожи в области сосудистого протеза (пиодермии);
- несоблюдение требований асептики при манипуляциях с ЦВК (ненадлежащая обработка операционного поля, рук врача);
- неадекватный выбор доступа, размера, типа и материала катетера;
- частые пункции сосудистого русла;
- плохой уход за сосудистым протезом.
Среди этиологических агентов, вызывающих КАИК, преобладают возбудители, которые являются самой частой причиной ВБИ: стафилококки (47%, из них золотистый стафилококк ‒ 25%), энтеробактерии (27%), ацинетобактеры (13%), синегнойная палочка (9%), кандиды (5%), энтерококки (3%) и др. Большую роль в возникновении внутрисосудистых инфекций, играет срок катетеризации: по опубликованным данным, через 7 дней нахождения катетера в вене КАИК развивается у 5%пациентов, через 1 месяц и более – у 36%.
Факторы риска
Инфицированию внутривенных катетеров способствуют сопутствующие состояния: сахарный диабет, иммунодефициты и иммуносупрессия, гипоальбуминемия. В группу повышенного риска по развитию катетер-ассоциированных инфекций кровотока входят пациенты, имеющие значительную катетеризационную нагрузку (длительную и неоднократную пункцию центральных вен):
- находящиеся на гемодиализе;
- получающие массивную инфузионно-трансфузионную терапию;
- проходящие химиотерапию;
- требующие проведения эфферентных методов детоксикации;
- нуждающиеся в парентеральном питании.
Патогенез
Механизм развития КАИК реализуется тремя основными путями. Чаще всего инфекция проникает в кровоток с обсемененных кожных покровов по наружной поверхности катетера (экстралюминально). Такой путь наиболее актуален в ранние сроки после постановки катетера (первые 10-15 суток). В последующем увеличивается доля интралюминального инфицирования, когда инфекция распространяется по внутренней стороне протеза через контаминированные инфузионные среды, канюли шприцев и систем для переливания. Также возможно гематогенное инфицирование, при котором возбудители оседают на катетере, разносясь с током крови из других источников (при пневмонии, панкреатите и пр.).
Внутрисосудистое устройство является инородным телом, поэтому в ответ на его введение организм вырабатывает различные белковые вещества, отграничивающие его от собственных тканей. В их числе ‒ фибрин и фибронектин, к которым легко прикрепляется коагулаза – фермент, продуцируемый многими патогенами, в частности, золотистым стафилококком и кандидой.
В результате такой адгезии внутри сосудистого протеза образуется биопленка, защищающая микробные колонии от воздействия антибиотиков и клеток иммунной системы. Это способствует переходу инфекции в персистирующую хроническую форму. Микробные биопленки образуются на внутренней поверхности имплантируемых устройств в 40% случаев.
Наличие биопленки снижает чувствительность патогенов к антибиотикам в сотни раз, способствует увеличению в структуре ВБИ доли антибиотикорезистентных штаммов, устойчивых практически ко всем известным противомикробным препаратам. Рост колоний микроорганизмов сопровождается фрагментацией биопленки и попаданием патогенов в кровоток, что приводит развитию бактериемии и сепсиса.
Классификация
В настоящее время в медицинских кругах используется классификация катетер-ассоциированных инфекций кровотока, рекомендованная Комитетом по контролю за госпитальными инфекциями (США). Согласно ей, различают следующие формы КАИК:
- Колонизация катетера, подтвержденная микробиологическим исследованием, при отсутствии любых клинических проявлений.
- Флебит: эритема, уплотнение, болезненность катетеризированной вены при пальпации.
- Ограниченная инфекция в месте установки катетера: инфильтрат, болезненность тканей, гиперемия, наличие гнойного отделяемого, очаг не более 2 см.
- Инфекция подкожного кармана, содержащего установленную порт-систему: гиперемия и некроз кожи над имплантируемым устройством, гнойное отделяемое в подкожном кармане.
- Туннельная инфекция: признаки воспаления, распространяющегося по ходу катетера более 2-х см от места его установки.
- Инфекции кровотока: бактериемия, фунгемия, сепсис, при которых один и тот же возбудитель высевается из кровотока и из удаленного ВСУ.
- КАИК, ассоциированные с инфузионной средой: контаминированными растворами, гемокомпонентами.
Симптомы КАИК
Катетер-асоциированные инфекции кровотока могут быть локальными (37%) и генерализованными (63%). Первые из них ограничены местом установки сосудистого протеза, вторые характеризуются бактериемией и системным поражением. Местные инфекции представлены инфильтратами, абсцессами, флебитами, непосредственно связанными с установленным внутрисосудистым устройством. Генерализованные КАИК проявляются сепсисом.
На высокую вероятность КАИК указывает появление признаков воспаления вокруг сосудистого катетера: уплотнение и покраснение кожи, боли, отделение гнойного экссудата, нарушение проходимости протеза. Общие симптомы инфекционного процесса ‒ лихорадка с ознобом ‒ обычно возникают через 20 минут–1,5 часа после использования катера (забора крови, вливания растворов). В тяжелых случаях лихорадка становится фебрильной и практически постоянной, снижается АД, нарастают признаки интоксикации. Развивается катетер-ассоциированный ангиогенный сепсис.
Осложнения
Длительное нахождение катетера в сосудистом просвете повышает риск развития тромбофлебита, тромбоза глубоких вен. КАИК могут осложниться септикопиемией ‒ формированием метастатических гнойных отсевов различной локализации. Среди них – бактериальный эндокардит, абсцедирующая пневмония, септический артрит, гематогенный остеомиелит и др. Причиной гибели пациентов становится септический шок, полиорганные нарушения, фатальные тромбоэмболии.
Диагностика
Клиническим критерием КАИК считается появление у пациента симптомов инфекции кровотока спустя 48 часов и более после установки ЦВК при отсутствии других источников инфекции. Однако из-за низкой специфичности клинических данных диагноз катетер-ассоциированной инфекции требует обязательного лабораторного подтверждения. Для этого производится парный посев:
- крови из периферической вены и дистального конца внутрисосудистого катетера (либо смыва из него). КАИК считается достоверной при одновременном выделении одной и той же гемокультуры из периферической крови и сосудистого зонда (>15 КОЕ полуколичественно и >102 КОЕ количественно);
- крови из сосудистого протеза и вены. На КАИК указывает более чем 3-кратное превышение количества колоний в образце крови из катетера по сравнению с венозным образцом.
Забор крови необходимо производить двукратно, до начала антибиотикотерапии, на высоте лихорадки. Для уточнения осложнений осуществляются инструментальные исследования. При подозрении на гнойный тромбофлебит выполняется УЗДС сосудов, флебография. Исключить или подтвердить септический эндокардит помогает трансторакальная ЭхоКС. Методами диагностики гнойных процессов костно-суставной системы является рентген, УЗИ суставов.
Ангиогенные инфекции дифференцируют с бактериемией, ассоциированной с другими первичными источниками: пневмонией, гнойными ранами, интраабдоминальными абсцессами и др.
Лечение катетер-ассоциированных инфекций кровотока
Системную антибиотикотерапию начинают, не дожидаясь результатов бакпосева, при необходимости в дальнейшем ее корректируют с учетом выделенной флоры и чувствительности. Обычно используются пенициллины, цефалоспорины, гликопептиды, аминогликозиды длительностью не менее 14 дней. Для терапии грибковой инфекции назначают амфотерицин В, флуконазол. При явлениях тромбофлебита показано введение антикоагулянтов, фибринолитиков. В отношении флегмон, гнойного артрита, остеомиелита, абсцессов различной локализации применяется соответствующая хирургическая тактика.
Прогноз
Катетер-ассоциированные инфекции кровотока являются серьезным вызовом современной медицине ввиду их распространенности и антибиотикорезистентности. Они удлиняют сроки госпитализации, утяжеляют исход основного заболевания, требуют значительных финансовых затрат для лечения. Неосложненные ангиогенные инфекции обычно разрешаются в течение нескольких суток. КАИК, осложненные местным нагноительным процессом или бактериемией, имеют серьезный прогноз и высокую летальность.
Профилактика
Современные протоколы четко регламентируют правила установки и ухода за ВСУ. Наибольшее внимание при этом уделяется соблюдению норм асептики и антисептики (дезинфекция операционного поля и рук персонала, хранение крышек катетеров в растворе хлоргексидина, обработка кожи и смена повязок вокруг ВСУ). Необходимо правильно осуществлять выбор внутрисосудистого устройства и места для катетеризации, максимально ограничивать срок эксплуатации внутривенных зондов, использовать гепариновые и антибактериальные замки.
1. Профилактика катетер-ассоциированных инфекций кровотока и уход за центральным венозным катетером (ЦВК). Клинические рекомендации. – 2017.
2. Комплексная клинико-этиологическая и эпидемиологическая характеристика катетер-ассоциированных инфекций кровотока/ Квашнина Д. В., Ковалишена О.В., Белянина Н.А.// Медицинский альманах. – 2017.
3. Распространенность и критерии диагностики катетер-ассоциированных инфекций кровотока/ Везирова З.Ш.// Вестник хирургии Казахстана. – 2014.
4. Инфекции, связанные с внутрисосудистыми устройствами: терминология, диагностика, профилактика и терапия/ Багирова Н.С.// Злокачественные опухоли. – 2014.
Читайте также:

