Реанимационные мероприятия при септическом шоке
Обновлено: 12.05.2024
Лечение септического шока. Принципы лечения септического шока.
Неотложному хирургическому лечению подлежат все очаги инфекционного воспаления, как первичные, так и вторичные, которые должны быть диагносцированы и санированы в самый короткий срок (вскрытие, вторичная хирургическая обработка, дренирование). Хирургическим методам санации инфекционных очагов принадлежит основная роль в борьбе с интоксикацией организма. Без их правильного и своевременного проведения любое другое лечение окажется бесперспективным. Исходя из вышеизложенного, естественной рекомендацией для начала лечения данной патологии была бы оперативная санация септического очага. Однако это не так.
Кратковременность протекания процесса и его бурный характер буквально в течение нескольких часов приводит к декомпенсации жизненно важных функций, без коррекции которых речи о взятии больного на операционный стол быть не может, тем более, что в настоящее время нет единой оперативной тактики лечения данной патологии. Исходя из этого, объем неотложной помощи при лечении септического шока должен быть следующим:
1. Устранение признаков ОДН и ОССН. По показаниям — перевод на ИВЛ.
2. Нормализация показателей центральной гемодинамики путем использования внутривенных инфузий декстранов, кристаллоидов, глюкозы и др. растворов под контролем ЦВД и почасового диуреза.
3. Коррекция основных показателей КЩС и водно-электролитного баланса.
4. Превентивное лечение неизбежного для данной патологии дистресс-синдрома легких.
5. Антибактериальная терапия. (Необходимо помнить, что назначение бактерицидных антибиотиков может усугубить течение шока, поэтому необходимо использовать бактериостатические препараты).
6. Купирование ДВС-синдрома.
7. Лечение аллергического компонента заболевания путем назначения глюкокортикоидов.
8. Симптоматическая терапия.
9. Санация очага инфекции начинается сразу после компенсации важнейших функций организма.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Симптомы септического шока
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
- Осмотр и физикальное исследование. Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
- Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов. У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение. При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
- Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.
Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
2. Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.
Респираторная поддержка при сепсисе - показания к ИВЛ
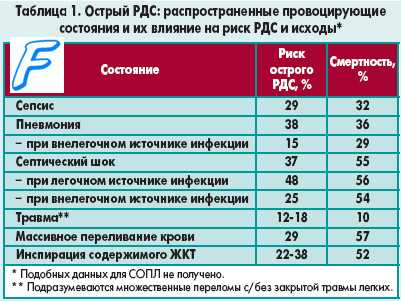
Дыхательные нарушения у больных сепсисом имеют сложный комплексный характер. По современным представлениям, спектр дыхательных нарушений при сепсисе является очень широким — от острого легочного повреждения (ОЛП) до острого респираторного дистресс-синдрома (ОРДС). ОЛП развивается примерно у 40 % больных сепсисом, ОРДС — у 25—42 %, причем частота возрастает при развитии артериальной гипотензии. В 1994 г. на согласительной евро-американской конференции по ОРДС было разработано унифицированное определение ОЛП и ОРДС.
Именно снижение величины дыхательного коэффициента положено в основу разделения респираторного дистресс-синдрома и острого легочного повреждения.
Эти критерии позволяют производить более точную эпидемиологическую оценку, несмотря на варьирование абсолютного количества случаев в пределах от 5 до 71 на 100 000 населения.
В 1988 г. была опубликована шкала легочных повреждений, которая позволяет не только разделить пациентов по тяжести повреждения, но и имеет прогностическое значение. Первоначальная оценка более 3,5 балла коррелировала с выживанием только 18 % пациентов, 2,5—3,5 — 30 %, 1,1— 2,4 - 59 %, а оценка ниже 1,1 балла — 66 %.
Критерии ОЛП и ОРДС
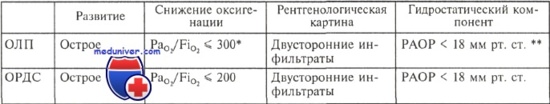
* PaО2/FiО2 — дыхательный коэффициент: отношение давления кислорода в артериальной крови к концентрации кислорода во вдыхаемом воздухе.
** РАОР —давление заклинивания в легочной артерии.
Дыхательная недостаточность является ведущим компонентом полиорганной дисфункции и недостаточности у больных сепсисом. Потребность в респираторной поддержке возникает у больных тяжелым сепсисом и септическим шоком. Сложность проблемы заключается в развитии тяжелого интерстициального отека и последующего повреждения легочной ткани, которые приводят к снижению эффективности переноса газов через альвеолярную мембрану легких.
Инсуфляция кислорода в дыхательные пути с помощью носовых катетеров или маски оказывает положительное влияние только на начальных стадиях острого легочного повреждения. Нарастание интерстициального отека легких приводит к тому, что обычно функционирующий объем альвеол оказывается недостаточным, и возникает необходимость в проведении ИВЛ с созданием положительного давления в дыхательных путях для увеличения объема участвующих в дыхании альвеол, однако создание высокого давления опасно развитием баротравмы легких.
Повышение содержания кислорода во вдыхаемом воздухе также имеет свои пределы из-за токсического действия кислорода на альвеолярную мембрану, нарушения синтеза сурфактанта (белок, поверхностно активное вещество, предупреждающее спадение альвеол) и возникновение других проблем. В тяжелых случаях респираторного дистресс-синдрома для обеспечения жизненнонеобходимых параметров вентиляции приходится прибегать к методам ИВЛ, которые находятся далеко за параметрами физиологического дыхания, требуют применения специального оборудования и тщательного многофакторного контроля.
Балльные шкалы острого легочного повреждения, респираторного дистресс-синдрома, степени легочного повреждения служат объективными показателями, на основании которых определяется тактика лечения и прогноз исхода заболевания у больных с наличием острой дыхательной недостаточности, развившейся в результате сепсиса. Рандомизированные исследования являются основой доказательной медицины. Однако проведение достаточных по репрезентативности рандомизированных исследований требует жесткой систематизации медицинских знаний. До получения данных рандомизированных исследований во многих областях медицины практические рекомендации могут содержать разделы, которые отражают мнение экспертов в определенной области, как правило, основанных на современных данных. Следование этим рекомендациям является хорошим тоном, но не обязательным с точки зрения доказательной медицины. Настоящий раздел содержит рекомендации по особенностям лечения острой дыхательной недостаточности больных сепсисом, основанные на данных нерандомизированных исследований.
Шкала легочного повреждения (общая сумма баллов делится на количество выявленных компонентов)
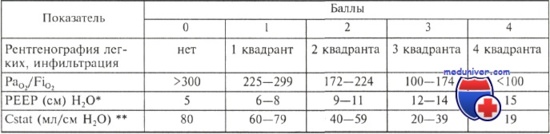
* PEEP — положительное давление в дыхательных путях в конце выдоха (произвольный параметр проведения ИВЛ).
** Cstat — растяжимость легочной ткани при определенных параметрах тестирования.
Адекватная респираторная поддержка улучшает оксигенацию и результаты лечения больных сепсисом
В некоторых случаях адекватная оксигенация (показатель сатурации О2 выше 90 %) может быть достигнута с помощью инсуфляции кислорода через назальную канюлю или лицевую маску. Эндотрахеальная интубация применяется для создания постоянного положительного давления в конце выдоха (PEEP), повышения среднего давления в дыхательных путях и снижения концентрации кислорода во вдыхаемом воздухе (FiО2
Целью респираторной терапии является достижение адекватной доставки кислорода в ткани, испытывающие гипоксию, в условиях нарушенной микроциркуляции.
При проведении ИВЛ изменением различных параметров можно добиваться различного давления на вдохе и достигать различных результатов лечения. Показатели измерения ок-сигенации методом пульоксиметрии (определение насыщения кислорода в крови с помощью специального датчика, надеваемого на ногтевое ложе пальцев рук) обычно хорошо коррелируют с насыщением артериальной крови кислородом.
Однако у 7 % пациентов такой корреляции не наблюдается из-за выраженной тахикардии, низкого сердечного индекса или высокого давления заклинивания легочной артерии (определяемого с помощью катетера Сван-Ганса, установленного в устье легочной артерии).
У таких больных необходимо проводить мониторинг оксигенации артериальной крови и поддерживать сатурацию на уровне 88—90 % (что соответствует насыщению артериальной крови кислородом на уровне 60 мм рт. ст.) с концентрацией кислорода во вдыхаемой смеси (FiО2) ниже 60 %.
Необходимо избегать применения неинвазивной вентиляции с положительным давлением у больных сепсисом
Метод неинвазивной вентиляции легких с положительным давлением заключается в применении специальной герметичной лицевой маски, позволяющей точно дозировать концентрацию кислорода во вдыхаемом воздухе и создавать положительное давление в дыхательных путях. Этот метод является эффективным у небольшой группы пациентов в сознании без увеличения бронхиальной секреции на ранних этапах развития дыхательной недостаточности (менее 72 ч), что редко бывает при ОЛП/ОРДС. Задержка дыхания с началом ИВЛ может быть причиной развития осложнений, поэтому применение этого метода не рекомендуется для больных сепсисом.
Интубация трахеи не влияет на исход лечения больных сепсисом, в то время как проведение ИВЛ достоверно улучшает результаты лечения больных с сепсисом и дыхательной недостаточностью. Показания к интубации трахеи и началу проведения ИВЛ у больных с сепсисом основаны на стандартных клинических признаках дыхательной недостаточности. Показанием для начала ИВЛ являются: тахипноэ (частота дыхания более 40 в минуту), включение в акт дыхания дополнительной мускулатуры, нарушение сознания, тяжелая гипоксемия, которая не может быть компенсирована инсуфляцией кислорода.
При ОЛП/ОРДС поддержание нормального уровня рН и содержания углекислоты в артериальной крови (Расо2) необязательно. Применение умеренной гиперкапнии позволяет снижать дыхательный объем у пациентов с ОЛП/ОРДС, которым проводится ИВЛ, что позволяет снизить высокое давление на воохе, риск баро-и волюмотравмы легких. Выбор параметров ИВЛ, который позволяет снизить дыхательный объем и объем минутной вентиляции для предотвращения чрезмерного растяжения альвеол и повреждения легочной ткани у больных сепсисом, приводит к повышению концентрации углекислоты в артериальной крови (Расо2). Безопасность и эффективность применения ИВЛ с гиперкапнией были показаны в серии некрупных исследований.
До настоящего времени допустимый верхний предел концентрации углекислоты в артериальной крови точно не определен. Накопление углекислоты приводит к пропорциональному снижению рН артериальной крови. Считается необходимым поддерживать параметры ИВЛ, которые бы обеспечивали адекватную оксигенацию крови и не способствовали снижению рН крови ниже 7,2. Применение таких параметров ИВЛ не сопровождалось развитием осложнений и приводило к снижению летальности больных сепсисом.
Применение низкого дыхательного объема улучшает результаты лечения ОЛП, а вентиляция с ограничением по давлению не способствует улучшению результатов лечения ОЛП. При применении ИВЛ у больных с ОЛП необходимо использовать небольшие дыхательные объемы (примерно 6 мл/кг идеальной массы тела) для поддержания плато давления в конце выдоха ниже 30 см Н2О. Крупные исследования по сравнению влияния разных дыхательных объемов на уровень инспираторного давления дали различные результаты, причем причина этих различий до настоящего времени непонятна. В недавнем крупном исследовании больных с ОЛП было показано, что общая летальность снизилась на 10 % в группе пациентов, которым проводилась ИВЛ с дыхательным объемом 6 мл/кг идеальной массы тела. Эта методика недавно была поддержана группой международных экспертов.
Применение ИВЛ в положении на животе позволяет улучшить газообмен пациентов с ОЛП, однако не доказано его положительного влияния на исходы лечения больных сепсисом. Применение ИВЛ в положении пациента на животе способствует дополнительному включению в дыхание задненижних отделов легких. Показанием к применению этого метода является тяжелый ОРДС с необходимостью применения высоких концентраций кислорода во вдыхаемой смеси (FiО2 > 60 %). Ограничением для его применения являются наличие противопоказаний и отсутствие опыта проведения ИВЛ в этом положении у персонала ОРИТ. В некрупных рандомизированных исследованиях были доказаны физиологические преимущества этого метода ИВЛ, заключавшиеся в повышении оксигенации крови у 65 % больных с ОЛП/ОРДС.
Улучшение газообмена наблюдалось даже спустя 18 ч после перекладывания пациента на спину. Однако ограниченное количество пациентов и отсутствие четких показаний, методики применения и оценки эффективности снижают его привлекательность.
Ингаляция оксида азота влияет на оксигенацию, но не влияет на результаты лечения больных с ОЛП/ОРДС. Оксид азота (NО) является физиологическим регулятором базального тонуса сосудов. Известно, что физиологическим ответом на гипоксию является спазм сосудов легких. Вдыхание оксида азота может оказывать мощное сосудорасширяющее действие на легочные сосуды и улучшать оксигенацию. Именно поэтому были проведены исследования, которые подтвердили, что ингаляция оксида азота улучшала оксигенацию и способствовала снижению отека легких у больных с ОЛП/ОРДС путем влияния на гидростатическое давление.
Однако улучшение оксигенации и снижение отека легких не приводило к достоверному снижению летальности, поэтому рекомендуется ограничить применение оксида азота у пациентов с тяжелой гипоксемией, представляющей угрозу для жизни, которая не может быть компенсирована применением обычных методов ИВЛ. До настоящего времени нет определенных рекомендаций по рациональному применению инфузионной терапии у больных ОЛП/ОРДС. Из-за отсутствия данных сравнительных исследований, посвященных инфузионной терапии, нет жестких правил применения кристаллоидных и коллоидных препаратов. У больных с ОЛП/ОРДС и синдромом высокой сосудистой проницаемости следует комбинировать применение кристаллоидных и коллоидных растворов во избежание избыточной гидратации легких. Коллоидные растворы рационально назначать пациентам с низким онкотическим давлением крови. Нет рекомендаций по оптимальному объему инфузионной терапии несмотря на то, что с момента открытия этого синдрома дискуссии в отношении инфузионной терапии были очень острыми. Имеются противоречивые мнения экспертов относительно пользы коллоидных и кристаллоидных растворов.
Считается, что для разрешения актуальных вопросов требуется более пристальное внимание специалистов и проведение крупных исследований в этой области.
Применение кортикостероидных гормонов не показано для профилактики и лечения ранней (экссудативной) фазы ОРДС. В отношении лечения поздней (фибропролиферативной) фазы ОРДС данных пока недостаточно. Не рекомендуется применять кортикостероидные гормоны пациентам с высоким риском или наличием критериев ОЛП/ОРДС. Не получено данных, подтверждающих пользу применения кортикостероидных гормонов для профилактики и раннего лечения ОРДС. Эффективность применения кортикостероидов в более поздней фазе ОРДС в настоящее время изучается.
Ежедневная тренировка спонтанного дыхания и следование протоколу отлучения пациентов от ИВЛ снижает продолжительность ИВЛ. Всем пациентам с приемлемым уровнем респираторной поддержки и стабильным состоянием рекомендуется ежедневно производить оценку возможности самостоятельного дыхания. Для выявления пациентов, способных к самостоятельному дыханию, необходимо проводить короткий скрининг и тренировать самостоятельное дыхание. Из процесса скрининга исключаются пациенты, нуждающиеся в проведении ИВЛ. Основными критериями, указывающими на возможность начала отлучения от ИВЛ, являются: снижение потребности в концентрации кислорода во вдыхаемом воздухе ниже 50 % (FiО2
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Сепсис представляет собой клинический синдром с развитием жизнеугрожающей органной дисфункции, вызванный нарушением регуляции ответа на инфекцию. При септическом шоке происходит критическое снижение перфузии тканей; также может возникнуть острая недостаточность многих органов, в том числе легких, почек и печени. Наиболее частыми причинами у иммунокомпетентных пациентов являются различные виды грамположительных и грамотрицательных бактерий. Обуславливающими факторами у пациентов с иммунодефицитом могут быть нетипичные виды бактериальной или грибковой инфекции. Симптомами являются лихорадка, гипотония, олигурия и помутнение сознания. Диагноз основывается на клинических исследованиях в сочетании с результатами бактериологического посева, указывающими на наличие инфекции; раннее выявление и лечение имеют решающее значение. В качестве лечения используют агрессивную инфузионную реанимацию, антибиотики, хирургическое удаление инфицированного участка или некротической ткани, дренаж гнойных выделений и поддерживающую терапию.
Сепсис представляет собой спектр заболеваний с риском смерти, колеблющимся от умеренного (например, 10%) до значительного (например, > 40%) в зависимости от различных возбудителей и факторов со стороны хозяина, наряду со своевременностью выявления и предоставления соответствующего лечения.
Септический шок является разновидностью сепсиса со значительно повышенным уровнем смертности в связи с серьезными нарушениями кровообращения и/или клеточного метаболизма. Септический шок предполагает наличие персистирующей гипотонии (определяется как потребность в вазопрессорах для поддержания среднего артериального давления ≥ 65 мм.рт.ст., и уровень сывороточного лактата > 18 мг/дл [2 ммоль/л], несмотря на реанимационные мероприятия, проведенные в достаточном объеме [1] Общие справочные материалы Сепсис представляет собой клинический синдром с развитием жизнеугрожающей органной дисфункции, вызванный нарушением регуляции ответа на инфекцию. При септическом шоке происходит критическое. Прочитайте дополнительные сведения ).
Понятие синдрома системного воспалительного ответа (ССВО), которое определяется специфическими нарушениями жизненно важных функций и результами лабораторных исследований, уже давно используется для выявления сепсиса на ранних стадиях. Однако было обнаружено, что критерии ССВО имеют недостаточную чувствительность и специфичность при повышенном риске смерти, что является основным аспектом использования такой концептуальной модели. Отсутствие специфичности может быть обусловлено тем, что ССВО чаще является адаптивным, а не патологическим ответом.
Общие справочные материалы
1. Singer M, Deutschman CS, Seymour CW, et al: The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA 315:801–810, 2016.
Этиология сепсиса и септического шока

Большинство случаев септического шока вызвано внутрибольничными грамотрицательными бактериями или грамположительными кокками и часто возникает у пациентов с ослабленным иммунитетом и у пациентов с хроническими заболеваниями. Реже возбудителями являются грибы рода Candida. Следует заподозрить послеоперационную инфекцию (глубокую или поверхностную) в качестве причины септического шока у пациентов, которые недавно перенесли операцию. Неспецифическая, редкая форма шока, вызванная токсинами стафилококков и стрептококков называется синдромом токсического шока Синдром токсического шока (СТШ) Синдром токсического шока обусловлен экзотоксинами стафилококков или стрептококков. Проявления включают высокую температуру, гипотонию, диффузную эритематозную сыпь и полиорганную недостаточность. Прочитайте дополнительные сведения .
Лейкопению (особенно, связанную с раком или лечением цитотоксическими лекарственными средствами)
Наличие инвазивных устройств (в том числе эндотрахеальных трубок, сосудистых или мочевых катетеров, дренажей и других инородных материалов)
Первоочередным лечением являются антибиотики или кортикостероиды
К наиболее распространенным локализациям инфекции относятся легкие, мочевые и желчные пути и желудочно-кишечный тракт.
Патофизиология сепсиса и септического шока
Патогенез септического шока полностью не изучен. Воспалительные агенты (например, бактериальный токсин) провоцируют выработку провоспалительных медиаторов, включая фактор некроза опухоли (ФНО) и интерлейкин-1 (ИЛ-1). Эти цитокины вызывают нейтрофильно-эндотелиальную клеточную адгезию, активируют механизмы свертывания крови и обуславливают образование микротромбов. Они также способствуют высвобождению других медиаторов, включая лейкотриены, липоксигеназу, гистамин, брадикинин, серотонин и IL-2. Им противостоят противовоспалительные медиаторы, такие как IL-4 и IL-10, в результате механизма обратной отрицательной связи.
Сначала артерии и артериолы расширяются, уменьшается периферическое артериальное сопротивление; сердечный выброс, как правило, увеличивается. Этот этап называется тепловым шоком. Позже сердечный выброс может уменьшиться, падает артериальное давление (с увеличением периферического сопротивления или без него) и появляются типичные признаки шока.
Даже на стадии увеличенного сердечного выброса вазоактивные медиаторы приводят к тому, что кровоток минует капилляры (распределительный дефект). Ослабленный капиллярный ток в результате такого шунтирования, наряду с обструкцией капилляров микротромбами, уменьшает доставку кислорода и снижает выведение углекислого газа и других продуктов распада. Гипоперфузия приводит к дисфункции, а иногда и к недостаточности одного или более органов, включая почки, легкие, печень, мозг и сердце.
Коагулопатия может развиться из-за внутрисосудистой коагуляции с участием основных факторов свертывания крови, усиленного фибринолиза, и чаще комбинации обоих.
Симптомы и признаки сепсиса и септического шока

Симптомы и признаки сепсиса могут быть малозаметными и часто легко принимаются за проявления других заболеваний (например, белой горячки Делирий Делирий – это острое, преходящее, обычно обратимое, флуктуирующее нарушение внимания, восприятия и уровня сознания. Причинами, приводящими к развитию делирия, могут быть практически любые заболевания. Прочитайте дополнительные сведения , первичной дисфункции сердца, эмболии легких Тромбоэмболия Легочной Артерии (ТЭЛА) Тромбоэмболия легочной артерии – это окклюзия легочных артерий тромбами любого происхождения, чаще всего образующихся в крупных венах ног или малого таза. Факторами риска тромбоэмболии легочной. Прочитайте дополнительные сведения ), особенно у послеоперационных больных. У пациентов с сепсисом, как правило, отмечаются лихорадка, тахикардия, обильное потоотделение и тахипноэ; артериальное давление остается в норме. Также могут присутствовать другие признаки инфекции, являющейся ричиной сепсиса. По мере ухудшения состояния больного с сепсисом или при развитии септического шока ранним симптомом, особенно у пожилых или у совсем молодых людей, может быть спутанность сознания или снижение активности. Артериальное давление снижается, однако кожа остается парадоксально теплой. Позже, конечности становятся прохладными и бледными с периферическим цианозом и покрываются пятнами. Дисфункция органов приводит к появлению дополнительных симптомов и признаков в зависимости от пораженного органа (например, олигурия, одышка).
Диагностика сепсиса и септического шока
Артериальное давление (АД), частота сердечных сокращений и мониторинг кислородного статуса
Общий анализ крови (ОАК) с лейкоцитарной формулой, уровень электролитов, креатинина и лактата
Показания инвазивного центрального венозного давления (ЦВД), PaO2 и сатурации кислорода в центральной вене (ScvO2)
Бактериологический посев крови, мочи и других потенциальных очагов инфекции, в том числе из ран у пациентов после операции
Сепсис подозревают, когда у пациента с известной инфекцией развиваются системные симптомы воспаления или органной дисфункции. Аналогичным образом, у пациентов с необъяснимыми признаками системного воспаления необходимо изучить наличие инфекционных заболеваний в анамнезе, провести медицинский осмотр и лабораторные исследования, которые включают общий анализ мочи и бактериологический посев мочи (особенно у пациентов с постоянными катетерами), бактериологический посев крови и посевы других подозрительных жидкостей организма. Пациентам с подозрением на хирургическую или скрытую причину сепсиса может потребоваться УЗИ, КТ или МРТ в зависимости от предполагаемого источника. При тяжелом сепсисе уровни C-реактивного белка и прокальцитонина в крови часто повышены и могут облегчить постановку диагноза, но эти показатели не являются специфичными. Диагноз основывается прежде всего на клинических проявлениях.

Другие причины шока (например, гиповолемия, инфаркт миокарда Острый инфаркт миокарда (ИМ) Острое поражение миокарда - это миокардиальный некроз в результате резкой обструкции коронарной артерии. Симптоматика данных состояний включает дискомфорт в грудной клетке, сопровождающийся. Прочитайте дополнительные сведения [ИМ]) должны быть исключены с помощью анамнеза, объективного обследования, электрокардиограммы и анализа кардиомаркеров в сыворотке крови. Даже в отсутствие инфаркта миокарда гипоперфузия, обусловленная сепсисом, может привести к появлению признаков ишемии на электрокардиограмме, включая неспецифические отклонения ST-T, инверсии зубца T, наджелудочковые и желудочковые аритмии.
Важно выявить дисфункцию органа как можно раньше. Был разработан ряд систем оценки, но шкала динамической оценки органной недостаточности (шкала SOFA) и шкала quick SOFA (qSOFA) были одобрены в отношении риска смерти и являются относительно простыми в использовании. Шкала Quick SOFA основывается на показателях артериального давления, частоте дыхания и на баллах по шкале комы Глазго и не требует ожидания лабораторных результатов. Для пациентов с подозрением на инфекцию, которые не находятся в отделении интенсивной терапии (ОИТ), шкала qSOFA является более эффективным прогностическим показателем смертности в стационаре, чем синдром системной воспалительной реакции (SIRS) и шкала SOFA. Для пациентов с подозрением на инфекцию, которые находятся в отделении интенсивной терапии (ОИТ), шкала SOFA является более эффективным прогностическим показателем смертности в стационаре, чем синдром системной воспалительной реакции (SIRS) и шкала qSOFA (1 Справочные материалы по диагностике Сепсис представляет собой клинический синдром с развитием жизнеугрожающей органной дисфункции, вызванный нарушением регуляции ответа на инфекцию. При септическом шоке происходит критическое. Прочитайте дополнительные сведения ).
Пациенты с ≥ 2 из следующих критериев соответствуют критериям SIRS и должны пройти дальнейшие клинические и лабораторные исследования:
Температура > 38 ° C (100,4 ° F) или
Частота сердечных сокращений > 90 ударов/минута
Частота дыхания > 20 вдохов/минута или PACO2
Количество лейкоцитов > 12 000/мкл (12 X 10 9 /л), 9 /л) или незрелые (палочкоядерные) нейтрофилы > 10%
Пациентам с ≥ 2 из следующих критериев qSOFA должны быть проведены дальнейшие клинические и лабораторные исследования:
Частота дыхания ≥ 22 вдохов/минута
Систолическое артериальное давление ≤ 100 мм.рт.ст.
Проводят общий анализ крови, исследование газового состава артериальной крови, рентгенологическое исследование органов грудной клетки, анализ уровней сывороточных электролитов, азота мочевины крови и креатинина, PCO2 и печеночных проб. Измерение уровня лактата в сыворотке или сатурации кислорода в центральной вене (ScvO2) (или сразу оба анализа) могут помочь в определении лечения. Количество лейкоцитов может быть уменьшено ( 4 000/мкл [ 9 /л]) или увеличено (> 15 000/мкл [> 15 × 10 9 /л]), а количество полиморфноядерных нейтрофилов может снизиться до 20%. В ходе развития сепсиса количество лейкоцитов может увеличиваться или уменьшаться в зависимости от тяжести сепсиса или шока, иммунологического статуса пациента и этиологии инфекции. Одновременное использование кортикостероидов может увеличить количество лейкоцитов и, таким образом, маскировать изменения в анализах, связанные с проявлениями болезни.

Гипервентиляция с дыхательным алкалозом Дыхательный алкалоз Дыхательный алкалоз – это первичное снижение парциального давления углекислого газа (PСО2) с компенсаторным снижением уровня бикарбонат-ионов (HCO3 − ) или без него; рН может быть высоким. Прочитайте дополнительные сведения (низкий PaCO2 и повышенный pH артериальной крови) появляются рано, частично как реакция компенсации лактацидемии. Уровень сывороточного бикарбоната обычно низкий, а уровни лактата в сыворотке и крови повышаются. Шок прогрессирует, метаболический ацидоз ухудшается, и снижается pH крови. Раннее развитие гипоксемической дыхательной недостаточности Острая гипоксемическая дыхательная недостаточность (ОГДС, ОРДС) Острая гипоксемическая дыхательная недостаточность представляет собой острую артериальную гипоксемию, которая является стойкой к дополнительной подаче кислорода. Это вызвано внутрилегочным шунтированием. Прочитайте дополнительные сведения приводит к снижению соотношения PaO2:FIO2, а иногда и к выраженной гипоксемии с PaO2 70 мм.рт.ст. Диффузные инфильтраты на рентгенограмме грудной клетки могут появляться вследствие развития острого респираторного дистресс-синдрома ОРДС Острая гипоксемическая дыхательная недостаточность представляет собой острую артериальную гипоксемию, которая является стойкой к дополнительной подаче кислорода. Это вызвано внутрилегочным шунтированием. Прочитайте дополнительные сведения (ОРДС). Уровень мочевины и креатинина обычно прогрессивно возрастают в результате почечной недостаточности. Значения билирубина и трансаминазы могут повыситься, хотя клинически выраженная печеночная недостаточность редко встречается у пациентов с нормальными исходными функциональными пробами печени.
У большинства пациентов с тяжелым сепсисом развивается относительная недостаточность коры надпочечников Вторичная надпочечниковая недостаточность Вторичная недостаточность надпочечников – это гипофункция надпочечников, обусловленная дефицитом адренокортикотропного гормона (АКТГ). Симптомы такие же, как при болезни Аддисона, и включают. Прочитайте дополнительные сведения (т.е. нормальный или немного повышенный исходный уровень кортизола, который не увеличивается в значительной степени в ответ на дальнейший стресс или экзогенный адренокортикотропный гормон [АКТГ]). Функция надпочечников может быть проверена путем измерения сывороточного кортизола в 8 часов утра, уровень 5 мкг/дл ( 9 мкг/дл (

Измерения гемодинамики с помощью центрального венозного или легочного артериального катетера Методика Мониторинг пациентов реанимационных отделений зависит от непосредственного наблюдения и объективного обследования и является периодическим, в зависимости от болезни пациента. Непрерывное наблюдение. Прочитайте дополнительные сведения могут использоваться, когда неясен тип шока или необходимы большие объемы жидкости (например, > 4–5 литров 0,9% физиологического раствора в течение 6–8 часов).
Эхокардиография, проведенная у постели больного в отделении интенсивной терапии, является практичным и неинвазивным альтернативным методом контроля гемодинамики. При септическом шоке сердечный выброс увеличивается, а периферическое сосудистое сопротивление уменьшается, в то время как при других формах шока Этиология и классификация Шок – это состояние гипоперфузии органов с вытекающей клеточной дисфункцией и смертью. Механизмы могут включать снижение объема циркулирующей крови, снижение сердечного выброса и вазодилатацию. Прочитайте дополнительные сведения сердечный выброс, как правило, снижается, а периферическое сосудистое сопротивление увеличивается.
Показатели ЦВД и давления заклинивания в лёгочной артерии (ДЗЛА) вероятнее всего будут в норме при септическом шоке, в отличие от гиповолемического, обструктивного или кардиогенного шока.

Анафилактический шок. Клиника шока. Диагностика шока ( шокового состояния ). Лечение шока. Лечение гиповолемического шока.
Принципы лечения травматического, ожогового шока. Лечение септического шока. Лечение анафилактического шока.
Методы оживления. Искусственная вентиляция легких. Восстановление сердечной деятельности.
Остановка сердца.

Реанимация больных.

Синдром эндогенной интоксикации и сепсис.
Лечение сепсиса и респираторный дистресс синдром.

Лечение респираторного дистресс синдрома легких.

ДВС синдром и острая почечная недостаточность.
Печеночная недостаточность.
Язвы. Эмболии. Шок.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

