Реферат по лабораторной диагностике холеры
Обновлено: 26.04.2024
Возбудитель холеры относится к роду Vibrio. Это изогнутая, грамотрицательная, не образующая споры палочка, имеющая один полярно расположенный жгутик. По чувствительности к специфическому фагу (IV тип по Мукерджи) различают два биотипа холерного вибриона — классический (возбудитель азиатской холеры) и Эль-Тор. Каждый из них по 0-антигену подразделяется на 3 серологических типа: Огава (АВ), Инаба (АС) и редко встречающийся Гикошима (АВС), который некоторые авторы рассматривают как вариант серотипа Огава. Н-антиген холерных вибрионов — общий для всех серотипов.
Холерные вибрионы образуют термолабильный экзотоксин — холероген (относительная молекулярная масса — 82—84 кд). Он состоит из комплекса тяжелой субъединицы А, активирующей аденилатциклазу, и субъединицы В, представленной 4—6 легкими цепями и обеспечивающей связывание холеро-гена с рецепторами эпителиальных клеток тонкой кишки.
Биолого-патогенетические свойства возбудителя
Миновав желудочный барьер, вибрионы попадают в тонкую кишку с благоприятной для них средой и заселяют (колонизируют) поверхность кишечного эпителия. Процесс колонизации включает в себя хемотаксис вибрионов к слою слизи, покрывающему верхушки ворсинок тонкой кишки, проникновение через эту слизь, адгезию к рецепторам на исчерченной каемке кишечных эпителиоцитов и размножение на поверхности эпителия ворсинок и крипт. У больных холерой возбудитель может быть обнаружен на всем протяжении желудочно-кишечного тракта. В желудке при рН не менее 5,5 вибрионы не обнаруживаются, в стуле их концентрация достигает 10 6 —10 7 (иногда ^—Ю 9 ).
Размножившись до определенной концентрации, возбудитель вызывает заболевание посредством вырабатываемого им холерогена. Основную роль в развитии болезни играют вибрионы, которые находятся в тесной связи со слизистой оболочкой тонкой кишки, так как они выделяют холероген в непосредственной близости от его рецепторов на эпителиальных клетках — ган-глиозида GM1. После прикрепления холерного токсина к ганглиозиду субъединица А проходит через мембраны внутрь эпителиальной клетки, где происходит высвобождение фрагмента А1. Последний энзиматически расщепляет НАД и передает его АДФ-рибозную половину на регуляторный протеин аденилатциклазного комплекса, находящегося на внутренней стороне мембраны эпителиоцита. В результате происходит активация аденилатциклазы, приводящая к повышению содержания цАМФ — одного из внутриклеточных стимуляторов кишечной секреции. Связывание холерного токсина с рецепторами на эпителиальных клетках происходит чрезвычайно быстро (через 1—3 мин); биохимические нзменения в клетке являются необратимыми.
Возникающее заболевание сопровождается потерей огромных количеств жидкости с низким содержанием белка и высокой концентрацией ионов натрия, калия, хлоридов, гидрокарбонатов. Эта жидкость по составу отличается как от экссудата, так и от транссудата и ближе к составу кишечного секрета.
Восприимчивость
К холерному вибриону восприимчивы люди всех возрастов. Чаще и тяжелее болеют холерой лица, злоупотребляющие алкоголем или перенесшие резекцию желудка. Кислотность желудочного сока играет важную роль в определении минимальной инфицирующей дозы — в опытах на добровольцах при нейтрализации желудочного сока гидрокарбонатом натрия количество вибрионов, необходимых для воспроизведения специфического процесса у человека, уменьшается с 10" до 10 4 —10 Ь микробных клеток.
Клинические особенности
Иммунологическая диагностика
Обнаружение антигена. Возбудитель холеры и его специфические антигены (корпускулярный, растворимый, холероген) выявляют в фекалиях, рвотных массах, крови, дуоденальном и кишечном содержимом, желчном пузыре, в объектах окружающей среды (смывы с различных предметов), в воде открытых водоемов, сточных водах, гидробионтах и др.
Из современных методов индикации антигенов холерного вибриона наибольшее распространение получила РНГА, чувствительность которой с антительными эритроцитарными диагностикумами составляет 10 5 —10 1 ' бактерий в 1 мл или 0,04 мкг/мл 0-антигена. При клинически выраженных формах холеры, когда в испражнениях больных содержится огромное количество вибрионов (10'—10 9 в 1 мл), прямое исследование фильтратов прогретых на водяной бане испражнений в РНГА с антительным диагностикумом позволяет дать ответ о наличии специфического антигена уже через 2-—3 ч. Рвотные массы больных, испражнения вибриононосителей и контактных лиц, содержащие меньшее количество вибрионов, целесообразно исследовать после предварительного 6-часового подращивания на 1% пептонной воде. При исследовании испражнений и рвотных масс оказалось, что лишь в 52% случаев диагноз холеры был подтвержден бактериологически у больных, в анамнезе значительной части которых имелось указание на употребление антибиотиков при появлении первых признаков заболевания. С помощью РНГА заболевания холерой удалось дополнительно установить еще у 21 % больных [Поляков И. И. и др., 1973]. При исследовании испражнений, содержимого кишечника и желчного пузыря умерших от острых кишечных заболеваний, испражнений здоровых лиц и проб воды обычно в практических условиях наблюдали полное совпадение результатов серологического и бактериологического методов исследования, что позволяет считать РНГА с антительным эритроцитарным диагностикумом достаточно надежным экспресс-методом при массовом обследовании на холеру.
Некоторыми авторами при индикации специфических антигенов холерного вибриона отдается предпочтение РТНГА. Холерные диагностикумы для этой реакции готовят из бараньих или человеческих О (I) группы эритроцитов, сенсибилизированных холерными 0-антигенами. Чувствительность метода — 10 4 —10 6 бактерий в 1 мл при исследовании нативных испражнений и 10'—10 5 — после предварительного подращивания. Минимальное количество 0-антигена, выявляемого с помощью РТНГА, равно 0,04—0,16мкг/мл. РТНГА дает положительные результаты у 91% больных холерой, у 40% ре-конвалесцентов и 12% контактировавших с больными, 0-антиген холерного вибриона может быть определен через 1 мес от начала заболевания в фекалиях у всех переболевших людей, а спустя 5—6 мес — у половины обследованных, что, по-видимому, свидетельствует о более длительной экскреции специфического антигена в нежизнеспособной форме. Совпадение результатов бактериологического метода и РТНГА, по различным данным, наблюдается в 63—100% случаев. Имеющиеся материалы дают основание считать целесообразным широкое испытание РТНГА.
Положительную оценку при диагностике холеры получил МФА, позволяющий выявлять холерные вибрионы при содержании их не менее 10° в 1 мл. Использовать МФА целесообразно при исследовании нативного материала от больных и трупов. У больных холерой положительные результаты с помощью МФА были получены в течение 2 ч в 70—90% наблюдений при полном совпадении с результатами бактериологического анализа. Применение МФА при исследовании воды и смывов возможно лишь после предварительного подращивания или концентрирования материала. Представляется перспективным использование иммунотушевой окраски холерных вибрионов.
Содержание сывороточных IgM и I gG на протяжении болезни сопоставимо с аналогичными показателями в контрольной группе, хотя есть данные об увеличении уровня IgM в острой стадии и снижении его в период реконвалесценции. Некоторые исследователи не установили разницы в содержании IgA при поступлении больных в стационар и в стадии реконвалесценции; другие отмечают повышение его уровня у переболевших [Покровский В. И., Малеев В. В., 1978; Адамов А. К., 1981]. Сказанное не дает достаточных оснований утверждать, что изменение уровня сывороточных иммуно-глобулинов при холере носит специфический характер.
Специфическая активность иммуноглобулинов различных классов зависит от формы и длительности инфекционного процесса при холере. Антитела в сыворотке крови переболевших относятся, преимущественно к IgM. У вибриононосителей продуцируются, наоборот, высокоактивные IgG-антитела. Активность IgA-антител в сыворотке крови вибриононосителей незначительно выше по сравнению с больными. Чем тяжелее протекает заболевание, тем выше активность продуцируемых антител, относящихся к иммуноглобули-нам класса М, и ниже активность IgG-антител.
Самым простым и легко воспроизводимым методом определения антимикробных антител является РА с живыми культурами холерного вибриона, но чувствительность этой реакции ограничена. Диагностические титры (1 : 40 и выше) появляются, как правило, к концу 1-й недели заболевания, но лишь у 19,7% больных холерой. Исследование парных сывороток, полученных с интервалом 7—10 дней при наличии 4-кратного и более нарастания титров антител увеличивает частоту положительных результатов до 89,6%
Гораздо большее значение придается в настоящее время выявлению виб-риоцидных антител. Вибриоцидный тест (ВТ) является более чувствительным в сравнении с РА, давая высокие титры, особенно у реконвалесцентов холеры (до 1 : 100 000). Нужно, однако, иметь в виду, что вибриоцидные антитела (титры до 1:1000) могут обнаруживаться и в сыворотках невакцинированных здоровых людей, никогда не болевших холерой, и у лиц, инфицированных бруцеллами, Yersinia enterocolitica 09, цитробактером. Агглютинины относительно меньше чувствительны к такой неспецифической стимуляции. Как и РА, ВТ позволяет регистрировать подъем специфических антител (4-кратный и более) у 90—95% больных с бактериологически подтвержденным диагнозом холеры [Watanabe Y., 1974].
В качестве антигена в РА и ВТ используют холерные вибрионы обоих серотипов. При необходимости пользоваться одним предпочтение отдают серотипу Огава, который чаще, чем Инаба, вступает в перекрестные реакции с гетерологичным серотипом холерного вибриона и реже дает неспецифические реакции с микробами других семейств.
Хотя эти серологические реакции являются наиболее чувствительными, необходимость применения в них живых вибрионов создает определенные трудности при массовых обследованиях. Поэтому наибольшего внимания заслуживают антигенные эритроцитарные диагностикумы, которые позволили внедрить в практику РНГА и РТНГА. Эти реакции обладают достаточной чувствительностью и специфичностью, позволяя обнаруживать антитела у больных и переболевших холерой в титрах 1 : 640—1 : 1280. Наблюдаемые различия в титрах при параллельном использовании РНГА и ВТ обусловлены главным образом различиями в физико-химической природе выявляемых антител: IgG-антитела более эффективно обнаруживают бактерицидным методом (ВТ), IgM-антитела — в РНГА.
Для выявления антитоксинов в сыворотках применяют РН, результаты которой учитывают по отсутствию холерогенного эффекта в перевязанной петле тонкой кишки взрослых кроликов, в кишечнике крольчат-сосунков, на коже морских свинок (кроликов) в опытах in vivo и по отсутствию цитото-ническогодействия в культуре клеток СНО и Y-1 — в опытах in vitro. Наиболее стандартизованы кожная проба и модель перевязанной кишечной петли. У 73% больных в эндемичном по холере районе с помощью кожной пробы выявлено диагностически значимое 9-кратное и большее увеличение титров токсиннейтрализующих антител. Частота сероконверсии вибриоцидных антител и агглютининов в этой же группе больных была выше и составила 98 и 88% соответственно [Watanabe Y., 1974].
Титры антитоксических антител, регистрируемые ИФМ, выше титров, которые определяются с помощью внутрикожного теста, что обусловлено различиями в выявляемых классах иммуноглобулинов: кожный тест документирует нейтрализующую активность только IgG-антител, вероятно, в силу их большей авидности, в то время как ИФМ регистрирует и уровень IgM-антител.
Таким образом, изучение титров и динамики нарастания циркулирующих антител в сыворотках крови больных при холере расширяет возможности ее лабораторной диагностики. Ретроспективный диагноз холеры с большей степенью вероятности может быть установлен в РА и ВТ, но лишь на основании изучения парных сывороток больных. Определение уровня антитоксина полезно в тех случаях, когда необходимо исключить предшествующую специфическую вакцинацию, так как антитела этого типа не индуцируются существующими холерными вакцинами и очень редко встречаются у здоровых людей. Однако подъем антитоксических титров у больных на фоне диагностически значимой сероконверсии вибриоцидных и агглютинирующих антител повышает достоверность серологической диагностики холеры.
Возникновение патологического процесса, вызванного холерными вибрионами, ведет к появлению антител к этим микроорганизмам и во внешних секретах пищеварительного тракта — интестинальной жидкости (ко-проантитела) и слюне. Отличительной чертой динамики копроантител является их раннее появление (у 72% — на 2—3-й день болезни, у 100% — на 4-й день) и быстрое исчезновение из кишечного содержимого. В интестинальной жидкости выздоравливающих от холеры людей антитела против вибрионов относятся к иммуноглобулинам A, G и М, но преобладающими являются SIgA-антитела, количество которых у больных холерой возрастает примерно в 30 раз, но составляет около '/4 того, что наблюдается у больных диарейными заболеваниями нехолерной этиологии. Последнее связано с адсорбцией SIgA на холерных вибрионах, что приводит к стойкому снижению количества вибрионов в стуле больных и сокращает продолжительность их выделения из кишечника. Концентрация этого иммуноглобулина и время его появления в кишечном содержимом не связаны с сывороточным IgA. Количество IgG- и IgM-антител в кишечном содержимом реконвалесцентов холеры также увеличивается (в 5—7 раз), но в фекалиях антитела класса IgM не обнаруживают.
Для обнаружения антител в интестинальной жидкости и фекалиях больных могут быть использованы ВТ, РИМ с холерными антигенами, меченными радиоактивным йодом, непрямой флюоресцентно-серологический метод. Нарастание специфических антител указывает на наличие заболевания холерой. Однако кишечно-копрологическая диагностика холеры еще недостаточно разработана.
В слюне больных и вибриононосителей повышен уровень IgA и IgG. Одновременно появляются и специфические антитела (агглютинины), содержание которых у больных холерой выше, чем у виброноносителей (30 АЕ и 14 АЕ соответственно). Диагностический титр специфических агглютининов слюны может оказаться значительно ниже сывороточного.
Определению состояния повышенной чувствительности при холере в реакции ГЗТ посвящены единичные работы. Описаны положительные аллергические реакции у 89% переболевших холерой и вибриононосителей (при отсутствии их в контрольной группе) в ответ на внутрикожное введение аллергена из убитых холерных вибрионов. Однако имеющихся данных недостаточно, чтобы высказать суждение об аллергической перестройке организма при холере или о диагностической значимости применяемых тестов.
Иммунитет
После болезни у человека вырабатывается выраженный иммунитет, который сохраняется длительное время, поэтому случаи повторных заболеваний холерой крайне редки. Опыты на добровольцах показали, что в течение 3 лет (срок наблюдения) люди, переболевшие холерой в результате экспериментального заражения, оставались устойчивыми к повторному заражению холерными вибрионами [Levine M. et al., 1981].
Основная роль в иммунитете к холере принадлежит антителам, продуцируемым местно (в кишке), хотя определенный вклад в защиту вносят циркулирующие антитела при высоких их концентрациях, когда они проникают в просвет кишки из крови, что подтверждено экспериментами на животных. Более высокий уровень защиты наблюдается при синергическом действии антибактериальных и антитоксических антител в кишке. Основная роль антибактериальных SIgA состоит в том, чтобы препятствовать хемотаксису вибрионов к эпителию и прилипанию их к поверхности слизистой оболочки кишечника в результате блокирующего действия на структуры для прилипания (лиганды) на поверхности бактериальных клеток. Снижение колонизации и адгезии холерных вибрионов способствует более быстрому их выведению из кишечника при перистальтике и тем самым уменьшает возможность приживления возбудителя в кишечном тракте.
Действие кишечных IgA-антител против холерогена обусловлено главным образом блокадой его В-субъединицы, что препятствует связыванию токсина с ганглиозидом GM1 на поверхности эпителиоцитов. Антитела, блокирующие токсический сайт на А-субъединице холерогена, оказывают меньшее защитное действие.
Список использованной литературы
Диагностика холеры. Микробиологическая диагностика холеры. Выявление холеры. Лечение холеры. Профилактика холеры.
Основу диагностики холеры составляют выделение и идентификация возбудителя. Цели исследований на холеру — выявление больных и вибрионосителей; установление причины смерти при исследовании трупов; контроль над эффективностью лечения больных и санации носителей, контроль над объектами внешней среды и эффективностью дезинфекционных мероприятий. Материал для исследований — испражнения, рвотные массы, жёлчь, секционный материал (фрагменты тонкой кишки и жёлчного пузыря), постельное и нательное бельё, вода, ил, сточные воды, гидробионты, смывы с объектов окружающей среды, пищевые продукты, мухи и др.
При проведении исследований на холеру необходимо соблюдать следующие правила:
• Материал исследований на холеру следует доставлять в лабораторию не позже 2 ч после забора (так как возбудитель быстро погибает, особенно в испражнениях). При невозможности срочной доставки образцы помещают в транспортные среды (1% пептоннан вода с рН 8,2-8,6).
• Ёмкости для материала нельзя обеззараживать химическими веществами, так как возбудитель чувствителен даже к их следовым количествам. Все образцы помещают в герметически закрываемую транспортную тару.
Посев холеры проводят на жидкие среды обогащения, щелочной МПА, элективные и дифференциально-диагностические среды (например, TCBS-arap). Изучают рост на первой среде накопления и выполняют высев на щелочной агар и вторую среду накопления (что повышает высевае-мость возбудителя). Если на первом этапе при исследовании нативного материала ускоренными методами получают положительные результаты, пересев на вторую среду накопления не проводят. Подозрительные колонии пересевают для выделения чистых культур.

Затем определяют морфологические, биохимические свойства и антигенную структуру холеры с помощью агглютинирующих О-, OR-, Инаба- и Огава-антисывороток. Важное диагностическое значение имеет типирование с помощью холерных диагностических бактериофагов. Все V. cholerae лизируются бактериофагом IV группы, а вибрионы биовара Эль-Тор — фагами группы V.
• Для ускоренной биохимической идентификации возбудителя холеры предложен набор СИБ из 13 тестов (оксида-за, индол, лактоза, глюкоза, сахароза, манноза, арабиноза, маннит, инозит, аргинин, орнитин, лизин), дифференцирующий от представителей семейства Enterobacteriaceae, бактерий родов Plesiomonas, Aeromunas и др.
• При выделении Vibrio cholerae группы, отличной от 01, возбудитель необходимо типировать с помощью других антисывороток. При выделении таких бактерий от больного с диареей обязательным считают проведение всего объёма исследований дли диагностики холеры.
• Определение AT в крови больных холерой носит вспомогательный характер. Их выявляют в РА, а также путём обнаружения вибриоцидных AT и антитоксинов.
Лечение холеры. Профилактика холеры.
Восполняют потерю жидкости и электролитов, проводят антибактериальную терапию холеры препаратами тетрациклинового ряда. Альтернативные антибактериальные препараты — левомицетин, ко-тримоксазол и фуразолидон.
Профилактика холеры включает организацию санитарно-гигиенических мероприятий, предупреждающих занос заболевания; проведение санитарно-просветительной работы среди населения; раннее выявление больных и носителей; массовое профилактическое назначение тетрациклинов в районах эпидемической опасности.
Для специфической иммунопрофилактики холеры разработаны убитая вакцина из штаммов Огава и Инаба, холероген-анатоксин для подкожного введения и бивалентная вакцина из анатоксина и О-Аг Огава и Инаба. Эффективность их использования не превышает 60-70%, невосприимчивость сохраняется в течение 3-6 мес, поэтому вакцин опрофилактику применяют по эпидемиологическим показаниям.
В очагах холеры хороший эффект даёт профилактический приём тетрациклина.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Холера - инфекция вызванная Vibrio cholerae: диагностика, лечение, профилактика
Вибрионы — мелкие грамотрицательные изогнутые подвижные оксидаза-положительные палочки. Существует более восьми видов вибрионов. Для человека наиболее патогенны Vibrio cholerae и V. parahaemolyticus.
Выделяют серогруппы холерного вибриона (Vibrio cholerae), различающиеся по строению соматического О-антигена. Холеру вызывают только O1 и 0139 серогруппы. Вибрионы выживают в солянокислой среде желудка, проникают через слизь к эпителию тонкой кишки, прикрепляются к нему посредством GM1-ганглиозида и начинают вырабатывать полимерный белковый токсин (холерный токсин), стимулирующий повышенный синтез внутриклеточной аденилатциклазы, в результате чего увеличивается секреция воды и электролитов в просвет кишечника. Эпидемиология инфекции вызванной Vibrio cholerae.
Холерой болеют исключительно люди. Заболевание передаётся через заражённую воду и пищу (особенно морские продукты). Чаще всего инфекцию регистрируют в развивающихся странах, где население в недостаточной мере соблюдает санитарные нормы и отсутствует необходимое количество безопасных источников водоснабжения. Эпидемия часто возникает при изменении условий окружающей среды, при этом деятельность человека (войны, исход беженцев, миграция населения) способствует распространению инфекции. Периодически возникали пандемии холеры, в настоящее время идёт седьмая пандемия.
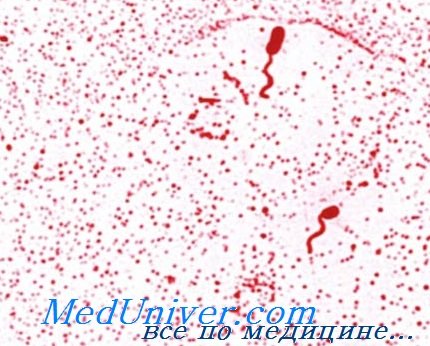
Возбудитель холеры - Vibrio cholerae
Клинические признаки холеры. Большинство заболеваний, вызываемых V. cholerae, протекает в лёгкой форме или бессимптомно. Клиника холеры характеризуется появлением обильного безболезненного жидкого стула (до 20 л в день), который может сопровождаться рвотой. Со временем развивается тяжёлое обезвоживание организма, осложняющееся электролитными нарушениями.
Диагностика инфекции вызванной Vibrio cholerae. В эндемичных регионах диагностика заболевания основана на данных клинической картины. Методом лабораторной экспресс-диагностики холеры является иммобилизация вибрионов группоспецифической антисывороткой в копрофильтрате. Для культивирования микроорганизма используют селективные среды, содержащие цитрат тиосульфата, соли жёлчи и сахарозу или обогащенный щелочной пептонный бульон.
Для подтверждения диагноза исследуют также биохимические свойства возбудителя и проводят серотипирование.
Лечение холеры. Проводят пероральную регидратацию растворами солей и глюкозы; тяжелобольным пациентам рекомендовано внутривенное введение жидкости. Применяют тетрациклин, ципрофлоксацин (коротким курсом), которые снижают тяжесть клинических проявлений.
Профилактика и контроль инфекции вызванной Vibrio cholerae. Для профилактики эпидемий холеры большое значение имеет санитарное просвещение населения и использование безопасных источников водоснабжения. В настоящее время проходят клинические испытания нескольких вакцин (живых ослабленных; вакцин, состоящих их субъединиц холерного токсина).
Видео эпидемии холеры и их значение
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Холера – это острая кишечная инфекция, возникающая при поражении человека холерным вибрионом. Холера проявляется выраженной частой диареей, обильной многократной рвотой, что приводит к значительной потере жидкости и обезвоживанию организма. Признаками дегидратации служат сухость кожных покровов и слизистых, снижением тургора тканей и сморщивание кожи, заострение черт лица, олигоанурия. Диагноз холеры подтверждается результатами бактериологического посева каловых и рвотных масс, серологическими методиками. Лечение включает изоляцию холерного больного, парентеральную регидратацию, терапию тетрациклиновыми антибиотиками.
МКБ-10
Общие сведения
Холера – особо опасная инфекция, вызываемая энтеропатогенной бактерией Vibrio cholerae, протекающая с развитием тяжелого гастроэнтерита и выраженным обезвоживанием вплоть до развития дигидратационного шока. Холера имеет тенденцию к эпидемическому распространению и высокую летальность, поэтому отнесена ВОЗ к высокопатогенным карантинным инфекциям.
Наиболее часто эпидемические вспышки холеры регистрируются в странах Африки, Латинской Америки, Юго-Восточной Азии. По оценкам ВОЗ, ежегодно холерой заражается 3-5 млн. человек, около 100-120 тыс. случаев заболевания заканчивается смертельно. Т. о., на сегодняшний день холера остается глобальной проблемой мирового здравоохранения.

Причины холеры
Характеристика возбудителя
На сегодняшний день обнаружено более 150 типов холерных вибрионов, различающихся по серологическим признакам. Холерные вибрионы разделяют на две группы: А и В. Холеру вызывают вибрионы группы А. Холерный вибрион представляет собой грамотрицательную подвижную бактерию, выделяющую в процессе жизнедеятельности термостабильный эндотоксин, а также термолабильный энтеротоксин (холероген).
Возбудитель устойчив к действию окружающей среды, сохраняет жизнеспособность в проточном водоеме до нескольких месяцев, до 30 часов в сточных водах. Хорошей питательной средой является молоко, мясо. Холерный вибрион погибает при химическом дезинфицировании, кипячении, высушивании и воздействии солнечного света. Отмечается чувствительность к тетрациклинам и фторхинолонам.
Пути передачи
Резервуаром и источником инфекции является больной человек или транзиторный носитель инфекции. Наиболее активно выделяются бактерии в первые дни с рвотными и фекальными массами. Тяжело выявить инфицированных лиц с легко протекающей холерой, однако они представляют опасность в плане заражения. В очаге обнаружения холеры обследованию подвергаются все контактировавшие, вне зависимости от клинических проявлений. Заразность с течением времени уменьшается, и обычно к 3-й неделе происходит выздоровление и освобождение от бактерий. Однако в некоторых случаях носительство продолжается до года и более. Удлинению срока носительства способствуют сопутствующие инфекции.
Холера передается бытовым (грязные руки, предметы, посуда), пищевым и водным путем по фекально-оральному механизму. В настоящее время особое место в передаче холеры отводится мухам. Водный путь (загрязненный источник воды) является наиболее распространенным. Холера является инфекцией с высокой восприимчивостью, наиболее легко происходит заражение людей с гипоацидозом, некоторыми анемиями, зараженных гельминтами, злоупотребляющих алкоголем.
Симптомы холеры
Диспепсия
Инкубационный период при заражении холерным вибрионом продолжается от нескольких часов до 5 дней. Начало заболевания острое, обычно ночью или утром. Первым симптомом выступает интенсивный безболезненный позыв к дефекации, сопровождающийся дискомфортным ощущением в животе. Первоначально стул имеет разжиженную консистенцию, но сохраняет каловый характер. Довольно быстро частота дефекаций увеличивается, достигает 10 и более раз за сутки, при этом стул становится бесцветным, водянистым.
При холере испражнения обычно не зловонны в отличие от других инфекционных заболеваний кишечника. Повышенная секреция воды в просвет кишечника способствует заметному увеличению количества выделяемых каловых масс. В 20-40% случаев кал приобретает консистенцию рисового отвара. Обычно испражнения имеют вид зеленоватой жидкости с белыми рыхлыми хлопьями, похожими на рисовые.
Нередко отмечается урчание, бурление в животе, дискомфорт, переливание жидкости в кишечнике. Прогрессирующая потеря жидкости организмом приводит к проявлению симптомов обезвоживания: сухость во рту, жажда, затем появляется ощущение похолодания конечностей, звон в ушах, головокружение. Эти симптомы говорят о значительном обезвоживании и требуют экстренных мер по восстановлению водно-солевого гомеостаза организма.
Поскольку к диарее зачастую присоединяется частая рвота, потеря жидкости усугубляется. Рвота возникает обычно спустя несколько часов, иногда на следующие сутки после начала диареи. Рвота обильная, многократная, начинается внезапно и сопровождается интенсивным ощущением тошноты и болью в верхней части живота под грудиной. Первоначально в рвотных массах отмечаются остатки непереваренной пищи, затем желчь. Со временем, рвотные массы также становятся водянистыми, приобретая иногда вид рисового отвара.
При рвоте происходит быстрая потеря организмом ионов натрия и хлора, что приводит к развитию мышечных судорог, сначала в мышцах пальцев, затем всех конечностей. При прогрессировании дефицита электролитов мышечные судороги могут распространиться на спину, диафрагму, брюшную стенку. Мышечная слабость и головокружение нарастает вплоть до невозможности подняться и дойти до туалета. При этом сознание полностью сохраняется.
Выраженной болезненности в животе, в отличие от большинства кишечных инфекций, при холере не отмечается. 20-30% больных жалуются на умеренную боль. Не характерна и лихорадка, температура тела остается в нормальных пределах, иногда достигает субфебрильных цифр. Выраженная дегидратация проявляется снижением температуры тела.
Дегидратация
Дегидратация организма различается по стадиям:
- на первой стадии потеря жидкости не превышает 3% от массы тела;
- на второй - 3-6%;
- на третьей - 6-9%;
- на четвертой стадии потеря жидкости превышает 9% массы тела.
При потере более 10% массы тела и ионов происходит прогрессирование дегидратации. Возникает анурия, значительная гипотермия, пульс в лучевой артерии не прощупывается, периферическое артериальное давление не определяется. При этом диарея и рвота становятся менее частыми в связи с параличом кишечной мускулатуры. Данное состояние называют дегидратационным шоком.
Нарастание клинических проявлений холеры может прекратиться на любом этапе, течение может быть стертым. В зависимости от тяжести дегидратации и скорости нарастания потери жидкости различают холеру легкого, среднетяжелого и тяжелого течения. Тяжелая форма холеры отмечается у 10-12% пациентов. В случаях молниеносного течения развитие дегидратационного шока возможно в течение первых 10-12 часов.
Осложнения
Холера может осложняться присоединением других инфекций, развитием пневмонии, тромбофлебита и гнойного воспаления (абсцесс, флегмона), тромбозом сосудов брыжейки и ишемией кишечника. Значительная потеря жидкости может способствовать возникновению расстройств мозгового кровообращения, инфарктом миокарда.
Диагностика
Тяжело протекающая холера диагностируется на основании данных клинической картины и физикального обследования. Окончательный диагноз устанавливают на основании бактериологического посева каловых или рвотных масс, кишечного содержимого (секционный анализ). Материал для посева необходимо доставить в лабораторию не позднее 3-х часов с момента получения, результат будет готов через 3-4 суток.
Существуют серологические методики выявления заражения холерным вибрионом (РА, РНГА, виброцидный тест, ИФА, РКА), но они не являются достаточными для окончательной диагностики, считаясь методами ускоренного ориентировочного определения возбудителя. Ускоренными методиками для подтверждения предварительного диагноза можно считать люминисцентно-серологический анализ, микроскопию в темном поле иммобилизованных О-сывороткой вибрионов.
Лечение холеры
Поскольку основную опасность при холере представляет прогрессирующая потеря жидкости, ее восполнение в организме является основной задачей лечения этой инфекции. Лечение холеры производится в специализированном инфекционном отделении с изолированной палате (боксе), оборудованной специальной койкой (койка Филипса) с весами и посудой для сбора испражнений. Для точного определения степени дегидратации ведут учет их объема, регулярно определяют гематокрит, уровень ионов в сыворотке, кислотно-щелочной показатель.
Первичные регидратационные мероприятия включают восполнение имеющегося дефицита жидкости и электролитов. В тяжелых случаях производится внутривенное введение полиионных растворов. После этого производят компенсаторную регидратацию. Введение жидкости происходит в соответствии с ее потерями. Возникновение рвоты не является противопоказанием к продолжению регидратации. После восстановления водно-солевого баланса и прекращения рвоты начинают антибиотикотерапию. При холере назначают курс препаратов тетрациклинового ряда, а в случае повторного выделения бактерий – хлорамфеникол.
Специфической диеты при холере нет, в первые дни могут рекомендовать стол №4, а после стихания выраженной симптоматики и восстановления кишечной деятельности (3-5-й день лечения) - питание без особенностей. Перенесшим холеру рекомендовано увеличить в рационе содержащие калия продукты (курага, томатный и апельсиновый соки, бананы).
Прогноз и профилактика
При своевременном и полном лечении после подавления инфекции наступает выздоровление. В настоящее время современные препараты эффективно действуют на холерный вибрион, а регидратационная терапия способствует профилактике осложнений.
Специфическая профилактика холеры заключается в однократной вакцинации холерным токсином перед посещением регионов с высоким уровнем распространения этого заболевания. При необходимости через 3 месяца производят ревакцинацию. Неспецифические меры профилактики холеры подразумевают соблюдение санитарно-гигиенических норм в населенных местах, на предприятиях питания, в районах забора вод для нужд населения. Индивидуальная профилактика заключается в соблюдении гигиены, кипячении употребляемой воды, мытье продуктов питания и их правильной кулинарной обработке. При обнаружении случая холеры эпидемиологический очаг подлежит дезинфекции, больные изолируются, все контактные лица наблюдаются в течение 5-ти дней на предмет выявления возможного заражения.
Читайте также:

