Респираторные инфекции с кишечными синдромом
Обновлено: 06.05.2024
Резюме
Актуальность Эпштейна - Барр вирусной инфекции объясняется широкой циркуляцией вируса Эпштейна - Барр среди детского и взрослого населения, его тропностью к иммунокомпетентным клеткам с пожизненной персистенцией после первичного инфицирования и полиморфизмом клинических проявлений от субклинических форм, инфекционного мононуклеоза до формирования онкологических, аутоиммунных гематологических заболеваний. Персистенция Эпштейна -Барр вируса приводит к подавлению клеточного звена иммунитета, снижению продукции интерферонов и факторов неспецифической защиты, что способствует реактивации персистирующей инфекции, чаще всего без мононуклеозоподобного синдрома, и появлению атипичных мононуклеаров в крови с формированием лимфопролиферативного, интоксикационного, астеновегетативного синдромов, длительного субфебрилитета, что диктует необходимость применения иммунокоррегирующей терапии. В статье приведен клинический случай, в котором изложены описание и анализ течения хронической Эпштейна - Барр вирусной инфекции у ребенка дошкольного возраста (5 лет 8 мес.) с отягощенным преморбидным фоном. Эпизоды реактивации хронической персистирующей инфекции протекали под маской острой респираторной инфекции с лимфопролиферативным синдромом, гнойного тонзиллита, гнойного аденоидита. Терапия, включавшая антибиотики, препараты с противовирусной активностью коротким курсом, бактериальные лизаты, физиотерапию, имела временный и непродолжительный эффект. В силу отсутствия полного мононуклеозоподобного синдрома в клинике и атипичных мононуклеаров в гемограмме обследование на Эпштейна - Барр вирусную инфекцию не проводилось до пятилетнего возраста, в связи с чем она не была верифицирована, и, соответственно, ребенок не получал адекватной иммунотропной терапии. Только в 5 лет 8 мес. при очередном эпизоде активации хронической Эпштейна - Барр вирусной инфекции в состав комплексной терапии был включен меглюмина акридонацетат, на фоне которого была достигнута хорошая клинико-лабораторная динамика. Описанный клинический случай демонстрирует эффективность включения в состав комплексного лечения Эпштейна - Барр вирусной инфекции меглюмина акридонацетата, обладающего противовирусным, иммуномодулирующим и противовоспалительным действиями, что позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем - и астеновегетативного синдрома и достигнуть перехода активной хронической Эпштейна - Барр вирусной инфекции в латентную форму.
Ключевые слова: острая респираторная инфекция, гнойный тонзиллит, гнойный аденоидит, лимфопролиферативный синдром, меглюмина акридонацетат, иммунотропная терапия.
Chronic Epstein-Barr viral infection in children: a clinical case
Svetlana P. Kokoreva, Veronika B. Kotlova®, Oleg A. Razuvaev
Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia
Abstract
The urgency of Epstein-Barr virus infection is explained by wide circulation of Epstein-Barr virus among children and adults, its tropism to immunocompetent cells with lifelong persistence after primary infection and polymorphism of clinical manifestations from subclinical forms, infectious mononucleosis to formation of oncological, autoimmune hematological diseases. Persistence of Epstein - Barr virus leads to suppression of cellular immunity, decreased production of interferons and nonspecific protection factors, which contributes to reactivation of persistent infection, most often without mononucleosis-like syndrome, and the appearance of atypical mononuclears in blood with the formation of lymphoproliferative, intoxication, astheno-vegetative syndrome, long-term subfebrile condition, which dictates the need for immunocorrective therapy. This article presents a clinical case describing and analyzing the course of a chronic Epstein-Barr virus infection in a preschool child (5 years 8 months) with a pre-morbid background. Episodes of reactivation of chronic persistent infection occurred under the mask of acute respiratory infection with lymphoproliferative syndrome, purulent tonsillitis, purulent adenoiditis. Therapy, including antibiotics, short-course antiviral agents, bacterial lysates, and physiotherapy, had a temporary and short-lived effect. meglumine acridonacetate. The described clinical case demonstrates the effectiveness of the inclusion of meglumine acridonacetate, which has antiviral, immunomodulatory and anti-inflammatory effects, in the complex treatment of Epstein-Barr virus infection, This allowed to obtain fairly rapid positive clinical dynamics of relieving intoxication and febrile and lymphoproliferative syndromes in the acute period, and subsequently - astheno-vegetative syndrome and achieve the transition of active chronic Epstein - Barr virus infection into a latent form.
Keywords: acute respiratory infection, purulent tonsillitis, purulent adenoiditis, lymphoproliferative syndrome, meglumine acridonacetate, immunotropic therapy.
Введение
Сегодня Эпштейна - Барр вирусная инфекция (ЭБВИ) представляет собой междисциплинарную проблему и активно изучается не только инфекционистами, но и врачами других специальностей: педиатрами, оториноларингологами, ревматологами, гематологами, онкологами, неврологами, иммунологами. Это объясняется тем, что вирус Эпштейна - Барр (ВЭБ) является одним из наиболее распространенных возбудителей, выявляемых как в детском возрасте, так и среди взрослого населения. По данным различных исследователей, инфицированность ВЭБ составляет 17,7% в периоде новорожденности и возрастает до 90% и выше у лиц старших возрастных групп 1. Являясь оппортунистической инфекцией, она в большинстве случаев протекает бессимптомно. Особенностью манифестных форм ЭБВИ является полиморфизм клинических симптомов, начиная от инфекционного мононуклеоза до фульминантных тяжелейших форм, аутоиммунных и онкологических заболеваний, реализующихся спустя годы после диагностированной ЭБВИ. Доказано, что манифестация клинических проявлений развивается при первичном инфицировании и реактивации персистирующей инфекции 4.
В случае адекватного иммунологического ответа первичное инфицирование приводит к формированию латентной формы инфекции - персистирующей неактивной ЭВБИ. Приравниваясь к здоровому носительству, она является естественным завершением иммунологических изменений. При снижении иммунитета происходит реактивация инфекции с манифестными проявлениями -активация персистирующей инфекции. При тяжелом течении могут формироваться органные поражения: менингоэнцефалит, миокардит, гепатит, гломерулонефрит и другие с возможным летальным исходом 8.
Но чаще в клинической практике встречаются варианты повторной реактивации ЭБВИ с неспецифической симптоматикой, когда при отсутствии остро развившегося полного мононуклеозоподобного синдрома и появления атипичных мононуклеаров в периферической крови, характерных для инфекционного мононуклеоза, возникают утомляемость, слабость, артралгии, головная боль, снижение памяти и внимания, депрессия, субфебрилитет. При этом принято говорить о хронической инфекции, если симптоматика сохраняется в течение полугода. Дети с хронической ЭБВИ имеют, как правило, отягощенный преморбидный фон, страдают хроническим тонзиллитом, хроническим аденоидитом; у них формируются различные варианты лимфопролиферативного синдрома, умеренно выраженный интоксикационный синдром, астенизация, может быть субфебрилитет; у этой категории больных отмечаются частые рекуррентные заболевания, что объясняется иммуносупрессивным воздействием ВЭБ 13.
Изучение форм ЭБВИ стало быстро развиваться благодаря возможностям современной лабораторной диагностики, которая позволяет оценить время инфицирования и активность инфекционного процесса [15, 16]. Для острой первичной инфекции типично появление ДНК вируса в крови и иммуноглобулинов М к капсидному антигену (аVCAJgM) и (или) иммуноглобулинов к раннему ЕА-антигену (аЕАIgG), которые циркулируют с третьей недели инфицирования, а также низкоавидных иммуноглобулинов к капсидному антигену (аVCAIgG). Со временем низкоавидные аVCAIgG трансформируются в высокоавидные, сохраняясь пожизненно. Начиная со второго месяца с момента заражения появляются антитела к ядерному антигену (аEBNAIgG). У части пациентов они сохраняются всю жизнь, у части -элиминируются. Положительный результат исследования полимеразной цепной реакции (ПЦР) крови не позволяет судить о форме инфекции, так как может регистрироваться как при первичном инфицировании, так и при реактивации персистирующей инфекции. На фоне высокоавидных аVCAIgG и (или) аEBNAIgG при реактивации персистирующей инфекции появляются капсидные антитела класса М и (или) ранние антитела. Давность инфицирования вне обострения инфекционного процесса подтверждается обнаружением высокоавидных аVCAIgG и аEBNAIgG. Положительные результаты ПЦР слюны могут быть у 15-25% здоровых серопозитивных людей. Это происходит в силу пожизненной персистенции вируса в В-лимфоцитах, которые, находясь в лимфоидной ткани миндалин при латентной инфекции или ее активации, дают положительный результат исследования [17].
Иммунокорригирующая терапия Эпштейна - Барр вирусной инфекции
На сегодняшний день общепринятых принципов этиотропного лечения ЭБВИ не разработано, так как препараты с противовирусной активностью не позволяют элиминировать возбудитель из организма, и основой лечения является симптоматическая и патогенетическая терапия. Однако длительная персистенция ВЭБ, приводящая к угнетению клеточного иммунитета, факторов неспецифической защиты, интерферон-продуцирующей функции лейкоцитов, свидетельствует о необходимости использования иммунокорригирующих препаратов [18, 23-26].
В педиатрической практике хорошо зарекомендовали себя индукторы эндогенного интерферона, в частности меглюмина акридонацетат (Циклоферон®), которые имеют ряд преимуществ по сравнению с экзогенными интерферонами. При их назначении не вырабатываются аутоантитела на собственный интерферон, время выработки стимулированных эндогенных интерферонов контролируется макроорганизмом, что не приводит к его передозировке. Кроме того, индукторы эндогенного интерферона имеют высокую биодоступность 28. Циклоферон® является низкомолекулярным индуктором интерферона и, соответственно, оказывает противовирусное, иммуномодулирующее, противовоспалительное действия, стимулируя синтез а- и у-интерферона, что способствует усилению Т-клеточного иммунитета - нормализации субпопуляций СD3-лимфоцитов, СD4-лимфо-цитов, NK-клеток и иммунорегуляторного индекса. Прямое действие меглюмина акридонацетата реализуется через нарушение репликации вируса, блокирование вирусной ДНК или РНК, увеличение дефектных вирусных частиц и снижение вирус-индуцированного синтеза белка [32, 33]. Его клиническая эффективность доказана у детей при острой респираторной вирусной инфекции (ОРВИ) и гриппе, так как на ранней стадии инфицирования он подавляет репликацию вируса, стимулирует и поддерживает уровень всех видов интерферона. Из всех индукторов интерферона Циклоферон является самым быстрым, вызывая продукцию интерферона через 2-72 ч после введения, реализуя таким образом противовирусный и иммуномодулирующий эффекты уже через 2-3 ч после приема 34. Наибольшую эффективность у детей препарат имеет при низком интерфероновом статусе 38. Доказано прямое противовирусное действие Циклоферона с подавлением размножения вируса на стадии репликации и вирусного потомства, его способность индуцировать синтез эндогенного интерферона в отношении герпетических вирусов, и показана его клиническая эффективность у детей при различных герпесвирусных инфекциях, в том числе и ЭБВИ 43. В качестве примера успешного использования иммуно-тропной терапии при герпесвирусной инфекции приводим клинической случай течения и исхода хронической ЭБВИ у ребенка дошкольного возраста.
Anamnesis vitae: ребенок от третьей беременности (в семье есть двое детей 8 и 10 лет), протекавшей с угрозой прерывания (терапия дюфастоном) на фоне хронической фетоплацентарной недостаточности, третьих срочных родов путем кесарева сечения. Вес при рождении -3260 г, оценка по Апгар - 7-8 баллов. По поводу конъюгационной гипербилирубинемии была переведена на второй этап выхаживания. С рождения находилась на искусственном вскармливании в связи с гипогалактией у матери. До года наблюдалась неврологом по поводу перинатального поражения нервной системы, профилактические прививки с 12 мес. Из перенесенных заболеваний мама отмечала нетяжелые ОРИ в 1,5 года и острую кишечную инфекцию в 2 года 4 мес.
Предварительный диагноз - острая респираторновирусная инфекция, осложненная аденоидитом. Синусит (?).
Динамика и исходы. В гемограмме лейкоцитоза нет -9,5 х 10 9 /л, абсолютный лимфомоноцитоз (п4%, с28%, л56%, м12%), СОЭ - 18 мм/час. Биохимические тесты без патологических изменений, СРБ - 3 мг (норма - 0-10). При рентгенологическом исследовании придаточных пазух носа данных по синуситу не выявлено. Получен отрицательный результат ПЦР-исследования мазков из носоглотки (респираторный скрин). Лор-врачом диагностирован гнойный аденоидит. По данным ультразвукового исследования органов брюшной полости выявлялись умеренная гепатомегалия, мезентериальная лимфаденопатия.
Терапия в отделении включала антибиотики (цефтриаксон парентерально), Виферон-1 per rectum 2 раза в сутки, симптоматические средства, физиолечение. На фоне проводимого лечения в течение трех суток состояние ребенка оставалось без убедительной клинической динамики: продолжала лихорадить, сохранялись интоксикационный и лимфопролиферативный синдромы. На четвертый день пребывания в стационаре результаты лабораторного обследования: ПЦР+ крови на ВЭБ, аVCAJgM+ и аVCAIgG+ авидность 100%, аEAIgG–, аEBNAIgG+, что позволило диагностировать реактивацию хронической ЭБВИ. К лечению добавлен Циклоферон в таблетках по схеме на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-е сутки. На третий день у девочки нормализовалась температура, восстановился аппетит, улучшилось самочувствие. Стал менее выраженным лимфопролиферативный синдром: носовое дыхание более свободное, уменьшился насморк. На 10-й день лечения ребенок жалоб не предъявлял. При объективном осмотре меньше выражены гипертрофия небных миндалин 1-й степени, шейная лимфаденопатия (размеры лимфоузлов уменьшились до 0,5 см), гепатомегалия 1,5 см. Выписана с клиническим улучшением с рекомендацией продолжить прием Циклоферона по схеме.
Клинический диагноз - хроническая Эпштейна - Барр вирусная инфекция, реактивация: лимфопролиферативный синдром, обострение хронического аденоидита, астеновегетативный синдром.
При объективном осмотре сохранялась умеренная гипертрофия небных миндалин, пальпировались мелкие, 0,3-0,5 см, безболезненные подчелюстные, передне-и заднешейные лимфоузлы, гепатомегалия отсутствовала, клинических проявлений астеновегетативного синдрома не отмечалось. Гемограмма соответствовала возрастной норме. В лабораторных тестах отсутствовали маркеры активной ЭБВИ: ПЦР крови - ДНК ВЭБ не обнаружено, аVCAJgM отрицательные, аEAIgG отрицательные, обнаружены аVCAIgG с авидностью 100% и аEBNAIgG.
Рисунок. Этапы формирования у пациентки хронической Эпштейна - Барр вирусной инфекции
Figure. Stages of chronic Epstein - Barr virus infection development in a patient
Заключение
Описанный клинический пример демонстрирует течение хронической ЭБВИ у больной в возрасте 5 лет 8 мес. с развитием лимфопролиферативного и астено-вегетативного синдромов. При реактивации хронической ЭБВИ, протекавшей с клиническими проявлениями ОРИ, гнойного тонзиллита, применялись антибиотики, препараты интерферона, глюкокортикостероиды интраназально, физиотерапия с временным эффектом. Назначение Циклоферона в составе комплексного лечения позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем -и астеновегетативного синдрома и достигнуть перехода активной хронической ЭБВИ в латентную форму, что подтверждается отсутствием маркеров активности хронической инфекции в течение года после использования Циклоферона.
Информация об авторах:
Кокорева Светлана Петровна, д.м.н., доцент, заведующая кафедрой инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Котлова Вероника Борисовна, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Разуваев Олег Александрович, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Information about the authors:
Svetlana P. Kokoreva, Dr. Sci. (Med.), Associate Professor, Head of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Veronika B. Kotlova, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Oleg A. Razuvaev, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Особенности течения и терапии респираторного микоплазмоза у детей в эпидемический сезон 2020-2021 гг.
Список литературы
References
Установлена доля острых респираторных вирусных инфекций с гастроинтестинальным синдромом в структуре заболеваемости у детей в возрасте от 6 мес. Доказана лечебная эффективность и безопасность включения анаферона детского в комплексную терапию острых респираторных вирусных инфекций с сопутствующим поражением желудочно-кишечного тракта и более быстрая ликвидация всех симптомов с улучшением показателей иммунного статуса.
Ключевые слова: сочетанное поражение, респираторный тракт, желудочно-кишечный тракт, индуктор интерферона, иммунный статус
В дальнейшем появление современных методов лабораторной диагностики, а также вспышки новых, ранее неизвестных заболеваний (SARS, птичий грипп, Norwalk), расширили круг вирусных инфекций, в клиническом течении которых возможно острое сочетанное поражение РТ и ЖКТ [6,11,12]. Причиной симптомокомплекса может быть как моноинфекция, когда возбудитель репродуцируется в эпителиальных клетках и РТ, и ЖКТ, так и микст-инфекция с различной локализацией места репродукции возбудителей [2,8].
Значимость данной проблемы для детей объясняется также необходимостью совершенствования методов лечения. Учитывая полиэтиологичность изучаемой патологии и преимущественно ранний возраст пациентов, одним из наиболее перспективных путей является использование в терапии препаратов ИФН, которые, в отличие от химиопрепаратов, имеют значительно меньше противопоказаний и более широкий спектр показаний к применению [3]. К ним относится и анаферон детский (АД), созданный на основе сверхмалых доз антител к ИФН-γ в гомеопатических разведениях С12, С30 и С50, успешно применяемый при лечении гриппа и респираторно-синцитиально-вирусной инфекции [9].
Методика исследования
С целью установления удельного веса ОРВИ с гастроинтестинальным синдромом в структуре острых респираторных заболеваний (ОРЗ) проведен анализ 15 785 историй болезней детей, находившихся в инфекционно-боксовых отделениях Детской инфекционной больницы № 5 им. Н.Ф.Филатова (Санкт-Петербург) с симптомами ОРЗ в период с 2003 по 2006 г.
Лечебная эффективность АД изучена в двойном слепом плацебоконтролируемом, рандомизированном клиническом исследовании у 150 детей в возрасте от 6 мес, госпитализированных с симптомами острого сочетанного поражения РТ и ЖКТ. Из них 100 детей получили препарат, 50 - плацебо.
АД и плацебо назначали по лечебной схеме согласно инструкции в течение 7-14 сут в зависимости от клинической выраженности заболевания [7]. Кроме того, по показаниям дети получали патогенетически обусловленную базисную терапию.
В обеих группах преобладали дети первых 3 лет жизни (в 83 и 82% случаев). Мальчиков было больше, чем девочек (55 и 45% соответственно). У большинства пациентов заболевание протекало на неблагополучном преморбидном фоне, представленном, в основном, проявлениями дермато- или респираторного аллергоза, хроническими заболеваниями уха, горла, носа и других органов, частыми ОРЗ в анамнезе и т.п. В целом сравниваемые группы были репрезентативными по основным данным.
С целью установления этиологии заболевания, помимо рутинного бактериологического, мы проводили комплексное вирусологическое исследование в лабораториях ГУ НИИ гриппа РАМН. Вирусные антигены и их нуклеиновые кислоты в материалах из носоглотки определяли методами иммунофлюоресценции, ПЦР, ИФА и реакцией непрямой гемагглютинации; в фекалиях - методами ИФА и просвечивающей электронной микроскопии. Завершающим этапом диагностики было выявление нарастания титров специфических противовирусных антител в серологических реакциях парных сывороток методами реакций торможения и непрямой гемагглютинации, реакции связывания комплемента и ИФА.
У части пациентов в динамике наблюдения оценивали иммунологические показатели: содержание общего IgE в сыворотке крови, секреторного IgA в носовых смывах, сывороточного, спонтанного и индуцированного in vitro ИФН-α и ИФН-γ, а также маркеров иммунокомпетентных клеток CD3, CD4, CD8, CD20 и CD16 [1,5].
Результаты исследования
По данным стационара, за 4 года сочетанное поражение РТ и ЖКТ официально регистрировалось у каждого 4-5-го ребенка, находящегося на стационарном лечении с симптомами ОРЗ (в 2003 г. - в 22%, 2004 г. - в 16.6%, 2005 г. - в 19.3%, 2006 г. - в 26.2% случаев).
В отличие от данных стационара, где причина дисфункции ЖКТ осталась не расшифрованной в 69.1% случаев, включение в спектр исследования пациентов вирусологических методов резко изменило представления об этиологической структуре заболевания. У большинства наблюдаемых детей доминировала вирусная инфекция: по данным исследования материалов из носа - в 7488% случаев, фекалий - в 45.5-50.0%, по результатам серологических исследований - в 49-40%. В целом причина заболевания осталась неизвестной только в 9% случаев и в половине случаев она была представлена микст-вариантом с преобладанием вирусных ассоциаций.
Наиболее часто (у каждого 3-4-го пациента) регистрировались адено-, рота- и коронавирусная инфекции в виде моно- или микст-вариантов. Несколько реже регистрировалась респираторно-синцитиальная (в 21.5% случаев, в основном в виде микст), гриппозная (в 15.3% случаев), а также норо- и энтеровирусная инфекции.
Из бактериальных возбудителей в 12% случаев выявлена условно-патогенная флора, в том числе золотистый стафилококк, протей, клебсиелла и грибы рода Candida.
Таблица 1. Лечебная эффективность АД у детей с острым сочетанным поражением РТ и ЖКТ (M±m)
| Клинические симптомы | Продолжительность симптомов, дни | |
| АД (n=100) | плацебо (n=50) | |
| Лихорадочная реакция | 2.10±0.06* | 3.37±0.19 |
| Интоксикация | 2.68±0.08* | 4.63±0.19 |
| Катаральные явления в носоглотке | 4.33±0.10* | 6.79±0.23 |
| Дисфункция ЖКТ | 3.29±0.12* | 4.65±0.26 |
| Острый период заболевания | 4.68±0.08* | 6.78±0.22 |
Заболевание у всех детей имело среднетяжелую форму течения с острым началом и повышением температуры тела выше 37.5°С (в половине случаев выше 38.6°С). Выраженность симптомов зависела от этиологии. Так, катаральные явления в носоглотке были наиболее значимыми при аденовирусной инфекции, при коронавирусной в трети случаев в процесс вовлекались бронхи и легкие. Максимальная выраженность симптомов поражения ЖКТ наблюдалась при рота- и норовирусной инфекциях. Они были основной причиной развития эксикоза у детей.
Рис. Продолжительность обнаружения антигенов в носовых ходах (а) и частота внутрибольничных инфекций (б) на фоне АД (светлые столбики) или плацебо (темные столбики) при остром сочетанном поражении РТ и ЖКТ у детей.
Таблица 2. Динамика уровня ИФН разных типов у детей с острым сочетанным поражением РТ и ЖКТ на фоне АД и плацебо (M±m)
| Показатель | Время исследования | Уровень ИФН, пг/мл | |
| АД (n=70) | плацебо (n=26) | ||
| Сывороточный ИФН-α | При поступлении На 2-3-и сутки При выписке | 44.8±2.9 64.5±2.4* + 48.0±2.0* | 40.8±4.5 40.0±4.0 34.8±3.8 |
| Сывороточный ИФН-γ | При поступлении На 2-3-и сутки При выписке | 59.2±2.9 77.2±4.2* + 58.7±3.4* | 54.4±5.1 55.0±4.0 42.5±4.0 |
| Спонтанная продукция ИФН-α | При поступлении На 2-3-и сутки При выписке | 75.5±3.9 92.0±3.9* + 66.2±2.8 | 73.3±5.6 77.7±5.8 64.0±5.1 |
| Спонтанная продукция ИФН-γ | При поступлении На 2-3-и сутки При выписке | 45.5±2.4 63.1±2.6* + 50.0±2.9 | 43.3±4.0 47.5±4.5 43.8±4.0 |
| Индуцированная продукция ИФН-α | При поступлении На 2-3-и сутки При выписке | 115.0±4.8 159.3±8.9* + 139.0±6.3* + | 127.9±0.7 126.5±8.8 104.4±5.9 |
| Индуцированная продукция ИФН-γ | При поступлении На 2-3-и сутки При выписке | 91.5±5.4 123.5±7.4* + 101.6±4.5* | 89.8±5.6 91.3±5.6 75.4±3.0 |
Включение АД в комплексную терапию способствовало достоверному увеличению уровня секреторного IgA - фактора местной защиты в носовых смывах детей, в отличие от пациентов контрольной группы (в 72.6 и 32.9% случаев соответственно). Вероятно, активизация местного иммунитета способствовала сокращению периода выделения вирусных антигенов, обнаруживаемых методом иммунофлюоресценции в носовых ходах больных и, в конечном счете, уменьшению частоты развития внутрибольничных инфекций (рисунок).
Заболевания сопровождались изменением содержания большинства Т-лимфоцитов, в частности, снижением уже при первом обследовании числа CD3, CD4 и CD8. На 2-3-и сутки у пациентов, принимавших АД, достоверно увеличивалось относительное содержание CD3 (в основном за счет субпопуляции CD4 с 34.6+1.6 до 40.1+1.3%) и CD16 (с 14.3+0.9 до 17.0+1.1%), которые уменьшались или оставались на прежнем уровне в группе плацебо (CD4 - с 31.0+1.1 до 26.3+1.3%; CD16 - с 16.8+1.4 до 14.6+1.4%), что явилось показателем уменьшения числа клеток, принимающих непосредственное участие в формировании гуморального иммунитета.
На фоне приема АД наблюдалось достоверное увеличение индуцированной и спонтанной продукции ИФН-α и ИФН-γ, в отличие от детей контрольной группы, как и общего содержания данных цитокинов в сыворотке крови (табл. 2). Кроме того, несмотря на дальнейшее снижение уровня ИФН к моменту выздоровления, у детей, получавших препарат, он сохранялся на достоверно более высоком уровне.
Применение АД не вызывало каких-либо нежелательных явлений, в том числе аллергических реакций, что подтверждалось отсутствием повышения в сыворотке крови уровня общего IgE, а в ряде случаев - даже его снижением, в отличие от детей контрольной группы.
Таким образом, сочетанное поражение РТ и ЖКТ регистрируется у каждого 4-5-го пациента, госпитализированного по поводу ОРЗ, преимущественно у детей первых 3 лет жизни. В этиологии симптомокомплекса лидирует вирусная инфекция (адено-, рота- и коронавирусная в виде как моно-, так и микст-вариантов). Терапия должна быть комплексной, зависящей от ведущего синдрома и может включать индуктор ИФН - АД.
По оценкам экспертов ВОЗ, практически каждый ребенок в течение первых пяти лет жизни переносит ротавирусный гастроэнтерит, независимо от расы и социально-экономического статуса. Ежегодно ротавирусы вызывают в мире более 137 млн случаев острого гастроэнтерита, из которых до 592 000 заканчивается летально. В России в настоящее время заболеваемость ротавирусной инфекцией постоянно растет, что обусловлено как увеличением случаев инфицированности, так и улучшением диагностики данной патологии.
Эпидемиология. Общепризнанно, что источником инфекции является только человек (больной манифестной формой или вирусовыделитель), в фекалиях содержится огромное количество вирусов (до 1010-1011 вирусных частиц в 1 г). Ротавирусы млекопитающих и птиц в естественных условиях для человека не патогенны. Фекально-оральный механизм передачи реализуется пищевым (молоко, молочные продукты, заменители грудного молока), водным и контактно-бытовым путями. Дискутируется возможность аэрозольного пути передачи. Ротавирусная инфекция (РВИ) может протекать в виде спорадических случаев, групповых заболеваний и массовых вспышек. Спорадические заболевания регистрируются в течение всего года, однако большинство больных выявляется в зимне-весенний период, в отличие от летне-осеннего, характерного для других кишечных инфекций. По нашим данным, 63,9% случаев ротавирусного гастроэнтерита приходилось на зимне-весенний период, 25,8% регистрировались осенью и 10,3% - летом.
Естественная восприимчивость к РВИ очень высокая. Наибольшее число заболевших отмечается среди детей в возрасте от 6 до 18 месяцев, и в первую очередь находящихся на искусственном вскармливании. По нашим наблюдениям дети младше 3 лет составляют 70-80% заболевших. Инфекция регистрируется также и у новорожденных, но не всегда сопровождается у них клиническими проявлениями. Иммунитет после перенесенной инфекции непродолжительный и сероспецифичный.
Патогенез. В последние годы большое внимание уделяется изучению патогенеза РВИ. Установлено, что после попадания ротавирусов в организм в первые сутки он обнаруживается в эпителиоцитах двенадцатиперстной и в верхнем отделе тонкой кишки. Инфицирование ротавирусом зависит от ряда причин: состояния pH желудочного сока (кислая среда губительна для ротавируса), наличия ингибитора трипсина (трипсин является активатором репродукции вируса), количества функционально незрелых энтероцитов. Ротавирусы поражают "зрелый" эпителий микроворсинок, в щеточной каемке которого находятся дисахаридазы, возможно поражение до 2/3 слизистой оболочки тонкой кишки. Проникновение внутрь клетки вызывает повреждение цитоскелета эпителиоцитов и их отторжение. Одновременно ускоряется продвижение эпителиальных клеток от основания крипты к верхушке микроворсинки, появляется пул низкодифференцированных клеток, являющихся функционально незрелыми, что приводит к нарушению выработки дисахаридаз и накоплению избыточного количества негидролизованных углеводов, преимущественно лактозы в просвете кишки. Не всосавшиеся вещества с высокой осмотической активностью, оказавшись в просвете кишки, приводят к нарушению реабсорбции воды, электролитов и развитию водянистой диареи. Поступая в толстую кишку, эти вещества становятся субстратами для ферментации кишечной микрофлорой с образованием большого количества органических кислот, водорода, углекислого газа, воды. Результатом являются повышенное газообразование в кишечнике и снижение рН кишечного содержимого.
Диагностика. Для подтверждения РВИ используются вирусологические, молекулярно-генетические, серологические методы. Материалом для исследования служат фекалии, рвотные массы, сыворотка крови. Исследования, направленные на обнаружение вируса или вирусных антигенов, желательно проводить в 14-е сутки болезни. Существуют экспресс-тесты для выявления антигенаротавируса в фекалиях на основе иммунохроматографического метода (рота-тест). Для обнаружения генетического материала ротавируса в фекалиях все более широко применяется метод диагностики с помощью ПЦР. В специализированных лабораториях хорошие результаты получены при морфологической идентификации ротавируса с помощью электронной или иммунной микроскопии, или электрофореза в полиакриламидном геле. Наиболее распространенным способом диагностики является обнаружение антигенов ротавируса в фекалиях с помощью ИФА, для этих целей также может использоваться реакция латекс-агглютинации, реакция иммунофлюоресценции, реакция твердофазной коаагглютинации, реакция преципитации. Серологическая диагностика РВИ имеет вспомогательное значение.
Терапия. Основой лечебных мероприятий при ротавирусном гастроэнтерите является патогенетическая терапия. Она включает диетотерапию, оральную регидратацию, инфузионную и дезинтоксикационную терапию. Используются энтеросорбенты (Смекта, Фильтрум-СТИ и др.), пробиотики (Энтерол, Бифиформ, Линекс, Аципол, Ацилакт, Бифидумбактерин форте, Бактисубтил и др.), пребиотики (Дюфалак, Хилак форте), ферменты (панкреатические: Креон, Панцитрат, Панкреатин, Мезим форте; Лактаза). Проводится посиндромная терапия: спазмолитическая, жаропонижающая и т.д.
В настоящее время активно изучается эффективность использования противовирусных препаратов при РВИ. По нашим данным, назначение в острый период заболевания индукторов интерферона (таких как Циклоферон или Анаферон детский) способствует сокращению сроков клинических проявлений РВИ и быстрой санации макроорганизма от вируса. Применение препарата Кипферон оказывает стимулирующее влияние на системный и местный антителогенез, приводит к повышению концентрации интерферонов. В качестве этиотропных средств могут быть использованы Арбидол, Виферон, Комплексный иммуноглобулиновый препарат, Гепон или антиротавирусный иммуноглобулин.
В очаге заболевания проводится комплекс мероприятий, направленных на предупреждение инфекционных заболеваний с фекально-оральным механизмом передачи.
Профилактика. С 1998 года в США у детей с 6-недельного возраста использовалась ротавирусная генноинженерная вакцина RRV-TV, созданная на основе ротавируса штамма макаки-резуса, реассортированного с четырьмя человеческими штаммами. Однако оказалось, что это приводит к повышению частоты инвагинации кишечника (в 1,6 раза), что послужило причиной запрета применения данной вакцины. В настоящее время за рубежом и в нашей стране проходят третью (завершающую) фазу клинические испытания живых аттенуированных вакцин из рекомбинантных штаммов ротавирусов человека и животных для вакцинации детей начиная с 3-месячного возраста.
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
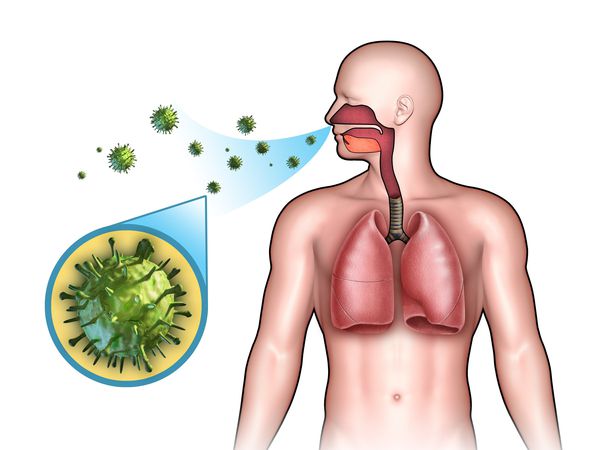
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
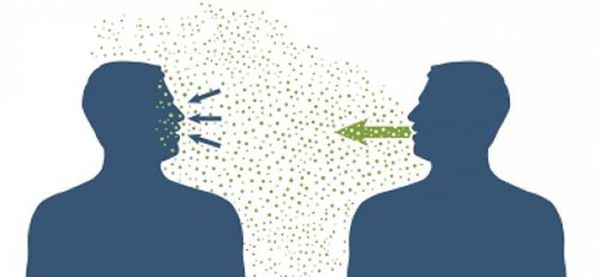
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
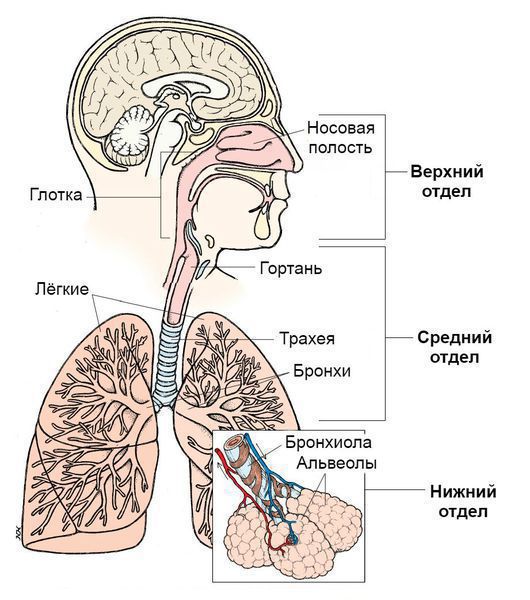
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
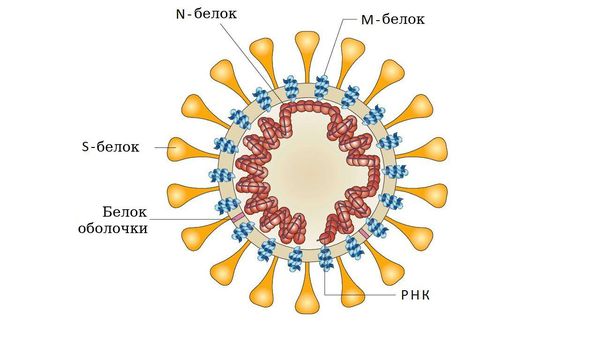
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
По вовлечению отдельных частей дыхательной системы:
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:
Читайте также:

