Ревизионное эндопротезирование тазобедренного сустава при инфекциях
Обновлено: 25.04.2024
РЕВИЗИОННАЯ ХИРУРГИЯ ТАЗОБЕДРЕННОГО СУСТАВА: РОЛЬ ИНДИВИДУАЛЬНЫХ АРТИКУЛИРУЮЩИХ СПЕЙСЕРОВ
ССЫЛКА ДЛЯ ЦИТИРОВАНИЯ:
Г. М. КАВАЛЕРСКИЙ, В. Ю. МУРЫЛЕВ, Я. А. РУКИН, П. М. ЕЛИЗАРОВ, А. В. МУЗЫЧЕНКОВ
Первы й Московски й Государственны й Медицински й Университет Имени И. М. Сеченова, Москва
При лечении глубокой перипротезной инфекции золотым стандартом остается двухэтапное ревизионное эндопротезирование. Удаление эндопротеза с санацией перипротезной зоны и установкой спейсера, затем, при условии купирования инфекции, не ранее, чем через 3 месяца – ревизионное эндопротезирование. Разработан индивидуальный артикулирующий цементный спейсер с антибиотиком для первого этапа ревизионного эндопротезирования. Подобные спейсеры являются высокоэффективным решением для двухэтапной ревизионной хирургии тазобедренного сустава. Артикулирующие спейсеры индивидуального изготовления использованы у 11 пациентов, в двух случаях (18,2 %) выявлены рецидивы инфекции, в одном случае спейсер оставлен, как окончательный вариант для реконструкции тяжелого поражения тазобедренного сустава. Использование описанной технологии позволило заполнить все имеющиеся дефекты бедренной кости и вертлужной впадины, сохранить опорную и двигательную функцию тазобедренного сустава до ревизионного эндопротезирования.
ключевые слова: тазобедренный сустав, глубокая перипротезная инфекция, двухэтапное ревизионное эндопротезирование, индивидуальный артикулирующий спейсер.
Введение
Есть несколько методик радикального лечения глубокой перипротезной инфекции тазобедренного сустава. Первая заключается в удалении эндопротеза и санации, без последующего ревизионного эндопротезирования. Однако, результатом этой операции будет укороченная нижняя конечность, со сниженной опороспособностью, пациент будет всю жизнь передвигаться с хромотой и вероятнее всего с дополнительной опорой.
Другие методики подразумевают удаление эндопротеза с последующей установкой ревизионного эндопротеза. Одни авторы предлагают выполнять такую операцию в один этап: удалять эндопротез, санировать инфицированный очаг и сразу устанавливать ревизионный имплант [8]. Данная методика требует ряда особых условий, таких как: отсутствие метициллинрезистентных стафилококков, хорошее состояние мягких тканей и отсутствие свищей. Даже при соблюдении этих условий, применение одноэтапного ревизионного эндопротезирования в условиях глубокой перипротезной инфекции тазобедренного сустава остается дискутабельным.
Золотым стандартом лечения глубокой перипротезной инфекции остается двухэтапное ревизионное эндопротезирование [4]. Первый этап: удаление эндопротеза с санацией перипротезной зоны и установкой спейсера, второй этап при условии купирования инфекции, не ранее, чем через 3 месяца – ревизионное эндопротезирование. Задача спейсера: поддержание концентрации антибиотика в области тазобедренного сустава, заполнение объема после удаления эндопротеза, соответственно профилактика избыточного образования рубцов и формирования гематом, поддержание длины и опороспособности нижней конечности. Разработан целый ряд спейсеров: неартикулирующие и артикулирующие, цементные, из компонентов эндопротезов и т. д. Нами предложены индивидуальные армированные артикулирующие спейсеры с антибиотиком для первого этапа лечения глубокой перипротезной инфекции.
Материалы и методы
С 2010 по апрель 2015 года на базе кафедры травматологии, ортопедии и хирургии катастроф Первого Московского государственного медицинского университета им. И. М. Сеченова в ГКБ им. С. П. Боткина с применением индивидуальных артикулирующих спейсеров мы прооперировали 11 пациентов с глубокой перипротезной инфекцией тазобедренного сустава. Среди оперированных пациентов женщин было 7 (63,6 %), а мужчин 4 (36,4 %). Средний возраст пациентов составил 61,3 лет (от 33 до 72 лет). В этой группе глубокая перипротезная инфекция после первичного эндопротезирования тазобедренного сустава отмечена у 8 пациентов (72,7 %), а после ревизионного эндопротезирования у 3 пациентов (27,3 %).
Двухэтапное ревизионное эндопротезирование тазобедренного сустава заключается в следующем. Первый этап – удаление вертлужного и бедренного компонентов эндопротеза; санация области эндопротеза с применением механических методов (некрэктомия, пульс-лаваж), физических методов (обработка раны с использованием ультразвука), химических методов (применение антисептиков). Во время первой операции осуществляется забор не менее 4 – 6 образцов тканей для выявления микробного агента и чувствительности к антибиотикам. После санации производится установка индивидуального артикулирующего спейсера.
Первый этап представляет собой комплексное обследование пациента с глубокой перипротезной инфекцией тазобедренного сустава, включающее рентгенографию пораженного тазобедренного сустава, компьютерную томографию с 3D моделированием имеющихся дефектов вертлужной впадины и бедренной кости, изучения анамнеза с выяснением дизайна и размера импланта, ранее установленного пациенту.
Вторым этапом на основании полученных данных изготавливается модель спейсера. В качестве модели может служить тестовый бедренный компонент импланта, ранее установленного пациенту. При наличии больших дефектов используются модели, изготовленные методами 3D моделирования и стереолитографии по томографическим снимкам пораженного тазобедренного сустава. В других случаях модели изготавливаются методами лепки из гипса или путем механообработки стеклопластика. Возможна комбинация описанных методов.
Для спейсера тазобедренного сустава в проксимальном отделе фиксируется гипсовый шар диаметром, на 4 мм меньшим диаметра вертлужной впадины пациента. В последующем шарообразная часть цементного спейсера будет вправляться в вертлужную впадину и выполнять артикулирующую функцию.
Третий этап заключается в формировании силиконовой формы. Изготовленная модель заливается силиконом, выдерживающим автоклавирование. Габаритные размеры формы выбирают из расчета максимального габаритного размера изделия + 20 мм, что обеспечивает и достаточную гибкость, и одновременно прочность для сохранения формы изделия (рис. 1).
После окончания полимеризации силиконовая форма разрезается, и модель из нее вынимается. Для последующего точного совмещения формы линия разреза намеренно делается искривленной. Силиконовая форма отправляется в стерилизацию.
четвертый этап формирования спейсера осуществляется в стерильных условиях в операционной. После удаления эндопротеза и санации операционной раны, производится подготовка костного цемента для спейсера. Костный цемент (как правило 120 – 160 г) в сухом виде смешивают с сухим антибиотиком. Имеются особые требования к антибиотику, применяемому в спейсерах. Он должен быть доступен в порошкообразной форме и не разрушаться при температуре полимеризации цемента, которая может достигать 120 140°. Таких антибиотиков немного, к ним относятся гентамицин, ванкомицин, эритромицин, клиндамицин и тобрамицин. В нашей практике мы либо применяем уже заранее приготовленный на заводе цемент с гентамицином или смешиваем цемент с ванкомицином из расчета 1 г антибиотика на 40 г цемента в операционной. В некоторых случаях мы добавляем ванкомицин в цемент с гентамицином.
Полученный порошок смешивают с жидкой частью костного цемента. После замешивания костный цемент заливается в силиконовую форму. По форме спейсера в цемент укладывается армирующий стержень (рис. 2).

части силиконовой формы точно сопоставляются по линии разреза, и хирург ожидает полимеризации цемента. После полимеризации мы получаем индивидуальный армированный артикулирующий спейсер тазобедренного сустава с антибиотиком, который точно соответствует анатомии пациента (рис. 3). Спейсер устанавливают в очищенное ложе эндопротеза, осуществляют вправление спейсера и ушивание раны.

Послеоперационное ведение таких пациентов имеет некоторые особенности. В настоящее время мы отказались от применения промывной системы с антисептиками у пациентов с глубокой перипротезной инфекцией тазобедренного сустава. Дренажи удаляем через 48 – 72 часа. В течение 6 – 8 недель после операции проводится антибиотикотерапия с учетом результатов посевов (в стационаре парентерально, амбулаторно – перорально). Пациентам рекомендована ходьба с костылями с дозированной нагрузкой на оперированную ногу. Спустя 3 месяца пациенты проходят обследование на предмет перипротезной инфекции, включающее анализы крови (СОЭ, С-реактивный белок, лейкоциты, лейкоцитарная формула) и пунктат синовиальной жидкости (содержание нейтрофилов, в том числе палочкоядерных, бактериоскопию и посевы). Если тесты на перипротезную инфекцию дают отрицательный результат, выполняется ревизионное эндопротезирование. При сомнительном результате тесты повторяются через 2 – 3 месяца. В случае подтвержденного рецидива перипротезной инфекции выполняется повторная санация с заменой артикулирующего спейсера.
Результаты
В этой группе 9 пациентам (81,8 %) выполнено ревизионное эндопротезирование. В 2 случаях (18,2 %) отмечен рецидив инфекции, потребовавший ревизионной операции. В одном случае рецидив возник на фоне спейсера, что потребовало замены спейсера с последующим ревизионным эндопротезированием. В другом случае рецидив возник после установки ревизионного эндопротеза, что потребовало удаления эндопротеза и установки спейсера. К сожалению, вновь развился рецидив инфекции, спейсер пришлось удалить, без дальнейшей установки эндопротеза.
В одном случае у пациента индивидуальный артикулирующий спейсер функционирует уже в течение 5 лет. Приводим клинический пример.
Пациент К. В. Д., 1949 года рождения. В 1990 году в результате дорожно-транспортного происшествия переломовывих правого бедра. Развился правосторонний посттравматический коксартроз. В 1995 году выполнено тотальное эндопротезирование правого тазобедренного сустава. В 2007 году отмечены боли, имела место клинико-рентгенологическая картина нестабильности эндопротеза правого тазобедренного сустава (рис. 4).
03 октября 2007 года выполнено ревизионное эндопротезирование правого тазобедренного сустава. Выполнена массивная костная пластика дефекта вертлужной впадины большим объемом костного аллотрансплантанта, установлено антипротрузионное кольцо, в бедренную кость установлена длинная ревизионная ножка wagner (рис. 5).

Отмечено тяжелое течение раннего послеоперационного периода с развитием двусторонней пневмонии и сепсиса. Инфекционные осложнения были купированы, рана зажила первичным натяжением. Отмечался рецидивирующий вывих эндопротеза тазобедренного сустава. В феврале 2008 года выполнено ревизионное эндопротезирование с заменой головки эндопротеза на более длинную, рецидивы вывихов устранены.
В 2010 году открылся свищ в области послеоперационного рубца с гнойным отделяемым (рис. 6). Таким образом развилась поздняя глубокая перипротезная инфекция. По данным КТ с 3D моделированием изготовлена гипсовая модель тазобедренного сустава пациента со всеми дефектами. С помощью гипсовой модели отлита силиконовая форма. 24 июня 2010 года выполнено удаление эндопротеза правого тазобедренного сустава. В стерильной силиконовой форме из 160 г костного цемента с 4 г гентамицина отлит индивидуальный армированный артикулирующий спейсер, который установлен пациенту (рис. 7).
Данный пациент ежегодно, регулярно является на динамические осмотры. Ходит с тростями, функцией тазобедренного сустава на спейсере удовлетворен, без трудностей управляет автомобилем. От ревизионного эндопротезирования правого тазобедренного сустава отказывается, да и мы, учитывая высокий риск рецидива инфекции при хирургическом вмешательстве, не настаиваем на выполнении данной операции рис. 8).
В данном случае индивидуальный артикулирующий спейсер, несмотря на свое временное предназначение, выполняет постоянную функцию с удовлетворительным результатом для столь тяжелого поражения тазобедренного сустава.
Заключение
Лечение глубокой перипротезной инфекции тазобедренного сустава представляет собой очень трудную задачу, что связано с формированием микробных пленок, все возрастающей антибиотикорезистентностью и полиморфностью микрофлоры, высокой травматичностью операции удаления компонентов эндопротеза, особенно стабильных. Лечение рецидивов перипротезной инфекции сопровождается высоким процентом рецидивов. В нашей серии получено 18,2 % рецидива перипротезной инфекции тазобедренного сустава, что соотносится с данными других авторов. Так A. D. toms и соавт. показывают 38 % частоту рецидива инфекции при лечении глубокой перипротезной инфекции тазобедренного сустава [9], Katsufumi uchiyama и соавт. показывают 32,3 % частоту рецидива [10].
Индивидуальные артикулирующие спейсеры представляют собой высокоэффективное решение для двухэтапной ревизионной хирургии тазобедренного сустава. Они позволяют заполнить все имеющиеся дефекты бедренной кости и вертлужной впадины, сохранить опорную и двигательную функцию тазобедренного сустава до ревизионного эндопротезирования. В некоторых случаях подобные спейсеры могут служить окончательным решением, без планирования ревизионного эндопротезирования. Стоимость изготовления такого спейсера в несколько раз ниже, чем продающиеся на рынке официнальные спейсеры, а эффективность при практически любом разрушении тазобедренного сустава выше.
Целый ряд вопросов требует дальнейших разработок. Это касается и поиска эффективных антибиотиков, способных проникать в микробную пленку и борьбы с антибиотикорезистентностью, и разработки методов более бережного удаления стабильных компонентов эндопротеза в условиях инфицированного тазобедренного сустава. Не менее важным является улучшение методов профилактики глубокой перипротезной инфекции тазобедренного сустава.
Список литературы
1. John Meehan, Amir A. Jamali, Hien Nguyen. Prophylactic Antibiotics in hip and Knee Arthroplasty. j bone joint Surg Am. 2009;91:2480-90.
2. Mahomed NN, Barrett JA, Katz JN, Phillips CB, Losina E, Lew RA, Guadagnoli E, Harris WH, Poss R, Baron JA. Rates and outcomes of primary and revision total hip replacement in the united States Medicare population. j bone joint Surg Am. 2003;85:27-32.
3. Ridgeway S, Wilson J, Charlet A, Kafatos G, Pearson A, Coello R. Infection of the surgical site a er arthroplasty of the hip. j bone joint Surg br. 2005;87:844-50.
4. Javad Parvizi, Bahar Adeli, Benjamin Zmistowski, Camilo Restrepo, Alan Seth Greenwald. Management of Periprosthetic joint Infection: e current Knowledge. j bone joint Surg Am. 2012;94:e104(1-9).
7. Costerton JW, Stewart PS, Greenberg EP. bacterial bio lms: a common cause of persistent infections. Science 1999;284:131822.
8. Valérie Zeller, Luc Lhotellier, Simon Marmor, Philippe Leclerc et al. one-Stage exchange Arthroplasty for chronic Periprosthetic hip Infection: Results of a large Prospective cohort Study. j bone joint Surg Am, 2014 jan 01; 96.
10. Katsufumi Uchiyama, Naonobu Takahira, Kensuke Fukushima, Mitsutoshi Moriya, Takeaki Yamamoto, Yojiro Minegishi, Rina Sakai, Moritoshi Itoman, Masashi Takaso. two-Stage Revision total hip Arthroplasty for Periprosthetic Infections using Antibiotic-Impregnated cement Spacers of Various types and Materials. e Scienti c world journal. Volume 2013 (2013), Article ID 147248.
Информация об авторах:
REVISION SURGERY OF THE HIP JOINT: THE ROLE OF INDIVIDUAL ARTICULATING SPACERSE
G. M. KAVALERSKIY, V. YU. MURILEV, YA. A. RUKIN, P. M. ELIZAROV, A. V. MUZICHENKOV
Sechenov First Moscow State Medical University, Moscow
Information about the authors:
Gennadiy Kavalerskiy – I.M. Sechenov First Moscow State Medical university, MD, professor, head of department of trauma, orthopedics and Disaster Surgery
Valeriy Murilev – I.M. Sechenov First Moscow State Medical university, MD, professor of department of trauma, orthopedics and Disaster Surgery
Yaroslav Rukin – I.M. Sechenov First Moscow State Medical university, MD, assistant professor of department of trauma, orthopedics and Disaster Surgery
Pavel Elizarov – I.M. Sechenov First Moscow State Medical university, MD, assistant professor of department of trauma, orthopedics and Disaster Surgery
Alexey Muzichenkov – I.M. Sechenov First Moscow State Medical university, assistant of department of trauma, orthopedics and Disaster Surgery
e gold standard for the treatment of deep periprosthetic infection remains a two-stage revision. e removal of the prosthesis with debridement periprosthetic area and implantation of a spacer, the second phase – revision hip arthroplasty. we have developed an individual articulating cement spacer with antibiotics for the rst phase of revision cases. ese spacers are a highly e ective solution for a two-stage revision surgery of the hip joint. Individual articulating spacers used in 11 patients, in two cases (18.2%) were developed recurrence of the infection. In one case spacer became the nal option for the reconstruction of the hip joint. e recurrence rate of infection is less than the data of other authors. Spacers lled all the defects of the femur and acetabulum, and preserved the support and motor function of the hip joint.
Key words: hip, deep periprosthetic infection, two-stage revision hip replacement, individual articulating spacer.
Это высокотехнологичное оперативное удаление родного нежизнеспособного сустава с последующей имплантацией искусственного ТБС (эндопротеза). Во всем мире ежегодно выполняют до 500 тыс. подобных вмешательств людям с патологиями тазобедренного сустава, отзывы о лечении достаточно хорошие. Процент развития серьезных послеоперационных осложнений ничтожно мал – 1-2 %, что внушает большие надежды на успех.

Видео разрушения ТБС:
Ревизионная хирургия назначается в связи необходимостью замены изношенного протеза по окончании срока эксплуатации или вышедшего из строя устройства по причине возникших осложнений (инфекции, травм и пр.).
Показания
Если консервативное лечение уже не в силах улучшить качество жизни, хирургия является единственным способом возобновления нормальной амплитуды движений и ликвидации боли. Основные показания следующие:
- деформирующий артроз, или коксартроз (одна из самых частых причин дегенеративно-дистрофической природы); и любого другого системного генеза дегенеративно-дистрофические патологии с дислокацией в ТБ отделе; (вторая по распространенности проблема, нуждающаяся зачастую в срочной установке эндопротеза);
- врожденная или приобретенная дисплазия (вывих) ТБС (преимущественно встречается первый тип аномалии); , то есть омертвение хряща вследствие локального нарушения кровообращения.
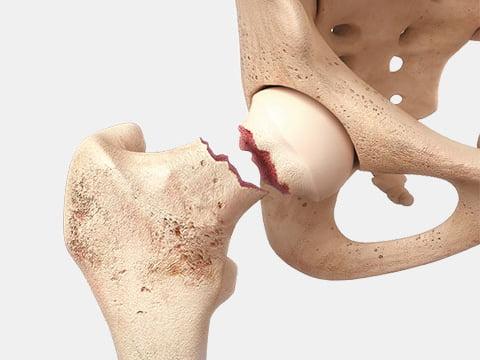
Один из видов перелома шейки бедра.
При переломах шейки перспективы на восстановление самые что ни на есть отличные, поскольку до травмы хромоты еще не было.

Пожилым людям такое лечение может существенно продлить жизнь за счет сохранения движения.
Еще недавно после переломов ТБС пациент был приковыван к постели, где он доживал максимум свой последний год. В травматологии, попросту не было еще способа установки искусственного сустава. Сегодня если своевременно поменять шейку сустава вместе с головкой бедра на долговечный имплантат, человек продолжает жить как и до травмы. Особенно актуальным такая хирургия является для пожилых людей, у которых срастание костей проблематично.
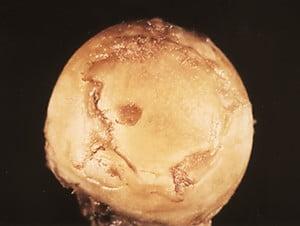
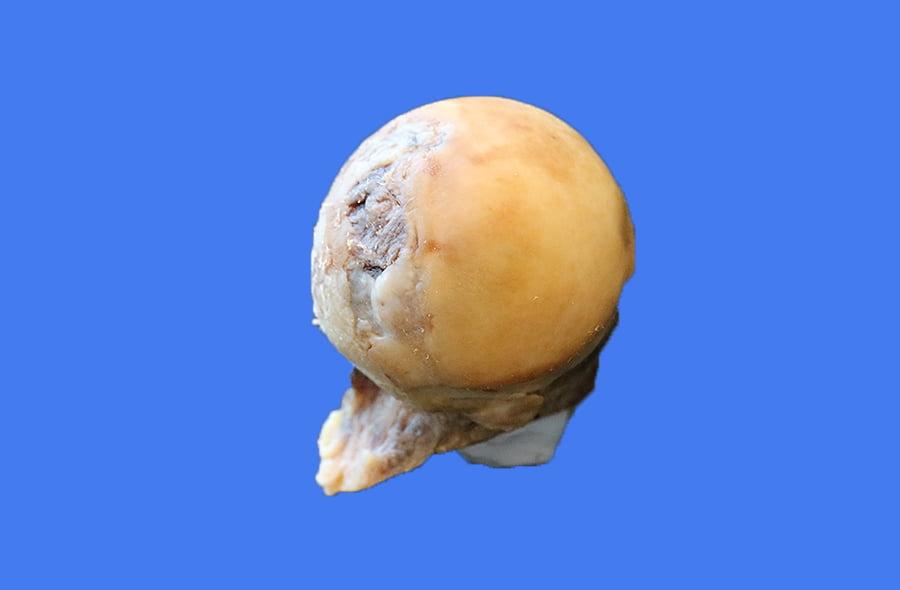
Поверхность головки ТБС на последней стадии артроза.
Процедура учитывает возрастное бессилие организма – агрессивным методам наркоза (общей анестезии) пожилого человека не подвергают, обезболивание может проводиться при помощи высокоэффективной и безопасной местной анестезии. После операции разрешается ранняя активизация пациента, при этом реабилитация проходит относительно легко и быстро.
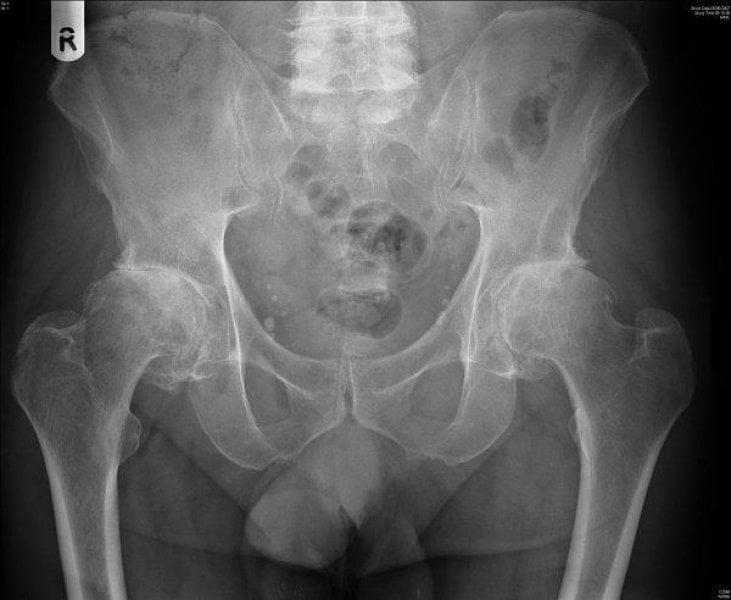
Двухсторонний коксартроз, обратите внимание на симметричное отсутствие суставной щели обоих суставов.
Отметим, жидкое протезирование не лечит суставы. Если кто-то все еще надеется на чудодейственное исцеление необратимых изменений посредством внутрисуставных инъекций, раскроем секрет, он попросту теряет деньги и время. Хрящ уже не восстановится, если имеется коксартроз 3 степени, и уколы здесь делать бессмысленно.
Противопоказания
Их не много, что дает возможность довольно широко применять методику, дарить пациентам свободу и легкость движений, причем даже людям преклонных лет:
- сердечный порок с критическим сбоем ритма сердца;
- тяжелой формы дыхательная и сердечно-сосудистая недостаточность;
- хронические заболевания в декомпенсированной фазе;
- сложно поддающийся контролю сахарный диабет;
- местные инфекционные и воспалительные процессы;
- общие инфекционно-воспалительные патологии в обострении;
- серьезные психические нарушения;
- ярко выраженный остеопороз костных тканей; ; (условное противопоказание);
- непереносимость материалов эндопротеза и используемых медикаментов.
Лучшие клиники эндопротезирования тазобедренного сустава, например, в Чехии, Германии, Израиле, принимают людей, которым было отказано в лечении в медучреждениях на территории своего государства.
Виды операций
В зависимости от характера поражений ТБС подбирается хирургическая техника. Если необходима полная замена, будет применен тотальный эндопротез; если обновление поверхности головки, тогда берется поверхностного вида имплантат; и т.д.
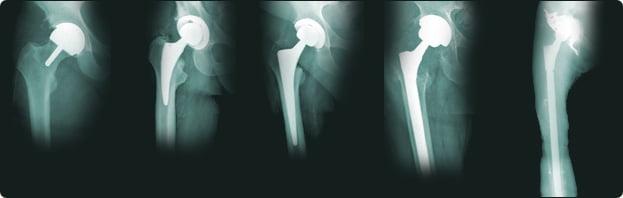
Разные виды, от частичного, до онкологического.
Хирургический подход может быть:
Малоинвазивный способ
В таком медицинском направлении, существует две хирургические техники выполнения артропластики:
Оперировать технически намного проще, если операционная рана будет большой. Поэтому ортопеды-травматологи утверждают, что классическая процедура на крупных суставах, все же, в неоспоримом приоритете.
Во многих клиниках практикуют малоинвазивный подход, используя почти в 2 раза меньший разрез, чем при традиционном вмешательстве. Однако и передовые хирурги с достаточным опытом все больше сходятся во мнении, что лучше лишний раз не рисковать, а использовать проверенную, традиционно устоявшуюся тактику, стандарт протезирования – создавать аккуратный разрез с прямого бокового доступа, длиной приблизительно в 13 см.
Согласно минимально инвазивному приему разрез равен примерно 7 см. Наиболее часто применяемые доступы, обеспечивающие менее травматичный с точки зрения физиологии подход, задне- и переднебоковые. Достоинствами миниинвазивного вида являются сохранность отводящих мышц, компактность операционной раны, ускоренный темп реабилитационного восстановления. Клинические исследования показывают, что интраоперационные кровопотери при щадящем вмешательстве незначительные, болевой синдром в постоперационную фазу менее выражен по сравнению со стандартной процедурой.
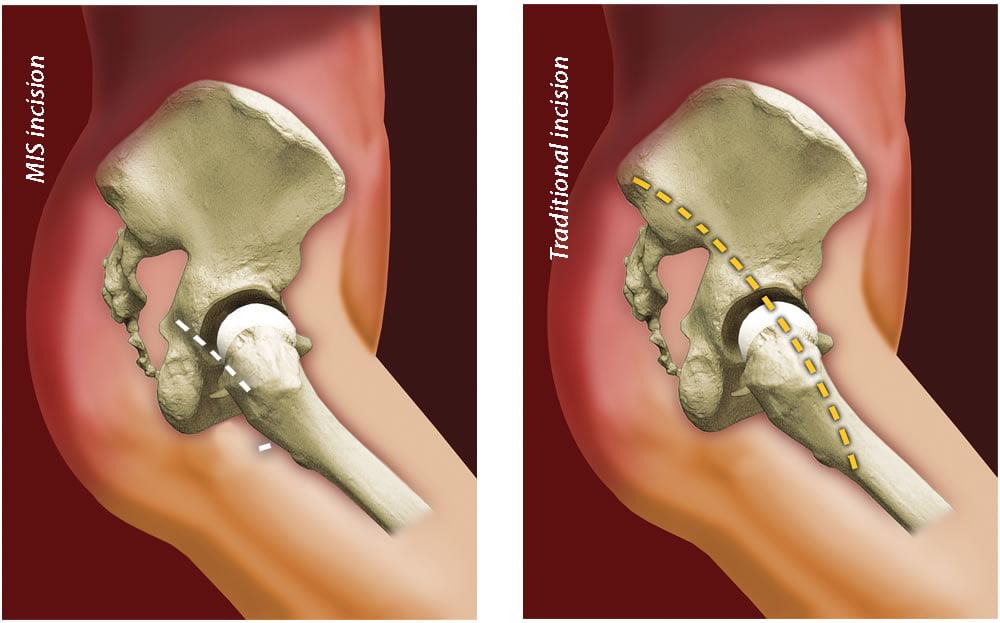
Наглядное сравнение размеров разрезов при классической(справа) и малоинвазивной(слева) методике.
Госпитализация
Всю необходимую информацию относительно подготовительных предоперационных мероприятий предоставляет лечащий доктор. Также на этой стадии хирург определяется с выбором эндопротеза и планирует каждый шаг, а анестезиолог подбирает подходящий вид анестезии на основании показателей здоровья пациента.
В клинике поступившего больного тщательно обследуют различные специалисты:
- осмотр у основного специалиста (ортопеда-травматолога);
- рентген, МРТ, УЗИ т/б сустава, при необходимости эндоскопическое обследование проблемного отдела;
- консультация узкопрофильных врачей (терапевт, кардиолог, иммунолог, анестезиолог, стоматолог, гастроэнтеролог и пр.);
- общий и биохимический анализ крови;
- коагулограмма (определяет работу системы гемостаза, в частности механизм и время свертываемости крови);
- тест на группу и резус-фактор крови;
- клинический анализ мочи;
- флюорография;
- электрокардиограмма.
Анестезия
Теперь осветим главные моменты, касающиеся наркоза, который применяется при замене двух тазобедренных суставов. По правилам допускается использование общей (полной эндотрахеальной), спинальной, эпидуральной анестезии или комбинацию двух последних видов.
К первому методу обращаются в крайне редких случаях, почти 90% операций выполняется либо под спинальным, либо под эпидуральным обезболиванием, оба подхода относятся к местному (регионарному) типу наркоза и не сопровождаются отключением сознания.
- Если вам будет показана спинальная анальгезия, тогда в субарахноидальное пространство позвоночника будет внедрена ультратонкая игла, через которую анестезиолог в спинномозговую жидкость произведет введение оптимальной дозы раствора-анестетика, за счет чего произойдет блокада передачи нервных импульсов.
Сам укол практически безболезненный.
- Если эпидурально, тогда наркоз будет подаваться через тонкий катетер в перидуральное пространство позвоночного столба. Такой прием приводит к полной потери болевой чувствительности в активной зоне оперирования.

Частичный наркоз лучше как для врача, так и для пациента.
Ход операции
Хирург самостоятельно определяет, по какой технологии производить замену, какой применить доступ и какую модель импланта устанавливать, исходя из конкретной клинической ситуации. А сейчас проведем краткое описание этапов хирургии.
- После действия анестезии и широкой антисептической обработки кожных покровов, коагулятором или скальпелем выполняется разрез по межвертельной линии до открытия сустава.
- Далее выполняется под правильным углом и уровнем пересечение бедренной кости в зоне шейки. Разверткой врач создает канал в подвергнувшемся остеотомии трубчатом элементе.
- Затем в созданный выпор вставляют клиновидную ножку, которая идеально должна совпадать с его параметрами, поэтому обработка данной кости должна пройти на безупречном уровне. На конусообразную верхушку ножки насаживается шаровидное тело имплантата.
- Сзади или спереди, в зависимости от примененного доступа, бедро смещают в сторону и приступают к подготовке вертлужной впадины. Используя долото и фрезы, специалист всецело удаляет гиалиновый хрящ с ее днища. Имплантат (чашу) вставляют в очищенное ложе. В него помещают полиэтиленовый вкладыш.
- Осуществляется вправление компонента бедра в чашку. После в рану ставится дренаж, рассеченные ткани ушиваются, на конечность накладывается повязка.
Принцип хирургии при всех видах оперативных вмешательств, о которых мы упомянули ранее, почти одинаков.
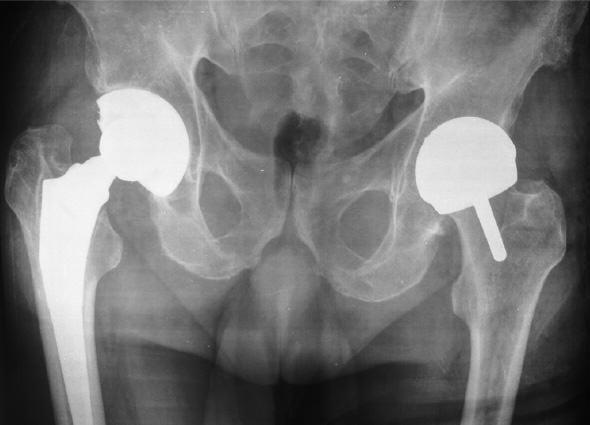
Интересный случай, двухсторонняя замена ТБС, но по разным технологиям. Слева тотальное протезирование, справа поверхностное.
Одновременное двустороннее эндопротезирование ТБС, рекомендуется в исключительно редких ситуациях, операционная травма будет больше, а, следовательно, и риск осложнений возрастет.
Виды фиксации сустава
В ортопедии и травматологии разработаны 3 способа фиксации, это:
- цементный;
- бесцементный;
- комбинированный.

Вертлужные компоненты импланта ТБС, розовая поверхность из керамики, белая из полиэтилена.
Бесцементная фиксация – это самый распространенный прием. Его принцип заключается в заколачивании деталей, у которых поверхность шероховатая, в подготовленные кости. Сразу, естественно, прочной связи с костями не свершится, имплантат должен хорошо обрасти соединительнотканными структурами, на что уйдет до 3 месяцев.

Комбинированное протезирование – это сочетание двух рассмотренных технологий единовременно в ходе одной операции. Подобной версии технология предназначена для тех, у кого обнаружена различная плотность кости бедра и таза. Когда какая-то из костей имеет хорошие показатели минеральной плотности, в то время как другая находится в неудовлетворительном состоянии.
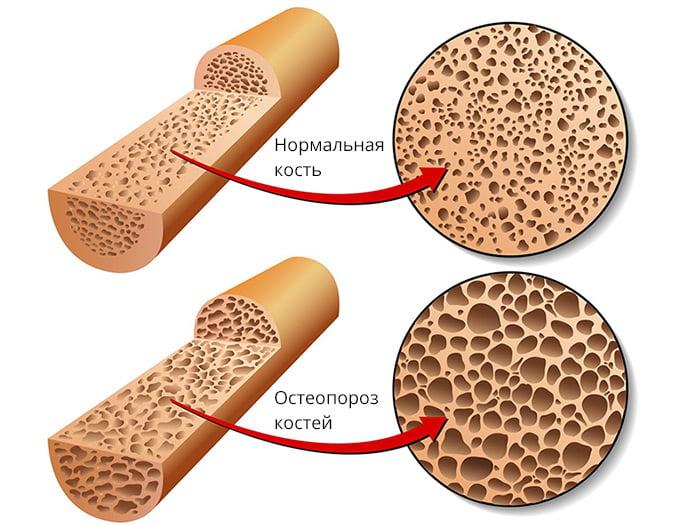
Остеопороз как видите делает кость рыхлее.
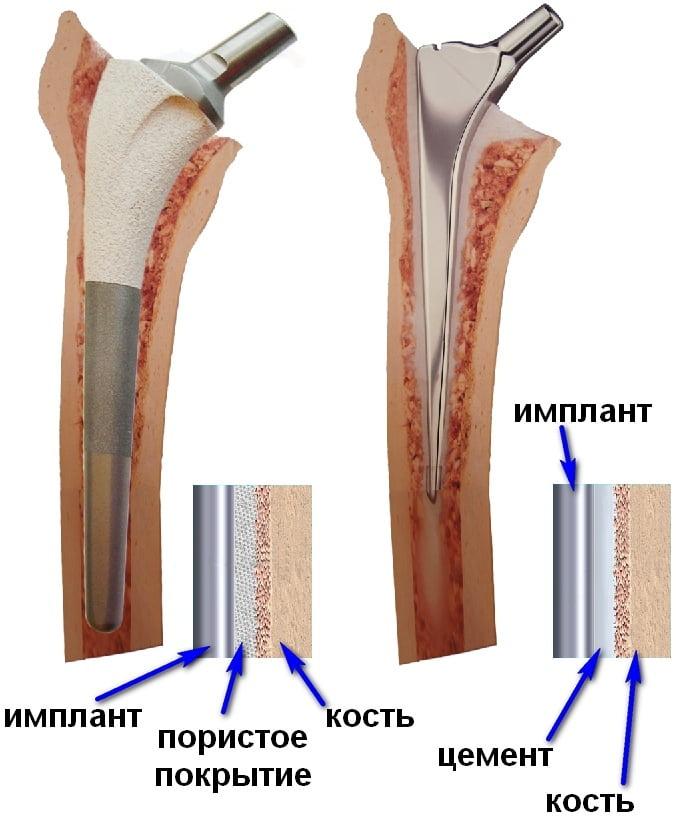
Именно состояние кости определяет какой тип фиксации будет использован.
Виды эндопротезов
Эндопротезная продукция, представлена следующими производителями:
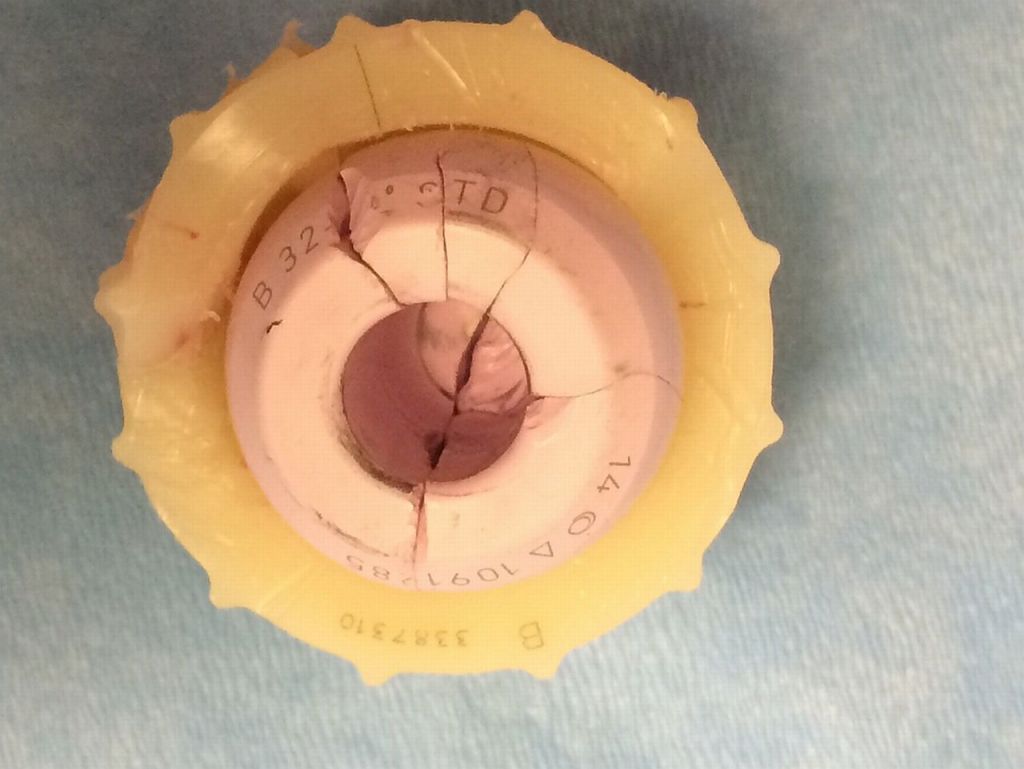
Керамика может треснуть, и если этому суждено случиться, то это в равной степени может произойти независимо от производителя импланта, потому что керамика всегда используется одной торговой марки.
Нельзя выделить из числа перечисленных брендов лучшего. Технологический подход, сборка, материалы, разнообразие типоразмеров, видовой ассортимент у всех одни и те же. Любой имплантат располагает самыми отменными техническими характеристиками. Поэтому отдавать свой приоритет какой-то определенной фирме попросту не имеет смысла. Высококачественные составляющие из диоксида циркония для всех моделей из керамики производит крупный концерн Ceramtech (США).

Линейка керамических компонентов.

Пара трения
Пара трения может быть разной: полностью металлической, керамической или в сочетании с полиэтиленом. Подбор узла трения определяется многими критериями: возрастом, весом, полом, физическим статусом, предполагаемым уровнем активности, заболеваниями в анамнезе и характером и тяжестью основной патологии. Больному может быть рекомендована любая из сочетающихся вариаций, фигурирующая в этом списке:
- металл-металл;
- металл-полиэтилен; ;
- керамика-полиэтилен.

Примеры полностью керамической пары трения.

В данном случае изображена комбинированная пара трения с полиэтиленом в качестве вертлужного компонента.
Объективно лучший вариант керамика-перекрестносвязанный полиэтилен. Это – современная комбинация, которая обеспечивает превосходную амортизацию и скольжение, отлично имитируя работу здорового сустава и гарантируя полную амплитуду движений.
Срок службы протеза
При корректно проведенной операции, грамотной реабилитации и строгом соблюдении правильного образа жизни, искусственный аналог тазобедренного сустава прослужит 20-30 лет. По возвращении домой необходимо не забывать об особенном режиме:
- чаще ходить, не допуская переутомления; сказал специалист, который наблюдает вас;
- продолжать заниматься лечебной гимнастикой, освоенной вами еще в медучреждении;
- следить за общим самочувствием и обращаться в больницу при любых недомоганиях, даже если они не связаны с протезированной ногой;
- следить за осанкой в момент сидения и в вертикальном положении;
- не перекрещивать ноги, кроме того, вы должны сидеть после эндопротезирования так, чтобы колени не находились на одном уровне с бедрами и, тем более, не превышали его;
- избегать интенсивных видов спорта, требующих совершения прыжков, поднятия тяжести, резких рывков телом и махов ногами.
Такое лечение позволяет жить активно без боли, но перегибать палку не стоит, потому что может произойти такой износ импланта как на фото.
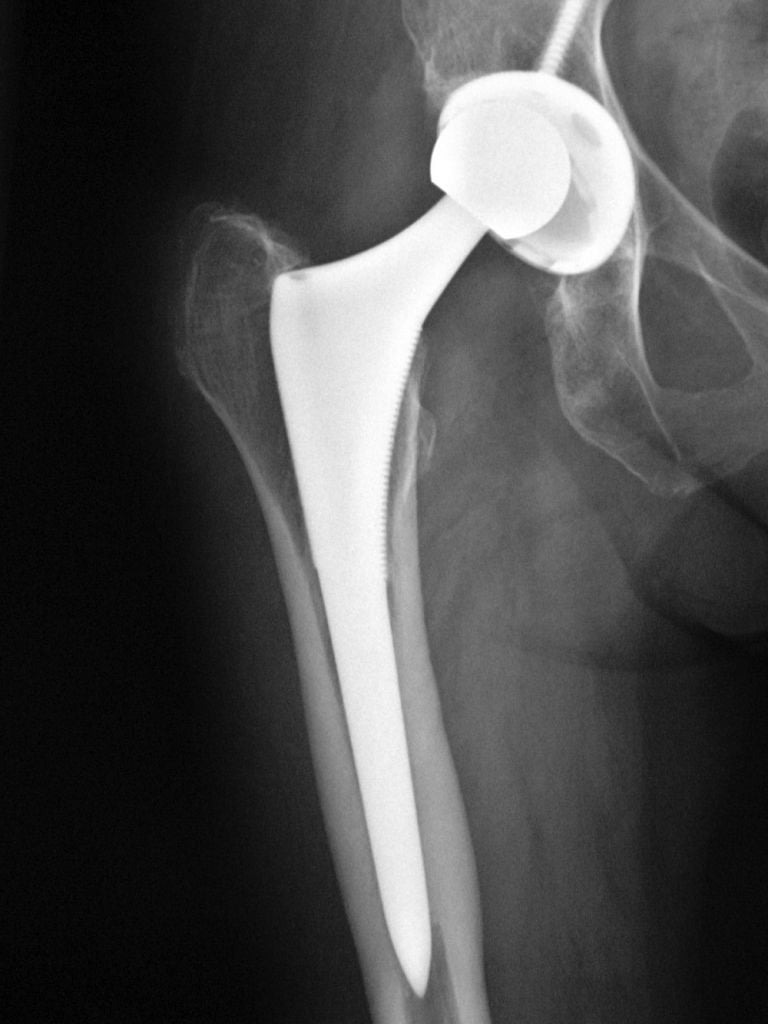
У слишком активных пациентов со временем может истончиться полиэтиленовый вкладыш, как это изображено на данном снимке.
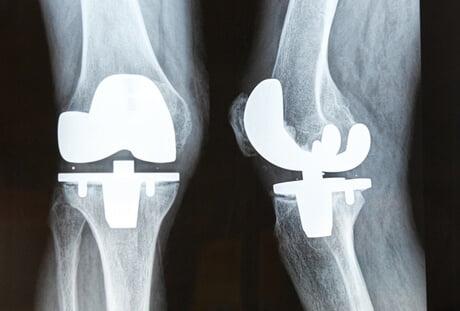
Рентен после первичной операции. Имплант стоит корректно.
После установки онкологического эндопротеза в ревизионной операции нуждается около 30% пациентов. Органосохраняющее лечение опухолей чаще сопровождается осложнениями, чем обычная замена сустава.
Операция по ревизионной замене коленного сустава длится намного дольше, чем при обычной. Это повышает риск развития инфекционных, тромбоэмболических и других осложнений.
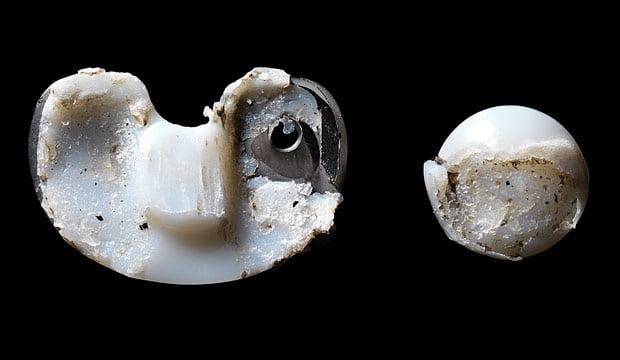
Извлеченный компонент эндопротеза по причине износа.
Цена повторной замены, то в случае асептической нестабильности она увеличивается на 25-100%, а при развитии перипротезной инфекции – в целых 3-4 раза. Цены на ревизионные эндопротезы также немного выше, чем на обычные.
В каких случаях нужна замена эндопротеза
Таблица 1. Наиболее частые осложнения, требующие замены эндопротеза.
| Осложнение | Причины развития | Суть и цель ревизионной операции |
| Перипротезная инфекция | Микробная контаминация раны в ходе операции или гематогенное занесение бактерий из очагов инфекции в организме. | Очистить рану от некротических масс, удалить компоненты эндопротеза, провести массивную антибиотикотерапию. Установить новый эндопротез через 3-6 месяцев после первого этапа лечения. |
| Асептическое расшатывание | Неправильный подбор и установка компонентов эндопротеза или развитие остеолиза. | Извлечение расшатавшегося импланта. Установка и надежная фиксация нового, ревизионного эндопротеза. Назначение препаратов, угнетающих остеолиз. |
| Перипротезный перелом | Установка большого протеза, инфекция, остеопороз, остеолизис. Спровоцировать перелом может падение или резкое движение. | Проведение металлоостеосинтеза, при необходимости – замена отдельных компонентов или всего протеза. |
| Несостоятельность мышц, связок, мягких тканей | Неудачный оперативный доступ к коленному суставу во время первичного эндопротезирования. | Проведение ревизионной операции с использование модифицированного доступа. |
| Повреждение компонентов эндопротеза | Травмы, падения, вывихи, неправильная установка импланта. | Замена поврежденных компонентов эндопротеза, их правильная пространственная ориентация. |
| Рецидив новообразования | Неполное удаление или высокая степень злокачественности опухоли. | Иссечение новообразования. Подбор и установка эндопротеза, который может полностью восстановить дефицит костной ткани. |
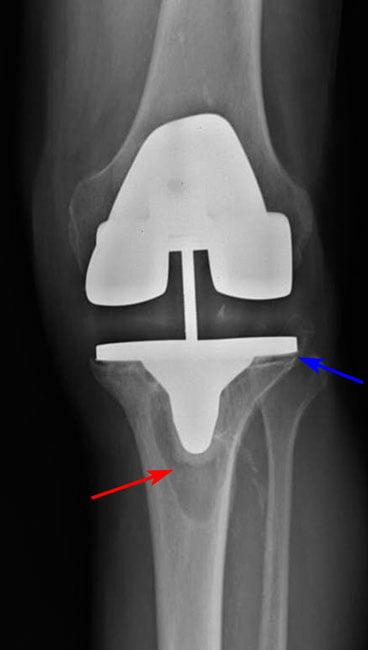
Рис 2. Остеолизис (красная стрелка) вокруг большеберцовой части приводит к ослаблению протеза (синяя стрелка).
Асептическое расшатывание
По данным разных авторов, осложнение является причиной 23-86% ревизионных хирургических вмешательств.
Асептическое расшатывание развивается вследствие остеолиза – невоспалительной резорбции костной ткани вблизи импланта. Причиной может быть системный остеопороз или сопряженное с возрастом нарушение метаболизма костей. Асептическая нестабильность возникает из-за неправильной имплантации компонентов эндопротеза.
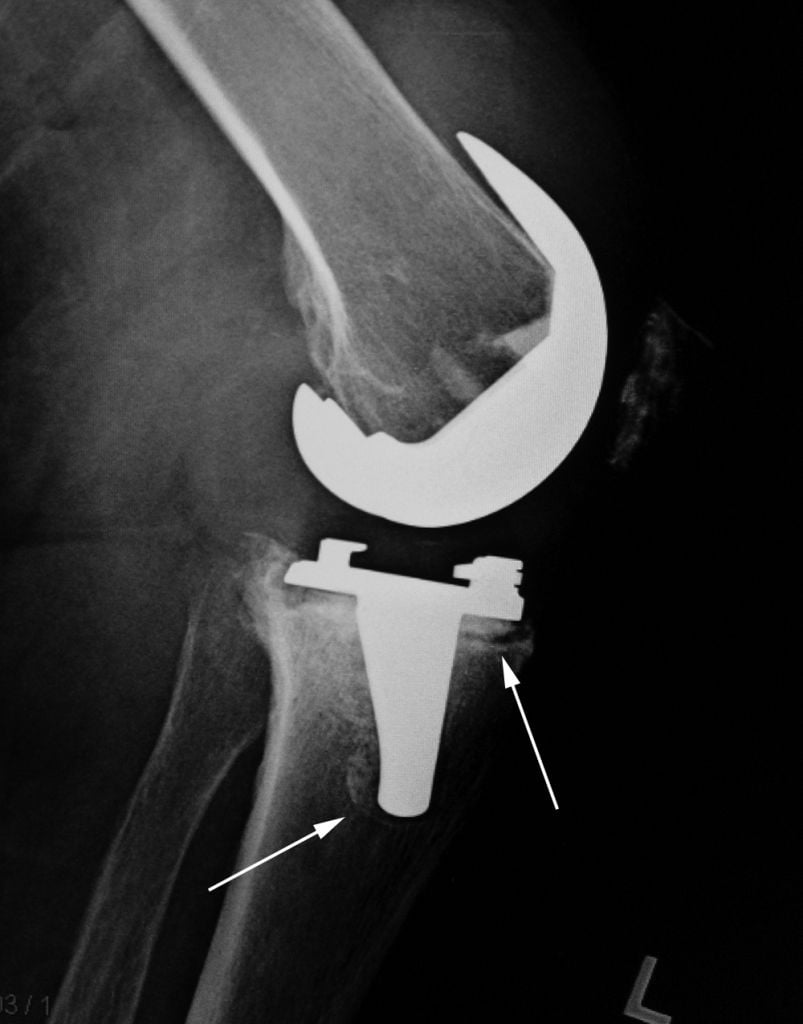
На снимке еле видны зоны прорежения костной ткани.
- выбор неподходящего протеза;
- неправильный подбор размера, типа и способа фиксации импланта;
- технические ошибки во время самого хирургического вмешательства;
- неадекватная пространственная ориентация эндопротеза.
Асептическая нестабильность бывает ранней и поздней. Первая развивается на протяжении 5 лет после операции и обычно говорит об ошибках врачей. Вторая возникает в более поздние сроки, чаще вследствие резорбции костной ткани. Существует ряд препаратов, приём которых помогает избежать остеолиза.

Инфекция — отторжение
Для патологии характерно воспаление костной ткани вблизи протеза с последующим развитием септической нестабильности сустава. Осложнение занимает 2-е место среди всех причин ревизионных операций.
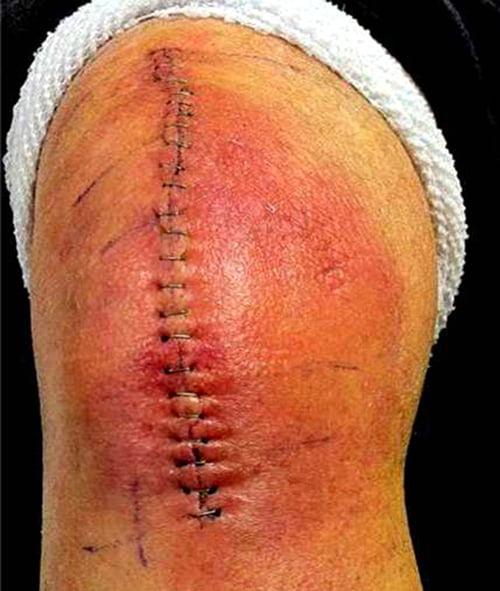
Красный и горячий шов это повод навестить врача.
Абсолютным показанием к повторной замене коленного сустава является только поздняя перипротезная инфекция, развивающаяся позднее 1 месяца после операции. Более ранние осложнения лечат консервативно или путем хирургического удаление некоторых компонентов протеза.

Повреждение импланта
Среди всех повреждений эндопротеза чаще всего встречается изнашивание тибиального полиэтиленовго вкладыша. Устранить проблему обычно удается открытым дебридментом. Суть операции заключается в артротомии, хирургической обработке суставной полости и замене вкладыша.
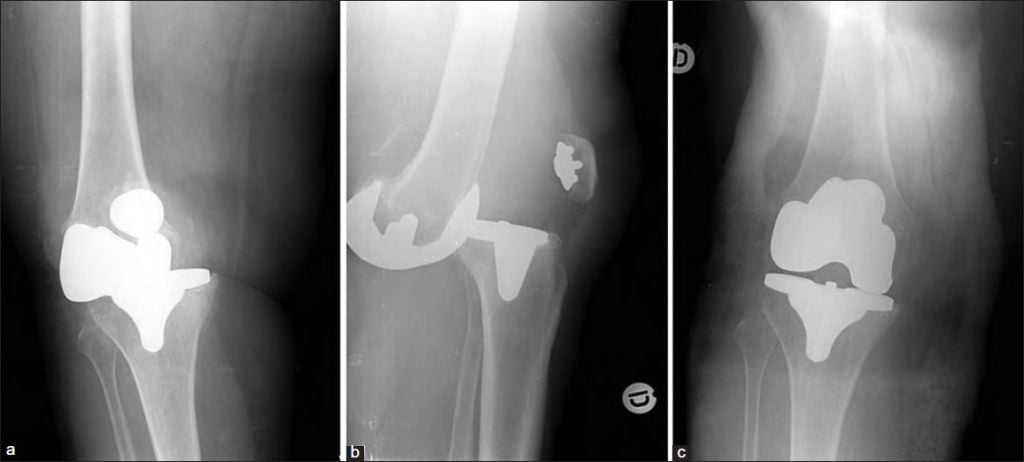
Результат травм или падений.
Ревизионное эндопротезирование необходимо делать в случае повторных вывихов, перелома одного или нескольких компонентов протеза.
Контрактуры или несостоятельность разгибательного аппарата
Показанием к ревизионной операции является нестабильность компонентов эндопротеза, возникшая из-за развития контрактур или несостоятельности разгибательного аппарата голени. Причиной может быть повреждение тканей в ходе операции или отсутствие реабилитации в восстановительном периоде.
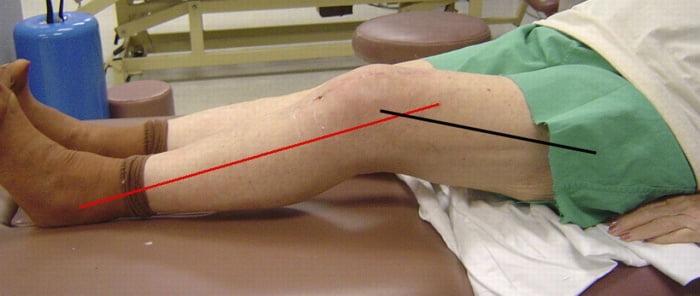
Переломы костей вблизи импланта
Переломы костей редкое осложнение. Они возникают на фоне остеолиза или после установки онкологического эндопротеза. Повторная замена сустава при переломе является необходимой. Она должна быть выполнена в максимально краткие сроки.
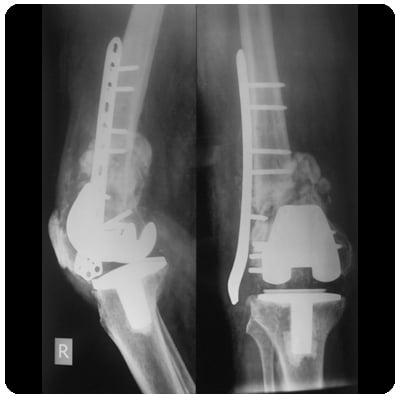
Конструкция после перелома.
Местный рецидив новообразования
Повторное хирургическое вмешательство требуется людям ранее перенесшим онкологическое эндопротезирование коленного сустава. Помимо обычных осложнений (асептическое или септическое расшатывание, переломы и т.д.) показанием к ревизионной операции может быть рецидив, то есть повторное развитие, опухоли.
Противопоказания к ревизионному эндопротезированию
Все противопоказания к повторной операции делятся на абсолютные и относительные. При наличии первых выполнять хирургическое вмешательство запрещено, поскольку это может привести к тяжелым осложнениям.
- неспособность пациента самостоятельно передвигаться;
- гемипарез на стороне планируемого хирургического вмешательства;
- острый или обострившийся тромбофлебит;
- тяжелые хронические заболевания сердечно-сосудистой системы;
- дыхательная недостаточность 3 ст.;
- наличие несанированных очагов хронической инфекции в организме;
- выраженная остеопения;
- серьезные психические или нейромышечные расстройства;
- отсутствие костномозгового канала бедренной кости.
Среди относительных противопоказаний нужно выделить печеночную недостаточность, тяжелые хронические декомпенсированные заболевания, гормональную остеопатию и ВИЧ-ассоциированные иммунодефицитные состояния.
Обследование перед операцией
Перед повторной заменой сустава пациент должен пройти обследование. Помимо общеклинических исследований ему назначают рентгенографию коленного сустава в 2-х проекциях, КТ, МРТ, денситометрию и УЗДГ вен нижних конечностей. Больному также делают развернутую коагулограмму и ЭхоКГ.
Сдача анализов, инструментальные методы исследования и консультации узких специалистов помогают оценить общее состояние пациента и тактику ревизионного эндопротезирования. Это дает возможность избежать непредвиденных осложнений и сделать хирургическое вмешательство успешным.
При выполнении ревизионного эндопротезирования большое значение имеет правильность подбора импланта. Поэтому в больнице, где выполняется хирургическое вмешательство, должна быть в наличии полная линейка эндопротезов.
Вмешательство при нестабильности без потери костной массы
В этом случае устанавливают как первичный, так и ревизионный эндопротез (окончательное решение врачи принимают после оценки состояния коллатеральных связок коленного сустава). Небольшие дефекты заполняют цементом, костной алло- или аутокрошкой.

Операция при выраженной потери костной массы
При выраженной потере губчатой и кортикальной костной массы нельзя использовать стандартные модели протезов. Причина этого – отсутствие нужной опоры для импланта. Поэтому в данной ситуации больному выполняют костную аллопластику и устанавливают специальный шарнирный эндопротез.

Операция при инфекционном сложении
Хирургическое вмешательство чаще всего выполняют в два этапа, интервал между которыми может составлять от 3 до 6 месяцев. На первом этапе хирурги удаляют эндопротез и некротические массы, обрабатывают рану антисептиками и устанавливают цементный спейсер с антибиотиками широкого спектра действия. Только после исчезновения признаков инфекции больному устанавливают новый эндопротез.
Реабилитация в послеоперационном периоде
В первые дни после операции больному проводят тщательную профилактику тромбоэмболических осложнений. С этой целью ему бинтуют ноги эластичными бинтами или чулками. Вместе с этим больному подбирают комплекс упражнений, позволяющий восстановить нормальную подвижность сустава. Отметим, что в первые дни медперсонал практически учит человека двигаться, ходить, подниматься по лестнице.
Первое время шов надежно прячется.
В более позднем восстановительном периоде пациенту нужна лечебная гимнастика, физиотерапия и некоторые другие реабилитационные мероприятия. Именно они помогают восстановить функциональную активность колена и вернуть больного к полноценной жизни. Отсутствие полноценной реабилитации повышает риск развития осложнений и нередко приводит к неудовлетворительным результатам ревизионного эндопротезирования.
Парапротезная инфекция – это инфекционный процесс в области сустава, возникающий после эндопротезирования и патогенетически связанный с наличием имплантата. Проявляется локальными признаками воспаления: отеком, болезненностью, местной гиперемией и гипертермией, нарушением функции конечности в сочетании с симптомами общей интоксикации. Нередко протекает со стертой клинической симптоматикой. Диагностируется с учетом анамнеза, лабораторных анализов, рентгенологических методик, МРТ, УЗИ. В зависимости от вида параэндопротезной инфекции выполняются ревизии с сохранением эндопротеза либо удаление имплантата с реэндопротезированием, артродезом, костно-мышечной пластикой.
МКБ-10
Общие сведения
Парапротезная инфекция – актуальная проблема современной травматологии и ортопедии. Последние десятилетия ознаменовались широким распространением эндопротезирования. Увеличилось не только общее количество операций, но и количество протезируемых суставов. Если раньше замене, в основном, подвергали тазобедренный сустав, то в наши дни рутинной практикой стало протезирование коленного, плечевого, других средних и мелких суставов конечностей. Соответственно, возросло число случаев развития инфекционного процесса в области оперативного вмешательства. Распространенность патологии при первичном эндопротезировании составляет 0,3-1%. Частота осложнения при повторной установке искусственного сустава, по различным данным, колеблется от 9 до 40%. В большинстве случаев осложнение возникает в первые два года после операции.

Причины
Непосредственной причиной парапротезной инфекции становятся болезнетворные бактерии, при этом существует определенная связь между типом возбудителя и видом протеза, обусловленная склонностью микробов к адгезии к тем или иным инородным материалам, находящимся в организме пациента. Так, в области металлических частей имплантата инфекция чаще вызывается золотистым стафилококком, в зоне полимерных – эпидермальным стафилококком. Наряду со стафилококковой флорой воспаление могут провоцировать стрептококки, кишечная палочка и некоторые другие микроорганизмы. Обстоятельствами, способствующими возникновению воспалительного процесса, считаются:
- Особенности вмешательства. Установлено, что при длительности операции более 3 часов вероятность осложнения увеличивается, что связано с продолжительным контактом тканей с внешней средой, нарушениями кровообращения, локальными обменными расстройствами и общей реакцией организма на стресс. Большое значение имеют интраоперационные осложнения, технические трудности и значительная кровопотеря, усугубляющие действие перечисленных факторов.
- Особенности установки эндопротеза. Риск развития инфекции в зоне искусственного сустава повышается при применении дополнительных биологических и синтетических материалов, нестабильности имплантата. В первом случае имеет значение реакция организма на наличие чужеродных элементов, во втором появляется постоянный источник травматизации окружающих тканей, создаются благоприятные условия для внедрения инфекционных агентов.
К числу особенностей организма пациента, способствующих появлению данного осложнения, относят пожилой возраст, наличие тяжелой соматической патологии и иммунные нарушения различного генеза. Негативную роль играет многократное или длительное применение антибиотиков перед операцией, обуславливающее устойчивость микроорганизмов к антибактериальной терапии, нарушение рекомендаций врача относительно режима активности и реабилитационных мероприятий в послеоперационном периоде.
Патогенез
Парапротезная инфекция – разновидность имплантат-ассоциированной инфекции, которая возникает после эндопротезирования вследствие способности патогенных микробов к колонизации имплантатов. Бактерии, вызывающие это осложнение, обладают свойством формировать биофильмы (биологические пленки) на поверхностях чужеродных материалов в организме больного. Выделяют два механизма возникновения биопленок. Первый – неспецифическое взаимодействие непосредственно между поверхностью протеза и микроорганизмами за счет сил поверхностного натяжения, водородных связей, гидрофобности, электростатического поля и т. д.
Второй – контакт бактерий с белками, располагающимися на поверхности искусственной конструкции. После установки части эндопротеза очень быстро покрываются слоем белков, среди которых преобладают альбумины. При адгезии микробов к этим белкам формируются микроколонии. Вначале имплантат колонизируется аэробными микроорганизмами, в последующем в глубоких слоях биофильма создается благоприятная среда для развития анаэробной микрофлоры. При увеличении биопленки или под влиянием внешних воздействий ее части отрываются от поверхности имплантата, происходит диссеминация процесса. Исследование перечисленных механизмов позволило объяснить устойчивость инфекции и неэффективность консервативной терапии этого осложнения.
Классификация
Существует много вариантов классификации параэндопротезной инфекции, однако общепризнанная международная систематизация этого осложнения пока отсутствует. Обычно травматологи-ортопеды используют классификацию Ковентри-Фитцджеральда, в основе которой лежит временной период между операцией и манифестацией инфекционного процесса. Различают четыре типа парапротезной инфекции:
- Острая послеоперационная. Признаки инфицирования определяются в течение месяца после вмешательства.
- Поздняя хроническая. Осложнение диагностируется во временном промежутке от 1 месяца до 1 года с момента операции.
- Острая гематогенная. Симптомы патологии возникают через 1 и более год после установки искусственного сустава.
- Положительная интраоперационная культура. Характеризуется бессимптомным течением при выявлении бактерий в 2-х и более интраоперационных образцах ткани.
В российской клинической практике также применяют систематизацию инфекций в области хирургических вмешательств, разработанную сотрудниками Новосибирского НИИТО. Согласно этой классификации различают три вида послеоперационных инфекционных процессов: ранний острый (возникший в первые 3 месяца), поздний острый (развившийся в течение 3-12 месяцев), хронический (диагностированный спустя 1 год и более после операции). При постановке диагноза отмечают наличие или отсутствие нестабильности эндопротеза.
С учетом формы выделяют флегмоноподобную, свищевую, латентную и атипичную инфекции, с учетом глубины – поверхностную и глубокую. Несмотря на то, что поверхностная инфекция протекает без вовлечения эндопротеза (то есть, имеет другой патогенез), поражает только кожные покровы и подкожную клетчатку, поддается консервативной терапии, специалисты рассматривают ее в рамках параэндопротезной инфекции, поскольку такой подход позволяет учесть все возможные варианты инфекционных осложнений эндопротезирования.
Симптомы парапротезной инфекции
Проявления патологии зависят от времени возникновения и глубины процесса. Поверхностная инфекция развивается в период восстановления после операции, сопровождается воспалением мягких тканей при интактности оперированного сустава. Характеризуется гиперемией, локальной припухлостью, повышением местной температуры, незначительными или умеренными болями, нарушением заживления раны, расхождением ее краев, наличием гнойного отделяемого. Возможно образование участков поверхностного некроза, формирование лигатурных свищей. Выраженность общей интоксикации определяется распространенностью поражения кожи и жировой клетчатки.
Глубокая парапротезная инфекция может манифестировать как в раннем послеоперационном периоде, так и спустя продолжительное время после вмешательства. Поражает мышцы и фасции. Проявляется отечностью мягких тканей, болью в проекции сустава, ограничением функции конечности, общими интоксикационными симптомами: повышением температуры тела до 38 °С и выше, ознобами, слабостью, разбитостью, тахикардией, тахипноэ. Возможно сочетание глубокого и поверхностного процесса, рассматриваемое специалистами как разновидность глубокой инфекции. Из-за распространенности иммунологических нарушений в популяции патология часто протекает со сглаженной симптоматикой. Снижение иммунитета усугубляют переливания крови, лекарственная терапия и другие лечебные мероприятия, проводимые на пред- и послеоперационном этапе.
Осложнения
Наиболее частые осложнения параэндопротезной инфекции обусловлены распространением гнойного процесса. Наблюдается образование абсцессов и флегмон. Особенно опасны глубокие затеки в полость таза, иногда формирующиеся при поражении оперированного тазобедренного сустава. В тяжелых случаях возможно развитие сепсиса. При часто рецидивирующей патологии снижается или утрачивается трудоспособность, ухудшается качество жизни больных, персистирующий очаг инфекции оказывает негативное влияние на деятельность внутренних органов.
Диагностика
Диагноз обычно выставляют специалисты в области ортопедии, наблюдающие пациентов, перенесших эндопротезирование сустава. Из-за часто встречающихся стертых форм и неспецифичности результатов дополнительных методик распознавание парапротезной инфекции может представлять определенные затруднения. Программа обследования обычно включает следующие методы:
- Опрос, осмотр. Признаком, указывающим на вероятность возникновения данной патологии, является замена сустава в анамнезе. Ортопед уточняет жалобы, время появления и динамику развития симптомов, оценивает внешний вид и функцию сустава, выявляет признаки воспаления, участки некроза, свищевые ходы и пр.
- Ультразвуковое сканирование. УЗИ сустава применяется в качестве скринингового метода, позволяет обнаружить абсцессы или гематомы, выполнить прицельную пункцию гнойного очага для последующего изучения содержимого в процессе бактериологического исследования.
- Рентгенологические методики. Результаты обычной рентгенографии часто неоднозначны. О наличии заболевания могут свидетельствовать остеолиз и периостальная реакция, без видимых причин возникшие после успешного вмешательства. Для оценки динамики процесса обязательно выполняют контрольные снимки. При свищах производят рентгенофистулографию для определения локализации свищевых ходов и затеков.
- Магнитно-резонансная томография. Является уточняющим методом, назначается на этапе предоперационного обследования для оценки размеров и расположения глубоких (в том числе – внутритазовых) абсцессов, уточнения объема хирургического вмешательства.
- Лабораторные анализы. При острой патологии в ОАК обнаруживаются признаки воспаления: лейкоцитоз, нейтрофилез, лимфоцитопения, сдвиг формулы влево, повышение СОЭ. При хронических формах изменения крови могут быть выражены незначительно. Более специфичны результаты исследования на С-реактивный белок, отражающие динамику воспалительного процесса, а также данные бакпосева раневого отделяемого. Микробиологический анализ синовиальной жидкости часто отрицательный из-за формирования биопленок.
Лечение парапротезной инфекции
В случаях поверхностного инфекционного процесса тактика такая же, как при других инфицированных ранах. Осуществляется санация поверхностного гнойного очага на фоне антибиотикотерапии, операции на суставе не требуются. При глубокой инфекции тактика определяется типом патологии с учетом времени ее возникновения, наличием либо отсутствием нестабильности сустава, расположением и размером гнойных затеков, состоянием костей и мягких тканей, устойчивостью флоры к антибактериальным препаратам и некоторыми другими факторами. Лечение только хирургическое. Существуют следующие варианты вмешательств:
- Ревизия с сохранением имплантата. Проводится при раннем инфицировании, сохранении стабильности сустава, незначительном поражении элементов эндопротеза. Сустав вскрывают, исследуют его поверхности. Инфицированные окружающие ткани иссекают, полиэтиленовый вкладыш заменяют (при необходимости – вместе с головкой протеза), рану ушивают, дренируют.
- Ревизионное эндопротезирование. Рекомендуется при поздней хронической и иногда – острой гематогенной парапротезной инфекции, предполагает одно- двух- или трехэтапную замену имплантата. Чаще всего используют двухэтапное реэндопротезирование, на первом этапе выполняют ревизию раны, затем после курса антибиотикотерапии устанавливают новый протез. При трехэтапном вмешательстве на втором этапе производят костную пластику.
- Артродез сустава. Показан при рецидивирующей инфекции, резистентности патогенной флоры к антибиотикам. Предусматривает удаление эндопротеза и наложение аппарата внешней фиксации для создания неподвижного соединения между концами костей.
- Ампутация или экзартикуляция. Осуществляется редко, в качестве показаний рассматривается наличие упорно рецидивирующего очага инфекции, представляющего угрозу для жизни больного, при одновременной утрате функции конечности.
Прогноз и профилактика
1. Медицинские и социальные проблемы эндопротезирования суставов конечностей/ Москалев В.П., Корнилов Н.В., Шапиро. К.И. - 2001
2. Инфекционные осложнения после эндопротезирования крупных суставов как актуальная проблема современной ортопедии/ Муконин А.А.// Новые медицинские технологии - 2006 -№ 8
3. Лечение параэндопротезной инфекции тазобедренного сустава: клинические рекомендации/ Министерство здравоохранения РФ - 2013
Читайте также:

