Сафоцид при молочнице отзывы
Обновлено: 26.04.2024
Бактериальный вагиноз и вульвовагинальный кандидоз: оптимальные схемы лечения больных с сочетанной инфекцией
Журнал: Российский вестник акушера-гинеколога. 2013;13(3): 42‑46
Кузнецова И.В. Бактериальный вагиноз и вульвовагинальный кандидоз: оптимальные схемы лечения больных с сочетанной инфекцией. Российский вестник акушера-гинеколога. 2013;13(3):42‑46.
Kuznetsova IV. Bacterial vaginosis and vulvovaginal candidiasis: optimal treatment regimens for patients with mixed infection. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(3):42‑46. (In Russ.).
Вагиниты являются широко распространенной проблемой и одним из самых частых поводов обращения к акушеру-гинекологу. Среди разнообразных вариантов вагинальной инфекции бесспорными лидерами считаются вульвовагинальный кандидоз (ВВК) и бактериальный вагиноз (БВ), выявляемые соответственно у 17-39% и 22-50% женщин с патологическими выделениями (белями) из влагалища [5]. Распространенность ВВК и БВ чрезвычайно высока. Приблизительно 75% женщин репродуктивного возраста сталкиваются с ВВК, по крайней мере, 1 раз в течение жизни, у 40-45% отмечаются 2 редицива заболевания и более. Большинство случаев ВВК классифицируются как неосложненный кандидоз [8], но примерно у 10% больных ВВК имеет осложненное течение.
Бактериальный вагиноз считается самой частой формой заболеваний влагалища и встречается приблизительно у 30% женщин [4]. При бесспорном инфекционном происхождении ВВК и БВ их заразность для полового партнера не доказана [4, 13], и они не относятся к инфекциям, передаваемым половым путем (ИППП). Тем не менее ряд факторов, связанных с сексуальным поведением, увеличивает риск возникновения этих заболеваний. К ним относятся: начало половой жизни, практика орогенитального секса, смена полового партнера, частое спринцевание влагалища [4].
Проблемы, связанные с ВВК и БВ, доставляют пациенткам множество неудобств, связанных не только с изменением количества и качества влагалищных выделений, но и жжением, раздражением кожи, ощущением сухости, диспареунией, дизурией [5]. Помимо сиюминутного дискомфорта, БВ и ВВК увеличивают риск спонтанного аборта, преждевременных родов, анте- и интранатального инфицирования плода [12, 19, 22], послеродового эндомиометрита, способствуют развитию цервицитов, воспалительных заболеваний органов таза с вовлечением мочевыделительной системы, распространению вирусной инфекции, в том числе ВИЧ и генитального герпеса, гонореи, хламидиоза, трихомониаза, повышают риск воспалительных послеоперационных осложнений [7, 33, 38].
По данным США, Европы, Канады, наиболее частым возбудителем ВВК является Candida albicans (около 80-90% случаев). Остальные грибы рода Candida носят общее название не-albicans и представляют разнородную группу микроорганизмов, среди которых наиболее часто встречается C. glabrata [37]. Согласно результатам эпидемиологического исследования ARTEMISK DISK в России, основным возбудителем кандидозов (различных локализаций, в том числе ВВК) стала C. albicans - 76,1%, на втором месте оказалась C. glabrata - 5,3%, далее C. krusei - 3,4%, C. parapsilosis - 3,1%, что в целом соответствует распространенности тех или иных видов грибов в Северной Америке и Европе [32]. Вульвовагинальный кандидоз, вызванный Candida не-albicans, расценивается как осложненное заболевание. Помимо этого, к осложненным формам ВВК относят тяжелый вагинит, ВВК у лиц со сниженным иммунным ответом, рецидивирующий ВВК.
Какие именно причины лежат в основе частых (4 раза в год и более) повторных эпизодов заболевания, до конца не ясно. Системная иммуносупрессия не может служить достаточным обоснованием рецидивирующего ВВК. Это наглядно демонстрируется наблюдениями за ВИЧ-инфицированными больными, у которых колонизация влагалища грибами Candida значительно повышается, но при этом частота рецидивирующего ВВК растет умеренно, намного отставая от роста частоты эпизодов орофарингеального кандидоза [28]. Более вероятно, что рецидивы ВВК обусловливает подавление либо снижение местных защитных иммунорегуляторных механизмов с изменением цитокинового профиля [18]. Существует версия, что причиной симптомных кандидозов является повышенная локальная чувствительность к грибам [15].
Диагностика ВВК основывается на обнаружении почкующихся дрожжевых клеток и/или псевдомицелия при световой микроскопии нативных препаратов или микроскопии мазков, окрашенных по Граму. При осложненном ВВК рекомендуется культуральное исследование (посев на питательную среду). Candida spp. - одноклеточные микроорганизмы размерами 6-10 мкм. Многие Candida spp. диморфны, образуют бластомицеты (клетки-почки), псевдомицелий (цепочки почкующихся дрожжевых клеток) и/или мицелий. В отличие от мицелия, псевдомицелий не имеет общей оболочки и перегородок. Возбудители Candida не-albicans, особенно С. glabrata, не формируют псевдомицелий и плохо распознаются при световой микроскопии, в связи с чем наличие симптомов ВВК при отрицательных результатах микроскопии диктует необходимость выполнения культурального исследования.
Для БВ этиологическая роль конкретного микроорганизма в качестве единственной причины заболевания до сих пор не доказана. Чаще всего с БВ ассоциируют Gardnerella vaginalis и Mobiluncus curtisii, но эти микроорганизмы можно обнаруживать и у здоровых женщин [16]. Появление методов амплификации нуклеиновых кислот (МАНК) и полимеразной цепной реакции, позволяющих идентифицировать микроорганизмы, плохо поддающиеся культивированию, расширило микробную палитру БВ. Оказалось, что в отличие от микробного спектра содержимого влагалища здоровых женщин (от 1 до 6 видов бактерий с преобладанием лактобактерий), у женщин с БВ наблюдается значительно большее разнообразие микроорганизмов (от 9 до 17 в образце, в среднем - 12,6), причем в каждом образце было выявлено 58% совершенно новых клонов [11]. Всего у женщин с БВ были идентифицированы 35 видов уникальных бактерий, включая несколько видов, у которых не оказалось ближайших родственных культур, а особое место среди видов микроорганизмов, которые с внедрением МАНК стали с большой частотой обнаруживать при БВ, занял Atopobium vaginae [11, 14, 39]. Кроме A. vaginae, список некультивируемых микроорганизмов пополнили БВ-ассоциированные бактерии - BVAB 1, BVAB 2, BVAB 3, Megasphera spp., Eggerthella spp. и Leptotrichia spp. [17, 20].
Для оценки видового разнообразия бактериальной флоры, обнаруживаемой при БВ, был разработан ДНК-биочип [1], использование которого позволило выявить у 80 женщин с БВ [2] 29 различных видов микроорганизмов, причем чаще всего идентифицировался A. vaginae. Важно, что с наибольшей частотой A. vaginae обнаруживался при длительном рецидивирующем течении заболевания, причем независимо от других БВ-ассоциированных микроорганизмов (G. vaginalis, Mobiluncus spp., Ureaplasma urealyticum, Mycoplasma hominis) [2]. Хотя A. vaginae обнаруживали в содержимом из влагалища не только при БВ, но и у здоровых женщин, соотношение распространенности A. vaginae среди пациенток с БВ явно выше, чем среди здоровых женщин [1].
Несмотря на очевидную разницу между аэробной грибковой и полимикробной, преимущественно анаэробной, инфекцией, ВВК и БВ могут сочетаться, создавая дополнительные сложности в лечении. Диагностика такой микстинфекции базируется на данных микроскопии мазка, окрашенного по Граму, и/или результатах культурального исследования. При микроскопии влагалищного мазка обнаруживаются преимущественно поверхностный эпителий, ключевые клетки. Лейкоцитарная реакция отражает наличие воспаления. При большом (массивном) количестве микроорганизмов доминируют анаэробы и гарднереллы, присутствуют дрожжевые клетки и/или фрагменты псевдомицелия, лактобациллы отсутствуют. Культуральное исследование демонстрирует массивное (более 9 lg КОЕ/мл) количество микроорганизмов, но в аэробных условиях присутствуют только грибы Candida. Лактобациллы отсутствуют или их титр очень низок, доминируют бактероиды, гарднерелла, анаэробные кокки и др.
Сочетание ВВК и БВ требует одновременного лечения обеих инфекций. Но даже в отсутствие клинических и лабораторных признаков ВВК лечение БВ антибиотиками может привести к развитию симптомов кандидоза в случаях предшествующей колонизации влагалища грибами [30].
Существует два эффективных способа лечения бактериального вагиноза. Один из них - метронидазол или его производные из группы 5-нитроимидазолов. Истинная устойчивость анаэробных микроорганизмов к нитроимидазолам - явление нечастое. Как правило, эффективность метронидазола при БВ в суточных дозах от 800 до 1200 мг в течение 1 нед превышает 90%, причем эффект в течение 1 мес сохраняется у 80% пациенток. Одномоментное лечение БВ метронидазолом в дозе 2 г эффективно в отношении купирования симптомов, но процент рецидивов при этом выше, чем при использовании недельного курса того же препарата. Существенным недостатком перорального приема метронидазола является его плохая переносимость, а тинидазол в режиме 5-дневного приема хотя и переносится лучше, но имеет тот же потенциал побочных воздействий, что и метронидазол [23]. Местная терапия 2% кремом с клиндамицином или гелем с метронидазолом столь же эффективна, как и системная терапия [12, 27], при этом клиническая эффективность клиндамицина продемонстрирована и при наличии устойчивости обнаруженных в анализах микроорганизмов к этому антибиотику [7, 27]. Согласно рекомендациям Центра по контролю заболеваемости США (CDC), различные формы метронидазола (таблетки и гель) и 2% крем (свечи) клиндамицина являются стандартами терапии БВ в США.
Метронидазол назначается в дозе 500 мг 2 раза в день в течение 7 дней, или 0,75% гель метронидазола 5 г интравагинально 1 раз в день в течение 5 дней, или 2% крем клиндамицина по 5 г интравагинально в течение 7 дней. В качестве альтернативы эти рекомендации предлагают лечение клиндамицином внутрь по 300 мг 2 раза в день 7 дней или свечи клиндамицина по 100 мг интравагинально на ночь 3 суток подряд. Бесспорно, наиболее приемлемой для женщин является самая короткая схема лечения, предполагающая 3-дневный курс клиндамицина в свечах. Что касается назначения одномоментного лечения метронидазолом (внутрь в дозе 2 г), то удобство этой схемы нивелируется относительно низкой эффективностью, и поэтому она в настоящее время не рекомендуется CDC даже в качестве альтернативного варианта [12]. В Европейских рекомендациях [13] по ведению больных с выделениями из влагалища также указано на невысокую эффективность одномоментного применения метронидазола в дозе 2 г при БВ. Согласно Российским рекомендациям [3], предпочтительным методом является местное (интравагинальное) назначение метронидазола или клиндамицина: клиндамицин, крем 2% по 5,0 г интравагинально на ночь, 6 дней; метронидазол, гель 0,75% по 5,0 г интравагинально на ночь, 5 дней. Альтернативная схема подразумевает возможность использования свечей клиндамицина (100 мг) в течение 3 дней. Внутрь 5-нитроимидазолы или клиндамицин рекомендуют назначать только при неэффективности интравагинальной терапии: метронидазол 500 мг внутрь 2 раза в сутки в течение 7 дней; клиндамицин 300 мг 2 раза в сутки в течение 7 дней; орнидазол 500 мг внутрь в течение 5 дней.
Серьезную проблему представляют резистентные к терапии случаи БВ [40]. В случае неэффективности стандартной терапии метронидазолом возможно ее повторение с увеличением продолжительности, а при повторной неудаче рекомендуют еще одну попытку повторения с предварительным курсом лечения антибиотиками с целью элиминировать сопутствующую аэробную микрофлору, способную снижать эффективность воздействия нитрогруппы 5-нитроимидазолов на анаэробы [12, 13]. Однако целесообразность такого подхода представляется спорной по двум причинам. Во-первых, длительные курсы перорального применения метронидазола плохо переносятся. Во-вторых, причиной отсутствия эффекта от терапии могут быть не аэробные микроорганизмы, а ассоциированные с БВ анаэробы, нечувствительные к нитроимидазолам.
Устойчивостью к метронидазолу могут обладать некультивируемые или труднокультивируемые микроорганизмы, они же и обеспечивают упорное рецидивирующее течение БВ. Повторные эпизоды вагинита наблюдаются у 30% женщин в течение 3 мес после лечения [40]. Серия исследований, проведенных в Австралии, показала, что после перорального применения метронидазола рецидивы БВ в течение 1 года наблюдений отмечались у 58% пациенток [9]. Факторы риска рецидива ассоциировались с наличием БВ в предшествующем анамнезе, регулярной половой жизнью с постоянным партнером, лесбиянством. Использование презерватива не влияло на риск, а гормональная контрацепция имела протективный эффект. При молекулярном анализе некультивируемых организмов авторы исследования обнаружили, что неудачи долговременного эффекта терапии метронидазолом достоверно чаще были связаны с выявлением A. vaginae [10].
Невозможность идентификации некультивируемых микроорганизмов в рутинной практике до начала терапии становится залогом ее неэффективности [7, 11]. Устойчивость A. vaginae к метронидазолу была продемонстрирована неоднократно [14]. В ряде публикаций [7, 41] было показано, что A. vaginae в исследованиях in vitro обладает большей чувствительностью к клиндамицину, чем к метронидазолу. Клинические исследования подтверждают достоверно более высокую эффективность стандартной интравагинальной терапии БВ, ассоциированного с A. vaginae, клиндамицином (2% крем по 5 г интравагинально 6 дней) по сравнению с метронидазолом (0,75% гель по 5 г интравагинально 5 дней, на ночь). Аналогичные результаты были получены в исследованиях, сравнивавших топическую терапию метронидазолом и клиндамицином при БВ, предположительно ассоциированным с морфотипами Mobiluncus [26].
По-видимому, особенности чувствительности микроорганизмов, участвующих в развитии БВ, являются ведущим фактором неэффективности лечения или повышенной частоты рецидивов. Стратегии лечения половых партнеров и реколонизации влагалища лактобациллами не продемонстрировали значимого эффекта по снижению частоты рецидивов и нормализации микробиоты влагалища [6, 40], хотя отдельные исследования по использованию эубиотиков и пробиотиков дают обнадеживающие результаты [24]. В то же время нельзя сбрасывать со счетов участие аэробных микроорганизмов, в том числе грибов, в ухудшении прогноза лечения БВ. Сравнение геля метронидазола и влагалищных таблеток, содержащих метронидазол с нистатином, обнаружило снижение частоты рецидивов при использовании комплексного препарата [27] даже в отсутствие данных об исходной грибковой инфекции.
Таким образом, несмотря на сравнимую эффективность метронидазола и клиндамицина, последний имеет очевидные преимущества в лечении рецидивирующего БВ ввиду более широкого спектра воздействия на микроорганизмы, включая некультивируемые или трудно культивируемые формы. Применение 3-дневного курса вагинальных таблеток клиндамицина сравнимо по эффективности с другими курсами терапии, но кратковременность лечения обеспечивает большую приемлемость метода для пациенток. Однако применение клиндамицина чревато возникновением ВВК, что требует профилактических мер.
Для лечения ВВК предложено несколько групп лекарственных средств местного и системного действия. Эффективность их эквивалентна, как было продемонстрировано в систематическом обзоре 19 рандомизированных контролируемых исследований (РКИ), сравнивавших методы топической и пероральной терапии антимикотиками [25], хотя авторы обзора отметили тенденцию к лучшим отдаленным последствиям проведения пероральной терапии, связанным с меньшей частотой рецидивов [35]. Бесспорным лидером пероральной терапии с хорошим профилем безопасности и эффективности является флуконазол, который при неосложненном кандидозе используется в дозе 150 мг однократно [34].
Наличие рецидивирующего ВВК предполагает продолжительные режимы лечения. Из них наибольшей популярностью в мире пользуется применение флуконазола в дозе 150 мг 1 раз в неделю в течение 6 мес после первоначального купирования очередного острого эпизода трехкратным приемом 150 мг флуконазола с интервалом 72 ч. По результатам РКИ, 6-месячное использование флуконазола сопровождалось значимо меньшим числом рецидивов после его окончания (9%) по сравнению с плацебо (64%), причем ни одна из пациенток не прекратила лечение из-за побочных эффектов [37]. Несмотря на то что у части больных симптомы ВВК возвращаются через несколько месяцев после окончания лечения, схема супрессивной терапии флуконазолом является на сегодняшний день единственным методом, имеющим доказательную базу эффективности. Для контроля симптомов ВВК в отсутствие достаточного эффекта шестимесячного курса рассматривается возможность его пролонгации до года. Другие лечебные подходы, в том числе использование йогурта, лактобацилл, десенситизация к антигену Candida, низкоуглеводистая диета, пока не подтвердили свою эффективность в клинических исследованиях [31].
Вероятной причиной рецидивов ВВК и/или устойчивости к терапии являются особенности возбудителя инфекции. Известно, что чувствительностью к азоловым антимикотикам обладает C. albicans, самый частый возбудитель ВВК. Candida не-albicans отличается устойчивостью к большинству антимикотических средств, и лечение таких больных всегда представляет большую проблему. В США и Европе эта проблема разрешается с помощью 2-недельного курса желатиновых вагинальных капсул, содержащих 600 мг борной кислоты, к такому виду терапии чувствительна C. glabrata, самый распространенный не-albicans возбудитель [36]. Еще один способ терапии предлагает местное использование амфотерицина В (свечи 50 мг) изолированно или в комбинации с флуцитозином в течение 14 дней [29]. К сожалению, в России эти методы лечения недоступны, поэтому в отечественной клинической практике задача элиминации устойчивых возбудителей может решаться только с помощью повышения дозы азоловых антимикотиков.
Планирование лечения ВВК и БВ, а также микстинфекции, должно базироваться на доказательных данных эффективности схем лечения. Метронидазол и клиндамицин при БВ, пероральные и топические антимикотики при ВВК доказали свою сравнимую эффективность и могут назначаться как средства равного выбора первой линии терапии. Но при повторных эпизодах вагинитов или микстинфекции следует вспомнить об особенностях возбудителей БВ и ВВК, предрасполагающих к формированию хронических форм заболеваний. Учитывая сложности диагностики причины БВ и прогноза течения ВВК, в подобных ситуациях оптимальным режимом терапии может стать назначение клиндамицина, перекрывающего широкий спектр некультивируемых анаэробов, в виде местной терапии и флуконазола как средства профилактики и лечения ВВК. Трехдневный курс клиндамицина с однократным приемом флуконазола, безусловно, может считаться наиболее приемлемым вариантом терапии для пациенток.
Статистика утверждает, что молочницей хоть раз в жизни переболела каждая вторая женщина. Это неудивительно, поскольку возбудитель заболевания – грибок из рода Candida – всегда присутствует на слизистых оболочках вагинальной области. Заболевание (кандидоз) развивается, когда для жизнедеятельности грибка создаются оптимальные условия, и его популяция стремительно увеличивается.

Классификация
Семейство Candida насчитывает около полутора сотен видов грибков. Из них в организме человека способны жить 20 видов. В 90% случаев заболевание вызывают грибки разновидности Candida albicans.
- при первичном заражении – при родах или в течение первого года жизни;
- при вторичном заражении – во время интимной близости (практически 100% вероятность), контактно-бытовым путем (белье, предметы обихода, пища).
- у женщин – в виде вульвовагинита (кольпита);
- у мужчин – в виде баланопостита.
Основные признаки молочницы у женщин:
- зуд, жжение, раздражение, набухание, краснота слизистых оболочек;
- творожистые выделения из половых органов, запах выделений – кисломолочный;
- боль при половом акте;
- жжение при мочеиспускании.
Заниматься сексом до полного излечения молочницы нельзя. Если заболевание диагностировано у вашего полового партнера, а вас симптомы не беспокоят, пролечиться все равно придется.
Основные признаки заражения грибком Кандида у мужчин:
- зуд, чувство жжения;
- покраснение, отечность головки, крайней плоти, белесый налет;
- боль во время полового акта.

Кандида диагностируется у женщин и мужчин
Кандидоз диагностируют по:
- внешним признакам;
- результатам бакпосева мазков из влагалища и уретры;
- ПЦР.
Как вылечить молочницу у женщины?
Candida любит теплые влажные места с минимальным доступом воздуха, поэтому на слизистой влагалища грибку более чем комфортно. Чтобы избавиться от неприятного соседства, нужно использовать препараты:
- местного действия: вагинальные свечи, таблетки, кремы с эконазолом, клотримазолом, миконазолом, эконазолом (Клотримазол, Пимафукорт);
- системного действия: таблетки, капсулы с флуконазолом, итраконазолом (Нистатин, Флуконазол, Дифлузол, Дифлюкан);
- препараты для укрепления иммунитета, пробиотики, симбиотики (Вобэнзим, Лактовит, Дактиале, Дерма-Про, Вагилак, Виферон).

Невылеченное заболевание быстро распространяется
В среднем курс лечения занимает от 3 до 6 дней. Споры грибка созревают в течение 20 дней, поэтому может понадобиться повторный курс лечения. Некоторые препараты (например, Бетадин) можно применять во время менструации.
В 20% случаев назначенное врачом лечение не помогает. Если через неделю молочница продолжает вас беспокоить:
- это – не кандидоз. Придется пересдать анализы, пройти дополнительные обследования.
- заболевание вызвано не Candida albicans, а другой разновидностью грибка, которая уничтожается сложнее;
- это – рецидив, возможный при диабете, во время антибиотикотерапии, сниженном иммунитете.
Если рецидивы кандидоза случаются более 4 раз в год, врач назначит профилактическое лечение. Исследования показали удлинение безрецидивного периода до 1,5 лет у пациенток, которые применяли препарат ГЕПОН®. Он действует на источник инфекции и корректирует симптомы молочницы. У 83% пациенток с кандидозом через два дня после применения проходили краснота, отечность, раздражение и боль.

Хронический и рецидивирующий кандидоз требует смены образа жизни
Препараты местного действия могут причинять неудобства – вытекать, пачкать одежду. Чтобы они равномерно распределялись по поверхности слизистой влагалища и не причиняли дискомфорт, лучше всего использовать их перед сном. Свечи и таблетки нужно располагать приблизительно посредине влагалища. Расположенные слишком близко лекарства вытекут, а слишком далеко – могут травмировать нежную шейку матки.
Как вылечить молочницу у мужчины?
Побороть кандидоз помогут:
- местно – кремы с клотримазолом;
- системно – флуконазол (препараты Флуконазол, Дифлазон, Форкан, Медофлюкон, Микосист).
Длительность среднестатистического курса лечения – 5 дней.
Во время лечения нижнее белье и полотенца следует менять ежедневно. Гигиенические процедуры проводятся средствами без ароматизаторов и добавок. Несмотря на то, что большинство препаратов применяется местно, во время лечения нельзя употреблять алкоголь.

Мужчинам назначают препараты местного и системного действия
Как избежать рецидива кандидоза?
Candida – условно-патогенный микроорганизм, который обычно присутствует в составе микрофлоры интимных зон. Чтобы вновь не спровоцировать его чрезмерное размножение:
- укрепляйте иммунитет;
- не носите тесное синтетическое нижнее белье;
- соблюдайте правила личной гигиены;
- употребляйте достаточное количество витаминов, сократите количество быстрых углеводов;
- сократите количество продуктов и напитков, в которых содержатся плесень и дрожжи;
- используйте средства контрацепции;
- избегайте стрессов.

Во время лечения молочницы придется подкорректировать рацион
Независимо от образа жизни молочница может развиться:
- при изменении гормонального фона (беременность, прием противозачаточных таблеток, эндокринные заболевания);
- после операций;
- в результате антибиотикотерапии;
- в ходе серьезных заболеваний;
- при дисбактериозе влагалища;
- после переохлаждения.
Что будет, если не лечить молочницу?

Невылеченная вовремя молочница чревата серьезными проблемами
- снизит иммунитет, в результате чего разовьются вторичные половые инфекции;
- спровоцирует эрозию слизистой;
- нарушит менструальный цикл;
- станет причиной воспаления шейки матки.
-
приведет к простатиту, везикулиту, способным спровоцировать бесплодие.
Как вылечить молочницу при беременности?
Статистика утверждает, что грибки Candida выявляются у 80% будущих мам. До родов с ними нужно обязательно распрощаться. Если это мероприятие отложить на потом, во время родов произойдет инфицирование малыша. Передача грибка возможна и после – во время кормления или гигиенических процедур. Это чревато молочницей во рту, у девочек – на половых органах, и чередой последующих проблем со здоровьем малыша.
Для лечения будущих мам гинекологи предпочитают использовать препараты местного действия – свечи, таблетки, кремы. Суппозитории Пимафуцин и Примафунгин можно использовать в любом триместре беременности, таблетки Тержинан – во втором. Препараты системного действия назначаются в случае, если местно вылечить заболевание не удалось. Назначает препараты и расписывает схему лечения только врач в зависимости от клинической картины, самодеятельность здесь недопустима.

Самолечение кандидоза недопустимо
Как вылечить молочницу во рту?
Поскольку грибки рода Кандида живут на всех слизистых оболочках, они могут провоцировать заболевания в полости рта. Характерные признаки:
Невылеченный вовремя кандидоз переходит с языка на щеки, затем – на губы и глотку. При попытке соскоблить налет появляется кровь.
Кандидоз слизистых оболочек ротовой полости диагностируется визуально (на запущенных стадиях), по результатам бакпосева и ларингоскопии. При лечении детей препараты подбираются с учетом возрастной категории.
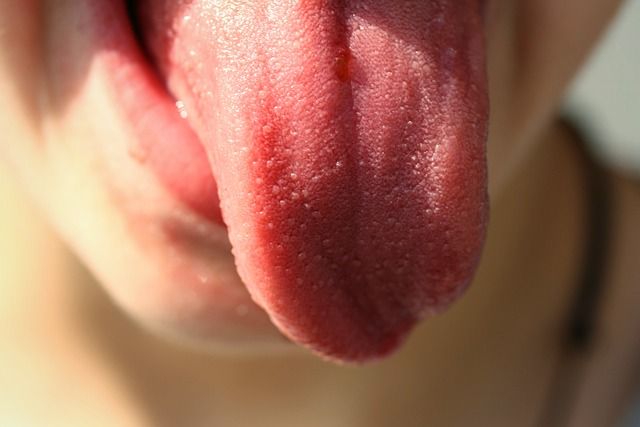
Грибки Кандида способны жить даже во рту
Молочница во рту особенно опасна для грудничков. Дискомфорт в ротовой полости заставляет их отказываться от сосания, из-за чего быстро развиваются обезвоживание и истощение. Грибковая инфекция способна распространяться на другие жизненно важные органы – кишечник, легкие и т. д. У девочек развивается влагалищный кандидоз, который провоцирует воспаления и развитие синехий.

Запущенная молочница угрожает жизни младенца
Чтобы побороть заболевание на начальной стадии, достаточно обрабатывать ротовую полость и пораженные участки антисептическим раствором (например, Мирамистином, Гексоралом, Максиколдом) и противогрибковым препаратом (например, Кандидом, Нистатином). Можно полоскать рот содовым раствором. На более тяжелых стадиях применяются препараты системного действия – Флуконазол, Микосист, Фуцис, Дифлюкан. Губы и кожу можно обрабатывать антигистаминными препаратами (Фенистил). Избегайте их попадания на слизистые (глаза, нос, ротовая полость).
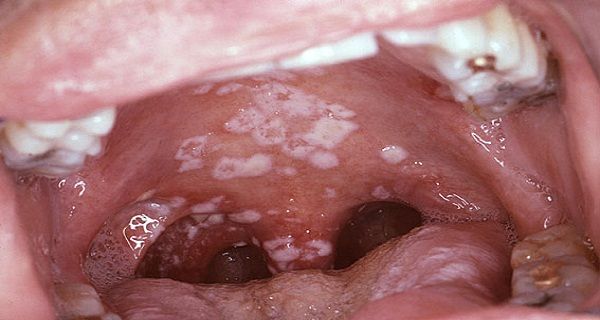
Невылеченный грибок колонизирует небо, пищевод, легкие, другие органы
На период лечения сократите потребление сладостей, избегайте копченостей, острых, соленых блюд, продуктов с содержанием дрожжей, плесени.
Ни в коем случае не смазывайте пораженные участки слизистых и кожи вареньем из розы. Это способствует разрастанию колоний грибка.
Лечение всех видов молочницы нужно проводить под контролем врача. Укрепляйте иммунитет, следуйте рекомендациям диетологов, используйте контрацептивы, и неприятное соседство с большой долей вероятности вам не грозит. Будьте здоровы!
Источники
- Богомолова, Н.С. Кандидозы в хирургической клинике: видовой состав возбудителей, чувствительность к антибиотикам, превентивная терапия / Н.С. Богомолова [и др.] // Анестезиология и реаниматология. - 2011. - №5. - С. 43-48;
- Вознесенский, А.Г. Клиническая фармакология противогрибковых препаратов / А.Г. Вознесенский // Гедеон Рихтер в СНГ. - 2001. - № 2(6). - С. 50-53;
- Волосач, О.С. Метод комбинированной иммунотерапии пациентов с хроническими воспалительными заболеваниями, осложненными кандидозом : инструкция по применению № 084-0909 : утв. 17.09.2009 г. / Министерство здравоохранения Республики Беларусь ; сост. О.С. Волосач, В.М. Цыркунов, С.Б. Позняк, С.М. Дешко.
Как лечить молочницу (отвечает гинеколог Л.Шупенюк)
Как вылечить молочницу у женщин и мужчин. Простые советы. Эффективные средства
Флуконазол 1 таблетка содержит: активное вещество: флуконазол — 150 мг; вспомогательные вещества: целлюлоза микрокристаллическая, кальция гидрофосфат, кроскармеллоза натрия, магния стеарат, кремния диоксид коллоидный, краситель пунцовый [Понсо 4R] [Е 124]. Азитромицин 1 таблетка, покрытая пленочной оболочкой, содержит: активное вещество: азитромицина дигидрат — 1048 мг (в пересчете на азитромицин — 1000 мг); вспомогательные вещества: натрия лаурилсульфат, кроскармеллоза натрия, повидон-К30, магния стеарат, кремния диоксид коллоидный; состав оболочки: гипромеллоза (гидроксипропилметилцеллюлоза), диэтилфталат, тальк, титана диоксид, макрогол-4000, краситель пунцовый [Понсо 4R] [Е 124]. Секнидазол 1 таблетка, покрытая пленочной оболочкой, содержит: активное вещество: секнидазол — 1000 мг; вспомогательные вещества: крахмал кукурузный, целлюлоза микрокристаллическая, кремния диоксид коллоидный, карбоксиметилкрахмал натрия, повидон (PVPK — 30), тальк, магния стеарат; состав оболочки: гипромеллоза (гидроксипропилметилцеллюлоза), диэтилфталат, тальк, титана диоксид, макрогол-4000.
Фармакодинамика
Флуконазол Триазольное противогрибковое средство, является мощным селективным ингибитором синтеза стеролов в клетке грибов. Обладает высокоспецифичным действием, ингибируя активность ферментов грибов, зависимых от цитохрома P450. Блокирует превращение ланостерола клеток грибов в мембранный липид — эргостерол; увеличивает проницаемость клеточной мембраны, нарушает ее рост и репликацию. Флуконазол продемонстрировал активность in vitro и в клинических исследованиях в отношении следующих микроорганизмов: Candida albicans, Candida glabrata (многие штаммы умеренно чувствительны), Candida parapsilosis, Candida tropicalis, Cryptococcus neoformans. Активен при оппортунистических микозах, в т.ч. вызванных Candida spp. (включая генерализованные формы кандидоза на фоне иммунодепрессии), Cryptococcus neoformans и Coccidioides immitis (включая внутричерепные инфекции), Microsporum spp. и Trichophyton spp; при эндемических микозах, вызванных Blastomyces dermatidis, Histoplasma capsulatum (в т.ч. при иммунодепрессии). Не обладает антиандрогенной активностью. Азитромицин Антибактериальное средство широкого спектра действия, азалид, действует бактериостатически. Связываясь с 50S субъединицей рибосом, угнетает пептидтранслоказу на стадии трансляции, подавляет синтез белка, замедляет рост и размножение бактерий, в высоких концентрациях оказывает бактерицидный эффект. Обладает активностью в отношении ряда грамположительных, грамотрицательных, анаэробных, внутриклеточных и других микроорганизмов. В большинстве случаев к азитромицину чувствительны: аэробные грамположительные микроорганизмы: Staphylococcus aureus (метициллин-чувствительный), Streptococcus pneumoniae (пенициллин-чувствительный), Streptococcus pyogenes, Streptococcus agalactiae, стрептококки групп C, G; аэробные грамотрицательные микроорганизмы: Haemophilus influenzae, Haemophilus parainfluenzae, Legionella pneumophila, Moraxella catarrhalis, Pasteurella multocida, Neisseria gonorrhoeae; анаэробные микроорганизмы: Clostridium perfringens, Fusobacterium spp., Prevotella spp., Porphyriomonas spp., Peptostreptococcus spp.; другие микроорганизмы: Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci, Mycoplasma pneumoniae, Mycoplasma hominis, Borrelia burgdorferi. Микроорганизмы с приобретаемой резистентностью к азитромицину: Streptococcus pneumoniae (пенициллин-устойчивый). Микроорганизмы, изначально устойчивые: аэробные грамположительные микроорганизмы: Enterococcus faecalis, Staphylococcus spp. (метициллин-устойчивые стафилококки с очень высокой частотой обладают приобретенной устойчивостью к макролидам); грамположительные бактерии, устойчивые к эритромицину; анаэробы: Bacteroides fragilis. Секнидазол Противомикробное и противопротозойное средство; производное нитроимидазола. Оказывает бактерицидное (против грамположительных и грамотрицательных анаэробных бактерий) и амебицидное (внутри- и внекишечное) действие. Секнидазол особенно активен в отношении Trichomonas vaginalis, Giardia lamblia, Entamoeba histolytica. Взаимодействует с ДНК микробной клетки, вызывает нарушение спиральной структуры, разрыв нитей, подавление синтеза нуклеиновых кислот и гибель клетки.
Фармакокинетика
Флуконазол Абсорбция — высокая, биодоступность — 90%. Одновременный прием пищи не влияет на абсорбцию препарата. После приема внутрь натощак 150 мг время достижения максимальной концентрации — 0,5-1,5 ч, максимальная концентрация флуконазола в плазме (Cmax ) составляет 90% от концентрации в плазме при внутривенном введении в дозе 2,5–3,5 мг/л. Связь с белками плазмы — 11-12%. Концентрация в плазме находится в прямой зависимости от дозы. Флуконазол хорошо проникает во все биологические жидкости организма. Концентрация активного вещества в грудном молоке, суставной жидкости, слюне, мокроте и перитонеальной жидкости аналогична таковой в плазме. Постоянные значения в вагинальном секрете достигаются через 8 ч после приема внутрь и удерживаются на этом уровне не менее 24 ч. Хорошо проникает в спинномозговую жидкость (СМЖ), при грибковом менингите концентрация в СМЖ составляет около 85% от таковой в плазме. В потовой жидкости, эпидермисе и роговом слое (селективное накопление) достигаются концентрации, превышающие сывороточные. Объем распределения приближается к общему содержанию воды в организме; период полувыведения (T 1/2 ) флуконазола составляет около 30 ч. Выводится преимущественно почками (80% — в неизмененном виде, 11% — в виде метаболитов). Клиренс флуконазола пропорционален клиренсу креатинина (КК). Фармакокинетика флуконазола существенно зависит от функционального состояния почек, при этом существует обратная зависимость между T1/2 и КК. После гемодиализа в течение 3 ч концентрация флуконазола в плазме снижается на 50%. Длительный период полувыведения из плазмы крови позволяет принимать флуконазол при вагинальном кандидозе однократно. Азитромицин Азитромицин быстро всасывается из желудочно-кишечного тракта (ЖКТ), что обусловлено его устойчивостью в кислой среде и липофильностью. После приема внутрь 500 мг максимальная концентрация азитромицина в плазме крови достигается через 2,5 — 2,96 ч и составляет 0,4 мг/л. Биодоступность составляет 37%. Азитромицин хорошо проникает в дыхательные пути, органы и ткани урогенитального тракта (в частности в предстательную железу), в кожу и мягкие ткани. Высокая концентрация в тканях (в 10-50 раз выше, чем в плазме крови) и длительный период полувыведения обусловлены низким связыванием азитромицина с белками плазмы крови, а также его способностью проникать в эукариотические клетки и концентрироваться в среде с низким рН, окружающей лизосомы. Это, в свою очередь, определяет большой кажущийся объем распределения (31,1 л/кг) и высокий плазменный клиренс. Способность азитромицина накапливаться преимущественно в лизосомах особенно важна для элиминации внутриклеточных возбудителей. Доказано, что фагоциты доставляют азитромицин в места локализации инфекции, где он высвобождается в процессе фагоцитоза. Концентрация азитромицина в очагах инфекции достоверно выше, чем в здоровых тканях (в среднем на 24-34%) и коррелирует со степенью воспалительного отека. Несмотря на высокую концентрацию в фагоцитах, азитромицин не оказывает существенного влияния на их функцию. Азитромицин сохраняется в бактерицидных концентрациях в течение 5-7 дней после приема последней дозы. В печени деметилируется, образующиеся метаболиты не активны. У азитромицина очень длинный период полувыведения — 35-50 ч. Период полувыведения из тканей значительно больше. Азитромицин выводится, в основном, в неизмененном виде — 50% кишечником, 6% почками. Секнидазол После приема внутрь быстро всасывается из ЖКТ; биодоступность — около 80%. После однократного приема внутрь 2 г максимальная концентрация в плазме достигается через 3-4 ч. Метаболизируется в печени. Период полувыведения секнидазола из плазмы крови составляет около 25 ч. Препарат медленно выводится из организма, в основном почками; около 50% принятой дозы экскретируется за 120 ч. Проходит через гематоэнцефалический и плацентарный барьеры, экскретируется в грудное молоко.
Сафоцид: Противопоказания
Сафоцид: Побочные действия
Передозировка
Случаи передозировки набора таблеток Сафоцид не описаны. В случае передозировки следует немедленно обратиться к врачу. Флуконазол. Симптомы: галлюцинации, параноидальное поведение. Лечение: симптоматическое; промывание желудка (при необходимости), форсированный диурез. Гемодиализ в течение 3 часов снижает концентрацию флуконазола в плазме крови приблизительно на 50%. Азитромицин. Симптомы: тошнота, временная потеря слуха, рвота, диарея. Лечение: симптоматическое; прием активированного угля, контроль жизненно важных функций. Секнидазол. Симптомы: усиление дозозависимых побочных эффектов. Лечение: симптоматическое; промывание желудка, прием активированного угля.
Особые указания
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
Современные комбинированные препараты при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин
Журнал: Клиническая дерматология и венерология. 2013;11(3): 63‑68
Леонтьев И.Г., Леонтьев Д.И. Современные комбинированные препараты при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин. Клиническая дерматология и венерология. 2013;11(3):63‑68.
Leont'ev IG, Leont'ev DI. Current combination drugs in the treatment of urogenital trichomoniasis and associated urethrogenic infections in males. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):63‑68. (In Russ.).
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
Несмотря на некоторое снижение заболеваемости урогенитальным трихомониазом, воспалительные заболевания мочеполовой системы и репродуктивных органов, обусловленные Trichomonas vaginalis, остаются актуальной медико-социальной проблемой [1—3]. Кроме того, в последние годы по-прежнему регистрируются неудачи при лечении трихомониаза, наблюдается трихомонадоносительство, резистентность возбудителя к противотрихомонадным препаратам [2—9]. Трихомонадная инфекция является причиной возникновения воспалительных заболеваний органов мочеполовой системы у 23—40% мужчин [10]. Одна из особенностей трихомонад — их исключительная способность к ассоциации с другими возбудителями инфекций, передаваемыми половым путем (ИППП), поэтому трихомониаз у человека довольно часто протекает в составе микстинфекции (вместе с гонореей, хламидийной инфекцией, M. genitalium, Ureaplasma spp., кандидозом) [4, 11—13], что затрудняет его лечение и способствует возникновению посттрихомонадных осложнений. Нередко трихомонады выполняют роль резервуаров, сохраняя этих возбудителей в неизмененном виде (эндоцитобиоз), а некоторые из них внутри трихомонады даже активно размножаются. С этой точки зрения комбинированное применение антипротозойных препаратов и антибиотиков обосновано, особенно в острый и подострый период болезни. Инфекция распространяется из уретры в предстательную железу (ПЖ) через выводные протоки ПЖ, семявыбрасывающие протоки на семенном бугорке в собственные протоки семенных пузырьков [14]. Острый уретрит — один из самых распространенных синдромов среди ИППП, диагностируемых у мужчин [15]. Наиболее частым осложнением урогенитального трихомониаза и ассоциированных уретрогенных инфекций является воспаление ПЖ [14]. Использование комбинированного антибактериального препарата Сафоцид при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций явилось предметом наших исследований.
В состав набора таблеток Сафоцид входят три препарата для лечения и профилактики разных видов инфекций: секнидазол 1 г (2 таблетки), азитромицин 1 г (1 таблетка), флуконазол 150 мг (1 таблетка).
Секнидазол относится к синтетическим производным нитроимидазола. Его фармакологическое действие — противомикробное и противопротозойное. Проникая в клетку и трансформируясь в ней с образованием свободных радикалов, препарат взаимодействует с ДНК, вызывая ее дегенерацию, подавляет синтез нуклеиновых кислот. После приема внутрь всасывается около 80% препарата. Максимальная концентрация в сыворотке крови достигается через 4 ч. Секнидазол метаболизируется в печени, его период полувыведения составляет 19 ч, выводится почками (в течение 72 ч — 16% от принятой дозы). Преимущества препарата перед другими производными нитроимидазола — однократность приема, высокая эффективность, короткий курс приема, сокращенный период наблюдения.
Азитромицина дигидрат является представителем подгруппы макролидных антибиотиков — азалидов, при создании в очаге воспаления высоких концентраций оказывает бактерицидное действие. Азитромицин хорошо проникает в органы и ткани урогенитального тракта (в частности в ПЖ). При пероральном приеме данный антибиотик очень быстро всасывается из желудочно-кишечного тракта в кровь, не вызывает обычных для антибиотиков побочных явлений со стороны желудочно-кишечного тракта, транспортируется в очаг воспаления полиморфноядерными нейтрофилами. В плазме крови длительно поддерживается его высокая концентрация, а максимальная концентрация достигается через 2—3 ч после приема. Азитромицин сохраняется в бактерицидных концентрациях в очаге воспаления в течение 5—7 сут после прекращения приема. Способность препарата преимущественно накапливаться в лизосомах играет важную роль в элиминации внутриклеточных микроорганизмов. Концентрация азитромицина в очагах инфекции достоверно выше, чем в здоровых тканях (в среднем на 24—34%) и коррелирует со степенью воспалительного отека. Азитромицин имеет весьма длительный период полувыведения — 34—68 ч, поэтому эффект продолжается и после окончания антибиотикотерапии. Азитромицин является антибиотиком широкого спектра действия и соответствует международному стандарту лечения негонококковых уретритов [16].
Флуконазол — представитель класса триазольных противогрибковых средств, 80% которого выводится с мочой в неизмененном виде. При этом в моче создается концентрация препарата, достаточная для лечения инфекции, вызванной Candida spp. Высокая биодоступность (более 90%) при приеме внутрь и длительный период полувыведения (около 30 ч) делают этот противогрибковый препарат удобным для применения. Для лечения кандидоза флуконазол назначают в дозе 3 мг/кг в сутки (для взрослых 150 мг/сут). Обычно используется пероральная форма флуконазола.
Цель настоящей работы — изучение эффективности, безопасности и переносимости Сафоцида, применяемого однократно, а также его влияния на клиническое течение и лабораторные показатели при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин.
Дизайн исследования
В исследование были включены мужчины, ранее не принимавшие противопротозойные и противогрибковые препараты, и не принимавшие антибиотики из группы макролидов в течение предшествующих 30 сут. В клиническое обследование не вошли больные с сифилисом и гонореей. Клинические проявления заболевания и лабораторные показатели регистрировали до лечения, а также через 1—2, 7—10 и 30 сут после лечения.
Материал и методы

Спектр возбудителей был следующим: T. vaginalis+C. trachomatis — 10 (29%) человек, T. vaginalis+C. trachomatis+M. genitalium — 12 (35%), T. vaginalis+U. urealyticum+M. genitalium — 7 (21%) больных, T. vaginalis+M. genitalium +C. albicans — 5 (15%) мужчин (рис. 2). Рисунок 2. Распределение больных по спектру возбудителей. Следует отметить высокую частоту выделения T. vaginalis в ассоциации с C. trachomatis и M. genitalium по сравнению с ассоциацией с другими микробами. Эту особенность можно рассматривать как возможный признак симбиоза указанных микроорганизмов. Полученные результаты указывают на эффективность и необходимость проведения комплексных лабораторных исследований при скрининге ИППП.
Жалобы больных были разнообразными (рис. 3, рис. 4). Рисунок 3. Структура жалоб в исследуемых группах. Рисунок 4. Клинико-лабораторные признаки.
Гиперемию кожи крайней плоти и головки полового члена отметили 5 (15%) пациентов, болезненность при пальпации уретры — 14 (41%), выделения из уретры — 22 (65%), эритему и отек наружного отверстия уретры — 22 (65%), зуд и жжение в уретре — 30 (88%), дизурию — 26 (77%). Болезненность при пальпации ПЖ испытывали 12 (35%) человек, отечность и болезненность ПЖ наблюдались у 12 (35%), увеличение содержания лейкоцитов в отделяемом уретры выявлено у 34 (100%), увеличение содержания лейкоцитов в первой порции мочи — у 8 (24%), увеличение содержания лейкоцитов в секрете ПЖ — у 12 (35%).
Лечение проводили по схеме, рекомендованной фирмой-производителем: однократный прием внутрь одновременно 4 таблеток, входящих в состав блистера Сафоцида, за 1 ч до или через 2 ч после еды.
Мужчины с установленным диагнозом урогенитального трихомониаза и ассоциированных уретрогенных инфекций, их половые партнеры были информированы о характере и особенностях течения заболевания. Всем половым партнерам также было рекомендовано обследование и лечение. Были даны следующие рекомендации: во время лечения исключить половые контакты, использовать барьерные методы контрацепции при половых контактах вплоть до констатации выздоровления. К полному излечению относили клиническое и этиологическое выздоровление.
Контроль излеченности по трихомониазу осуществляли через 7—10 сут после окончания терапии Сафоцидом, по хламидийной инфекции и инфекции, вызванной M. genitalium и Ureaplasma spp., — через 30 сут после окончания антибиотикотерапии.
Результаты
Через 1—2, 7—10 и 30 сут после лечения у всех пациентов проведена оценка эффективности и безопасности Сафоцида. Кроме результатов клинико-лабораторных исследований, учитывали любые неблагоприятные явления с момента последнего визита.

При оценке динамики стихания клинических симптомов отмечено, что на фоне лечения достаточно быстро купируются основные проявления инфекции (табл. 1). Так, при лечении больных с использованием Сафоцида гиперемия кожи крайней плоти исчезла у 4 (80%) из 5 пациентов, болезненность при пальпации уретры — у 13 (92,8%) из 14 пациентов, уретральные выделения исчезли у 20 (91%) из 22 пациентов, эритема и отек наружного отверстия уретры регрессировали у 21 (95,4%) из 22, зуд, жжение в уретре удалось купировать у 28 (93,3%) из 30, дизурия уменьшилась у 24 (92,4%) из 26, болезненность при пальпации ПЖ — у 10 (83,4%) из 12. По окончании лечения при ректальном исследовании отечность ПЖ регрессировала у 11 (91,6%) из 12 пациентов.
Содержание лейкоцитов в отделяемом уретры по окончании лечения нормализовалось у 33 (97,06%) из 34 пациентов. В первой порции мочи количество лейкоцитов уменьшилось у 7 (87,5%) из 8 пациентов. Нормализация количества лейкоцитов в секрете ПЖ отмечена у 10 (83,4%) из 12 пациентов.
У 2 пациентов с уретропростатитом наблюдались необильные слизисто-гнойные выделения из уретры, сохранились зуд, дизурия и болезненность при пальпации ПЖ. Кроме того, у них сохранился лейкоцитоз в секрете ПЖ, в мазках были обнаружены трихомонады, что рассматривалось нами как отсутствие этиологического и клинического выздоровления.

Спектр возбудителей имел следующий вид: Trichomonas vaginalis до лечения был обнаружен у 34 (100%) человек, а после курса терапии — у 2 (5,8%), С. trachomatis — у 22 (64,7%) и 1 (2,9) соответственно, M. genitalium — у 24 (70,5%) и 2 (5,8%), U.urealyticum — у 7 (20,5%) и 1 (2,9%), C. albicans — у 5 (15%) и 1 (2,9%) пациента соответственно (рис. 5). Рисунок 5. Динамика бактериологических показателей (абсолютные числа).
Из приведенных данных следует, что эффективность лечения с использованием Сафоцида составляет при Trichomonas vaginalis — 94,2%, при С. trachomatis — 97,1%, при M. genitalium — 94,2%, при U. urealyticum — 97,1%, при C. аlbicans — 97,1%.
Показатели биохимической гепатограммы и общего анализа крови, как до начала терапии, так и по ее завершении, оставались в пределах нормы (табл. 2 и 3).
Таким образом, как ближайшие, так и отдаленные результаты лечения урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин свидетельствуют о высокой эффективности и безопасности Сафоцида в стандартных терапевтических дозах (секнидазол — 2000 мг, азитромицин — 1000 мг, флуконазол — 150 мг). Почти все больные лечение перенесли без побочных эффектов. Лишь в 2 (5,8%) случаях была отмечена 2-часовая головная боль, которая купировалась самостоятельно (без применения специальной терапии).
Заключение
На основании проведенных клинических исследований можно сделать следующие выводы.
Сафоцид — эффективный препарат для лечения урогенитального трихомониаза и ассоциированных уретрогенных инфекций.
Клиническая эффективность Сафоцида составляет 80—95,4% (в зависимости от симптомов), а бактериологическая — 94,2—97,1% (в зависимости от возбудителя).
Препарат отличается хорошей переносимостью и небольшим количеством побочных эффектов (наблюдались у 2 пациентов из 34), имеет доступную цену, а также малую токсичность, что соответствует требованиям ВОЗ, которым должны отвечать препараты для лечения ИППП. Возможны пероральный прием и однократное применение.
Препарат Сафоцид содержит все необходимые современные эффективные компоненты в одной упаковке, что позволяет использовать его при лечении смешанных инфекций. Кроме того, Сафоцид удобен в применении, что позволяет использовать его в амбулаторной практике.
Читайте также:

