Сахарный диабет инфекционное заболевание или нет
Обновлено: 26.04.2024
Статья почвящена инфекционным факторам развития сахарного диабета у детей. Подчеркивается необходимость настороженности врачей в отношении энтеровирусной инфекции, полиморфизма ее проявлений, тяжелых поражений многих органов и систем с формированием сомат
The article is dedicated to infectious factors of diabetes mellitus in children. The need for doctors caution in respect of enteroviral infection, polymorphism of its representations, severe lesions of multiple organs and systems with formation of somatic problems were highlighted.
Сахарный диабет (СД) является одним из наиболее важных и сложных для современной медицины заболеваний, что обусловлено его широким распространением, клиническим полиморфизмом и тяжестью осложнений [1–6]. Летальность при СД выше в 2–3 раза по сравнению с больными без него. Всемирная организация здравоохранения (ВОЗ) характеризует инсулинзависимый СД (ИЗСД, или СД 1-го типа) как эпидемию неинфекционного генеза из-за значительного роста среди детей и подростков [2–5]. Прогнозируется, что заболеваемость ИСЗД за период с 2005 по 2020 гг. у детей младше 5 лет увеличится в 2 раза, а общая распространенность его у детей до 15 лет возрастет на 70%, поэтому госпитализация также увеличится [7].
В настоящее время смертность от острых осложнений СД (диабетической комы) не превышает 1%, но вместе с повышением продолжительности жизни больных возникла новая проблема — сосудистые осложнения СД [8]. Развитие СД сопровождается 3–4-кратным увеличением риска смерти от сердечно-сосудистых заболеваний (ССЗ) и уменьшением ожидаемой продолжительности жизни по сравнению с лицами, не имеющими СД. Возникающие кардиоваскулярные нарушения в детском возрасте при ИЗСД становятся основной причиной смертности у взрослых пациентов. Миокардиодистрофия в большинстве случаев приводит к развитию сердечной недостаточности, артериальной гипертензии (АГ), прогрессированию макро- и микрососудистых осложнений СД 1-го типа.
На сегодняшний день существуют только единичные работы, посвященные данной проблеме у детей. Основная же масса представленных работ касается взрослого контингента, хотя известно, что формирование осложнений начинается в детском возрасте, когда данные изменения еще обратимы и есть возможность предотвратить их прогрессирование. Кроме того, имеет место неоднозначная трактовка результатов исследования ввиду их малочисленности и отсутствия единой комплексной оценки всех звеньев патогенеза сосудистых осложнений.
Основным патогенетическим механизмом, участвующим в развитии кардиоваскулярных нарушений при СД 1-го типа, является диффузный генерализованный патологический процесс, который поражает всю систему микроциркуляции — микроангиопатия с нарушением метаболизма сердечной мышцы, изменение нервной регуляции сердца, развитие изменений в рамках кардиоренального синдрома и эндотелиальной дисфункции. У детей и подростков, больных СД 1-го типа, на ранних его стадиях происходит также развитие диабетической микроангиопатии зрительного анализатора, обусловленного хронической гипергликемией, хронической гипоксией, активизирующей процессы ангиогенеза [9]. Признанным механизмом повреждения миокарда при СД является уменьшение коронарного резерва вследствие гипергликемии (микроангиопатии), гипертриглицеридемии, эндотелиальной дисфункции.
Поражение сердца при СД развивается вследствие воздействия ряда неблагоприятных факторов, приводящих к повреждению миокарда, его реактивной гипертрофии, фиброзу на фоне функциональных и структурных изменений мелких сосудов, метаболических нарушений и кардиальной автономной нейропатии [10]. СД является мощным и независимым фактором риска развития мерцательной аритмии и трепетания предсердий. Следует отметить, что нередко асимптоматические пароксизмы и пароксизмы, сопровождающиеся клинической симптоматикой, находятся в соотношении 12:1, и задачей клиницистов является раннее предупреждение этих состояний [11]. СД и мерцательная аритмия тесно связаны между собой по ряду факторов, ускоренному развитию атеросклероза с формированием фибросклероза с ишемизирующим воздействием на миокард, ремоделированием иннервации предсердий и другие.
Клинический полиморфизм при энтеровирусной инфекции проявляется не только разнообразием клинических форм, но и тем, что у одного и того же больного данная инфекция может проявляться в различных вариантах.
Было проведено изучение морфологических маркеров вирусов при биопсии у 57 больных с аритмогенной кардиопатией правого желудочка (АКПЖ) (средний возраст пациентов 48 ± 12 лет). Результаты исследования (биопсийного и аутопсийного) свидетельствовали в пользу врожденного генеза кардиомиопатии. В преобладающем количестве случаев у пациентов были выявлены энтеровирусы. Экспрессия антигена энтеровирусов была обнаружена в цитоплазме кардиомиоцитов, гладкомышечных клетках, эндотелиоцитах сосудов [12].
Отечественная история изучения значения различных вирусов как причин манифестации ИЗСД относится к 1980-м гг. и связана с именами таких ученых, как Л. С. Лозовская, В. В. Смирнов, Н. А. Мазурина и др. [14, 15].
К энтеровирусной инфекции в последние годы приковано внимание специалистов всего мира. Преимущественно зарубежными учеными в последние годы были собраны метаанализы, разрабатываются программы, методы диагностики и профилактики энтеровирусной инфекции. Столь пристальное внимание обусловлено серьезностью и тяжестью последствий энтеровирусной инфекции во многих областях медицины и, в частности, в эндокринологии. ВОЗ характеризует ИЗСД как эпидемию. К сожалению, среди отечественных специалистов-эндокринологов пока нет такой настороженности и понимания значения этой инфекции как причины развития ИЗСД, хотя за рубежом уже создается вакцина от энтеровирусной инфекции для предупреждения развития СД [16, 17].
Учитывая важность настоящей проблемы, первоначально мы преследовали основную цель — выявить изменения со стороны сердечно-сосудистой системы у детей, умерших от ИЗСД за 20-летний период времени (1991–2011). Однако, принимая во внимание данные литературы последних лет, в ходе исследования был проведен анализ патологоанатомических данных и поиск этиотропных вирусов, которые обладают полиорганным поражением (сердца, бета-клеток поджелудочной железы и др. органов).
За данный период времени, по материалам вскрытий Морозовской ДГКБ, умерло 16 детей (8 мальчиков и 8 девочек) с диагнозом СД 1-го типа (рис. 1).
Как видно из рис. 1, большинство летальных исходов у детей с СД 1-го типа приходилось на 1991–2003 гг. В последующие годы, очевидно, в связи с отработкой методов лечения и контроля как во всем мире, так и у нас в стационаре, количество летальных исходов значительно уменьшилось.
ИЗСД впервые выявленный был у 11 детей, СД 1-го типа со стажем от 1,5 до 12,5 лет — у 5 детей (31,3%). Возраст детей был следующим: 1–3 года — 2 чел.; 3–6 лет — 3; 6–9 лет — 4; 9–12 лет — 1; 12–15 лет — 6. Таким образом, 56,3% детей были в возрасте от 1 до 9 лет и 43,7% — старше 9 лет. Основным диагнозом при поступлении у всех больных был СД 1-го типа, кетоацидотическая кома. Причина летального исхода — отек головного мозга.
Анализируя клиническую симптоматику дебюта заболевания и тех симптомов, с которыми дети поступали в стационар, следует сказать, что у 14 больных (87,5%) заболевание началось с характерных симптомов — жажды и похудания, однако у 11 детей (68,8%) имели место симптомы инфекционного заболевания, такие как острое респираторное заболевание (4 чел.), боль в горле (1 чел.), пневмония (1 чел.), энцефалит (1 чел.), аппендицит (?) (у детей с болями в животе) (табл. 1). У одного ребенка диагноз был установлен случайно во время диспансеризации, другой поступил в стационар в кардиологическое отделение с пароксизмальной тахикардией. Сложность диагностики во многом была связана с краткостью пребывания в стационаре. Так, 9 детей (56,3%) погибли в первые сутки пребывания в отделении реанимации и интенсивной терапии (ОРИТ), находясь в коме.
По данным патологоанатомического исследования оказалось, что у большего количества детей (14 из 16) имели место различные фетодисплазии, которые ни у одного ребенка, несмотря на возраст (многие из них старшего возраста) не были выявлены. Среди фетодисплазий выделены 2 группы: у 5 детей — нарушение лобуляции легких, у 8 — пороки развития (головного мозга — 3, сердца — 1, почек — 2, добавочная селезенка — 1, гепатобластома — 1).
Основными осложнениями были следующие:
- двухсторонняя пневмония — 10 (62,5%);
- панкреатит — 10 (62,5%);
- менингит, энцефалит — 6 (37,5%);
- миокардит — 6 (37,5%);
- вторичный иммунодефицит — 3 (18,8%).
Возбудители, выделенные по результатам патологоанатомических исследований, представлены в табл. 3.
У 12 детей были выделены следующие вирусы — энтеровирусы (у 8 пациентов), вирусы респираторной группы (аденовирусы, респираторно-синцитиальный вирус, парагрипп, грипп) — у 5 больных. У двух больных были обнаружены герпесвирусы.
Таким образом, преобладающими возбудителями были энтеровирусы, обнаруженные у 8 детей (50% случаев). Однако у 5 детей с неуточненной генерализованной инфекцией (им не было проведено вирусологическое обследование) изменения в органах были однотипны таковым у 8 больных с энтеровирусами, поэтому, возможно, энтеровирусная инфекция имела место у большего количества детей. Энтеровирусная инфекция была представлена следующими серотипами: Коксаки А (3, 4, 5) — у 6 детей; Коксаки В — у 4, энтеровирусы — у 3 детей; смешанное течение — у 4. Для энтеровирусной инфекции были характерны поражения следующих органов: сердца — 7 пациентов (87,5% случаев), головного мозга — 6 (75%), поджелудочной железы — 5 (62,5%), печени — 5 (62,5%), почек — 4 (50%), фетодисплазии — 6 (75%), желудочно-кишечного тракта — 2 (25%).
Изменения со стороны сердечно-сосудистой системы были оценены нами ретроспективно по анализу электрокардиограммы (ЭКГ) (прижизненно), а также после вскрытия (по его результатам и гистологии). По результатам ЭКГ регистрировалась перегрузка правых отделов сердца, аритмия, брадикардия, удлинение систолы желудочков, нарушение внутрижелудочковой проводимости. У одного ребенка имела место пароксизмальная тахикардия. Артериальная гипотензия превалировала и была выявлена у 6 детей, гипертензия — у 2.
У всех 16 детей с ИЗСД проводилась морфологическая и гистологическая оценка состояния сердечно-сосудистой системы по следующим параметрам: масса сердца, наличие гипертрофии камер сердца, фиброэластоз, состояние коронарных сосудов.
На вскрытии у 7 детей имело место увеличение размеров сердца, у 7 — уменьшение, причем эти изменения не зависели от давности течения СД. Дилатационная кардиомиопатия была выявлена у большинства — у 12 детей (75% случаев), фиброэластоз эндокарда — у 11 больных (68,7% случаев), миокардит — у 6 (37,5%). Коронарные сосуды изменены не были практически ни у кого из детей, за исключением одного ребенка, у которого обнаружено утолщение коронарных артерий (сочетание энтеро- и вирусов респираторной группы). Описаны общие следующие изменения миокарда: миокард дряблый, очаги гистиоцитарной инфильтрации, очаговый склероз, фиброз, миксоматоз клапанов, утолщение створок, их сращение, агломерация папиллярных мышц. Отмечается белковая дистрофия кардиомиоцитов, гибель клеток, распад миофибрилл. В сосудах — очаговый фиброз, дистрофия стенок. Выявленные изменения, в первую очередь, имели место у всех детей с энтеровирусной инфекцией.
Следует заметить, что изменения со стороны сердца и поджелудочной железы взаимосвязаны у детей. Наши данные аналогичны таковым, полученным авторами из г. Новосибирска А. В. Деминой и С. В. Нетесовым, которые выделяли формы энтеровирусной инфекции, связанные с серологическими штаммами. Например, перикардит и миокардит встречался при вирусах Коксаки В 1–5 типов, вирусах ЕСНО 1-го, 6-го, 9-го, 19-го типов; а диабет регистрировался при вирусах Коксаки А 9-го, В 1–5 типов [18].
Со слов мамы, ранее не болел, но врачи отмечали вегетососудистую дистонию по гипотоническому типу.
По результатам патологоанатомического исследования был установлен следующий диагноз: генерализованная смешанная инфекция: менингоэнцефалит с лейкомаляцией, мелкоочаговый продуктивный панкардит, продуктивный полиневрит, продуктивный гепатит, интерстициальный нефрит. Вирусологическое обследование: были выделены следующие вирусы: энтеровирусы групп А, В, С, а также вирусы респираторной группы (гриппа, парагриппа, аденовирус).
Выявлены следующие фетодисплазии: трехстворчатого клапана, гипоплазия хрящевых пластин субсегментарных бронхов, двудолевое правое легкое, добавочная селезенка, атрофия тимуса, внутренняя гидроцефалия.
Патологоанатомический эпикриз: смерть ребенка 3 лет с множественными дисплазиями, генерализованной смешанной инфекцией, СД 1-го типа впервые выявленным с развитием кетоацидоза и гиперосмолярной комой наступила от лейкомаляции вещества головного мозга.
Патологоанатомические исследования сердца: на разрезе — истончение миокарда правого желудочка до 0,2 см (норма — 0,27 см), расширение полостей желудочков, утолщение миокарда левого желудочка. Папиллярные мышцы в правом желудочке практически отсутствуют, хордальные нити прикрепляются к стенке желудочка, остальные укорочены, хаотически расположены, третьи — несколько удлинены. На створках клапанов мелкие мукоидные прозрачные узелки. Гистология сердца: утолщение коронарных артерий, мукоидное набухание клапанов, мелкие очаги лимфоидной инфильтрации в эпикарде, миокарде, эндокарде, отек интерстиция. В некоторых нервных стволах эпикарда — гибель клеточных элементов и гистиоцитарная инфильтрация.
На рис. 2 представлены гистологические изменения сердца ребенка.
_575.jpg)
Данный случай демонстрирует взаимосвязь поражений многих органов и систем, в частности, сердца и поджелудочной железы с энтеровирусной инфекцией. Принимая во внимание наличие фетодисплазий, заражение, вероятнее всего, произошло во внутриутробном периоде. Известно, что энтеровирусная инфекция может иметь персистирующее течение, принимать аутоиммунные формы и обостряться под действием вирусов респираторной группы, как, возможно, в данном случае.
Подводя итог данной работы, хочется еще раз подчеркнуть особую важность и необходимость настороженности врачей многих специальностей в отношении энтеровирусной инфекции, полиморфизма ее проявлений, тяжелых поражений многих органов и систем с формированием соматических проблем (миокардит, панкреатит, интерстициальный нефрит, ИЗСД, менингит и т. д.). На сегодняшний день необходимо развивать диагностику энтеровирусной инфекции, так как даже при большом желании мы не имеем возможности полноценного обследования на эту инфекцию не только в Москве, но и в России в целом. Увеличение количества случаев энтеровирусной инфекции в виде вспышек, эпидемий, рост заболеваемости менингитами, СД 1-го типа во всем мире — тому подтверждение.
Литература
Т. А. Полилова*
М. С. Савенкова*, доктор медицинских наук, профессор
В. В. Смирнов* , 1 , доктор медицинских наук, профессор
Е. Е. Петряйкина**, доктор медицинских наук, профессор
И. Е. Колтунов**, доктор медицинских наук, профессор
Л. Н. Каск**
Н. В. Бузина**
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
Сахарный диабет – это группа эндокринных заболеваний, связанных с нарушением углеводного обмена. При этом организм испытывает относительный или абсолютный недостаток гормона поджелудочной железы – инсулина, что провоцирует превышение нормального уровня глюкозы в крови. Длительное отсутствие лечения приводит к гипергликемии, когда клетки органов начинают испытывать голод даже при обильном и своевременном питании. Диагностикой и лечением патологии занимается врач-эндокринолог.
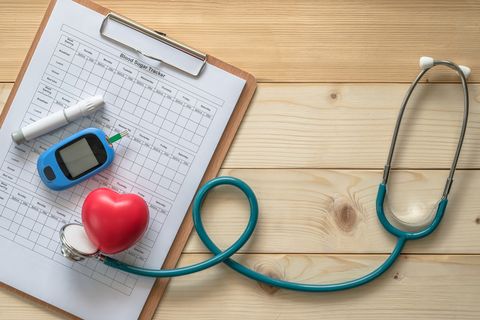
Общие сведения
Статистика! Официально в мире насчитывается более 250 млн. больных диабетом, из них в России живут более 8 млн. человек (6% населения). Однако с учетом того, что ранние стадии диабета 2 типа почти лишены симптомов, реальное количество больных может достигать отметки в 400 млн человек. Наиболее подвержены патологии представители монголоидной и негроидной рас, в то время как частота встречаемости среди европеоидов значительно ниже. Это может быть связано как с биохимией, так и с особенностями питания различных расовых групп.
Причины и механизм развития
В медицине нет единого мнения от чего появляется сахарный диабет, поэтому его относят к мультифакторным заболеваниям, где большое значение имеет плохая наследственность и факторы риска.
Внимание! Высокий риск врожденного диабета характерен для детей, родившихся с большой массой тела – 4 кг и более. В этом случае ребенок с рождения находится на учете у эндокринолога с регулярным отслеживанием его состояния в процессе взросления.
Развитие заболевания тесно связано с инсулином и реакцией на него организма. Гормон является основным участником метаболизма углеводов, а именно – отвечает за усвоение глюкозы. Этот простой сахар называют универсальным источником энергии для всего организма. При этом одни органы для его усвоения требуют присутствия инсулина и являются инсулинзависимыми (печень), другие способны делать это напрямую, поэтому носят название инсулиннезависимых (головной мозг).
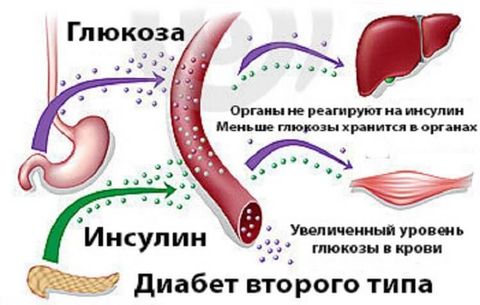
- Выработка инсулина снижается до критического уровня или прекращается полностью.
- Организм вырабатывает инсулин в достаточном количестве, однако клетки и органы приобретают резистентность к данному гормону и попросту не замечают его.
В результате клетки и органы испытывают энергетический голод, а почти весь сахар продолжает циркулировать в крови, не подвергаясь метаболическому преобразованию, что провоцирует явление гипергликемии.
На заметку! Функция инсулина не ограничивается поддержанием уровня глюкозы. Дополнительно гормон участвует в синтезе жирных кислот, что делает его одновременным участником и липидного обмена. Этот факт подтверждает глубокую взаимосвязь обмена веществ в организме и объясняет частое осложнение диабета атеросклерозом сосудов.
Классификация диабета
Сахарный диабет имеет 2 основных типа, которые принципиально различаются по этиологии патологического процесса и на начальных стадиях требуют различного подхода к лечению:
- Инсулинозависимый диабет 1-го типа – развивается в ответ на аутоиммунную агрессию организма против бета-клеток поджелудочной железы, вырабатывающих инсулин. В результате уровень гормона патологически снижается, что грозит высокими показателями гипергликемии. Характерен для детей и молодых людей. У людей старшего возраста проявляется как следствие панкреонекроза при осложненном панкреатите. Требует гормонозаместительной терапии инсулином.
- Инсулиннезависимый диабет 2-го типа развивается в виде повышенной резистентности организма к инсулину с сохранением рабочей функции поджелудочной железы. Характерен для людей старше 40 лет. На ранних стадиях корректируется без гормонального лечения с помощью диеты.
Помимо 2-х основных групп различают так называемые ситуационные и специфические виды диабета:
- гестационный – обратимая патология, характерная для тяжело протекающей беременности;
- панкреатогенный – возникает как вторичное повреждение на фоне первичных травм и заболеваний поджелудочной железы;
- LADA-диабет (латентный аутоиммунный диабет) – отличается вялой симптоматикой, но требует инъекционного лечения инсулином;
- MODY-диабет – генетическая форма диабета.
Сахарный диабет: симптомы заболевания
На ранних стадиях симптомы диабета могут быть слабовыраженными, отсутствовать вовсе или смешиваться с симптоматикой других патологий, что требует проведения дифференциальной диагностики. Однако существует ряд признаков, к которым следует отнестись с особым вниманием. Среди них:
- сухость во рту при нормальном уровне потребления воды;
- частые позывы к мочеиспусканию;
- сухость и зуд кожи на ладонях, локтях, ступнях;
- постоянное чувство голода;
- быстрый набор веса;
- медленное заживление ран;
- повышенная потливость;
- постоянное чувство усталости, низкая работоспособность,
Осложненное течение болезни
Длительное отсутствие лечебных мер добавляет к основным симптомам признаки осложнения:
- резкое падение зрения и нарушения структуры глазного яблока;
- повышение артериального давления;
- нарушения липидного обмена с атеросклерозом сосудов;
- головные боли;
- сильная отечность тканей;
- запах ацетона в моче;
- неврологические боли в области сердца;
- снижение чувствительности рук и ног.
На заметку! В запущенных случаях ацидоза (закисления организма) у пациентов развивается лактоцидотическая кома, которая может привести к тяжелым последствиям, вплоть до смертельного исхода. Срочная госпитализация для восстановления кислотно-щелочного баланса – единственно возможное решение. В условиях стационара проводят гемодиализ, искусственную гипервентиляцию и принудительное ощелачивание организма малыми дозами бикарбоната натрия.
Диагностика

Основное клиническое проявление диабета – гипергликемия, или повышенный сахар крови, поэтому основной способ диагностики диабета – анализ крови на уровень глюкозы. В норме показатель должен быть не выше 6,1 ммоль/л натощак и не более 11 ммоль/л через 2 часа после приема пищи. Следует помнить, что единичный анализ крови на глюкозу не даст объективного результата. Чтобы определить текущее состояние, вынести диагноз и назначить лечение, проводят.
- тест на толерантность к глюкозе;
- биохимический анализ крови;
- исследование крови на электролиты;
- пробу Реберга – для оценки состояния почек;
- обследование глазного дна;
- анализ на уровень эндогенного инсулина;
- исследование сосудов – УЗД, реовазография, капилляроскопия и др.;
- УЗИ органов, ЭКГ.
Как проходит лечение
Основные направления лечебных мероприятий:
- стабилизация и приведение в норму жизненных показателей;
- медикаментозная компенсация углеводного обмена;
- лечение осложнений (при наличии таковых);
- адаптация пациента к особому образу жизни (диета, физическая активность, поддержание водного баланса, инъекции инсулина и/или прием негормональных лекарств и т.п.).
Внимание! Терапия сахарного диабета длится месяцами и требует неукоснительного соблюдения всех назначений. Полное излечение инсулинозависимого диабета считают невозможным, однако при высоком уровне самоконтроля можно значительно улучшить качество жизни.
В качестве альтернативного способа лечения диабета 1-го типа может применяться метод трансплантации. Используют как пересадку всей железы, так и отдельных ее участков – островков Лангерганса, ответственных за выработку инсулина. Основной подход к лечению диабета 2-го типа – диетотерапия. Она же является отличной мерой профилактики нарушений обмена веществ.
Прогноз и профилактика

Основные меры профилактики:
Нарушения иммунитета у пациентов с СД значительно повышают риск развития COVID-19. Согласно последним клиническим рекомендациям, тактика лечения зависит от тяжести инфекционного процесса, а ключевое звено терапии – строгий гликемический контроль
За время пандемии COVID-19 многие крупные исследования подтвердили прямую взаимосвязь между тяжестью течения инфекционного заболевания и наличием в анамнезе сахарного диабета. Мета-анализ 8 исследований с участием почти 50 тысяч пациентов с COVID-19 показал, что сахарный диабет (СД) занимает второе место среди наиболее распространенных сопутствующих заболеваний после артериальной гипертензии [1].
По мнению специалистов, высокий риск развития инфекции у пациентов с СД объясняется нарушениями иммунитета в связи с гипергликемией и ее острыми и хроническими последствиями. Кроме того, повышенный уровень цитокинов увеличивает риск развития тяжелой формы инфекции. [2]Исследования китайских ученых выявили, что сахарный диабет чаще встречается среди пациентов именно с тяжелым течением COVID-19, чем среди пациентов с нетяжелой формой заболевания: 16,2% против 5,7%, и прогноз COVID-19 у пациентов СД был хуже [3].
Согласно данным ряда работ, диабет выступает и как фактор риска смертности у пациентов с COVID-19. Большое национальное выборочное исследование показало, что смертность пациентов с диабетом была значительно выше, чем у пациентов без него: 10% против 2,5% [3]. Показатель летальности больных без коморбидных состояний в Китае составлял 0,9%, в то время как у пациентов с СД он достиг 7,3%. [4] Исследование клинических характеристик случаев смерти с COVID-19 выявило, что одной из причин смертности пациентов является диабетический кетоацидоз [5].
Потенциальные механизмы развития тяжелых форм СOVID-19 при СД
У пациентов с сахарным диабетом в сыворотке крови выявляется высокий уровень IL-6, TNF-a и других воспалительных цитокинов [6], и эксперименты на животных моделях заставили предположить, что СД приводит к усиленной выработке TLR4-индуцированного IL-6 [7]. Коронавирус, включая SARS, вероятно активирует TLR3 и TLR4, что приводит к неконтролируемому иммунному ответу и IL-6-доминантному цитокиновому шторму. Именно он, по всей видимости, и является одной из ведущих причин смерти от коронавирусной пневмонии. [8]
Чрезмерная активация TLR4 сигнального пути у пациентов с СД может способствовать прогрессированию заболевания до тяжелых форм и даже летального исхода.
Взаимное влияние COVID-19 на сахарный диабет: порочный круг
Если СД ухудшает прогноз и повышает степень тяжести инфекционного процесса, то и вирус SARS-CoV-2 повышает уровень гликемии и ухудшает течение СД.
В исследовании с участием пациентов с SARS было обнаружено, что даже при легкой форме COVID-19 у больных был высокий уровень гликемии натощак. В другом исследовании было показано, что вирусный белок ACE2 демонстрирует сильное иммуноокрашивание в островках поджелудочной железы, но слабое в экзокринных тканях. Предполагается, что вирус SARS-CoV-2 серьезно повреждает островковые клетки поджелудочной железы и способствует развитию диабета или ухудшению его течения. [9]
Колебания уровня глюкозы у больных СД и COVID-19
Неконтролируемые колебания гликемии у пациентов с сахарным диабетом при COVID-19 являются неблагоприятным прогностическим фактором и увеличивают риск развития осложнений обоих этих заболеваний.
Среди причин данного явления можно отметить [9]:
- Нерегулярное питание и снижение физической активности. К нарушению питания могут приводить и желудочно-кишечные симптомы COVID-19.
- Увеличение секреции глюкокортикоидов на фоне стресса и прием глюкокортикоидов в рамках терапии.
- Случайный или вынужденный перерыв в приеме ПССП в стационарах и выбор неоптимальной альтернативной сахароснижающей терапии.
- Прямое влияние вируса на поджелудочную железу. COVID-19 может тоже стимулировать выработку большого количества воспалительных цитокинов и привести к экстремальному стрессу у некоторых тяжелых и критических пациентов.
Принципы терапии СД при COVID-19
Согласно новейшим рекомендациям по диагностике, профилактике и лечению коронавирусной инфекции, ведение пациентов с сахарным диабетом зависит от тяжести инфекционного процесса, и в обязательном порядке требует более ответственного гликемического контроля. [9]
Легкая степень тяжести
Если температура тела больного ниже 38 °C, и при наличии кашля, слабости и боли в горле отсутствуют критерии среднетяжелого и тяжелого течения, лечение проводится в домашних условиях. Необходимости слишком сильно изменять исходный режим нет, и терапию ПССП или плановую инсулинотерапию можно продолжать.
Однако прогрессирование COVID-19 может быть быстрым, особенно на фоне гипергликемии. Поэтому больным диабетом с COVID-19, даже легкой степени, настоятельно рекомендуется увеличить частоту измерения глюкозы.
При повышении гликемии необходимо усилить терапию СД. При гликемии выше 13-15 ммоль/л нужно оценить уровень кетонов в моче и добавить генно-инженерный инсулин или аналог инсулина длительного действия.
Критериями среднетяжелого течения являются:
- Лихорадка выше 38 °C
- ЧДД более 22/мин
- Одышка при физических нагрузках
- Пневмония (подтвержденная с помощью КТ легких)
- SpO2
- СРБ сыворотки крови более 10 мг/л
У пациентов с СД среднетяжелое течение является показанием к госпитализации. Отечественные рекомендации предписывают отменить прием метформина, агонистов рецепторов ГПП-1 (арГПП-1), ингибиторов натрий-глюкозного котранспортера 2 типа (иНГЛТ-2), препаратов сульфонилмочевины. При гликемии выше 15,0 ммоль/л показано назначение инсулина короткого действия или базис-болюсной инсулинотерапии.
Для пациентов, которые находятся в процессе непрерывного почечного диализа, пропорция глюкозы и инсулина во вводимом растворе должна быть изменена в зависимости от результатов мониторинга глюкозы, во избежание серьезной гипогликемии или гипергликемии.
Каждые 3-4 часа требуется проводить контроль гликемии, 1-2 раза в день – контроль кетонов в моче.
При тяжелом течении отмечается
- ЧДД более 30/мин
- SpO2 ±
- PaO2 /FiO2 ≤300 мм рт. ст.
- Прогрессирование изменений в легких по данным рентгенографии и/или КТ
- Появление признаков других патологических состояний
- Снижение уровня сознания, ажитация.
- Нестабильная гемодинамика (систолическое АД менее 90 мм рт. ст. или диурез менее 20 мл/час)
- Лактат артериальной крови > 2 ммоль/л
- qSOFA> 2 баллов
Внутривенное введение короткого инсулина с помощью инфузомата следует рассматривать как терапию первой линии. Все другие сахароснижающие препараты должны быть отменены.
Целевая гликемия определяется тяжестью состояния пациента. Контроль показателей проводится каждые три часа при уровне ниже 13,0 ммоль/л и каждый час при превышении данного порога. Дважды в день необходимо также контролировать содержание кетонов в моче и лактата в крови.
Особенности лечения коронавирусной инфекции
При назначении терапии COVID-19 необходимо учитывать некоторые физиологические аспекты пациентов с сахарным диабетом, их ослабленный иммунный статус и влияние некоторых препаратов на уровень глюкозы.
Ведение пациентов с СД и COVID-19 после выписки из стационара
На время самоизоляции требуется предусмотреть обеспечение пациентов препаратами инсулина и антикоагулянтами. Возобновление сахароснижающей терапии другими препаратами возможно после полного выздоровления.
Из-за высокой уязвимости пациентов с СД требуется максимально ограничить их посещение лечебных учреждений. Для этого стоит рекомендовать больным пользоваться услугами телеконсультаций, пролонгировать период выписки рецептов и средств самоконтроля, обеспечить доставку лекарственных средств на дом.
Роль инсулинов в лечении СД при COVID-19
Согласно всем российским и международным рекомендациям, инсулины являются препаратами выбора у пациентов с коронавирусной инфекцией.
При СД1 оптимальным режимом служит инсулиновая помпа или базис-болюсная инсулинотерапия. При СД2 инсулины рекомендуются при любой степени тяжести: средние или длительного действия при легкой степени тяжести на фоне гипергликемии; короткого действия или базис-болюсная инсулинотерапия при средней степени тяжести; внутривенное введение инсулинов короткого действия при тяжелом состоянии. Стоит отметить, что и при глюкокортикоид-ассоциированном диабете инсулин также является препаратом первого выбора.
Современные препараты инсулинов ультракороткого сверхбыстрого, ультракороткого, короткого, среднего, длительного и сверхдлительного (инсулин деглудек) действия, а также комбинированные инсулины (ИДегАсп) позволяют подобрать оптимальный режим терапии СД на фоне COVID-19 при любых индивидуальных гликемических целях и состоянии любой степени тяжести.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
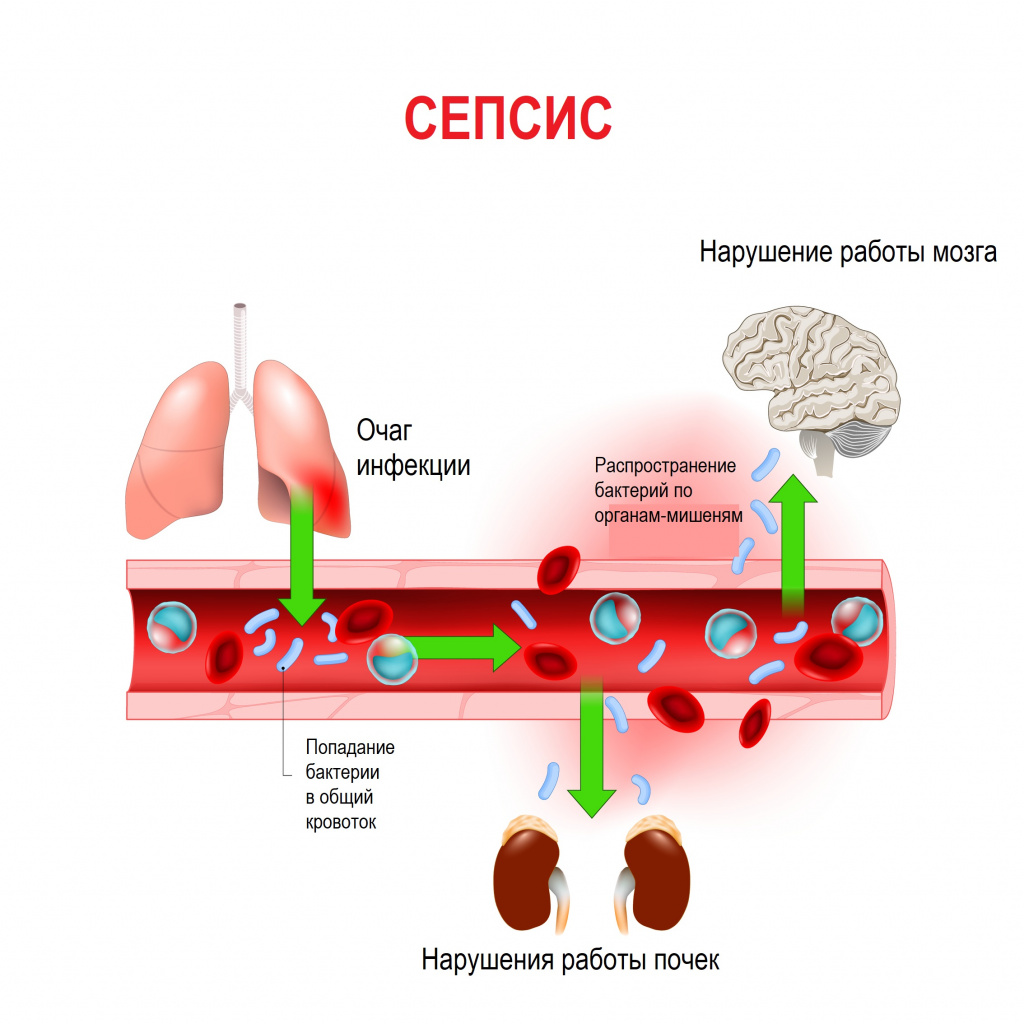
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
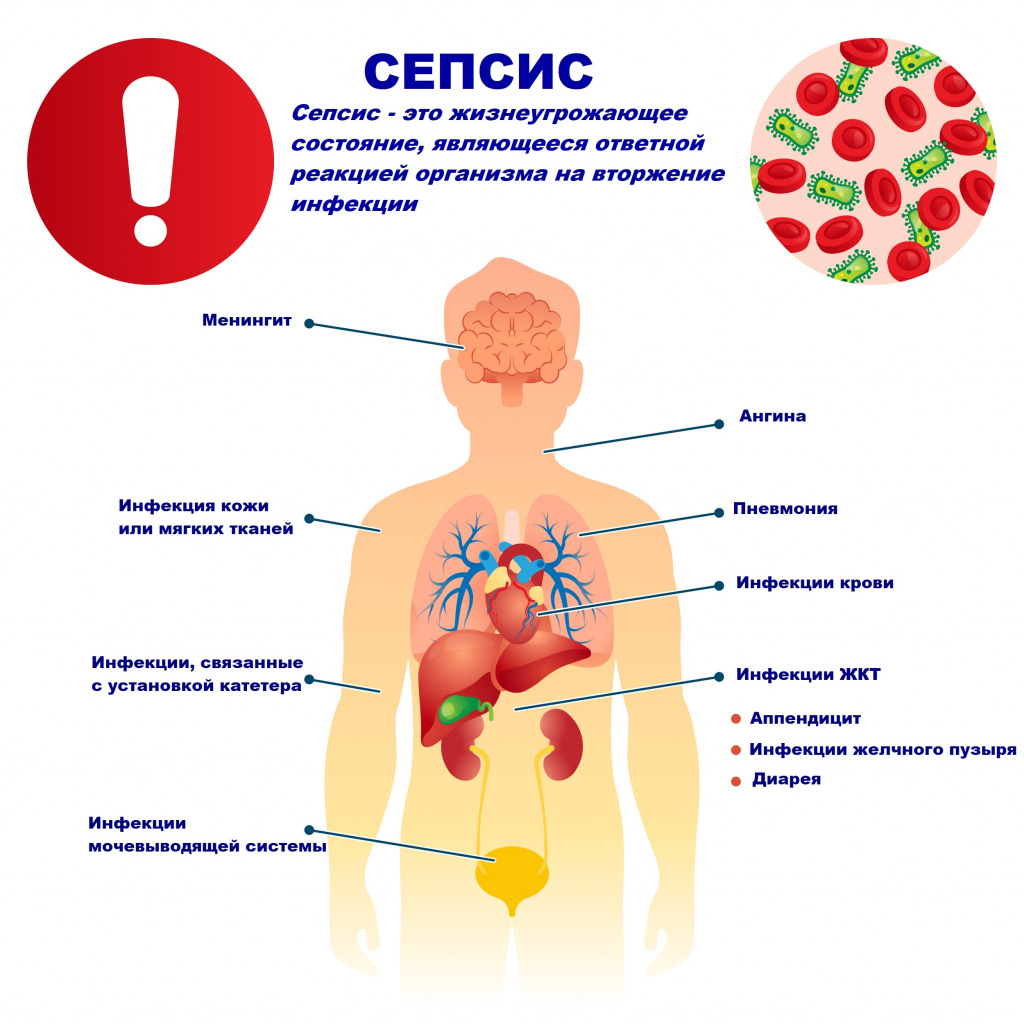
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также:

