Сенсибилизация лимфоцитов на инфекционные антигены
Обновлено: 26.04.2024
Реакции гиперчувствительности четвертого типа ( IV типа ). Гиперчувствительность замедленного типа. Реакции гиперчувствительности замедленного типа.
Реакции гиперчувствительности IV типа также называют гиперчувствительность замедленного типа (ГЗТ). Они обусловлены клеточными иммунными реакциями. В отличие от реакций немедленного типа, они развиваются не ранее чем через 24-48 ч после повторного введения Аг. Развитие реакций гиперчувствительности замедленного типа (ГЗТ) индуцируют продукты микроорганизмов и гельминтов, природные и неприродные Аг и гаптены (лекарства, косметические красители).
Классические примеры гиперчувствительности замедленного типа (ГЗТ) — туберкулиновая проба и контактный дерматит. Распознавание Аг, связанного с белками организма, иммунокомпетентными клетками вызывает активацию Т-хелперов, что приводит к клональной пролиферации Т-эффекторов ГЗТ. Сенсибилизированные лимфоциты секретируют цитокины, привлекающие другие лимфоциты и макрофаги в очаг аллергической реакции. На более поздних этапах в реакцию включаются полиморфно-ядерные фагоциты, стимулирующие воспалительный ответ.
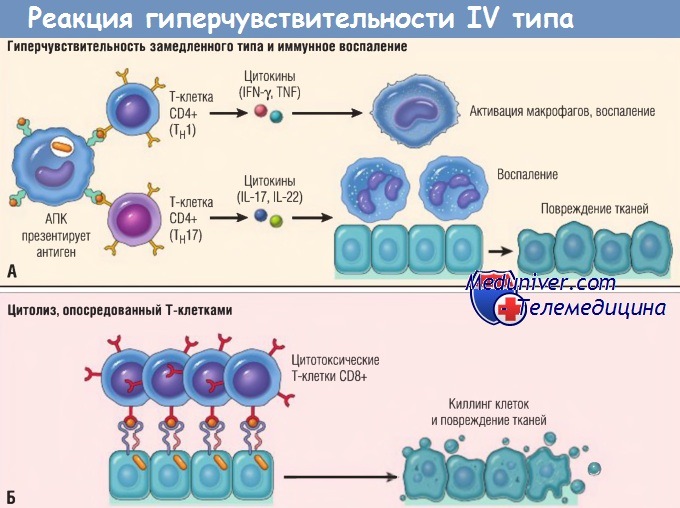
Механизмы реакций гиперчувствительности типа IV, опосредованных Т-клетками.
(А) В реакциях гиперчувствительности замедленного типа Тн1-клетки CD4+ (а иногда Т-клетки CD8+, не показаны) отвечают на тканевые антигены секрецией цитокинов,
которые стимулируют воспаление и активируют фагоцитоз, приводя к повреждениям тканей. Тн17-клетки CD4+ способствуют воспалению, мобилизуя нейтрофилы (в меньшей степени моноциты).
(Б) При некоторых заболеваниях цитотоксические Т-клетки CD8+ непосредственно убивают клетки тканей.
IFN — интерферон; IL — интерлейкин; TNF — фактор некроза опухоли; АПК — антигенпрезентирующая клетка.
• Гаптены приобретают способность инициировать реакции гиперчувствительности замедленного типа (ГЗТ) после взаимодействия с высокомолекулярными соединениями, в частности с белками. В свою очередь белки вызывают гиперчувствительность замедленного типа (ГЗТ) при длительной иммунизации малыми дозами в сочетании с адъювантами. Многие низкомолекулярные органические вещества или неорганические вещества (например, хром), связываясь с белками кожи, выполняют роль гаптенов и сенсибилизируют организм при длительном контакте. В результате развивается контактная аллергия, клинически проявляющаяся контактными дерматитами.
• Способность отвечать развитием гиперчувствительности замедленного типа (ГЗТ) на различные микробные продукты (например, Аг возбудителей туберкулёза, бруцеллёза) применяют при постановке кожных проб для диагностики инфекционного процесса или установления возможного контакта организма с возбудителем.
Реакции гиперчувствительности четвертого типа ( IV типа ). Гиперчувствительность замедленного типа. Реакции гиперчувствительности замедленного типа.
Реакции гиперчувствительности IV типа также называют гиперчувствительность замедленного типа (ГЗТ). Они обусловлены клеточными иммунными реакциями. В отличие от реакций немедленного типа, они развиваются не ранее чем через 24-48 ч после повторного введения Аг. Развитие реакций гиперчувствительности замедленного типа (ГЗТ) индуцируют продукты микроорганизмов и гельминтов, природные и неприродные Аг и гаптены (лекарства, косметические красители).
Классические примеры гиперчувствительности замедленного типа (ГЗТ) — туберкулиновая проба и контактный дерматит. Распознавание Аг, связанного с белками организма, иммунокомпетентными клетками вызывает активацию Т-хелперов, что приводит к клональной пролиферации Т-эффекторов ГЗТ. Сенсибилизированные лимфоциты секретируют цитокины, привлекающие другие лимфоциты и макрофаги в очаг аллергической реакции. На более поздних этапах в реакцию включаются полиморфно-ядерные фагоциты, стимулирующие воспалительный ответ.

Механизмы реакций гиперчувствительности типа IV, опосредованных Т-клетками.
(А) В реакциях гиперчувствительности замедленного типа Тн1-клетки CD4+ (а иногда Т-клетки CD8+, не показаны) отвечают на тканевые антигены секрецией цитокинов,
которые стимулируют воспаление и активируют фагоцитоз, приводя к повреждениям тканей. Тн17-клетки CD4+ способствуют воспалению, мобилизуя нейтрофилы (в меньшей степени моноциты).
(Б) При некоторых заболеваниях цитотоксические Т-клетки CD8+ непосредственно убивают клетки тканей.
IFN — интерферон; IL — интерлейкин; TNF — фактор некроза опухоли; АПК — антигенпрезентирующая клетка.
• Гаптены приобретают способность инициировать реакции гиперчувствительности замедленного типа (ГЗТ) после взаимодействия с высокомолекулярными соединениями, в частности с белками. В свою очередь белки вызывают гиперчувствительность замедленного типа (ГЗТ) при длительной иммунизации малыми дозами в сочетании с адъювантами. Многие низкомолекулярные органические вещества или неорганические вещества (например, хром), связываясь с белками кожи, выполняют роль гаптенов и сенсибилизируют организм при длительном контакте. В результате развивается контактная аллергия, клинически проявляющаяся контактными дерматитами.
• Способность отвечать развитием гиперчувствительности замедленного типа (ГЗТ) на различные микробные продукты (например, Аг возбудителей туберкулёза, бруцеллёза) применяют при постановке кожных проб для диагностики инфекционного процесса или установления возможного контакта организма с возбудителем.
Клеточный иммунитет при вирусной инфекции. Эффекторные и регуляторные Т-клетки во время вирусной инфекции.
Антитела могут нейтрализовать вирус на месте внедрения и, тем самым, предотвратить возникновение инфекции. Однако при уже развивающейся инфекции для ее прекращения и элиминации вирусов, кроме специфических антител необходим клеточный иммунитет, под которым понимают иммунную активность самих клеток иммунной системы, тогда как под гуморальным — активность их продуктов. Однако при вирусных инфекциях у млекопитающих и птиц, как правило, имеет место интегрированный клеточный и гуморальный иммунный ответ.
Клеточные иммунные реакции на инфицированные вирусом клетки могут опосредоваться антиген-специфическими субпопуляциями Т-клеток, а также клетками, неспособными распознавать специфические вирусные антигены. Следует отметить, что в выздоровлении от вирусных инфекций первым принадлежит более важная роль, чем вторым. Иными словами, основу клеточного иммунитета составляют сенсибилизированные лимфоциты. Известно, что при отсутствии клеточного иммунитета инфекции часто имеют персистирующии и прогрессирующий характер, что свидетельствует о дефекте долговременных защитных механизмов.
Цитотоксические и NK-клетки узнают клетки-мишени, прочно к ним прикрепляются и выделяют на их поверхность молекулы специального белка (перфорина), которые внедряются в наружную мембрану, полимеризуются и вызывают в ней образование пор, через которые вытекает цитоплазма, и инфицированная клетка вскоре погибает. Перфорин, обладающий серин-эстеразной активностью (granzymes), напоминает компонент (С9), ответственный за комплемент-опосредованный лизис.
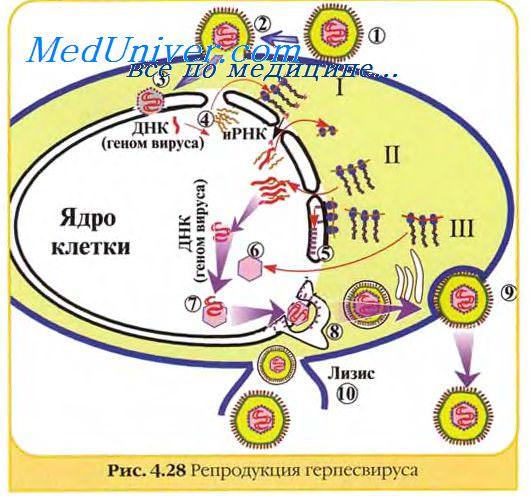
Возможно, что образование пор в плазматической мембране клеток-мишеней, — не единственный механизм цитотоксического действия Т-лимфоцитов, однако этот механизм весьма эффективен.
Установлено, что опосредуемый антигеном апоптоз клеток приводит к более эффективной доставке антигена к антиген-представляющим клеткам, например, к дендритным клеткам.
Эффекторные и регуляторные Т-клетки во время вирусной инфекции
После антигенной стимуляции, индуцирующей преимущественно клеточный иммунитет, в тимусзависимых областях лимфоидных органов наблюдается созревание и пролиферация антиген-специфических Т-лимфоцитов.
Т-эффекторы, осуществляющие клеточно-опосредованные формы иммунного ответа, характеризуются, прежде всего, цитотоксической активностью. Цитотоксические реакции весьма неоднородны по своим механизмам и могут опосредоваться клетками, антителами, комплементом.
Среди лимфоцитов, обладающих киллерной активностью, основную роль в элиминации вирусов из пораженных ими клеток играют вирусспецифические цитотоксические Т-лимфоциты (Тц-лимфоциты) и естественные киллеры (NK-лимфоциты). Хотя последние проявляют защитное действие на ранней стадии инфекции, тем не менее, ведущее значение в разрушении инфицированных клеток и освобождении организма от возбудителя принадлежит Тц-лимфоцитам.
Антигенспецифические Тц-лимфоциты при вирусных инфекциях взаимодействуют с клетками-мишенями и разрушают их при помощи рецепторного аппарата в отсутствии антител и комплемента. Они имеют двойную специфичность: к вирусным антигенам на поверхности инфицированных клеток и к главному комплексу гистосовместимости клеток хозяина. Для индукции Тц-клеток необходимы Т-хелперы (Тх-лимфоциты), активизированные вирусным антигеном. При ряде вирусных инфекций клетки распознают иные антигенные структуры вирусов, чем В-клетки и антитела. Это связано с рецептором Тц-клеток, распознающим вирусные антигены на клеточной поверхности, природа которого неизвестна. Следовательно, Т-клетки и антитела распознают вирусные антигены посредством различных механизмов. При этом они, как правило, распознают различные эпитопы. На молекуле НА вируса гриппа Тц-лимфоциты и антитела реагируют, соответственно, с НА2 и НА1. Вирусные антигены, являющиеся индукторами и мишенями Тц-клеток при различных вирусных инфекциях человека и животных, исследованы недостаточно. Для многих вирусов конкретные вирусные антигены, являющиеся индукторами и мишенями Тц-клеток, не идентифицированы, а имеющиеся данные зачастую противоречивы.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Т-лимфоциты и В-лимфоциты иммунитета. Предварительная обработка Т- и В-лимфоцитов
а) Клеточно-опосредованный и гуморальный иммунитеты обеспечивают два типа лимфоцитов - Т- и В-лимфоциты. Хотя при исследовании под микроскопом большинство лимфоцитов в нормальной лимфоидной ткани выглядят одинаковыми, эти клетки подразделяют на две основные популяции. Одна популяция — Т-лимфоциты — ответственна за формирование активированных лимфоцитов, обеспечивающих клеточно-опосредованный иммунитет. Другая популяция — В-лимфоциты — ответственна за формирование антител, обеспечивающих гуморальный иммунитет.
Оба типа лимфоцитов образуются у эмбриона из полипотентных гемопоэтических стволовых клеток, формирующих лимфоциты как один из наиболее важных результатов их дифференцировки. Почти все сформированные лимфоциты в результате заселяют лимфоидную ткань, однако прежде чем это произойдет, они дополнительно дифференцируются или проходят предварительную обработку.
Лимфоциты, которые в итоге станут активированными Т-лимфоцитами, сначала мигрируют к тимусу, где подвергаются предварительной обработке. Эти ответственные за клеточно-опо-средованный иммунитет лимфоциты называют Т-лимфоцитами, что подчеркивает роль тимуса.
Другая популяция лимфоцитов, В-лимфоциты, предназначенные для формирования антител, проходят предварительную обработку в печени плода в середине периода внутриутробной жизни, а также в костном мозге в конце внутриутробной жизни плода и после рождения. Эта популяция клеток впервые была открыта у птиц, имеющих специальный орган для их предварительной обработки, который называют бурсой Фабриция (фабрициевой сумкой). Ответственные за гуморальный иммунитет лимфоциты называют В-лимфоцитами, что подчеркивает роль бурсы.
На рисунке ниже показаны две лимфоцитарные системы для формирования: (1) активированных Т-лимфоцитов; (2) антител.
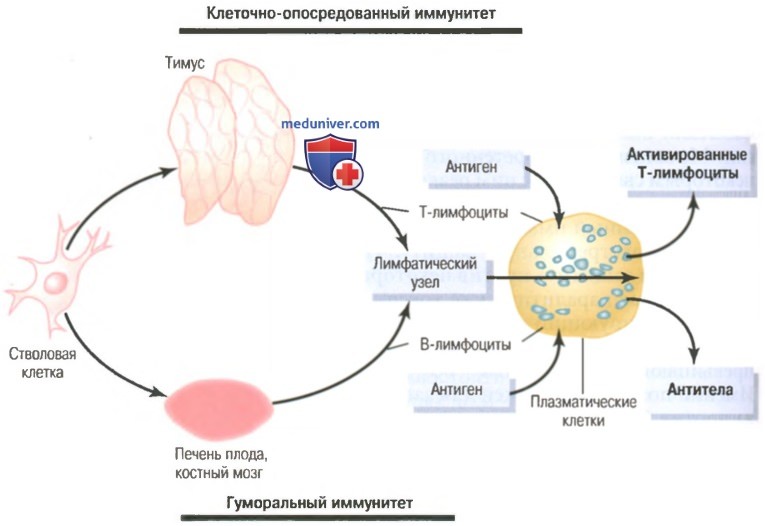
Формирование антител и активированных лимфоцитов в лимфатическом узле в ответ на действие антигенов.
Этот рисунок также демонстрирует происхождение лимфоцитов тимуса (Т-лимфоцитов) и бурсы (В-лимфоцитов), ответственных за клеточно-опосредованные и гуморальные иммунные процессы, соответственно
Предварительная обработка Т- и В-лимфоцитов
Все лимфоциты организма происходят от коммитированных в лимфоцитарном направлении стволовых клеток эмбриона, но эти клетки не могут непосредственно превратиться в активированные Т-лимфоциты или антитела. Прежде чем это станет возможным, клетки должны подвергнуться дальнейшей дифференцировке в соответствующих областях, где они проходят специфическую обработку.
а) Т-лимфоциты проходят предварительную обработку в тимусе (вилочковой железе). После образования в костном мозге Т-лимфоциты сначала мигрируют к вилочковой железе. Здесь они быстро делятся, одновременно становясь чрезвычайно разнообразными, т.е. предназначенными для реакции против разных специфических антигенов. Это значит, что один лимфоцит, обработанный в тимусе, проявляет специфическую реактивность в отношении одного антигена. Следующий лимфоцит специфически реагирует на другой антиген. Это продолжается до тех пор, пока в тимусе не появятся тысячи разных типов лимфоцитов со специфической реактивностью в отношении тысяч разных антигенов. Эти разные типы предварительно обработанных Т-лимфоцитов оставляют тимус и распространяются кровью по всему телу, временно оседая в лимфоидной ткани.
Кроме того, благодаря обработке в тимусе любой оставляющий его Т-лимфоцит не реагирует с белками или другими антигенами собственных тканей организма (иначе Т-лимфоциты погубили бы собственное тело человека в течение всего нескольких дней). Тимус выбирает, какие Т-лимфоциты могут его покинуть, сначала смешивая их практически со всеми специфическими аутоантигенами собственных тканей тела. Если Т-лимфоцит реагирует, он разрушается и фагоцитируется, вместо того, чтобы выделяться. Это происходит с основной частью клеток (вплоть до 90%). Таким образом, клетки, выделяющиеся из тимуса, не реагируют против собственных антигенов тела; они реагируют лишь на антигены внешних источников, например бактерий, токсинов или тканей, пересаженных от другого человека.
Основная часть предобработки Т-лимфоцитов в тимусе происходит перед рождением ребенка и в течение нескольких месяцев после рождения. Удаление вилочковой железы после этого периода ослабляет (но не исключает) Т-лимфоцитарную иммунную систему. Однако удаление тимуса за несколько месяцев до рождения может нарушить развитие всего клеточно-опосредован-ного иммунитета. Поскольку именно клеточный тип иммунитета в основном отвечает за отторжение трансплантированных органов, например сердца или почек, органы можно пересаживать с меньшей вероятностью отторжения, если у животного в соответствующее время до его рождения удалить тимус.
б) В-лимфоциты проходят предварительную обработку в печени и костном мозге. О деталях предварительной обработки В-лимфоцитов известно гораздо меньше, чем о предобработке Т-лимфоцитов. Известно, что у человека предварительная обработка В-лимфоцитов осуществляется в печени в середине внутриутробного периода развития, а также в костном мозге в конце внутриутробного периода и после рождения.
Существуют два важных различия между В- и Т-лимфоцитами. Во-первых, В-лимфоциты активно секретируют реактивные агенты, называемые антителами, в отличие от Т-лимфоцитов, реагирующих с антигеном непосредственно. Антитела — это крупные белковые молекулы, способные соединяться с антигенной субстанцией и разрушать ее. Во-вторых, разнообразие В-лимфоцитов выражено больше, чем у Т-лимфоцитов, т.е. формируются миллионы типов В-лимфоцитарных антител с разными специфическими реактивностями. После предобработки В-лимфоциты, как и Т-лимфоциты, мигрируют к лимфоидной ткани по всему телу, где временно располагаются рядом, но несколько обособленно от областей локализации Т-лимфоцитов.
Видео физиология защитной функции крови (иммунитета) и группы крови - профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
По способу получения различают активную С. и пассивную (пассивный перенос). Активная С. развивается при искусственном введении или естественном попадании аллергена (см.) в организм. Пассивную С. наблюдают после введения интактному реципиенту сыворотки крови или лимфоидных клеток от активно сенсибилизированного донора. Если возникает С. плода, то такую С. называют внутриутробной. С. может быть моновалентной — при повышении чувствительности к одному аллергену и поливалентной — при С. ко многим аллергенам. Перекрестной С. называют повышение чувствительности сенсибилизированного организма к другим антигенам, имеющим общие детерминанты с аллергеном, вызвавшим С.
В зависимости от химической природы, физического состояния и количества попавшего в организм аллергена, а также от реактивности организма в его реакцию на аллерген будут включаться различные иммунные механизмы. Это различие находит выражение в особенностях образующихся антител (см.) — их преимущественной принадлежности к тому или иному классу или подклассу иммуноглобулинов (см.) и их титрах, а также в образовании сенсибилизированных лимфоцитов (см.). Так, напр., слабые антигены (пыльца растений, домашняя пыль, перхоть и шерсть животных) вызывают преимущественное образование реагинов (см. Антитела аллергические). На корпускулярные нерастворимые аллергены (клетки тканей, бактерии, споры грибов и др.) организм реагирует чаще всего образованием антител, приводящих к включению цитотоксическнх механизмов и (или) появлению сенсибилизированных лимфоцитов. Растворимые аллергены (антитоксические сыворотки, гамма -глобулины, продукты лизиса бактерий и др.), особенно в больших количествах, вызывают появление антител, участвующих в образовании иммунных комплексов и эффектах преципитации.
Влияние реактивности организма (см.) на функцию иммунной системы реализуется несколькими путями. Во-первых, иммунный ответ на каждый антиген детерминирован генетически. От особенностей функционирования структурных генов, контролирующих синтез иммуноглобулинов (см.), зависит класс, подкласс, аллотип и идиотип образующихся антител. Iг-гены — гены иммунного ответа — определяют интенсивность иммунного ответа по количеству образующихся антител и (или) выраженности аллергической реакции замедленного типа, опосредуемой сенсибилизированными лимфоцитами. Так, напр., есть индивидуумы, к-рые отвечают избыточным образованием IgE-антител на нек-рые слабые антигены (пыльцу растений, перхоть и др.). Конкретный механизм избыточного образования IgE-антител связывают, в частности, с недостаточной активностью соответствующих T-клеток-супрессоров. Во-вторых, на иммунный ответ влияет состояние барьерных функций кожи и слизистых оболочек, к-рое определяет возможность поступления в организм многих экзогенных аллергенов. Напр., дефицит секреторного IgA способствует проникновению через слизистые оболочки аллергена, что приводит к образованию реагинов. В-третьих, состояние регуляторных систем, влияя на межклеточные взаимодействия в процессе иммунного ответа, на циркуляцию клеток и т. д., оказывает модулирующее влияние на характер иммунного ответа. Именно от этих факторов зависит образование сенсибилизированных лимфоцитов, вид антител, их титр и тем самым особенность аллергической реакции.
Все это вместе взятое дало основание для выделения следующих четырех типов С., из к-рых первые три связаны с особенностями образующихся антител, а четвертый — с образованием сенсибилизированных лимфоцитов.
С. при цитотоксическом типе аллергии стала предметом внимания исследователей с 1898 г., когда впервые в эксперименте введением эритроцитов животного одного вида в организм животного другого вида были получены гемолизины. Значительный вклад в развитие учения о цитотоксинах (см.) внесли отечественные ученые. В 1901 г. И. И. Мечников создал учение о клеточных ядрах (цитотоксинах), Е. С. Лондон сформулировал признаки, отличающие цитотоксины от хим. веществ, оказывающих токсическое действие на клетки; А. А. Богомолец в 1908 г. получил супрареноцитотоксическую сыворотку, а в 1925 г. под его руководством была получена антиретикулярная цитотоксичсская сыворотка (см.), к-рая нашла применение в леч. практике. Во всех этих исследованиях были получены цитотоксические антитела на антигены гомологичных или гетерологичных клеток. У людей механизм аллергии цитотоксического типа может включаться при попадании в организм изоантигенов, напр, при переливании крови, при гемолитической болезни новорожденных. В последнем случае мать, отрицательная по резус-антигену (см. Резус-фактор), во время родов или реже во время беременности при повреждениях плаценты сенсибилизируется эритроцитами резус-положительного плода, что приводит к образованию у нее антирезусных антител, к-рые относятся гл. обр. к IgG и свободно проходят через плаценту. Было также установлено, что цитотоксические антитела могут образовываться и к клеткам собственных тканей в тех случаях, если клетки получают аутоаллергенные свойства. Причины приобретения клетками аутоаллергенных свойств весьма разнообразны. Большую роль в этом процессе играет действие на клетки различных хим. веществ, чаще всего лекарственных средств, попадающих в организм и способных изменять антигенную структуру клеточных мембран за счет конформационных изменений молекул антигенов, повреждения клеточной мембраны и появления скрытых (репрессированных) антигенных детерминант, образования комплексов аллергенов с клеточной мембраной, в к-рых лекарственное или другое хим. вещество играет роль гаптена. Аналогичное действие на клетку могут оказывать лизосвмные ферменты нейтрофилов, выделяющиеся при фагоцитозе, а также бактериальные ферменты, вирусы. Во всех этих случаях антитела относятся гл. обр. к IgG или IgM. Механизмы реализации цитотоксического действия различны. В одних случаях оно связано с активацией комплемента (см.) так наз. комплементоопосредованная цитотоксичность. В других случаях включается так наз. антителозависимая клеточноопосредованная цитотоксичность. При этом антитела фиксируются на клетках-мишенях. Через Fc-конец своей молекулы они связываются с Fc-рецепторами различных клеток (К-клеток, моноцитов, нейтрофилов). Эти клетки и осуществляют цитотоксическое действие. Включение того или иного механизма цитотоксического типа аллергий зависит от характера и свойств образовавшихся антител, т. к. именно с ними связана способность присоединять комплемент, соединяться с Fc-рецепторами различных клеток. Так, напр., IgM, IgG1, IgG3 хорошо фиксируют комплемент, у IgG2 эта способность менее выражена, a IgG4 и IgE не фиксируют его вообще. С. при цитотоксическом типе аллергии играет существенную роль в нек-рых случаях лекарственной аллергии, в развитии ряда аутоаллергических (аутоиммунных) процессов (см. Аутоаллергические болезни).
Сенсибилизация при аллергии типа Артюса (повреждение иммунным комплексом) вызывается введением в организм больших количеств растворимого аллергена. Он вызывает образование антител, к-рые могут относиться к разным классам иммуноглобулинов, однако чаще всего они относятся к иммуноглобулинам классов IgG и IgM. Эти антитела называют также преципитирующими за их способность при соединении с соответствующим антигеном образовывать in vitro преципитат. В организме человека постоянно идут иммунные реакции с образованием комплекса антиген — антитело (см. Антиген — антитело реакция), т. к. в организм постоянно попадают какие-либо антигены извне или таковые образуются в самом организме. Эти реакции являются выражением защитной, или гомеостатической, функции иммунитета (см.) и не сопровождаются цитотоксическим или литическим действием. Однако при определенных условиях комплекс антиген — антитело может обладать повреждающим действием и способствовать развитию заболевания. В таких случаях говорят о том, что имела место С. Комплекс антиген — антитело может проявить повреждающее действие при следующих условиях: комплекс должен иметь определенную величину, по экспериментальным данным более 19S, что соответствует мол. весу (массе) 9•10 5 — 1•10 6 ; он должен быть образован с нек-рым избытком антигена; проницаемость сосудистой стенки должна оказаться повышенной, т. к. в этом случае комплекс антиген — антитело может откладываться в тканях. Обычно повышение проницаемости сосудистой стенки вызывается вазоактивными аминами, освобождающимися из тромбоцитов, а для этого к С. при аллергии типа Артюса должна присоединиться С. реагинового типа. С. при аллергии типа Артюса лежит в основе сывороточной болезни (см.), экзогенных аллергических альвеолитов (см.) и др.
Сенсибилизация при аллергии замедленного типа (син. повышенная чувствительность замедленного типа) развивается в случаях, когда в ответ на попадание в организм аллергена образуются так наз. сенсибилизированные лимфоциты (Т-эффекторы, или Т-киллеры). Они относятся к Т-популяции лимфоцитов (см. Иммунокомпетентные клетки), и их образование приводит к развитию С. замедленного типа. Соединяясь с аллергеном, эти лимфоциты вызывают аллергическую реакцию замедленного типа. Механизм С. такого типа лежит в основе развития многих инфекционно-аллергических заболеваний (см. Инфекционная аллергия), контактных дерматитов (см.) и др.
Развитие С. сопровождается изменением реактивности ряда систем и органов организма и активности нек-рых ферментных систем в течение определенного срока, что находит свое выражение в изменении чувствительности к действию различных неспецифических факторов. Так, А. Д. А до установил повышение возбудимости баро- и хеморецепторов каротидного синуса у сенсибилизированных собак, а И. А. Ходакова обнаружила у таких животных смену кортизолового типа стероидогенеза на кортикостероновый; в лаборатории Н. Д. Беклемишева установлено, что развитие С. к бактериальным антигенам у экспериментальных животных сопровождается выраженными изменениями окислительно-восстановительных процессов. Выявлено изменение чувствительности больных бруцеллезом и ревматизмом к действию физических факторов. Такое изменение чувствительности организма к действию самых различных факторов окружающей среды иногда называют неспецифической С. в отличие от специфической С., связанной с включением иммунных механизмов в ответ на данный аллерген.
Для выявления С. используют различные методы, к-рые применяются in vivo и in vitro. К методам in vivo относятся кожные пробы (см.). С. при реагиновом типе аллергии выявляется всеми видами кожных проб. Для нее характерно развитие уртикарной реакции (волдырь, иногда с псевдоподиями, окруженный зоной гиперемии) в первые 15— 20 мин. после введения аллергена в кожу. С. при аллергии типа Артюса выявляется при внутрикожном введении аллергена; реакция развивается через 4—6 час., место введения аллергена имеет вид очага воспаления. С. при замедленном типе аллергии выявляется внутрикожными и аппликационными пробами; реакция развивается через 24—48 час. С. при реагиновом типе аллергии выявляют при помощи реакции Прауснитца — Кюстнера (см. Прауснитца — Кюстнера реакция). Различными провокационными пробами (см.) можно успешно выявить С. при реагиновом типе аллергии и С. при аллергии типа Артюса; несколько труднее т. о. выявить замедленный тип сенсибилизации. Н. Д. Беклемишев считает, что лихорадка, появляющаяся после внутривенного введения бактериального аллергена, свидетельствует о С., характер-. ной для аллергии замедленного типа, т. к. аллерген, соединяясь с сенсибилизированными лимфоцитами, вызывает выделение определенных лимфокинов, к-рые стимулируют образование эндогенных пирогенов.
Широко используются многочисленные лабораторные методы выявления С. in vitro. Нек-рые из них позволяют выявить С. безотносительно к ее типу, напр, реакция бластотрансформации лимфоцитов (см.), тест ППН (см. Лейкоцитарные тесты). С помощью других лаб. методов выявляется преимущественно определенный тип С. Так, напр., С. при реагиновом типе аллергии диагностируется с помощью радиоаллергосорбентного метода (см.) и реакции Шультца — Дейла (см. Шультца — Дейла реакция) и др.; С. при цитотоксическом типе аллергии — с помощью реакции Кумбса (см. Кумбса реакция) и реакции Штеффена (см. Штеффена реакция); С. при аллергии типа Артюса — различными способами определения иммунных комплексов и преципитир у тощих антител; С. при аллергии замедленного типа определяют методом торможения миграции ;макрофагов (см.) или торможения миграции лейкоцитов, по образованию лихмфотоксинов и других лимфокинов. Диагностическая ценность этих методов не равнозначна. Их применение определяется задачами исследования и характером процесса.
Профилактика сенсибилизации
Общие принципы профилактики Сенсибилизации сводятся к уменьшению поступления в организм различных аллергенов и ликвидации условий, способствующих С. Для этого необходимы постоянное совершенствование схем проведения прививок и повышение качества используемых препаратов, рациональное ограничение использования гетерологичных антитоксических сывороток, особенно противостолбнячных, и замена их, где это возможно, на гомологичные гамма-глобулины, ограничение бесконтрольного приема лекарственных средств, проведения санации очагов хронической инфекции, соблюдение правил гигиены в быту, ограничивающих поступление в организм пылевых и других аллергенов, совершенствование технологических процессов в целях ограничения действия на организм промышленных аллергенов. Особое внимание должно быть уделено выявлению детей с дефицитом секреторного IgA и другими иммунодефицитными состояниями, способствующими развитию С. (см. Иммунологическая недостаточность), и коррегирующей терапии.
Библиография: Адо А. Д. Антигены как чрезвычайные раздражители нервной системы, М., 1952, библиогр.; он же, Общая аллергология, М., 1978; Беклемишев Н. Д. Инфекционная аллергия, Алма-Ата, 1968; Беклемишев Н. Д. и Суходоева Г. С. Аллергия к микробам в клинике и эксперименте, М., 1979, библиогр.; Гущин И. С. Об элементах биологической целесообразности аллергической реактивности, Пат. физиол. и эксперим. тер., в. 4, с. 3, 1979, библиогр.; Пыцкий B. И. Кортикостероиды и аллергические процессы, М., 1976; Coombs R. R. А. a. Gell P. G. H. Classification of allergic reactions responsible for clinical hypersensitivity and disease, в кн.: Clin, aspects immunol., ed. by P. G. H. Gellj a. o., p. 761, Oxford a. o., 1975.
Читайте также:

