Сепсис в судебной медицине
Обновлено: 25.04.2024
Кафедра хирургии и ОВП с курсом эндохирургии факультета последипломного образования Российского государственного медицинского университета им. акад. И.П. Павлова, Новомосковская городская клиническая больница
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
Что такое сепсис: 25-летний опыт развития концепции
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2017;(1): 82‑87
Кафедра хирургии и ОВП с курсом эндохирургии факультета последипломного образования Российского государственного медицинского университета им. акад. И.П. Павлова, Новомосковская городская клиническая больница
Кафедра хирургии и ОВП с курсом эндохирургии факультета последипломного образования Российского государственного медицинского университета им. акад. И.П. Павлова, Новомосковская городская клиническая больница
ФГУ Эндокринологический научный центр Минздравсоцразвития РФ
Несмотря на то что в последние годы были получены данные, свидетельствующие о снижении летальности вследствие сепсиса в клиниках с высоким технологическим уровнем организации лечебного процесса и корректной отчетностью [31], он был и остается нерешенной проблемой глобального здравоохранения [5, 12, 23, 26]. Проблема лечения пациентов с сепсисом не ограничивается высоким уровнем острой смертности непосредственно при первичном обращении, а заключается еще и в том, что частота повторной 30-дневной госпитализации пациентов этой категории достигает 19,9—23,4%, из которых 66,9—78% обусловлены инфекцией [13, 16, 24, 25], причем в течение года больные имеют многократно повышенный риск рецидива угрожающей их жизни инфекции [25, 34].
Cиндром системной воспалительной реакции — ССВР (Systemic Inflammatory Response Syndrome — SIRS)—это патологическое состояние, обусловленное одной из форм хирургической инфекции или альтерацией тканей неинфекционной природы (травмой, операцией, панкреатитом, ожогом, ишемией или аутоиммунным повреждением тканей и др.). Для выявления клинических признаков ССВР при сепсисе было рекомендовано использовать два или более признаков из четырех: температура тела 38 °C и выше или 36 °C и ниже; частота сердечных сокращений 90 в минуту и выше; частота дыхания более 20 в минуту или гипервентиляция (paCO2 32 мм рт.ст. и ниже); уровень лейкоцитов крови более 12·10 9 /мл или менее 4·10 9 /мл, или незрелых форм более 10%. Сепсису и тяжелому сепсису были даны определения.
Сепсис—это патологический процесс, в основе которого лежит реакция организма в виде генерализованного (системного) воспаления на инфекцию различной природы (бактериальную, вирусную, грибковую). Иначе говоря, под сепсисом предлагалось понимать наличие четко установленного инфекционного начала, послужившего причиной возникновения и прогрессирования двух или более признаков ССВР. Тяжелый сепсис —этосепсис, сочетающийся с органной дисфункцией (как минимум двух систем органов), гипотензией, нарушением тканевой перфузии. Проявлением последней, в частности, служат повышение концентрации лактата, олигурия, острое нарушение сознания.
Септический шок (СШ) —сепсис с признаками тканевой и органной гипоперфузии и артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов.
Одним из прогнозируемых, высокозначимых итогов консенсуса ACCP/SCCM (1991 г.) должна была стать возможность проведения согласованных эпидемиологических исследований, посвященных распространенности сепсиса в отдельных регионах мира, что способствовало бы динамичному развитию концепции в части выявления явных и скрытых дефектов в системе избранных координат [23]. Однако за столь длительный период это удалось реализовать лишь в ряде стран с высоким уровнем медицинских, информационных и коммуникационных технологий, а в большинстве стран мира, в том числе в Российской Федерации, этот принцип проведения эпидемиологических исследований оказался несостоятельным. В немалой степени этому способствовало получение при попытках анализа клинико-эпидемиологических корреляций в рамках определений сепсиса ACCP/SCCM (1991 г.) в разных странах абсолютно разноречивых результатов, касающихся как распространенности сепсиса в мире, так и частоты и значимости его отдельных клинических форм. В итоге это сказалось на полярно различающихся результатах лечения сепсиса [1, 26].
Среди РКС следует особо выделить признания значимости гипергликемии (более 7,7 ммоль/л) при отсутствии сахарного диабета, признаков нарушения сознания, гиперлактатемии более 1 ммоль/л, острой олигурии менее 0,5 мл/кг/ч, креатининемии более 44 мкмоль/л, нарушения коагуляции (АЧТВ более 60 с или МНО более 1,5, тромбоцитопения менее 100·10 9 /л), гипербилирубинемии более 70 ммоль/л и пареза кишечника.
Обоснованность логики внедрения РКС иллюстрируют результаты исследования А. Whippy и соавт. [35], согласно которым после введения в дополнение к критериям ACCP/SCCM (1991 г.) обязательного скрининга на уровень лактата в крови ранняя диагностика сепсиса в медицинском центре троекратно возросла (с 35,7 до 119,4 на 1000 госпитализаций). Примечательно, что у группы пациентов высокого риска по сепсису эффективность диагностики достигла 97% против 27%, если были использованы только критерии ACCP/SCCM (1991 г.).
Одно из национальных исследований, проведенных в США, продемонстрировало, что из 24,2 млн ежегодных госпитализаций пациентов с клиническими проявлениями ССВР (17,8% всех госпитализаций взрослых) на долю инфекционной природы синдрома приходится только 26% [17]. По итогам исследования М. Churpek и соавт. [11], основанного на анализе почти 270 тыс. ургентных госпитализаций в отделение интенсивной терапии, констатировано присутствие минимум двух критериев ССВР у 47% пациентов. Хотя летальность при наличии явлений ССВР была достоверно выше, чем без таковых (4,3% против 1,2%; р<0,001), итоговый вывод авторов заключался в том, что использование критериев ССВР для скрининга больных с сепсисом было лишено практической целесообразности.
В 2014 г. были опубликованы результаты объемного (анализировалось около 7 млн клинических наблюдений) исследования V. Liu и соавт. [22]. Дизайн этого исследования предусматривал изучение частоты летальных исходов в двух отдельных проектах с учетом дифференциации пациентов на когорты с выраженным сепсисом (при наличии бесспорных симптомов согласно рекомендациям ACCP/SCCM) и со скрытым (или латентным) сепсисом (с изолированными признаками острой инфекции либо острой органной недостаточности). В первом проекте частота явного сепсиса составила 11,4%, скрытого — 16,7%, во втором проекте явный сепсис был выявлен в 4,3%, а скрытый — в 10,9% всех госпитализаций в региональные клиники. Суммарная летальность при явном сепсисе оказалась почти в 2 раза ниже, чем при латентном. В первом проекте летальность составила 36,9% при явном сепсисе и 55,9% при латентном, во втором проекте — 34,7 и 52,0% соответственно. Большинство летальных исходов регистрируется при скрытом сепсисе, что свидетельствует в первую очередь о несовершенстве и низкой практической значимости исходных критериев ССВР и сепсиса (ACCP/SCCM, 1991 г.), поскольку стандарты для начала терапии пациентов при латентном течении инфекции определены менее четко, чем при явном.
В современных условиях, т. е. спустя 25 лет с момента принятия критериев ACCP/SCCM (1991 г.) [10] и получивших общемировое признание дополнений, внесенных в 2001 г. [21] и подтвержденных для использования в 2012 г. [12], их интерпретация представляет сложность для врачей во всем мире. В американском исследовании С. Rhee и соавт. [27] 94 врачам, занимающимся интенсивной терапией (88%), пульмональной реанимацией (39%), анестезиологам (19%), хирургам (9%) и врачам скорой помощи (9%) были предложены ситуационные задачи, в которых моделировалось по одному клиническому случаю с признаками ССВР без сепсиса, с сепсисом, с ТС, с СШ и без признаков инфекции. Средний стаж практической деятельности респондентов составил 8 лет, 90% из них практиковали в академических больницах. Большинство врачей (83%) были уверены в своей способности применять традиционные определения сепсиса, согласно критериям ACCP/SCCM (1991 г.), а при ознакомлении с текстом заданий 74% посчитали их формулировки реалистичными и понятными. Инициаторов исследования в первую очередь интересовала способность респондентов диагностировать ТС и СШ. В результате 17% респондентов классифицировали один из пяти случаев как ТС/СШ, 27,7% оценили два случая, 33,0% — три случая, 19,2% — четыре случая, 3,2% оценили все пять случаев как ТС/СШ.
Применительно к пониманию сущности определения СШ, а главное, к признанию общепринятых критериев его подтверждения, казалось бы, не должно быть противоречий. Однако даже при этой предельно конкретной форме течения септического синдрома в современной литературе встречается множество разночтений как в определении критериев цифрового выражения глубины гипотонии, так и в выборе оптимальных маркеров тканевой гипоперфузии, будь то, к примеру, уровень лактатемии, гипоксемии или дефицита оснований [28]. Та же гиперлактатемия, как правило, встречается при всех типах шока и является результатом не только перфузионных, но и гликолитических и органносистемных нарушений [32].
Рассматривать гипотонию в качестве единственного критерия СШ у пациентов с инфекцией не вполне логично с позиции современного понимания патобиологии сепсиса. Это связано с тем, что низкие показатели артериального давления могут быть обусловлены приемом гипотензивных препаратов или потенцированным эффектом комбинации нескольких фармакологических препаратов [28]. Неоднородности практического определения СШ и прогноза его терапии в значительной степени способствуют такие зависимые от клинициста управляемые составляющие вмешательств, как состав, объем, темпы осуществления инфузионной, вазопрессорной и инотропной терапии [18, 20]. D. Gaieski и соавт. [15], используя 4 разных метода статистического анализа динамики заболеваемости и летальности от септического шока в США, получили показатели, различающиеся в зависимости от выбранного метода максимально в 3,5 раза.
Судьбоносной, сыгравшей важную роль в том, что была сформирована рабочая группа с целью выработки международного консенсуса по дефиниции сепсиса [16], стала статья коллектива авторов под руководством J.-L. Vincent [33]. В статье лаконично сформирован постулат, согласно которому сепсис следует определять как системную реакцию на инфекцию только при обязательном формировании какой-либо органной дисфункции.
Российская хирургическая мысль не осталась в стороне от процесса поиска оптимальных определений и диагностических критериев различных категорий сепсиса. А.Б. Ларичев считает, что восприятие ССВР как классификационной категории сепсиса противоречит логике современного понимания генерализованного воспаления [2]. По мнению И.В. Нехаева [4], для констатации сепсиса обязательно наличие синдрома полиорганной недостаточности — СПОН (для формулировки диагноза ТС) или шока (для формулировки диагноза СШ).
С.С. Маскиным и соавт. [3] на модели распространенного гнойного перитонита (РГП) были предложены в качестве критериев абдоминального сепсиса (АС) следующие классификационные параметры: наличие трех или четырех критериев ССВР + синдром кишечной недостаточности II—III стадий + наличие критериев недостаточности одного органа (системы), соответствующее оценке по шкале SOFA до 3 баллов. Критериям абдоминального ТС, по мнению исследователей, соответствует ситуация, при которой констатировано наличие СПОН, оцененное по шкале SOFA в 4 балла и более. Модель апробировалась на когорте из 335 пациентов, при этом РГП без сепсиса был констатирован у 26,0±1,4%, АС — у 45,1±2,4% и ТС — у 28,9±1,6% из них. Результаты лечения оценивались в рамках дифференцированного подхода к контролю источника внутрибрюшной инфекции, продемонстрировавшего, что летальность при РГП и отсутствии сепсиса составила 11,4±1,2%, при АС — 34,4±2,8%, при ТС и СШ — 46,3±4,7% (p
Патологоанатомическая диагностика сепсиса : методические рекомендации / О.Д.Мишнёв, А.И.Щёголев, О.А.Трусов. — Москва, 2004.
библиографическое описание:
Патологоанатомическая диагностика сепсиса : методические рекомендации / Мишнёв О.Д., Щёголев А.И., Трусов О.А. — 2004.
код для вставки на форум:
Российское общество патологоанатомов
О.Д.Мишнев, А.И.Щеголев, О.А.Трусов
ПАТОЛОГОАНАТОМИЧЕСКАЯ ДИАГНОСТИКА СЕПСИСА
Введение
Сепсис – полиэтиологическое инфекционное заболевание, характеризующееся генерализованным характером, ацикличностью течения и особым образом измененной реактивностью. Сепсис развивается из местных очагов инфекции и рассматривается, как правило, в качестве осложнения заболеваний, послуживших причиной генерализации инфекции. Последние годы, несмотря на интенсивную терапию, характеризуются ростом числа больных сепсисом и высокой летальностью.
Сепсис представляет собой заболевание, в отношении этиологии, патогенеза, патологической анатомии, диагностики, лечения которого всегда были и ещё будут проводиться дискуссии. Клиницисты обращаются к патологоанатомам в надежде получить желаемое и в то же время, по их мнению, объективное и адекватное объяснение летального исхода при сепсисе. Однако, справедливости ради, следует констатировать, что, как правило, такое объяснение для них a priori, до вскрытия, в современных клиниках уже имеется, и оно может быть получено на основании комплекса клинических и лабораторных признаков доказательной медицины.
Именно эти показатели, очевидно, следует использовать и патологоанатому при анализе истории болезни и результатов вскрытия для решения своих диагностических проблем. Многие клиницисты интересуются на вскрытии, т.е. a posteriori, не столько познанием на морфологическом субстрате причины и действия, сколько прагматичным согласованием формальных параметров, определяемых при сличении клинического и патологоанатомического диагнозов. Это определяет первоочередную задачу совместной междисциплинарной работы – нахождения общих точек соприкосновения клиницистов и патологоанатомов для полноценного и современного анализа результатов патологоанатомического исследования умерших от сепсиса.
Теоретические аспекты проблемы сепсиса, представленные в мировой литературе конца ХХ – начала нынешнего века и воспринимаемые как революционные и во многом совершенные, дающие основания для разработки оптимальных методов лечения и недопущения летальных исходов при сепсисе, не были неожиданными для патологоанатомов России. В этом заслуга наших Учителей и в первую очередь И.В. Давыдовского, а также А.В.Смольянникова, Д.С.Саркисова, А.П.Авцына, Н.К.Пермякова и других, которые первоочередное внимание уделяли макробиологической составляющей сепсиса, не забывая при этом об этиопатогенетической роли возбудителей инфекции.
Принятие и выполнение решений Согласительной конференции пульмонологов и специалистов по интенсивной терапии (ACCP/SCCV), состоявшейся в 1991 году в Чикаго, привело к унификации терминологии и к упрощению клинической диагностики сепсиса. Однако отсутствие рандомизированных патологоанатомических исследований и, соответственно, клинико-морфологических сопоставлений является одной из важных причин неполного взаимопонимания клиницистов и патологоанатомов при оценке формы и танатогенеза заболевания, а также при обсуждении расхождений клинического и патологоанатомического диагнозов. К сожалению, до настоящего времени предметом дискуссий является отнесение тех или иных клинических и морфологических признаков к проявлениям сепсиса.
Также следует остановиться на распространённой ныне тенденции считать условным выделение разновидностей сепсиса по входным воротам, поскольку генерализованная реакция организма на инфекцию по своей сути является единой и требует незамедлительного лечения, а в Международной классификации болезней отсутствует подразделение сепсиса на разновидности по данному основанию. Возможно, что такой прагматичный подход является обоснованным, однако мы рекомендуем патологоанатомам не забывать о морфологических особенностях различных форм сепсиса в зависимости от входных ворот.
Действительно, для патологоанатома и клинициста не будет представлять большой сложности достижение взаимопонимания при анализе результатов секции больного, погибшего от сепсиса при наличии типичных морфологических признаков и соответствующих клинических данных. Гораздо большие трудности возникнут в том случае, когда больного лечили от сепсиса (и по результатам вскрытия довольно успешно – именно так!), а смерть наступила от другой причины, видимо не связанной с сепсисом. В этом случае необходимо учитывать не только медицинские составляющие (организационные, научно–практические), но также социальные и экономические вопросы, которые в настоящее время никогда не следует упускать из вида. Также сложными для патологоанатомической диагностики являются наблюдения лечённого сепсиса в плане танатогенеза и установления непосредственной причины смерти. Наконец, наблюдения посмертно диагностированного сепсиса, который не был выявлен в клинике, должны стать предметом обсуждения на клинико–патологоанатомических конференциях.
Определения терминов и понятий
Сепсис (в переводе с греческого sēpsis – гниение) – представляет собой особую форму тяжелой генерализованной инфекции, при которой макроорганизм не способен локализовать инфекционный процесс (Белянин В.Л., Рыбакова М.Г., 2004).
Бактериемия – симптом, обозначающий наличие в крови живых микроорганизмов (не обязательно только при сепсисе).
Диссеминация – употребляется, как правило, для характеристики распространения поражений при инфекционном процессе в пределах одного органа (например, диссеминированный туберкулез легких).
Генерализация – обозначает, как правило, поражение многих органов и систем (например, генерализованная вирусная, туберкулезная инфекция).
Синдром системного воспалительного ответа (ССВО) (Systemic Inflammatory Response Syndrome (SIRS), синдром системной воспалительной реакции (ССВР)) патологическое состояние, обусловленное одной из форм хирургической инфекции или альтерации ткани неинфекционной природы (травма, панкреатит, ожог, ишемия или аутоиммунные повреждения тканей и др.). Это понятие предложено классификацией ACCP/SCCV, что привело к существенному пересмотру концептуальных положений о патогенезе, клинике, лечении, профилактике возникновения сепсиса и его осложнений. ССВР (SIRS) характеризуется наличием более чем одного из четырёх следующих основных клинических признаков: гипертермия, тахикардия, тахипноэ, лейкоцитоз (или лейкопения). Подобные клинические признаки встречаются при сепсисе, но при этом обязательным является наличие инфекционного очага поражения в тканях или органах. Патологоанатомическая характеристика SIRS является объектом перспективных научных исследований.
Септицемия – клинико–патологоанатомическая форма сепсиса, при которой отсутствуют метастатические септические очаги. Септицемия – это сепсис без гнойных метастазов. По поводу правомочности применения этого понятия в качестве диагноза одной из форм сепсиса до сих пор продолжается дискуссия. Некоторые клиницисты и патологоанатомы советуют вообще отказаться от этого термина (Пермяков Н.К., 1992). Этот термин не представлен и в классификации ACCP/SCCV. Тем не менее, он рекомендован МКБ-10 как унифицированный для всех разновидностей сепсиса, и вплоть до нового пересмотра он должен применяться клиницистами и патологоанатомами при определении шифра большинства клинико–патологоанатомических форм сепсиса.
Септикопиемия – клинико–патологоанатомическая форма сепсиса. Для неё характерно наличие гнойного воспаления (абсцессов, апостем, флегмон, интерстициального гнойного воспаления) в различных органах и тканях, возникающего в результате гематогенного распространения микробных эмболов из септического очага. Септикопиемия – это сепсис с гнойными метастазами.
Термин септикопиемия не представлен в МКБ–10.
Термин сепсис носит обобщающий характер, как и термин септический процесс. Классификация ACCP/SCCV рекомендует в клинике использовать термин сепсис, а не септицемия или септикопиемия. В настоящее время не рекомендуется использовать термин септическое состояние, лишенный конкретной основы.
Тяжёлый сепсис (или сепсис-синдром) – форма сепсиса, предложенная в классификации ACCP/SCCV, при котором отмечаются признаки полиорганной недостаточности. В.Л.Белянин и М.Г.Рыбакова (2004) считают, что с точки зрения патоморфолога понятие тяжёлый сепсис (сепсис–синдром) нельзя признать удачной терминологической находкой.
Септический шок – другая форма тяжёлого сепсиса в классификации ACCP/SCCV, сопровождающаяся артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов.
Септический (бактериальный, инфекционный) эндокардит (острый и подострый) характеризуется, прежде всего, воспалительными поражениями клапанного аппарата сердца, развивающимися наряду с септическими проявлениями. Представляет собой самостоятельное заболевание (первоначальную причину смерти) и имеет собственный шифр. Следует отличать от поражений эндокарда при других формах сепсиса.
Септический очаг – различают первичный и метастатические септические очаги. Первичный септический очаг представляет собой фокус воспаления, преимущественно гнойного, в котором происходит накопление микроорганизмов, распространяющихся затем гематогенно и лимфогенно по тканям и органам. Метастатические септические очаги (вторичные септические очаги, метастатические очаги при сепсисе, септические метастазы, метастатические гнойники, гнойные метастазы) представляют собой очаги воспаления, возникающие вследствие гематогенного перемещения септического процесса в ткани и органы из другого очага.
Системный инфекционный процесс – поражение какой-либо системы органов (например: нервной при клещевом энцефалите; пищеварительной при шигеллезе и т.д.).
Гнойно-резорбтивная лихорадка. Понятие гнойно-резорбтивной лихорадки предложено И.В.Давыдовским для обозначения клинических и патологоанатомических проявлений местного гнойно-некротического процесса, морфологически ограниченного демаркационным валом (в отличие от септических очагов) от окружающих тканей. В настоящее время этот термин почти не используется, а состояние больного обозначается как интоксикация или разновидность эндотоксикоза.
Эндотоксикоз – очень широкое понятие для обозначения осложнений и проявлений заболеваний и состояний организма. Основным фактором патогенеза эндотоксикоза является воздействие на организм токсических продуктов, образующихся в нем в результате нарушения тех или иных функций.
Этиология
Возбудителями сепсиса могут являться многие микроорганизмы (табл. 1). Это многочисленные бактерии: стрептококки, стафилококки, менингококки, пневмококки, кишечная палочка, синегнойная палочка, клебсиеллы, протей, сальмонеллы, а также грибы преимущественно Кандида и аспергиллус. Сепсисом может осложниться течение туберкулеза, сыпного тифа, брюшного тифа и других инфекционных заболеваний, возбудителями которых являются патогенные микроорганизмы. Генерализованные вирусные инфекции не принято рассматривать в качестве сепсиса, хотя об этом имеются указания в современных зарубежных клинических исследованиях.
Таблица. 1. Наиболее вероятная этиология сепсиса в зависимости от локализации первичного очага инфекции
ФГБУ "Российский центр судебно-медицинской экспертизы" Минздравсоцразвития России
Центральная клиническая больница с поликлиникой Управления делами Президента РФ;
кафедра хирургии факультета фундаментальной медицины Московского государственного университета им. М.В. Ломоносова, Москва
Центральная клиническая больница с поликлиникой Управления делами Президента РФ, Москва, Россия, 121356
Центральная клиническая больница с поликлиникой Управления делами Президента РФ, Москва, Россия, 121356
Постмортальная судебно-медицинская диагностика фульминантного сепсиса, вызванного грамотрицательной бактерией (Capnocytophaga canimorsus) после укуса собаки
Авторы приводят пример из практики, когда в ходе судебно-медицинского комиссионного исследования трупа постмортально диагностирован фульминантный сепсис, вызванный грамотрицательной бактерией (Capnocytophaga canimorsus) после укуса собаки. Для установления этиологического фактора фульминантного сепсиса экспертами было проведено исследование материала вскрытия методом ПЦР. Данный метод является новым в постмортальной диагностике этиологии сепсиса в нашей стране, не имеет аналогов за рубежом и может успешно использоваться в судебно-медицинской и патологоанатомической практике.
ФГБУ "Российский центр судебно-медицинской экспертизы" Минздравсоцразвития России
Центральная клиническая больница с поликлиникой Управления делами Президента РФ;
кафедра хирургии факультета фундаментальной медицины Московского государственного университета им. М.В. Ломоносова, Москва
Центральная клиническая больница с поликлиникой Управления делами Президента РФ, Москва, Россия, 121356
Центральная клиническая больница с поликлиникой Управления делами Президента РФ, Москва, Россия, 121356

Рис. 1. Апоплексия надпочечников. Ув. 200.

Рис. 2. Кровоизлияния и выраженные изменения нейронов в стволе головного мозга. Ув. 200.

Рис. 3. Капиллярный тромбоз петель клубочков. Ув. 400.
Таким образом, тщательно собранный клинический анамнез, исследование укушенных ран, причиненных собакой, танатогенетический анализ, проведенные дифференциальная диагностика и молекулярно-биологическое исследование (материал вскрытия) методом ПЦР позволили установить истинный характер заболевания.
Важно отметить, что в ходе исследования мы получили полезный опыт использования метода ПЦР в судебно-медицинской практике, который является новым в постмортальной диагностике этиологии сепсиса и не имеет аналогов в России и за рубежом.
В ходе исследования мы получили полезную информацию от врачей-инфекционистов, что род Capnocytophaga относится к грамотрицательным бактериям, обитающим в полости рта и глотке млекопитающих. Он принадлежит к семейству Flavobacteriaceae, порядку Flavobacteriales, классу Flavobacteria, типу Bacteroidetes, и включает восемь различных видов: 1) Capnocytophaga ochracea; 2) Capnocytophaga gingivalis; 3) Capnocytophaga granulesis; 4) Capnocytophaga haemolytica; 5) Capnocytophaga sputigena; 6) Capnocytophaga leadbetteri (выделены из полости рта человека); 7) Capnocytophaga canimorsus; 8) Capnocytophaga cynodegmi (выделены из полости рта животных).
Получен также опыт описания и экспертной оцен-ки повреждений от укуса собаки (стаффордширского бультерьера).
Акушерский сепсис – это системное осложнение инфекций женской мочеполовой системы и молочной железы, развившееся во время беременности, изгнания плода и в послеродовом (послеабортном) периоде. Проявляется тяжёлым общим состоянием, нарастающей слабостью, лихорадкой, сердцебиением, одышкой, снижением артериального давления. По мере прогрессирования присоединяются помутнение сознания, выраженное затруднение дыхания, резкое уменьшение объёма отделяемой мочи. Диагноз устанавливается на основании данных физикального осмотра, УЗИ, лабораторных исследований крови. Лечение комплексное: хирургическая санация гнойников, антибиотикотерапия, интенсивная терапия.
МКБ-10
Общие сведения

Причины
Акушерский сепсис всегда вторичен, его источником является локальная инфекция. Основные возбудители гнойно-воспалительных заболеваний – представители оппортунистической флоры (пиогенный стрептококк, стрептококк группы B, золотистый стафилококк, кишечная палочка, клебсиелла, протей, пептококк, пептострептококк, бактероид, грибок кандида), чаще всего населяют нижние отделы мочеполовой сферы и кишечника и приводят к патологии только под воздействием определённых факторов. К основным причинам и источникам инфицирования относятся:
- Хирургические операции и травмы тканей. Раневая поверхность служит воротами инфекции и способствует значительному снижению местного иммунитета. Гнойный процесс может стать исходом кесарева сечения, раннего отхождения околоплодных вод (при неправильном положении плода, многоплодии), полученных в родах разрывов и оперативных вмешательств на промежности.
- Лечебно-диагностические манипуляции. Возбудитель передаётся при контакте с обсеменённым инструментом, кроме того, микротравмы, полученные при исследовании, создают благоприятные условия для лимфо- и гематогенного заражения. В группе факторов риска - цервикальный серкляж, амниоцентез, кордоцентез, уретральная катетеризация, экстракорпоральное оплодотворение, многократные влагалищные исследования в ходе родов.
- Физиологические изменения, вызванные беременностью. Растущая матка сдавливает и смещает окружающие анатомические структуры, а прогестерон снижает тонус гладкой мускулатуры. Эти факторы приводят к нарушению уродинамики и создают предпосылки для развития гестационного пиелонефрита и уросепсиса.
- Застой грудного молока. В результате лактостаза происходит активный рост стафилококков, вызывающих мастит. Нарушение оттока молока – основная причина послеродовых абсцессов и флегмон.
С другой стороны, гнойные процессы могут осложниться сепсисом лишь при условии гипо- или гиперреактивности иммунного ответа. Функциональные расстройства иммунной системы приводят к усилению активности оппортунистических микроорганизмов и формированию патологической реакции на гнойное воспаление. К факторам риска относятся ожирение, сахарный диабет, анемия, острые и хронические воспаления (генитальные и экстрагенитальные), недостаток питания, возраст старше 35 лет.
Патогенез
Массивное поражение ткани инфекцией сопровождается перманентным или периодическим выбросом в кровоток медиаторов воспалительного ответа, что истощает регуляторную функцию иммунной системы и запускает ряд неконтролируемых реакций в дистантных органах и тканях. В результате повреждается эндотелий, ухудшается микроциркуляция (перфузия), снижается транспорт кислорода. Эти изменения приводят к нарушениям гомеостатической регуляции, развитию синдрома острой полиорганной недостаточности (СПОН) и ДВС-синдрома.
Желудочки сердца расширяются, происходит снижение сердечного выброса, нарушается сосудистый тонус. В лёгких образуются ателектазы, развивается респираторный дистресс-синдром. В результате снижения объёма циркулирующей крови (ОЦК) и гемостатических нарушений ухудшается микроциркуляция почечной ткани и кровоснабжение коркового слоя с последующей острой функциональной недостаточностью. В печени нарушаются обменные процессы, а недостаток кровоснабжения влечёт формирование некротических участков. Гипоперфузия приводит к патологической проницаемости слизистой оболочки кишечника с выбросом токсинов и микроорганизмов в лимфатическую систему, в результате ишемии на стенках органов ЖКТ образуются стрессовые язвы. Нарушение обменных процессов и микроциркуляции головного мозга обусловливает неврологические расстройства.
Классификация
Акушерский сепсис классифицируют по разным критериям: по возбудителю, по метастатическому распространению (септицемия, характеризующаяся наличием лишь первичного очага, и септикопиемия – наличие гнойных отсевов в других тканях и органах) или по клиническому течению. В современном акушерстве принята классификация, отражающая последовательные этапы формирования системной воспалительной реакции:
- Синдром системного воспалительного ответа (ССВО). Предвестник септического состояния – системная реакция на воспалительный процесс любой этиологии. Устанавливается при наличии воспалительного заболевания и на основании не менее двух клинических проявлений ССВО: тахикардии, тахипноэ или гипервентиляции, гипо- или гипертермии, лейкоцитоза (лейкопении) или повышения доли незрелых нейтрофилов. У 12% больных сепсисом признаки ССВО отсутствуют.
- Сепсис. Патологический системный ответ на первичную или присоединившуюся инфекцию. Диагноз выставляется при наличии инфекционного очага или на основании верифицированной бактериемии и остро развившихся признаков функциональной недостаточности двух и более органов (СПОН).
- Септический шок. Крайняя форма патологической реакции. Сопровождается выраженными, стойкими, плохо поддающимися медикаментозной коррекции гипотензией и нарушением перфузии.
Симптомы акушерского сепсиса
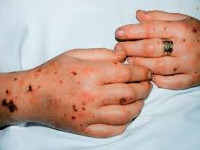
Послеродовый сепсис манифестирует на второй-третий день после изгнания плода сукровично-гнойными выделениями, явлениями общей интоксикации (тахикардией, одышкой, слабостью, потерей аппетита, иногда рвотой и диареей) и повышением температуры до 39-40°C с ознобами. Гипертермия обычно устойчивая, однако могут наблюдаться формы с постепенным повышением или большим разбросом суточной температуры и редкими приступами ознобов. Отмечаются боли в животе или молочных железах, могут регистрироваться генерализованные высыпания. Выраженность симптомов и длительность заболевания различны в зависимости от формы клинического течения.
Для молниеносного акушерского сепсиса нарастание симптоматики характерно в течение суток, при острой форме клиническая картина разворачивается в течение нескольких дней. При подострой форме признаки выражены менее ярко, процесс развивается неделями. Хрониосепсис характеризуется слабо выраженными изменениями (субфебрилитетом, повышенным потоотделением, головной болью и головокружениями, сонливостью, диареей) и вялым течением в течение многих месяцев. Рецидивирующая форма представляет череду затуханий (периодов ремиссии без заметных проявлений) и обострений (периодов с яркой симптоматикой) и характерна для септикопиемии, когда ухудшение состояния обусловлено повторными эпизодами образования вторичных гнойников.
Особенно тяжёлым течением и рядом специфических признаков отличается анаэробный сепсис, ассоциированный с гангреной матки. Заболевание протекает молниеносно или остро, сопровождается интенсивной некупируемой болью внизу живота, крепитацией и усилением боли при пальпации матки, выделением из влагалища газа и зловонной жидкости с пузырьками воздуха, бронзовой окраской кожи, бурым цветом мочи. Явления септического шока проявляются уже в самом начале болезни.
Осложнения
У больных, переживших острый период, может развиться тяжёлое, нередко летальное осложнение – суперинфекция. Значительное ухудшение качества жизни или гибель пациентки часто влекут другие последствия сепсиса: сопряжённые с ишемией или гнойным метастазированием необратимые органные изменения почек, печени, лёгких, сердца, головного мозга, прободение и кровотечения из гастроэнтеральных стресс-язв, артериальная тромбоэмболия и флеботромбоз. Сепсис у беременных может вызвать преждевременные роды, гибель плода, энцефалопатию и ДЦП рожденного ребенка.
Диагностика
В диагностике акушерского сепсиса участвуют акушер-гинеколог, терапевт, реаниматолог, микробиолог, осложнённые формы требуют привлечения нефролога, кардиолога, невролога, гепатолога. В ходе гинекологического исследования и общего осмотра по наличию очага гнойного воспаления в органах малого таза или молочной железе, а также признакам ССВО можно заподозрить септическое состояние. Проводятся следующие исследования:
- Определение возбудителя. Культуральный анализ крови и влагалищного мазка позволяют выявить инфекционный агент и подобрать эффективный препарат для лечения инфекции. Бактериемия подтверждает наличие септического процесса. При отсутствии бактериемии для дифференцирования локальной и генерализованной инфекции проводится тест на прокальцитонин.
- Инструментальные исследования. УЗИ малого таза и почек подтверждает (выявляет) наличие первичного гнойного очага в мочеполовых органах. УЗИ органов брюшной полости, рентгенография органов грудной клетки, ЭхоКГ позволяют обнаружить вторичные абсцессы в печени, лёгких, сердце.
- Клинико-биохимические анализы крови. Общий анализ крови обнаруживает лейкоцитоз, лейкопению, сдвиг лейкоцитарной формулы влево – значения, косвенно подтверждающие септическое состояние. Данные биохимического исследования говорят о нарушениях водно-электролитного баланса и функций почек, печени. Анализ газов крови выявляет нарушения КЩС и дыхательную недостаточность. По результатам коагулограммы определяются нарушения свёртывания крови. Тестирование уровня лактата в плазме позволяет обнаружить тканевую гипоперфузию и оценить тяжесть шока. Иммунограмма свидетельствует о расстройствах иммунной активности.
Акушерский сепсис следует дифференцировать с гестозами, амниотической эмболией и тромбоэмболией лёгочной артерии, острыми инфекциями (тяжёлым гриппом, бруцеллёзом, тифом, малярией, милиарным туберкулёзом), острым панкреатитом, лейкозами, лимфогранулематозом. Для дифференциальной диагностики может потребоваться консультация кардиохирурга, инфекциониста, фтизиатра, онкогематолога.
Лечение акушерского сепсиса
Лечебные мероприятия проводятся в условиях гинекологического или обсервационного акушерского отделения, больные с тяжёлыми формами сепсиса переводятся в отделение реанимации и интенсивной терапии. Лечение комплексное, включает хирургические и консервативные методы и направлено на борьбу с инфекцией и коррекцию витальных функций:
- Инфузионная терапия. Лечение предусматривает коррекцию гомеостатических расстройств (гипотонии, коагулопатии, нарушений кислотно-щелочного и водно-солевого и обмена, дефицита ОЦК), восстановление тканевой перфузии, дезинтоксикацию. С этими целями вводятся солевые и коллоидные растворы, альбумин, криоплазма, инотропы и вазопрессоры.
- Антибактериальная терапия. Направлена на уничтожение инфекционного агента с целью блокировки воспалительного каскада. Стартовое лечение включает внутривенное введение комбинации препаратов широкого спектра. После выделения возбудителя приступают к этиотропной антибиотикотерапии.
- Хирургическое лечение. Ликвидация гнойных очагов повышает эффективность интенсивной терапии и улучшает прогноз. Лечение предполагает санацию первичного и вторичных очагов – вскрытие и опорожнение абсцессов, кюретаж, вакуум-аспирацию или удаление матки (гистерэктомию).
В случае необходимости проводится искусственная вентиляция лёгких, энтеральное питание пациентки. Дополнительные методы интенсивной терапии включают применение кортикостероидов, выполнение хирургической детоксикации (плазмаферез, гемосорбция, гемофильтрация) после оперативного лечения нагноений, иммунотерапию.
Прогноз и профилактика
На ранних стадиях, когда не развились выраженные признаки СПОН, устойчивая гипотензия и ДВС-синдром, прогноз благоприятный. При развитии септического шока смертность может достигать 65% (в среднем – 45%). Профилактические мероприятия состоят в своевременном лечении воспалительных заболеваний (как на этапе планирования, так и в течение беременности), борьбе с внебольничными вмешательствами (внутриматочными и вагинальными манипуляциями, криминальными абортами, домашними родами), рациональной превентивной антибиотикотерапии при оперативных вмешательствах, полноценном питании, стабилизации уровня глюкозы в крови при сахарном диабете.
3. Клинические рекомендации по диагностике и лечению тяжелого сепсиса и септического шока в лечебно-профилактических организациях Санкт-Петербурга. – 2016.
4. Гнойно-воспалительные заболевания и сепсис в акушерстве. Клинические рекомендации (протокол лечения)/ Коллектив авторов. – 2015.
Читайте также:

