Септицемия неуточненная что это такое
Обновлено: 12.05.2024
Симптомы сепсиса при ангине и его лечение
Код по МКБ-10: A40.0 - сепсис вызванный стрептококком группы А
Код по МКБ-10: A40.1 - сепсис вызванный стрептококком группы В
Код по МКБ-10: A40.2 - сепсис вызванный стрептококком группы D
Код по МКБ-10: A40.3 - сепсис вызванный пневмотококком
Код по МКБ-10: A40.8 - сепсис вызванный другим стрептококком
Код по МКБ-10: A40.9 - сепсис без уточнения
а) Симптомы и клиника. К клиническим проявлениям тонзиллогенного сепсиса относятся озноб, лихорадка септического типа, болезненность вдоль внутренней яремной вены, которая пальпируется в виде плотного тяжа под передним краем грудино-ключично-сосцевидной мышцы, или болезненность лимфатических узлов яремно-двубрюшной группы. Область нёбных миндалин гиперемирована, однако значение этого признака невелико.
Отмечаются выраженные общие симптомы, такие как лейкоцитоз со смещением лейкоцитарной формулы влево, сухой язык, слабый частый пульс, спленомегалия, а также симптомы, связанные с появлением септических очагов в легких, печени, коже.
б) Причины и механизмы развития сепсиса при ангине. Бактерии попадают в кровь из нёбных миндалин или из расположенного поблизости гнойного очага. Возможны три пути распространения инфекции:
1. Гематогенный, по тонзиллярным венам в лицевую и далее во внутреннюю яремную вену. Развитие тромбофлебита приводит к образованию септических тромбов, фрагменты которых заносятся в легкие и другие органы.
2. Лимфогенный, по эфферентным лимфатическим путям из нёбных миндалин в регионарные лимфатические узлы яремно-двубрюшной группы и вдоль внутренней яремной вены с развитием септического тромбофлебита и далее, как в пункте 1.
3. Per continuitatem, за счет расширения границ воспаления на окружающие ткани окологлоточного пространства и мягкие ткани шеи, включая внутреннюю яремную вену.
Возбудителями тонзиллогенного сепсиса могут быть ряд микроорганизмов. Их можно выявить при посеве крови, взятой на высоте озноба. Возможна смешанная инфекция.
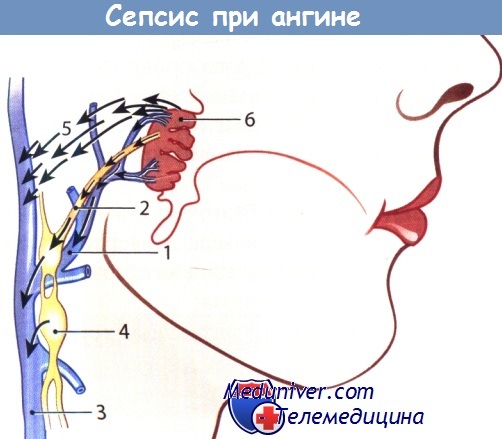
Развитие тонзиллогенного сепсиса:
1 - распространение инфекции по венам; 2 - распространение инфекции по лимфатическим путям;
3 - внутренняя яремная вена; 4 - регионарные лимфатические узлы вокруг внутренней яремной вены;
5 - распространение инфекции по протяжению (per continuitatem) через мягкие ткани шеи на внутреннюю яремную вену; 6 - нёбная миндалина.
в) Диагностика. Диагноз устанавливают на основании клинических проявлений бактериемии (озноб и симптомы септицемии), эпизодов острого или обострения хронического тонзиллита или эпизодов острого тонзиллита в анамнезе, быстрого повышения СОЭ и количества лейкоцитов в крови, болезненности яремно-двубрюшных лимфатических узлов или внутренней яремной вены, характерного защитного спазма шейных мышц, обусловливающего щадящее положение головы и шеи. Для диагностики прибегают также к посеву крови.
г) Лечение сепсиса при ангине. При подозрении на тяжелый сепсис начинают безотлагательное лечение пенициллином или антибиотиками широкого спектра действия для предотвращения образования септических (метастатических) очагов в отдаленных органах и тканях. После получения результатов бактериологического исследования подбирают соответствующие антибиотики.
К другим обязательным мерам относятся:
1. Тонзиллэктомия для исключения очага инфекции.
2. Перевязка внутренней яремной вены дистальнее уровня тромбоза и резекция пораженного сегмента вены.
3. Широкий разрез и дренирование абсцесса мягких тканей шеи.
д) Течение и прогноз. Тонзиллогенный сепсис - опасное для жизни осложнение тонзиллита, однако при своевременном назначении антибактериальной терапии и выполнении хирургического вмешательства прогноз благоприятный.
P.S. При первом же подозрении на тонзиллогенную септицемию с повторными ознобами следует срочно выполнить тонзиллэктомию и назначить массивные дозы антибиотиков. Развитие сепсиса говорит об иммунодефиците.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Септицемия на языке медиков обозначает заражение крови. Болезнь возникает из-за попадания в кровоток болезнетворных микроорганизмов. Распространение микробов может начаться из любого источника воспаления – раны на коже, инфекционных поражений органов или тканей. Наиболее подвержены септицемии маленькие дети, так как иммунная система у них находится на стадии формирования и инфекция из органа может легко проникнуть в кровеносное русло.
При септицемии больного беспокоит высокая температура, лихорадка, возникает бред, развивается дыхательная недостаточность, тахикардия. Заболевание отличается стремительным развитием, поэтому важную роль здесь играют своевременное выявление и адекватная терапия.

[1], [2], [3], [4], [5], [6], [7], [8], [9]
Код по МКБ-10
Причины септицемии
Причиной возникновения септицемии являются болезнетворные микробы – в большинстве случаев это бактерии, но вызвать заболевание могут также грибки, вирусы и другие условно-патогенные микроорганизмы.
Микробы могут проникать в организм через рот, открытые ранки на теле, различные очаги воспаления (например, при гайморите, отите, воспалении почек и т.д.). В большинстве случаев иммунная система справляется с патогенными микроорганизмами, но при попадании в кровеносное русло сразу большого количества бактерий (что часто происходит в запущенных стадиях гайморита, отита, цистита и пр.) иммунитет не в состоянии противостоять и начинается заражение крови со всеми вытекающими последствиями.
Часто септицемия является тяжелым осложнением инфекционных заболеваний.
Вместе с бактериями в кровь попадают продукты их жизнедеятельности – отравляющие вещества, которые, собственно, и становятся причиной поражения тканей, органов, токсического шока, нарушения работы систем организма, что в конечном итоге может привести к смерти больного.

[10], [11], [12], [13], [14], [15], [16], [17], [18], [19]
Симптомы септицемии
Как уже упоминалось, данное состояние отличается стремительным развитием, поэтому распознавание первых признаков болезни поможет начать своевременное лечение и тем самым спасти жизнь человеку.
Для начала заболевания характерны типичные симптомы простуды – общая слабость, температура, отказ от еды, озноб. Со временем могут появиться понос или рвота, характерные для кишечной инфекции.
Далее появляется учащенное дыхание, тахикардия.
Состояние при септицемии быстро ухудшается, токсины в крови повреждают кровеносные сосуды, что приводит к подкожным кровоизлияниям, проявляющимися в виде высыпаний на коже. Вначале сыпь похожа на маленькие точки, но довольно быстро на коже образуются крупные синие участки. Заболевание прогрессирует стремительными темпами и в некоторых случаях высыпания меняют свой характер прямо на глазах.
При сильной интоксикации появляются бредовые состояния, потеря сознания.
Септикопиемия является одной из форм заражения крови, для которой характерно появление гнойников на различных органах и тканях организма. Заболевание проявляется умеренно и протекает без ярковыраженных симптомов. Основной причиной развития септикопиемии являются синегнойная палочка и стафилококк.
Ряд специалистов считают заболевание второй стадией септицемии. Однако, развитие септикопиемии во многом зависит от состояния иммунной системы и способности организма противостоять болезнетворным микробам, поэтому данное состояние не всегда заканчивается появлением вторичных гнойниковых образований.
Бактериальная септицемия или бактериальный эндокардит является особой формой заражения крови, для которой характерны гнойники на сердечных клапанах и повышенная реакция организма на интоксикацию.
Чаще всего причиной развития этой формы болезни становятся энтерококки и стафилококки (белый, зеленящий, золотистый), реже – протеи, клебсиеллы, синегнойная и кишечная палочки.
Бактерии выделяют в кровеносное русло токсины, в ответ иммунная система образует антитела, что может вызвать повышенную реакцию организма.
Выделяют несколько форм данной формы заболевания – острая, подострая, хроническая.
При заболевании обычно поражаются клапаны аорты, реже наблюдается поражение митрального клапана, также возможны изменения септического характера одновременно в двух клапанах.
Кроме этого наблюдается поражение внутренних органов и систем – увеличение селезенки, поражение сосудов, почек, суставов и пр.
Характерными симптомами являются кровоизлияния в нижнее веко, под кожу, появление узелков на ладонях, некроз подкожной клетчатки, утолщение фаланг пальцев (симптом барабанных палочек).
Возбудителем диплококковой септицемии является диплококк. Заражение крови сопровождается воспалительными процессами в легких, суставах, кишечнике.
Выделяют несколько видов диплококков – гонококки, менингококки, пневмококки, внеклеточные диплококки.
Данная форма болезни развивается крайне редко у человека, обычно заболеванию подвержен мелкий и крупный рогатый скот (ягнята, телята), лошади, поросята. Смертность в результате диплококковой септицемии составляет до 70%.
Стрептококки являются самыми распространенными возбудителями инфекционных заболеваний у человека. Стрептококковая септицемия может быть вызвана бактериями различных групп – стрептококки А, В, D, Streptococcus pneumoniae.
Данная форма болезни часто является осложнением инфекционных болезней, вызванных стрептококками – ангина, отит, пневмония, менингит и т.д.
Вирусная геморрагическая септицемия - более редкая форма заражения крови, встречающаяся у человека. Болезнь провоцируют вирусы, проникающие в кровоток.
Заболевание приводит к поражению всех органов и систем, и кровоизлияния под кожей или на слизистых оболочках.
Септицемия неуточненная является общим понятием, которое включает различные заболевания неустановленной этиологии – грибковый сепсис, бактериемия стафилококковая, токсико-инфекционный шок.
Данный диагноз ставится, если невозможно определить точный тип микроорганизмов, вызвавших заражение крови. Смертность в данном случае может достигать 90%, в некоторых случаях наблюдается стремительное развитие болезни, когда смерть может наступить через несколько часов.
Диагностика септицемии
Диагноз устанавливается по типичным признакам заражения крови, который подтверждается лабораторными исследованиями.
Для выявления возбудителя септицемии назначается посев крови. При этом анализ должен делаться несколько раз подряд, так как микроорганизмы имеют определенный жизненный цикл, а назначенное лечение может значительно изменить количество бактерий в кровеносном русле и состав крови.
Помимо крови исследуется отделимое из очага воспаление, что также поможет определить тип возбудителя.
При определении типа микробов проводится анализ на восприимчивость к антибиотикам.
Также стандартной процедурой является общий и биохимический анализ крови, мочи. Помимо этого может быть назначено УЗИ брюшной полости, грудной клетки и пр.

[20], [21], [22], [23], [24], [25]
К кому обратиться?
Лечение септицемии
Лечение должно происходить только в стационаре в отделении интенсивной терапии или реанимации.
Лечение основано на тех же принципах, что и терапия инфекционных заболеваний, однако при выборе препаратов учитываются состояние пациента и высокий риск летального исхода.
При септицемии используют антибиотики (при выборе учитывается чувствительность микроорганизмов), препараты для снижения интоксикации (гемосорбция, УФ-облучение крови, плазмаферез и пр.), повышения иммунитета, при необходимости назначают средства, корректирующие нарушенные процессы в организме.
Больному необходим максимальный покой, диетическое питание (пациентам в тяжелом состоянии вводятся питательные растворы внутривенно).
Очень важным моментов в лечении является очищение первичного очага инфекции, для этого часто используются антибиотики из разных групп, в некоторых случаях дополнительно назначается гормональная терапия.
При сильной интоксикации пациенту внутривенно вводятся гамма-глобулин, плазма, раствор глюкозы.
При выявлении вторичных гнойников назначается срочное оперативное лечение – вскрытие и очищение гнойников, промывание гнойных ран, иссечение пораженных участков.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Сепсис новорожденных - генерализованная форма гнойно-воспалительной инфекции, вызванной условно-патогенной бактериальной микрофлорой, патогенез которой связан с дисфункцией иммунной системы (преимущественно фагоцитарной) с развитием неадекватной системной воспалительной реакции (СВР) в ответ на первичный септический очаг.
Системная воспалительная реакция - общебиологическая неспецифическая иммуноцитологическая реакция организма в ответ на действие повреждающего эндогенного или экзогенного фактора. В случае развития инфекции СВР возникает в ответ на первичный гнойно-воспалительный очаг. Для СВР характерно бурное нарастание продукции провоспалительных (в большей степени) и противовоспалительных (в меньшей степени) цитокинов, неадекватное действию повреждающего фактора, что индуцирует апоптоз и некроз, обусловливая повреждающее действие СВР на организм.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Код по МКБ-10
Эпидемиология сепсиса новорожденных
В отечественной литературе нет достоверных данных о частоте инфекции среди новорождённых, что в значительной степени связано с отсутствием общепринятых диагностических критериев диагноза. По зарубежным данным, частота септических состояний среди новорождённых составляет 0,1-0,8%. Особый контингент больных - дети, находящиеся в отделениях реанимации и интенсивной терапии (ОРИТ), а также недоношенные новорождённые, среди них частота развития данного заболевания в среднем составляет 14%.
В структуре неонатальной смертности септические состояния составляет в среднем 4-5 на 1000 живорождённых. Показатели летальности от инфекции крови также довольно стабильны и составляют 30-40%.

[11], [12], [13], [14], [15]
Чем вызывается сепсис новорожденных?
Септическое состояние обусловлен исключительно условно-патогенной микрофлорой. В ряде случаев, например при иммунодефиците новорождённого, инфекция крови может быть составной частью генерализованной смешанной инфекции - вирусно-бактериальной, бактериальногрибковой и т.д.
Причиной данного заболевания у детей могут стать свыше 40 условно-патогенных микроорганизмов, но чаще всего инфекция крови обусловлен стрептококками, стафилококками, кишечной палочкой, клебсиеллой и другими грамотрицательными бактериями и анаэробами.
Этиологическая структура сепсиса новорождённых зависит от времени инфицирования плода и новорождённого.
Ранний (врождённый) неонатальное септическое состояние чаще всего обусловлен грамположительными кокками S. agalacticae относящимися к стрептококкам группы В. Данный возбудитель может быть причиной антенатального и интранального инфицирования плода;
Наиболее вероятная этиология раннего сепсиса новорождённых в зависимости от времени инфицирования плода и новорождённого
S. agalacticae
E. coli (редко)
S. agalacticae
E. coli
S. aureus
S. aureus et epidermidis
E. coli
Klebsiella spp.
S. pyogenes
E. coli и другие представители семейства кишечных грамотрицательных бацилл вызывают инфицирование плода значительно реже.
Поздний неонатальный сепсис новорожденных обычно возникает вследствие постнатального инфицирования. Основные возбудители - E. coli, S. aureus и Klebsiella pneumoniae; стрептококки группы В встречаются редко. Возрастает значение стрептококков группы А, псевдомонад и энтерококков.
В структуре грамотрицательных возбудителей данного заболевания, составляющих около 40%, в течение последних 10 лет произошли некоторые изменения. Возросла роль Pseudomonas spp. Klebsiella spp. и Enterobacter spp. Как правило, эти возбудители вызывают инфекцию крови у пациентов ОРИТ, находящихся на искусственной вентиляции лёгких (ИВЛ) и парентеральном питании, хирургических больных.
На этиологическую структуру постнатальной заболеваемости существенное влияние оказывает локализация первичного септического очага. Например, в этиологии пупочного вида инфекции ведущую роль играют стафилококки и E. coli, а в этиологии кожного и риноконъюнктивального септического состояния - стафилококки и ß-гемолитические стрептококки группы А. Также спектр возбудителей госпитальной инфекции зависит от входных ворот инфекции. Например, при катетеризационном септическом состоянии преобладающую роль играют стафилококки или смешанная генерализованная инфекция, обусловленная ассоциацией стафилококков с грибами рода Candida. При абдоминальном госпитальной инфекции часто выделяют энтеробактерии, анаэробы.
Наиболее вероятные возбудители сепсиса новорождённых в зависимости от локализации первичного очага инфекции
Локализация первичного очага
Наиболее вероятные возбудители
S. aureus et epidermidis
E. coli
K. pneumoniae
S. aureus et epidermidis Ps. aeruginosa (при ИВЛ)
Acinetobacter spp. (при ИВЛ)
Enterobacteriaceae spp.
Enterobacter spp.
Брюшная полость (после хирургических вмешательств)
Enterobacteriaceae spp.
Enterococcus spp.
Ps. aeruginosa
Анаэробы
Кожа, риноконъюнктивальная область
S. epidermidis et aureus
S. pyogenes et viridans
Ротоглотка и носоглотка, среднее ухо
S. epidermidis et aureus
S. pyogenes et viridans E. coli
E. coli и другие виды семейства Enterobacteriaceae Enterococcus spp.
Венозное русло (после применения внутривенного катетера)
S. aureus et epidermidis
Этиология генерализованных инфекций у иммунокопрометированных пациентов (в том числе у глубоко незрелых новорождённых) также имеет ряд особенностей и зависит от характера иммуносупрессии (приобретённые дисфункции иммунной системы, вторичная иммунная недостаточность, медикаментозная иммуносупрессия, врождённая, наследственная или приобретённая нейтропения, первичные иммунодефициты и ВИЧ-инфекция). Далеко не всегда инфекцией, развивающейся на таком фоне, бывает именно сепсис новорождённых.
Патогенез сепсиса новорожденных
Пусковой момент заболевания - наличие первичного гнойного очага на фоне изначальной несостоятельности противоинфекционной защиты. В этой ситуации массивное микробное обсеменение, превосходящее возможности противомикробной защиты, приводит к прорыву инфекционного начала в системный кровоток больного (бактериемия).
Наиболее вероятные возбудители генерализованных инфекций при иммунодефицитах у младенцев
Наиболее вероятные возбудители
Вторичные иммунные дисфункции, включая дисфункции при гестационной незрелости
Enterobacteriaceae spp.
Staphylococcus spp.
S. pyogenes
Грибы рода Candida
Цитомегаловирус
Enterobacteriaceae spp.
S. Aureus
Грибы рода Aspergillus et Candida
S. aureus E. coli
Грибы рода Candida
Оппортунистическая микрофлора (грибы, микобактерии, цитомегаловирус и т.д.)
Enterobacterioceae spp.
S. aureus et epidermidis Гемолитические стрептококки группы А
Помимо описанного выше, нейтрофилы играют роль фагоцитов. Значимость фагоцитоза, осуществляемого нейтрофилами и макрофагами, существенно различается - истинный фагоцитоз осуществляют именно макрофаги. Нейтрофильный фагоцитоз, хотя и протекает более интенсивно, чем у мононуклеаров, обусловлен другими биохимическими процессами, потому что задача у них иная. Основная функция нейтрофилов - инициация воспалительной реакции. Биологически активные вещества, секретируемые нейтрофильными гранулоцитами, имеют провоспалительную направленность; среди них различают цитокины, работающие в очагах острого воспаления (ИЛ-8, ИЛ-1, фактор некроза опухоли, гранулоцитарно-макрофагальный колониестимулирующий фактор и гранулоцитарный колониестимулирующий фактор) и участвующие в регуляции хронического воспаления (ИЛ-6, у-интерферон, трансформирующий фактор роста). Нейтрофилы синтезируют широкий спектр поверхностных адгезивных молекул, с помощью которых они взаимодействуют с клетками эндотелия сосудов, иммунной системы, тканей и органов. В результате адгезии изменяется чувствительность самих нейтрофилов к цитокинам и другим медиаторам, что позволяет им адекватно реагировать на изменения в тканях и органах. Цитотоксичность нейтрофилов значительно выше, чем у киллерных лимфоидных клеток (Т-лимфоцитов) и натуральных киллеров (NК-клеток). Факторы цитотоксичности нейтрофилов нацелены на ядерные структуры клеток-мишеней, структурные элементы генетического аппарата поглощённого объекта, разрушение генома с использованием факторов, индуцирующих апоптоз (ФИА). Клетки, подвергающиеся апоптозу, становятся объектами фагоцитоза и быстро разрушаются.
Нейтрофилы активно фагоцитируют микроорганизмы, не заботясь об истинном их переваривании, выбрасывают в межклеточное пространство значительные количества ФИА, чтобы как можно быстрее вызвать повреждения генетического аппарата патогенных микроорганизмов. Влияние высвобождения содержимого нейтрофильных гранул на процессы воспаления огромно. Содержимое нейтрофильных гранул индуцирует агрегацию тромбоцитов, выход гистамина, серотонина, протеаз, производных арахидоновой кислоты, активаторов свёртывания крови, системы комплемента, кинин-каллекреиновой системы и др. ФИА нейтрофилов губительны для любых клеток, так как вызывают разрушение нуклеопротеиновых комплексов генома.
Таким образом, в условиях инфекционного процесса нейтрофилы инициируют СВР, участвуют в презентации антигена возбудителя для активации специфического иммунного ответа организма. При чрезмерной активации нейтрофилов их цитотоксическое действие не ограничивается чужеродными клетками, реализуясь в отношении собственных клеток и тканей организма.
Чрезмерная СВР лежит в основе гиперактивации гипоталамо-гипофизарно-надпочечниковой системы, в норме обеспечивающей адекватную реакцию организма на стресс. Активация этой системы приводит к выбросу АКТГ и повышению содержания кортизола в крови. Чрезмерная активация гипоталамо-гипофизарно-надпочечниковой системы при септическом шоке, молниеносном течении данного заболевания приводит к неадекватной реакции на выброс АКТГ. Наряду с этим значительно снижается функциональная активность щитовидной железы, с чем связано замедление окислительного метаболизма, ограничивающее адаптивные возможности организма новорождённого. При тяжёлом септическом состоянии (молниеносное течение, септический шок) у ряда больных падает содержание соматотропного гормона (СТГ). Низкое содержание СТГ в условиях базальной гиперкортизолемии способствует бурному развитию некротических процессов (СТГ тормозит воспалительный процесс).
Другое проявление неадекватной СВР - неуправляемая активация свёртывающей системы крови, в условиях нарастающей депрессии фибринолиза неизбежно приводящая к тромбоцитопатии и коагулопатии потребления.
Таким образом, СВР, индуцированная чрезмерной активацией нейтрофилов периферической крови, активацией гипоталамо-гипофизарно-надпочечниковой системы и системы гемостаза, лежит в основе формирования полиорганной недостаточности, приводящей к глубоким расстройствам гомеостаза, иногда несовместимым с жизнью.
Для мононуклеаров нейтрофилы - клетки-помощники. Основная роль моноцитов и макрофагов - истинный фагоцитоз с дальнейшим тщательным перевариванием полуразрушенных нейтрофилами частиц клеток-мишеней, самих нейтрофилов и воспалительного клеточного дендрита. Фагоцитоз, осуществляемый макрофагами, способствует стиханию процессов воспаления и заживлению повреждённых тканей.
Формирование медиаторного ответа на бактериальную инфекцию, лежащего в основе синдрома СВР, - генетически контролируемый процесс, в котором участвуют рецепторы клеток, распознающие различные структуры микробного происхождения и индуцирующие экспрессию факторов неспецифической резистентности.
Синдром СВР лежит в основе прогрессирующей органной дисфункции, в ряде случаев достигающей степени органной недостаточности. Для патогенеза септического состояния характерно стремительное развитие полиорганной недостаточности и глубокие расстройства гомеостаза. Один из признаков нарушения гомеостаза при инфекции крови - выраженная пролиферация условно-патогенной микрофлоры, создающая предпосылки для возникновения новых инфекционных очагов и дополнительной транслокации инфекционного начала в системный кровоток. В настоящее время популярна концепция, согласно которой нарушения гомеостаза связаны с попаданием в кровь эндотоксина или липополисахаридного комплекса эндотоксина грамотрицательных бактерий, бурно колонизирующих верхние отделы тонкого кишечника в условиях тканевой гипоксии. Эндотоксин значительно усиливает СВР, провоцирует нарушения гомеостаза, рефрактерную к лечению гипотензию. Поступление в кровоток антигенов приводит к дезорганизации СВР - медиаторному хаосу. Антигенная перегрузка - причина выраженной иммуносупрессии в условиях бактериемии и нарушения микроциркуляции, способствующая формированию метастатических гнойных очагов, поддерживающих СВР, токсинемию и антигенемию. Дезорганизация СВР - основа развития септического шока.
Симптомы сепсиса новорождённых
Симптомы сепсиса новорожденных, независимо от формы (септицемия или септикопиемия), характеризуются тяжесть общего состояния новорождённого. Выражены нарушения терморегуляции (у доношенных морфофункционально зрелых новорождённых - лихорадка, у недоношенных, маловесных детей, на отягощённом преморбидном фоне - прогрессирующая гипотермия), нарушено функциональное состояние ЦНС (прогрессирующее угнетение). Характерен грязновато-бледный или сероватый оттенок кожных покровов с желтушностью и геморрагиями, участками склеремы. Выражена мраморность кожи, возможен акроцианоз. Рано возникает и быстро нарастает желтуха. Нередко развивается общий отёчный синдром. Характерна склонность к спонтанной кровоточивости. Черты лица нередко заострены.
Дыхательная недостаточность развивается без воспалительных изменений на рентгенограмме, часто происходит повреждение сердца по типу токсической кардиопатии, сопровождающееся развитием острой сердечной недостаточности. Характерно увеличение размеров селезёнки и печени, вздутие живота, выражена венозная сеть на передней брюшной стенке, часто наблюдаются срыгивания, рвота и анорексия, дисфункция желудочно-кишечного тракта вплоть до пареза кишечника. Типично отсутствие прибавки массы тела, формирование гипотрофии.
Для недоношенных детей типично подострое течение данного заболевания в виде синдрома дыхательных расстройств (одышка с периодами брадипноэ или апноэ), брадикардии, нарушения сосательного рефлекса, тенденции к гипотермии. Перечисленные симптомы сепсиса новорожденных отражают различные степени развития полиорганной недостаточности. Наиболее типичные синдромы полиорганной недостаточности при инфекции крови, а также характерные для них изменения, обнаруживаемые при лабораторных и инструментальных методах обследования, отражены в таблице.
Первичный септический очаг
Как было отмечено выше, изучая клиническую картину заболевания при позднем сепсисе новорождённых, в большинстве случаев можно обнаружить первичный септический очаг.
После внедрения первичной хирургической обработки пуповинного остатка произошло снижение частоты возникновения омфалита; в настоящее время эти заболевания встречаются не более чем в трети случаев. На этом фоне значительно возросла частота развития лёгочного (до 20-25%) и кишечного септического состояния (не менее 20%). Другие локализации первичного очага встречаются значительно реже и не превышают 2-6%. В отдельных случаях входные ворота инфекции установить не удаётся. Это особенно характерно для детей с малым гестационным возрастом, у которых слабо выражены процессы альтерации.
Клинические и лабораторные критерии органной недостаточности при септическом состоянии (Балк Р. и др., 2001, в модификации)
Септицемия - сепсис: причины, диагностика, лечение
Этиология септицемии. Причиной бактериемии могут быть представители нормальной микрофлоры организма, которые становятся патогенными при некоторых состояниях (зубной абсцесс, холецистит, аппендицит, дивертикулит и др.). Послеоперационную хирургическую септицемию могут вызывать различные микроорганизмы, включая представителей нормальной микрофлоры кожи.
Решение этой проблемы играет особенно важную роль при протезировании (ортопедическом, сердечно-сосудистом, нейрохирургическом и др.). Инфекции мочевыводящих путей в основном вызывают грамотрицательные бактерии. Пневмонию может сопровождать бактериемия, вызванная штаммами Streptococcus pneumoniae, а кожные инфекции — бактериемия, вызванная Streptococcus pyogenes или Staphylococcus aureus. Септицемия, вызванная Neisseria meningitidis или Streptococcus pneumoniae, может сопровождаться развитием менингита.
Клинические признаки септицемии. Парадоксально, но септицемия, обычно сопровождаемая высокой температурой и шоковым состоянием с потерей сознания, может протекать бессимптомно. Лихорадка может отсутствовать у детей и пожилых людей, а до возникновения шока пациенты могут находиться в сознании и жаловаться лишь на сонливость и общее недомогание.
Шок, вызываемый грамположительными и грамотрицательными бактериями, клинически дифференцировать невозможно. Инфекциям, обусловленным некоторыми микроорганизмами, свойственны определённые симптомы (геморрагическая сыпь при инфекции, вызванной N. meningitidis).
Диагностика и лечение септицемии. До начала лечения (за исключением инфекции, вызванной N. meningitidis) необходимо сделать посев как минимум двух образцов крови пациента. Цель дальнейшего обследования (посев мочи, спинномозговой жидкости, ультразвуковое исследование органов брюшной полости, посев мокроты и соскобов с кожи и др.) — определение источника сепсиса. Рентгенологическое исследование грудной клетки и брюшной полости должны быть выполнены.
Эмпирическая этиотропная терапия, направленная на тот спектр микроорганизмов, с которыми наиболее вероятно связан очаг инфекции, должна быть начата немедленно. Антибактериальная терапия должна проводиться с парентеральным введением препаратов.
Послеродовый сепсис
Причина этого тяжёлого заболевания, обычно протекающего с бактериемией, — микроорганизмы, проникающие в организм через плацентарное ложе или шейку матки в течение семи дней после родов. Возбудителями могут быть как патогенные бактерии, проникающие в организм при хирургических манипуляциях (S. pyogenes), так и представители нормальной микрофлоры, такие, как Bateriodes (особенно при наличии остаточных частей плаценты).
Инфекция сопровождается лихорадкой, болями в спине, выделением лохий с неприятным запахом, шоком и синдромом диссеминиро-ванного внутрисосудистого свёртывания. При возникновении лихорадки в раннем послеродовом периоде необходимо выполнить посев крови, мочи, а также микроскопическое исследование маточных мазков.
Очень важно начать незамедлительную эмпирическую парентеральную терапию цефалоспоринами третьего поколения и метронидазолом либо комплексное лечение пиперациллином и тазобактамом. Кроме того, необходимо удалить из матки остатки плаценты. В некоторых случаях может потребоваться интенсивная терапия.
Видео патофизиология сепсиса
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Септицемия у детей. Клиника, лечение
Бактерия может вызвать очаговую инфекцию или пролиферировать в кровяном русле, вызывая септицемию. В ответ на септицемию в организме-хозяине повышается содержание воспалительных цитокинов и активируются эндотелиальные клетки, что может вызвать септический шок. Самой частой причиной септического шока у детей является менингококковая инфекция, которая может сопровождаться менингитом. К счастью, его заболеваемость в Великобритании значительно снизилась в связи с проведением иммунизации. Pneumococcus — самый частый микроорганизм, вызывающий бактериемию, для него не характерно развитие септического шока. У новорождённых наиболее частой причиной септицемии является стрептококк группы В или грамотрицательные бактерии родового канала.
Клинические проявления септицемии:
• Анамнез.
Лихорадка.
Недостаточное питание.
Низкий социальный статус.
Летаргия.
Фокальная инфекция в анамнезе. Например, менингит, остеомиелит, гастроэнтерит, целлюлит. Предрасположенность к заболеваниям, например СКА, иммунодефицит.
• Осмотр.
Лихорадка.
Сыпь пурпурного цвета (менингококковая сыпь).
Возбуждение.
Шок.
Полиорганная недостаточность.

Принципы лечения септицемии
Детей с септическим шоком следует срочно стабилизировать и перевести в отделение интенсивной терапии.
Антибиотики. Выбор зависит от возраста ребёнка и предрасположенности к инфекции.
Жидкости. Часто наблюдается значительная гиповолемия в связи с нарушением распределения жидкости, обусловленным выделением вазоактивных медиаторов иммунными и эндотелиальными клетками организма-хозяина. На фоне повышенной проницаемости капилляров, вызванной дисфункцией эндотелиальных клеток, происходит потеря внутрисосудистых белков и жидкости. Часть циркулирующей плазмы проникает в интерстициальную жидкость. Для оценки водного баланса может потребоваться мониторинг центрального венозного давления и катетеризация мочевого пузыря. Повышенная проницаемость легочных капилляров может привести к отёку лёгких, приводящему к дыхательной недостаточности и необходимости ИВЛ.
Стабилизация кровообращения. Поскольку воспалительные цитокины и циркулирующие токсины угнетают сократительную способность миокарда, развивается его дисфункция.
Диссеминированное внутрисосудистое свёртывание. Нарушение образования тромбов вызывает генерализованный микрососудистый тромбоз с потреблением факторов свёртывания. При кровотечении нарушение в системе свёртывания крови должно быть компенсировано переливанием свежезамороженной плазмы и тромбоцитарной массы.
Стероидные гормоны. Эффективность глюкокортикоидов при септическом шоке не доказана.
Септицемия:
• Самая частая причина септического шока у детей — менингококковая инфекция.
• Может протекать без менингита.
• Жизненно важным считают раннее начало антибактериальной терапии и восполнение жидкости в организме.
• При полиорганной недостаточности необходима госпитализация в детское отделение интенсивной терапии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

