Синдром мальабсорбции при вич
Обновлено: 26.04.2024
Категории МКБ: Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других состояний (B23), Болезнь, вызванная вирусом иммунодефицита человека [вич], неуточненная (B24), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других уточненных болезней (B22), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде злокачественных новообразований (B21), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде инфекционных и паразитарных болезней (B20), Острый ВИЧ-инфекционный синдром (B23.0)
Общая информация
Краткое описание
ВИЧ-инфекция - инфекционная болезнь, развивающаяся в результате многолетнего персистирования в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (далее - ВИЧ), характеризующаяся медленно прогрессирующим дефектом иммунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (далее - СПИД) [1].
B20 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде инфекционных и паразитарных болезней;
B21 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде злокачественных новообразований;
B22 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других уточненных болезней;
Пользователи протокола: инфекционисты, терапевты, врачи общей практики, клинической лабораторной диагностики, фтизиатры.
Класс I - польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III - имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
Классификация
• нейтропения (
• хронический герпес (оролабиальный, генитальный или аноректальный длительностью более месяца или висцеральный любой локализации);
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
• число лимфоцитов CD4 (абсолютное и процентное содержание) - двукратное измерение с интервалом не менее 7 дней;
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: не проводится.
Заболевание начинается постепенно.
• половые контакты (гетеро- или гомосексуальные; тип контактов: оральный, вагинальный, анальный) с ВИЧ-статус партнерами (если известно);
• патологическое увеличение лимфатических узлов, персистирующая генерализованная лимфоаденопатия.
Ротоглотка: стоматит, язвенно-некротические поражения, разрастание слизистой полости рта, преимущественно боковой поверхности языка.
Мочеполовая система и перианальная область: признаки следующих заболеваний: нефропатия, инфекция, вызванная вирусом папилломы человека (остроконечные кондиломы половых органов и заднего прохода, рак шейки матки).
Неврологический и психический статус: нарушение когнитивных функций (Приложение 1), парезы, симптомы нейропатии, нарушение сознания, менингеальные синдром.
Биохимический анализ крови: повышение уровня креатинина и мочевины в крови, гипонатриемия, гипокалиемия (при развитии ОПП).
• полимеразная цепная реакция РНК ВИЧ: определяемая вирусная нагрузка.
МРТ/КТ головного мозга: отек головного мозга, признаки менингоэнцефалита, дисциркуляторная энцефалопатия, объемные процессы;
• консультация невропатолога: при признаках/подозрении на криптококковый менингит, ВИЧ-энфефалопатию, токсоплазмоз ЦНС, ПМЛ, лимфомы головного мозга, периферической полинейропатии;
• консультация психиатра: при признаках/подозрении психического расстройства. ВИЧ-энцефалопатии/деменции;
Дифференциальный диагноз
Дифференциальный диагноз: проводится с оппортунистическими инфекциями и другими вторичными заболеваниями по результатам консультаций специалистов.
Лечение
Курс лечения АРТ – пожизненный, применяется тройная схема, кратность приема АРВ препаратов зависит от формы выпуска.
• эмтрицитабин (FTC) 200 мг, капсула; 200 мг 1 раз в сутки.
• рилпивирин* (RPV) 25 мг таблетка; 25 мг 1 раз в сутки.
• дарунавир (DRV) 400 мг, 600 мг, 800 мг таблетка; 600 мг 2 раза в сутки в комбинации с ритонавиром в дозе 100 мг 2 раза в сутки;
• типранавир* (TPV) 250 мг капсула; применяется усиленный ритонавиром, 2 раза в сутки 500 мг+200 мг ритонавира.
ИИ с целью: блокирования фермента ВИЧ, участвующий во встраивании провирусной ДНК в геном клетки-мишени.
• долутегравир (DTG) 50 мг таблетка; 50 мг 1 раз в сутки.
• элвитегравир 150 мг/кобицистат 150 мг /эмтрицитабин 200 мг /тенофовир 300 мг* 1 таблетка 1 раз в сутки;
* При регистрации в Республике Казахстан.
В приоритетном порядке АРТ назначается всем пациентам в 3-4 стадии ВИЧ-инфекции или пациентам с количеством CD4+ лимфоцитов ≤ 350 кл/мкл.
− ВИЧ-позитивным лицам в дискордантных парах (для снижения риска трансмиссии ВИЧ неинфицированным партнерам), при условии предварительного консультирования обоих партнеров;
− при подготовке ВИЧ-инфицированного пациента к применению вспомогательных репродуктивных технологий.
Схема АРТ состоит не менее, чем из трех антиретровирусных препаратов. Предпочтение отдается комбинированным препаратам в фиксированных дозировках.
b NVP использовать у лиц с низким числом лимфоцитов CD4 (у женщин с СД4 менее 250/мкл, у мужчин с СД4 менее 400/мкл)
с вместо AZT при умеренной анемии или гранулоцитопении (уровень гемоглобина> 90 г/л или количество нейтрофилов> 1000 клеток/мкл) рекомендуется назначать ABC, или TDF, а при более выраженной анемии или гранулоцитопении – АВС или TDF.
d использование комбинированного препарата фиксированной дозировки DRV/c (при регистрации)
При невозможности использования вышеперечисленных препаратов ddI может быть назначен в качестве НИОТ в комбинации 3TC/FTC +EFV.
• пациенты, получающие противотуберкулезные препараты.
− при количестве CD4+ лимфоцитов от 50 до 250 клеток/мкл и нормальном уровне АЛТ или АСТ – NVP в сочетании с АВС, или TDF, или AZT + 3ТС, или FTC;
− при любом количестве CD4+ лимфоцитов – LPV/r или DRV/r или ATV/r в сочетании с АВС, или TDF, или AZT + 3ТС, или FTC.
Рекомендуемые схемы АРТ: назначается схема из предпочтительных АРВП – 2 НИОТ + 1 ИП/r, или 2НИОТ + 1 ННИОТ, или 2 НИОТ + 1 ИИ.
LPV/r в сочетании с AZT/3TC. В качестве третьего компонента схемы АРТ являются LPV/r в таблетках (400/100 мг 2 раза в сутки).
При непереносимости LPV/r можно использовать (в порядке приоритетности) – DRV/r (600/100 мг 2 раза в сутки), NVP (при CD4 < 250 клеток/мкл и нормальном уровне АЛТ и АСТ). Частота назначения LPV/r и DRV/r – не реже 2 раз в сутки.
При непереносимости LPV/r и DRV/r, можно назначить ATV/r или другие ИП/р. В качестве нуклеозидной основы рекомендуется ZDV/3TC. Применение EFV не рекомендуется в I триместрe беременности.
Для лечения пациентов с низким уровнем CD4+-лимфоцитов рекомендуется применять схемы, включающие бустированный ИП.
В качестве нуклеозидной основы рекомендуется применять комбинацию ABC с 3TC или TDF с 3TC в стандартных дозах (или комбинированный препарат TDF/FTC). Однако у пациентов с ВН более 100 000 копий/мл препараты, содержащие ABC, применять не рекомендуется.
В качестве альтернативы третьим препаратом можно назначить FPV/r из-за минимального влияния на функцию почек либо LPV/r.
ТDF не рекомендуется больным с почечной недостаточностью.
более чем в 2,5 раза выше верхней границы нормы (ВГН) – EFV или RPV (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ < 100000 копий/мл) в сочетании с TDF+3TC или TDF/FTC;
• при уровне активности АЛТ или АСТ более чем в 2,5 раза выше ВГН – DTG, бустированный RTV ИП (DRV/r или LPV/r) в сочетании с TDF+3TC или TDF/FTC.
При снижении числа CD4+ лимфоцитов менее 500 клеток/мкл рекомендуют начать АРТ одновременно с терапией ХГС.
При количестве CD4+лимфоцитов менее 350 клеток/мкл начинают лечение ВИЧ-инфекции, а затем присоединяют терапию ХГС.
Не рекомендуется сочетание рибавирина с зидовудином (увеличивается частота развития анемии), диданозином (повышается вероятность декомпенсации заболевания печени).
Оптимальным сочетанием НИОТ является TDF + 3TC или FTC в стандартных дозировках. При невозможности применять TDF назначают АВС.
• при нормальном уровне активности АЛТ/АСТ или повышении его не более чем в 2,5 раза выше ВГН – EFV, RPV (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ < 100000 копий/мл) или DTG (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ >100000 копий/мл) в сочетании с АВС или TDF + 3TC или TDF/FTC.
• при уровне активности АЛТ/АСТ более чем в 2,5 раза выше ВГН – DTG или бустированный ИП (LPV/r или DRV/r) в сочетании с АВС или TDF + 3TC или TDF/FTC.
У больных при сочетании ВИЧ-инфекции и ХГС, не получающих лечения ХГС, в состав схемы АРТ может быть включено сочетание ZDV+3TC.
Все ЛЖВ с диагностированным туберкулезом нуждаются в лечении ТБ и ВИЧ-инфекции, независимо от числа лимфоцитов CD4.
Первым начинают противотуберкулезное лечение, а затем как можно быстрее (в первые 8 недель лечения) назначают АРТ.
Больным ВИЧ/ТБ, имеющим выраженный иммунодефицит (число лимфоцитов CD4 менее 50 клеток/мкл), необходимо начать АРТ немедленно – в течение первых 2 недель после начала лечения ТБ.
При наличии туберкулезного менингита начало АРТ следует отложить до завершения фазы интенсивной терапии ТБ.
В начале АРТ у больных, получающих противотуберкулезное лечение, предпочтительным ННИОТ является EFV, который назначают вместе с двумя НИОТ.
При отсутствии EFV рекомендована схема лечения - 3TC (или FTC) + ZDV + ABC (или TDF).
В таблице 3 представлены варианты замены антиретровирусных препаратов при развитии нежелательныхэффектов.
Неудача лечения определяется как постоянно выявляемая вирусная нагрузка более 1000 копий/мл по результатам двух последовательных измерений, проведенных с интервалом в 2-4 недели, но не ранее, чем через шесть месяцев после начала использования АРВ-препаратов.
Основные лекарственные средства, имеющие 100% вероятность применения: см пункт Медикаментозное лечение, оказываемое на амбулаторном уровне.
• эмтрицитабин (FTC) 200 мг, капсула;
• рилпивирин* (RPV) 25 мг таблетка;
• дарунавир (DRV) 400 мг, 600 мг, 800 мг таблетка; 600 мг в комбинации с ритонавиром в дозе 100 мг 2 раза в сутки;
• типранавир* (TPV) 250 мг капсула; применяется усиленный ритонавиром, 2 раза в сутки 500 мг+200 мг ритонавира.
• элвитегравир 150 мг/кобицистат 150 мг /эмтрицитабин 200 мг /тенофовир 300 мг* 1 таблетка 1 раз в сутки;
• элвитегравир 150 мг/кобицистат 150 мг* 1 таблетка 1 раз в сутки.
Хирургические вмешательства: нет.
• туберкулеза (при исключении у пациента активного туберкулеза) –однократно изониазид (5 мг/кг), но не более 0,3 г в сутки + пиридоксин (при наличии) в дозе 25 мг/сут не менее 6 месяцев;
• пневмоцистной пневмонии в случае CD4 < 200 клеток/мкл, токсоплазмоза, в случае CD4 < 100 клеток/мкл – котримоксазол (960 мг 3 раза/неделю). Отменить профилактику если у пациента более 3 месяцев количество CD4+ - лимфоцитов стабильно превышает 200 кл/мкл, возобновить при падении количества CD4+ - лимфоцитов
• Диспансерное наблюдение пациентов получающих АРТ осуществляется совместно ПМСП и территориальным центром СПИД с кратностью посещений не менее 1 раза в 3 месяца.
• Вирусная нагрузка определяется перед началом АРТ. В дальнейшем следует измерять ВН первый раз не позднее 3 месяцев, затем 1 раз в 6 месяцев, при достижении неопределяемого уровня ВН.
• В случае отсутствия снижения ВН через 6 месяцев от начала лечения на 1 lоg10 или последовательного двукратного повышения ВН после исходной супрессии, следует провести генотипический тест на определение резистентности ВИЧ к антиретровирусным препаратам.
• Число лимфоцитов CD4 нужно измерять через 3 месяца, затем каждые 6 месяцев, при необходимости чаще в течение 1-го года АРТ, далее не реже 1 раз в год (за исключением случаев неэффективности лечения).
• Лабораторные исследования необходимо проводить не менее одного раза в 6 месяцев.
Таблица 4. Сроки проведения лабораторных исследований
х - лабораторное исследование показано независимо от используемых АРВ-препаратов;
x (АРВ-препарат) - исследование показано пациентам, которые получают указанный в скобках препарат.
b Пациентам с хроническими гепатитами биохимические показатели определяют согласно клиническому протоколу диагностики и лечения хронического вирусного гепатита В и С у взрослых в РК.
Через 3 месяца после начала приема АРВ-препарата клинически проявляющиеся побочные эффекты должны отсутствовать (а также субклинические, которые со временем могут проявиться клинически )
b Вирусная нагрузка уменьшается постепенно: у большинства пациентов (за исключением имеющих изначально высокую вирусную нагрузку) через 24 недели АРТ она должна быть < 50 копий/мл либо демонстрировать выраженную тенденцию снижения до этого уровня.
При расхождении между вирусологическими и иммунологическими показателями, приоритет за вирусологическими.
Число лимфоцитов CD4 необходимо определять каждые 3 месяца, по стабилизации СД4 лимфоцитов на фоне АРТ - 1 раз в 6 месяцев.
Цель АРТ - снижение ВН до неопределяемого уровня (пороговый уровень
При показателях ВН от 200 до 400 коп/мл – развитие резистентности возможно, необходимо усилить работу по соблюдению приверженности к АРТ.
Госпитализация
III степень (тяжелая) - повседневная жизнь существенно нарушена, часто требуется дополнительная помощь близких, медицинская помощь и лечение, возможно в стационаре;
IV степень (крайне тяжелая, жизнеугрожающая) - нормальная повседневная жизнь невозможна, требуется постоянная помощь посторонних, серьезное лечение, чаще всего в стационаре.
Информация
Источники и литература
Информация
5) Трумова Жанна Зиапеденовна – доктор медицинских наук, профессор РГП на ПХВ «Казахский национальный медицинский университет имени С.Д.
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Оценку нарушений познавательной деятельности (когнитивных функций) целесообразно проводить у всех ВИЧ-инфицированных пациентов без отягощающих факторов(тяжелые психиатрические заболевания, злоупотребление психоактивными веществами, в том числе алкоголем, текущие оппортунистические инфекции центральной нервной системы, другие неврологические заболевания) в течение 6 мес. со времени постановки диагноза. Данный подход позволяет точно определить исходные показатели и, соответственно, более точно оценить дальнейшие изменения. Для раннего скрининга когнитивных функций необходимо задать пациенту 3 вопроса (S.Simionietal. AIDS 2009, EACS 2012):
1. Часто ли у Вас бывают случаи потери памяти (например, Вы забываете значительные события, даже самые недавние, назначенные встречи и т.д.)?
Нейропсихологическое обследование должно включать в себя тесты для изучения следующих характеристик познавательной деятельности: слухоречевая и зрительная память, счет, скорость восприятия информации, внимание, , двигательные навыки. (Antinorietal.Neurology, 2007). В случае выявления патологии требуется обследование пациента у невролога, проведение МРТ головного мозга и исследовании спинномозговой жидкости (СМЖ) на вирусную нагрузку и, если есть к тому показания, провести исследование генотипической резистентности к препаратам в двойной пробе СМЖ и плазмы крови. Если у пациента выявлена патология нейрокогнитивных функций на этапе скрининга или при дальнейшем нейропсихологическом обследовании, необходимо рассмотреть возможность включения в схему препаратов, потенциально воздействующих на центральную нервную систему. К ним относятся либо те препараты, проникновение которых в СМЖ было продемонстрировано в исследованиях, проведенных у здоровых ВИЧ-инфицированных пациентов(концентрация выше IC90 у более чем 90% обследуемых пациентов), либо те, для которых доказана краткосрочная (3–6 мес.) эффективность воздействия на когнитивные функции или на снижение ВН на СМЖ, при условии, что оценка проводится в отсутствие каких-либо других совместно принимаемых препаратов или в рамках контролируемых исследований, результаты которых рецензируются экспертами (EACS 2012).
Мальабсорбция – хроническое расстройство процессов переваривания, транспорта и всасывания питательных веществ в тонком кишечнике. Симптомы мальабсорбции включают диарею, стеаторею, боли в животе, гиповитаминоз, похудание, астеновегетативный синдром, нарушение электролитного обмена, анемию. Диагностика синдрома мальабсорбции основана на лабораторных (ОАК, копрограмма, биохимия крови) и инструментальных методах (рентгенография тонкого кишечника, МСКТ, УЗИ брюшной полости). Лечение направлено на устранение причин мальабсорбции, коррекцию витаминной, микроэлементной, белковой и электролитной недостаточности, дисбактериоза.

Общие сведения
Мальабсорбция (нарушение всасывания в кишечнике) – это синдром, характеризующийся набором клинический проявлений (диарея, стеаторея, полигиповитаминоз, похудание), развивающихся вследствие нарушения пищеварительной и транспортной функций тонкого кишечника, что в свою очередь ведет к патологическим изменениям обмена веществ. Врожденный синдром мальабсорбции диагностируется в 10% случаев; его проявления манифестируют вскоре после рождения или в первые 10 лет жизни ребенка. Частота приобретенной мальабсорбции коррелирует с распространенностью причинно значимых заболеваний (гастрогенных, гепатобилиарных, панкреатогенных, энтерогенных и др.).

Классификация
В гастроэнтерологии синдром мальабсорбции классифицируют по степени тяжести:
- первая (легкая) степень (потеря в весе до 10 килограмм, общая слабость, снижение работоспособности и некоторые признаки гиповитаминозов);
- вторая (средней тяжести) степень (похудание более чем на 10 килограмм, выраженный полигиповитаминоз, нарушение водно-электролитного гомеостаза, анемия, снижение уровня половых гормонов);
- третья (тяжелая) степень (значительный дефицит массы тела, тяжелая поливитаминная и электролитная недостаточность, остеопороз, выраженная анемия, отеки, судороги, серьезные эндокринные нарушения).
По происхождению различают:
- Врожденный синдром мальабсорбции (у больных, страдающих врожденными заболеваниями ферментной системы – синдром Швахмана-Даймонда, муковисцидоз, болезнь Хартнупа и другие патологии, связанные с недостаточностью ферментов и нарушением транспорта веществ в клетках слизистой кишечника).
- Приобретенный синдром мальабсорбции (как следствие энтеритов, болезни Уиппла, синдрома короткой кишки, хронического панкреатита, цирроза печени и других приобретенных заболеваний желудочно-кишечного тракта).
Симптомы мальабсорбции
У больных с синдромом мальабсорбции отмечаются изменения со стороны кишечника: диарея, стеаторея, вздутие и урчание, иногда болезненность в животе. Боль, как правило, локализуется в верхней части живота, может иррадиировать в поясницу или иметь опоясывающий характер, если имеет место хронический панкреатит. У больных с недостаточностью лактазы боли схваткообразного характера.
При мальабсорбции количество кала, как правило, заметно увеличено, кал имеет кашеобразную или водянистую консистенцию, зловонный. При холестазе и нарушении всасывания жирных кислот кал приобретает жирный блеск (иногда вкрапления жира) и обесцвечивается (стеаторея). Со стороны нервной системы проявляется астеновегетативный синдром – слабость, утомляемость, апатия. Это связано с нарушением водно-электролитного гомеостаза и недостаточностью необходимых для нервной системы веществ.
Патологические изменения кожных покровов: сухость, пигментные пятна, дерматиты, экзема, выпадение волос, ломкость и помутнение ногтей, экхимозы – связаны с недостаточностью витаминов и микроэлементов. По тем же причинам часто отмечается глоссит (воспаление языка). Недостаток витамина К проявляется образованием петехий (красных точек на коже) и подкожных кровоизлияний.
Осложнения мальабсорбции
Основные осложнения синдрома мальабсорбции связаны с недостатком питательных веществ, поступающих в кровь: анемия (железодефицитная и витаминзависимая мегалобластная), нарушения фертильности, нейровегетативные расстройства, дистрофия, полиорганные патологии, связанные с полигиповитаминозом и недостаточностью микроэлементов.
Диагностика

При синдроме мальабсорбции основные признаки выявляются путем лабораторного исследования крови, кала, мочи. В общем анализе крови могут отмечаться признаки анемии (железодефицитной и В12-дефицитной), недостаточность витамина К влияет на протромбиновое время (происходит удлинение). При биохимическом анализе отмечают уровень альбуминов в крови, кальций и щелочную фосфатазу. Проводится исследование количества витаминов.
Исследование кала показывает увеличение его суточного объема (при голодании – уменьшение). Копрограмма выявляет присутствие в кале мышечных волокон и крахмала. При некоторых ферментных недостаточностях может изменяться рН кала. При подозрении на нарушения всасывания жирных кислот проводят тест на стеаторею.
Перед началом сбора кала для исследования необходимо, чтобы пациент употреблял около 100 грамм жира в сутки на протяжении нескольких дней. Затем собирают суточный кал и определяют количество жира в нем. В норме его не должно быть более чем 7 грамм. Если содержание жиров в кале превышает это значение, можно подозревать мальабсорбцию. При количестве жира более 14 грамм вероятны функциональные нарушения в работе поджелудочной железы. В случае тяжелой степени мальабсорбции и при целиакии с калом выводится половина и более поступивших с пищей жиров.
Функциональные тесты для выявления нарушений абсорбции в тонком кишечнике – D-ксилозный тест и тест Шиллинга (оценка всасывания В12). В качестве дополнительной диагностической меры проводят бактериологическое исследование кала. При рентгенологическом исследовании можно выявить признаки заболевания тонкого кишечника: слепые петли, в некоторых петлях могут образовываться горизонтальные уровни жидкости или газа, видны межкишечные анастомозы, дивертикулы, стриктуры, изъязвления.
При проведении УЗИ брюшной полости, МСКТ и магнитно-резонансной томографии визуализируются органы брюшной полости и диагностируются их патологии, которые могут быть первопричиной развившегося синдрома мальабсорбции. Эндоскопия тонкого кишечника выявляет болезнь Уиппла, амилоидоз и лимфоангиоэктазию кишечника, позволяет произвести забор материала для гистологического исследования, аспирировать содержимое кишечника для бактериологического исследования (на предмет избыточного обсеменения тонкого кишечника микроорганизмами и присутствия патологической флоры).
В качестве дополнительных диагностических мер оценивают состояние внешней секреции поджелудочной железы (секретин-церулеиновый, бентриаминовый, ЛУНД и ПАБК тесты, определение уровня иммунореактивного трипсина); выявляют синдром избыточного бактериального роста (дыхательный водородный и углекислый тесты); диагностируют недостаточность лактазы (лактозная проба).
Лечение мальабсорбции
В терапии синдрома мальабсорбции первоочередной задачей является лечение заболевания, послужившего причиной к развитию данного состояния.
В зависимости от степени тяжести и выраженности клинических симптомов гастроэнтеролог назначает пациенту специальную диету, парентерально вводятся витамины и микроэлементы, электролитные и белковые смеси. Дисбактериоз корректируют с помощью про- и эубиотиков, проводят регидратацию (восстановление утраченной организмом жидкости). Если основное заболевание требует оперативного вмешательства, то больным проводят хирургическое лечение по поводу основной патологии. Операции часто назначают больным, страдающим болезнью Крона, лимфангиэктазией кишечника, болезнью Гиршпрунга, а также тяжелыми осложнениями воспалительных заболеваний кишечника.
Профилактика
Профилактические меры против развития синдрома мальабсорбции должны быть в первую очередь направлены на профилактику заболеваний, способствующих его возникновению – нарушений работы органов пищеварительного тракта, воспалений кишечника, поджелудочной железы, печени, эндокринных расстройств. При врожденных дефектах ферментативной системы профилактическими мерами будут своевременное выявление той или иной ферментной недостаточности и ее медикаментозная коррекция.
Прогноз
Иногда в легких случаях синдром мальабсорбции корректируется с помощью диеты. В остальных случаях прогноз при этом заболевании напрямую зависит от течения основной патологии, выраженности нарушений всасывания и недостаточности поступления веществ в кровь.
Если основной фактор, вызвавший возникновение этого синдрома, устранен, коррекция последствий продолжительной дистрофии может потребовать длительного времени. Прогрессирование мальабсорбции грозит развитием терминальных состояний и может вести к летальному исходу.
Носовые кровотечения у ВИЧ-инфицированных пациентов
Журнал: Российская ринология. 2021;29(4): 189‑193
Актуальность исследования причин, механизмов возникновения, диагностики и лечения носовых кровотечений (НК) у ВИЧ-инфицированных пациентов определяется сравнительно высокой встречаемостью (12% всей патологии уха и верхних дыхательных путей) и трудностью определения лечебной тактики.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Проведение анализа и выявление истинных причин рецидивирующих носовых кровотечений, имеющих диапедезный характер, у ВИЧ-инфицированных пациентов.
ПАЦИЕНТЫ И МЕТОДЫ
РЕЗУЛЬТАТЫ
По результатам анализа крови снижение тромбоцитов до 53,4±53,24 выявлено у 20 (80%) пациентов; снижение CD4 + -лимфоцитов 500 мкл – 1 — у 8 (32%); у 17 (68%) пациентов определялась вирусная нагрузка в среднем 683 180±362 899 копий в 1 мл плазмы. У всех пациентов были диагностированы ВИЧ-ассоциированные заболевания, наиболее частые из них — ВИЧ-ассоциированная иммунная тромбоцитопения (64%), анемия средней и тяжелой степени тяжести (16%), ЦМВ-инфекция (пневмония, эзофагит, колит) (28%), активная ЦМВ-инфекция с полиорганным поражением (28%), грибковое поражение носоглотки (12%). Пациентам проведена патогенетическая и симптоматическая терапия. Всем ранее не лечившимся больным назначена АРТ, а принимающим лечение выполнена его коррекция. Медикаментозное лечение привело к нормализации параклинических показателей и купированию носовых кровотечений.
ЗАКЛЮЧЕНИЕ
Рецидивирующие носовые кровотечения при ВИЧ-инфекции встречаются сравнительно часто и являются следствием ВИЧ-ассоциированных нарушений гемостаза, что необходимо учитывать при определении лечебной тактики. С другой стороны, больные с рецидивирующими носовыми кровотечениями требуют всестороннего обследования с целью уточнения возможных причин таких геморрагий, в том числе исключения ВИЧ-инфекции.
Дата принятия в печать:
Введение
Актуальность исследования причин и лечения носовых кровотечений (НК) у ВИЧ-инфицированных пациентов определяется широким распространением НК, трудностями, связанными с лечением и профилактикой рецидива НК у этой группы пациентов [1]. Как правило, НК удается купировать довольно быстро. Однако в некоторых случаях кровотечения упорно рецидивируют, сопровождаются значительной кровопотерей, представляя реальную угрозу для жизни больного [2].
НК является одной из причин обращения к оториноларингологу лиц, страдающих ВИЧ-инфекцией на всех стадиях развития заболевания: от острой до проградиентной. Удельный вес НК среди общего числа госпитализированных ЛОР-больных варьирует от 5,9 до 37% [3, 4]. По данным стационара инфекционного профиля, около 80% пациентов с ВИЧ-инфекцией имеют патологию ЛОР-органов [5], а 12% из них страдают рецидивирующими НК [6].
В большинстве случаев НК у больных ВИЧ-инфекцией обусловлены наличием ВИЧ-ассоциированного заболевания, в основе которого лежит нарушение кроветворной функции костного мозга в результате миелодисплазии [3] и поражения сосудов слизистой оболочки полости носа [4]. Лечение этой патологии основывается на коррекции гомеостаза, включающей антиретровирусную терапию (АРТ)/коррекцию АРТ и комбинацию глюкокортикоидов (при тяжелых формах), поливалентных иммуноглобулинов и/или препарата иммуноглобулин человека антирезус Rh0(D). При неэффективности консервативного лечения НК у пациентов с ВИЧ-инфекцией показана спленэктомия [7]. До выполнения спленэктомии рекомендуется провести вакцинацию против пневмококковой и менингококковой инфекций (H. influenzae и N. meningitidis), поскольку эти возбудители приводят к острому воспалительному процессу верхних дыхательных путей и жизнеугрожающим состояниям: менингиту, бактериальному эндокардиту, пневмонии [8].
В последнее время обсуждается возможность замены спленэктомии на терапию ритуксимабом, так как было установлено, что вероятность ответа на лечение этим препаратом (повышение уровня тромбоцитов выше 50 000 мкл –1 ) составляет >60% [7]. Заместительная терапия тромбоцитарной массой актуальна лишь в исключительных ситуациях, при угрожающих кровотечениях [9]. Корректировка витаминно-минерального комплекса в рационе питания также является важной составляющей в ведении таких больных [10].
Цель настоящего исследования — изучение механизма возникновения рецидивирующих НК у пациентов с ВИЧ-инфекцией и оценка консервативного лечения этой группы больных, включающего АРТ, иммуноглобулин человека нормальный (Human normal immunoglobuline).
Пациенты и методы
Результаты
Конкурирующие диагнозы у ВИЧ-инфицированных пациентов с рецидивирующим носовым кровотечением
ВИЧ-ассоциированная иммунная тромбоцитопения
Анемия средней и тяжелой степени тяжести
ЦМВ-инфекция (пневмония, эзофагит, колит)
Активная ЦМВ-инфекция с полиорганным поражением
Грибковое поражение носоглотки
Дефицит массы тела >10%
Генерализованный туберкулез в анамнезе
ОРДС (острый респираторный дистресс-синдром)
ОПН (острая почечная недостаточность)
Оментобурсит с разлитым серозным перитонитом
Анемия средней и тяжелой степени, выявленная у 4 пациентов, была связана с предшествующими эпизодами острой кровопотери и истощением эритроцитарного звена. По данным литературы, анемия встречается у 30—40% ВИЧ-инфицированных пациентов [7] и может развиться в результате повреждения ВИЧ-инфекцией энтероцитов и париетальных клеток желудка, что в свою очередь приводит к развитию синдрома мальабсорбции, которая проявляется снижением всасывания микроэлементов. Эрозирование и изъязвление слизистой оболочки желудочно-кишечного тракта приводят к образованию очагов хронических и/или острых кровопотерь, что требует консультации профильных специалистов [20, 21].
У 2 пациентов с саркомой Капоши определялись характерные изменения в виде очерченных синюшных пятен и эрозированных узлов на слизистой оболочке полости носа и носоглотки, а НК у них имело рецидивирующий характер. Наличие саркомы Капоши у этих больных было подтверждено результатами гистологического исследования биопсийного материала (наличие в препаратах щелевидных сосудов, экстравазированных эритроцитов и гиалиновых глобул).
Всем ранее не лечившимся больным была назначена АРТ, а у принимающих лечение пациентов выполнена его коррекция. При назначении АРТ учитывали показатели гемостаза, поскольку некоторые лекарственные препараты, например зидовудин, обладают миелосупрессией, что может дополнительно подавлять процесс гемопоэза [24].
По завершении комплексного лечения у больных ВИЧ-инфекцией с НК произошло увеличение количества тромбоцитов (в среднем до 130±92,04 ·10 12 /л).
Заключение
Таким образом, рецидивирующие НК при ВИЧ-инфекции встречаются сравнительно часто и являются следствием ВИЧ-ассоциированных нарушений гемостаза, что необходимо учитывать при определении лечебной тактики. С другой стороны, больные с рецидивирующими НК требуют всестороннего обследования с целью уточнения возможных причин таких геморрагий, в том числе исключения ВИЧ-инфекции.
Примечание. Болезнь Уиппла с артропатией может кодироваться дополнительно - "Артропатия при других уточненных болезнях, классифицированных в других рубриках" - M14.8*.
Этиология и патогенез
Отдельные авторы полагают, что возбудителем болезни Уиппла могут быть анаэробные коринебактерии, гемофильные бактерии, L-формы стрептококков.
Таким образом, вопрос об этиологии заболевания остается открытым.
Патогенез
Инфицирование бактериями слизистой кишечника приводит к массивной инфильтрации собственной пластинки и, как следствие, блокаде лимфатических путей кишечника. Аналогичные изменения, в частности - блокаду лимфатических путей, выявляют в серозных оболочках других органов (печени, суставов, плевры перикарда). Изменения обнаруживают в миокарде и головном мозге. Изменения в кишечнике, в свою очередь, вызывают нарушения всасывания и транспортировки всех питательных веществ и развитие тяжелой мальабсорбции. Высокое гидростатическое давление в лимфатической системе и нарушение проницаемости слизистой способствуют экссудации воды и белка в просвет кишечника и развитию у больных тяжелой белковой недостаточности.
Наряду с генерализацией инфекции, большое значение в патогенезе болезни Уиппла придается иммунологическим нарушениям, в частности - изменениям соотношения регуляторных субпопуляций Т-лимфоцитов, утрате способности макрофагов лизировать возбудителя и прочим.
Патанатомия
Характерные для болезни Уиппла изменения:
- стенка тонкой кишки уплотнена и растянута;
- слизистая оболочка имеет зернистую поверхность;
- ворсинки слизистой утолщены и укорочены;
- поражение кишки имеет пятнистый характер;
- мезентериальные лимфатические узлы увеличены;
- отмечается утолщение брыжейки.
В пораженных органах (тонкая кишка, мезентериальные лимфатические узлы, селезенка, печень) можно обнаружить макрофаги с крупными гранулами в цитоплазме, визуализирующиеся при окраске бриллиантовым фуксином (краситель Шиффа).
При электронной микроскопии внутри макрофагов выявляются микроорганизмы Tropheryma whippelii (палочковидные структуры размером от 0,3-1,5 до 2,5 мкм). В результате антибиотикотерапии бациллы исчезают в фазе стойкой ремиссии заболевания, а при обострении появляются снова.
В лимфатических узлах и брыжейке выявляются гранулы, содержащие включения жира. Жировые инфильтраты обнаруживаются также на плевре, перикарде, в печени.
Эпидемиология
Возраст: преимущественно старше 30 лет
Признак распространенности: Крайне редко
Соотношение полов(м/ж): 4
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
мигрирующие боли в суставах, припухлость суставов, миалгии, миозит, диарея, стеаторея, приступообразные боли в животе после еды, потеря массы тела, лимфаденопатия, лихорадка, кашель, боль в грудной клетке, расстройства психики
Cимптомы, течение
3. Симптомы поражения органов дыхания:
- непродуктивный кашель, связанный с рецидивирующим трахеобронхитом, плевритом (в 50% случаев);
- боль в грудной клетке (в результате плеврита или перикардита).
5. Повышение температуры тела (в 45% случаев), сопровождающееся ознобом с последующим выраженным потоотделением.
6. Симптомы поражения кожи:
- сухость кожи и ее диффузная гиперпигментация в основном на открытых участках тела (у 40% больных гиперпигментированы участки кожи вокруг глаз и в области скул);
- ломкость ногтей, выпадение волос.
7. Симптомы поражения сердечно-сосудистой системы (в 30–55% случаев). Наиболее часто отмечается эндокардит, возникающий на фоне отсутствия предшествующей патологии клапанов сердца. Повышение температуры тела при эндокардите может не наблюдаться.
- нарушения памяти и мотивационной сферы.
Заболевание начинается постепенно и имеет хроническое течение со склонностью к рецидивам (возникают в 40% случаев).
3. Стадия генерализации заболевания: характеризуется нарастанием кахексии и длится около 5 лет; при отсутствии своевременной диагностики и лечения завершается летальным исходом.
Диагностика
Диагностика болезни Уиппла представляет значительные сложности и большинству пациентов правильный диагноз выставляется через несколько лет безуспешной терапии по поводу других заболеваний.
- синхронные сокращения жевательных мышц или лицевых мышц;
- выявление возбудителя Tropheryma whippelii в биоптатах тонкого кишечника;
- обнаружение ДНК возбудителя методом ПЦР.
Подозрение на болезнь Уиппла может возникнуть при наличии одного из следующих критериев:
1. Повышение температуры неустановленной этиологии, ночная потливость, озноб.
2. Появление стеатореи, диареи, боли в животе.
3. Мигрирующие артралгии и полиартралгия.
4. Лимфаденопатия неясного генеза.
5. Наличие одного из следующих неврологических признаков:
- суправентрикулярная офтальмоплегия;
- ритмичные миоклонии;
- деменция;
- депрессия, тревожность, психозы;
- признаки поражения гипоталамической области (полидипсия, булимия, снижение либидо, аменорея, бессонница).
Инструментальная диагностика
1. Рентгенография кишечника. Специфические признаки отсутствуют. Могут выявляться:
- расширение тонкой кишки (более чем у 50% больных);
- грубый рельеф слизистой оболочки тонкой кишки;
- дефекты наполнения в результате сдавления увеличенными мезентериальными лимфатическими узлами.
2. Эндоскопическое исследование тонкой кишки. Специфические признаки отсутствуют. Могут отмечаться гиперемия и отечность слизистой оболочки тонкой кишки.
3. УЗИ органов грудной клетки и брюшной полости. Выявляются увеличенные забрюшинные, медиастинальные, мезентериальные лимфоузлы, визуализирующиеся как очаги повышенной эхогенности. Возможно обнаружение асцита Асцит - скопление транссудата в брюшной полости
, гепатоспленомегалии Гепатоспленомегалия - одновременное значительное увеличение печени и селезенки
, плеврального или перикардиального выпота.
4. Компьютерная томография органов грудной клетки и брюшной полости. Выявляются увеличенные забрюшинные, медиастинальные, мезентериальные лимфоузлы, визуализирующиеся как очаги пониженной плотности. Могут обнаруживаться асцит, гепатоспленомегалия, плевральный или перикардиальный выпот.
5. Биопсия кишечника. При световой микроскопии выявляются внутриклеточные и внеклеточные включения жира в слизистой оболочке тонкой кишки и в брыжеечных лимфатических сосудах. Наблюдается расширение брыжеечных лимфатических сосудов.
Возможно обнаружение инфильтрации слизистой оболочки тонкой кишки "пенистыми" макрофагами, которые содержат гранулы с PAS-положительной реакцией (свидетельствуют о грамположительных микроорганизмах в слизистой оболочке). PAS-позитивное вещество представляет собой продукты распада бактерий, фагоцитированных Фагоцитоз - процесс, при котором специально предназначенные для этого клетки крови и тканей организма (фагоциты) захватывают и переваривают чужеродные частицы, разрушенные клетки, бактерии и пр.
макрофагами. Следует иметь в виду, что PAS-позитивные включения в цитоплазме макрофагов могут также выявляться при других инфекциях (гистоплазмоз, саркоидоз и прочие).
6. МРТ головного мозга - выполняется при наличии симптомов со стороны центральной нервной системы. Могут обнаруживаться очаги пониженной плотности в коре головного мозга (неспецифичный для болезни Уиппла признак), диффузные изменения в полушариях мозжечка, в области гипоталамуса, базальных ганглиев, гиппокампа Гиппокамп - часть лимбической системы головного мозга (обонятельного мозга). Участвует в механизмах формирования эмоций, консолидации памяти (то есть перехода кратковременной памяти в долговременную)
.
Лабораторная диагностика
1. Общий анализ крови:
- гипохромная микроцитарная анемия (у 90% больных); при дефиците фолиевой кислоты анемия приобретает смешанный характер;
- снижен уровень гемоглобина;
- возможно повышение количества лейкоцитов и тромбоцитов, СОЭ.
3. Биохимический анализ крови:
- могут выявляться гипопротеинемия, гипохолестеринемия, гипоальбуминемия (обусловлена нарушением синтеза альбуминов и потерей больших количеств сывороточного альбумина через сосуды пищеварительного тракта);
- в сыворотке крови снижено содержание калия, кальция, магния, железа.
4. ПЦР позволяет выявить наличие возбудителя заболевания, даже если в пробе присутствует всего несколько молекул ДНК возбудителя.
5. Тест с D-ксилозой (оценка абсорбционной функции тонкой кишки): после приема 25 г D-ксилозы пациент в течение 5 часов собирает мочу. При ненарушенных процессах всасывания в тонкой кишке количество выделенной за это время D-ксилозы должно быть не менее 5 г.
6. Тест Шиллинга (оценка всасывания витамина В 12) . Пациент принимает меченый витамин В 12, в норме показатели его экскреции с мочой в течение суток составляют не менее 10%. Если данные показатели ниже 5%, всасывание витамина B 12 в тонкой кишке нарушено.
7. Исследование кала. В 90% случаев выявляется стеаторея. Кал собирается в течение 72 часов, затем в нем определяется содержание жира. В норме этот показатель составляет 7 г . При болезни Уиппла потери жира с калом могут достигать 50 г в сутки.
Дифференциальный диагноз
В связи с редкостью заболевания, многообразием клинических проявлений и поражением многих органов и систем, дифференциальная диагностика болезни Уиппла чрезвычайно затруднительна.
Следует предполагать наличие всех заболеваний, сопровождающихся синдромом мальабсорбции (хронической диарея, потеря веса, анемия), а также синдром раздраженного кишечника, хронический панкреатит с секреторной недостаточностью.
Хроническое поражение эпителия кишечника, как правило, наблюдается при амилоидозе, болезни Крона, радиационном энтерите, ишемии кишечника, тропической мальабсорбции, целиакии, кишечной лимфангиэктазии.
Болезнь Уиппла также должна быть дифференцирована с кишечной инфекцией, в особенности - с инфекцией, вызванной Mycobacterium avium-intracellulare (MAI), ввиду схожести гистологических признаков. При обработке кислым красителем MAI окрашиваются позитивно. Диагноз может быть подтвержден при помощи ПЦР.
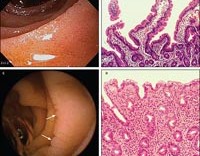
Гистологические изменения тощей кишки при определенных мальабсорбционных нарушениях
Пальцевидные ворсинки, покрытые микроворсинками: соотношение крипт около 4:1; цилиндрические эпителиальные клетки с нормальным числом микроворсинок (щеточная кайма); умеренная круглоклеточная инфильтрация собственной пластинки
Фактическое отсутствие ворсинок и удлиненных крипт; увеличенное скопление лимфоцитов и круглых клеток (главным образом плазматических клеток) в собственной пластинке; кубовидные эпителиальные клетки со скудными, беспорядочными микроворсинками
Собственная пластинка плотно инфильтрирована PAS-положительными макрофагами; ворсинчатые структуры могут быть сглажены в тяжелых случаях
Осложнения
Осложнения характеризуются кахексией, анемией, энергетической недостаточностью вследствие мальабсорбции.
Лечение
Цели лечения:
- устранение симптомов заболевания;
- нормализация массы тела;
- эрадикация микроорганизмов Tropheryma whippelii.
Методы лечения
Диета с ограничением жиров, повышенным содержанием белка и витаминов. Лечебное питание должно способствовать борьбе с диареей и восполнять нутритивные дефициты. Целесообразно использовать специальные смеси для энтерального питания с коротко- и среднецепочечными триглицеридами, которые всасываются не в лимфатических, а в кровеносных сосудах.
Медикаментозное лечение
Назначаются глюкокортикостероиды (спорный подход), антибиотики, ферменты. Осуществляется коррекция поливитаминной недостаточности.
В ряде случаев показана симптоматическая терапия.
1. Антибактериальная терапия
Спектр рекомендуемых антибактериальных препаратов различен и включает стрептомицин, хлорамфеникол, пенициллин, ко-тримоксазол, цефалоспорины. Большинство авторов, однако, останавливается на антибиотиках тетрациклинового или пенициллинового ряда.
Если у пациента отсутствует неврологическая симптоматика, лечение может сразу же начинаться с ко-тримоксазола.
Лечение у больных с неврологической симптоматикой начинается с парентерального введения антибиотиков (в течение 14 дней).
Одна из рекомендованных схем: цефтриаксон (2 г в/в ежедневно) или прокаин (1,2 млн ЕД в/м 1 раз в день), или пенициллин G (1,5-6 млн ЕД в/в каждые 6 часов) в сочетании со стрептомицином (1,0 г в/м 1 раз в день, в течение 10-14 дней) + триметоприм-сульфаметоксазол (160/800 мг перорально 2 раза в день, в течение 1 года).
Пациентам с аллергией на сульфаниламиды указанные выше препараты могут быть заменены пероральным приемом пенициллина VK или ампициллином.
В результате антибактериальной терапии отмечается быстрое клиническое улучшение, в течение нескольких дней стихают лихорадка и боли в суставах. Кишечные симптомы обычно исчезают в течение 1-4 недель.
Антибактериальная терапия должна проводиться не менее 1 года.
Показатели эффективности лечения:
- отрицательный результат ПЦР;
- исчезновение Tropheryma whippelii в биоптатах слизистой оболочки тонкой кишки (микроорганизмы Tropheryma whippelii исчезают через 4-8 недель, а пенистые макрофаги - в течение года после начала лечения).
Контроль эффективности лечения необходимо начинать через 2-3 месяца после назначения антибактериальных препаратов.
После получения первых негативных результатов терапия продолжается в течение 1 года, так как рецидивы могут возникать через несколько месяцев и даже лет после отмены лечения.
Выявление бактерий после отмены антибактериальных препаратов может быть предвестником рецидива болезни (возникает в 40% случаев). В случае рецидива терапия продолжается еще в течение 1-2 лет.
2. Гормональная терапия: преднизолон в дозе до 20-30 мг в сутки. Этот метод лечения не относится к числу основных.
3. Полиферментные препараты.
4. Коррекция дефицита витаминов. В большинстве случаев при болезни Уиппла нарушено всасывание жирорастворимых витаминов (А, Е, К). Витамины можно применять парентерально.
5. Симптоматическая терапия: при наличии судорожного синдрома пациенты нуждаются в приеме антиконвульсантов, например, вальпроевой кислоты (депакин, конвулекс).
Хирургическое лечение
Иногда у пациентов с поражением центральной нервной системы развивается гидроцефалия. Таким больным проводится вентрикулоперитонеальное шунтирование.
Прогноз
При отсутствии лечения в 100% случаев исход заболевания - летальный. Показатели 5-летней выживаемости у нелеченных больных составляют 80% после появления артралгий и 20% после развития симптомов поражения желудочно-кишечного тракта.
При адекватной терапии ремиссия достигается у 60-70% пациентов. В 30-40% случаев отмечаются рецидивы.
Госпитализация
Профилактика
Тропическая спру выявляется у людей, находившихся не менее месяца в Индии, странах Азии, Африки и Центральной Америки, а также у коренных жителей этих регионов. В Пуэрто-Рико, например, заболевание регистрируется у 8% населения.
Факторы и группы риска
- неполноценное питание (преобладание растительной пищи);
- недостаточное употребление в пищу белка, дефицит витаминов;
- эндогенная недостаточность фолиевой кислоты;
- эндокринные дисфункции (период лактации у женщин, угасание половой функции);
- нервно-психическое перенапряжение.
Клиническая картина
Cимптомы, течение
Клинические проявления заболевания могут возникать не только в момент пребывания пациентов в тропических странах, но и спустя значительное время (иногда через несколько месяцев) после их возвращения.
Течение болезни может быть острым или хроническим, медленно прогрессирующим, с периодами ремиссии и обострений.
Диагностика
Сбор анамнеза. Следует выяснить находился ли пациент в странах с тропическим или субтропическим климатом. Если срок пребывания превышает один месяц, отмечается повышенный риск возникновения тропической спру.
Тропическая спру может манифестировать остро (диарея, повышенная температура тела), однако диагностика заболевания затруднена в связи с тем, что истинная причина этих симптомов устанавливается, как правило, только после начала хронизации патологического процесса (поливитаминная недостаточность, мегалобластная анемия).
При наличии проявлений синдрома мальабсорбции, диареи и мегалобластной анемии, больной нуждается в дальнейшем обследовании.
В пользу тропической спру свидетельствуют следующие результаты лабораторных тестов:
- обнаружение стеатореи и нарушения всасывания хотя бы двух компонентов (например, жира и D-ксилозы);
- выявление атрофии ворсин тонкого кишечника (по результатам биопсии).
При дифференциальной диагностике с целиакией Целиакия - хроническое заболевание, обусловленное недостаточностью ферментов, участвующих в переваривании глютена.
Подробно имеют значение положительный эффект от назначения антибиотиков, фолиевой кислоты и отсутствие эффекта от безглютеновой диеты. Также, в отличие от целиакии, у пациентов с тропической спру более выраженные изменения наблюдаются в терминальном отделе подвздошной кишки.
Физикальные данные. Тропическая спру манифестирует неспецифическими симптомами: повышение температуры тела, тошнота, боли в животе, анорексия, диарея, стеаторея, общая слабость. По мере прогрессирования болезни возникают признаки поливитаминной недостаточности (глоссит, стоматит), снижение веса, периферические отеки; развивается мегалобластная анемия.
Рентгенография кишечника выявляет сглаженность рельефа слизистой оболочки, нарушения прохождения бариевой взвеси по кишечнику; иногда определяются горизонтальные уровни скоплений жидкости и газа в кишечных петлях.
Данное исследование применяется для дифференциальной диагностики тропической спру и туберкулеза тонкого кишечника.
ФГДС позволяет обнаружить воспалительные и атрофические изменения в тонком кишечнике и произвести забор биопсийного материала.
При биопсии слизистой оболочки тонкой кишки обнаруживают:
- частичную атрофию ворсин тощей кишки (редко - тотальную атрофию);
- крипты кишечника более глубокие, чем в норме; инфильтрированы лимфоцитами, плазматическими клетками и эозинофилами;
- эпителиальные клетки увеличены, содержат крупные ядра (из-за дефицита фолиевой кислоты и витамина В 12);
- под базальной мембраной характерны жировые включения.
Лабораторная диагностика
Общий анализ крови
Обнаруживается мегалобластная анемия, которая является следствием дефицита фолиевой кислоты и витамина В 12, уровни показателей которых снижены более чем у 60% пациентов.
Биохимический анализ крови
При тропической спру вследствие синдрома мальабсорбции, отмечаются:
-гипокалиемия;
-гипокальциемия;
-гипомагниемия;
-гипофосфатемия;
-гипоальбуминемия;
-гипохолестеринемия;
- повышение активности аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ).
Важно определять показатели метаболизма железа в организме:
- содержание железа, ферритина и трансферрина сыворотки крови;
- общая железосвязывающая способность сыворотки крови;
- расчетный коэффициент насыщения трансферрина железом.
Тест с D-ксилозой
С помощью D-ксилозного теста производится оценка абсорбционной функции тонкой кишки. Больной принимает внутрь 25 г D-ксилозы, после чего в течение 5 часов собирает мочу. Если процессы всасывания в тонкой кишке не нарушены, то количество выделенной за это время D-ксилозы должно быть не менее 5 г. Позитивные результаты теста регистрируются более чем у 90% пациентов.
Копрологическое исследование
Кал собирается в течение 72 часов у пациента, находящегося на диете, содержащей 80-100 г жира. В собранном кале определяется количество выделяемого жира. В норме этот показатель составляет 7 г. Потери жира с калом при тропической спру превышают 15 г в сутки.
Также проводится исследование кала на яйца глист.
Читайте также:

