У кого лечили врожденный токсоплазмоз
Обновлено: 25.04.2024
Обследовано 537 беременных, обратившихся в Городской центр по токсоплазмозу в период с 2010 по 2013 гг и 145 новорожденных. Показано, что токсоплазмоз играет важную роль в акушерско-гинекологической патологии. Обнаружение у женщин токсоплазменных антител
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни. Токсоплазмоз несет потенциальную угрозу для плода при заражении им во время беременности. Одним из наиболее распространенных методов профилактики врожденного токсоплазмоза является проведение скринингового серологического обследования беременных на токсоплазмоз и назначение антимикробной терапии и/или прерывание беременности при его выявлении.
Для лабораторной диагностики токсоплазмоза беременных чаще всего применяют серологические методы: реакцию непрямой иммунофлюоресценции (РНИФ), иммуноферментный анализ (ИФА Toxo IgG, IgM). Диагноз подтверждается достоверно нарастающей динамикой показателей этих тестов, их высоким уровнем либо наличием антител класса IgM и изучением их динамики.
Трудности профилактики токсоплазмоза до настоящего времени обусловливаются, прежде всего, отсутствием официально утвержденной национальной программы исследований в данной области, проводимых на современном уровне.
Целью настоящей работы было раннее выявление токсоплазмоза у беременных и новорожденных и обоснование целесообразности использования антимикробной терапии для профилактики врожденной инфекции.
Пациенты и методы проведения исследования
Под нашим наблюдением находилось 537 беременных, впервые обратившихся в Городской центр по токсоплазмозу (ГЦТ) в период с 2010 по 2013 г., в возрасте от 18 до 40 лет (средний возраст составил 27,6 ± 1,34 года), и 145 новорожденных.
Основанием для наблюдения являлся факт обнаружения в сыворотке крови пациентов антител классов IgМ и/или IgG к Toxoplasma gondii и высокие уровни антител в РНИФ.
Основную группу составили 48 беременных с инаппарантным токсоплазмозом и 34 их новорожденных, контрольную группу — 489 беременных, инфицированных токсоплазмами, и 107 их новорожденных.
Для решения поставленных задач проводились клинические наблюдения, комплекс лабораторных и функциональных методов диагностики в динамике у беременных женщин, состоящих под наблюдением у гинеколога женской консультации. У всех беременных тщательно изучался эпидемиологический анамнез. При этом наибольшее внимание уделялось наличию акушерской, гинекологической и соматической патологии, выявлению признаков острого манифестного токсоплазмоза во время беременности и в предшествующие 6 месяцев (субфебрилитет, признаки интоксикации, полилимфаденит, диарейный синдром, артралгии, миалгии и т. д.).
Всем беременным в женских консультациях не менее двух раз проводились ультразвуковое исследование плода (на сроке гестации 9–10 и 28–30 недель) и органов брюшной полости, электрокардиографическое исследование (ЭКГ), общий анализ крови, биохимический анализ крови, коагулограмма, общий анализ мочи. Диагноз токсоплазмоза устанавливался клинически и подтверждался лабораторными тестами: РНИФ и ИФА IgG, IgM. Все исследования проводились в ГЦТ при первичном обследовании, в динамике и по окончании лечения (если оно проводилось).
Помимо исследования крови матери, нами проводилось определение специфических антител IgG и IgM в пуповинной крови новорожденных. Кровь забиралась из сосудов пуповины сразу вслед за ее пережатием и пересечением после родов.
Результаты исследования и их обсуждение
При обработке данных эпидемиологического анамнеза выявлено, что среди факторов риска инфицирования токсоплазмами женщин важную роль играют контакты с домашними животными, в частности с кошками (84,5% случаев контакта), контакт с почвой (работа на загородных дачных участках (56,4% случаев)), употребление термически слабообработанных мясных продуктов (47,6% случаев), а также производственная занятость (23,7% случаев).
У основной группы пациентов инаппарантный токсоплазмоз протекал без клинических проявлений.
Анализ изучения данных гинекологического анамнеза выявил высокую частоту встречаемости хронических воспалительных заболеваний и специфических урогенитальных инфекций, играющих важную роль в этиопатогенезе внутриутробного инфицирования у женщин основной группы по сравнению с контрольной. Частота встречаемости нарушений менструальной функции и бесплодия была значительно выше у беременных, инфицированных токсоплазмами.
Наличие токсоплазменной инфекции оказывает существенное влияние на течение беременности и родов, являясь причиной большинства присоединяющихся впоследствии осложнений и одной из основных причин невынашивания беременности. Отягощенный акушерский анамнез (самопроизвольные выкидыши, замершая беременность, частота медицинских абортов и др.) имел место у 2/3 из числа женщин, инфицированных токсоплазмами. Данные за врожденные пороки развития и раннюю неонатальную смерть отмечены только в группе женщин, инфицированных токсоплазмами.
Анализ результатов ИФА IgG и IgM позволил выделить основную группу беременных с инаппарантным токсоплазмозом и контрольную — беременных, инфицированных токсоплазмами в зависимости от уровня антител: низкими (52–132 ME), средними (135–280 ME) и высокими (280–1000 ME). Высокие уровни токсоплазменных антител IgM регистрировались у женщин с инаппарантной формой токсоплазмоза, а при инфицировании токсоплазмами — не регистрировались.
Уровни антител в реакции непрямой иммунофлюоресценции (РНИФ) определялись в соотношении 1:40, 1:80, 1:160 — у контрольной группы и в соотношении 1:320, 1:640, 1:1280, 1:2560 — у основной группы беременных.
Всем пациентам основной группы назначалась антимикробная терапия со II триместра беременности по схеме: спирамицин 3 млн МЕ в сутки и фолиевая кислота по 1 таблетке 3 раза в день. Длительность лечения определялась индивидуально, в зависимости от снижения уровней токсоплазменных антител и не превышала трех курсов.
Спирамицин — макролидный антибиотик природного происхождения, является эффективным и наиболее безопасным средством лечения токсоплазмоза. Он единственный из антибактериальных препаратов, который может назначаться в ранние сроки беременности без временных ограничений, начиная с первого триместра.
Результаты серологических показателей до лечения и после, а также перед родами представлены в табл. 1 и 2.
При проведении исследования пуповинной крови методом ИФА и РНИФ новорожденных от матерей с инаппарантной формой токсоплазмоза основной группы, получивших курс антимикробной терапии, и новорожденных от матерей, инфицированных токсоплазмами, контрольной группы были выявлены специфические токсоплазменные антитела IgG у 34 детей основной и 107 новорожденных контрольной группы. Токсоплазменные антитела IgΜ не обнаруживались ни у одного ребенка. При этом уровень антител новорожденных соответствовал уровню антител у матери, что связано с передачей антител трансплацентарно.
Полученные результаты динамического наблюдения детей, родившихся от матерей с инаппарантным токсоплазмозом и матерей, инфицированных токсоплазмами, не выявили отставание в физическом, моторном и нейропсихическом развитии.
Контрольное серологическое исследование детей, проведенное в возрасте от 12 месяцев до года, не выявило как специфических антител класса IgM, так и нарастания титров токсоплазменных антител класса IgG, как у детей основной, так и контрольной групп.
На основании наших исследований можно утверждать, что инаппарантный токсоплазмоз должен рассматриваться как фактор высокого риска развития осложнений течения беременности и родов, что в последующем может отражаться на состоянии здоровья ребенка.
Анализируя представленные данные, подтверждается необходимость проведения комплексных лабораторных исследований на токсоплазмоз среди беременных женщин, включающих в себя комплекс серологических методик; представитель природных макролидов спирамицин рассматривается в настоящее время как антибиотик первоочередного выбора в первом триместре беременности при лечении инаппарантного токсоплазмоза матери и профилактике врожденной инфекции плода.
Выводы
- Для определения риска развития врожденного токсоплазмоза при первичном обследовании беременных на ранних сроках, наиболее информативными являются данные эпидемиологического анамнеза (возможность заражения во время беременности) и результаты серологического скрининга РНИФ и ИФА IgM и IgG к Toxoplasma gondii в сыворотке крови.
- Динамика показателей РНИФ и уровней антител IgG и IgM в ИФА служат маркером эффективности проведенной терапии.
- Своевременное выявление токсоплазмоза на ранних сроках беременности и назначение комбинированной этиотропной терапии предотвращает развитие врожденного токсоплазмоза.
- В результате катамнестического наблюдения (продолжительностью до года) за детьми, родившимися от матерей с инаппарантным токсоплазмозом, включенных в исследование, не было выявлено клинико-лабораторных и инструментальных признаков врожденного токсоплазмоза, что свидетельствует о эффективности проводимой медикаментозной профилактики этого заболевания.
Литература
- Лысенко А. Я., Владимова М. Г., Кондрашин А. В., Майори Дж. Клиническая паразитология. Под ред. Лысенко А. Я. Женева, ВОС; 2002.
- Guerina N., Hsu H., Meissner C., Maguire J., Lynfield R., Stechenberg B. et al. Neonatal serologic screening and early treatment for congenital Toxoplasma gondii infection // N Engl J Med. 2004; 330 (26): 1858–1863.
- Беляева Н. М., Зембатова С. Х., Иванова Л. П., Дзуцева Ф. К., Никитина Г. Ю., Борисенко Ю. В. Особенности диагностики и лечения токсоплазмоза у беременных // Лечащий Врач. 2011. № 11. 24–26.
- Peyron F., Wallon M., Liou C., Garner P. Treatments for toxoplasmosis in pregnancy (Cochrane Review). In The Cochrane Library 2003; Oxford: Update Software.
- Лобзин Ю. В., Васильев В. В., Тимченко В. Н., Васильева И. С. Токсоплазмоз беременных: достижения и нерешенные вопросы // Российский медицинский журнал. М., 2001; 37–39.
- О выявлении и профилактике токсоплазмоза в г. Москве: Методические рекомендации. М., 2013.
- Беляева Н. М., Зембатова С. Х., Дзуцева Ф. К. Проблема токсоплазмоза у беременных и новорожденных. Материалы IV Всероссийского Конгресса по инфекционным болезням. М., 2012; 51–52.
Н. М. Беляева*, доктор медицинских наук, профессор
С. Х. Зембатова* , 1
Л. П. Иванова*
Ф. К. Дзуцева**
Ю. В. Борисенко**, кандидат биологических наук
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГЦТ ДЗМ, Москва
Abstract. 537 pregnant women applied to City Toxoplasmosis Center during the period of 2010–2013 and 145 newborns were been checked. As it is shown in the article toxoplasmosis has important role in obstetric-gynecologic pathology. Finding toxoplasmosis antibodies IgM in women’s organisms as well as high levels of indirect immunofluorescence reaction marker of inapparent toxoplasmosis should be considered as indication of necessity of preventing and medical measures.
Врожденный токсоплазмоз – это паразитарная патология, которая возникает при трансплацентарном инфицировании ребенка Toxoplasma gondii. У большинства детей протекает бессимптомно. Возможные проявления заболевания: интоксикационный синдром, пятнисто-папулезная сыпь, лимфаденопатия, желтуха, гепатоспленомегалия, отеки нижних конечностей. Часто провоцирует развитие патологий органа зрения, слуха, ЦНС; реже – миокарда, легких и печени. Антенатальная диагностика базируется на проведении биопсии, постнатальная – на совокупности анамнестических и клинико-лабораторных данных (ИФА, ПЦР). Этиотропное лечение врожденного токсоплазмоза проводится при помощи схем на основе препаратов пириметамина и сульфадимезина или спирамицина.
МКБ-10
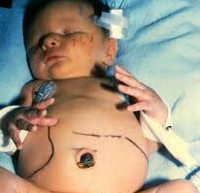
Общие сведения
Врожденный токсоплазмоз – заболевание в педиатрии и неонатологии, возникающее в результате трансплацентарного заражения плода на фоне острой формы токсоплазменной инфекции у матери. Впервые Toxoplasma gondii была описана французами К. Николь и Л. Монсо в 1908 году. В 1939 г. американцы Э. Вольф, Д. Кауэн и Б. Пэйдж подтвердили трансплацентарный механизм передачи возбудителя. Промежуточными хозяевами могут выступать более 400 видов животных. Согласно статистическим данным ВОЗ, число инфицированных токсоплазмой людей в мире составляет порядка 1,5 млрд. человек, в России – около 30% всего населения. Частота врожденной формы 1,5:1000 новорожденных. Даже на фоне лечения средний показатель смертности у детей до 5 лет составляет 12%, осложнения возникают почти у 90%.

Причины врожденного токсоплазмоза
Врожденный токсоплазмоз развивается только при инфицировании матери Toxoplasma gondii во время вынашивания ребенка. Механизм заражения беременной женщины – фекально-оральный. Наиболее распространенные причины: контакт с животными из семейства кошачьих и употребление термически необработанной пищи. Инвазивная форма возбудителя – ооциста – формируется в кишечнике животных и выделяется с калом, после чего может на протяжении 12 и больше месяцев сохранять контагиозность в условиях внешней среды. В крайне редких случаях этиологическим фактором может стать трансплантация контаминированных органов или переливание крови. Заражение плода T. gondii происходит трансплацентарным путем. После рождения ребенка развивается интенсивный гемолиз, возникают геморрагии на слизистых оболочках, расширение камер сердца, пневмония или интерстициальный отек легких, некроз печени и селезенки, увеличение лимфоузлов, воспаление и отек тканей головного мозга, некробиоз сетчатки. При гистологическом исследовании непосредственно пораженных тканей определяется некроз, гранулематозная или диффузная пролиферация ретикулоцитов, инфильтрация плазмоцитами и лимфоцитами, перифокально – множество токсоплазм. Впоследствии на месте некротизированных участков формируется фиброз, переходящий в кальциноз.
Классификация врожденного токсоплазмоза
В зависимости от периода инфицирования плода врожденный токсоплазмоз может протекать в трех формах:
- Хроническая форма. Заражение происходит в I-II триместрах беременности. Риск передачи возбудителя – 13-18%. При такой форме могут развиваться атрофия головного мозга, гидроцефалия, деформация желудочков мозга, анофтальмия, колобома, атрофия сетчатки, врожденные пороки сердца и других органов и систем.
- Подострая форма. Инфицирование – III триместр. Риск заражения ребенка – 75-85%. Проявления могут включать в себя энцефалит, менингоэнцефалит, очаговый некроз сетчатки, увеит.
- Острая форма. Токсоплазма попадает в организм ребенка непосредственно перед родами. Возможные симптомы: гипертермия, пятнисто-папулезная сыпь, интенсивная желтуха, гепатоспленомегалия, анемия, миокардит, пневмония.
Симптомы врожденного токсоплазмоза
Врожденный токсоплазмоз может проявляться в различные периоды жизни ребенка – от первых дней до нескольких месяцев. Специфических симптомов данное заболевание не имеет. Зачастую присутствующая клиника нечеткая и имитирует другие врожденные патологии. Наиболее вероятные проявления врожденного токсоплазмоза: ухудшение общего состояния, пятнисто-папулезная сыпь различной локализации, генерализованная лимфаденопатия, увеличение печени и селезенки, желтуха, отеки нижних конечностей, субфебрильное повышение температуры тела. Тяжесть симптомов зависит от степени инфицирования токсоплазмами, триместра беременности, в котором произошло инфицирование, и иммунных сил матери. Примерно 70-90% детей не имеют каких-либо проявлений в ранние периоды жизни, но почти у всех спустя некоторое время возникают осложнения. Классический врожденный токсоплазмоз проявляется триадой Сэбина – обструктивная гидроцефалия, хориоретинит и массивное внутричерепное обызвествление. Наблюдается данный комплекс не более чем у 3% детей. Помимо триады, часто возникают миокардит, миозит, гепатит и пневмония. Клинические проявления напрямую зависят от присутствующих патологических изменений. Вероятность развития поздних осложнений на фоне латентного врожденного токсоплазмоза составляет порядка 90%. Период возникновения может быть разным – от нескольких месяцев до нескольких лет. Наиболее часто наблюдается поражение глаз, органа слуха и ЦНС. Самое распространенное осложнение – ретинит (примерно 85% случаев). К другим последствиям перенесенного врожденного токсоплазмоза относят олигофрению, гидроцефалию, повышение внутричерепного давления, острый и хронический энцефалит, эпилепсию, полную глухоту и/или слепоту, микрофтальм, увеит, хроническую гипертермию, редко – шизофрению.
Диагностика врожденного токсоплазмоза
Диагностика врожденного токсоплазмоза может проводиться в антенатальном и постнатальном периоде. Антенатальное исследование подразумевает использование инвазивных методов с дальнейшими лабораторными анализами. Абсолютное показание к их проведению – острый токсоплазмоз матери в сумме с нарушениями развития плода по результатам акушерского УЗИ. Выбор методики исследования зависит от срока беременности. При гестации от 10 недель проводится биопсия хориона, от 16 недель – амниоцентез, от 18 – кордоцентез. Для верификации инфекции полученный материал исследуют при помощи ПЦР. Постнатальная диагностика включает в себя сбор анамнестических данных и проведение клинического и лабораторного исследования. Данная мера является обязательной для всех детей, входящих в группу риска внутриутробного инфицирования. Неспецифическая диагностика и ее результаты зависят от присутствующих симптомов и синдромов. Список исследований может включать в себя ОАК (анемия, тромбоцитопения, лейкоцитоз); рентгенографию ОГК (признаки инфильтрации легких); нейросонографию и КТ головного мозга; биохимическое исследование крови с измерением АЛТ и АСТ, определением СРБ, уровня билирубина и его фракций (все показатели выше нормы); офтальмоскопию (некроз сетчатки); спинномозговую пункцию (признаки воспаления). Специфические методы подразумевают серодиагностику биологических жидкостей методом ИФА, при котором наблюдается возрастание титра антител IgG в 4 и больше раз и высокий уровень IgM на протяжении 10-14 суток. При необходимости проводится ПЦР с целью идентификации ДНК токсоплазмы.
Лечение врожденного токсоплазмоза
Лечение новорожденного с выраженной клинической картиной врожденного токсоплазмоза проводится только в условиях стационара, в отделении патологии новорожденных. Соблюдение специфического режима и рациона не требуется, их коррекция проводится в соответствии с состоянием ребенка. При наличии отягощенного анамнеза матери этиотропную терапию начинают с момента постановки предварительного диагноза. В других случаях перед началом лечения требуется проведения лабораторных методов исследования. Используемые схемы: пириметамин и сульфадимезин на 1-1,5 месяца; спирамицин или другие макролиды на 4-6 недель. В некоторых случаях применяют системные глюкокортикостероиды – преднизолон. Симптоматическое лечение зависит от присутствующих симптомов и синдромов, выявленных педиатром или неонатологом. При стойком повышении внутричерепного давления или развитии гидроцефалии показано хирургическое лечение. При необходимости дальнейшее лечение может проводиться амбулаторно под контролем педиатра, инфекциониста и других специалистов. В таких же условиях проводится терапия субклинической и латентной формы врожденного токсоплазмоза. Решение об отказе от приема препаратов принимается на основе клинико-лабораторных показателей, находящихся в пределах возрастной нормы, и заключения всех лечащих врачей.
Прогноз и профилактика врожденного токсоплазмоза
Прогноз при врожденном токсоплазмозе зависит от триместра, в котором произошло инфицирование плода и тяжести клинических проявлений. При развитии патологии в I триместре может наблюдаться самопроизвольное прерывание беременности и выкидыш или дальнейшее развитие тяжелых форм заболевания, однако аномалии органов при этом не возникают. При адекватной и своевременной терапии прогноз для жизни благоприятный, для выздоровления – сомнительный. Неспецифическая профилактика врожденного токсоплазмоза включает в себя ограничение контакта домашних животных с беременной женщиной, соблюдение гигиенических норм, прием в пищу только термически обработанных продуктов, тщательное мытье овощей и фруктов. При наличии факторов, указывающих на возможное инфицирование матери, проводится специфическая диагностика, направленная на идентификацию T. gondii. При подтверждении диагноза показано немедленное проведение этиотропной терапии. Специфической профилактики врожденного токсоплазмоза не разработано.
Токсоплазмоз при беременности – это паразитарное заболевание, вызванное проникновением T.gondii в организм беременной женщины. В большинстве случаев данная патология протекает бессимптомно, реже сопровождается гриппоподобным симптомокомплексом. Диагностика токсоплазмоза при беременности включает в себя серологическое исследование с определением IgM и IgG, ультразвуковое обследование плода и амниоцентез с последующим проведением ПЦР околоплодных вод. Вариант медикаментозного лечения зависит от инфицирования плода и может состоять из антибиотиков макролидного ряда или комбинации сульфаниламида и антагониста фолиевой кислоты.
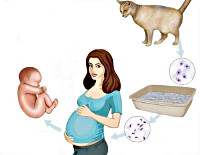
Общие сведения
Токсоплазмоз при беременности – это инфекционное заболевание, вызванное токсоплазмами, которое имеет большое значение в акушерстве и гинекологии за счет трансплацентарного пути передачи. Согласно статистике, порядка 15-25% женщин в возрасте от 15 до 45 лет инфицированы T.gondii. Общая частота врожденного токсоплазмоза составляет от 1 до 10 случаев на 10 000 новорожденных, из них 3-10% имеют тяжелые аномалии развития. При этом порядка 55% женщин, родивших инфицированных детей, не отмечали у себя каких-либо признаков заболевания. Как правило, более высокому риску развития токсоплазмоза при беременности подвержены женщины с иммунодефицитом и проживающие или путешествующие в эндемических зонах: Франции, Латинской Америке и южной Африке.

Причины токсоплазмоза при беременности
Возбудитель токсоплазмоза при беременности – Toxoplasma gondii. Она являет собой облигатного внутриклеточного паразита размером от 4 до 8 мкм. В зависимости от среды токсоплазма может находиться в трех формах: ооциста, тканевая циста и тахизоит. Первые две являются инвазивными для человека. Инфицирование цистами происходит при использовании зараженных мясных продуктов питания, ооцитами – при контакте с землей во время садовых работ или употреблении немытых овощей и фруктов. Токсоплазмы в форме ооцисты способны сохранять жизнеспособность длительное время, в особенности находясь в теплых и влажных условиях, что существенно повышает риск их передачами. При попадании в организм паразиты из инвазивных форм трансформируются в тахизоиты, которые обуславливают клинику заболевания и инфицирование плода на фоне токсоплазмоза при беременности.
Выделяют несколько вариантов пути заражения человека T.gondii – употребление в пищу сырого фарша или плохо термически обработанного мяса, контакт с испражнениями кошки или землей, содержащими ооцисты, трансплацентарная передача от матери к ребенку и переливание инфицированной крови. Значительная часть случаев (до 65%) токсоплазмоза при беременности возникает на фоне употребления инфицированных продуктов питания и воды, проходит в виде первичного инфицирования. При контакте с кошками основную опасность представляют питомцы, которые живут на улице или питаются сырым мясом.
Инфицированный человек может быть источником только в случае донорства крови или органов. Риск развития токсоплазмоза при беременности существенно возрастает при посещении регионов с высоким распространением токсоплазм: Франции, Латинской Америки и южной части Африки. Принято считать, что даже при единичном попадании в организм T.gondii человек остается инфицированным всю жизнь, а само заболевание протекает в субклинической форме. Однако только в отдельно взятых случаях токсоплазмоз при беременности вызывается активацией персистирующей инфекции.
Симптомы токсоплазмоза при беременности
Более чем 90% случаев токсоплазмоза при беременности протекает бессимптомно, в форме здорового носительства. Развитие выраженной клиники более вероятно у беременных с ослабленным иммунитетом – на фоне сопутствующих инфекционных или бактериальных заболеваний, употребления ГКС, ранних этапов СПИДа и т. д. Инкубационный период в таких случаях может колебаться от 1 до 3 недель после попадания паразита в организм. Для острого токсоплазмоза при беременности характерен гриппоподобный вариант течения: подъем температуры тела до 37,5-38°C, общая слабость и недомогание, головная боль, увеличение лимфатических узлов, реже – гепатоспленомегалия. У беременных редко возникает токсоплазмозный хориоретинит, еще реже – конъюнктивит, кератит или иридоциклит. Только на фоне выраженного дефицита иммунитета токсоплазмоз при беременности может вызывать тяжелые осложнения в виде энцефалита, гепатита, миокардита или пневмонии.
Токсоплазмоз относится к группе TORCH-инфекций, в которую входят инфекционные заболевания, способные оказывать тератогенное влияние. В основном опасность для плода представляет первичное заражение матери, хронический токсоплазмоз при беременности редко становится причиной внутриутробной передачи. Инфицирование происходит в промежутке от 1 до 4 месяцев после проникновения в плаценту тахизоитов, риск заражения возрастает со сроком гестации. Согласно статистике, частота передачи паразитов плоду на фоне отсутствия лечения токсоплазмоза при беременности в третьем триместре в 10-12 раз выше, чем в первом. Несмотря на это, чем раньше произошло инфицирование плода – тем хуже прогноз. При проникновении токсоплазм в организм плода в первом триместре могут наблюдаться спонтанные аборты, тяжелые аномалии развития. Более поздний врожденный токсоплазмоз проявляется тетрадой Сэбина: хориоретинит, водянка головного мозга, судорожный синдром, внутричерепная кальцификация. Также могут присутствовать выраженная задержка внутриутробного развития и микроцефалия. Их наличие свидетельствует о перенесенном остром токсоплазмозе при беременности.
Диагностика токсоплазмоза при беременности
Постановка диагноза токсоплазмоза при беременности основывается на анамнестических данных, выявленных симптомах, результатах лабораторных и инструментальных исследований. При сборе анамнеза акушером-гинекологом или инфекционистом выясняются все обстоятельства, при которых могло произойти инфицирование токсоплазмами: употребление сырого мяса, немытых овощей или фруктов, контакт с уличными кошками, работа с землей в саду, пребывание в эндемических зонах. Физикальный осмотр у женщин с токсоплазмозом при беременности может выявить гриппоподобный симптомокомплекс, но в подавляющем большинстве случаев он малоинформативен.
Ведущее место в диагностике токсоплазмоза при беременности играют серологические тесты, ультразвуковое сканирование и пункция амниотической оболочки плода. Лабораторная диагностика зачастую является первым шагом и реализуется она путем иммуноферментного анализа (ИФА) или специальных тест-систем. Суть этого исследования заключается в определении иммуноглобулинов класса М (IgM) и G (IgG). Их полное отсутствие опровергает диагноз токсоплазмоза при беременности. Наличие IgM и его нарастание в 4 раза и более указывает на первичное инфицирование T.gondii. Далее титр постепенно продолжает нарастать и достигает максимума через 5-20 дней после инвазии. Первое проявление IgG в крови матери наступает через 7-14 дней и достигает максимальной концентрации в промежутке от 3 до 6 месяцев. В большинстве случаев высокий уровень IgG свидетельствует о латентном течении токсоплазмоза при беременности. При получении позитивных результатов следует повторить исследование 3-4 раза в течение 2-3 недель.
Проведение УЗИ женщинам с подозрением на токсоплазмоз при беременности необходимо для оценки состояния плода. В большинстве случаев выявить какие-либо выраженные признаки врожденного токсоплазмоза не удается или присутствующих изменений недостаточно для подтверждения диагноза. К основным проявлениям инфицирования плода на фоне токсоплазмоза при беременности относятся общая задержка внутриутробного развития и нарушения структуры ЦНС – гидро- или микроцефалия, образование кальцификатов. Прерывание беременности рекомендуется только при обнаружении тяжелых морфологических аномалий.
Лечение токсоплазмоза при беременности
Лечение необходимо только в случаях острого токсоплазмоза при беременности, сопровождающегося клиническими проявлениями. При отсутствии клинических симптомов инфекции выздоровление наступает самостоятельно. В зависимости от поражения плода выделяют два направления медикаментозной терапии токсоплазмоза при беременности. При отсутствии признаков заражения плода по результатам ПЦР амниотической жидкости используются антибиотики макролидного ряда (спирамицин). Данные средства способны накапливаться в тканях плаценты и предотвращать вертикальный путь передачи.
При подтверждении или подозрении на инфицирование плода на фоне токсоплазмоза при беременности фармакотерапия должна состоять из антагониста фолиевой кислоты (пириметамин) и сульфаниламида (сульфадиазин). Первый способен подавлять деление клеток в костном мозге, поэтому его назначение всегда дополняется препаратами фолиевой кислоты. Также использование препарата противопоказано в I триместре беременности в связи с потенциальным тератогенным эффектом. Такой вариант лечения направлен на снижение тяжести заболевания у ребенка и улучшение общего прогноза.
Прогноз и профилактика токсоплазмоза при беременности
Прогноз для женщины на фоне токсоплазмоза при беременности благоприятный. Практически все случаи заканчиваются клиническим выздоровлением. Прогноз для будущего ребенка напрямую зависит от триместра, в котором произошло инфицирование – проникновение паразитов в организм плода в I триместре связано с высоким риском спонтанного аборта или тяжелых аномалий развития.
Профилактика токсоплазмоза при беременности подразумевает разрыв всех механизмов передачи инфекции и скрининг беременных. Первая часть превентивных мер включает в себя употребление только чистой воды и продуктов, прошедших качественную термическую обработку, ограничение работы с землей и контакта с кошками, тщательное мытье овощей и фруктов и т. д. Скрининг токсоплазмоза показан только беременным с высоким риском заражения и включает в себя ежемесячный серологический контроль.
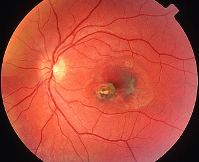
Общие сведения

Причины токсоплазмозного увеита
Возбудителем токсоплазмозного увеита является Toxoplasma gondii, которая относится к типу простейших, классу споровиков. Жизненный цикл состоит из двух фаз развития – половой и бесполой. Процесс размножения токсоплазм происходит только в эпителиоцитах кишечника кошачьих. Фаза бесполого развития реализуется в клетках большинства органов и тканей человека, включая глазное яблоко. Данный этап жизненного цикла характеризуется склонностью к инвазии, что обуславливает не только функциональные, но и органические изменения органа зрения при токсоплазмозном увеите.
Врожденная форма заболевания наблюдается при вертикальном (трансплацентарном) пути передачи возбудителя от матери к ребенку. Причина приобретённого токсоплазмозного увеита – инфицирование от плотоядных, сельскохозяйственных животных или птиц. Чаще переносчиками выступают кошки, голуби. Возбудители проникают в системный кровоток через небольшие повреждения кожи или интактную слизистую оболочку. Менее распространённым путём заражения является алиментарный, который реализуется при употреблении мяса больных животных, а также овощей и фруктов, не прошедших полноценную обработку. Развитие токсоплазмозного увеита может быть связано с переливанием крови или трансплантацией инфицированных органов.
Проникновение возбудителей в лимфатические узлы приводит к регионарному лимфадениту. Очаги инфекции формируются при диссеминации токсоплазмы в кровеносном русле. Возникновение токсоплазмозного увеита возможно только при проникновении инфекционного агента через гематоофтальмический барьер. Реже зрительная дисфункция наблюдается при нарушении проницаемости гематоэнцефалического барьера и поражении зрительной коры головного мозга.
Симптомы токсоплазмозного увеита
С клинической точки зрения специалисты в сфере офтальмологии различают врожденную и приобретённую формы заболевания. В большинстве случаев в патологический процесс вовлечена сосудистая оболочка, поэтому токсоплазмозный увеит проявляется симптоматикой хориоретинита. Реже развивается генерализованный увеит. При этом интактными остаются передние отделы глазного яблока. Орган зрения чаще поражается в хроническом периоде болезни. Приобретенная форма заболевания при отсутствии нарушений со стороны иммунной системы протекает латентно. При хроническом течении возбудитель может длительное время находиться в стадии персистенции и провоцировать периодическое развитие рецидивов.
Клинические проявления врожденной формы токсоплазмозного увеита зависят от того, в каком триместре беременности произошло инфицирование. Заражение в I триместре несовместимо с жизнью, при инфицировании во II и III триместрах отмечается подострое или хроническое течение токсоплазмозной инфекции. Очень редко токсоплазмозный увеит протекает латентно и является только причиной развития вторичного страбизма. Данный вариант патологии часто сочетается с олигофренией, гидроцефалией, микрофтальмом, злокачественным течением миопии.
При генерализованном увеите поражение передних отделов глазного яблока протекает в форме токсико-аллергической реакции, спровоцированной специфическим воспалением увеальной сосудистой оболочки глаза. Наиболее распространёнными сопутствующими патологиями, наблюдающимися при токсоплазмозном увеите, являются миопия, катаракта и колобома хориоидеи, птоз век. Об осложненном течении заболевания свидетельствует хориоидальная неоваскуляризация.
Диагностика токсоплазмозного увеита
Диагностика токсоплазмозного увеита основывается на проведении офтальмологом наружного осмотра, офтальмоскопии, биомикроскопии, визометрии, биопсии, гониоскопии, цитологического исследования, иммуноферментного анализа (ИФА). При наружном осмотре пациентов с врожденным токсоплазмозным увеитом выявляется гиперемия бульбарной конъюнктивы, птоз века, нистагм. Офтальмоскопически визуализируется поражение центральных отделов глазного дна. Очаг воспаления или хориоретинальная гранулема с бело-желтым или коричневым оттенком чаще всего имеют диаметр около ⅓ от диаметра диска зрительного нерва. Реже образуются крупные очаги, диаметр которых больше диаметра ДЗН.
Длительное течение токсоплазмозного увеита приводит к дегенерации зоны поражения с последующим развитием коагуляционного некроза. При проведении офтальмоскопии определяется округлый очаг белого цвета с четко очерченными фестончатыми краями. По периферии очага атрофии наблюдается скопление пигмента, интра- и субретинальное кровоизлияние. Для генерализованной формы токсоплазмозного увеита с вовлечением переднего отдела глазного яблока характерно появление преципитатов на роговой оболочке. При гониоскопии в передней камере выявляется клеточная взвесь.
При проведении биомикроскопии со щелевой лампой при остром течении токсоплазмозного увеита определяются участки кровоизлияния, скопления экссудата, помутнение стекловидного тела. Эндозоиты можно обнаружить в экссудате или внутри клеток структур увеального тракта в процессе цитологического исследования биоптата. В цистах располагаются цистозоиты. Подтвердить наличие токсоплазм можно при биопсии неповрежденных тканей по периферии зоны специфического воспаления или некроза. Биомикроскопия при приобретённом токсоплазмозном увеите позволяет выявить большое количество преципитатов в задних отделах глазного яблока, множественные задние синехии в сочетании с помутнением стекловидного тела. При проведении ИФА в острой фазе заболевания повышается титр антитоксических антител класса IgM. Изолированное выявление IgG указывает на хроническое течение токсоплазмозного увеита или фазу реактивации.
Лечение токсоплазмозного увеита
Тактика лечения токсоплазмозного увеита определяется формой и особенностями течения заболевания. Используются иммуномодуляторы, общеукрепляющие средства. Специфическая терапия показана только пациентам с риском снижения остроты зрения. Препаратами выбора являются лекарственные средства из группы синтетических антибактериальных препаратов в комплексе с сульфаниламидами. Курс лечения длится от 2 до 4 недель. В течение всего курса показано применение фолиевой кислоты и проведение общего анализа крови в динамике. Это обусловлено тем, что препараты указанных групп могут приводить к снижению уровня лейкоцитов и тромбоцитов. При изолированном развитии токсоплазмозного увеита рекомендовано парабульбарное введение глюкокортикоидов. В случае развития системных проявлений токсоплазмоза показана пульс-терапия глюкокортикоидами.
При необходимости хирургического вмешательства антитоксоплазмозную терапию необходимо проводить в пред- и послеоперационном периоде. Лазерная коагуляция выполняется с целью отграничения зоны воспаления, но не используется для удаления токсоплазмозных очагов, что связано с их глубоким расположением и высоким риском развития послеоперационных осложнений. При выявлении атрофического очага большого размера у пациента с врожденной формой токсоплазмозного увеита специфическое лечение рекомендовано только при возникновении рецидива заболевания.
Прогноз и профилактика токсоплазмозного увеита
Специфические превентивные меры не разработаны. Неспецифическая профилактика токсоплазмозного увеита направлена на укрепление иммунитета. При необходимости назначаются иммуномодуляторы. Также пациентам необходимо нормализовать режим сна и отдыха, избегать возникновения стрессовых ситуаций. Риск инфицирования снижается при соблюдении правил личной гигиены, уходе за домашними животными, правильной термической обработке продуктов питания.
Прогноз зависит от степени тяжести заболевания. При легких формах специальная терапия не требуется, поскольку для токсоплазмозного увеита характерно благоприятное течение. При увеите средней степени тяжести применение иммуномодуляторов и стимуляция защитных сил организма способствуют достижению длительной ремиссии. Инфицирование женщины в І триместре беременности ассоциировано с неблагоприятным прогнозом для плода.
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни.
.jpg)
Токсоплазмоз — широко распространенная зоонозная паразитарная инфекция, характеризующаяся полиморфизмом клинических проявлений и значительной вариабельностью течения процесса: от здорового, бессимптомного носительства до тяжелых, летальных форм болезни.
Этиология. Возбудитель токсоплазмоза Toxoplasma gondii относится к царству Protozoa, классу Coccidia, отряду Eucoccidiorida, типу Apicomplexa. T. gondii — условно патогенный внутриклеточный паразит, поражающий в организме промежуточных хозяев, в том числе человека, любые ядерные клетки гистеофагоцитарной системы.
Эпидемиология. Пораженность или инфицированность токсоплазмами населения Российской Федерации в среднем составляет около 20,0%. Показатели пораженности выше в регионах с теплым климатом; среди лиц ряда профессиональных групп: рабочие мясокомбинатов и звероводческих ферм, животноводы, ветеринарные работники и др. Инфицированность женщин, как правило, в 2–3 раза выше, чем у мужчин.
Заболеваемость токсоплазмозом во много раз ниже показателей инфицированности, однако трудности диагностики, несмотря на обязательную регистрацию, не позволяют судить об истинном уровне инфекции.
Восприимчивость к токсоплазмозу — практически поголовная. Распространение инфекции — повсеместное в виде носительства и спорадических заболеваний. Основной источник инфекции — дикие и домашние кошки.
Основной фактор передачи токсоплазм — сырое или недостаточно термически обработанное мясо, мясные продукты с находящимися в нем цистами токсоплазм. К дополнительным факторам передачи инфекции относятся плохо вымытая зелень, овощи, фрукты (с земли), грязные руки с находящимися на них ооцистами возбудителя.
Основные пути передачи:
- пищевой — связанный с употреблением в пищу термически плохо обработанного мяса, содержащего цисты паразита;
- контактный — ассоциированный с больными кошками, выделяющими токсоплазмы с фекалиями;
- трансплацентарный — при котором становится возможным проникновение токсоплазм в плод, с последующим развитием врожденного токсоплазмоза у новорожденного;
- парентеральный — при котором не исключается передача инфекции реципиенту при переливании крови, пересадке органов и тканей.
Беременная с токсоплазмозом не представляет эпидемиологической опасности ни для окружающих, ни для медицинского персонала, что делает возможным лечение этих пациентов как в амбулаторных условиях, так и в любом соматическом стационаре.
Патогенез. Вышедшие из цист или ооцист возбудители внедряются в эпителиальные клетки тонкого кишечника, где они размножаются, образую первичный аффект и проникая затем в региональные лимфатические узлы, а из них с током лимфы — в кровь. Диссеминация возбудителя приводит к поражению самых различных органов и тканей.
При беременности, в условиях сниженного иммунитета, наряду с первичным заражением токсоплазмами, опасным является и реактивация паразита (при инфицировании до беременности), что в значительной степени определяет течение и исход беременности.
При выходе токсоплазм из цист происходит диссеминация возбудителей. Их концентрация в тканях ассоциирована со способностью токсоплазм проникать трансплацентарно, что приводит к развитию внутриутробной патологии на любом сроке беременности.
Заражение плода наблюдается у беременных как с первичным инфицированием токсоплазмами, так и реактивацией возбудителя во время беременности у серопозитивных женщин. Поражение плода может возникать на любом сроке гестации, но особую опасность представляет его инфицирование в первом и втором триместрах. При заражении в третьем триместре беременности преобладают бессимптомные формы течения заболевания, а поздние клинические признаки проявляются через месяцы и годы.
Заражение на ранних сроках эмбриогенеза заканчивается спонтанным выкидышем, мертворождением, вызывает тяжелые нарушения развития — анэнцефалию, анофтальмию, гидроцефалию, гепатоспленомегалию и др. (табл.).
Формирование иммунитета приводит к исчезновению возбудителя из крови, прекращается его размножение в клетках. Образуются истинные тканевые цисты, которые могут длительно, десятилетиями, в интактном состоянии сохраняться в организме (носительство токсоплазм).
Клиника. Приобретенный токсоплазмоз по характеру течения делится на острый и хронический. Кроме того, в зависимости от длительности болезни и выраженности клинических симптомов возможно подострое, а также инаппарантное (субклиническое) течение инфекции, которое характеризуется определенной динамикой либо высоким уровнем специфических антител в крови, при отсутствии клинических проявлений болезни. Таким образом, наиболее удобной для практического здравоохранения, с нашей точки зрения, является следующая классификация приобретенного токсоплазмоза: острый, подострый, хронический, инаппарантный и носительство.
Клинические проявления токсоплазмоза у беременных не имеют каких-либо существенных отличий от уже известной клинической картины заболевания.
Лабораторная диагностика. Для лабораторной диагностики токсоплазмоза чаще всего применяют серологические методы: реакцию непрямой иммунофлюоресценции (РНИФ) и иммуноферментный анализ (ИФА). Диагноз подтверждается достоверно нарастающей динамикой показателей этих тестов, их высоким уровнем либо наличием антител класса IgM. Существенное значение в диагностике токсоплазмоза, особенно в дифференциации острого и хронического процессов, имеет определение классов иммуноглобулинов, в частности антител класса IgM. Надежно диагностировать токсоплазменную инфекцию можно лишь при сравнении результатов серологических реакций в динамике. Антитела всех классов существенно повышаются к концу второй — началу третьей недели от момента инфицирования и достигают диагностического уровня. Диагноз токсоплазмоза при наличии соответствующей клиники может быть поставлен при положительной серологической конверсии, когда второй анализ сыворотки становится положительным.
Диагностика токсоплазмоза у беременных женщин включает в себя весь комплекс необходимых клинических, параклинических и специальных (иммунобиологических) исследований, которые применяются для диагностики токсоплазмоза вообще.
Обязательным условием обследования беременной на токсоплазмоз должна быть консультация врача-инфекциониста для подтверждения либо исключения текущего инфекционного манифестного или бессимптомного (инаппарантного) токсоплазменного процесса.
Учитывая исключительную важность результатов иммунологического обследования в диагностике токсоплазмоза у беременных, необходимо правильно интерпретировать полученные данные.
Вариант 3: клинические проявления инфекции отсутствуют; серологические реакции положительные в низких, средних, иногда высоких титрах (РНИФ 1:640, ИФА IgG ≥ 200 Ед/мл; ИФА IgM — положительно). При исследовании парных сывороток (через 3–4 недели) регистрируется достоверное нарастание уровня специфических антител класса IgM.
Заключение: инаппарантный токсоплазмоз — реальная угроза инфицирования плода.
Вариант 4: имеются клинические проявления токсоплазмоза; серологические реакции положительные в низких и средних (иногда высоких) титрах: РНИФ 1:1280, ИФА IgG ≥ 200 Eд/мл; ИФА IgM — положительно, при исследовании парных сывороток в динамике регистрируется достоверное нарастание уровня специфических антител; выявляются специфические антитела класса IgM-класса. Заключение: острый токсоплазмоз.
Рекомендации: экстренная превентивная этиотропная терапия (не ранее чем со II триместра беременности); в I триместр — рассмотреть вопрос о прерывании беременности; проводят кордо- и амниоцентез на 22–23 неделях беременности; новорожденный обследуется на токсоплазмоз, и при подтверждении диагноза проводится этиотропная терапия (диспансерное наблюдение 5 лет).
Вариант 5: имеются клинические проявления инфекции; серологические реакции положительные в высоких или средних показателях; при исследовании парных сывороток в динамике регистрируется снижение уровня специфических антител (РНИФ ≤ 1:1280, ИФА IgG — 200 Eд/мл; ИФА IgM — положительно). Заключение: подострый токсоплазмоз. Рекомендации: этиотропная терапия (не ранее чем со II триместра); в I триместр — ставится вопрос о прерывании беременности; новорожденный обследуется на токсоплазмоз и при подтверждении диагноза проводится этиотропная терапия (диспансерное наблюдение 5 лет).
Вариант 6: имеются клинические проявления токсоплазмоза; серологические реакции положительны в низких или средних показателях (РНИФ 1:640, ИФА IgG — 200 Eд/мл; ИФА IgM — отрицательно); при исследовании парных сывороток (через 3–4 недели) динамики уровня антител нет; антитела класса IgM отсутствуют. Заключение: хронический приобретенный токсоплазмоз. Рекомендации: этиотропная терапия не проводится; при необходимости специфическая терапия вне беременности; прерывание беременности не показано.
Лечение. Показанием к назначению этиотропной терапии у беременных женщин являются острый, подострый и инаппарантный токсоплазмоз. Лечение хронического токсоплазмоза следует проводить строго по клиническим показаниям либо до, либо после беременности. При отсутствии жалоб и клинических показаний не нуждаются в лечении женщины, переболевшие токсоплазмозом до беременности. Эти женщины расцениваются как практически здоровые лица, не требующие специального медицинского наблюдения. Лечение беременных женщин следует проводить не ранее 12–16 недель беременности (со II триместра беременности).
Назначаются препараты группы пириметамина (Фансидар, Ровамицин).
Фансидар содержит сульфадоксин 500 мг и пириметамин 25 мг. Этиотропная терапия состоит из 2–3 циклов. Назначается 1 таблетка 1 раз в 3 дня № 8 таблеток на цикл. Учитывая возможность угнетения кроветворения под действием этиотропных препаратов, рекомендуется назначение фолиевой кислоты (в средних терапевтических дозах), а также проведение общих анализов крови и мочи. При непереносимости препаратов группы пириметаминов назначают Ровамицин, 1 таблетка которого содержит спиромицина 3 млн МЕ. Назначают по 3 млн МЕ 3 раза в день с семидневным перерывом. Хорошая переносимость Ровамицина больными, отсутствие лекарственного взаимодействия, высокая эффективность позволяют назначать его для лечения токсоплазмоза у беременных. При непереносимости пириметаминов возможна замена на антибиотики, например, эритромицин.
Противопоказаниями для назначения Фансидара и его аналогов, а также сульфаниламидных препаратов и антибиотиков являются: нарушения эритропоэза с анемией, заболевания почек с нарушением их функций, заболевания печени, декомпенсация сердечной деятельности.
В зависимости от сроков беременности целесообразно проведение не менее двух полных курсов этиотропной терапии с перерывами между ними 1–1,5 месяца.
Как показала практика, у пациенток с инаппарантным течением острого токсоплазмоза хороший эффект дает комплексное применение Фансидара с иммуномодуляторами (Галовит, Полиоксидоний). Уже после первого цикла лечения наблюдается значительное снижение IgM.
Профилактика врожденного токсоплазмоза. Профилактика врожденного токсоплазмоза должна строиться с учетом того факта, что только первичное заражение женщины во время беременности может привести к инфицированию плода. Оптимально профилактика врожденного токсоплазмоза должна включать в себя обследование женщин детородного возраста на токсоплазмоз до или, в крайнем случае, во время беременности. Неиммунные беременные женщины должны быть обязательно взяты на диспансерное наблюдение и обследоваться на токсоплазмоз 1 раз в триместр.
Литература
- О выявлении и профилактике токсоплазмоза в Москве. Методические рекомендации (№ 25). М., 2007.
- Лысенко А. Я. Клиническая паразитология. Женева, 2002.
- Hill D., Dubey J. P. Toxoplasma gondii: transmission, diagnosis and prevention // Clin. Microbiol. Infect. 2002. № 10.
- Desmonts G., Couvreur J. Toxoplasmosis in pregnancy and its transmission to the fetus // Bull. N. Y. Acad. Med. 1974. № 2.
Ф. К. Дзуцева*
Г. Ю. Никитина**
Ю. В. Борисенко*
Л. П. Иванова***, кандидат медицинских наук, доцент
С. Х. Зембатова***
*Городской центр по токсоплазмозу, **ГКБ им. С. П. Боткина, ***РМАПО, Москва
Читайте также:

