В лондоне вылечили вич
Обновлено: 05.05.2024
Как сообщает New York Times, почти три года назад мужчине сделали пересадку стволовых клеток костного мозга от донора, имеющего врожденную резистентность к вирусу вследствие мутации одного их генов CCR5. Через 18 месяцев после отказа от антиретровирусной терапии врачи не нашли следов ВИЧ в организме, несмотря на использование самых чувствительных тестов.
Первый случай подобной элиминации вируса был зафиксирован 10 лет назад, когда в Берлине ВИЧ-положительному американцу по имени Тимоти Браун, больному лейкемией, также были пересажены гемопоэтические клетки от резистентного донора.
Сама пересадка была продиктована крайне токсичной химиотерапией, положенной в этом случае онкологическим больным и по факту уничтожающей собственную иммунную систему пациента.
Долгое время ученым не удавалось повторить указанный опыт и считалось, что технология, примененная при его лечении, не может быть воспроизведена на других пациентах, поскольку ее успех был случайностью.
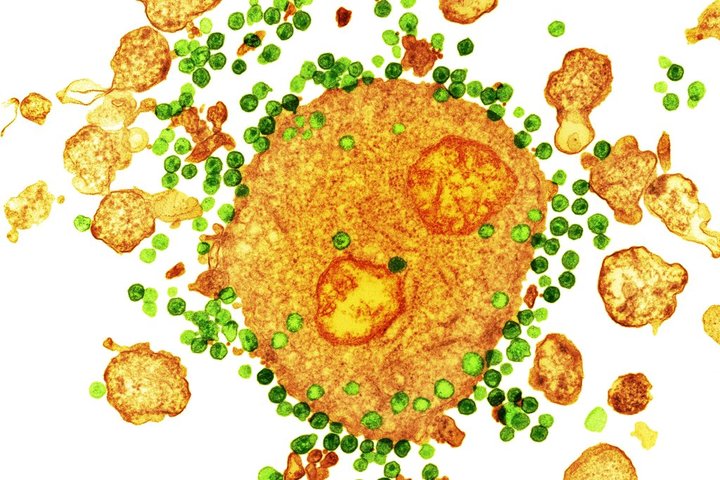
A colored transmission electron micrograph of the H.I.V. virus, in green, attaching to a white blood cell, in orange.CreditCreditNIBSC/Science Source
Напомним, что основной причиной, почему ВИЧ-инфекция до сих пор остается неизлечимой, несмотря на наличие препаратов высокоэффективной антиретровирусной терапии, способных прекратить ее размножение в организме, остается недоступность для медикаментов тех копий вируса, которые прячутся в так называемых клетках макрофагах и других резервуарах ВИЧ, одним из которых является костный мозг человека.
Ранее исследования пересадки стволовых клеток как технологии по элиминации вируса в организме человека были также апробированы на мавританских макаках-крабоедах.
Отдельное исследование по уничтожению вируса в макрофагах в 2018 году опубликовал журнал Nature. В статье говорилось о том, что ученым удалось очистить организм подопытных обезьян от SHIV — модифицированной версии человеческого вируса иммунодефицита, прячущегося именно в этих клетках.
Сделать это удалось с помощью двух веществ: антител PGT121, открытых семь лет назад в крови одного ВИЧ-положительного пациента из Африки, и лекарства GS-9620, стимулирующего работу гена TLR7, который отвечает за активацию врожденного иммунитета.
Как передается ВИЧ
ВИЧ может передаваться через:
- незащищенный половой акт (вагинальный или анальный) и оральный секс с инфицированным человеком;
- переливание зараженной крови;
- совместное использование загрязненных игл, шприцев, хирургического оборудования или других острых инструментов.
Он также может передаваться от матери к ребенку во время беременности, родов и кормления грудью.
На конец 2018 года во всем мире насчитывалось 37,9 млн человек, живущих с ВИЧ. С начала 1981 года инфекцией заразились около 74,9 млн человек, 32 млн во всем мире умерли от болезней, сопровождающих ВИЧ.
По оценкам Всемирной организации здравоохранения (ВОЗ), 0,8% взрослых в возрасте 15–49 лет во всем мире живут с ВИЧ. В России положительный статус имеют около 1 млн человек — это примерно 0,71% населения страны. Большинство случаев заражения связано с гетеросексуальными контактами и употреблением наркотиков — 62,7% и 33,6% соответственно.
Хотя сейчас нет доказанного лекарства от вируса иммунодефицита, существуют эффективные препараты, позволяющие большинству людей с вирусом жить долгой и относительно здоровой жизнью.
По данным ВОЗ, 86% людей, имеющих доступ к лечению, продемонстрировали уменьшение вирусной нагрузки. В России антиретровирусную терапию (так называется терапия комплексом лекарств, которые постепенно снижают вирусную нагрузку на пациента) получают 48,5% ВИЧ-положительных пациентов — у 76,3% из них врачи фиксируют снижение вирусной нагрузки.
Лондонским пациентом СМИ назвали второго в истории человека, полностью излечившегося от ВИЧ. Мужчина в течение года сохранял анонимность, но в начале марта в интервью The New York Times раскрыл свое имя и рассказал историю своей болезни: как, будучи ВИЧ-положительным, готовился умереть от лимфомы Ходжкина, но победил обе болезни.
В 2012 году во время планового осмотра у Кастильехо обнаружили лимфому Ходжкина на четвертой стадии. Лечение осложнялось тем, что проведение химиотерапии предполагало постоянный пересмотр схемы антиретровирусной терапии.
Спустя несколько лет лечение не привело к видимым результатам. В 2015 году Кастильехо предложили сделать операцию по пересадке костного мозга — для многих пациентов с лимфомой это последний шанс победить болезнь.
Подождите, как это произошло?
Пересадка происходит так: сначала врачи с помощью высоких доз лекарств в ходе химиотерапии убивают клетки костного мозга пациента, а затем внутривенно вводят донорские клетки костного мозга, которые при удачном проведении процедуры постепенно занимают положенное место.
Ученым удалось найти для Кастильехо донора с CCR5 delta 32 — мутацией, которая существует у небольшого количества людей и не позволяет вирусу ВИЧ-1 попасть в клетку тем путем, каким он обычно это делает.
Другими словами, подобная мутация делает носителей устойчивыми к ВИЧ. Над редактированием этого рецептора работал ныне заключенный в тюрьму китайский врач Цзянькуй Хэ, поставивший эксперимент по созданию первых в мире генетически модифицированных детей.
Спустя год после операции мужчина полностью восстановился и прекратил принимать препараты антиретровирусной терапии в октябре 2017 года. Все тесты, взятые у него в последующие 18 месяцев, показывали нулевую вирусную нагрузку — это значит, что в течение 1,5 лет у Кастильехо наблюдалась ремиссия, что можно расценивать как победу над ВИЧ.
Что это значит для науки и для ВИЧ-положительных
Во-первых, пересадка костного мозга — дорогая и очень опасная процедура, на которую врачи могут пойти только в случае, если для отдельно взятого пациента отсутствуют другие стратегии лечения. Дело в том, что такая процедура может привести к ряду тяжелых осложнений вплоть до летального исхода — поэтому врачи прибегают к этой операции только в крайних случаях.
Во-вторых, для лечения ВИЧ клетки самого пациента не подходят, а найти гистосовместимого донора очень сложно. Если даже клетки донора подходят для пересадки конкретному пациенту, для успеха процедуры необходимо содержание в них фермента CCR5 delta 32. Это редкая мутация, носителем которой является каждый сотый житель Земли.
В-третьих, даже при соблюдении гистосовместимости и наличия CCR5 delta 32 процедура может пройти неудачно. Дело в том, что фермент не позволяет ВИЧ заразить клетки обычным способом, уцепившись за определенный белок. Однако вирус может вступить в контакт и с другим белком. Это означает, что массово лечить ВИЧ таким же способом, как в случае Кастильехо, не получится.
Жителю Лондона, чье имя скрывает медицинская тайна, в 2003 году поставили диагноз ВИЧ. Поскольку вирус ослабляет иммунитет, одним из частых осложнений у ВИЧ-инфицированных больных становится рак. Лондонского больного в 2012 году настигло опасное злокачественное заболевание, лимфома Ходжкина. Болезнь перешла в тяжелую стадию, и единственным шансом для спасения жизни была пересадка костного мозга. Донором стал человек с особой генетической мутацией, так называемой CCR5 delta 32.
Лондонский пациент перенес пересадку костного мозга успешно, хотя это весьма рискованная процедура. Более того, после пересадки у него в крови стало уменьшаться количество вирусных частиц. А затем и вовсе исчезли следы вируса иммунодефицита. Даже после того, как в течение полутора лет не применялись препараты против ВИЧ (антиретровирусная терапия), болезнь не вернулась.
МЕТОД БУДУЩЕГО - РЕДАКТИРОВАНИЕ ГЕНОМА ВМЕСТО ТРАНСПЛАНТАЦИИ
Профессор Равиндра Гупта, который возглавлял научно-медицинскую команду для спасения больного, дает объяснения с осторожностью. Пока он говорит не о полном излечении ВИЧ, а о долгой ремиссии. Однако многие эксперты считают этот медицинский случай очень серьезным успехом в борьбе против СПИДа.
- История лондонского пациента подтверждает правильность революционного подхода к лечению ВИЧ, - говорит Юрий Дейгин. - А именно, речь идет о передаче больному особой генной мутации, делающей человека невосприимчивым к ВИЧ-инфекции. На сегодня этого реально достичь путем пересадки костного мозга от донора с мутацией CCR5 delta 32. В дальнейшем, если успешно будут решены этические и медицинские вопросы (безопасность, эффективность), возможно удастся не прибегать к пересадке всего костного мозга, а модифицировать нужным образом ДНК только иммунных клеток ВИЧ-инфицированных людей с помощью генной терапии. Или даже в качестве профилактики вносить необходимые мутации человеку еще до рождения - как это недавно сделал китайский генетик Хэ Цзянькуй, в результате чего родились генно-модифицированные близняшки Лула и Нана. Но такая генная терапия - еще вопрос отдаленного будущего. В частности, редактирование генома при рождении в медицинским целях может стать доступным, думаю, не раньше чем лет через 15 - 20.
- Подход, который был использован в случае лондонского пациента, действительно перспективный. Однако в ближайшее время он вряд ли перейдет в клиническую практику лечения ВИЧ, - считает руководитель Института персонализированной медицины Сеченовского университета, доктор медицинских наук Филипп Копылов. - Пересадку костного мозга, которая является единственным методом спасения при ряде онкологических заболеваний крови, маловероятно начнут массово использовать именно для лечения ВИЧ. Потому что, с одной стороны, есть эффективная антиретровирусная терапия (при ее грамотном применении и строгом соблюдении пациенты с ВИЧ живут столько же, сколько люди без вируса. - Ред.). С другой стороны, пересадка костного мозга это очень рискованная и тяжелая для организма процедура. Ведь по сути родной костный мозг человека полностью заменяется на другой, и идет столкновение двух систем. Нужно бороться с отторжением. В то же время для науки и медицины очень важно понимание и подтверждение, что определенная мутация может быть полезна в борьбе против ВИЧ. Именно в этом направлении нужно работать.
КСТАТИ
- Обратите внимание: пересадка костного мозга в обоих случаях применялась как метод для лечения онкологических заболеваний, - подчеркивает профессор Филипп Копылов. - Чтобы лечить таким образом именно ВИЧ, необходимо официально зарегистрировать данное медицинское показание для метода лечения. А для этого нужны клинические испытания, одобрение соответствующего органа (в США - FDA) и т.д.
Возрастная категория сайта 18 +
Спустя год с тех пор, как мир узнал о лондонском пациенте — втором человеке в истории, излечившемся от ВИЧ, — он вышел из тени, чтобы раскрыть свою идентичность. Это Адам Кастильехо.
Его рост метр восемьдесят, это крепкий длинноволосый мужчина с приятной улыбкой. Адаму Кастильехо 40, он излучает жизнерадостность и здоровье. Но его путь к исцелению был изнурительным и мучительным, он включал почти десять лет лечения и полного отчаяния.
В прошлом марте ученые объявили, что мистер Кастильехо, которого тогда называли исключительно лондонским пациентом, вылечился от ВИЧ после пересадки костного мозга. У донора была редкая мутация — неспособность инфицироваться ВИЧ, и, по сути, иммунную систему Кастильехо заменили устойчивой к вирусу. Метод, оказавшийся настолько эффективным, использовался для лечения рака и не подходит для повсеместного лечения ВИЧ из-за связанных с ним высоких рисков.
Кастильехо готовился открыться шаг за шагом: создал отдельную электронную почту и телефонный номер для жизни в роли лондонского пациента, или, как он сам себя называет, ЛП, завел аккаунт в Твиттере. Кроме того, стал еженедельно общаться с мистером Брауном, единственным человеком в мире, который мог полностью понять, что ему пришлось пережить. В декабре Кастильехо подготовил заявление, которое прочитал продюсер на Радио 4 BBC.
Кастильехо вырос в Каракасе. Его отец был испанско-голландского происхождения (что оказалось крайне важным для лечения) и работал пилотом в экотуристической компании. Мужчина с почтением отзывается об отце, который умер 20 лет назад, и на которого он очень похож. Но родители развелись, когда он был еще ребенком, так что в основном его воспитывала мать (она и сейчас живет с ним в Лондоне).
За этим последовали годы жесткой химиотерапии. Ситуацию усугублял ВИЧ-статус мужчины. Каждый раз, когда онкологи налаживали его лечение, инфекционистам приходилось менять препараты антиретровирусной терапии, рассказал доктор Саймон Эдвардс, который был посредником между двумя командами врачей.
В то же время от очередного варианта лечения, которое должно было помочь, но не помогало, Кастильехо становилось все хуже. Он видел, как другие пациенты в клинике умирают или поправляются, а он возвращался снова и снова. При этом его тело слабело с каждым раундом.
В конце 2014 года многолетняя невыносимая физическая и эмоциональная нагрузка сделала свое дело, и за две недели до Рождества Кастильехо исчез. Друзья и семья подали заявление о пропаже, а через четыре дня его нашли в пригороде Лондона с провалом в памяти: он не помнил, как туда попал и что делал перед этим.
Весной 2015 года врачи сказали, что он не доживет до Рождества. Последний вариант, когда не остается никаких других, который предлагают людям с лимфомой, — трансплантация донорского костного мозга. Но у его врачей не было такого опыта, тем более с ВИЧ-положительными людьми.
Тогда он вместе с близким другом Питером стал искать альтернативы, к кому обратиться. И нашел. В одной лондонской больнице работает доктор Йен Гэбриел, эксперт по пересадке донорского костного мозга для лечения рака, в том числе людям с ВИЧ.
Уже через неделю он встретился с доктором Гэбриелом, который попытался в третий и последний раз использовать собственные стволовые клетки пациента для пересадки. Когда это не сработало, врач объяснил, что латиноамериканское происхождение Кастильехо может усложнить поиск донора костного мозга с полностью совпадающим генетическим профилем иммунной системы. Но совпадения с несколькими донорами нашлись на удивление быстро, включая одного из Германии — видимо, благодаря наследственности отца, наполовину голландца, — и у этого донора была крайне редкая генетическая мутация CCR5 Дельта 32. Из-за нее ВИЧ не может проникнуть в CD4+ клетки, и, соответственно, люди становятся устойчивы к вирусу иммунодефицита. Трансплантация костного мозга этого донора давала надежду вылечить как рак, так и ВИЧ.

Кастильехо до сих пор настойчиво называет себя ЛП, а не Адамом. Он намерен насладиться своей личной жизнью по полной программе. Фото: Эндрю Теста для The New York Times.
Эдвардс привлек доктора Гупту, своего бывшего коллегу, одного из немногих вирусологов в Лондоне, занимавшихся исследованиями ВИЧ. Изначально Гупта был настроен скептически, ведь такой метод сработал лишь однажды, 12 лет назад, с берлинским пациентом Брауном.
Доктор Гупта стал очень пристально наблюдать за Кастильехо. В конце 2015 года, когда он готовился к трансплантации, возникла новая серьезная проблема — подскочила вирусная нагрузка, так как вирус оказался устойчив к препаратам, которые он принимал. Операцию отложили на несколько месяцев, пока не подобрали необходимую терапию. Наконец, пересадку провели 13 мая 2016 года.

Доктор Саймон Эдвардс, который занимался Адамом Кастильехо с 2012 года, служил посредником между командой онкологов и специалистами по инфекционным заболеваниям, которые занимались терапией ВИЧ.
Фото: Эндрю Теста для The New York Times.
Даже когда он вышел из больницы, из всех занятий врачи разрешили ему только прогулки. Поэтому он часами гулял по своему фешенебельному району Шордич. Каждое воскресенье он заходил на цветочный рынок и награждал себя бейглом с солониной, чтобы отметить очередную маленькую победу и полюбоваться яркими росписями на стенах и винтажными нарядами.
Через год, окрепнув, он стал задумываться, не прекратить ли ему принимать терапию от ВИЧ, чтобы узнать, избавился ли он от вируса. Он принял последнюю дозу антиретровирусных препаратов в октябре 2017 года. Семнадцать месяцев спустя, в марте 2019 года, доктор Гупта объявил о его исцелении.
Ни врач, ни сам Кастильехо не были готовы к тому, что произошло после. Доклад доктора Гупты на конференции встречали стоячей овацией, ему пожимали руки дюжины врачей. А лондонского пациента завалили 150 запросами СМИ, которые просили открыть лицо и имя. Только тогда Кастильехо начал понимать, какую роль может сыграть в просвещении людей в области лечения рака, ВИЧ и пересадки костного мозга.
Никто не знал, что убило Роберта Рейфорда. Афроамериканскому мальчику было всего 15, когда он оказался в городской больнице Сент-Луиса в конце 1968 года, и медики не смогли понять, что с ним.
Необъяснимая опухоль в районе гениталий быстро распространилась по всему телу Рейфорда. Хламидии, обычно локализующиеся в области заражения, циркулировали по его кровеносной системе. Мелкая пурпурная сыпь на внутренней стороне бедра подсказывала, что это рак, но такую форму обычно встречали только у пожилых евреев-ашкенази и итальянцев, а не у чернокожих подростков, никогда не покидавших Миссури.
по теме

Общество
Цветные женщины: стареющие, невидимые, ВИЧ-позитивные
Это открытие доказало, что СПИД появился в США более чем на десятилетие раньше, чем предполагали популярные теории, и отвело Рейфорду сомнительное место в истории ретровируса, который с тех пор убил порядка 35 миллионов людей во всем мире.
Резервуары и недобитые вирусы
по теме

Общество
Как отбеливают историю ВИЧ: смерть чернокожего подростка от СПИДа в 1969 году
Редкая мутация и опасная процедура
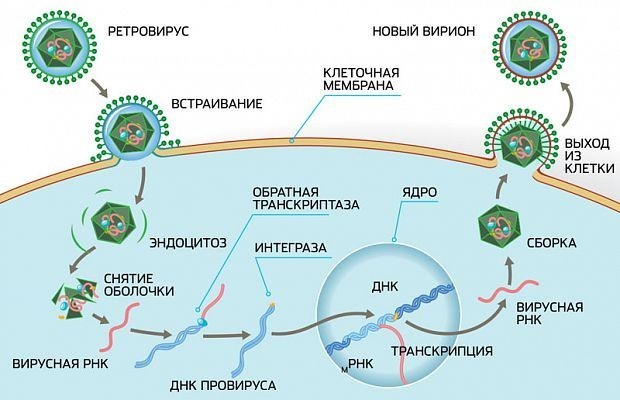
Ученые выбрали донора с редкой генетической мутацией — устойчивостью к ВИЧ. Чтобы вирус иммунодефицита попал в клетку, ему необходимо прикрепиться к белку CCR5, находящемуся на поверхности самой клетки. А мутация как раз меняет форму этого белка, не позволяя вирусу закрепиться и проникнуть внутрь.
Иммунная система Лондонского пациента была восстановлена с помощью таких устойчивых к заражению клеток, тем самым ВИЧ был полностью удален из его организма.
Но лечение Брауна было гораздо серьезнее: он пережил облучение всего тела и две пересадки стволовых клеток, каждая из которых смертельно опасна, если клетки не приживутся. Были случаи, когда несколько пациентов, прошедших через подобное, умерли: из-за рецидивов рака, самой процедуры трансплантации, либо снова заболели ВИЧ.
Во-первых, ее слишком опасно назначать людям, получающим антиретровирусную терапию и уже ведущим здоровую жизнью. Во-вторых, трансплантация стволовых клеток связана с риском: когда клетки не приживаются, тело бунтует и даже может убить пациента. И, в-третьих, для процедуры нужно найти донора с мутацией CCR5, также имеющего сходный с пациентом состав крови. А это крайне редкая комбинация факторов.
Для Гупты главный итог эксперимента с Лондонским пациентом — не столько сама операция, сколько подтверждение идеи, что через работу с CCR5 можно излечиться от ВИЧ. Он считает, что самый очевидный способ использования этого открытия — редактирование генов. Хотя изменение генома человека в профессиональном сообществе вызывает дискуссии, в том числе и с этической точки зрения.
Так, в ноябре 2018 года стало известно, что в Китае рождены генетически модифицированные девочки-близнецы. Их особенность — врожденный иммунитет против ВИЧ-инфекции. Эксперимент провел профессор Хэ Цзянькуй из Южного университета науки и технологий в Шэньчжэне.
Но Гупта ищет иные варианты генных модификаций. Редактирование генов эмбрионов влияет на все клетки будущего взрослого, и эти изменения передаются будущим поколениям. Но редактирование клеток взрослого не приводит к таким последствиям. Главная проблема — убедиться в аккуратности процедуры. Кроме того, потребуются десятилетия, если это вообще возможно, чтобы сделать эту процедуру более простой.
Читайте также:

