Замершая беременность из-за гематогенной инфекции
Обновлено: 07.05.2024
При беременности у женщины происходит природное снижение иммунитета абсолютно во всех случаях. Это норма, необходимый процесс для вынашивания ребенка, профилактика отторжения плода как чужеродного в принципе организма. Потому инфекции, которые до момента зачатия дремали, становятся активными. Это опасно для плода, особенно в первые 3 месяца после зачатия.
Факты о ВУИ
В менее чем 10 беременностях из 100 инфекция передается будущему малышу от его мамы. И примерно 0,5% новорожденных появляются на свет с соответствующими симптомами. Но, если в организме матери присутствует та или иная инфекция, это еще не полная гарантия того, что она будет и у ребенка.
Часть инфекционных болезней, которые угрожают развитию эмбриона, для матери проходят безсимптомно, не нанося особого вреда ее организму. В основном плод заражается той же инфекцией, что и мать, если она заразилась этой болезнью впервые.
Если у беременной вовремя обнаружить и пролечить болезнь, то риск для будущего малыша минимальный.
Как заражается эмбрион?
ВУИ развивается тремя путями:
- гематогенным или трансплацентарным, как например, вирусы, листериоз, токсоплазмоз, сифилис (заражение в первом триместре приводит к уродствам малыша и порокам развития; при заражении эмбриона в последние 3 месяца гестации новорожденный появляется на свет с симптоматикой острой формы заболевания)
- восходящим (так могут передаваться герпетическая инфекция, хламидиоз, микоплазмоз; ребенок заражается через половые пути женщины, в основном это происходит при родах. Если инфекция попала в околоплодные воды, у ребенка будет поражен ЖКТ, дыхательный пути, кожа)
- нисходящим (инфекция попадает к эмбриону через маточные трубы, что бывает, если у матери развивается оофорит, аднексит)
Возбудители ВУИ
Большая часть бактерий и вирусов может передаваться еще нерожденному ребенку, что вызывает серьезные последствия. Те вирусы, которые провоцируют острые респираторные вирусные заболевания, к плоду не попадают. Они могут быть опасны для малыша, только если беременная женщина имеет высокую температуру.
Краснухой мать может заразиться воздушно-капельным путем. Не обязательно при этом находиться вплотную к больному человеку, заражение вероятно и на расстоянии. При этом последствием для плода станет фетальный синдром краснухи.
Цитомегаловирус передается через биологические жидкости. В основном это слюна, но может быть сперма и моча, а также кровь. У ребенка инфекция может проявиться соответствующей симптоматикой после рождения, а может протекать в латентной форме.
Вирус простого герпеса 2 передается в основном при незащищенном половом акте. Если такое случилось у беременной, то ее ребенок родится с врожденной формой герпеса. Парвовирус В19, как и краснуха, передается воздушно-капельным путем беременной женщине. В итоге у плода возникает водянка и анемия.
Ветряная оспа передается не только по воздуху, но и бытовым путем. Ребенок получает при внутриутробном инфицировании пороки развития (если заражение произошло в первом триместре). Если заражение случилось перед родами, то будет врожденная форма данного заболевания, и это очень опасное состояние.
Листериоз (это бактериальная инфекция) может развиться у беременной, если она кушает зараженные сыры, мясо или овощи. У ребенка развивается в итоге пнемония и/или сепсис. Сифилис беременным передается половым путем, если партнер был заражен. У ребенка после рождения развивается эта болезнь со всеми вытекающими последствиями. Туберкулез, что также является бактериальной инфекцией, передается по воздуху. Эмбрион может умереть в утробе матери, родиться раньше срока, с врожденной формой туберкулеза.

Последствия внутриутробной инфекции
Врожденное заражение может быть острым или хроническим. Последствия острого инфицирования:
- шок
- пневмония
- тяжелый сепсис
Симптомы острой внутриутробной инфекции у новорожденных:
- уменьшающаяся с каждым днем активность
- длительный сон
- плохое питание
Но в большинстве случаев симптоматики нет. Отдаленные последствия ВУИ:
- задержка двигательного развития
- психические проблемы
- нарушения зрения
- частичная или полная глухота
Если инфекция проникла через матку, последствиями могут быть:
- мертворождение
- антенатальная гибель эмбриона
- выкидыш
Если плод выжил, у него будут такие проявления ВУИ:
- Лихорадка
- Кожные высыпания
- Водянка плода
- Анемия
- Желтуха и увеличенная печень
- Пневмонии
- Миокардит
- Хориоретинит, катаракта
- Микро- и гидроцефалия
Внутриутробное инфицирование опасно вне зависимости от срока гестации. Но некоторые возбудители болезней опаснее всего в первые 3 месяца. Яркий пример — вирус краснухи. Очень серьезные последствия будут при заражении на самой последней недели беременности матери ветряной оспой. Последствия могут быть самыми разными. О них можно узнать у своего врача по результата УЗИ, анализов, сроку беременности и обнаруженному возбудителю болезни. Это значит, что каждый случай индивидуален в плане протекания болезни и в плане последствий.
Группы риска по внутриутробному заражению
Осторожными нужно быть женщинам, которые:
- проживают в семье с детьми, которые ходят в детсад, школу, другие учреждения
- работают в сфере медицины, контактируя с носителями болезней или больными людьми
- работают в дошкольных и школьных детских учреждениях
- имеют 2 и больше медицинских аборта
- больны воспалительными патологиями, протекающими в хронической форме
- имеют несвоевременное излитие околоплодных вод
- имеют в анамнезе пороки развития эмбриона и антенатальную гибель плода
- когда-то родили зараженного ребенка (одного или больше)
Симптомы и последствия
Ниже перечислены признаки, которые указывают на инфекцию у беременной:
- кашель, одышка
- сыпь
- лимфоузлы болезненны и увеличены
- высокая температура
- болезненность и припухлость суставов
- насморк, слезотечение, конъюнктивит
- боль в груди
Но эти симптомы в некоторых случаях указывают на аллергическую реакцию. Если это так, то нет риска внутриутробной инфекции малыша. В любом случае, при появлении одного и больше из выше перечисленных признаков нужно идти на очную консультацию к врачу.
ЦМВ (цитомегаловирус)
ЦМВ (цитомегаловирус) относится к группе герпесовирусов. Им заражаются при половых контактах, при тесных бытовых контактах, а также через кровь (если была сделана операция грязными инструментами или переливание от больного донора). Если имело место первичное заражение беременной, то вирус попадает в плаценту, а оттуда к малышу. У ребенка может не быть последствий, что и бывает в большинстве случаев. Но 10 из 100 детей, у которых были больные матери, рождаются с симптоматикой ВУИ.
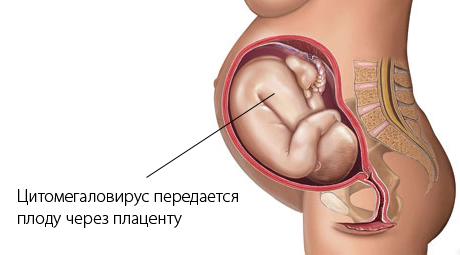
Последствиями внутриутробного заражения ЦВМ могут стать выкидыши и мертворождения, а также:
- нейросенсорная тугоухость
- недовес при рождении
- гидроцефалия
- микроцефалия
- пневмония
- гепатоспленомегалия
- задержка психомоторного развития
- слепота различных степеней
Если имело место тяжелое сочетанное поражение, 1/3 новорожденных умирают в первые 2-3 месяца после родов. Также очень вероятны такие отдаленные последствия как умственная отсталость, слепота и глухота. Если заражение легкое, то последствия мене серьезные. На сегодня нет лекарства, которое бы помогло при проявлениях цитомегаловируса у недавно рожденных детей. При заражении беременной ЦВМ беременность не прерывают, потому что у ребенка может и не быть симптомов. Врачи прописывают для беременной лечение, чтобы минимизировать развитие осложнений.
ВПГ (вирус простого герпеса)
Врожденная герпетическая инфекция развивается, если у беременной был ВПГ, особенно 2 тип (который передается половым путем). Симптомы появляются в первый месяц после рождения. В основном ВУИ происходит при первичном инфицировании беременной. Ребенок подхватывает инфекцию в большинстве случаев при родах, когда проходит через родовые пути. Но возможность передачи возбудителя болезни через плаценту также нужно учитывать.
Последствия герпеса для ребенка:
- вялость, плохой аппетит
- выкидыш, мертворождение
- характерные высыпания на коже
- лихорадка
- нарушение свертываемости крови
- желтуха
- поражение мозга
- поражение глаз
- пневмония
Тяжелый врожденный герпес чреват инвалидизацией ребенка:
Краснуха
Краснуха очень опасна для эмбриона! Она вызывает различные уродства. Самый высокий риск приходится на беременность до 16-й недели. Последствия ВУИ возбудителем данной болезни:
- микроцефалия
- маловесность при рождении
- выкидыш, мертворождение
- пороки сердца
- глухота (в половине случаев ВУИ)
- катаракта
- поражение кожи
- пневмония
- гепатоспленомегалия
- менингит и энцефалит
Парвовирус В19
Последствия для ребенка при ВУИ:
- отеки
- анемия
- поражение мозга
- гепатит
- миокардит
Ветряная оспа
Если больная заразилась ветрянкой, это очень опасно для плода. Если беременная заразилась, а ей в скором времени срок рожать, то есть риск, что ее ребенок умрет. Плод заражается в 25 случаях из 100, но симптомы проявляются не всегда.
Врожденная ветрянка у малышей имеет такие признаки:
- повреждение мозга
- атрофия зрительного нерва, недоразвитие глаз
- недоразвитие конечностей
- сыпь, рубцы зигзагообразной формы
- пневмония
Новорожденных при ВУИ ветрянкой не лечат, потому что симптоматика не прогрессирует. Если мать заразилась за 5 суток до дня родов и позже, врачи могут советовать ввести новорожденному иммуноглобулин, потому что ему не передались антитела от матери.
Гепатит В
- гепатит В с последующим выздоровлением
- рак печени
- носительство и хроническая форма гепатита типа В
- острая форма гепатита (развивается печеночная недостаточность, ребенок умирает)
- задержка психомоторного развития
- нехватка кислорода
- маловесность
- выкидыш, мертворождение
ВИЧ-инфекция
Вирус иммунодефицита человека (ВИЧ) поражает особые иммунные лимфоциты. Заражение происходит в основном половым путем. Ребенок заражается, прибывая в утробе матери, или проходя при рождении через инфицированные половые пути роженицы. Если не лечить ребенка с врожденной формой ВИЧ, он не выживет даже двух лет, потому что вирус быстро прогрессирует в слабом организме. Смерть происходит от инфекций, которые у здоровых детей не могут привести к летальному исходу.
Чтобы обнаружить ВИЧ у новорожденного, в основном применяется ПЦР. В первые 3-6 месяцев после рождения нет смысла делать анализ на антитела. Важно обнаруживаться ВИЧ у тех, кто ждет ребенка. Им весь срок дают антиретровирусные лекарства, то есть в основном с 4-й недели гестации дается зидовудин. Они не должны кормить грудью своег7о новорожденного. Это в разы повышает шансы здоровья малыша.
Листериоз
Эта болезнь вызывается бактерией листерией. Она может проникать к эмбриону через плаценту, чего не могут многие бактерии. Пути заражения описаны выше. У беременной проявлений болезни может и не быть. В части случаев присутствуют:
- высокая температура
- понос
- рвота
- симптомы, похожие на таковые при гриппе
Последствия заражения плода:
- множественные гнойные очаги, сыпь
- сепсис
- менингит
- лихорадка
- отказ от еды
- мертворождение, спонтанный аборт
Если симптоматика проявилась в первые 7 дней после родов, то дети умирают в 60 случаях из 100. Потому, если у беременной точный диагноз листериоза, ей на 2 недели приписывают ампициллин. ВУИ также лечится, если ребенок действительно заразился от матери.
Сифилис
Первичный сифилис у беременных, который не лечили, передается почти в 100 случаях из 100. Из 10 детей погибают при этом 6, у других обнаруживается врожденная форма болезни. У больной беременной сначала образуется первичная язва, а потом болезнь переходит в латентную форму, время от времени обостряясь.
Заражение эмбриона происходит, даже если у матери болезнь протекает в скрытой форме, с 4-й недели гестации. Последствия ВУИ такие:
- глухота задержка психического развития
- поражение глаз, ушей, рук, ног, зубов
- трещины на коже
- высыпания на кожных покровах
- анемия, желтуха у малыша
- преждевременные роды или рождение мертвого плода
Токсоплазмоз
Передается человеку в основном от кошек, но может передаваться и от других животных. Заразиться беременная может, когда убирает за питомцем или кушает недостаточно термически обработанное мясо, грязные овощи. К моменту беременности большинство женщин уже болели этой болезнью, потому ребенку она не передастся.
При первичном заражении в период беременности в 50 случаях из 100 возбудитель преодолевает плацентарный барьер, заражая эмбрион. Последствия ВУИ для младенца:
- гидро-, микроцефалия
- поражение глаз
- желтуха, увеличение печени и селезенки , менингит, судороги
- мертворождение, выкидыш
- задержка психомоторного развития
TORCH-инфекции
Торч-инфекциями называются такие:
Они опасны при заражении беременной. Некоторые протекают в скрытой или стертой форме, потому их нужно выявлять анализами. Потому на этапе планирования зачатия пара сдает анализы на TORCH-инфекции. Если в организме будущей мамы не обнаруживаются антитела к возбудителю краснухи, ей делают прививку. Также во время беременности лучше не контактировать с кошками, чтобы не заразиться токскоплазмозом.
Диагностика внутриутробной инфекции
Беременным делают анализ крови, который позволяет обнаружить гепатиты В и С, а также сифилис. Регулярно делают мазки из влагалища на микрофлору. Используется метод ПЦР, который позволяет обнаружить циркулирующие в крови вирусы при наличии таковых.
УЗИ безопасна для беременных. Она не показывает наличие инфекции, но дает возможность обнаружить пороки, вызванные инфекцией, и задержку внутриутробного развития плода. Также УЗИ является методом контроля при выполнении кордоцентеза. ВУИ подозревают, если на УЗИ обнаруживаются такие признаки:
- сформировавшиеся пороки развития
- много- или маловодие
- отек плаценты, амниотические тяжи
- синдром задержки внутриутробного развития
- увеличение живота и расширение чашечно-лоханочной системы почек
- увеличение сердца, печени и селезенки
- множественные отложения кальция в мозге, печени, кишечнике
- увеличение желудочков мозга
Сероиммунологический метод диагностики базируется на определении иммуноглобулинов. Он рекомендован женщинам из групп риска, которые перечислены выше. Иногда необходимы такие методы как кордоцентез и амниоцентез. При первом методе берется кровь из пуповины, чтобы выявить имеющуюся там инфекцию. Амниоцентез означает исследование околоплодных вод.
У новорожденного, если у врача имеется подозрение на ВУИ, берут анализы биологических жидкостей, например, слюны или крови.
Цитомегаловирусная инфекция у беременных — это клинически манифестное или латентно протекающее инфекционное заболевание, вызванное цитомегаловирусом, возникшее до зачатия или во время гестации. Проявляется гипертермией, катаральными симптомами, шейным и подчелюстным лимфаденитом, сиалоаденитом, общей интоксикацией, беловато-голубыми белями, реже — гепатомегалией, спленомегалией, генерализованной лимфаденопатией. Диагностируется с помощью серологических и молекулярных лабораторных методов. Лечение проводится специфическим человеческим иммуноглобулином, рекомбинантным альфа-2-интерфероном, при тяжелом течении — синтетическими аналогами нуклеозидов.
МКБ-10
Общие сведения
Цитомегаловирусная инфекция (цитомегалия, ЦМВИ) — одно из наиболее распространенных инфекционных заболеваний, внутриутробно поражающих плод и вызывающих различные врожденные аномалии. В зависимости от региона антитела к цитомегаловирусу определяются у 40-98% пациенток репродуктивного возраста. Цитомегалия чаще встречается в группах населения с низким уровнем социального и экономического развития. В России серопозитивными к ЦМВИ являются до 90% женщин, инфицированность среди беременных старше 30 лет достигает 97-98%. В европейских странах врожденная цитомегалия выявляется с частотой 3-5 случаев на 1000 родов, в других государствах этот показатель составляет от 0,2 до 2,2%.

Причины
Заболевание вызывается крупным ДНК-содержащим цитомегаловирусом (ЦМВ), принадлежащим к семейству герпес-вирусов. Специалисты выделяют три штамма возбудителя, каждый из которых может самостоятельно инфицировать организм одного и того же человека. Заражение происходит до зачатия либо во время беременности. Вирусы пожизненно персистируют в организме женщины, поражая практически все виды тканей. Часть инфекционистов считает ЦМВ условно-патогенным микроорганизмом, клинически значимая реактивация которого наблюдается только при значительном угнетении иммунитета.
Усиление патогенности цитомегаловируса в гестационном периоде связано с физиологической иммуносупрессией, защищающей генетически чужеродный плод от отторжения. Под влиянием эстрогенов, прогестерона, кортизола у беременной уменьшается абсолютное и относительное количество Т-лимфоцитов, непосредственно участвующих в элиминации вирусов и поврежденных клеток, снижается их цитотоксичность. В результате ускоряется репликация цитомегаловирусов, они быстрее распространяются по организму и при недостаточном уровне защитных антител преодолевают плацентарный барьер.
Патогенез
Особенностью цитомегаловирусной инфекции является множественность путей заражения. Вирус распространяется аэрогенным, контактным, фекально-оральным, гемотрансфузионным, половым, вертикальным способами, в том числе трансплацентарно от беременной к плоду. Из-за сравнительно низкой вирулентности для инфицирования важен тесный контакт с зараженным. Возбудитель ЦМВИ определяется практически во всех биологических средах: слюне, крови, моче, слезной жидкости, ликворе, грудном молоке, цервикальном, вагинальном, уретральном секрете, сперме, слизи из прямой кишки, околоплодных водах.
После попадания в организм цитомегаловирусы адсорбируются на поверхности клеток, проникают в них, проходят полный цикл репликации ДНК, после чего сформированные вирионы распространяются на соседние клетки, с кровью разносятся по организму. Наиболее чувствителен к вирионам протоковый эпителий слюнных желез, в первую очередь околоушных, других экзокринных желез.
После лимфогенной и гематогенной генерализации обычно наступает фаза непродуктивной инфекции (скрытого носительства) с длительным сохранением вирусной частицы внутри зараженной клетки и передачей при делении дочерним клеткам. У женщин с нормальным иммунитетом клиническая манифестация не происходит, заболевание сразу приобретает характер носительства. Цитомегаловирус может длительное время персистировать в неактивной форме в чувствительных клетках. Проникновение ЦМВ в лимфоциты и мононуклеары обеспечивает его защиту от противовирусных антител.
При падении иммунитета у беременных возможна реактивация цитомегаловирусной инфекции с разрушением ядер клеток, в которых персистировал вирус, гематогенной диссеминацией, поражением железистых органов, развитием васкулитов, индукцией специфического цитомегалического метаморфоза клеток разных тканей. При гестации вирусы из межворсинчатого пространства проникают через плаценту и гематогенно инфицируют плод. Установлено, что ЦМВ способен повреждать мембрану трофобласта.
Классификация
Систематизация основных форм цитомегаловирусной инфекции у беременных проводится с учетом выраженности клинической картины и времени манифестации патологического процесса. Такой подход наиболее оправдан с точки зрения прогнозирования возможных осложнений заболевания и выбора оптимальной тактики ведения беременности. Специалисты в сфере акушерства и гинекологии, инфекционных болезней различают следующие варианты инфекции:
- Первично-манифестнаяЦМВИ. Самый неблагоприятный вариант течения патологии. Возникает в результате первичного инфицирования беременной, у которой отсутствуют специфические IgG. Отличается высокой вероятностью трансплацентарного переноса вируса (до 30-75%) и внутриутробного поражения плода. В период гестации выявляется не более чем у 4% пациенток. При заражении с острой симптоматикой в I триместре рекомендован аборт.
- Носительство. Наиболее частая форма цитомегаловирусной болезни у беременных. Носительницами являются женщины, у которых до зачатия была активная форма заболевания или инфекция на фоне сильного иммунитета сразу перешла в непродуктивную фазу. Иммуноглобулины G, циркулирующие в крови пациентки, защищают плод от заражения ЦМВ. При исключении иммуносупрессорных воздействий риск патологического течения гестации минимален.
- Реактивация латентной инфекции. При значительном снижении иммунитета у носительниц цитомегаловируса развивается характерная клиническая картина. Заболевание в той или иной степени обостряется у 40-50% серопозитивных беременных. В 0,15-0,36% случаев вирус передается трансплацентарно ребенку. Наибольший риск врожденных аномалий наблюдается при обострении цитомегаловирусной болезни на 7-12 неделях гестационного срока.
Симптомы ЦМВИ у беременных
Возможны беловато-голубые влагалищные выделения. При существенном снижении иммунитета определяется увеличение печени, селезенки с появлением тяжести, дискомфорта, распирания в правом и левом подреберьях, генерализованное увеличение лимфоузлов. Длительность острой фазы, как правило, составляет до 2-3 недель.
Осложнения
Осложненное течение гестации наблюдается преимущественно при острой или реактивированной инфекции. У таких пациенток чаще возникают спонтанные выкидыши, связанные с тяжелыми эмбрио- и фетопатиями, преждевременные роды, вызванные гипертонусом матки, замершие беременности, мертворождение. Из-за повреждения мембраны трофобласта ЦМВИ может осложниться приращением плаценты, гипертрофией и ранним старением плацентарной ткани, фетоплацентарной недостаточностью, внутриутробной гипоксией и задержкой развития плода.
Во время родов возможна преждевременная отслойка плаценты, массивная кровопотеря из-за атонического кровотечения. В послеродовом периоде отмечаются латентные эндометриты. В последующем повышается вероятность развития дисменореи.
При острой первичной цитомегаловирусной болезни существенно возрастает риск трансплацентарного инфицирования плода и развития многоводия. Дети зачастую рождаются недоношенными, с низкой малой тела. Особенно опасно заражение ЦМВ в 1-м триместре, часто вызывающее микроцефалию, хориоретинит, нейросенсорную тугоухость, другие аномалии развития.
Врожденная цитомегалия после внутриутробного инфицирования может протекать бессимптомно, проявляться тяжело протекающими манифестными формами или в виде последствий поражения отдельных органов (гепатомегалии, затяжной желтухи, нарушений сосания и глотания, стойкого снижения мышечного тонуса, тремора, анемии, тромбоцитопении, отставания в умственном и моторном развитии, пневмонии, миокардита, панкреатита, колита, нефрита). Отдаленными последствиями ЦМВИ у детей являются слепота, глухота, речевые нарушения, проявляющиеся на 2-5-м году жизни.
У беременных со значительной иммуносупрессией ЦМВИ протекает тяжелее, экстрагенитальные осложнения выявляются чаще. Неблагоприятными формами заболевания считаются цитомегаловирусные поражения легких (интерстициальная пневмония), мозга (менингит, энцефалит), периферической нервной системы (миелит, полирадикулоневрит), сердца (миокардит, перикардит), кроветворения (тромбоцитопения, гемолитическая анемия). Прямая угроза для жизни беременной возникает при быстрой генерализации инфекции с развитием сепсиса, инфекционно-токсического шока, ДВС-синдрома.
Диагностика
Сложность своевременного выявления ЦМВИ связана с отсутствием симптоматики у большинства беременных и полиморфностью клинической картины при манифестации. Учитывая повышенный риск перинатального заражения ребенка цитомегаловирусной инфекцией, в качестве скрининга рекомендовано проведение анализа на TORCH-комплекс. Ведущими методами диагностики являются лабораторные анализы, позволяющие верифицировать инфекционного агента, обнаружить серологические маркеры и определить остроту процесса. План обследования пациенток с подозрением на цитомегалию включает такие исследования, как:
- Иммуноферментный анализ. ИФА считается наиболее достоверным и информативным методом диагностики цитомегаловирусной болезни. Наличие активной инфекции подтверждает выявление IgM и более чем 4-кратное нарастание титра IgG. О давности инфицирования свидетельствуют данные об авидности иммуноглобулинов G (при показателе
- ПЦР-диагностика. Цитомегаловирусные нуклеиновые кислоты определяют в биологических секретах, которые могут содержать возбудителя. Обычно для анализа берут кровь, мочу, цервикальный секрет, буккальные мазки. Обнаружение вирусной ДНК подтверждает инфицированность, а количественные методы исследования позволяют контролировать течение инфекции.
Для оценки состояния плода, выявления фетоплацентарной недостаточности, возможных аномалий по показаниям проводятся:
- УЗИ плода и плаценты;
- допплерография маточно-плацентарного кровотока;
- фетометрия;
- КТГ;
- фонокардиография плода;
- биопсия хориона.
Цитомегалию дифференцируют с ВИЧ-инфекцией, инфекционным мононуклеозом, токсоплазмозом, листериозом, герпесом, вирусными гепатитами, бактериальным сепсисом, лимфогранулематозом, острым лейкозом. При необходимости пациентку консультирует инфекционист, вирусолог, иммунолог, онколог, онкогематолог.
Лечение ЦМВИ у беременных
Выбирая тактику ведения гестации, учитывают клиническую форму ЦМВИ и срок инфицирования. Женщинам с цитомегалией, первично-манифестировавшей в период 1 триместра, рекомендовано проведение аборта. Прерывание беременности по медицинским показаниям также показано пациенткам с клинически и лабораторно подтвержденной первичной инфекцией при обнаружении до 22 недели УЗ-признаков пороков развития плода. В остальных случаях возможна пролонгация гестации.
Беременным с носительством медикаментозное лечение не назначается. При отсутствии клинических и лабораторных признаков реактивации цитомегаловирусной болезни требуется коррекция образа жизни, направленная на предотвращение значительной иммуносупрессии. Больным необходимы достаточные отдых и сон, исключение чрезмерных физических и психологических нагрузок, полноценное питание, прием витаминно-минеральных комплексов, профилактика ОРВИ, осторожность при назначении препаратов, снижающих иммунитет.
Беременным с активной формой инфекции проводится лечение, направленное на купирование обострения и прекращение экскреции цитомегаловируса. Сложность выбора адекватной медикаментозной терапии связана с фетотоксичностью большинства противовирусных средств. С учетом возможных показаний и противопоказаний для лечения ЦМВИ при гестации применяются:
- Антицитомегаловирусный человеческий иммуноглобулин. Гипериммунные препараты позволяют восстановить титр специфических IgG, блокировать репликацию возбудителя и ограничить его диссеминацию. Использование иммуноглобулина человека существенно снижает риск внутриутробного инфицирования вирусом цитомегалии.
- Рекомбинантный α-2-интерферон. Препарат стимулирует Т-хелперы и Т-киллеры, повышая уровень Т-клеточного иммунитета. Усиливает активность фагоцитов и скорость дифференцировки В-лимфоцитов. Угнетает репликацию цитомегаловирусов и способствует их инактивации различными иммунными агентами. Рекомендован в виде ректальных свечей.
- Синтетические аналоги нуклеозидов. Назначаются только при тяжелых генерализованных формах цитомегаловирусной инфекции, когда риск токсических эффектов препаратов оправдан спасением жизни беременной. Противовирусные препараты ингибируют ДНК-полимеразу вирусных частиц и за счет этого тормозят синтез цитомегаловирусной ДНК.
Индукторы интерфероногенеза, иммуномодуляторы применяют крайне редко из-за возможного преждевременного прерывания гестации. В качестве немедикаментозных методов допустимо проведение эндоваскулярного лазерного облучения крови и плазмафереза.
Роды при ЦМВИ
Предпочтительным методом родоразрешения являются естественные роды. Кесарево сечение выполняется при наличии абсолютных акушерских или экстрагенитальных показаний или при сочетании относительных (внутриутробном инфицировании цитомегаловирусом, хронической гипоксии плода, II-III степенях задержки его развития, первичном и вторичном бесплодии в анамнезе).
Прогноз и профилактика
Своевременное выявление латентной ЦМВИ и профилактика ее активации существенно улучшают исход беременности как для женщины, так и для плода. Прогноз неблагоприятен при генерализации первичной цитомегаловирусной инфекции. При установленном диагнозе цитомегалии показано планирование зачатия с учетом рекомендаций акушера-гинеколога, купирование активного процесса, прегравидарная иммунокоррекция с использованием пептидных иммуностимуляторов и рекомбинантных интерферонов.
Противовирусная терапия женщин с манифестной ЦМВИ на 75% снижает риск реактивации инфекции в наиболее опасном по возникновению осложнений 1 триместре. Общая профилактика заражения предполагает соблюдение правил личной гигиены с частым мытьем рук, отказ от близких прямых контактов с другими людьми.
1. Цитомегаловирусная инфекция и беременность/ Мельникова С.Е., Троик Е.Б.// Детская медицина Северо-Запада – 2012 - Т. 3, №3.
2. Цитомегаловирусная инфекция и беременность (прегравидарная подготовка и терапия)/ Короткова Н.А., Прилепская В.Н.// Эффективная фармакотерапия. – 2016 - №22.
3. Цитомегаловирусная инфекция. Этиология, эпидемиология, патогенез, клиника, лабораторная диагностика, лечение, профилактика/ Марданлы С.Г., Кирпичникова Г.И., Неверов В.А. — 2011.
4. Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ Извекова И.Я., Михайленко М.А., Краснова Е.И.// Лечащий врач. – 2018.
Анэмбриония – это разновидность замершей беременности, при которой после оплодотворения и имплантации яйцеклетка не развивается в эмбрион, но сохраняется пустое плодное яйцо. Беременность не прогрессирует, поэтому постепенно исчезают признаки токсикоза и другие ранние симптомы в виде сонливости, болей в молочных железах, перепадов настроения. Анэмбриония диагностируется по результатам УЗИ органов малого таза на 5-ой неделе беременности, может подтверждаться при помощи анализов крови на ХГЧ, альфа-фетопротеин. Специфическое лечение состоит в удалении остатков эмбриона медикаментозным путем или с помощью вакуум-аспирации.
МКБ-10

Общие сведения
Анэмбриония, или непузырный занос, может быть следствием изначального отсутствия эмбриона в полости матки или его гибели в сроке до 5 недель. У женщин с диагностированной беременностью в среднем каждая пятая заканчивается самопроизвольным абортом или прекращает развитие. Самостоятельное опорожнение полости матки происходит у 53% в течение 2-х недель после диагностированной анэмбрионии. Если не удалить остатки плодного яйца в этот срок, то у 2,5% возникает кровотечение или инфекционно-воспалительные осложнения, которые требуют кюретажа и последующего лечения. Плодное яйцо при анэмбрионии может задерживаться в матке на срок больше 2-х недель, однако при этом появляются симптомы, которые требуют хирургической помощи.

Причины анэмбрионии
Точные причины данной патологии установить сложно, их предполагают ретроспективно на основании дополнительных симптомов и обследования женщины. Причиной анэмбрионии могут быть заболевания матери, а также действие различных внешних и внутренних патологических факторов. Основной риск потери беременности возникает на небольшом сроке, когда происходит первое деление бластомеров, имплантация зародыша в слизистую матки. Причины анэмбрионии могут заключаться в следующих нарушениях:
- Генетические и хромосомные отклонения. Являются основной причиной потери беременности на ранних сроках. Хромосомные аномалии возникают как на этапе оплодотворения при проникновении в яйцеклетку двух сперматозоидов, так и на следующих этапах деления клеток. Чем старше возраст матери, тем выше шанс возникновения хромосомных аберраций.
- Патология эндометрия. Причиной анэмбрионии может быть хронический эндометрит и синдром регенераторно-пластической недостаточности эндометрия. При хроническом воспалении происходят иммунные изменения, которые снижают рецептивные свойства слизистой оболочки, приводят к сладжированию эритроцитов в формирующихся ворсинах хориона и образованию микротромбов.
- Анатомические нарушения. Предпосылкой могут быть врожденные пороки развития матки или приобретенные структурные изменения, которые вызваны синехиями, миоматозными узлами, полипами. Этим патологиям сопутствуют признаки гормональных нарушений, изменение рецептивности эндометрия.
- Болезни свертывающей системы. Тромбофилия, которая возникает на фоне антифосфолипидного синдрома или недостаточности гемостаза, приводит к формированию тромбов в межворсинчатом пространстве. Питание эмбриона нарушается, что вызывает его гибель в начале беременности.
Анэмбриония связана с гибелью эмбриона и нарушением инертности матки, что приводит к задержке в полости пустого плодного яйца. Основные причины ареактивности миометрия следующие:
- Плотное прикрепление эмбриона. Глубокая инвазия ворсин хориона происходит при структурно-функциональной неполноценности эндометрия. Другая причина – незавершенная прегравидарная трансформация в зоне имплантации и высокая пролиферативная активность ворсин хориона.
- Иммунная недостаточность. Ткани эмбриона являются для материнского организма наполовину чужеродными, поэтому в норме при участии прогестерона происходит подавление иммунных реакций отторжения. Причины сохранения плодного яйца при анэмбрионии связаны с иммунологической ареактивностью миометрия к продуктам зачатия.
- Нарушение сократительной функции. Отторжение пустого яйца не происходит при хронических воспалительных заболеваниях матки из-за нарушения формирования рецепторов к утеротоническим веществам. Частая причина – биохимические дефекты метаболизма в тканях матки.
- Недостаток фолатов. Фолиевая кислота участвует в делении ДНК клеток. При ее дефиците в ранние сроки беременности происходит нарушение расхождения хромосом, их неправильное расположение. Также при нехватке фолатов увеличивается чувствительность к радиационному воздействию.
Патогенез
На 7-8 сутки после оплодотворения происходит имплантация эмбриона в стенку матки, трофобласт активно продуцирует ХГЧ, необходимый для сохранения беременности. К 3-й неделе развития у эмбриона формируются внезародышевые органы – хорион, желточный мешок и амнион. Чуть позже начинает биться сердце, но при помощи аппарата УЗИ это можно заметить после 5 недели гестации. Если происходит нарушение кровотока в месте имплантации, зародыш гибнет и постепенно редуцируется. Но плодный пузырек под действием сохраняющегося шлейфа высоких гормонов беременности продолжает визуализироваться. При нарушении сократимости матки не происходит его отторжения и изгнания.
Морфологическое исследование эндометрия после кюретажа при анэмбрионии показывает, что децидуальный слой клеток дистрофически изменен. В нем часто выявляется лимфоидная инфильтрация, очаговый отек стромы, расширенные железы с уплощенными эпителиальными клетками. Ворсины хориона увеличиваются, выстилающий их эпителий истончается и располагается в один слой синтициотрофобласта. Цитотрофобласт местами отсутствует.
Классификация
Анэмбрионию классифицируют по результатам ультразвукового исследования, которое позволяет определить размер плодного яйца и его содержимое. Размер матки не влияет на вид анэмбрионии, но учитывается при определении срока гестации. Выделяют два типа отсутствия эмбриона:
- 1 тип. Средний диаметр плодного яйца 2-2,5 см, зародыш не визуализируется. Размер матки соответствует 5-7 неделе беременности, что не отвечает сроку по первому дню последней менструации. При динамическом наблюдении увеличения размеров не происходит.
- 2 тип. Плодное яйцо продолжает расти, но эмбриона нет. Иногда наблюдаются его остатки в виде тонкой гиперэхогенной полоски. Анэмбриония этого типа может сохраняться до 11 недели, яйцо достигает размера 4,5-5 см.
Симптомы анэмбрионии
При нормально развивающейся беременности к 5-6 неделе присутствуют многие признаки гестации: симптомы токсикоза, нагрубание молочных желез, сонливость или бессонница, перепады настроения. При формировании анэмбрионии беременная может заметить, что в какой-то момент стала чувствовать себя лучше, исчезла утренняя тошнота, нет отвращения к запахам и гиперсаливации. Восстанавливается нормальный аппетит. Затем молочные железы теряют болезненность и повышенную чувствительность, становятся мягкими. Но эти признаки не всегда могут указать на анэмбрионию. Такие же симптомы характерны и для замершей беременности.
Осложнения
Женщины, которые своевременно не обращаются к гинекологу с признаками беременности или их исчезновением, могут столкнуться с тяжелыми осложнениями. При сохранении пустого плодного пузырька в матке до 2 недель и больше возникает воспалительная реакция, появляются симптомы острого эндометрита. Повышается температура, из влагалища появляются серозно-слизистые выделения, беспокоят признаки интоксикации – слабость, головная боль. При отсутствии лечения или несвоевременном начале острое воспаление может перейти на мышечный слой, околоматочную клетчатку, а в тяжелых случаях привести к перитониту. Если лечение не проводилось, развивается хронический эндометрит.
Признаком отторжения остатков эмбриона из матки служит появления кровянистых выделений из половых путей. Но при недостаточной сократимости матки, нарушениях гемостаза развивается кровотечение. Завершиться самостоятельно оно не может, поэтому требуется медицинская помощь. Последствием кровотечения становится инфицирование полости матки, анемия. Осложняется анэмбриония последующим привычным невынашиванием беременности, вторичным бесплодием.
Диагностика
Обследование и выбор метода лечения при анэмбрионии осуществляет врач акушер-гинеколог. Физикальный осмотр не дает точных сведений о патологии, лабораторные методы также неспецифичны. Наиболее точные данные можно получить при вагинальном УЗИ малого таза. Алгоритм обследования включает:
- Гинекологический осмотр. Признаки патологии заметить не всегда возможно, иногда при двуручном исследовании может определяться отставание размеров матки, ее размягчение. Присоединение воспаления характеризуется появлением серозно-сукровичных выделений из шейки матки.
- Лабораторные исследования. ХГЧ в крови падает в 6-8 раз ниже нормы для срока гестации. Альфа-фетопротеин увеличивается в 1,5 раза и больше, но не является признаком только анэмбрионии, аналогичные изменения происходят при замершей беременности. Трофобластический гликопротеин уменьшается в 6-18 раз, что говорит о гибели клеток синцитиотрофобласта. Концентрация прогестерона может сохраняться на прежнем уровне, а эстрогены снижаются.
- Инструментальные методы. Информативно УЗИ вагинальным датчиком. Признаками анэмбрионии являются плодное яйцо от 25 мм и больше и отсутствие в нем эмбриона. Если через 2 недели при повторном УЗИ не выявляется сердцебиение, то выставляется диагноз анэмбрионии.
Для правильной оценки результатов ультразвуковое исследование проводят в динамике. Если у плода в 5 недель не зафиксировано сердцебиение, нельзя однозначно сказать, что определена анэмбриония. Отсутствие желточного мешка является неблагоприятным прогностическим признаком, который соответствует возможной анэмбриональной беременности.
Лечение анэмбрионии
Лечение направлено на эвакуацию из полости матки остатков плодного яйца. Это можно сделать медикаментозным и хирургическим способом. Последний применяется чаще, но он связан с дополнительным риском инфицирования и присоединения осложнений. ВОЗ рекомендует в качестве основного способа лечения анэмбрионии использовать медикаментозный аборт.
Медикаментозное лечение
Медикаментозное прерывание гестации проводится при симптомах анэмбрионии до 83 дня беременности. Для процедуры последовательно применяются мифепристон и мизопростол. Дозировка последнего подбирается индивидуально и зависит от срока гестации по последней менструации. Кровотечение, которое означает выход остатков эмбриона, возникает на вторые сутки. Женщина должна явиться на прием через 14 дней после приема последней таблетки для оценки общего состояния и эффективности процедуры.
У медикаментозного аборта мало противопоказаний. Его можно применять при инфекциях половых путей без предварительной санации. Не рекомендуется метод при бронхиальной астме, наличии патологий сердечно-сосудистой системы, нарушении свертывания крови и у курящих женщин. Осложнениями медикаментозного аборта могут быть болевой синдром, кровотечение и неполный аборт, который потребует использования хирургических методов лечения.
Хирургическое лечение
Оптимальным и менее травматичным способом среди хирургических методов считается вакуум-аспирация. При анэмбрионии ее можно использовать до 12 недели беременности, т.к. плодное яйцо остается небольшого размера. Перед процедурой необходимо исследовать мазок на степень чистоты влагалища. При признаках воспаления проводится санация местными средствами. Вакуум-аспирация поводится в амбулаторных условиях, госпитализация в отделение гинекологии не требуется. После процедуры есть вероятность инфекционных осложнений, кровотечения и сохранения остатков эмбриональных тканей, что может потребовать проведения выскабливания.
Для кюретажа полости матки женщина госпитализируется в гинекологическое отделение после предварительного обследования. Процедура проводится под общей анестезией и требует наблюдения медперсонала в течение нескольких дней после нее. В послеоперационном периоде обязательно назначается антибиотикопрофилактика, чтобы снизить риск инфекционных осложнений, утеротоники для улучшения сократимости матки.
Реабилитация
Единичный случай анэмбрионии не представляет опасности, но при его повторении или другом типе прерывания гестации на маленьком сроке необходимо тщательное обследование и реабилитация. У большинства женщин имеются выраженные симптомы хронического эндометрита или наблюдается его латентное течение. Поэтому назначаются антибиотики широкого спектра действия.
Для коррекции метаболических и функциональных нарушений в эндометрии применяют противовоспалительные препараты, ферменты, иммуномодуляторы, назначают курсы физиотерапии. Для восстановления гормональной регуляции в течение 3-6 месяцев применяют комбинированные оральные контрацептивы. Планирование новой беременности проводится после тщательной прегравидарной подготовки.
Прогноз и профилактика
Для жизни женщины и последующей реализации репродуктивной функции прогноз благоприятный. После восстановления эндометрия и устранения возможных причин патологии можно планировать зачатие. Для профилактики анэмбрионии необходимо остерегаться действия внешних неблагоприятных факторов, избегать употребления токсичных веществ, алкоголя, курения. При подозрении на половые инфекции их нужно своевременно лечить. Женщинам за 2 месяца до зачатия необходимо начинать принимать фолиевую кислоту и продолжать курс до конца первого триместра.
1. Неразвивающаяся беременность. Методические рекомендации МАРС (Меж- дисциплинарной ассоциации специалистов репродуктивной медицины)//StatusPraesens. – 2015.
2. Фолатный цикл и полиморфизм C6777T MTHFR – ключ к пониманию причин анэмбрионии/ Веропотвелян Н.П., Кодунов Л.О., Погуляй Ю.С. // Здоровье женщины. - 2014 - №10 (96).
3. Морфологические критерии патогенетических вариантов неуточненных абортов/ Федорина Т.А., Линева О.И.// Акушерство и гинекология - 2006. - №4.
4. Невынашивание беременности: руководство для практических врачей/ Сидельникова В.М., Сухих Г.Т. - 2010.

Чрезвычайно много работ о роли инфекции при преждевременных родах и преждевременном излитии околоплодных вод, показывающих, что инфекция- основная причина преждевременных родов.
Вирусные заболевания (грипп, парвавирус, ЦМВ, герпес, Коксаки, гепатит, паротит, корь, краснуха, полиомиелит) во время беременности могут приводить к анэмбрионии, неразвивающейся беременности, самопроизвольным выкидышам, антенатальной гибели плода, к порокам развития плода. Чем меньше срок беременности, при котором произошлоинфицирование, тем выше вероятность остановки развития и формирования пороков развития.
В настоящее время установлено, что вирусы могут передаваться плодунесколькими путями, но наибольшее значение имеет трансплацентарный путь передачи инфекции.
Плацента представляет собой физиологический барьер, препятствующий проникновению вируса к плоду, однако на ранних этапах беременности быстро делящиеся клетки формирующегося трофобласта, имеющие высокий уровень обменных процессов, являются прекрасной средой для репликации вирусных частиц, которые могут оказывать прямое повреждающее действие на плаценту.
Переход вирусов через плаценту значительно облегчается при различных повреждениях её, например, при угрозе прерывания, при аутоиммунных нарушениях, токсикозах.
Плацента проницаема практически для всех вирусов.
Вирусы с током крови могут достигать плодных оболочек, адсорбироваться на них и инфицировать околоплодные воды, а затем и плод.
Инфицирование оболочек и вод может быть и при восходящей инфекции. Помимо вирусной инфекции в прерывании беременности играет существенную роль бактериальная инфекция (хламидии, стрептококк группы В, бактероиды, пептострептококки) и ассоциации бактериально-вирусные. Хорионамнионит обычно является результатом восходящей инфекции, что наиболее характерно для II триместра беременности.
Инфекция может прямо поражать плод, а возможно за счёт активации провоспалительных цитокинов, имеющих цитотоксический эффект.
Потеря беременности может быть связана с гипертермией, повышенным уровнем простагландинов, с преждевременным разрывом плодного пузыря за счёт микробных протеаз.
Выполнение так называемого сринингового TORCH-теста для выявления причин привычного невынашивания беременности необходимо для своевременной диагностики и лечения проблемы.
- Т - токсоплазма;
- O - others - другие инфекции;
- C - цитомегаловирус;
- R - rubella - краснуха;
- H - herpes - герпетическая инфекция.
По некоторым данным, повышение частоты преждевременного прерывания беременности во II и III триместрах связано с бактериальным вагинозом. Лечение бактериального вагиноза во время беременности снижает риск преждевременных родов.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Читайте также:

