Что такое этиотропное лечение гриппа а
Обновлено: 25.04.2024
Рассмотрены основные возбудители острых респираторных заболеваний (ОРЗ), эпидемиология, клинические проявления ОРЗ и формы поражения дыхательных путей, осложнения ОРЗ. Приведены подходы к лечению ОРЗ, включая используемые противовирусные и антибактериальн
An examination was performed on the basic agents of acute respiratory diseases (ARD), epidemiology, clinical manifestations of ARD and forms of the failure of the respiratory tract, complication of ARD. Are given approaches to the ARD treatment, including the utilized antiviral and antibacterial preparations and symptomatic means.
Каждый год острыми респираторными заболеваниями (ОРЗ) болеют от 20 до 40 миллионов человек, из которых 45–60% — дети. Однако диагностика и лечение острых респираторных заболеваний нередко вызывают определенные затруднения у специалистов, поэтому эпидемии ОРЗ до сих пор остаются одной из наиболее значимых медицинских и социально-экономических проблем. В среднем взрослые люди болеют ОРЗ 2–3 раза за год, а дети — до 6–10 раз в год [1]. Возбудители острых респираторных заболеваний — не только вирусы, но различные виды бактерий (табл. 1). Поэтому при лечении ОРЗ противовирусные препараты, как и антибиотики, эффективны далеко не всегда. Так, заболевания верхних дыхательных путей бактериальной и микоплазменной этиологии хорошо поддаются антибактериальной терапии, а при гриппе назначение антибиотиков лишь способствует истощению сапрофитной флоры, что может привести к снижению иммунного статуса, нарушению пищеварения и другим осложнениям. Установить точную причину заболевания бывает непросто, могут потребоваться лабораторные исследования, которые проводят при возникновении эпидемии.
Эпидемиология
Грипп
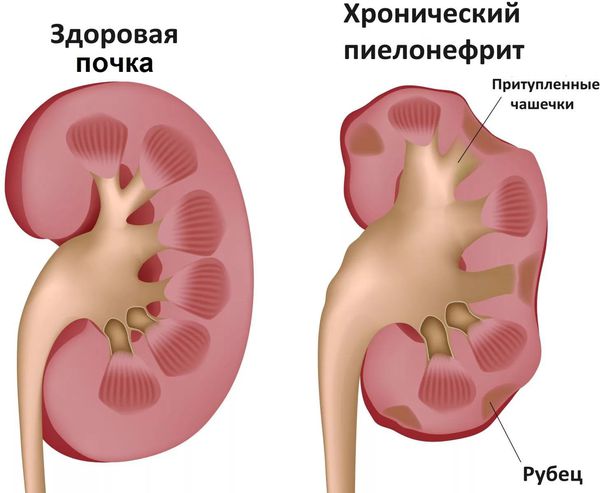
Вирус гриппа в отличие от других инфекционных агентов сильнее подавляет иммунитет, нередко вызывая серьезные осложнения: пневмонию, миокардит, менингит, гайморит, пиелонефрит, активизацию скрытых патологий. Специфические признаки гриппа — высокая температура, боль в глазных яблоках (патогномоничный признак, говорящий о высокой степени интоксикации) и в мышцах. Проявления со стороны верхних дыхательных путей незначительные: першение в горле, скудный насморк и небольшой сухой кашель (табл. 2).
В сезон ежегодных эпидемий грипп поражает не менее 10% населения земного шара, а во время пандемий число больных возрастает в 4–5 раз.
В период подъема заболеваемости ОРЗ выявляют: вирус гриппа А — 16,4%; вирус гриппа В — 15,7%; вирус парагриппа 1-го, 2-го, 3-го типа — 4,3%; аденовирус — 16,4%; респираторно-синцитиальный вирус — 6,4%; вирус простого герпеса — 2,1%; Mycoplasma pneumoniae — 2,1%; более двух вирусов — 33%; вирус не идентифицирован — 3,6% [4].
Клиника
При ОРЗ у пациентов всегда наблюдается два синдрома: общая интоксикация организма и поражение дыхательной системы на различных уровнях. Диагностировать ОРЗ, вызванное различными возбудителями, очень непросто, особенно в межэпидемический период гриппа.
Во всех случаях ОРЗ необходимо указать синдром поражения респираторного тракта, период и день начала болезни, степень тяжести состояния и развившиеся осложнения.
Синдром воспаления дыхательных путей включает следующие формы поражения:
- ринит;
- фарингит;
- ларингит;
- трахеит;
- бронхит;
- бронхиолит.
Вышеописанные состояния могут встречаться изолированно, но чаще наблюдаются в различных сочетаниях.
Следует отметить, что бронхит и бронхиолит рассматриваются как компонент ОРЗ, если они сопровождаются поражением верхних отделов респираторного тракта. При отсутствии таких изменений и при сочетании с пневмонией бронхит и бронхиолит не относят к ОРЗ. Для ОРЗ характерен только острый бронхит.
Каждая группа инфекционных возбудителей избирательно поражает определенные участки дыхательного тракта. Риновирусная инфекция — клетки эпителия носовых ходов, а при аденовирусных заболеваниях — развиваются тонзиллит, фарингит с выраженным экссудативным компонентом в сочетании с конъюнктивитом. При парагриппозной инфекции у пациента возникает ларингит, который у детей может протекать на фоне парагриппозного ложного крупа (стеноза гортани 1–3 степени).
Респираторная синцитиальная инфекция локализуется преимущественно в нижних отделах дыхательных путей, у больного развивается бронхит и бронхиолит.
Размножение вируса гриппа происходит в основном в верхних и средних отделах дыхательных путей, но клинически характерно наличие выраженного трахеита.
Аденовирусные заболевания начинаются остро, температура повышается до 38 °С и выше и продолжается иногда до 10 дней. Однако общая интоксикация выражена слабее, чем при гриппе. Даже при высокой лихорадке самочувствие больных остается относительно удовлетворительным.
Неосложненные респираторно-синцитиальные вирусные заболевания протекают с небольшим повышением температуры тела и незначительными проявлениями интоксикации. А нормальная температура тела (реже небольшой субфебрилитет) наблюдается при риновирусном заболевании.
Микоплазменное воспаление верхних дыхательных путей чаще всего развивается постепенно, но держится долго.
Пациенты часто настаивают на выборе гомеопатических средств при ОРЗ. Однако большинство гомеопатических средств не имеет доказанной эффективности при ОРЗ [5]. Эффективность большинства подобных средств сравнима или недостоверно превосходит эффективность плацебо. В некоторых гомеопатических средствах действующее вещество находится в таких концентрациях, что сомнительно его присутствие в каждой дозе (таблетке, грануле, капле). Например, препараты животных экстрактов с разведением более чем в 200 000 раз [6].
Осложнения
Если лихорадка продолжается более 5 дней или возникает у пациента после недлительного облегчения общего состояния, сопровождаясь ознобом или зябкостью, резкой головной болью с локализацией в лобной области, надбровных дугах, скорее всего, это говорит об осложнениях, наиболее тяжелым из которых является инфекционно-токсический шок, проявляющийся острой сердечно-сосудистой недостаточностью, отеком легких и отеком мозга, диссеминированным внутрисосудистым свертыванием. Молниеносная (гипертоксическая) форма гриппа обусловлена развитием инфекционно-токсического шока уже в первые сутки болезни.
Самое распространенное осложнение гриппа — пневмония, которая бывает первичной (гриппозной), вторичной (как правило, бактериальной) и смешанной (вирусно-бактериальной).
Дифференциальный диагноз между вышеописанными тремя состояниями поставить достаточно просто — если пневмония развивается в 1–3 сутки от начала заболевания — она с большей вероятностью первичная, в 3–7 — чаще всего бактериальная, после 7 — может быть как той, так и другой этиологии. Пневмония возникает в 15% случаев при гриппе А (H1N1) и в 26–30% при гриппе А (H3N2) и В [7].
Лечение острых респираторных заболеваний
Всем больным назначается постельный режим на время лихорадочного периода. Рекомендуется диета, богатая витаминами, обильное питье — потогонные горячие напитки из отваров и настоев лечебных трав — малины, калины или шиповника, теплые щелочные минеральные воды.
Противовирусные препараты
Для лечения и профилактики гриппа доказана эффективность ряда этиотропных противовирусных препаратов.
К I поколению относятся препараты, содержащие адамантановое ядро, являющиеся блокаторами ионных каналов, которые образуются вирусным белком М2 и препятствуют высвобождению его генома для начала транскрипции.
Однако эти средства бессильны перед вирусом гриппа В и некоторых других штаммов и вызывают побочные эффекты. Последние исследования клинических изолятов показали, что процент штаммов вируса гриппа А, резистентных к адамантанам, чрезвычайно возрос в мире и достигает до 90% в некоторых странах, например в Китае и США [8].
К препаратам II поколения относятся разработанные сравнительно недавно ингибиторы нейраминидазы: применяемый интраназально занамивир (Реленза) и применямый в виде капсул и суспензии для детей озельтамивир (Тамифлю). Занамивир и озельтамивир являются ингибиторами фермента вируса гриппа нейраминидазы. Оба препарата эффективны в отношении как вируса гриппа А, так и В [9].
К недостаткам вирус-специфических препаратов относится узкий спектр действия и формирование резистентных штаммов вирусов, снижающие их эффективность. При назначении противовирусных препаратов всегда следует помнить об эпидемиологической ситуации. В случае отсутствия эпидемии гриппа использование данных противовирусных препаратов неэффективно, учитывая незначительный процент гриппа в структуре ОРЗ (до 10%).
Антибактериальные препараты
Следует назначать при подозрении на бактериальный характер заболевания или возникновении осложнений — пневмонии, отите, синусите, инфекции мочевыводящих путей, тяжелых формах ОРЗ — особенно при имеющихся хронических очагах инфекции, например, хроническом гайморите, пиелонефрите.
Симптоматические средства
Как показывает клинический опыт, наилучшие результаты в лечении вирусных заболеваний удается достичь, используя полный арсенал перечисленных выше средств (рис.). Однако на практике в лечении вирусных заболеваний специалисты чаще используют симптоматические средства [10], отдавая предпочтение комплексным препаратам, содержащим несколько активных веществ, направленных на устранение симптомов ОРЗ: кашля, першения в горле, отечности носоглотки, лихорадки с ознобом, общей слабости, головной боли, миалгий и артралгий, которые пациенты переносят с трудом. Многокомпонентные симптоматические средства содержат сбалансированные дозы лекарственных препаратов, что снижает риск передозировки. Их удобно использовать — один препарат вместо нескольких. Кроме того, лечение обходится дешевле. Практически все подобные лекарства могут отпускаться без рецепта врача [11].
В качестве основного вещества используется либо анальгетик-антипиретик (парацетамол) или нестероидный противовоспалительный препарат (ацетилсалициловая кислота, ибупрофен и др.).
Прием препаратов, содержащих ацетилсалициловую кислоту, особенно при гриппе, ветряной оспе и инфекциях, вызванных вирусами Коксаки, опасен у детей до 15 лет, поскольку может вызывать синдром Рея, характеризующийся энцефалопатией и острой жировой дистрофией печени, быстро приводящей к печеночной недостаточности [12].
Благодаря высокому профилю эффективности и безопасности парацетамол рассматривается в качестве средства терапии первой линии в лечении лихорадки и купировании боли у пациентов разных групп, в том числе детей и лиц пожилого возраста. Считается, что выраженное анальгетическое действие препарата связано с его способностью накапливаться в центральной нервной системе, головном и спинном мозге и уменьшать образование простагландинов за счет ингибирования изоформы фермента циклооксигеназы — ЦОГ-3 [13].
Анальгезирующий эффект связан с периферическим блокированием импульсов на брадикинин-чувствительных хеморецепторах, ответственных за возникновение боли. В отличие от других нестероидных противовоспалительных препаратов действие парацетамола на синтез простагландинов ограничивается центрами терморегуляции и боли в гипоталамусе и не влияет на другие органы и ткани. По этой причине эрозивно-язвенные поражения желудочно-кишечного тракта, проявления бронхоспазма при приеме парацетамола развиваются крайне редко, препарат не воздействует на почечный кровоток и агрегацию тромбоцитов. Возможность развития поражений печени связывают в основном с длительным приемом парацетамола в дозах, значительно превышающих рекомендуемые максимальные [14].
В составе комбинированных препаратов используются деконгестанты. Одним из первых препаратов этой группы был эфедрин. В настоящее время применяются фенилпропаноламин, псевдоэфедрин и фенилэфрин, имеющие меньшую по сравнению с эфедрином частоту нежелательных эффектов. Эти препараты стимулируют альфа-1-адренорецепторы сосудистой стенки, что приводит к их сужению, снижению проницаемости, отека слизистой оболочки носа, количества отделяемого из носа и восстановлению свободного носового дыхания.
Однако в силу активации адренергических структур эти средства могут в той или иной степени повышать артериальное давление, потребность миокарда в кислороде, увеличивать вероятность сердечных аритмий у пациентов с сердечно-сосудистыми рисками, а также вызывать беспокойство и бессонницу [15].
По результатам крупного эпидемиологического исследования, проведенного в 2001 году в США, показана связь развития геморрагического инсульта с применением фенилпропаноламина.
Фенилэфрин — единственный системный деконгестант, разрешенный для безрецептурного отпуска в Российской Федерации в составе комбинированных средств от ОРЗ и гриппа. В дозе 10 мг фенилэфрин эффективно уменьшает отечность носовых ходов у больных с ринитом. В этой дозе он не повышает артериальное давление и не имеет центрального стимулирующего эффекта [16]. В отличие от адреномиметиков, которые применяют местно, фенилэфрин не вызывает раздражения или сухости слизистой оболочки носа, развития медикаментозного ринита.
Фенилэфринсодержащие препараты считаются самыми безопасными препаратами для симптоматического лечения ОРЗ.
В состав комбинированных средств часто входят блокаторы Н1-гистаминовых рецепторов I поколения: фенирамин, хлорфенирамин, прометазин. Эти препараты потенцируют антиэкссудативное действие стимуляторов альфа-1-адренорецепторов. Блокаторы Н1-гистаминовых рецепторов I поколения обладают седативными свойствами, улучшают сон. В то же время их следует с осторожностью назначать пациентам, занимающимся деятельностью, требующей повышенного внимания и быстрых реакций, в первую очередь вождением автомобиля.
Врачи должны информировать пациентов о недопустимости вождения автомобиля и выполнения работ, связанных с высокой концентрацией внимания, когда прописывают блокаторы Н1-гистаминовых рецепторов I поколения. Минимальной частотой седации из наиболее популярных антигистаминных средств в составе комбинированных препаратов обладает хлорфенирамин — 4%, фенирамин — 8,3% [17].
Для повышения работоспособности пациентов при ОРЗ, устранения ощущения вялости, уменьшения головной боли, связанной с вазоконстрикцией (сужения просвета кровеносных сосудов), в состав некоторых комбинированных средств входит кофеин, который также препятствует проявлению седативного действия антигистаминных препаратов. Однако такие препараты могут повышать артериальное давление, вызывать беспокойство и бессонницу.
Иногда в комбинированные препараты производители добавляют аскорбиновую кислоту, обладающую комплексным и патогенетическим действием, необходимым при ОРЗ и гриппе. Аскорбиновая кислота стимулирует выработку эндогенного интерферона, нормализует процессы перекисного окисления липидов, укрепляет сосудистую стенку, уменьшая ее проницаемость, и восполняет повышенную во время ОРЗ и гриппа потребность организма в витамине С. Суточная потребность здорового взрослого человека в аскорбиновой кислоте составляет 70–100 мг [18], а во время болезни — еще выше, но не более 200 мг в сутки, так как повышенная доза организмом не усваивается и выводится с мочой в неизменном виде. А избыток аскорбиновой кислоты может вызывать различные нежелательные побочные эффекты: аллергические реакции, раздражение слизистой желудочно-кишечного тракта, обострение мочекаменной болезни.
Кроме того, стоит отметить, что наиболее перспективными и выгодными для пациентов стоит все-таки считать препараты с 3-компонентным составом — антипиретиком, деконгестантом и антигистаминным средством (желательно фенирамин/хлорфенирамин), подобное сочетание позволяет бороться с большинством типичных симптомов, что позволяет применять один препарат для лечения большинства ОРЗ.
Выбор комплексных препаратов при лечении ОРЗ должен быть дифференцирован: необходимо учитывать клиническую картину заболевания, уровень безопасности, сопутствующие заболевания, условия, в которых находится пациент: дома, на работе или за рулем. Одним из оптимальных симптоматических средств, противодействующих неприятным проявлениям гриппа и ОРЗ, считается ТераФлю от гриппа и простуды Экстра — комплексный препарат с усиленной формулой, быстро снимающий все основные симптомы, характерные для гриппа: жар, головную боль, ломоту в теле, озноб, резь в глазах, а также местные симптомы: насморк и заложенность носа, боль в горле.
Преимущества комбинированных симптоматических препаратов:
- быстро снимают все основные симптомы гриппа и ОРЗ, благодаря комбинированной формуле из нескольких активных веществ;
- содержат оптимально подобранные дозы действующих веществ;
- делают применение удобным и экономически выгодным (один препарат вместо нескольких);
- могут использоваться для самостоятельного лечения пациентами (отпускаются без рецепта врача);
- позволяют быстро и эффективно улучшить качество жизни.
Литература
Р. В. Горенков, доктор медицинских наук, доцент
ГУ МОНИКИ им. М. Ф. Владимирского, Москва
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
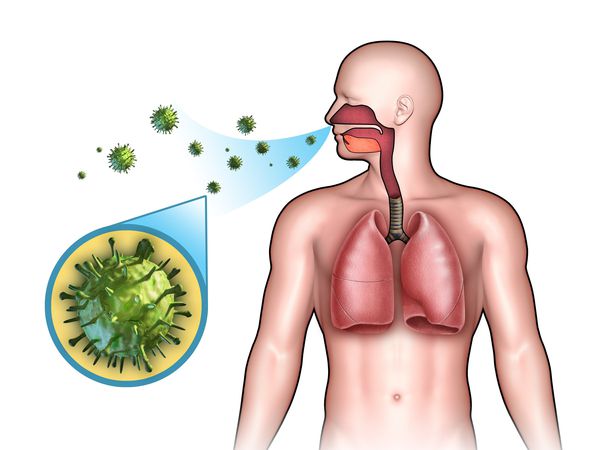
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
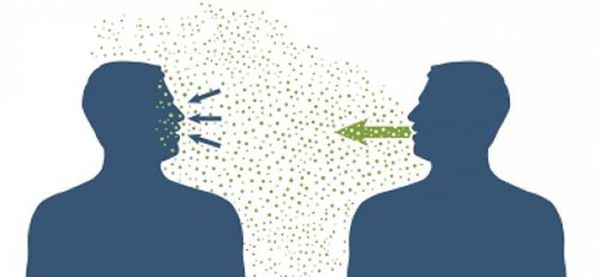
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
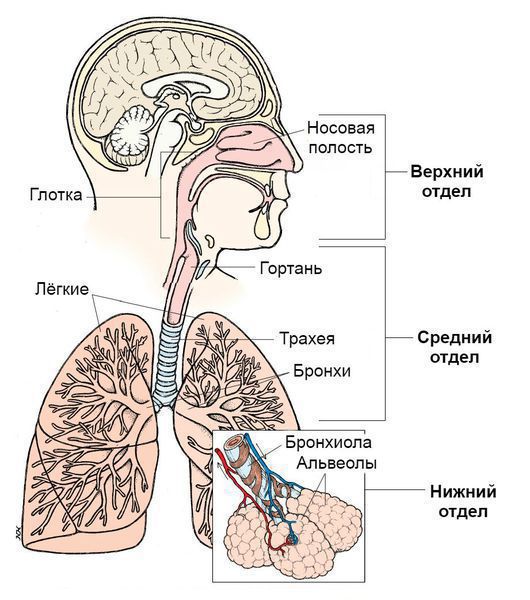
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
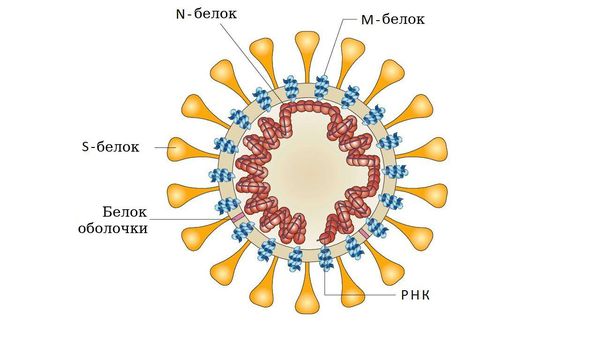
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
По вовлечению отдельных частей дыхательной системы:
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
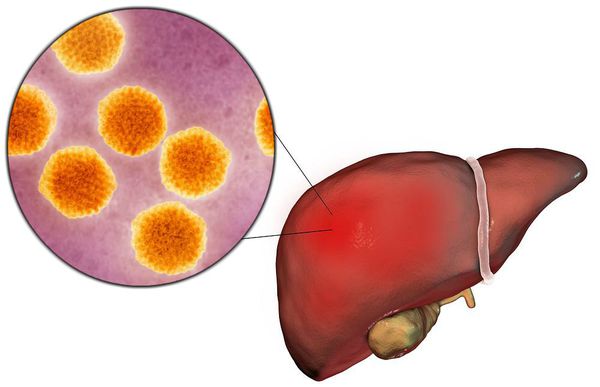
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
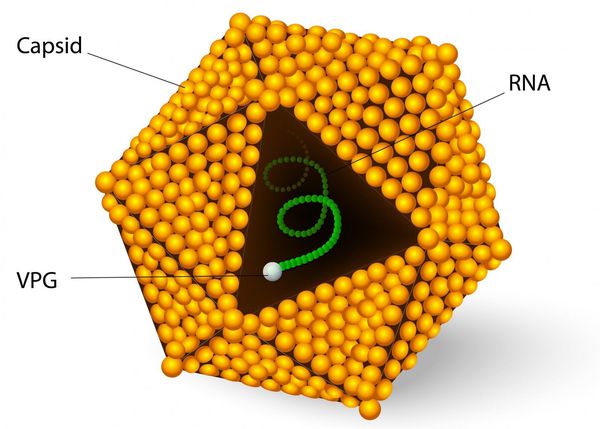
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
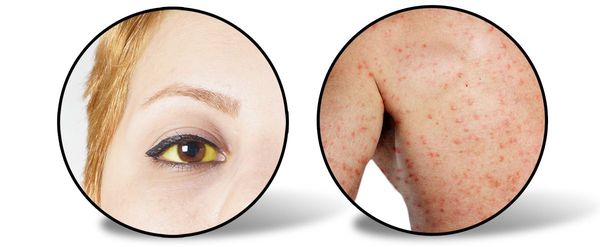
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
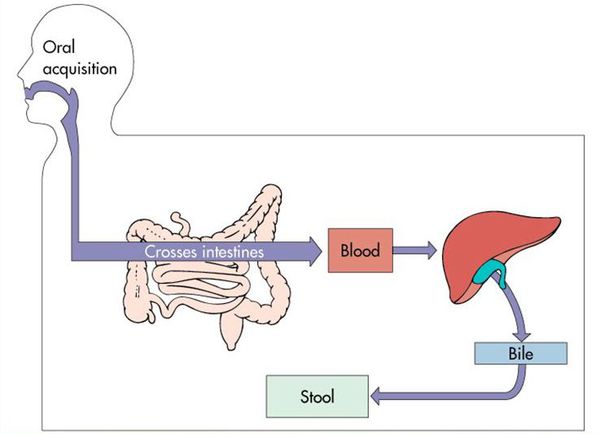
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
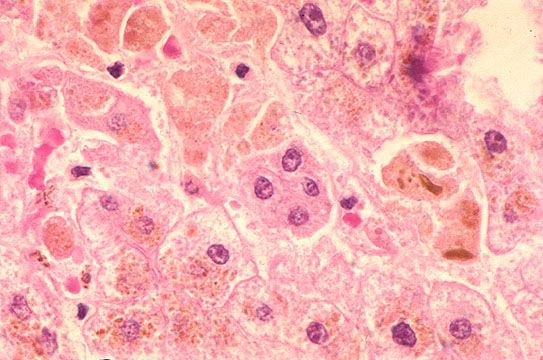
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
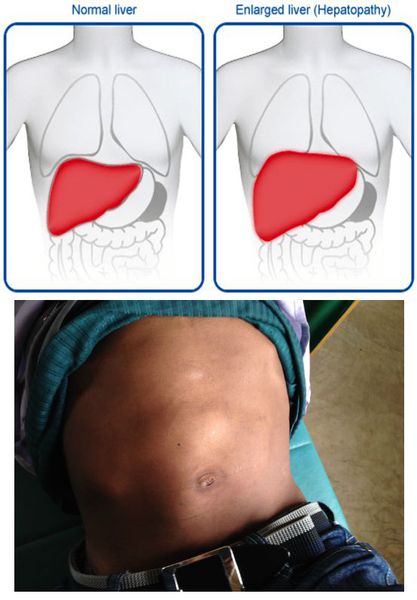
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
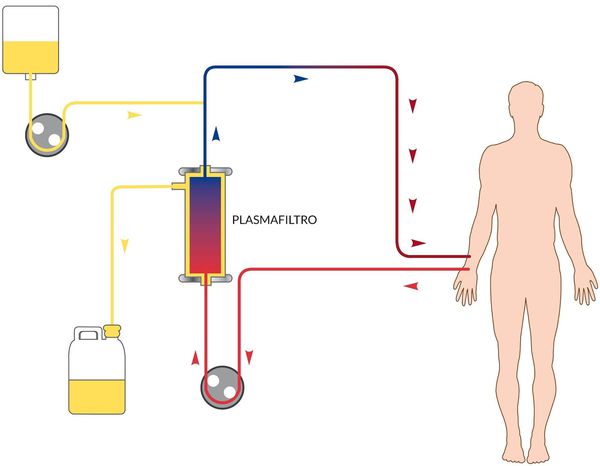
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
Ведущая роль в структуре ОРВИ принадлежит гриппу, так как вирусы гриппа вызывают эпидемии и пандемии. В России число ежегодно болеющих гриппом достигает 30 млн человек, а ежегодный суммарный экономический ущерб от ОРВИ оценивается в 40 млрд руб., составля
Ведущая роль в структуре ОРВИ принадлежит гриппу, так как вирусы гриппа вызывают эпидемии и пандемии. В России число ежегодно болеющих гриппом достигает 30 млн человек, а ежегодный суммарный экономический ущерб от ОРВИ оценивается в 40 млрд руб., составляя около 80% ущерба от всех инфекционных болезней. Сегодня очевидной становится необходимость качественно новых подходов к профилактике и лечению гриппа и ОРВИ, ибо даже вакцинация против гриппа не может защитить от возбудителей ОРВИ. По частоте инфицирования грипп составляет около 15% (тип А — 12%, В — 3%), парагрипп до 50%, аденоинфекции до 5%, РС — 4%, микоплазма 2,7%, энтеровирусы 1,2%, смешанные инфекции около 23% случаев. К группе высокого риска относятся дети, у которых заболевания респираторного тракта составляют до 90% всей инфекционной патологии и 65% от всех регистрируемых заболеваний.
Исследования иммунопатогенеза гриппа и ОРВИ убедительно показали, что вирусы гриппа, как и другие респираторные вирусы, грубо вмешиваются в сбалансированную систему цитокинов, а механизм иммунной защиты при гриппе и ОРВИ в целом, по мнению Г. Ф. Железниковой, В. В. Ивановой (2007), до конца еще не раскрыт. Неоднозначны литературные данные о характере цитокинового ответа при гриппе и ОРВИ. Сведения об изменении цитокинового профиля носят фрагментарный характер и не позволяют оценить сходство или различие цитокинового ответа при инфицировании разными респираторными вирусами.
Широкая распространенность респираторных вирусов обуславливает решающее значение этих агентов в становлении механизмов противоинфекционного иммунитета. Около 70% всех респираторных инфекций вызываются респираторными вирусами, среди которых чаще всего встречаются миксовирусы (вирусы гриппа, парагриппа, РС-вирус) и аденовирусы. Нередко возбудителем ОРВИ является микоплазма пневмонии и вирус простого герпеса. Вместе с тем только вирус гриппа вызывает опустошительные пандемии с высокой заболеваемостью и смертностью.
Вирус гриппа попадает в организм человека через дыхательные пути вместе с каплями влаги и частицами пыли. Чем меньше величина капель и частиц, тем глубже проникает вирус в дыхательные пути. Репродукция вируса происходит в клетках эпителия слизистой оболочки дыхательных путей. Пораженные клетки отторгаются, продукты их распада попадают в кровь, вызывая интоксикацию организма. Вирус, активируя систему протеолиза, повреждает клетки эндотелия сосудов, что приводит к повышению их проницаемости и дополнительному повреждению тканей. Центральным звеном в антивирусной защите клеток при гриппозной инфекции является дс-РНК-зависимая протеинкиназа и индукция интерферона 1 го типа. Гибель клеток (вирусиндуцированный апоптоз) при гриппе наступает через 20–40 часов после начала репликации вируса.
Гибель клеток сопровождается активацией дс-РНК-зависимой протеинкиназы, а высокая ее активность и синтез интерферона 1 го типа потенцируют апоптоз, в котором непосредственное участие принимают и вирусные белки (NA и NS1). На этом уровне и решается судьба инфицированной клетки. Продуктом индукции интерферона 1 го типа является Мх-белок, который подавляет активность вирусной РНК-зависимой РНК-полимеразы. Таким образом, угнетается репликативная активность вируса, а следовательно, интерферон 1 го типа является важным фактором защиты от вирусной инфекции на первом уровне. Защита верхних и нижних отделов респираторного тракта осуществляется также разными субпопуляциями лимфоцитов, которые контролируются интерфероном 1 го типа. Главными эффекторами противовирусного клеточного ответа в нижних отделах респираторного тракта являются вирусспецифические цитотоксические лимфоциты (ЦТЛ) СD8+, правда, накопление этих клеток требует определенного времени. Генерация ЦТЛ CD8+ более успешна, если антигенпредставляющими клетками (АПК) служат дендритные клетки, способные к активации, под влиянием очень малого количества вирусного белка.
Снижение иммунологической резистентности и глубокое подавление функциональной активности различных компонентов иммунной системы приводят к возникновению вторичных бактериальных осложнений.
Таким образом, терапия гриппа и ОРВИ должна быть комплексной, адекватной этиологии и тяжести течения заболевания и направленной на все звенья патогенеза этого широко распространенного и нередко тяжелого заболевания. Особые требования должны предъявляться к этиотропным и патогенетическим средствам для лечения гриппа и ОРВИ.
Препараты, применяемые для терапии респираторных вирусных инфекций, должны способствовать элиминации возбудителя; стимулировать защитные силы организма; корректировать возникающие в процессе болезни функциональные нарушения.
Сегодня постоянно увеличивается арсенал лекарственных средств, используемых при гриппе и ОРВИ, отличающийся разнообразием и охватывающий все возможные способы влияния на инфекционный процесс. Он включает химиопрепараты этиотропного действия, средства для иммунокорригирующей, патогенетической и симптоматической терапии (табл. 1).
Сюда же относятся и антибиотики широкого спектра действия для профилактики и постгриппозных бактериальных осложнений [6].
Следует отметить значительный вклад академика АМН СССР А. А. Смородинцева, профессора Н. П. Чижова, а также многих других сотрудников НИИ гриппа СЗО РАМН в разработку противовирусных препаратов и стратегию их применения при ОРВИ и гриппе.
Противовирусные препараты — вещества, обладающие антивирусной активностью, представлены этиотропными средствами (химиопрепараты — истинные химические соединения различных классов), патогенетическими лекарственными средствами являются препараты неспецифического действия — интерфероны, их индукторы и, частично, иммунотропные препараты [4].
Существует несколько способов контроля вирусных инфекций. Неспецифический тип контроля, обеспечиваемый препаратами неспецифического действия (интерфероны, их индукторы и иммунотропные препараты), является наиболее эффективным, его антивирусный спектр очень широкий, но длительность эффекта короткая. Специфический тип контроля обеспечивается вакцинацией против основных заболеваний, согласно Национальному календарю прививок, его эффективность и длительность эффекта высокая, но спектр узкий. Химический тип контроля реализуется химиопрепаратами, активность узкая, длительность высокая [6, 17].
Химиопрепараты являются средством этиотропной терапии заболеваний дыхательных путей, поэтому основным показателем их клинической пригодности служит химиотерапевтический индекс (отношение специфической эффективности к токсичности). К основным недостаткам антивирусных химиопрепаратов относится узкий спектр действия и формирование резистентных вирусных штаммов, что сводит на нет эффективность терапии. Резистентность обусловлена мутациями в том вирусном белке, который является мишенью действия для препарата. Лекарственная устойчивость является результатом изменений наследственных свойств вирусов и развивается при многократном применении препаратов [5, 14].
Еще в 70 е годы прошлого столетия для лечения гриппа были предложены ингибиторы функции М2 белка — препараты первой группы, препараты адамантанового ряда: римантадин, амантадин, а несколько позже появилась новые лекарственные формы римантадина — Альгирем и Орвирем. Альгирем — это полимерный препарат с улучшенными фармакологическими свойствами. Все эти препараты блокируют места связывания вируса с поверхностью клеточной мембраны. Подавление репродукции вируса гриппа сопровождается индукцией интерферона как второго уровня защиты, усиливая химиотерапевтическое действие препарата. Нежелательные эффекты римантадина возникают при длительном назначении высоких доз или при их кумуляции в организме. Более того, в последние годы появились сведения об устойчивости штаммов вируса гриппа А к этим препаратам. Резистентность препарата обусловлена мутациями в положениях 26, 27, 30, 34 М2 белка.
Разработка ингибиторов нейраминидазы (осельтамивира и занамивира) явилась новым значительным достижением в области фармакотерапии гриппа. Известно, что нейраминидаза — это фермент, играющий определенную роль в начальных стадиях проникновения вируса в клетку и контролирующий процесс почкования и высвобождения вирусных частиц от мембран инфицированных клеток. Еще в 1999 г. появился первый ингаляционный ингибитор нейраминидазы — занамивир (Реленза). Препарат обладает низкой системной биодоступностью, выводится почками и не обладает лекарственным взаимодействием.
Проведенными доклиническими исследованиями установлено, что препарат Арбидол благодаря особенностям своего химического строения относится к препаратам с низкой токсичностью (ЛД > 3000 мг/кг массы тела животных). Показана хорошая переносимость препарата различными животными, отсутствие аллергогенного, мутагенного и тератогенного действия. Препарат прошел и большие клинические испытания с участием более чем 14 тысячи пациентов. Его использовали в период эпидемии гриппа А и В, в том числе и в период эпидемического сезона гриппа 2009–2010 гг. Как показали клинические исследования, Арбидол сокращает общую продолжительность заболевания, выраженность и длительность отдельных симптомов гриппа, а также способствует снижению риска развития постгриппозных осложнений, в том числе и у пожилых пациентов.
Максимальный клинический эффект при лечении гриппа и ОРВИ негриппозной этиологии может быть получен при сочетанном применении химиопрепаратов с препаратами неспецифического действия либо при использовании только препаратов патогенетической направленности: интерферонов их индукторов и иммуномодуляторов, обладающих противовирусной активностью.
Представляется закономерным включение индукторов интерферона 1 го и 2 го типа, к которым и относится Циклоферон, Амиксин, Кагоцел, Ларифан и др., в комплексное лечение гриппа и ОРВИ.
Индукторы интерферона обладают универсально широким диапазоном антивирусной активности (этиотропное действие) и выраженным иммуномодулирующим эффектом, не обладают антигенностью, синтез эндогенного интерферона сбалансирован, контролируется организмом, предотвращая побочные эффекты, характерные для экзогенно вводимых интерферонов. Однократное введение индуктора приводит к длительной циркуляции эндогенного интерферона (при введении циклоферона до 72 часов, а при введении Амиксина — до 48 часов, Кагоцела до пяти суток) [4, 6–17].
Наиболее перспективным и безопасным для применения в детской практике является отечественный препарат Циклоферон. Взаимодействие при высокой концентрации препарата с ДНК в клетках индуцирует транскрипцию генов, препарат транспортируется в ядро и ядрышки, где происходит их накопление, увеличивая время пребывания препарата в клетках, повышая интерферонпродуцирующую активность. Достоинством циклоферона является его полифункциональность — сочетание широкого спектра фармакологических эффектов.
Нормализация показателей клеточного иммунитета и концентрации иммуноглобулина А наблюдается при комбинированном применении Циклоферона и Биовестина-лакто. Увеличивается число детей, не болеющих ОРВИ в течение 3–6 месяцев после приема препаратов, обеспечивается снижение повторных ОРВИ и осложнений, снижается кратность (в 2,2 раза) и длительность острых эпизодов (на 2,7 дня), восстанавливается нормальная флора слизистых оболочек носа и зева. Как показали многочисленные исследования, Циклоферон обладает эпидемиологической эффективностью (индекс эффективности 2,9 при колебаниях от 2,4 до 3,4, при показателе защиты от 58,5% до 67,1%), отмечено снижение уровня заболеваемости в 2,9 раза. Кроме того, Циклоферон обладает цитопротективным действием на слизистую оболочку полости носа, снижает степень деструкции плоского и цилиндрического эпителия, повышает содержание лизоцима, увеличивает уровень S-IgA в слюне.
При включении Циклоферона в терапию микоплазменной инфекции сокращается лихорадочный период, интоксикация, уменьшается длительность катарального симптома, бронхиальной обструкции (в среднем на 3–1,6 дня). Улучшение клинической симптоматики происходит на фоне усиления макрофагальной активности, активации синтеза интерферона (в 1,5–1,9 раза), снижения уровня TNF, нарастания концентрации иммуноглобулина А, включая и секреторный его компонент, у 67–87% пациентов [8].
В период повышенного подъема заболеваемости гриппом A/H1N1 (sw)/09/04 осенью 2009 года проведена оценка эффективности Циклоферона. При своевременно начатом лечении, у взрослых больных уменьшался синдром интоксикации, исчезали катаральные явления к пятому дню болезни. Снижение температурной реакции отмечено на вторые сутки, а ее нормализация наступала к четвертым суткам приема препарата, без использования антибактериальных средств. Защита от гриппа и ОРВИ наблюдалась у 76,5% медицинских работников, контактирующих с больными гриппом и ОРВИ в осенний период 2009 года [19].
К поздним индукторам интерферона относится наш отечественный препарат Амиксин. Амиксин — это современный препарат, обладающий прямым противовирусным эффектом и одновременно способностью стимулировать выработку собственного интерферона в человеческом организме. Действующее вещество Амиксина — тилорон — усиливает образование в организме интерферонов не только клетками иммунной системы (лейкоцитами), но и клетками печени, а также кишечника. Иммуномодулирующий эффект Амиксина выражается в усилении образования антител (в зависимости от дозы препарата), восстановлении нормального баланса между Т-хелперами и Т-супрессорами, повышении активности клеток иммунной системы.
Амиксин способствует образованию позднего интерферона, пик его продукции приходится на 18 часов от момента введения препарата. Полностью исчезает из кровотока к 48 часам (рис.).
.jpg)
Препарат рекомендован для лечения гепатита А, В, энтеровирусных инфекций, для профилактики ОРЗ и гриппа, лечения хламидиоза, герпеса, энцефалитов, цитомегаловирусной инфекции.
Препарат при многократном введении в дозах, в несколько раз превышающих рекомендованные в настоящее время терапевтические дозы, может кумулироваться организмом и проявлять токсичность (химико-терапевтический индекс 2–4). При рациональном применении Амиксина в соответствии с инструкцией по медицинскому применению, введение препарата не влияет на параметры крови и хорошо переносится больными.
Из иммунотропных препаратов, обладающих интерферониндуцирующей активностью, следует остановиться на Имунофане, Бронхо-мунале, Рибомуниле, ИРС-19. Мишенью для препаратов являются фагоцитарные клетки. Препараты повышают функциональную активность фагоцитов, синтез провоспалительных цитокинов, усиливают активность естественных (натуральных) киллеров. Препараты рекомендуются для коррекции иммунного дисбаланса, профилактики и лечения инфекционно-воспалительных заболеваний ЛОР-органов у детей [16–17].
Рибомунил, Имунофан, ИРС-19, Имудон также являются средством патогенетической терапии. Препараты представляют собой микробные лиофилизированные лизаты, эффект которых направлен на повышение антиинфекционной и противовоспалительной активности организма. Иммуностимулирующее действие препаратов выражается в стимуляции иммунотропных клеток, повышая активность клеток фагоцитов ретикулярной системы эндотелия. Иммуностимулирующие препараты оказывают влияние на фагоцитирующие клетки (нейтрофилы, моноциты), влияя на окислительный метаболизм полиморфно-ядерных нейтрофилов, а также лимфоциты.
Кроме этого, отмечается увеличение содержания в слюне лизоцима, обладающего бактерицидной активностью. При воспалении слизистой оболочки дыхательных путей (ларингит, трахеит, бронхит) важное значение имеет прием противокашлевых препаратов центрального действия (при сухом непродуктивном кашле, а также при продуктивном кашле, когда он ухудшает качество жизни пациента). В этих случаях возникает проблема выбора препарата, способного снять раздражение дыхательных путей и одновременно облегчить отхождение мокроты. Существует ряд противокашлевых, муколитических и отхаркивающих препаратов отечественного и зарубежного производства. К таким препаратам относятся: Коделак Бронхо, Стоптуссин, Линкас, Гербион.
Коделак Бронхо — это комбинированный препарат, оказывающий муколитическое, противовоспалительное и отхаркивающее действие. Препарат назначается детям с 12 летнего возраста и взрослым. Применение его не рекомендуется у беременных, кормящих матерей и у лиц с заболеваниями печени.
Стоптуссин повышает секрецию бронхиальных желез и снижает вязкость слизи. Повышение секреции вызывается как прямым действием препарата на бронхиальные железы, так и рефлекторным путем, за счет стимуляции афферентных парасимпатических волокон, оказывающих влияние на дыхательный центр.
Сироп Линкас — комплексный фитопрепарат, действие которого обусловлено свойствами входящих в его состав компонентов: адхатоды сосудистой, солодки гладкой, перца длинного, фиалки душистой, иссопа лекарственного, алтея лекарственного, зифуса настоящего, альпинии галанга. Сироп Линкас уменьшает кашель и облегчает боль в горле, обладает отхаркивающим и муколитическим действием.
Для лечения кашля с первых дней жизни можно использовать бальзамы и сиропы Эвкабал, его натуральные фитокомпоненты безвредны, поэтому применяются для лечения больных любого возраста. Бальзам можно использовать даже для лечения детей, начиная с трех месяцев, а сироп — с 6 месячного возраста.
К сосудосуживающим назальным препаратам относится препарат, содержащий адреномиметик альфа-ксилометазолин (Ксимелин спрей в дозировке 0,5% — для детей от двух до шести лет; спрей 0,1% — для детей старше 9 лет). Появился новый Ксимелин Эко — в виде дозированного спрея, в двух дозировках: 0,05% и 1%, с двух до 10 лет, и 0,1% — старше 10 лет и взрослым. Препарат не содержит консервантов, поэтому его можно использовать для лиц с атопическим состоянием.
Таким образом, список лекарственных препаратов, разрешенных для применения, постоянно расширяется, эти препараты занимают достойное место, обеспечивая улучшение качества оказания медицинской помощи больным с ОРВИ и гриппом.
Литература
О. И. Киселев*, доктор медицинских наук, профессор, академик РАМН
Т. В. Сологуб**, доктор медицинских наук, профессор
М. Г. Романцов**, доктор медицинских наук, профессор
*ГУ НИИ гриппа МЗ РФ, **СПбГМА им. И. И. Мечникова, Санкт-Петербург
Читайте также:

