Что такое реверсия вируса
Обновлено: 25.04.2024


В последнее время взрослые и дети все чаще страдают кишечными инфекциями.
Кишечные инфекции встречаются в любое время года: вирусные, чаще всего встречаются в холодное время года (с ростом заболеваемости гриппом и ОРВИ), бактериальные - в теплое время года. Частой причиной развития кишечных инфекций являются вирусы, которые подразделяются на несколько видов. Один из них — норовирусы.
Ежегодно в мире норовирусы являются причиной 64 тыс. эпизодов диареи, требующих госпитализации, 900 тыс. посещений поликлиник с детьми в развитых странах и до 200 иыс. Смертельных случаев детей в возрасте до 5 лет. В России на долю норовирусных кишечных инфекций среди всех кишечных инфекций приходится 5-27%.
Норовирусная инфекция – это острая кишечная инфекция, возбудителем которой является норовирус – один из разновидностей энтеровирусов.
Возбудитель инфекции – норовирус, вирус семейства Calviviridae.
Источник инфекции – больные клинически выраженными (70%) и бессимптомными (30%) формами. Вирус присутствует в фекалиях, рвотных массах человека.
При исследовании норовирусной инфекции на волонтерах, проведенном более 30 лет назад, было установлено существование двух групп людей, различающихся восприимчивостью к инфекции вирусом Narwolk. Одни лица неоднократно подвергались инфекции, тогда как другие были устойчивы к ней. В связи с этим, была выдвинута гипотеза о существовании генетического фактора, опеделяющего индивидуальную резистентность к данному заболеванию. Тем не менее, норовирусная инфекция крайне заразна. Заражаются люди всех возрастов.
Как происходит заражение?
Механизм передачи инфекции - фекально-оральный.
Основные пути передачи инфекции:
· пищевой —употребление немытых овощей или фруктов;
· водный — употребление жидкостей, зараженных вирусом;
· контактно-бытовой - использование обсемененной посуды, предметов обихода; немытые руки.
Человек, инфицированный вирусом, заразен для окружающих во время острой фазы заболевания и в последующие 48 часов (инкубационный период).
Наиболее восприимчивы к кишечным инфекциям:
• Люди преклонного возраста
• Лица с заболеваниями желудка и кишечника
• Люди, страдающие алкоголизмом
• Имеющие ослабленный иммунитет
Первые признаки заболевания возникают спустя 15-48 часов после заражения. В клинической картине норовирусной инфекции как у детей, так и у взрослых основной является триада симптомов: острая диарея, рвота, лихорадка. При норовирусной инфекции у заболевших наблюдаются следующие симптомы: тошнота (79%), рвота (69%), диарея (66%), головная боль (22%), лихорадка (37%), озноб (32%), симптомы ОРЗ (30%). Среднетяжелая форма норовирусной инфекции встречается в 20-40% случаев, легкое течение заболевания отмечается у 60-80% больных. Заболевание начинается остро с подъема температуры, эпизоды лихорадки могут продолжаться 1-2 дня. При развитии заболевания присоединяется рвота, которая продолжается не более 5 раз, далее присоединяется основной симптом заболевания – диарея.
Признаки заболевания обычно проходят самостоятельно через 12-72 часа. После выздоровления организм вырабатывает нестойкий иммунитет к вирусу — до восьми недель. По истечении этого периода времени у человека снова может развиться норовирусная инфекция.
Основную опасность при норовирусной инфекции, представляет обезвоживание от потери жидкостей и солей при рвоте и поносе. Жажда — первый признак обезвоживания.
Другие симптомы обезвоживания: головокружение, головная боль, усталость, сухость во рту, пересыхание губ и глаз, редкое мочеиспускание (менее 3-4 раз в сутки).
Если не восполнять запасы потерянной жидкости, обезвоживание усилится и может вызвать осложнения, такие как, падение кровяного давления и отказ почек. Это может привести к летальному исходу.
Госпитализации подлежат больные с выраженными признаками обезвоживания. Основная масса больных лечится на дому. Проводится регидратационная терапия. Восполнение жидкости в объемах, соответствующих потерям. Назначается щадящая диета до восстановления стула.
Несмотря на то, что норовирусы обладают высокой заразностью, устойчивостью и длительным сохранением жизнеспособности во внешней среде, вакцины от этого заболевания на сегодняшний день нет.
В очаге инфекции проводится активное выявление больных путем опроса, осмотра врачом-инфекционистом, при утренних осмотрах медицинским персоналом (для организованных детских групп); за лицами, подвергшимися риску заражения, устанавливается медицинское наблюдение сроком на 2 дня; в случае выявления лиц с подозрениями на данное заболевание, проводится их немедленная изоляция. Изоляция проводится до клинического выздоровления (отсутствие рвоты, диареи) или до выписки из стационара (в случае госпитализации).
При уходе за больным или контакте с предметами, окружающими больного, руки необходимо защищать перчатками, тщательно мыть их с мылом и обрабатывать спиртсодержащими антисептиками. Влажная обработка всех поверхностей, с которыми контактировал заболевший, должна проводиться не реже одного раза в день, обязательно с добавлением хлорсодержащих дезинфицирующих средств. Посуду, которую использовал больной, а также все моющиеся предметы необходимо кипятить. Вещи, запачканные рвотными массами, должны сразу стираться при температуре не менее 60 º.

Основные принципы профилактики инфекции:
• Соблюдение правил личной гигиены: тщательно мыть руки перед приемом, раздачей пищи, после посещения туалета, улицы.
• Следить за чистотой рук у детей, научить их соблюдать правила личной гигиены
• Употребление кипяченой или бутилированной воды
• Мытье овощей, фруктов перед употреблением под проточной водой, а для детей - кипяченой.
• Тщательная термическая обработка необходимых продуктов
• Употребление продуктов желательно сразу после приготовления
• Рекомендовано использовать индивидуальное полотенце или белье.
• Выезжая на отдых необходимо брать с собой запас чистой питьевой воды, не употреблять воду из откры
• Купаться только в отведенных для этих целей местах. При купании в водоемах и бассейнах не допускать попадания воды в рот.
Главная защита от норовирусной и других кишечных инфекций – это соблюдение правил личной гигиены, а также своевременное обращение за медицинской помощью.

Как бы странно это ни звучало, мы должны понимать, что тяжело болеют и даже умирают люди не от коронавируса, а от действия собственной иммунной системы. Наша иммунная система иногда работает так быстро и активно, пытаясь бороться с этим вирусом, что уничтожает наш собственный организм.
Начнем с того, что коронавирус проникает в наше тело через нос и рот.
Очень быстро он внедряется в нормально функционирующие клетки, копируя себя десятки тысяч раз. Вскоре количество вируса во рту, горле и носу становится очень велико.

Цитокины представляют собой небольшие белковые информационные молекулы, которые вызывают повышение температуры. На этой стадии болезни, кроме температуры у больного также появляется сухой кашель. Это происходит потому, что вирус продолжает раздражать верхние дыхательные пути, и наш организм доступными ему способами старается избавиться от раздражителя. Но даже в этом случае многим людям удается самостоятельно бороться с вирусом с помощью недели отдыха и парацетамола.

Настоящие проблемы возникают, когда вирус попадает в наши легкие. Организм начинает производить больше цитокинов, наша иммунная система работает очень активно в попытке бороться с вирусом. Все большее количество цитокинов становятся в результате опасными для организма.
У человека развивается пневмония, которая является очень серьезным осложнением коронавирусной инфекции. Альвеолы наполняются жидкостью, так что легкие не могут снабжать организм достаточным количеством кислорода. В таких случаях необходимо дополнительное введение кислорода. В очень серьезных случаях такое состояние может привести к смерти.
Есть и другие тяжелые последствия производства нашим организмом избыточного количества цитокинов. В какой-то момент наш организм производит так много цитокинов, что мы говорим о цитокиновом шторме (синдроме высвобождения цитокинов), когда концентрация цитокинов в крови превышает ее нормальные значения в десятки, сотни раз, и проявляется сильной головной болью, миалгиями, болями в поясничной области. В результате лейкоциты начинают атаковать здоровые клетки нашего организма, что приводит к повреждению не только легких но и сердца. Поврежденное сердце больше не в состоянии перекачивать достаточное количество крови, что вызывает нарушение функции или даже отказ таких жизненно важных органов, как печень, почки, мозг, и, в результате, может привести к смерти. Повторим, что все эти осложнения происходят не из-за самого вируса, а из-за деятельности иммунной системы, которая работает так активно, что разрушает наш собственный организм.

Вирусология занимает важное место среди биологических дисциплин. Современный медицинский или ветеринарный специалист должен знать не только клинико–патологическую сторону заболевания, но и иметь четкое представление о вирусах, их свойствах, методах лабораторной диагностики и свойствах постинфекционного и поствакцинального иммунитета.

Вирус (от лат. virus — яд) является простейшей неклеточной формой жизни в виде микроскопической биологической частицы, представляющей собой молекулы нуклеиновых кислот (ДНК или РНК), заключённых в защитную белковую оболочку (капсид) и способные инфицировать живые организма.
- мутации, то есть изменении последовательности нуклеотидов в определенной области генома вируса, что приводит к фенотипически выраженному изменению свойства;
- рекомбинации, то есть обменом генетическим материалом между двумя вирусами, близкими, но различными по наследственным свойствам.
Мутации у вирусов
- спонтанные;
- индуцированные (вызванные).
Но точечные мутации не всегда приводят к изменению фенотипа. Существует целый ряд причин, по которым такие мутации не могут проявляться. Одна из них - вырождение генетического кода. Код синтеза белка вырождается, что означает, что некоторые аминокислоты могут быть закодированы несколькими триплетами (кодонами). Например, аминокислота лейцин может быть закодирована шестью триплетами. Поэтому, если молекула РНК заменяет триплет ЦУУ на ЦУЦ, ЦУА на ЦУГ, то синтезированная молекула белка все еще будет содержать аминокислоту лейцин.
Поэтому ни структура белка, ни его биологические свойства не нарушаются. Природа использует своего рода синонимичный язык и, заменяя один кодон другим, закладывает в них одно и то же понятие (аминокислоту), тем самым сохраняя естественную структуру и функцию синтезируемого белка.

Другое дело, если аминокислота кодируется только одним триплетом, например, синтез триптофана кодируется и заменяется только триплетом УГГ, то есть синонимом, который отсутствует. В этом случае в белок включается еще одна какаялибо аминокислота, которая может привести к появлению мутантного признака.
Аберрация в фагах вызвана делециями (потерями) различного числа нуклеотидов, от одной пары до последовательности, вызывающей одну или несколько функций вируса. Как спонтанные, так и индуцированные мутации также делятся на прямые и обратные мутации. Мутации могут иметь разные последствия. В некоторых случаях они приводят к изменению фенотипических проявлений в нормальных условиях.

Например, увеличивается или уменьшается размер бляшек под агарным покрытием; увеличивается или ослабевает вирулентность для определенного вида животных; вирус становится более чувствительным к действию химиотерапевтического агента и т. д.
В других случаях мутация является фатальной, поскольку она нарушает синтез или функцию жизненно важного вирусного белка, например, такого как вирусная полимераза. В некоторых случаях мутации являются условно летальными, так как вирусспецифический белок сохраняет свои функции при определенных условиях и теряет эту способность в неразрешающих (непермиссивных) условиях.
Типичным примером таких мутаций являются термочувствительные – ТS-мутации, при которых вирус теряет способность к размножению при повышенных температурах (+39-42°С), сохраняя эту способность при нормальных температурах роста (+36-37°С). Морфологические или структурные мутации могут влиять на размер вириона, первичную структуру вирусных белков и изменения в генах, определяющих ранние и поздние вирусные ферменты, обеспечивающие размножение вируса. Мутации также могут быть различными по своему механизму.
В одних случаях происходит делеция, то есть потеря одного или нескольких нуклеотидов, в других - встраивание одного или нескольких нуклеотидов, а в некоторых случаях один нуклеотид заменяется другим. Мутации могут быть прямыми или обратными. Прямые мутации меняют фенотип, а обратные мутации – реверсии) - восстанавливаются. Реальная реверсия возможна, когда обратная мутация происходит вместе с первичным повреждением, и псевдореверсия, когда мутация происходит в другой области дефектного гена (интрагенное торможение мутации) или в другом гене (экстрагенное подавление мутации).
Реверсия - не редкое явление, потому что ревертанты обычно лучше приспособлены к данной клеточной системе. Поэтому при создании мутантов с определенными свой ствами, например, вакцинных штаммов, следует ожидать возможного превращения их в дикий тип. Вирусы отличаются не только своими небольшими размерами, селективной способностью к размножению в живых клетках, особенностями строения наследственного вещества, но и значительной изменчивостью от других представителей живого мира.
Изменения могут влиять на размер, форму, патогенность, антигенную структуру, тканевую тропность, устойчивость к физико-химическим воздействиям и на другие свойства вирусов. Значение причин, механизмов и характера изменений имеет большое значение при получении необходимых вакцин для вирусных штаммов, а также для разработки эффективных мер борьбы с вирусными эпизодами, в ходе которых, как известно, свойства вирусов могут существенно изменяться.
Мутация вирусов может происходить в результате химических изменений цистронов или нарушения последовательности их расположения в структуре молекулы вирусной нуклеиновой кислоты. В зависимости от условий различают естественную изменчивость вирусов, наблюдаемую в нормальных условиях размножения, и искусственную изменчивость, получаемую в результате многочисленных специальных пассажей или воздействия на вирусы определенных физических или химических факторов (мутагенов). В обычных природных условиях изменчивость проявляется не во всех вирусах одинаково.
Этот признак наиболее заметен у вируса гриппа и вирус ящера. Значительная изменчивость отмечается у вируса гриппа. Об этом свидетельствует большое количество вариантов у разных типов этих вирусов, а также значительные изменения его антигенных свойств в конце почти каждой эпизоотии.
Частота мутаций и механизмы их возникновения
Мутации бактериофагов изучались очень интенсивно не только с целью генетического анализа, но и с целью получения информации о свойствах самих фагов. Частота появления мутантов в потомстве фагов варьируется очень сильно: например, одни мутанты образуются с частотой не более 10, а другие-с частотой 10 и выше. Неблагоприятное воздействие высокочастотных мутаций обычно компенсируется эффектом отбора. Например, мутантный фаг может быть заменен диким типом, что дает более высокий выход фага. Высокая частота вспышек обычно характерна для таких мутаций, которые могут происходить как во многих локусах, так в одном и том же локусе.
В тех случаях, когда нормальный признак соответствует функциональной форме гена, а мутант появляется в результате изменения в любой точке локуса, частота прямых мутаций окажется выше, чем частота обратных мутаций, так как обратные мутации должны приводить к восстановлению нормального состояния. Иногда ревертанты на самом деле являются псевдоревертантами: это происходит либо из-за изменений в другом гене (мутации-супрессоры), либо из-за изменений в том же гене, которые вызывают другую, но также активную форму продукта.
У зрелых фагов частота спонтанных мутаций очень мала, но они могут быть индуцированы под влиянием таких мутагенных факторов, как рентгеновские или ультрафиолетовые лучи, азотистая кислота, гидроксиламин или алкилирующие агенты. Азотистая кислота дезаминирует основания нуклеотидов, а этилметилсульфат их этилирует. Гидроксиламин превращает шитозин в урацил. В результате ошибок, допущенных при репликации химически модифицированной нуклеиновой кислоты, происходят мутации, и потомство фагов, полученное из бактерии, содержит как нормальные, так и мутантные частицы. Однако, как и при обработке мутагенного фага, содержащего одноцепочную ДНК, образуется чистый мутантный клон.
Изучение мутационного процесса, происходящего при размножении фагов, непосредственно связано с анализом развития фагов. Давайте рассмотрим процесс спонтанной мутации. В бактериальной клетке, в которой произошла мутация фага, 6 образуются как нормальный, так и мутировавший фаги. Количество мутантных фаговых частиц, содержащихся в популяции фагов, происходящих из этой отдельной бактериальной клетки, очевидно, определяется характером размножения фагов, поскольку новые гены могут быть сформированы только путем репликации уже существующих. Если вероятность мутации одинакова для каждой репликации, то число мутантов зависит от механизма репликации.
Например, если каждая новая копия гена формируется независимо от других, то распределение мутантных копий в потомках фагов от разных инфицированных бактерий будет случайным. Если же, наоборот, каждая из полученных копий воспроизводится, то в свою очередь мутантные копии будут разделены на группы или клоны, состоящие из мутантных "сибсов".
Индуцированные хозяином модификации бактериофагов
Помимо мутаций, бактериофаги подвержены негенетическим изменениям, в которых главная роль принадлежит клетке-хозяину. Это явление было названо модификациями, вызванными хозяином. Значение этих модификаций для молекулярной биологии состоит в том, что они показали способность внутриклеточной среды вызывать такие изменения в химической структуре генетического материала, которые могут быть использованы для идентификации клеточных линий, синтезирующих ДНК.
Подобные явления были впервые обнаружены на фаговой ДНК, но они также справедливы и для каждой бактериальной клеточной ДНК. Есть также наблюдения, при которых это явление относится и к эукариотическим клеткам. В особых случаях могут возникнуть более сложные ситуации. Двустороннее ограничение фага двумя хозяевами иногда наблюдается, но оно не обязательно. Фаги, отторгнутые клетками, способны адсорбироваться на них и проникать в их ДНК добавляя часть собственной ДНК. Однако последняя часть быстро разрушается, и репликация не происходит.
Деградация ДНК вызывается специфическими эндонуклеазами (рестриктазами или R-нуклеазами), которые могут обнаруживать и расщеплять определенные участки ДНК, если они не были модифицированы под влиянием М-ферментов. После этого ДНК расщепляется экзонуклеазами на отдельные нуклеотиды. Бактериальный штамм может иметь одну или несколько R-нуклеаз и в то же время M-ферменты, которые защищают собственную ДНК клетки. Предложена удобная номенклатура этих ферментов. Согласно ряду данных, области детекции R-нуклеазы не всегда совпадают с областями расщепления ДНК; возможно, что фермент может мигрировать по цепочке до того, как найдет область, где происходит расщепление ДНК. Функциональная роль индуцированных хозяином модификаций неясна.
Как видим, мутирование вирусов проходит достаточно сложный и тернистый путь в приобретении новых вирулентных свойств. Эти свойства могут быть как ослабляющими для развития инфекционного процесса, так и крайне агрессивными в своём новом виде.

Среди различных микробных препаратов, применяемых для профилактики, лечения и диагностики инфекционных заболеваний большое место занимают вакцины - биопрепараты, предназначенные для создания активного искусственного иммунитета.
В качестве антигенов вакцины могут содержать убитые или живые микробные тела, либо извлеченные из них химическим путем полные антигены -глюцидо-липоидные полипептидные комплексы. В зависимости от количества антигенов различают моно-, ди-, три-, тетра- и поливакцины.
Для изготовления вакцин применяются такие штаммы микробов, которые удовлетворяют требованиям специальных инструкций по отбору, проверке и хранению культур, применяемых для изготовления вакцин. Изучение и апробация штаммов на предмет соответствия их требованиям инструкций производится Государственным контрольным институтом медицинских биологических препаратов, там же они хранятся в музее живых культур как эталонные, от них отвивают дубликаты и рассылают в сопровождении специального паспорта в институты, изготавливающие вакцины, для использования в производстве. В паспортах, сопровождающих такие штаммы, указываются основные их свойства - морфологические, культуральные, биохимические, антигенные.
Штаммы, полученные из контрольного института, используются в производстве вакцин только после проверки на местах. В производственных институтах проводится большая работа по изучению условий стабилизации свойств штаммов, предназначенных для изготовления вакцин. В настоящее время стабильность свойств культур обеспечивается хранением их в высушенном состоянии в условиях вакуума в запаянных ампулах. Бактериальные культуры, кроме того, можно хранить в пробирках на плотной питательной среде, оптимальной для данного вида микроба. Пробирки в этом случае запаивают, либо заливают пробки расплавленным воском или парафином, чтобы предохранить культуру от высыхания при длительном хранении. Штаммы, хранящиеся в лаборатории, регистрируются в специальных журналах, где записывают паспортные данные, а также результаты текущих проверок, регламентируемых инструкциями.
Требования инструкций к производственным штаммам разных видов и различных групп микроорганизмов направлены к одной цели - обеспечению малой реактогенности, полной безвредности и высокой эпидемиологической эффективности приготовленных из них вакцин. Методы определения этих свойств производственных штаммов в зависимости от того, к какому виду микробов они применяются, имеют специфические особенности, которые отражены в специальной части. В принципе иммуногенность их определяется путем выявления устойчивости животных, иммунизированных опытными вакцинами, приготовленными из этих штаммов, к заражению заведомо смертельными дозами соответствующих культур.
Вирулентность штаммов изучается путем заражения чувствительных животных, чаще всего мышей, и характеризуется заведомо смертельными, минимальными смертельными и 50 %-ными смертельными дозами культур испытуемых штаммов.
Для выявления токсичности животным вводится убитая нагреванием культура производственных штаммов.
Конкретные показатели иммуногенности, вирулентности и токсичности для разных видов микробов определяются инструкциями. Штаммы, обладающие меньшей иммуногенностью и вирулентностью или большей токсичностью, чем это установлено инструкцией, для производства вакцин не применяются.
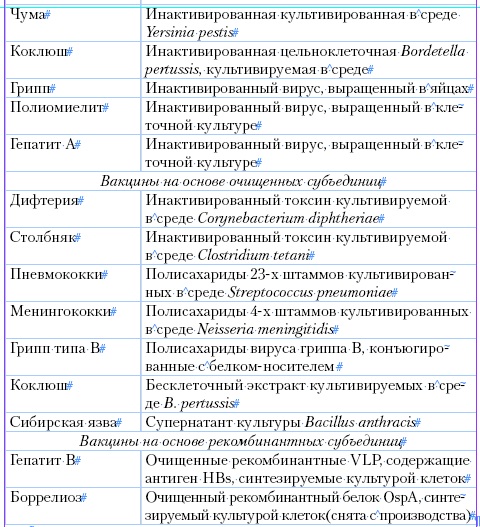
Таблица 1
Основные типы вакцин

Читайте также:

