История болезни вич инфекция и гепатит в
Обновлено: 25.04.2024
В течение последних месяцев у нее были многократные приступы лихорадки и поносов. Анализ кала на дисбактериоз, проведенный семейным врачом, был отрицательным. Также в течение нескольких месяцев у пациентки были увеличены (но безболезненные) шейные и паховые лимфатические узлы.
Пациентка, в связи с профессиональной деятельностью, в течение 4-х лет живет попеременно в Германии и Африке. Была проведена аппендэктомия (удаление червеобразного отростка (аппендикса), другие заболевания отрицает. Употребление никотина и алкоголя также отрицает.
Был проведен очный осмотр пациентки врачом:
Пациентка находится в незначительно сниженном общем состоянии, вес в норме (169 см, 60 кг).
ЧСС: 72 в мин.
АД: 125/80 мм рт. ст.
ЧД: 13 в мин.
Температура тела 36,7° С.
Кожа: теплая, сухая, тургор (натяженность и эластичность) нормальный. В левой половине грудной клетки имеется экзантема (кореподобное высыпание) с содержащими жидкость пузырьками и участками, покрытыми корочками.
Слизистые оболочки: влажные, слизистая оболочка полости рта воспалена. Белый, снимающийся налет на языке, мягком небе и глотке.
Лимфатические узлы: шейные, подмышечные и паховые узлы безболезненно увеличены.
Сердце: сердечные тоны ритмичные, патологические шумы отсутствуют.
Легкие: звучный перкуторный тон, везикулярное дыхание, хрипы отсутствуют.
Живот: без особенностей.
Область почек: без патологии.
Конечности: без особенностей.
Ориентировочный неврологический осмотр без особенностей.
Также был проведен лабораторный анализ:
эритроциты 4,2 млн/мКл;
гемоглобин 11,7 г/дл;
гематокрит 35,2%; 3,9 тыс/мкл;
MCV 83,8 фл; МСН 27,9 пг;
МСНС 33,2 г/дл;
тромбоциты 212 тыс/мкл;
натрий 138 ммоль/л;
калий 4,4 ммоль/л.
лейкоцитарная формула без особенностей.
протромбиновое СРБ 14 мг/л;
АЧТВ, глюкоза, мочевина, креатинин, АЛТ и АСТ в пределах нормальных значений.
На основании результатов анализов и осмотра пациентки можно сказать, что имеющиеся у нее высыпания на коже являются проявлением опоясывающего лишая. Типичными являются односторонние, строго сегментарные болезненные везикулярные высыпания. Другие, обнаруженные при осмотре симптомы, указывают на ротоглоточноую молочницу (кандидозный стоматит). Типичным для этого инфицирования дрожжевыми грибами рода Candida являются белые, отделяемые налеты на слизистой оболочке полости рта и глотки.
Результаты осмотра и анализов позволяют диагностировать наличие у пациентки ВИЧ-инфекции.
На наличие инфекции также указывают следующие признаки:
- опоясывающий лишай возникает у молодых пациентов преимущественно в рамках иммунодефицита, например, вследствие ВИЧ-инфекции;
- ротоглоточный кандидоз – возникает, прежде всего, у пациентов с ослабленными защитными функциями организма;
- приблизительно у половины ВИЧ-инфицированных, также как и у данной больной, развивается лимфаденопатия с персистирующим (> 3 месяцев) увеличением лимфатических узлов в минимум двух внепаховых локализациях;
- имеющиеся у пациентки общие симптомы (выраженная утомляемость, слабость, лихорадка, ночная потливость, потеря веса и поносы) являются малоспецифичными, но типичными для ВИЧ-инфекции.
С точки зрения дифференциального диагноза в первую очередь в поле зрения попадают :
врожденный или вторичный иммунодефицит.
ВИЧ-инфекция вызывается вирусом иммунодефицита человека. Перенос инфекции происходит половым путем, парентерально или вертикально. За начальной, напоминающей мононуклеоз стадией (острая ВИЧ-инфекция) как правило, следует бессимптомный интервал (клиническая латентная фаза), которая через несколько лет проявляется хронической симптоматической ВИЧ-инфекцией и заканчивается терминальной стадией СПИД. Для диагноза требуется серологическое (ELISA, белковый иммуноблот) или прямое (ПЦР) подтверждение наличия возбудителя. Инфицированным пациентам необходим врачебный контроль за течением заболевания и эффективностью терапии. Наиболее важным терапевтическим воздействием является комбинированная высокоактивная антиретровирусная терапия, которая со времени её внедрения в практику значительно улучшила прогноз пациентов с ВИЧ.
Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
Порядок оказания медицинской помощи взрослому населению при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции) установлен Приказом Минздрава России от 08.11.2012 N 689н
1. Настоящий Порядок устанавливает правила оказания медицинской помощи взрослому населению при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции) (далее соответственно - медицинская помощь, больные ВИЧ-инфекцией), в медицинских организациях.
3. Медицинские организации, оказывающие медицинскую помощь, осуществляют свою деятельность в со-ответствии с приложениями N 1 - 15 к настоящему Порядку.
5. Скорая, в том числе скорая специализированная, медицинская помощь больным ВИЧ-инфекцией оказывается в экстренной и неотложной формах вне медицинской организации, а также в амбулаторных и стационарных условиях.
6. При наличии медицинских показаний после устранения угрожающих жизни состояний больные ВИЧ-инфекцией переводятся в инфекционное отделение (койки) медицинской организации для оказания медицинской помощи.
7. При оказании скорой медицинской помощи больным ВИЧ-инфекцией в случае необходимости осуществляется их медицинская эвакуация, которая включает в себя санитарно-авиационную и санитарную эвакуацию.
8. Первичная медико-санитарная помощь больным ВИЧ-инфекцией предусматривает мероприятия по профилактике, диагностике и лечению ВИЧ-инфекции, формированию здорового образа жизни и санитарно-гигиеническому просвещению, направленному на изменение поведения больных ВИЧ-инфекцией, с целью обеспечения предотвращения дальнейшего распространения ВИЧ-инфекции.
- назначение обследования на ВИЧ-инфекцию с обязательным проведением до- и послетестового консультирования;
- направление больного с подозрением на ВИЧ-инфекцию к врачу-инфекционисту центра профилактики и борьбы со СПИД (далее - Центр СПИД).
11. При направлении больного к врачу-инфекционисту врач, направляющий пациента, представляет выписку из амбулаторной карты (истории болезни) с указанием диагноза, сопутствующих заболеваний и имеющихся данных лабораторных и функциональных исследований.
12. Первичная медико-санитарная помощь больным ВИЧ-инфекцией оказывается врачами-терапевтами, врачами-терапевтами участковыми и врачами общей практики (семейными врачами), врачами-инфекционистами, а также врачами-специалистами иных специальностей и медицинскими работниками со средним медицинским образованием в амбулаторных условиях и в условиях дневного стационара в медицинских организациях, осуще-ствляющих первичную медико-санитарную помощь.
13. Оказание больным ВИЧ-инфекцией медицинской помощи при заболеваниях, не связанных с ВИЧ-инфекцией, проводится соответствующими врачами-специалистами с учетом рекомендаций врачей-инфекционистов.
14. Специализированная, в том числе высокотехнологичная, медицинская помощь больным ВИЧ-инфекцией оказывается врачами-инфекционистами на основе установленных стандартов медицинской помощи в отделениях для лечения больных ВИЧ-инфекцией медицинских организаций, оказывающих медицинскую помощь по профилю "инфекционные заболевания".
При отсутствии в медицинской организации отделения для лечения больных ВИЧ-инфекцией оказание спе-циализированной медицинской помощи осуществляется в стационарных условиях на базе инфекционного отде-ления, имеющего в своем составе выделенные койки для лечения больных ВИЧ-инфекцией.
17. Специализированная помощь больным ВИЧ-инфекцией в медицинских организациях, оказывающих ме-дицинскую помощь по профилю "инфекционные заболевания", осуществляется после направления больного в соответствующую медицинскую организацию врачом-инфекционистом медицинской организации, оказывающей амбулаторную помощь, а также при самостоятельном обращении больного ВИЧ-инфекцией.
18. Специализированная помощь больным ВИЧ-инфекцией включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских тех-нологий, а также медицинскую реабилитацию.
20. Оказание медицинской помощи в стационарных условиях больным ВИЧ-инфекцией осуществляется по медицинским показаниям (тяжелое и средне тяжелое течение ВИЧ-инфекции; необходимость дополнительных клинических, лабораторных и инструментальных исследований для проведения дифференциальной диагностики; отсутствие клинического эффекта от проводимой терапии в амбулаторных условиях и при наличии эпидемических показаний).
21. Лечение больных ВИЧ-инфекцией в стационарных условиях осуществляется по направлению участкового врача, врача общей практики (семейного врача), врача-инфекциониста, медицинских работников, выявивших заболевание, требующее оказания медицинской помощи в стационарных условиях.
22. В медицинской организации, в структуре которой организовано инфекционное отделение для оказания специализированной медицинской помощи больным ВИЧ-инфекцией, рекомендуется предусматривать отделение анестезиологии и реанимации или палату (блок) реанимации и интенсивной терапии, клинико-диагностическую, бактериологическую, вирусологическую, иммунологическую лаборатории и лабораторию молекулярно-генетической диагностики возбудителей инфекционных болезней.
23. В медицинской организации, оказывающей специализированную медицинскую помощь больным ВИЧ-инфекцией в стационарных условиях, должна быть предусмотрена возможность проведения в экстренном поряд-ке клинических анализов крови и мочи, биохимического анализа крови, газового состава крови, кислотно-щелочного соотношения, коагулограммы, электрокардиографии, рентгенографии, эзофагогастродуоденоскопии, искусственной вентиляции легких.
24. При выявлении у больного ВИЧ-инфекцией, находящегося на стационарном лечении, показаний к направлению в отделение для лечения больных ВИЧ-инфекцией, перевод осуществляется только после консультации врача-инфекциониста и при стабильном состоянии пациента.
25. При выявлении у больного ВИЧ-инфекцией заболеваний, не требующих лечения в отделении для лечения больных ВИЧ-инфекцией (в том числе гематологического, онкологического заболевания или туберкулеза), лечение и наблюдение больного ВИЧ-инфекцией осуществляется в профильных отделениях или стационарах, имеющих в своем составе выделенные койки для лечения больных ВИЧ-инфекцией, на основе взаимодействия врачей-специалистов с врачом-инфекционистом.
При отсутствии выделенных коек для лечения больных ВИЧ-инфекцией наблюдение и лечение соответст-вующей патологии осуществляется в профильных медицинских организациях на общих основаниях.
26. При выявлении у больного ВИЧ-инфекцией медицинских показаний к высокотехнологичным методам лечения медицинская помощь оказывается ему в соответствии с установленным порядком оказания высокотех-нологичной медицинской помощи на общих основаниях.
27. Медицинская помощь больным ВИЧ-инфекцией с жизнеугрожающими острыми состояниями осуществляется (вне зависимости от стадии ВИЧ-инфекции) в отделениях реанимации и интенсивной терапии медицинских организаций на основе утвержденных стандартов медицинской помощи и на основе взаимодействия врача-реаниматолога и врача-инфекциониста.
28. Паллиативная помощь больным ВИЧ-инфекцией осуществляется в отделениях и палатах паллиативной помощи больным ВИЧ-инфекцией на основе установленных стандартов медицинской помощи в медицинских организациях, оказывающих медицинскую помощь по соответствующему профилю.
При отсутствии отделений и палат паллиативной помощи для лечения больных ВИЧ-инфекцией они могут быть направлены в хоспис, больницу сестринского ухода и в медицинские организации, обеспечивающие паллиативную помощь больным с наличием морфологически подтвержденного диагноза распространенной формы злокачественного образования, тяжелых необратимых неврологических нарушений и тяжелого хронического болевого синдрома.
Наличие хронического гепатита С (ХГС) и ВИЧ-инфекции одновременно ассоциируется со значительной частотой неблагоприятных исходов вследствие развития цирроза и/или первичного рака печени, а также общностью эпидемиологических, социальных и экономических факторов. При сочетании этих инфекций отмечаются более высокий титр вируса гепатита С, выраженное прогрессирование хронического гепатита и высокий риск цирроза печени. При этом цирроз печени развивается быстрее и в 3 раза чаще у ВИЧ-инфицированных, чем у больных моноинфекцией гепатита С.
Цель исследования: выявить клинические и лабораторные особенности больных ХГС и ВИЧ-инфекцией.
Материал и методы: в исследование включены 173 пациента с ХГС и ВИЧ-инфекцией. Стандартную терапию ХГС (пегилированный интерферон альфа-2а + рибавирин) получали 45 больных, антиретровирусную терапию — 29. Чаще определялся генотип 1 вируса гепатита С (91 пациент, 52,6%). ХГС преобладал у пациентов мужского пола (в группе 1 — 64,3%, в группе 2 — 71,1%) и в наиболее трудоспособном возрасте от 20 до 30 лет (в группе 1 — 68,8%, в группе 2 — 80%).
Результаты исследования: среди больных, поступивших в стационар, 55,5% имели смешанную форму гепатита (ХГС + токсический гепатит) и у 17,2% выявлен цирроз печени. У 22,6% больных противовирусная терапия была отменена вследствие развития побочных реакций или неэффективности. Значительное количество пациентов до поступления в стационар злоупотребляли алкоголем (54,7%), наркотиками (25,8%), имели хронические заболевания: панкреатит, бронхит.
Заключение: среди пациентов с ХГС и ВИЧ-инфекцией, поступающих в стационар, преобладают больные со смешанной формой гепатита (ХГС + токсический гепатит). Большинство больных не получают стандартную противовирусную терапию ХГС вследствие выраженного иммунодефицита, злоупотребления алкоголем, приема психотропных веществ или отказа от лечения.
Ключевые слова: ВИЧ-инфекция, хронический гепатит С, цирроз печени, противовирусная терапия, антиретровирусная терапия, интерферон альфа-2а, рибавирин, генотип, оппортунистические инфекции.
Для цитирования: Сундуков А.В., Мельников Л.В., Евдокимов Е.Ю. Характеристика больных хроническим гепатитом С и ВИЧ-инфекцией. РМЖ. Медицинское обозрение. 2018;2(7(II)):64-67.
A.V. Sundukov 1 , L.V. Melnikov 2 , E.Yu. Evdokimov 3
1 Evdokimov Moscow State University of Medicine and Dentistry
2 Penza State University
3 Central Research Institute of Epidemiology, Moscow
The presence of HIV infection together with chronic hepatitis C (CHC) is associated with a significant incidence of an adverse events due to the development of cirrhosis and/or primary liver cancer, as well as a similarity of epidemiological, social and economic factors. In the case of these infections, there is a higher titer of hepatitis C virus, significant progression of chronic hepatitis and a high risk of the liver cirrhosis. At the same time, liver cirrhosis develops faster and 3 times more often in HIV-infected patients than in patients with hepatitis C monoinfection.
Aim: to identify the clinical and laboratory features of patients with CHC and HIV infection.
Patients and Methods: the study included 173 patients with CHC and HIV infection. 45 patients underwent standard therapy (pegylated interferon alfa-2a + ribavirin) of CHC. Antiretroviral therapy was followed by 29 patients. The 1 genotype of the hepatitis C virus was identified more frequently (91 patients, 52.6%). CHC prevailed in male patients (group 1 — 64.3%, group 2 — 71.1%) at the most working age from 20 to 30 years (group 1 — 68.8%, group 2 — 80%).
Results: among the patients admitted to the hospital, 55.5% had a mixed form of hepatitis (CHC + toxic hepatitis) and 17.2% had cirrhosis of the liver. In 22.6% of patients, antiviral therapy was canceled due to the development of adverse events or non-
response to therapy. A significant number of patients before admission to the hospital abused alcohol (54.7%), drugs (25.8%), had chronic diseases: pancreatitis, bronchitis.
Conclusion: patients with mixed hepatitis (CHC + toxic hepatitis) prevail among patients with CHC and HIV infection admitted to hospital. Most patients do not receive standard antiviral therapy for CHC due to pronounced immunodeficiency, alcohol abuse, psychotropic substances intake, or refusal of treatment.
Key words: HIV infection, chronic hepatitis C, liver cirrhosis, antiviral therapy, antiretroviral therapy, interferon alfa-2a, ribavirin, genotype, opportunistic infections.
For citation: Sundukov A.V., Melnikov L.V., Evdokimov E.Yu. Characteristics of patients with chronic hepatitis C and HIV infection // RMJ. Medical Review. 2018. № 7(II). P. 64–67.
В статье приведены характеристика больных хроническим гепатитом С и ВИЧ-инфекцией с целью определения клинических и лабораторных особенностей больных с данными заболеваниями.
Введение
Актуальность проблемы вируса иммунодефицита человека (ВИЧ) и хронического гепатита С (ХГС) определяется широким распространением этих инфекций, многообразием клинических форм, значительной частотой неблагоприятных исходов вследствие развития цирроза и/или первичного рака печени, а также общностью эпидемиологических, социальных и экономических факторов. Эпидемиологическая ситуация в России по ВИЧ и ХГС остается сложной, и в последнее время отмечается увеличение смешанной инфекции (ВИЧ/ХГС). Из 42 млн ныне живущих ВИЧ-инфицированных людей примерно у 20% (8,4 млн) диагностирован ХГС [1–3]. Как правило, у данной категории пациентов в анамнезе отмечают случаи внутривенного введения наркотиков [4].
В настоящее время более 80% всех случаев ВИЧ-инфекции приходится на потребителей инъекционных наркотиков, и в этой группе маркеры вирусного гепатита С определяются более чем у 90% больных [4–7]. Наличие ХГС и ВИЧ-инфекции одновременно ассоциируется с более высоким титром вируса гепатита С, выраженным прогрессированием хронического гепатита и возрастающим риском цирроза печени. При этом цирроз печени развивается быстрее и в 3 раза чаще у ВИЧ-инфицированных, чем у больных моноинфекцией гепатита С [4, 7, 8].
Цель настоящего исследования: выявить клинические и лабораторные особенности больных ХГС и ВИЧ-инфекцией.
Материал и методы
Работа выполнялась с 2013 по 2017 г. на базе инфекционной клинической больницы (ИКБ) № 2 Москвы и Московского городского центра по борьбе с ВИЧ/СПИД.
Всего под нашим наблюдением находилось 173 пациента с ХГС и ВИЧ-инфекцией. При постановке диагноза использовались эпидемиологические, клинические, биохимические, инструментальные методы исследования. Этиологический диагноз основывался на определении специфических серологических маркеров вирусных гепатитов и результатах молекулярно-биологических исследований с определением генотипа вируса гепатита С в лаборатории ИКБ № 2.
Стадия ВИЧ-инфекции определялась по Российской классификации ВИЧ-инфекции (В.И. Покровский, 2001 г.) [4].
В зависимости от схемы лечения все больные были разделены на 2 группы. Группа 1 включала 128 (74%) больных, которые получали только патогенетическую дезинтоксикационную терапию: раствор 5% глюкозы, солевые растворы, витамины (аскорбиновая кислота, витамины группы В), абсорбенты, гепатопротекторы. Из них 29 (22,6%) человек получали антиретровирусную терапию (АРТ): ламивудин, зидовудин, ставудин, абакавир, эфавиренз и др. Среди не получающих АРТ были пациенты, которым по иммунологическим характеристикам было показано лечение против ВИЧ-инфекции. Однако на фоне злоупотребления алкоголем у этих пациентов отмечалось обострение ХГС, в связи с чем АРТ не назначалась.
Группа 2 состояла из 45 (26%) человек — 32 (71,1%) мужчин и 13 (28,9%) женщин. Они получали стандартную противовирусную терапию (пегилированный интерферон альфа-2а + рибавирин). Пегилированный интерферон альфа-2а назначался в дозе 180 мг 1 р./нед. подкожно, рибавирин — по 800–1200 мг/кг в зависимости от массы тела. Длительность терапии составила 48 нед. Лечение в группе 2 проводилось амбулаторно, назначение АРТ не требовалось.
Статистическую обработку данных проводили с использованием MS Excel 2003 и подсчетом критерия Стьюдента (t).
Результаты исследования
Распределение пациентов в группах в зависимости от генотипа вируса гепатита С представлено на рисунках 1 и 2. Распределение по генотипам ХГС было сопоставимо, при этом генотип 1 встречался наиболее часто: у 67 (52,3%) больных в группе 1 и у 22 (48,9%) — в группе 2. У остальных пациентов в группе 1 генотип 2 встречался у 28 (21,9%) человек, генотип 3 — у 33 (25,8%); в группе 2 — соответственно у 9 и 14 (20,0 и 31,1%).
Большинство больных имели III (бессимптомную) или IVА стадию ВИЧ-инфекции (табл. 1): в группе 1 таких было 95 (74,2%) человек, в группе 2 — 45 (100%). В группе 2 не было больных с поздними стадиями ВИЧ-инфекции, т. к. это является абсолютным противопоказанием для назначения этиотропной терапии ХГС (интерферон + рибавирин).
Смешанную форму гепатита (ХГС + токсический гепатит) диагностировали у 71 (55,5 %) пациента. Хронический гепатит с исходом в цирроз печени отмечался в 22 случаях (17,2 %). Данные представлены на рисунке 3.
Распределение больных в зависимости от пола и возраста представлено в таблице 2.
Чаще ХГС встречался у пациентов мужского пола (в группе 1 — 64,3%, в группе 2 — 71,1%) и в наиболее трудоспособном возрасте от 20 до 30 лет (в группе 1 — 68,8%, в группе 2 — 80%).
Распределение пациентов в зависимости от сопутствующей патологии и оппортунистических инфекций представлено в таблице 3.
Как видно из представленных данных, сопутствующие заболевания встречались в обеих группах, однако, учитывая, что пациенты группы 2 лечились амбулаторно и к врачу обращались в плановом порядке, частота встречаемости сопутствующей патологии у данной группы больных была достоверно ниже. Анализ больных показал, что в группе 1 наиболее часто встречались такие заболевания, как обострение хронического панкреатита (31,3%), обострение хронического бронхита (27,3%), пневмония (19,5%). Выявлена высокая частота наркомании в обеих группах (25,8% и 13,3% соответственно). Часть больных в группе 1 не получала стандартную (этиотропную) терапию ХГС вследствие ряда объективных и субъективных факторов, которые приведены в таблице 4.
Из представленных данных видно, что чаще всего стандартная терапия не назначалась из-за злоупотребления алкоголем и/или приема психоактивных веществ, а также вследствие выраженного иммунодефицита (СД4+ лимфоциты менее 350 клеток). Также большую группу составили пациенты, которым стандартная терапия назначалась, но была отменена в результате развития побочных эффектов (16,4%) и/или неэффективности лечения (6,2%).
В качестве иллюстрации отказа от противовирусной терапии ХГС приводим собственное наблюдение.
Клинический пример
Выводы
Таким образом, в результате анализа клинических и лабораторных данных больных ХГС и ВИЧ-инфекцией можно сделать следующие выводы:
среди пациентов с ХГС и ВИЧ-инфекцией, поступающих в стационар, преобладают больные со смешанной формой гепатита (ХГС + токсический гепатит);
среди токсических причин поражения печени в абсолютном большинстве случаев отмечено злоупотребление алкоголем;
большинство пациентов имеют генотип 1 вируса гепатита С;
основные причины неназначения противовирусной терапии гепатита С: злоупотребление алкоголем, наркомания, низкий иммунный статус и отказ пациента от лечения.
П римерно у 70% больных СПИДом на различных этапах заболевания возникают поражения кожи и слизистых оболочек. В статье обсуждаются некоторые кожные заболевания у взрослых пациентов, страдающих СПИДом, и рассматривается патогенез поражения кожи при иммунодефиците.
Оказалось, что мишенью вируса при инфекции ВИЧ-1 являются не только Т-хелперы, но и антигенпрезентирующие клетки Лангерганса. Поражение этих клеток - критический момент в развитии иммунодефицита. Более того, было показано, что контакт между зараженными ВИЧ клетками Лангерганса и Т-лимфоцитами в процессе презентации антигена вызывает массивную репликацию вируса СПИДа. Следующая за этим гибель Т-лимфоцитов приводит к их прогрессирующей элиминации из кожи и лимфатических узлов. Для оценки выраженности этого процесса используются кожные тесты с различными антигенами. Выяснилось, что независимо от числа Т-хелперов у пациентов с отрицательными результатами кожных проб СПИД прогрессирует быстрее и протекает тяжелее, чем у больных, которые реагируют на какие-либо антигены.
Полагают, что именно поражение иммунной системы кожи лежит в основе большого числа инфекционных и неинфекционных кожных заболеваний при СПИДе.
Первичные кожные проявления при инфекции ВИЧ-1
Острый период СПИДа примерно в 75% случаев может характеризоваться следующими кожными проявлениями: эритематозными высыпаниями на туловище, кореподобной сыпью на верхней части туловища и лице, а также сыпью на ладонях и подошвах, напоминающей вторичный сифилис. Встречаются также энантема, эрозии, изъязвления и кандидоз слизистых полости рта, глотки, пищевода и гениталий.
Вторичные кожные проявления при инфекции ВИЧ-1
Вирус простого герпеса вызывает образование болезненных незаживающих язв на границе между кожей и слизистыми оболочками, чаще всего вокруг рта и в перианальной области. Показана системная противовирусная терапия.
Опоясывающий герпес отмечается у 8 - 13% больных СПИДом. Эта патология, однако, не является признаком глубокого иммунодефицита, так как может возникать на любой стадии заболевания. Клинические проявления варьируют от незначительных везикулярных высыпаний до тяжелых геморрагических и некротических поражений.
Контагиозный моллюск. Заболевание встречается примерно у 20% больных и ассоциировано с выраженным иммунодефицитом. Характерные поражения локализуются на лице и гениталиях, их размер может достигать 1 см. Дифференциальный диагноз с целым рядом грибковых поражений (Cryptococcus neoformans, Histoplasma capsulatum, Penicillium marneffei) очень сложен. Для подтверждения диагноза показано проведение морфологического исследования.
Человеческий папилломавирус (HPV) у ВИЧ-1-инфицированных пациентов вызывает поражения нетипичной локализации, которые редко бывают тяжелыми. Как у женщин, так и у мужчин HPV-ассоциированные поражения гениталий коррелируют со степенью иммуносупрессии.
Частота заболеваний, вызванных золотистым стафилококком, по мере прогрессирования иммунодефицита возрастает. Системные проявления, связанные с этим микроорганизмом, выявляются на аутопсии у половины больных СПИДом. Помимо поражений, типичных для золотистого стафилококка (фолликулит, импетиго, абсцессы), встречаются также пиомиозит и ботриомикоз.
Типичными для больных СПИДом являются поражения кожи, вызванные микобактерией туберкулеза, - язвы, подкожные абсцессы и др. Биопсия пораженных участков кожи с целью морфологического обнаружения микобактерий позволяет поставить диагноз.
Сифилис у больных СПИДом не только быстрее прогрессирует, но и значительно хуже поддается лечению. Поражения кожи при этом часто распространенные и атипичные.
Бактериальный ангиоматоз вызывается риккетсиеподобным микроорганизмом Rochalimaea henselae. Поражения кожи при этом могут напоминать саркому Капоши, пиогенную гранулему или ангиомы. В половине случаев поражаются также внутренние органы. Данное заболевание может изредка встречаться и у иммунокомпетентных лиц.
Типичными для больных СПИДом являются следующие грибковые поражения:
- - оральные и вульвовагинальные кандидозы;
- - дерматофития;
- - криптококкоз; - кокцидиомикоз;
- - гистоплазмоз;
- -заболевание, вызванное P. marneffei.
В большинстве случаев для постановки диагноза используется морфологическое исследование.
Себорейным дерматитом страдают 20 - 40% ВИЧ-инфицированных и 40 - 80% пациентов, страдающих СПИДом. В качестве этиологического агента рассматривается дрожжеподобный гриб Pityrosporum orbiculare, но это лишь предположение, в пользу которого свидетельствует эффективность противогрибковых препаратов.
ВИЧ-инфицированность может влиять на тяжесть течения псориаза, но не на частоту его возникновения.
Зуд у данного контингента больных может быть обусловлен различными причинами: фолликулитом, вызванным микроорганизмами, повышенной чувствительностью к укусам насекомых, чесоткой, ВИЧ-ассоциированной ксеродермией, ВИЧ-ассоциированным эозинофильным фолликулитом (состояние, возникающее у пациентов с числом Т-хелперов менее 300/мкл).
Реакции на лекарственные препараты (амоксициллин, сульфаниламиды, котримоксазол) встречаются среди ВИЧ-инфицированных значительно чаще, чем в общем населении. При этом распространены тяжелые поражения кожи (буллезные высыпания, эпидермальный некролиз). У 40% пациентов, принимающих зидовудин, отмечаются продольные пигментированные полосы на ногтях.
Поражения кожи могут отмечаться при различных опухолях. У больных СПИДом наиболее распространены саркома Капоши и базально-клеточная карцинома. Показана связь возникновения этих поражений с иммуносупрессией.
Tschachler E, Bergstresser PR, Stingl G. HIV-related skin diseases. Lancet 1996;348:659-63.
ВИЧ-ИНФЕКЦИЯ И НОВООБРАЗОВАНИЯ
Е. Нурмухаметова
E. Nurmuckhametova
И звестно, что у ВИЧ-инфицированных пациентов возрастает частота возникновения определенных типов опухолей (в частности, саркомы Капоши, неходжкинских лимфом и др.), причем опухоль может быть первым проявлением заболевания у человека, не подозревавшего прежде о наличии у него ВИЧ-инфекции. Некоторые опухоли, часто встречающиеся у ВИЧ-инфициованных, имеют вирусную этиологию (например, саркома Капоши), другие - нет. Роль состояния иммунодефицита у этих пациентов и непосредственное участие ВИЧ в развитии тех или иных опухолей еще предстоит изучить.
Саркома Капоши
В западных странах саркома Капоши среди ВИЧ-инфицированных встречается в 2000 раз чаще, чем в общем населении. Так, в США и Европе эта опухоль выявляется у каждого 5-го мужчины-гомосексуалиста, страдающего СПИДом. Однако существование ВИЧ-негативной саркомы Капоши (например, саркома, распространенная в Африке среди иммунокомпрометированных пациентов, подвергнутых трансплантации почки) говорит о наличии иного этиологического агента, возможно, вируса, необходимого для развития опухоли. Таким агентом может служить вирус герпеса (HHV8). Этот вирус был обнаружен в подавляющем большинстве случаев сарком Капоши как у ВИЧ-положительных, так и у ВИЧ-отрицательных пациентов. HHV8 филогенетически наиболее близок к herpesvirus saimiri, вызывающему выраженную лимфопролиферацию у обезьян Нового Света, и к известному онковирусу человека - вирусу Эпштейна - Барр.
Очевидно, что в возникновении саркомы Капоши состояние иммунодефицита играет решающую роль. Кроме того, в настоящее время дискутируется роль tat-протеина ВИЧ в развитии этой опухоли.
Для лечения саркомы Капоши в настоящее время используются:
- • радиотерапия;
- • подкожные введения a(alfa)-интерферона;
- • цитостатики (винкристин, блеомицин, антрациклин).
В настоящее время изучается эффективность еще целого ряда препаратов (человеческий хорионгонадотропин, фоскарнет, ретиноиды).
Неходжкинские лимфомы
У 3 - 10% больных СПИДом на различных стадиях возникают неходжкинские лимфомы (НХЛ). СПИД-ассоциированные НХЛ отличаются от НХЛ у иммунокомпетентных пациентов: часто отмечаются вовлечение экстранодальных областей и первичное поражение центральной нервной системы (ЦНС). Около 60% лимфом являются крупноклеточными, 30% - беркиттоподобными; оставшиеся относятся к Т-клеточным или ни В, ни Т-клеточным.
Крупноклеточные лимфомы
Важно, что практически во всех случаях при лимфомах у пациентов, перенесших трансплантацию, выявляется вирус Эпштейна - Барр. При СПИД-ассоциированных крупноклеточных лимфомах частота его выявления составляет лишь 50%. Вероятно участие каких-то других факторов в развитии этих опухолей (например, HHV8, или расширение популяции В-лимфоцитов в результате синтеза лимфокинов ВИЧ-инфицированными клетками и т.д.). Частота СПИД-ассоциированных крупноклеточных лимфом увеличивается с возрастом.
Беркиттоподобные лимфомы
Частота этих опухолей повышена у ВИЧ-положительных пациентов, но не среди иммуносупрессированных больных, перенесших трансплантацию. Следовательно, иммуносупрессия как таковая не является достаточным условием для развития беркиттоподобной лимфомы. Лишь в 40% случаев при СПИД-ассоциированных лимфомах этого типа обнаруживается вирус Эпштейна - Барр. У 75% пациентов выявляется генная транслокация c-myc/Ig. Пик беркиттоподобных лимфом, как спорадических, так и СПИД-ассоциированных, отмечается в возрасте от 10 до 19 лет.
Другие лимфопролиферативные заболевания
К ним относятся:
- • первичные лимфомы ЦНС (до 42% всех СПИД-ассоциированных лимфом; в большинстве случаев определяется вирус Эпштейна - Барр);
- • болезнь Ходжкина;
- • болезнь Кастлемена (при этом выделяется HHV8);
- • Т-клеточные и смешанные лимфомы.
Терапевтическая тактика
При диссеминированном поражении методом выбора является терапия цитостатиками. Полной ремиссии удается достичь в 50% случаев, однако у большинства больных развивается рецидив. Медианная выживаемость составляет 5 - 8 мес.
Чешуйчатоклеточная карцинома
Наличие ВИЧ-инфекции способствует увеличению распространенности и тяжести течения анальной карциномы среди гомосексуалистов. В этом же контингенте отмечена большая частота выявления папилломавирусов 16 и 18, особенно при низком содержании клеток CD4. Вероятно, подавление иммунитета при СПИДе способствует активной репликации папилломавирусов, что приводит к интраэпителиальной дисплазии. Инвазивный рак при этом не возникает. Аналогичные данные были получены в отношении рака шейки матки у женщин.
Другие опухоли
По данным различных исследователей, существует определенная связь между ВИЧ-инфекцией и раком яичек (тератокарцинома и семинома), злокачественной меланомой, лейомиосаркомой у детей, немелкоклеточным раком легких и миеломой.
Schuiz TF, Boshoff CH, Weiss RA. HIV infection and neoplasia. Lancet 1996;348:587-91.
ИНФЕКЦИЯ HELICOBACTER PYLORI И ЖЕЛУДОЧНО-КИШЕЧНАЯ ЛИМФОМА
С уществует группа лимфом, имеющих сходную клиническую и патологическую картину, их обнаружение связано с именами Исааксона и Райта. Чаще всего поражена слизистая желудка, но могут быть затронуты и другие лимфоидные ткани, связанные со слизистой (ЛТСС). В-клетки желудочных лимфом могут быть сильно или слабо малигнизированы. Недавние исследования показали, что ранние поражения ЛТСС желудка могут быть вылечены путем ликвидации инфекции Helicobacter pylori и что адекватная антибиотикотерапия может способствовать быстрому и эффективному уменьшению поврежденных участков. W. Fischbach (Германия) предлагает следующую схему профилактики легких степеней поражения ЛТСС желудка (соответствующих стадии лимфомы ЕI) при подтвержденной инфекции H. рylori:
1) ликвидация инфекции H. рylori посредством тройной терапии (омепразол 20 мг 2 раза в день, амоксициллин 1000 мг 2 раза в день, кларитромицин 500 мг 2 раза в день в течение 7 дней);
2) контрольная эндоскопия с биопсией спустя 4 нед:
- а) в случае ликвидации инфекции H. рylori и исчезновения поражения ЛТСС требуется проведение контрольных обследований 1 раз в 2 мес в течение по меньшей мере полугода;
- б) инфекция H. рylori не ликвидирована: альтернативная антибиотикотерапия;
- в) проба на H. рylori отрицательная, но ЛТСС в прежнем состоянии: дальнейшее эндоскопическое обследование 1 раз в 2 мес;
3) в случае невыздоровления или осложнения необходимы хирургическое вмешательство, лучевая терапия или химиотерапия в соответствии со стадией заболевания и результатами гистологических анализов.
Вывод. В случае легкой формы желудочной лимфомы стадии EI (поражение ЛТСС) ликвидация инфекции H. рylori является перспективным методом лечения, которое должно проводиться в рамках клинического исследования.
Fischbach W. Helicobacter pylori infection and gastrointestinales Lymphom. Schweiz Med Wochenschr 1996;126:826-9.
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
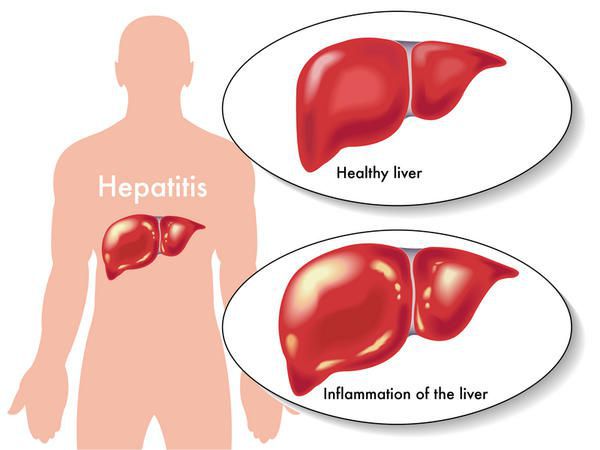
Этиология
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
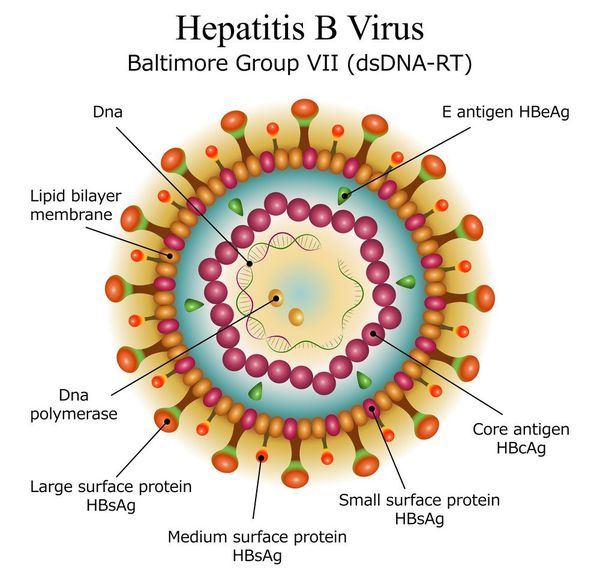
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
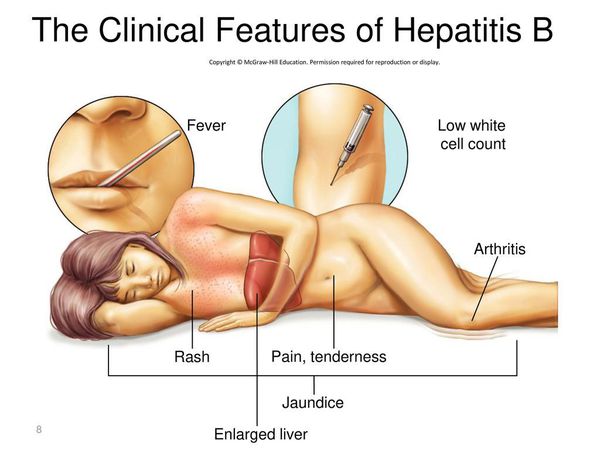
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
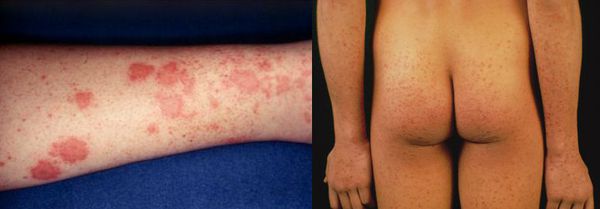
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
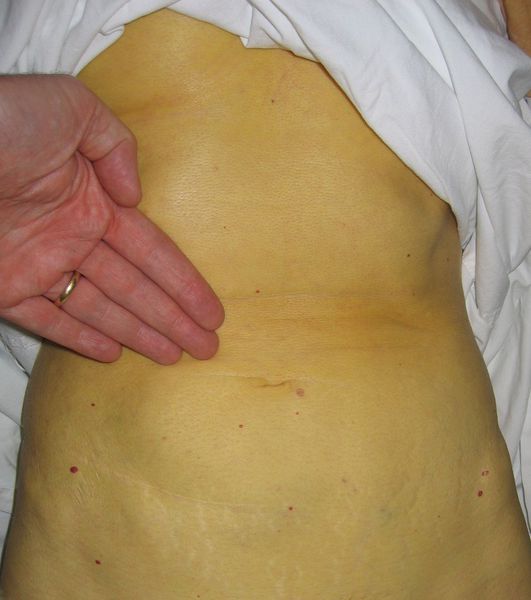
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
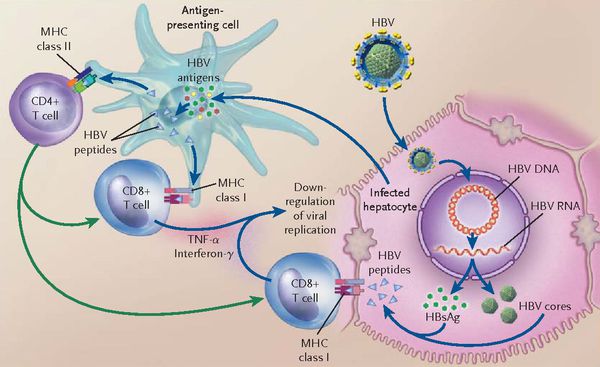
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Читайте также:

