Кровотечение у вич инфицированных
Обновлено: 25.04.2024
Категории МКБ: Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других состояний (B23), Болезнь, вызванная вирусом иммунодефицита человека [вич], неуточненная (B24), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде других уточненных болезней (B22), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде злокачественных новообразований (B21), Болезнь, вызванная вирусом иммунодефицита человека [вич], проявляющаяся в виде инфекционных и паразитарных болезней (B20), Острый ВИЧ-инфекционный синдром (B23.0)
Общая информация
Краткое описание
ВИЧ-инфекция - инфекционная болезнь, развивающаяся в результате многолетнего персистирования в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (далее - ВИЧ), характеризующаяся медленно прогрессирующим дефектом иммунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (далее - СПИД) [1].
B20 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде инфекционных и паразитарных болезней;
B21 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде злокачественных новообразований;
B22 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других уточненных болезней;
Пользователи протокола: инфекционисты, терапевты, врачи общей практики, клинической лабораторной диагностики, фтизиатры.
Класс I - польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III - имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
Классификация
• нейтропения (
• хронический герпес (оролабиальный, генитальный или аноректальный длительностью более месяца или висцеральный любой локализации);
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
• число лимфоцитов CD4 (абсолютное и процентное содержание) - двукратное измерение с интервалом не менее 7 дней;
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: не проводится.
Заболевание начинается постепенно.
• половые контакты (гетеро- или гомосексуальные; тип контактов: оральный, вагинальный, анальный) с ВИЧ-статус партнерами (если известно);
• патологическое увеличение лимфатических узлов, персистирующая генерализованная лимфоаденопатия.
Ротоглотка: стоматит, язвенно-некротические поражения, разрастание слизистой полости рта, преимущественно боковой поверхности языка.
Мочеполовая система и перианальная область: признаки следующих заболеваний: нефропатия, инфекция, вызванная вирусом папилломы человека (остроконечные кондиломы половых органов и заднего прохода, рак шейки матки).
Неврологический и психический статус: нарушение когнитивных функций (Приложение 1), парезы, симптомы нейропатии, нарушение сознания, менингеальные синдром.
Биохимический анализ крови: повышение уровня креатинина и мочевины в крови, гипонатриемия, гипокалиемия (при развитии ОПП).
• полимеразная цепная реакция РНК ВИЧ: определяемая вирусная нагрузка.
МРТ/КТ головного мозга: отек головного мозга, признаки менингоэнцефалита, дисциркуляторная энцефалопатия, объемные процессы;
• консультация невропатолога: при признаках/подозрении на криптококковый менингит, ВИЧ-энфефалопатию, токсоплазмоз ЦНС, ПМЛ, лимфомы головного мозга, периферической полинейропатии;
• консультация психиатра: при признаках/подозрении психического расстройства. ВИЧ-энцефалопатии/деменции;
Дифференциальный диагноз
Дифференциальный диагноз: проводится с оппортунистическими инфекциями и другими вторичными заболеваниями по результатам консультаций специалистов.
Лечение
Курс лечения АРТ – пожизненный, применяется тройная схема, кратность приема АРВ препаратов зависит от формы выпуска.
• эмтрицитабин (FTC) 200 мг, капсула; 200 мг 1 раз в сутки.
• рилпивирин* (RPV) 25 мг таблетка; 25 мг 1 раз в сутки.
• дарунавир (DRV) 400 мг, 600 мг, 800 мг таблетка; 600 мг 2 раза в сутки в комбинации с ритонавиром в дозе 100 мг 2 раза в сутки;
• типранавир* (TPV) 250 мг капсула; применяется усиленный ритонавиром, 2 раза в сутки 500 мг+200 мг ритонавира.
ИИ с целью: блокирования фермента ВИЧ, участвующий во встраивании провирусной ДНК в геном клетки-мишени.
• долутегравир (DTG) 50 мг таблетка; 50 мг 1 раз в сутки.
• элвитегравир 150 мг/кобицистат 150 мг /эмтрицитабин 200 мг /тенофовир 300 мг* 1 таблетка 1 раз в сутки;
* При регистрации в Республике Казахстан.
В приоритетном порядке АРТ назначается всем пациентам в 3-4 стадии ВИЧ-инфекции или пациентам с количеством CD4+ лимфоцитов ≤ 350 кл/мкл.
− ВИЧ-позитивным лицам в дискордантных парах (для снижения риска трансмиссии ВИЧ неинфицированным партнерам), при условии предварительного консультирования обоих партнеров;
− при подготовке ВИЧ-инфицированного пациента к применению вспомогательных репродуктивных технологий.
Схема АРТ состоит не менее, чем из трех антиретровирусных препаратов. Предпочтение отдается комбинированным препаратам в фиксированных дозировках.
b NVP использовать у лиц с низким числом лимфоцитов CD4 (у женщин с СД4 менее 250/мкл, у мужчин с СД4 менее 400/мкл)
с вместо AZT при умеренной анемии или гранулоцитопении (уровень гемоглобина> 90 г/л или количество нейтрофилов> 1000 клеток/мкл) рекомендуется назначать ABC, или TDF, а при более выраженной анемии или гранулоцитопении – АВС или TDF.
d использование комбинированного препарата фиксированной дозировки DRV/c (при регистрации)
При невозможности использования вышеперечисленных препаратов ddI может быть назначен в качестве НИОТ в комбинации 3TC/FTC +EFV.
• пациенты, получающие противотуберкулезные препараты.
− при количестве CD4+ лимфоцитов от 50 до 250 клеток/мкл и нормальном уровне АЛТ или АСТ – NVP в сочетании с АВС, или TDF, или AZT + 3ТС, или FTC;
− при любом количестве CD4+ лимфоцитов – LPV/r или DRV/r или ATV/r в сочетании с АВС, или TDF, или AZT + 3ТС, или FTC.
Рекомендуемые схемы АРТ: назначается схема из предпочтительных АРВП – 2 НИОТ + 1 ИП/r, или 2НИОТ + 1 ННИОТ, или 2 НИОТ + 1 ИИ.
LPV/r в сочетании с AZT/3TC. В качестве третьего компонента схемы АРТ являются LPV/r в таблетках (400/100 мг 2 раза в сутки).
При непереносимости LPV/r можно использовать (в порядке приоритетности) – DRV/r (600/100 мг 2 раза в сутки), NVP (при CD4 < 250 клеток/мкл и нормальном уровне АЛТ и АСТ). Частота назначения LPV/r и DRV/r – не реже 2 раз в сутки.
При непереносимости LPV/r и DRV/r, можно назначить ATV/r или другие ИП/р. В качестве нуклеозидной основы рекомендуется ZDV/3TC. Применение EFV не рекомендуется в I триместрe беременности.
Для лечения пациентов с низким уровнем CD4+-лимфоцитов рекомендуется применять схемы, включающие бустированный ИП.
В качестве нуклеозидной основы рекомендуется применять комбинацию ABC с 3TC или TDF с 3TC в стандартных дозах (или комбинированный препарат TDF/FTC). Однако у пациентов с ВН более 100 000 копий/мл препараты, содержащие ABC, применять не рекомендуется.
В качестве альтернативы третьим препаратом можно назначить FPV/r из-за минимального влияния на функцию почек либо LPV/r.
ТDF не рекомендуется больным с почечной недостаточностью.
более чем в 2,5 раза выше верхней границы нормы (ВГН) – EFV или RPV (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ < 100000 копий/мл) в сочетании с TDF+3TC или TDF/FTC;
• при уровне активности АЛТ или АСТ более чем в 2,5 раза выше ВГН – DTG, бустированный RTV ИП (DRV/r или LPV/r) в сочетании с TDF+3TC или TDF/FTC.
При снижении числа CD4+ лимфоцитов менее 500 клеток/мкл рекомендуют начать АРТ одновременно с терапией ХГС.
При количестве CD4+лимфоцитов менее 350 клеток/мкл начинают лечение ВИЧ-инфекции, а затем присоединяют терапию ХГС.
Не рекомендуется сочетание рибавирина с зидовудином (увеличивается частота развития анемии), диданозином (повышается вероятность декомпенсации заболевания печени).
Оптимальным сочетанием НИОТ является TDF + 3TC или FTC в стандартных дозировках. При невозможности применять TDF назначают АВС.
• при нормальном уровне активности АЛТ/АСТ или повышении его не более чем в 2,5 раза выше ВГН – EFV, RPV (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ < 100000 копий/мл) или DTG (при наличии противопоказаний к приему EFV и при уровне РНК ВИЧ >100000 копий/мл) в сочетании с АВС или TDF + 3TC или TDF/FTC.
• при уровне активности АЛТ/АСТ более чем в 2,5 раза выше ВГН – DTG или бустированный ИП (LPV/r или DRV/r) в сочетании с АВС или TDF + 3TC или TDF/FTC.
У больных при сочетании ВИЧ-инфекции и ХГС, не получающих лечения ХГС, в состав схемы АРТ может быть включено сочетание ZDV+3TC.
Все ЛЖВ с диагностированным туберкулезом нуждаются в лечении ТБ и ВИЧ-инфекции, независимо от числа лимфоцитов CD4.
Первым начинают противотуберкулезное лечение, а затем как можно быстрее (в первые 8 недель лечения) назначают АРТ.
Больным ВИЧ/ТБ, имеющим выраженный иммунодефицит (число лимфоцитов CD4 менее 50 клеток/мкл), необходимо начать АРТ немедленно – в течение первых 2 недель после начала лечения ТБ.
При наличии туберкулезного менингита начало АРТ следует отложить до завершения фазы интенсивной терапии ТБ.
В начале АРТ у больных, получающих противотуберкулезное лечение, предпочтительным ННИОТ является EFV, который назначают вместе с двумя НИОТ.
При отсутствии EFV рекомендована схема лечения - 3TC (или FTC) + ZDV + ABC (или TDF).
В таблице 3 представлены варианты замены антиретровирусных препаратов при развитии нежелательныхэффектов.
Неудача лечения определяется как постоянно выявляемая вирусная нагрузка более 1000 копий/мл по результатам двух последовательных измерений, проведенных с интервалом в 2-4 недели, но не ранее, чем через шесть месяцев после начала использования АРВ-препаратов.
Основные лекарственные средства, имеющие 100% вероятность применения: см пункт Медикаментозное лечение, оказываемое на амбулаторном уровне.
• эмтрицитабин (FTC) 200 мг, капсула;
• рилпивирин* (RPV) 25 мг таблетка;
• дарунавир (DRV) 400 мг, 600 мг, 800 мг таблетка; 600 мг в комбинации с ритонавиром в дозе 100 мг 2 раза в сутки;
• типранавир* (TPV) 250 мг капсула; применяется усиленный ритонавиром, 2 раза в сутки 500 мг+200 мг ритонавира.
• элвитегравир 150 мг/кобицистат 150 мг /эмтрицитабин 200 мг /тенофовир 300 мг* 1 таблетка 1 раз в сутки;
• элвитегравир 150 мг/кобицистат 150 мг* 1 таблетка 1 раз в сутки.
Хирургические вмешательства: нет.
• туберкулеза (при исключении у пациента активного туберкулеза) –однократно изониазид (5 мг/кг), но не более 0,3 г в сутки + пиридоксин (при наличии) в дозе 25 мг/сут не менее 6 месяцев;
• пневмоцистной пневмонии в случае CD4 < 200 клеток/мкл, токсоплазмоза, в случае CD4 < 100 клеток/мкл – котримоксазол (960 мг 3 раза/неделю). Отменить профилактику если у пациента более 3 месяцев количество CD4+ - лимфоцитов стабильно превышает 200 кл/мкл, возобновить при падении количества CD4+ - лимфоцитов
• Диспансерное наблюдение пациентов получающих АРТ осуществляется совместно ПМСП и территориальным центром СПИД с кратностью посещений не менее 1 раза в 3 месяца.
• Вирусная нагрузка определяется перед началом АРТ. В дальнейшем следует измерять ВН первый раз не позднее 3 месяцев, затем 1 раз в 6 месяцев, при достижении неопределяемого уровня ВН.
• В случае отсутствия снижения ВН через 6 месяцев от начала лечения на 1 lоg10 или последовательного двукратного повышения ВН после исходной супрессии, следует провести генотипический тест на определение резистентности ВИЧ к антиретровирусным препаратам.
• Число лимфоцитов CD4 нужно измерять через 3 месяца, затем каждые 6 месяцев, при необходимости чаще в течение 1-го года АРТ, далее не реже 1 раз в год (за исключением случаев неэффективности лечения).
• Лабораторные исследования необходимо проводить не менее одного раза в 6 месяцев.
Таблица 4. Сроки проведения лабораторных исследований
х - лабораторное исследование показано независимо от используемых АРВ-препаратов;
x (АРВ-препарат) - исследование показано пациентам, которые получают указанный в скобках препарат.
b Пациентам с хроническими гепатитами биохимические показатели определяют согласно клиническому протоколу диагностики и лечения хронического вирусного гепатита В и С у взрослых в РК.
Через 3 месяца после начала приема АРВ-препарата клинически проявляющиеся побочные эффекты должны отсутствовать (а также субклинические, которые со временем могут проявиться клинически )
b Вирусная нагрузка уменьшается постепенно: у большинства пациентов (за исключением имеющих изначально высокую вирусную нагрузку) через 24 недели АРТ она должна быть < 50 копий/мл либо демонстрировать выраженную тенденцию снижения до этого уровня.
При расхождении между вирусологическими и иммунологическими показателями, приоритет за вирусологическими.
Число лимфоцитов CD4 необходимо определять каждые 3 месяца, по стабилизации СД4 лимфоцитов на фоне АРТ - 1 раз в 6 месяцев.
Цель АРТ - снижение ВН до неопределяемого уровня (пороговый уровень
При показателях ВН от 200 до 400 коп/мл – развитие резистентности возможно, необходимо усилить работу по соблюдению приверженности к АРТ.
Госпитализация
III степень (тяжелая) - повседневная жизнь существенно нарушена, часто требуется дополнительная помощь близких, медицинская помощь и лечение, возможно в стационаре;
IV степень (крайне тяжелая, жизнеугрожающая) - нормальная повседневная жизнь невозможна, требуется постоянная помощь посторонних, серьезное лечение, чаще всего в стационаре.
Информация
Источники и литература
Информация
5) Трумова Жанна Зиапеденовна – доктор медицинских наук, профессор РГП на ПХВ «Казахский национальный медицинский университет имени С.Д.
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Оценку нарушений познавательной деятельности (когнитивных функций) целесообразно проводить у всех ВИЧ-инфицированных пациентов без отягощающих факторов(тяжелые психиатрические заболевания, злоупотребление психоактивными веществами, в том числе алкоголем, текущие оппортунистические инфекции центральной нервной системы, другие неврологические заболевания) в течение 6 мес. со времени постановки диагноза. Данный подход позволяет точно определить исходные показатели и, соответственно, более точно оценить дальнейшие изменения. Для раннего скрининга когнитивных функций необходимо задать пациенту 3 вопроса (S.Simionietal. AIDS 2009, EACS 2012):
1. Часто ли у Вас бывают случаи потери памяти (например, Вы забываете значительные события, даже самые недавние, назначенные встречи и т.д.)?
Нейропсихологическое обследование должно включать в себя тесты для изучения следующих характеристик познавательной деятельности: слухоречевая и зрительная память, счет, скорость восприятия информации, внимание, , двигательные навыки. (Antinorietal.Neurology, 2007). В случае выявления патологии требуется обследование пациента у невролога, проведение МРТ головного мозга и исследовании спинномозговой жидкости (СМЖ) на вирусную нагрузку и, если есть к тому показания, провести исследование генотипической резистентности к препаратам в двойной пробе СМЖ и плазмы крови. Если у пациента выявлена патология нейрокогнитивных функций на этапе скрининга или при дальнейшем нейропсихологическом обследовании, необходимо рассмотреть возможность включения в схему препаратов, потенциально воздействующих на центральную нервную систему. К ним относятся либо те препараты, проникновение которых в СМЖ было продемонстрировано в исследованиях, проведенных у здоровых ВИЧ-инфицированных пациентов(концентрация выше IC90 у более чем 90% обследуемых пациентов), либо те, для которых доказана краткосрочная (3–6 мес.) эффективность воздействия на когнитивные функции или на снижение ВН на СМЖ, при условии, что оценка проводится в отсутствие каких-либо других совместно принимаемых препаратов или в рамках контролируемых исследований, результаты которых рецензируются экспертами (EACS 2012).
Инфекционная клиническая больница №2, Москва
Московский областной НИИ акушерства и гинекологии;
кафедра акушерства и гинекологии ФУВ МОНИКИ им. М.Ф. Владимирского
Кафедра акушерства, гинекологии, перинатологии и репродуктологии факультета последипломного профессионального обучения врачей Московской медицинской академии им. И.М. Сеченова;
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова
Инфекционная клиническая больница №2, Москва
Клинико-патогенетические особенности маточных кровотечений у ВИЧ-инфицированных больных
Журнал: Российский вестник акушера-гинеколога. 2014;14(1): 59‑62
Гафуров Ю.Т., Краснопольская К.В., Назаренко Т.А., Сундуков А.В. Клинико-патогенетические особенности маточных кровотечений у ВИЧ-инфицированных больных. Российский вестник акушера-гинеколога. 2014;14(1):59‑62.
Gafurov IuT, Krasnopol'skaia KV, Nazarenko TA, Sundukov AV. Clinical and pathogenetic features of uterine bleeding in HIV-infected patients. Russian Bulletin of Obstetrician-Gynecologist. 2014;14(1):59‑62. (In Russ.).
Инфекционная клиническая больница №2, Москва
Проанализированы клинико-лабораторные особенности маточных кровотечений у 220 ВИЧ-инфицированных больных, госпитализированных в Инфекционную клиническую больницу №2 Москвы в неотложном порядке. Большинство пациенток были молодыми женщинами в возрасте от 21 года до 30 лет, имеющими 3-ю (субклиническую) стадию заболевания. Показано, что у 80% пациенток отсутствовали органические изменения эндо- и миометрия, а также гормональные нарушения, вызывающие ановуляцию и дисфункцию яичников. Среди этих больных у 74,4% выявлена тромбоцитопения или гипофункция плазменного звена свертывающей системы крови, что позволило сделать вывод о коагулопатическом генезе дисфункциональных маточных кровотечений у ВИЧ-инфицированных больных. Показано, что традиционное лечение не дает стойкого терапевтического эффекта, использование в комплексном лечении антиретровирусной терапии (АРТ) привело к компенсации состояния у 92,9% больных. Необходимость использования АРТ в комплексном лечении ВИЧ-инфицированных больных с дисфункциональными маточными кровотечениями подтверждают результаты их обследования в процессе лечения: значительный подъем уровня тромбоцитов, снижение вирусной нагрузки, восстановление уровня СD4+.
Инфекционная клиническая больница №2, Москва
Московский областной НИИ акушерства и гинекологии;
кафедра акушерства и гинекологии ФУВ МОНИКИ им. М.Ф. Владимирского
Кафедра акушерства, гинекологии, перинатологии и репродуктологии факультета последипломного профессионального обучения врачей Московской медицинской академии им. И.М. Сеченова;
Научный центр акушерства, гинекологии и перинатологии им. акад. В.И. Кулакова
Инфекционная клиническая больница №2, Москва
Инфекция, вызываемая вирусом иммунодефицита человека - ВИЧ-инфекция, в финале которой развивается синдром приобретенного иммунного дефицита (СПИД), является одним из опаснейших инфекционных заболеваний, которое унесло жизни более 30 млн человек [1]. ВИЧ-инфекция распространена повсеместно, и число ВИЧ-инфицированных больных неуклонно растет как в России, так и за рубежом.
Маточные кровотечения - частая причина неотложной госпитализации ВИЧ-инфицированных больных на гинекологические койки хирургического отделения ИКБ №2. В ряде работ высказано предположение, что причиной кровотечений может быть тромбоцитопения, которая часто выявляется у больных, инфицированных ВИЧ [4]. Впервые тромбоцитопения у больного, пораженного ВИЧ-инфекцией, была описана в 1983 г. По данным литературы [3], тромбоцитопения наблюдается примерно у 10-50% пациентов с ВИЧ-инфекцией.
Многочисленные механизмы, такие как иммуноопосредованное уничтожение тромбоцитов, усиленное уничтожение тромбоцитов в селезенке и снижение выработки тромбоцитов, могут способствовать развитию хронической тромбоцитопении [4]. Среди механизмов возникновения тромбоцитопении, связанной с ВИЧ-инфекцией, можно выделить ускоренное уничтожение тромбоцитов в результате действий иммунных комплексов, а также присутствие антитромбоцитарных и анти-ВИЧ-антител, которые вступают в перекрестную реакцию с тромбоцитарной мембраной [7].
При попытке связать степень тромбоцитопении с показателями иммунитета больных оказалось, что уровень клеток CD4+ не коррелирует с наличием тромбоцитопении, а вирусная нагрузка при развитии тромбоцитопении часто оказывается повышенной [4, 9].
Нам встретились различные мнения на этот счет. Некоторые специалисты считают, что гематологические нарушения служат общим проявлением развернутой стадии ВИЧ-инфекции, другие утверждают, что изменения свертывающей системы крови ассоциируются с прогрессированием заболевания [5, 6].
Клинический опыт показывает, что традиционное лечение дисфункциональных маточных кровотечений у ВИЧ-инфицированных больных не дает стойкого терапевтического эффекта, тем не менее работы, анализирующие особенности течения дисфункциональных маточных кровотечений у данной категории больных, представлены единичными исследованиями. Есть указания на то, что антиретровирусная терапия (АРТ) способна восстановить уровень тромбоцитов до нормы [2]. Значимость проблемы и отсутствие эффективных терапевтических решений обусловили необходимость проведения настоящего исследования [3, 8].
Цель исследования - изучение клинико-патогенетических особенностей маточных кровотечений у ВИЧ-инфицированных больных.
Материал и методы
В исследование включили 220 ВИЧ-инфицированных больных, которые находились на обследовании и лечении в Инфекционной клинической больнице (ИКБ) №2 Москвы в период с 2006 г. по настоящее время. Диагноз ВИЧ-инфекции был установлен на основании иммунного блотинга. Все больные были госпитализированы в неотложном порядке в хирургическое отделение в связи с наличием умеренных или обильных кровянистых выделений из половых путей. Больные, у которых были выявлены скудные, мажущие выделения из половых путей, не угрожающие жизни пациенток, направлялись для обследования и лечения в терапевтические отделения для ВИЧ-инфицированных больных и в данное исследование не вошли. Обследование и лечение проведено согласно Московским городским стандартам. Наряду с обязательным минимумом обследования гинекологических больных исследовали уровни вирусной нагрузки и иммунного статуса. Кроме того, оценили состояние гормонального статуса больных с определением уровней тропных гормонов (ФСГ, ЛГ, Прл) и половых стероидов (Е2 и Р), проводили ультразвуковое исследование органов малого таза, при котором определяли размеры и структуру матки, наличие патологии эндометрия, размеры и структуру яичников. Всем женщинам произведена гистероскопия с оценкой состояния полости матки, толщины эндометрия, диагностическое выскабливание эндометрия с гистологическим исследованием соскоба. Больные консультированы гематологом для исключения патологии свертывающей системы крови, обусловленной иными, кроме ВИЧ-инфекции, причинами.
Результаты и обсуждение
При анализе возрастного состава обследуемых больных выявлено, что 114 (51,8%) из них находились в возрасте от 21 года до 30 лет, 77 (35%) - в возрасте 31-40 лет, 24 (10,9%) пациентки были старше 40 лет, а 5 (2,3%) - 20 лет и моложе. У 161 (73,2%) пациентки имелась 3-я (субклиническая) стадия ВИЧ-инфекции. У 59 больных диагностирована стадия вторичных заболеваний: 4А - у 37 (16,8%), 4Б, 4В - у 22 (10%). Следовательно, госпитализация в связи с маточными кровотечениями в большинстве случаев потребовалась пациенткам молодого возраста (от 21 года до 30 лет) с 3-й стадией заболевания.
Длительность заболевания ВИЧ-инфекцией до 3 лет установлена у 62 (28,2%), от 3 до 6 лет - у 45 (20,5%), от 7 до 10 лет - у 61 (27,7%), более 10 лет - у 52 (23,6 %) больных.
У 103 (46,8%) больных наряду с ВИЧ-инфекцией был выявлен хронический вирусный гепатит С.
Рост, масса тела, объем подкожной жировой клетчатки у обследованных пациенток не отличались от среднепопуляционных. У 198 (90%) больных в анамнезе отмечен регулярный менструальный цикл, а кровотечение у большинства из них (124 - 56,4%) совпадало с началом очередных менструаций.
Среди общего числа обследованных женщин 92 (41,8%) имели нарушение менструального цикла по типу периодических меноррагий, продолжительностью от нескольких месяцев до 1 года, при этом женщины, как правило, к врачу не обращались, занимаясь самолечением. Из числа обследованных 75 (34,1%) пациенток обратились за медицинской помощью, имея недлительный анамнез заболевания - от 1 нед до 1 мес. 53 (24,1%) больные были госпитализированы в сроки менее 7 дней от начала заболевания.
При обследовании в приемном покое больницы у 102 (46,4%) больных выявлена анемия различной степени тяжести: у 52 (23,6%) легкой степени, у 19 (8,6%) - средней степени тяжести, у 31 (14,1%) - тяжелая.
Для определения состояния эндометрия и выяснения причин маточных кровотечений проведены ультразвуковое исследование органов малого таза, гистероскопия, диагностическое выскабливание эндометрия с гистологическим исследованием соскоба.
Результаты проведенных исследований позволили обнаружить возможные причины кровотечения у 44 больных. Ими явились: полипы эндометрия, в том числе плацентарный после прерывания беременности - у 15 (6,8%), железистый (железисто-фиброзный) - у 16 (7,3%), миома матки с деформацией полости - у 5 (2,3%), гиперплазия эндометрия - у 6 (2,7%), аденомиоз - у 2 (0,9%).
У 4 из 5 больных, госпитализировавшихся по поводу маточных кровотечений, не было выявлено органических изменений, т.е. имелось дисфункциональное маточное кровотечение.
В результате проведенного исследования было установлено, что возраст большинства больных с дисфункциональными маточными кровотечениями (53,4%) и плацентарными полипами (80%) колебался от 21 года до 30 лет. Данная статистика объясняется тем, что и ВИЧ-инфекция, и осложнения, связанные с прерыванием беременности, свойственны пациенткам молодого возраста. Напротив, такие заболевания, как гиперпластические процессы в эндометрии, миома матки, аденомиоз, равно как и у ВИЧ-негативных, чаще всего свойственны пациенткам старше 40 лет.

Причины маточных кровотечений и стадии заболевания представлены в табл. 1.
Как видно из данных, представленных в табл. 1, за исключением больных с гиперплазией эндометрия, во всех нозологических единицах большинство госпитализированных имели 3-ю (субклиническую) стадию.
Уточнение влияния хронического вирусного гепатита С на возникновение маточных кровотечений у ВИЧ-инфицированных больных показало, что число больных, страдающих маточными кровотечениями, в группе с хроническим вирусным гепатитом С и без последнего значимо не различалось.

У 176 (80%) больных кровотечения органической природы отсутствовали. Более того, при анализе динамики гормональных показателей в лечении менструального цикла установлено, что у 51,1% пациенток диагностирована овуляция (Р на 21-23-й день менструального цикла составлял 21,2±3,4 нг/мл), а при гистологическом исследовании эндометрия была диагностирована фаза секреции. Результаты ультразвуковой диагностики и гистологического исследования соскоба эндометрия в данной группе больных представлены в табл. 2.
Как видно из табл. 2, результаты ультразвуковой диагностики и гистологического исследования не имеют каких-либо особенностей при сравнении с нормой. Следовательно, гормональные нарушения не являлись причиной возникновения кровотечения.
Отсутствие органических причин нарушения менструального цикла заставило нас исследовать состояние свертывающей системы крови у этих больных, так как имеющиеся в литературе сведения указывают на наличие тромбоцитопении при ВИЧ-инфекции, что может быть причиной коагулопатических кровотечений.
Мы проанализировали показатели свертывающей системы крови и выявили, что у 85 (48,3%) больных имелась тромбоцитопения (менее 100,0·10 9 /л), а у 46 (26,1%) - гипофункция плазменного звена свертывающей системы крови. Причем у 18 больных выявлено сочетание тромбоцитопении и гипофункции плазменного звена свертывающей системы крови. Таким образом, у большинства больных имелись нарушения в состоянии свертывающей системы крови.
Среди 85 больных с тромбоцитопенией, потребовавших помощи в связи с маточным кровотечением, у 48 была 3-я (субклиническая) стадия ВИЧ-инфекции, у 37 - стадия вторичных заболеваний: 4А - у 22 и 4 Б, В - у 15 пациенток. У 43 (50,6%) больных наряду с ВИЧ-инфекцией был выявлен вирус гепатита С. Средняя длительность течения заболевания от момента выявления ВИЧ-инфекции до развития тромбоцитопении составила 5,5±0,62 года.
Только у 4 пациенток тромбоцитопения возникла на фоне применения АРТ, остальным больным (n=81) АРТ не была назначена. Мы определили уровень снижения тромбоцитов и состояние иммунитета, на фоне которого развилась тромбоцитопения. Средний уровень тромбоцитов при поступлении в стационар в связи с маточным кровотечением составил 33,3±8,86·10 9 /л, средний уровень лимфоцитов СD4+ - 204,0±36,95 кл/мкл, средний уровень вирусной нагрузки - до 4,57±0,303 lg. Следовательно, выраженное снижение уровня тромбоцитов произошло на фоне угнетения иммунитета, проявлением которого стали низкий иммунный статус больных и высокая вирусная нагрузка.
Исходя из данных литературы и собственного клинического опыта, указывающего на недостаточную эффективность общепринятых методов лечения дисфункциональных маточных кровотечений (гемостатики, комбинированные пероральные контрацептивы), мы в схему лечения включили АРТ.
На фоне АРТ у большинства (79 - 92,9%) женщин отмечен значимый рост уровня тромбоцитов крови и, как следствие, прекращение маточных кровотечений. Так, средний уровень тромбоцитов при поступлении в стационар составил 33,3±8,86·10 9 /л, а на фоне АРТ в течение 3-24 мес поднялся до 185,8±15,65·10 9 /л.
Как правило, на фоне АРТ вначале происходит снижение вирусной нагрузки, рост количества клеток СD4+, а затем рост числа тромбоцитов крови. Так, среднее количество клеток СD4+ до начала АРТ составляло 204,0±36,95 кл/мкл, а к моменту подъема уровня тромбоцитов до нормы увеличивалось до 493,3±47,12 кл/мкл.
Средний уровень вирусной нагрузки до начала АРТ составлял 4,57±0,303 lg, а к моменту подъема уровня тромбоцитов до нормы составил 0,91±0,393 lg.

Показатели роста количества тромбоцитов в крови, иммунного статуса и уровня вирусной нагрузки на фоне АРТ представлены на рисунке. Рисунок 1. Показатели тромбоцитов крови, иммунного статуса и вирусной нагрузки у больных с тромбоцитопенией на фоне АРТ.
У 15 больных для достижения эффекта наряду с АРТ применяли иммуноглобулин человека нормальный в суммарной дозе 1 г на 1 кг массы тела. Препарат вводили в течение 3-5 дней ежедневно или с интервалом 1 день.
У 6 (7,1%) больных, несмотря на весь комплекс проводимых мероприятий, эффекта достичь не удалось. Средний уровень тромбоцитов до лечения составлял 75,0±13,11·10 9 /л, а на фоне терапии снизился до 51,88±9,84·10 9 /л. Среднее число клеток СD4+ у этих больных до начала терапии составляло 293,3±53,81 кл/мкл, средний уровень вирусной нагрузки 5,15±0,493 lg, и, несмотря на лечение, среднее число клеток СD4+ снизилось до 191,3±43,35 кл/мкл, средний уровень вирусной нагрузки - до 3,79±0,29 lg. Подобная неудача объяснялась различными причинами: продолжающееся употребление наркотических средств, прогрессирование ВИЧ-инфекции, резистентность к проводимой терапии.
В качестве примера зависимости уровня тромбоцитов от АРТ можно привести больную Е. 1984 года рождения. С 2001 г. состоит на учете в МГЦ СПИД с диагнозом ВИЧ в стадии IIБ. Хронический вирусный гепатит С. В 2006 г. на фоне тромбоцитопении 28·10 9 /л поступила в хирургическое боксированное отделение ИКБ №2 с маточным кровотечением. После купирования кровотечения выписана, обследована в МГЦ СПИД: СD4+ - 166 кл/мкл, вирусная нагрузка - 19 000 копий /мл. У больной установлена стадия ВИЧ-инфекции 4А, начата АРТ. На фоне терапии уровень СD4+ поднялся до 573 кл/мкл, вирусная нагрузка не определялась, число тромбоцитов достигло нормальных значений - 245·10 9 /л. В 2011 г. больная самостоятельно прекратила АРТ и с маточным кровотечением госпитализирована в ИКБ №2. При поступлении число тромбоцитов составляло 18·10 9 /л. В стационаре кровотечение было остановлено, возобновлена АРТ. Через 3 мес после возобновления АРТ число тромбоцитов увеличилось до 143·10 9 /л, число СD4+ составило 448 кл/мкл, вирусная нагрузка - 683 копий /мл, эпизоды кровотечения прекратились.
Данный пример наглядно демонстрирует положительную динамику на фоне лечения тромбоцитопении как осложнения ВИЧ-инфекции с помощью АРТ.
Выводы
1. Более 50% больных, обратившихся за стационарной гинекологической помощью по поводу маточных кровотечений, составили молодые женщины в возрасте от 21 года до 30 лет, у 3 из 4 (73,2%) больных имелась 3-я субклиническая стадия ВИЧ-инфекции. У 46,8% больных наряду с ВИЧ-инфекцией был выявлен хронический вирусный гепатит С.
2. Из 220 больных, поступивших в стационар с маточным кровотечением, у 176 (80%) отсутствовали какие-либо органические изменения, т.е. имело место дисфункциональное маточное кровотечение. При изучении причин кровотечения у данной категории больных значимо чаще выявляли патологию свертывающей системы крови, причем тромбоцитопению диагностировали у 48,3% больных, а у 26,1% была выявлена гипофункция плазменного звена свертывающей системы крови.
3. У 92,9% больных с дисфункциональными маточными кровотечениями на фоне тромбоцитопении комплексное лечение с применением АРТ привело к клиническому купированию эпизодов маточных кровотечений, сопровождавшемуся значимым подъемом количества тромбоцитов на фоне снижения вирусной нагрузки и восстановления уровня СD4+.
Носовые кровотечения у ВИЧ-инфицированных пациентов
Журнал: Российская ринология. 2021;29(4): 189‑193
Актуальность исследования причин, механизмов возникновения, диагностики и лечения носовых кровотечений (НК) у ВИЧ-инфицированных пациентов определяется сравнительно высокой встречаемостью (12% всей патологии уха и верхних дыхательных путей) и трудностью определения лечебной тактики.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Проведение анализа и выявление истинных причин рецидивирующих носовых кровотечений, имеющих диапедезный характер, у ВИЧ-инфицированных пациентов.
ПАЦИЕНТЫ И МЕТОДЫ
РЕЗУЛЬТАТЫ
По результатам анализа крови снижение тромбоцитов до 53,4±53,24 выявлено у 20 (80%) пациентов; снижение CD4 + -лимфоцитов 500 мкл – 1 — у 8 (32%); у 17 (68%) пациентов определялась вирусная нагрузка в среднем 683 180±362 899 копий в 1 мл плазмы. У всех пациентов были диагностированы ВИЧ-ассоциированные заболевания, наиболее частые из них — ВИЧ-ассоциированная иммунная тромбоцитопения (64%), анемия средней и тяжелой степени тяжести (16%), ЦМВ-инфекция (пневмония, эзофагит, колит) (28%), активная ЦМВ-инфекция с полиорганным поражением (28%), грибковое поражение носоглотки (12%). Пациентам проведена патогенетическая и симптоматическая терапия. Всем ранее не лечившимся больным назначена АРТ, а принимающим лечение выполнена его коррекция. Медикаментозное лечение привело к нормализации параклинических показателей и купированию носовых кровотечений.
ЗАКЛЮЧЕНИЕ
Рецидивирующие носовые кровотечения при ВИЧ-инфекции встречаются сравнительно часто и являются следствием ВИЧ-ассоциированных нарушений гемостаза, что необходимо учитывать при определении лечебной тактики. С другой стороны, больные с рецидивирующими носовыми кровотечениями требуют всестороннего обследования с целью уточнения возможных причин таких геморрагий, в том числе исключения ВИЧ-инфекции.
Дата принятия в печать:
Введение
Актуальность исследования причин и лечения носовых кровотечений (НК) у ВИЧ-инфицированных пациентов определяется широким распространением НК, трудностями, связанными с лечением и профилактикой рецидива НК у этой группы пациентов [1]. Как правило, НК удается купировать довольно быстро. Однако в некоторых случаях кровотечения упорно рецидивируют, сопровождаются значительной кровопотерей, представляя реальную угрозу для жизни больного [2].
НК является одной из причин обращения к оториноларингологу лиц, страдающих ВИЧ-инфекцией на всех стадиях развития заболевания: от острой до проградиентной. Удельный вес НК среди общего числа госпитализированных ЛОР-больных варьирует от 5,9 до 37% [3, 4]. По данным стационара инфекционного профиля, около 80% пациентов с ВИЧ-инфекцией имеют патологию ЛОР-органов [5], а 12% из них страдают рецидивирующими НК [6].
В большинстве случаев НК у больных ВИЧ-инфекцией обусловлены наличием ВИЧ-ассоциированного заболевания, в основе которого лежит нарушение кроветворной функции костного мозга в результате миелодисплазии [3] и поражения сосудов слизистой оболочки полости носа [4]. Лечение этой патологии основывается на коррекции гомеостаза, включающей антиретровирусную терапию (АРТ)/коррекцию АРТ и комбинацию глюкокортикоидов (при тяжелых формах), поливалентных иммуноглобулинов и/или препарата иммуноглобулин человека антирезус Rh0(D). При неэффективности консервативного лечения НК у пациентов с ВИЧ-инфекцией показана спленэктомия [7]. До выполнения спленэктомии рекомендуется провести вакцинацию против пневмококковой и менингококковой инфекций (H. influenzae и N. meningitidis), поскольку эти возбудители приводят к острому воспалительному процессу верхних дыхательных путей и жизнеугрожающим состояниям: менингиту, бактериальному эндокардиту, пневмонии [8].
В последнее время обсуждается возможность замены спленэктомии на терапию ритуксимабом, так как было установлено, что вероятность ответа на лечение этим препаратом (повышение уровня тромбоцитов выше 50 000 мкл –1 ) составляет >60% [7]. Заместительная терапия тромбоцитарной массой актуальна лишь в исключительных ситуациях, при угрожающих кровотечениях [9]. Корректировка витаминно-минерального комплекса в рационе питания также является важной составляющей в ведении таких больных [10].
Цель настоящего исследования — изучение механизма возникновения рецидивирующих НК у пациентов с ВИЧ-инфекцией и оценка консервативного лечения этой группы больных, включающего АРТ, иммуноглобулин человека нормальный (Human normal immunoglobuline).
Пациенты и методы
Результаты
Конкурирующие диагнозы у ВИЧ-инфицированных пациентов с рецидивирующим носовым кровотечением
ВИЧ-ассоциированная иммунная тромбоцитопения
Анемия средней и тяжелой степени тяжести
ЦМВ-инфекция (пневмония, эзофагит, колит)
Активная ЦМВ-инфекция с полиорганным поражением
Грибковое поражение носоглотки
Дефицит массы тела >10%
Генерализованный туберкулез в анамнезе
ОРДС (острый респираторный дистресс-синдром)
ОПН (острая почечная недостаточность)
Оментобурсит с разлитым серозным перитонитом
Анемия средней и тяжелой степени, выявленная у 4 пациентов, была связана с предшествующими эпизодами острой кровопотери и истощением эритроцитарного звена. По данным литературы, анемия встречается у 30—40% ВИЧ-инфицированных пациентов [7] и может развиться в результате повреждения ВИЧ-инфекцией энтероцитов и париетальных клеток желудка, что в свою очередь приводит к развитию синдрома мальабсорбции, которая проявляется снижением всасывания микроэлементов. Эрозирование и изъязвление слизистой оболочки желудочно-кишечного тракта приводят к образованию очагов хронических и/или острых кровопотерь, что требует консультации профильных специалистов [20, 21].
У 2 пациентов с саркомой Капоши определялись характерные изменения в виде очерченных синюшных пятен и эрозированных узлов на слизистой оболочке полости носа и носоглотки, а НК у них имело рецидивирующий характер. Наличие саркомы Капоши у этих больных было подтверждено результатами гистологического исследования биопсийного материала (наличие в препаратах щелевидных сосудов, экстравазированных эритроцитов и гиалиновых глобул).
Всем ранее не лечившимся больным была назначена АРТ, а у принимающих лечение пациентов выполнена его коррекция. При назначении АРТ учитывали показатели гемостаза, поскольку некоторые лекарственные препараты, например зидовудин, обладают миелосупрессией, что может дополнительно подавлять процесс гемопоэза [24].
По завершении комплексного лечения у больных ВИЧ-инфекцией с НК произошло увеличение количества тромбоцитов (в среднем до 130±92,04 ·10 12 /л).
Заключение
Таким образом, рецидивирующие НК при ВИЧ-инфекции встречаются сравнительно часто и являются следствием ВИЧ-ассоциированных нарушений гемостаза, что необходимо учитывать при определении лечебной тактики. С другой стороны, больные с рецидивирующими НК требуют всестороннего обследования с целью уточнения возможных причин таких геморрагий, в том числе исключения ВИЧ-инфекции.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Антитела к ВИЧ-1/2 и антиген ВИЧ-1/2 (HIV Ag/Ab Combo): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
ВИЧ-инфекция - инфекционная болезнь, развивающаяся в результате многолетнего персистирования (постоянного пребывания) в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (далее - ВИЧ), характеризующаяся медленно прогрессирующим дефектом иммунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (далее - СПИД).
ВИЧ (Вирус Иммунодефицита Человека) – вирус, относящийся к семейству ретровирусов (семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных), который поражает клетки иммунной системы человека. Через несколько недель с момента заражения начинают вырабатываться антитела к ВИЧ.
Показания на проведение исследования
Показаниями для назначения анализа является подготовка к госпитализации и плановому оперативному вмешательству. В профилактических целях следует провести исследование при подозрении на заражение при половом контакте. В первую очередь это касается лиц групп риска: употребляющих наркотики, вводимые внутривенно, часто меняющих половых партнеров и не использующих средств защиты.
Вирус иммунодефицита человека размножается в организме человека достаточно медленно, и количественный результат в отношении антигенов и антител к вирусу можно получить, как правило, не ранее чем через 3-6 недель после инфицирования. При этом клинические симптомы заболевания еще отсутствуют.
Через три месяца антигены ВИЧ и антитела к вирусу определяются практически у всех заболевших. Благодаря появлению новых комбинированных тест-систем четвертого поколения получение точного результата качественного анализа на ВИЧ-инфекцию возможно уже через две недели с момента попадания вируса в организм. При этом исследовании выявляют антиген р24 ВИЧ – белок вирусного капсида (внешней оболочки вируса).
Анализ на антитела к ВИЧ 1/2 и антиген ВИЧ 1/2 назначают на этапе планирования и при ведении беременности, когда возможна передача вируса плоду. Анализ проводят и после родов, поскольку ребенок ВИЧ-положительной матери может быть инфицирован во время прохождения через родовые пути и при кормлении грудью.

Лихорадка, потеря веса без объективных причин, повышенная утомляемость, увеличение регионарных лимфатических узлов, потливость, особенно в ночное время, длительный кашель, диарея – эти устойчивые клинические симптомы неясного происхождения, отмечаемые в течение 2-3 недель, также служат показанием к проведению исследования на антитела к ВИЧ 1/2 и антиген ВИЧ 1/2.
Кожные проявления также могут быть симптомом ВИЧ-инфекции, поскольку развиваются на фоне ослабления иммунитета. К их числу относится рецидивирующая герпетическая сыпь, поражающая обширные участки кожи, полость рта, половые органы. Герпес поражает и глубокие слои кожи с развитием язвенно-некротической формы. Образуются язвы и эрозии с последующим образованием рубцов, которых не бывает при обычном герпесе.
Еще один характерный симптом ВИЧ-инфекции – волосатая лейкоплакия, которая связана с активацией латентной инфекции, вызванной вирусом Эпштейна-Барр (что свидетельствует об иммуносупрессии). Заболевание проявляется нитевидными образованиями белого цвета с дальнейшим ороговением пораженных участков языка и слизистой оболочки рта.
Обширные грибковые поражения (в первую очередь дрожжевыми грибками рода Candida) также служат типичным признаком, сопровождающим ВИЧ-инфекцию. Сначала кандидоз поражает слизистую оболочку рта и пищевода, затем распространяется на слизистые желудочно-кишечного и мочеполового тракта. При этом формируются обширные очаги, характеризующиеся болезненностью и склонностью к изъязвлению.
ВИЧ-инфекция может сопровождаться развитием обширного папилломатоза. У ВИЧ-инфицированных женщин папилломы цервикального канала склонны быстро вызывать рак шейки матки.
СПИД-индикаторным заболеванием служит саркома Капоши – многоочаговая сосудистая опухоль, которая поражает кожные покровы и слизистые оболочки. Ее очаги в виде красноватых или буроватых узелков и бляшек сливаются, быстро распространяясь по всему телу. Со временем они образуют опухолевые поля, которые изъязвляются и нагнаиваются.
К числу патологических состояний, которые почти у всех пациентов сопровождают ВИЧ-инфекцию, относят полиаденопатию (увеличение лимфатических узлов). Как правило, в первую очередь увеличиваются под- и надключичные, подбородочные, околоушные и шейные лимфоузлы. В дальнейшем к ним может присоединяться увеличение паховых и бедренных лимфатических узлов. Они могут быть мягкими или плотными на ощупь, безболезненными и подвижными. Иногда несколько лимфоузлов сливаются, образуя своеобразный конгломерат. Воспаление двух и более групп лимфоузлов считают признаком генерализованной лимфаденопатии. Поражение лимфатических узлов может наблюдаться в течение нескольких лет, при этом периоды обострения сменяются ремиссией.
К легочным заболеваниям, сопровождающим ВИЧ-инфекцию, относят туберкулез и пневмонию.
Анализ на антигены и антитела к ВИЧ рекомендуют сделать, если у пациента выявлены заболевания, передаваемые половым путем (сифилис, хламидиоз, гонорея, генитальный герпес, бактериальный вагиноз).
19539 04 Сентября
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
ВИЧ: причины появления, симптомы, диагностика и способы лечения.
Определение
ВИЧ (вирус иммунодефицита человека) – инфекционное хроническое заболевание, передающееся контактным путем, медленно прогрессирующее и характеризующееся поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИДа). СПИД – это финальная стадия ВИЧ-инфекции, когда из-за ослабленной иммунной системы человек становится беззащитным перед любыми инфекциями и некоторыми видами рака. Опасность представляют так называемые оппортунистические инфекции – заболевания, вызываемые условно-патогенной или непатогенной флорой: вирусами, бактериями, грибами, которые у здоровых людей не приводят к серьезным последствиям или протекают легко и излечиваются самостоятельно. При СПИДе они наслаиваются друг на друга, имеют затяжное течение, плохо поддаются терапии и могут стать причиной летального исхода.
Причины появления ВИЧ
Источником инфекции является человек, инфицированный ВИЧ, на любых стадиях заболевания. Вирус передается через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь (незащищенный секс с инфицированным партнером) – доминирующий фактор распространения ВИЧ-инфекции.
Передача ВИЧ от матери ребенку может произойти на любом сроке беременности (через плаценту), во время родов (при прохождении через родовые пути) и грудного вскармливания (при наличии язвочек, трещин на сосках матери и во рту ребенка).
Высокий риск инфицирования существует при внутривенном введении наркотических веществ нестерильными шприцами, при переливании ВИЧ-инфицированной крови и ее препаратов, использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, опасность могут представлять органы и ткани доноров, используемые для трансплантации.

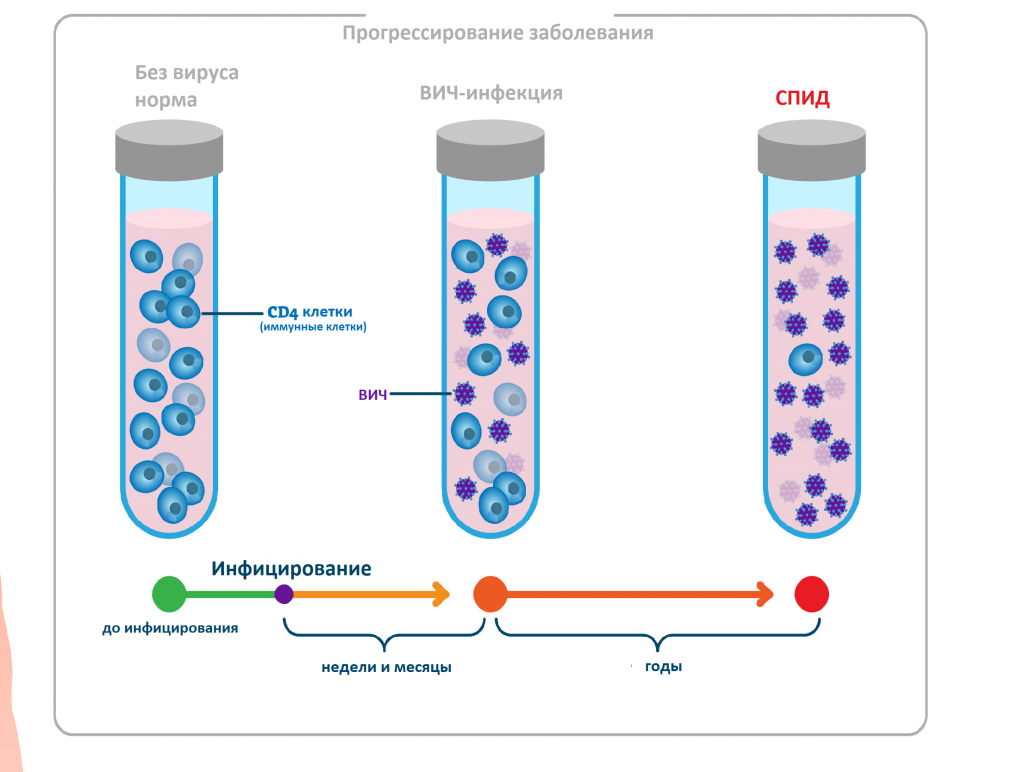
Попадая в кровоток, вирус проникает в Т-лимфоциты хелперы, или CD-4 клетки (рановидность лейкоцитов), которые помогают организму бороться с инфекциями. Т-хелперы имеют на поверхности так называемые CD4-рецепторы. ВИЧ связывается с этими рецепторами, проникает в клетку, размножается в ней и в конечном счете уничтожает ее. Со временем вирусная нагрузка увеличивается, а количество Т-хелперов снижается.
При отсутствии лечения через несколько лет из-за значительного снижения числа Т-хелперов появляются связанные со СПИДом состояния и симптомы.
Классификация заболевания
- Стадия инкубации - от момента заражения до появления реакции организма в виде клинических проявлений острой инфекции и/или выработки антител (специфических белков, продуцируемых в ответ на проникновение антигена, в данном случае – вируса).
- Стадия первичных проявлений клинических симптомов:
В дальнейшем продолжается активное размножение вируса и разрушение Т-лимфоцитов, развивается стадия вторичных изменений, для которой характерно прогрессирующее снижение веса, общая слабость, стойкое повышение температуры, озноб, выраженная потливость. Клинические проявления оппортунистических заболеваний обусловливают клиническую картину этой стадии: пациентов беспокоят кашель и одышка, тошнота, рвота, боли в животе, тяжелая диарея, кожные высыпания, сильные головные боли, снижение памяти и внимания и др.
Диагностика ВИЧ
Лабораторные методы исследования:
Скрининг (обследование здоровых людей) на ВИЧ должен быть проведен любому человеку, который считает, что может быть заражен, а также перед любой госпитализацией и операцией, всем беременным женщинам и их половым партнерам.
Обследование целесообразно проходить людям с высоким риском заражения ВИЧ, например, при наличии заболеваний, имеющих одинаковый с ВИЧ-инфекцией механизм передачи (вирусные гепатиты В и С, заболевания, передающиеся половым путем), лицам, имеющим регулярные незащищенные половые контакты, инъекционным наркоманам, детям, рожденным от матерей с ВИЧ-инфекцией, медицинским работникам, напрямую контактирующим с кровью на работе и др.
Существуют экспресс-тесты для скрининга ВИЧ, которые можно делать в домашних условиях. Для определения специфических антител/антигенов к ВИЧ (ВИЧ-1, 2, антиген p24) используют кровь, слюну или мочу. Точность любого экспресс-теста ниже, чем теста, проводимого в лаборатории.
Для стандартного скринингового обследования определяют антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) в крови с помощью иммуноферментного анализа (ИФА).
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 10 рабочих дней. Синонимы: Анализ крови на антитела к ВИЧ1 и 2 и антиген ВИЧ1 и 2; ВИЧ-1 p24; ВИЧ-1-антиген, p24-антиген; ВИЧ 1 и 2 антитела и антиген p24/25, ВИЧ тест-системы 4-г.
Читайте также:

