Лечение рнк вирусных инфекций
Обновлено: 25.04.2024
Острые респираторные инфекции (ОРВИ) являются наиболее распространенными среди всех инфекционных заболеваний. На долю ОРВИ, а также гриппа приходится не менее 70% инфекционных заболеваний. В России ежегодно регистрируется около
Острые респираторные инфекции (ОРВИ) являются наиболее распространенными среди всех инфекционных заболеваний. На долю ОРВИ, а также гриппа приходится не менее 70% инфекционных заболеваний. В России ежегодно регистрируется около 50 млн инфекционных заболеваний, из которых до 90% случаев приходится на ОРВИ и грипп.
Почти 90% населения как минимум один раз в году переносят одну из респираторных инфекций вирусной этиологии, что в целом предопределяет высокую заболеваемость и даже влияет на показатель смертности [2].
Столь высокая частота заболеваний респираторного тракта объясняется многообразием этиологических факторов (вирусы гриппа, парагриппа, аденовирусы, риновирусы, реовирусы, респираторно-синцитиальные (РС) вирусы, микоплазмы, хламидии, бактериальные агенты), а также легкостью передачи возбудителя и высокой изменчивостью вирусов.
Дифференциальная диагностика гриппа и ОРВИ затруднена из-за сходства клинической картины этих заболеваний, но вполне возможна. Основными отличиями можно считать начальные признаки заболевания, симптомы интоксикации, характер катаральных явлений и лихорадки, тип развивающихся осложнений и др. Клинический диагноз, подтвержденный данными лабораторных анализов, и определяет выбор терапии.
Клиническая картина ОРВИ и гриппа зависит от вируса-возбудителя (см. таблицу).
Следует отметить, что осложнения при ОРВИ, особенно в период эпидемии, регистрируются в 20–30% случаев. Основными причинами осложнений являются нарушения иммунной защиты, приводящие к длительной недостаточности в работе иммунной системы. Снижение антибактериальной резистентности организма приводит к затяжным периодам реконвалесценции и обусловливает возможность осложнений в течение длительного времени. Особое место среди осложнений занимает так называемый синдром послевирусной астении (СПА), который может развиваться у 65% больных в течение 1 мес от начала заболевания. Ведущими симптомами СПА являются усталость, эмоциональные нарушения и различные психические расстройства.
Круг препаратов, используемых при лечении ОРВИ и гриппа, широк и разнообразен. Он включает живые и инактивированные вакцины, химиопрепараты этиотропного действия, а также средства, применяющиеся для иммунокорригирующей и патогенетической терапии.
Тем не менее течение гриппа и других ОРВИ по-прежнему плохо поддается контролю. Это связано не только с полиэтиологичностью данных заболеваний, но и с уникальной изменчивостью вирусов и глобальным характером эпидемий. Распространение ОРВИ в значительной степени зависит от экологической, социально-экономической ситуации, наличия у пациентов аллергических заболеваний и ряда других факторов.
Противовирусные препараты
Химиопрепараты
Механизм действия этой группы препаратов основан на избирательном подавлении отдельных звеньев репродукции вирусов, без нарушения жизнедеятельности клетки макроорганизма. При респираторных инфекциях используются две группы препаратов — блокаторы М2-каналов и ингибиторы нейроаминидазы, а также рибавирин, активный против РС-вируса.
Блокаторы М2-каналов
В 1961 г. был синтезирован симметричный амин — амантадин, а затем и ряд его производных (римантадин, мидантан, дейтифорин). В нашей стране получил широкое применение римантадин, который используется для лечения и профилактики гриппа, вызванного вирусом типа А. Эффективность этого средства составляет 70–90%.
Противовирусный эффект реализуется путем блокирования особых ионных каналов (М2) вируса, что сопровождается нарушением его способности проникать в клетки и высвобождать рибонуклеопротеид. Тем самым ингибируется важнейшая стадия репликации вирусов. Примерно в 30% случаев может развиваться резистентность к римантадину [6].
Римантадин выпускается в форме ремантадина в таблетках по 50 мг и сиропа для детей от 1 до 7 лет альгирем—2 мг/мл. С лечебной целью препарат назначается с момента регистрации первых симптомов. Длительность терапии не должна превышать 5 дней во избежание появления резистентных форм вируса. Профилактически римантадин необходимо принимать не менее 2 нед.
Ингибиторы нейроаминидазы
Препараты этой группы эффективны не только против вирусов гриппа типа А, но и против вирусов типа В.
Нейроаминидаза (сиалидаза) — один из ключевых ферментов, участвующих в репликации вирусов гриппа. При ингибировании нейроаминидазы нарушается способность вирусов проникать в здоровые клетки, снижается их устойчивость к защитному действию секрета дыхательных путей и таким образом тормозится дальнейшее распространение вируса в организме. Ингибиторы нейроаминидазы способны уменьшать продукцию цитокинов (ИЛ-1 и фактора некроза опухоли), препятствуя развитию местной воспалительной реакции и ослабляя такие системные проявления вирусной инфекции, как лихорадка, боли в мышцах и суставах, потеря аппетита [7].
Предварительные исследования показали, что эффективность такого ингибитора в качестве профилактического средства составляет 70–80%. Прием этих препаратов позволяет сократить длительность болезни на 1–1,5 дней (если препарат начать принимать не позднее, чем через 36–48 ч с момента появления первых симптомов). В начале заболевания и на ранних его стадиях средняя продолжительность репликации вируса сокращается в среднем на 3 дня, а число тяжелых форм ОРВИ и гриппа, характеризующихся повышенной температурой, — на 85%. Препараты не оказывают вредного воздействия на центральную нервную систему. Однако следует отметить, что далеко не всегда представляется возможность их применения в первые 48 ч: из-за сложностей, связанных с дифференциальной диагностикой гриппа и других ОРВИ.
Представителями ингибиторов нейроаминидазы являются озельтамивир и занамивир.
Озельтамивир (тамифлю) назначается по 75–150 мг 2 раза в день в течение 5 дней. Для профилактики — по 75 мг 1 или 2 раза в день в течение 4–6 нед. У пациентов с клиренсом креатинина менее 30 мл/мин доза снижается в 2 раза.
Занамивир (реленца) является структурным аналогом сиаловой кислоты — естественного субстрата нейроаминидазы вирусов гриппа — и, следовательно, обладает способностью конкурировать с ней за связывание с активным центром. Ингалируется с помощью специального устройства — дискхалера. С лечебной целью назначается по 10 мг 2 раза в день (с интервалом 12 ч) в течение 5 дней, для профилактики — по 10 мг 1 раз в день в течение 4–6 нед. Ингаляционный способ введения имеет преимущество, так как обеспечивает достаточно быстрый противовирусный эффект в зоне первичного очага инфекции.
Побочные реакции данной группы препаратов составляют не более 1,5% случаев. Чаще всего это головная боль, головокружение, тошнота, диарея, явления синусита. У пациентов с обструктивными бронхолегочными заболеваниями возможно развитие бронхоспазма.
Препараты, активные против других вирусов
Рибавирин (виразол, ребетол), действующий на многие РНК- и ДНК-содержащие вирусы, в аэрозольной лекарственной форме используется при лечении инфекций, вызванных РС-вирусом. Предполагается, что препарат ингибирует ранние этапы вирусной транскрипции, нарушая синтез рибонуклеопротеидов, информационной РНК, блокируя РНК-полимеразу. Применяется ингаляторно с помощью небулайзера только в условиях стационара.
При приеме рибавирина могут отмечаться бронхоспазм, сыпь, раздражение глаз, причем не только у пациентов, но и у медперсонала. В редких случаях наблюдаются лейкопения, бессонница, раздражительность. Существует риск кристаллизации препарата в дыхательных путях и интубационных трубках. Обладает тератогенным действием.
Перспективным противовирусным препаратом является недавно разработанный в США пленоконарил. В исследованиях in vitro и в экспериментах на животных выявлена его активность против энтеровирусов и риновирусов. Данные первых плацебо-контролируемых исследований свидетельствуют об эффективности препарата при респираторных инфекциях и энтеровирусном менингите [8].
В России применяются оригинальные противовирусные препараты, созданные на основе отечественных разработок. Наиболее широко известный из них — арбидол. Он оказывает ингибирующее действие на вирусы гриппа типа А и В и другие респираторные вирусы, механизм которых до конца не выяснен. Предполагают, что подобное воздействие связано и с интерферониндуцирующими и с иммуномодулирующими свойствами препарата. В частности, арбидол стимулирует активность фагоцитарных клеток. Выпускается в таблетках по 0,1 г. В лечебных целях назначается по 0,2 г 3–4 раза в день в течение 3–5 дней. С профилактической целью применяется по 0,2 г/сут в течение 10–14 дней.
Интерфероны
Интерфероны (ИФН) относятся к числу регуляторов иммуногенеза. Они продуцируются различными клетками и не только реализуют противовирусный ответ, но и регулируют иммунологические реакции. Основные эффекты интерферонов можно подразделить на антивирусные, антимикробные, антипролиферативные, иммуномодулирующие и радиопротективные.
Несмотря на разнообразие генетического материала вирусов, ИФН подавляют их репродукцию на стадии, обязательной для всех вирусов: они блокируют начало трансляции, т. е. синтез вирусспецифических белков. Этим можно объяснить универсальность антивирусного действия интерферона. Под воздействием интерферона в организме усиливается активность естественных киллеров, Т-хелперов, цитотоксических Т-лимфоцитов, фагоцитарная активность, интенсивность дифференцировки В-лимфоцитов, экспрессия антигенов МНС I и II типа [1].
Для лечения вирусных инфекций применяются α- и β-интерфероны. Хороший эффект при лечении дает комбинированное применение химиопрепаратов и препаратов ИФН.
β-интерферон (бетаферон) выпускается в форме порошка, во флаконах, содержащих по 9,5 млн ЕД ИФН. При гриппе его закапывают или распыляют в носовые ходы не менее 4–5 раз в сутки [2].
Человеческий лейкоцитарный интерферон представляет собой смесь интерферонов, синтезируемых лейкоцитами донорской крови в ответ на воздействие вирусного индуктора. Препарат вводят ингаляторно или закапывают в носовые ходы водный раствор, приготавливаемый из сухого вещества в ампуле или флаконе.
Виферон — рекомбинантный интерферон-α 2b — выпускается в форме ректальных свечей и применяется при лечении ОРВИ и гриппа. Повреждение клеточных мембран, наблюдаемое в ходе развития инфекционного процесса, является причиной снижения противовирусной активности интерферона. Токоферола ацетат и аскорбиновая кислота, входящие в состав виферона, являются мембраностабилизирующими компонентами, антиоксидантами, в сочетании с которыми противовирусная активность рекомбинантного интерферона-α 2b возрастает в 10–14 раз [1].
Особенности введения лекарственной формы обеспечивают длительную циркуляцию в крови интерферона-α 2b.
Препарат применяется как у новорожденных детей, так и у взрослых больных при ОРВИ и гриппе в возрастных дозировках. Детям до 7 лет назначается виферон-1, детям старше 7 лет и взрослым — виферон-2.
Индукторы интерферона
Амиксин — низкомолекулярный синтетический индуктор эндогенного интерферона ароматического ряда, относящийся к классу флуоренонов. Основными структурами, продуцирующими интерферон в ответ на введение амиксина, являются клетки эпителия кишечника, гепатоциты, Т-лимфоциты, гранулоциты. В лейкоцитах человека амиксин индуцирует образование интерферона, уровень в крови которого составляет 250 ЕД/мл. После приема амиксина внутрь максимум интерферона у человека определяется последовательно в кишечнике, печени, крови через 4–24 ч [2].
При лечении гриппа и ОРВИ амиксин назначается в первые часы заболевания, на курс достаточно 5–6 таблеток. С целью профилактики назначается 1 раз в неделю в течение 4–6 нед.
Циклоферон является низкомолекулярным индуктором ИФН-α , что определяет широкий спектр его биологической активности. Он быстро проникает в клетки, накапливаясь в ядре и цитоплазме. Циклоферон интеркалирует ДНК клетки, с чем связан механизм его интерферониндуцирующей активности [3].
Циклоферон быстро проникает в кровь. Отмечается низкое связывание его с белками крови и в то же время широкое распространение в различных органах, тканях, биологических жидкостях организма.
Ввиду того что циклоферон является низкомолекулярным препаратом, он легко преодолевает гематоэнцефалический барьер, вызывая образование ИФН в мозге. Циклоферон быстро выводится из организма: 99% введенного препарата элиминируется почками в неизмененном виде в течение 24 ч.
Циклоферон хорошо переносится больными и назначается с первого дня от начала заболевания в виде таблетированной формы или парентерально [4].
Ридостин — высокомолекулярный индуктор ИФН природного происхождения. Ридостин представляет собой двуспиральную РНК, полученную из лизата киллерных дрожжей Saccharamyces cervisiae.
Системное введение ридостина стимулирует продукцию раннего ИФН. Максимальное накопление ИФН в сыворотке отмечается через 6–8 ч после инъекции; через 24 ч в кровотоке не определяется [1].
Препарат проявляет выраженный иммуномодулирующий эффект. Он стимулирует Т-клеточное и гуморальное звенья иммунитета, пролиферацию стволовых клеток костного мозга и фагоцитарную активность макрофагов и нейтрофилов периферической крови. Ридостин повышает уровень кортикостероидных гормонов; применяется для лечения и профилактики гриппа и других ОРВИ.
В настоящее время незаслуженно забывают препарат дибазол, применяемый для лечения и профилактики гриппа и ОРВИ. Дибазол обладает иммуномодулирующей активностью и индуцирует выработку эндогенного интерферона. Для профилактики назначается по 1 таблетке (0,02–0,05 г) 1 раз в день — 3–4 нед, для лечения — по 1 таблетке 3 раза в день — 5 дней.
Незаменимы в лечении гриппа и ОРВИ такие комплексные препараты, как гриппостад, ринза, терафлю, фервекс, а также препараты для наружного и местного применения — мазь от простуды доктор Мом, туссамаг бальзам от простуды.
Несмотря на многообразие препаратов, представленных для лечения ОРВИ и гриппа на современном этапе, выбор лекарственного препарата остается актуальной задачей для практикующего врача. Выбор тактики назначения и ведения больного с ОРВИ или гриппом напрямую связан с тяжестью течения инфекционного процесса, формой заболевания и наличием осложнений. Успех лечения зависит от правильной оценки состояния больного и раннего начала лечения.
Респираторно-синцитиальная вирусная инфекция (РСВИ) занимает важное место в патологии органов дыхания, как у детей, так и у взрослых. Респираторно-синцитиальный вирус (РСВ) - наиболее частая причина поражения Нижних дыхательных путей (НДП) у детей раннего возраста, причем заболевание может привести к летальному исходу. У детей старшего возраста и взрослых РСВ вызывает более легкое поражение респираторного тракта, проявляющееся ринофарингитом, бронхитом, включая обострение хронического бронхита, пневмонией.
Этиология и эпидемиология
РСВ входит в состав семейства Paramyxoviridae, являясь представителем рода Pneumovirus. Свое название вирус получил в результате характерного цитопатического действия в культуре клеток, ведущего к образованию синцития и симпластов. РСВ не содержит гемагглютинина и нейраминидазы.
РСВИ является, по существу, эндемичной, и в отдельные периоды происходит подъем заболеваемости. Вспышки наблюдаются в различное время года, чаще осенью и зимой. Подъем заболеваемости РСВИ нередко совпадает с эпидемией гриппа, и тогда у детей можно диагностировать микст-инфекцию. Как и грипп, РСВИ увеличивает количество осложнений и летальность от гриппа и пневмонии.
Продолжительность эпидемического подъема заболеваемости ограничивается 3-5 месяцами. Такие вспышки, как правило, имеют место ежегодно в одной и той же местности. В это время РСВ вызывает не только бронхиолиты и пневмонии, но также и легкие заболевания верхних дыхательных путей (ВДП) у детей. Вспышки РСВИ могут протекать в виде ограниченных локальных эпидемий в учреждениях для детей раннего возраста.
Источником инфекции являются больные и вирусоносители. Вирусы выделяются вместе с секретом слизистой оболочки ВДП во время разговора, кашля, чихания, и передача возбудителя здоровым осуществляется воздушно-капельным путем. Опасность заражения от больного человека сохраняется в течение 5-7 дней. Восприимчивость к РСВ очень высока, особенно у детей раннего возраста.
О распространении РСВИ среди различных возрастных групп населения позволяют судить серологические исследования. У большинства новорожденных имеются антитела, полученные от матери. Однако врожденный пассивный иммунитет довольно быстро утрачивается, и уже у детей 4-6-месячного возраста антитела не удается обнаружить. В этот период дети становятся высоко восприимчивыми к РСВ, заболеваемость возрастает, в результате чего увеличивается число детей, которые приобрели антитела, а вместе с ними и иммунитет. У детей в возрасте 5-10 лет антитела к РСВ обнаруживаются у 63-68% обследованных. Примерно такой же результат был получен и при обследовании здоровых взрослых (67%). Заболевания, вызванные РСВ, наблюдаются и среди взрослых различного возраста, при этом у большинства из них имеет место реинфекция, так как болезнь возникает несмотря на наличие нейтрализующих и комплементсвязывающих антител.
Клиника и патогенез
Инкубационный период длится не менее 3 дней, чаще 4-5 дней. Начинается заболевание как остро, так и подостро. У детей грудного возраста чаще наблюдается вовлечение в процесс НДП, в то время как у старших детей и у взрослых изменения обычно ограничиваются областью ВДП и протекают в виде ринита, фарингита, ларингита. Ринит отмечается у большинства пациентов, выделения из носа необильные серозно-слизистые. В ротоглотке может наблюдаться умеренная гиперемия слизистой. Наиболее частый симптом РСВИ - кашель, вначале непродуктивный, затем на 3-4 день болезни появляется мокрота.
Через 2-3 дня от начала болезни, а иногда и в более поздние сроки, обнаруживаются признаки поражения НДП с развитием бронхита, бронхиолита или бронхо-бронхиолита, обусловливающие возникновение БОС. Появляется одышка с втяжением уступчивых мест грудной клетки, обычно экспираторного типа. Дыхание шумное, свистящее.
При бронхите у большинства пациентов на фоне жесткого дыхания выслушивается большее или меньшее количество сухих свистящих хрипов, у части больных - средне- и крупнопузырчатые влажные хрипы. Выдох удлинен. Для бронхиолита характерно обилие мелкопузырчатых влажных и крепитирующих хрипов, выслушиваемых по всей поверхности обоих легких, обычно в конце вдоха. Из-за вздутия легких при перкуссии грудной клетки определяется коробочный звук.
Одним из важных признаков, характеризующих БОС, является цианоз. У детей первых месяцев жизни с бронхиолитом отмечается общий цианоз, дети становятся чугунного цвета. Поражение органов дыхания происходит на фоне лихорадки, которая в отдельных случаях может и отсутствовать.
При рентгенологическом обследовании наиболее характерным признаком РСВИ является повышение прозрачности легочных полей, расширение межреберных промежутков, усиление легочного рисунка за счет расширения крупных сосудистых стволов и обогащения его мелкими линейными тенями. Наблюдается перестройка всего легочного рисунка по сетчато-трабекулярному типу.
В крови в первые дни болезни может обнаруживаться лейкоцитоз за счет гранулоцитов, однако чаще имеет место нормоцитоз или, реже, лейкопения. СОЭ обычно повышена.
Общая продолжительность РСВИ составляет от 5-7 дней до 3-х недель.
У новорожденных и детей второго месяца жизни, особенно недоношенных, при РСВИ могут возникать приступы апноэ. Такие приступы, хотя часто повторяются во время острой инфекции, обычно купируются самостоятельно и, как правило, не сопровождаются неврологическими или системными повреждениями, но требуют наблюдения.
У детей старшего возраста и взрослых РСВИ обычно протекает в стертой форме или проявляется только как афебрильное заболевание ВДП, но может иметь и клиническую симптоматику гриппа. Полагают, что РСВ служит причиной 15% обострений хронического бронхита.
Особого внимания заслуживают тяжелые формы РСВИ у детей раннего возраста, проявляющиеся бронхиолитом или бронхо-бронхиолитом с бронхообструктивным синдромом (БОС), требующие неотложной помощи и могущие привести к летальному исходу. Половина больных этой группы приходится на детей первых 3 месяцев жизни, начиная с раннего неонатального периода. Бронхиолиты в изолированном виде обычно наблюдаются у детей первых месяцев жизни, однако в большинстве случаев, наряду с бронхиолитом, имеются клинические признаки поражения и крупных бронхов. Клинически эту группу больных характеризует выраженная дыхательная недостаточность, определяющая тяжесть болезни, в то время как явления интоксикации выражены слабо или в умеренной степени.
Клиническая диагностика РСВИ представляет определенные трудности ввиду сходства с другими респираторными заболеваниями. И все же некоторые клинические особенности отличают РСВИ от других ОРВИ. Для РСВИ в типичных случаях характерно поражение НДП с развитием бронхита или бронхиолита и возникновением БОС. Дифференциальная диагностика у детей первого полугодия жизни должна включать все другие причины острых заболеваний НДП - вирусы парагриппа, особенно 3 типа, аденовирусы, вирусы гриппа, риновирусы, а также Chlamydia trachomatis. Последняя вызывает интерстициальную пневмонию с кашлем, и, в некоторых случаях, затрудненное дыхание, хотя лихорадка обычно отсутствует. У детей с иммунодефицитом должна быть принята во внимание возможность инфекции Pneumocystis carinii. При бактериальной пневмонии шумного выдоха обычно не бывает, а симптомы общей интоксикации более выражены.
Для диагностики РСВИ имеют значение и эпидемиологические данные. Если это семейный очаг, то взрослые и дети старшего возраста переносят обычное, легкое респираторное заболевание, в то время как у детей раннего возраста наблюдается тяжелое течение, и у них часто возникает бронхит или бронхиолит.
Таким образом, имеющихся клинико-эпидемиологических данных нередко бывает достаточно для предположительного диагноза. Для окончательной верификации диагноза РСВИ используются различные лабораторные методы диагностики.
В практической работе в настоящее время наиболее широко используют экспресс-методы, направленные на определение антигена РСВ в материалах от больных. Антиген РСВ можно обнаружить методом иммунофлюоресценции либо ИФА. Оба метода достаточно специфичны и чувствительны и, по существу, имеют равновеликую ценность. Ответ получают через несколько часов.
Образцы для исследования лучше забирать при аспирации, устанавливая катетер над входом в гортань. Материал можно также получить из полости носа, используя сухой ватный тампон на металлическом стержне, реже пользуются носоглоточными смывами. Взятие материала из НДП для рутинного диагноза не является необходимым, хотя это может повысить результативность диагностики.
У умерших детей исследуют ткань легких, трахеи и бронхов на антиген РСВ или они используются для выделения вируса.
Специфический антиген выявляют методом иммунофлуоресценции в цитоплазме эпителиальных клеток носа с первых дней болезни и в последующие 10 дней. Однако при тяжелых формах болезни мы обнаруживали антиген РСВ до 29-49 дней от начала болезни.
При легких формах РСВИ, которые широко распространены, применяются симптоматические средства, и они не требуют каких-либо специфических мер.
При тяжелых формах заболевания, сопровождающихся БОС, необходима госпитализация детей. Лечение тяжелых форм РСВИ с поражением НДП носит неотложный характер. Первоочередными являются следующие мероприятия:
Несомненно, что главной задачей терапии является обеспечение адекватной оксигенации крови, что достигается как прямой ингаляцией кислорода, так и воздействием на различные механизмы БОС. Уже такое простое мероприятие, как своевременное удаление с помощью электроотсоса слизи, накапливающейся в ВДП, может привести к улучшению дыхательной функции.
При БОС показано применение средств, уменьшающих отек слизистой дыхательных путей, гиперсекрецию и бронхоспазм. Применяются бронходилятаторы и муколитики.
В связи с возникновением тяжелых, иногда критических состояний при БОС в качестве неотложной терапии показано применение глюкокортикоидов, которые применяют в сочетании с бронхолитиками. Преднизолон или гидрокортизона гемисукцинат вводят внутривенно, а затем переходят на пероральный прием. Преднизолон назначается из расчета 2-3 мг/кг, а гидрокортизона гемисукцинат 5-6 мг/кг в сутки.
Патогенетически обосновано применение диуретиков быстрого действия (фуросемид) в лечении обструктивного синдрома, если он обусловлен бронхиолитом. Фуросемид вводится в разовой дозе 1 мг/кг внутривенно или внутримышечно. Повторное введение фуросемида следует проводить с осторожностью, и чаще всего в его повторном введении в ближайшие 24 часа нет необходимости. Бикарбонат натрия для коррекции декомпенсированного ацидоза у детей с БОС не применяется.
Оптимальным вариантом поддержания функционального состояния слизистой дыхательных путей является пребывание ребенка в условиях кислородного аэрозоля (тумана) и применение медикаментозных аэрозольных ингаляций. Получение тумана достигается с помощью производителя аэрозолей эжекционного типа. Аэрозоль направляют под тент-палатку ДКП-1 или под колпак кювеза (для детей первых месяцев жизни). В камере создается кислородный аэрозольный туман с 50-60% содержанием кислорода и высокой влажностью (100%). С помощью производителя аэрозолей распыляют обычную воду, 2% раствор бикарбоната натрия, физиологический раствор, которые оказывают муколитическое действие и способствуют отхождению мокроты и снижению потери жидкости.
Постоянная ингаляционная терапия позволяет достичь, прежде всего, удовлетворительной оксигенации крови. При этом улучшаются и другие показатели газового состава крови и кислотно-щелочного состояния, особенно уменьшается метаболический компонент ацидоза.
С целью поддержания гомеостаза почти всем детям проводится инфузионная терапия, тем более, что полноценное энтеральное кормление часто не может быть обеспечено из-за тяжести состояния, однако она осуществляется в небольших объемах (20-25 мл/кг массы) и кратковременно. Обычно вводится 10% раствор глюкозы с электролитами.
В терапии БОС, особенно при выраженном бронхо-спазме, могут быть использованы бронходилятаторы короткого действия из группы b2-агонистов. Например, сальбутамол (0,2 мг/кг в день) при бронхиолите у детей в возрасте 1-9 месяцев.
Из средств этиотропной терапии для лечения РСВИ у детей раннего возраста в настоящее время в мире препаратом выбора является рибавирин, который является синтетическим нуклеозидом и принадлежит к противовирусным препаратам широкого спектра действия. Условием назначения рибавирина является лабораторно подтвержденный диагноз и ранние сроки заболевания. Показаниями для ингаляций рибавирина являются тяжелые формы РСВИ у детей раннего возраста и больные с врожденными пороками сердца. Применяется в виде длительных ингаляций аэрозолей в дозе 10 мг/кг в сутки. Длительность курса лечения 3-5 дней.
Применение рибавирина приводит к уменьшению тяжести клинической картины заболевания, сокращению длительности БОС, быстрой элиминации возбудителя, ускорению выздоровления.
При применении рибавирина следует самым строгим образом учитывать предупреждения о возможных токсических проявлениях.
Создание вакцин против РСВИ имеет долгую и поучительную историю. Более чем за 30 лет были получены инактивированные, живые аттенуированные и субъединичные РСВ-вакцины. Однако все они оказались неэффективными. Более того, после применения инактивированной вакцины естественное заражение РСВ приводило к более тяжелому течению заболевания. Тем не менее, усилия по созданию новых вакцин против РСВИ не ослабевают, и есть надежда, что эффективная вакцина будет разработана.
1. Медицинская микробиология (под ред. В.И. Покровского и О.К. Поздеева). М.: Гэотар Медицина,1998.
2. Simoes E.A. Respiratory syncytial virus infection. Lancet 1999; 354: 847-52.
4. Rodriguez W.J. Management strategies for respiratory syncytial virus infections in infants. J Pediatr 1999; 135: 45-50.
5. Ottolini M.G., Hemming V.G. Prevention and treatment recommendations for respiratory syncytial virus infection. Background and clinical experience 40 years after discovery. Drugs 1997; 54: 867-84.
6. Hussell T.; Openshaw P. Recent developments in the biology of respiratory syncytial virus: are vaccines and new treatments just round the corner? Curr Opin Microbiol 1999; 4: 410-4.
Риновирусная инфекция – острое вирусное поражение верхних отделов респираторного тракта - носа и носоглотки. Течение риновирусной инфекции характеризуется общеинфекционной симптоматикой (субфебрилитетом, познабливанием, недомоганием), першением в горле, чиханием, заложенностью и обильными выделениями из носа, ломотой в области переносицы, отсутствием обоняния. Диагноз риновирусной инфекции обычно устанавливается по клиническим данным; возможно проведение серологических и вирусологических исследований. При риновирусной инфекции показаны инстилляции сосудосуживающих капель и интерферона в нос, горячие ножные ванны, прием иммунокорректоров, противовоспалительных, антигистаминных средств.
Общие сведения
Риновирусная инфекция — разновидность ОРВИ, вызываемая риновирусами и протекающая в форме ринита и фарингита. На долю риновирусной инфекции приходится от 25% до 40% всех вирусных простудных заболеваний. Заболеваемость риновирусной инфекцией среди различных возрастных групп регистрируется круглогодично, однако эпидемический подъем обычно отмечается в сентябре и в апреле. Риновирусная инфекция более характерна для стран с умеренным и холодным климатом. В течение года человек может переболеть риновирусной инфекцией неоднократно. Риновирусная инфекция может провоцировать развитие хронического бронхита и бронхиальной астмы у детей и взрослых, поэтому актуальна не только для инфекционных болезней, но также для пульмонологии и педиатрии.

Причины риновирусной инфекции
Этиологическими агентами, вызывающими риновирусную инфекцию, выступают вирусы семейства пикорнавирусов. Различают 113 серологических типов риновирусов. Вирусные частицы возбудителей содержат РНК; их диаметр составляет 20-30 нм. Оптимальной для роста риновирусов является температура 33-34° С (именно такая температура поддерживается в носовых ходах человека). Вместе с тем, отсутствие внешней оболочки делает риновирусы малоустойчивыми в условиях изменения температуры, высушивания, воздействия дезсредств.
Резервуарами и распространителями риновирусной инфекции выступают носители возбудителя или больные люди, которые являются заразными за сутки до появления симптомов и в течение последующих 5-9 дней. Инфицирование окружающих происходит преимущественно воздушно-капельным путем. Контактно-бытовая передача риновирусной инфекции через руки и предметы обихода, контаминированные назальным секретом больного, не исключена, но на практике реализуется крайне редко ввиду нестойкости риновируса во внешней среде.
Восприимчивость к риновирусной инфекции высокая; вспышки чаще возникают в небольших коллективах (семье, группе детского сада, школьном классе и т. д.). Риск заболеваемости во многом зависит от преморбидного фона, состояния иммунитета, длительности контакта с больным или вирусоносителем. Риновирус проникает в организм через слизистую оболочку носовых ходов, где размножается в эпителиальных клетках. Этим обусловлено развитие местного очага воспаления с выраженным набуханием, отеком и гиперсекрецией слизистой оболочки носовой полости, которые достигают своей максимальной выраженности на 2-4 сутки после заражения. Активизация местной и общей иммунной защиты приводит к появлению в назальном секрете больных специфических IgA, а в крови – IgG. Этим объясняется, что риновирусная инфекция обычно протекает в форме ринита и ринофарингита. При ослаблении защитных факторов возможно развитие вирусемии с появлением инфекционно-токсических симптомов.
Симптомы риновирусной инфекции
Клинические симптомы риновирусной инфекции развиваются по истечении кратковременного инкубационного периода (от 1 до 5 дней). В первые сутки манифестной стадии появляется заложенность носа, обильные серозно-слизистые выделения из носовых ходов, подъем температуры не выше 38°С, познабливание, общее недомогание. Интоксикационный синдром выражен слабо или умеренно; большее беспокойство больным доставляют катаральные проявления (нарушение носового дыхания, насморк, чихание, чувство першения в горле, покашливание). Из-за обильного истечения назального секрета и частого использования носового платка отмечается гиперемия, шелушение и мацерация кожи вокруг носовых ходов, иногда на губах и в преддверии носа появляется герпес. Отмечается инъецированность конъюнктив и склер, слезотечение, гиперемия век.
Обычно риновирусная инфекция длится 5-7 дней и заканчивается полным выздоровлением без последствий. При осложненном сценарии развития риновирусной инфекции возможны болезненность в области переносицы, отсутствие вкуса и обоняния, боли в ухе и понижение слуха. Наслоение микробной инфекции чревато развитием гайморита, среднего отита, ларингита, трахеобронхита, пневмонии. Кроме этого, риновирусы способны вызывать обострение бронхиальной астмы и ХОБЛ.
Диагностика и лечение риновирусной инфекции
Обычно риновирусная инфекция диагностируется исключительно по клиническим признакам (обильная слизистая ринорея, мацерация кожи в преддверии носа, легкое недомогание, субфебрильная или нормальная температура тела) и эпидемиологической обстановки в ближайшем окружении. При осмотре зева определяется гиперемия и набухание слизистой ротоглотки, мелкая зернистость мягкого нёба.
Для уточнения этиологического диагноза может быть проведено выделение вируса из носовой слизи или смывов со слизистой оболочки носа на культуре тканей, однако ввиду быстротечности риновирусной инфекции на практике к нему прибегают редко. Реакция иммунофлюоресценции используется в целях экспресс-диагностики и позволяет выявить антигены риновирусов в эпителиальных клетках носовых раковин. Риновирусную инфекцию необходимо отличать от гриппа, парагриппа, аденовирусной, респираторно-синцитиальной, коронавирусной инфекции. Также следует исключить аллергический ринит, стрептококковый назофарингит, инородное тело носа. При осложненном течении риновирусной инфекции может потребоваться консультация отоларинголога или пульмонолога.
Течение риновирусной инфекции обычно доброкачественное; в большинстве случае заболевание купируется самостоятельно без специфического лечения. При риновирусной инфекции рекомендуется, главным образом, симптоматическая терапия: обильное теплое питье, инстилляция в носовые ходы сосудосуживающих препаратов и интерферона, промывания носа солевыми растворами, прием противовоспалительных и антигистаминных препаратов, горячие ножные ванны. Разработка вакцины против риновирусной инфекции затруднена ввиду большого количества серотипов риновируса. Общие противоэпидемические мероприятия аналогичны таковым при других ОРВИ (изоляция заболевших, частое проветривание и влажная уборка помещений с дезсредствами, кварцевание, профилактический прием иммунокорректоров).
Лекарства для лечения вирусных инфекций
Вирусы состоят в основном из генетического материала (нуклеиновой кислоты) и защитной оболочки, образованной белками, которая часто покрыта фосфолипидным бислоем со встроенными белками. У них отсутствует метаболическая система, а рост и репликация зависят от инфицированной клетки.
Целенаправленная терапевтическая супрессия репликации вируса достигается за счет ингибирования метаболических процессов, которые являются специфическими для вирусной репликации в инфицированных клетках.
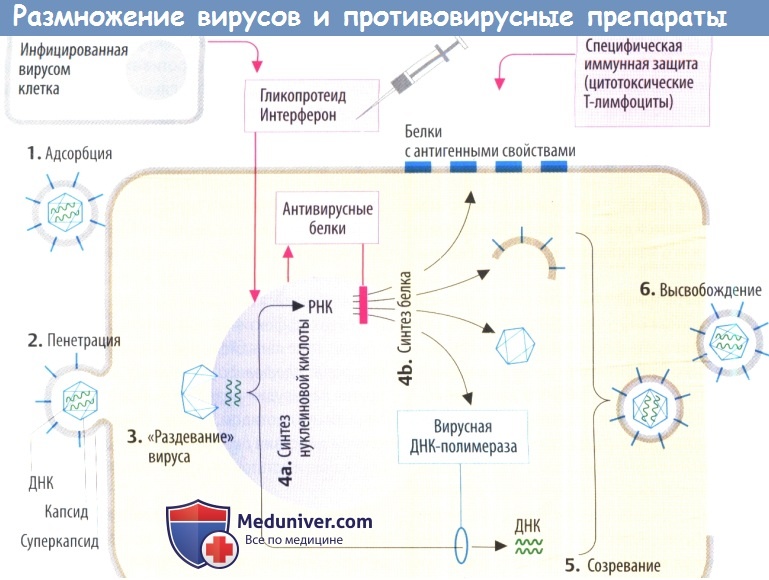
II. Противовирусные механизмы. Организм нарушает репликацию вируса с помощью цитотоксических Т-лимфоцитов, которые распознают и разрушают вируспродуцирующие клетки (на их поверхности находятся вирусные белки) или с помощью антител, которые связывают и инактивируют внеклеточные вирусные частицы. Вакцинация разработана с целью запуска специфической иммунной защиты.
а) Интерфероны (IFN) — гликопротеиды, которые в отличие от других препаратов высвобождаются из инфицированных вирусом клеток. В соседних клетках интерферон стимулирует образование антивирусных белков. Они ингибируют синтез вирусных белков за счет (предпочтительного) разрушения вирусной ДНК или ингибирования трансляции. Интерфероны не направлены против конкретного вируса, а имеют широкий спектр антивирусной активности, который, тем не менее, является видоспецифическим.
Следовательно, интерферон для использования у человека необходимо получать из его клеток, а именно лейкоцитов (IFN-a), фибробластов (IFN-β; или лимфоцитов (IFN-y). Интерфероны используются при лечении определенных вирусных заболеваний, а также злокачественных новообразований и аутоиммунных расстройств. Например, IFN-a применяется при хроническом гепатите С, волосатоклеточном лейкозе и рассеянном склерозе.
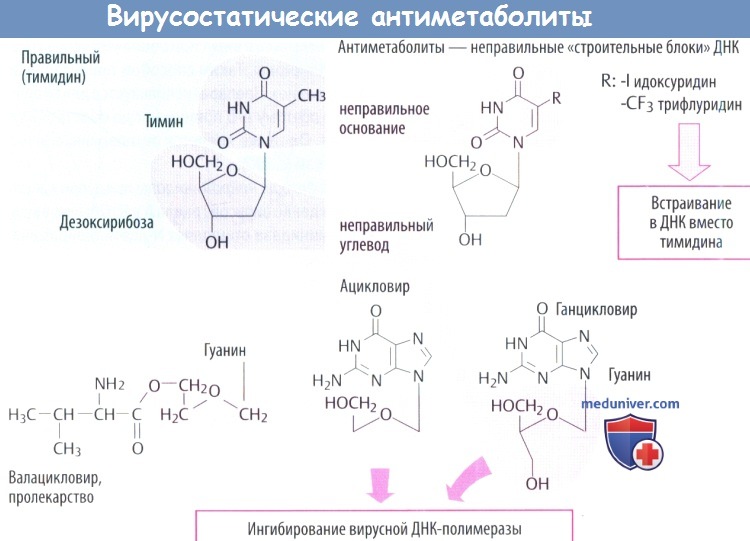
в) Идоксуридин и синергисты встраиваются в ДНК с отрицательными последствиями, в т. ч. нарушением синтеза ДНК человека. Поэтому идоксуридин и аналоги подходят только для местного использования (при простом герпетическом кератите).
г) Среди вирусостатических антиметаболитов ацикловир имеет высокую специфичность, т. к. его биоактивация происходит только в инфицированных клетках, где он предпочтительно ингибирует синтез вирусной ДНК.
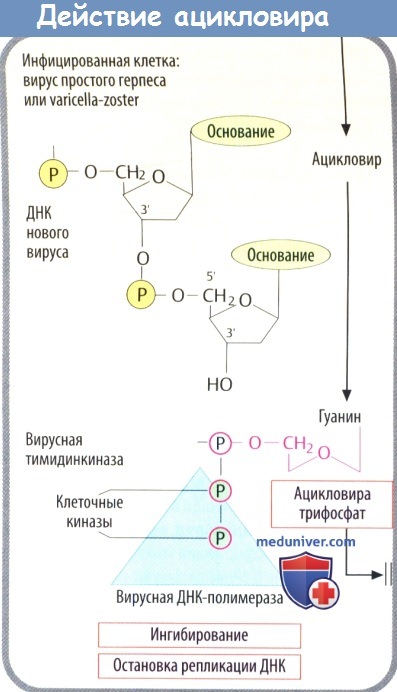
1. Кодируемая вирусом тимидинкиназа (специфичная для вирусов простого герпеса и ветряной оспы) осуществляет первый этап фосфорилирования. Два других фосфатных остатка присоединяются клеточной киназой.
2. Полярные фосфатные остатки делают мембрану непроницаемой для ацикловира трифосфата, что приводит к его накоплению в инфицированных клетках.
3. Ацикловира трифосфат является предпочтительным субстратом вирусной ДНК-полимеразы. Он ингибирует активность ферментов, а после встраивания в вирусную ДНК вызывает расщепление нити, т. к. у него отсутствует З'-ОН-группа дезоксирибозы, которая необходима для присоединения дополнительных нуклеотидов. При тяжелых инфекциях, вызванных вирусом простого герпеса (энцефалит, генерализованная инфекция) и вирусом ветряной оспы (тяжелый опоясывающий лишай), его вводят в виде в/в инфузии.
Ацикловир также применяют внутрь, несмотря на неполное (15-30%) кишечное всасывание. Кроме того, он используется местно.
г) У валацикловира гидроксильная группа этерифицирована с аминокислотой L-валином. Это позволяет использовать дипептидный переносчик тонкой кишки, что почти удваивает скорость кишечного всасывания препарата по сравнению с ацикловиром. В дальнейшем при отщеплении остатка валина образуется ацикловир.
д) Ганцикловир используется при лечении тяжелых цитомегаловирусных инфекций (тоже принадлежащих к группе герпеса). Они не образуют тимидинкиназу, поэтому фосфорилирование начинается другим вирусным ферментом. Ганцикловир хуже переносится, нередко приводит к развитию лейкопении и тромбопении. Он вводится в виде инфузии или внутрь как эфир валина (валганцикловир).
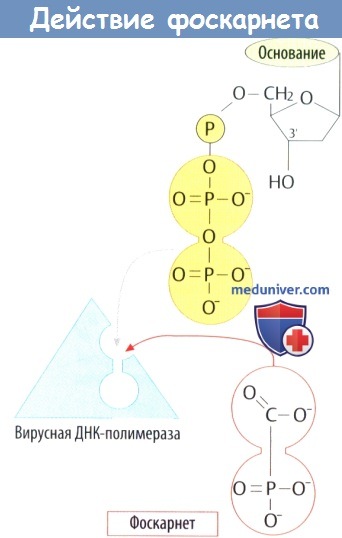
е) Фоскарнет представляет собой аналог дифосфата. Встраивание нуклеотида в нить ДНК приводит к отщеплению дифосфатного остатка. Фоскарнет ингибирует ДНК-полимеразу за счет взаимодействия со связывающим участком. Показания: системная терапия тяжелых цитомегаловирусных инфекций у больных СПИДом; местное лечение герпесвирусных инфекций.
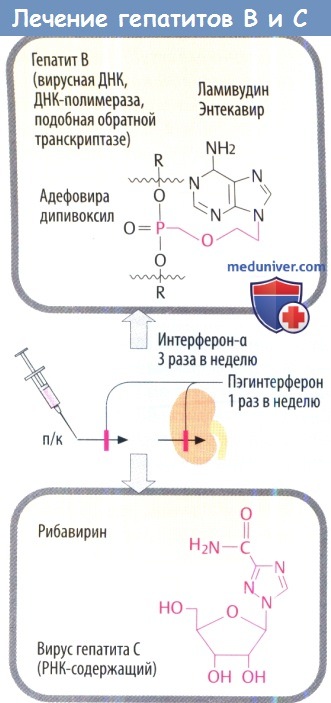
ж) Препараты для лечения вирусных гепатитов. Интерферон-а действует против вирусов гепатитов В и С (HBV, HCV) во время репликации. Присоединение молекулы полиэтиленгликоля к IFN-a (пегилирование) позволяет пегилированному IFN-a медленнее высвобождаться из места инъекции и выводиться почками, что увеличивает продолжительность действия пегилированного препарата.
Вирусостатические антиметаболиты необходимо рассматривать индивидуально в зависимости от возбудителя. Гепатит В: ламивудин, первоначально использовавшийся только как анти-ВИЧ препарат, в низких дозах эффективен против HBV. Телбивудин и энтекавир тоже являются производными нуклеозидов. Фосфонат адефовира дипивоксил, который активен против ламивудин-резистентного HBV, является атипичным нуклеотидом. Гепатит С: молекулярный механизм действия рибавирина, в котором изменены основание и остаток сахара (D-рибоза), неясен.
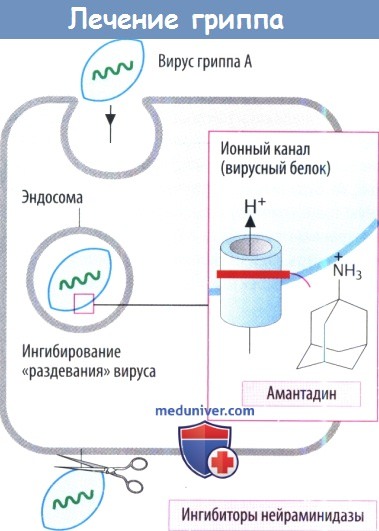
Препарат используется для профилактики, и поэтому его принимают до обострения симптомов. Он также является антипаркинсоническим средством.
Ингибиторы нейраминидазы предупреждают высвобождение вирусов гриппа А и В. Обычно вирусная нейраминидаза отщепляет N-ацетилнейраминовые (сиаловые) кислотные остатки на поверхности клеточной оболочки, что дает возможность вновь образованным вирусным частицам отделиться от клетки хозяина. Занамивир вводится в виде ингаляции. Оселтамивир подходит для применения внутрь, т. к. представляет собой сложный эфир пролекарства. Он используется при лечении и профилактики инфекций, вызванных гриппом.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

