Мрт вирус эпштейн барра
Обновлено: 25.04.2024
Диагностика вирусного энцефалита по МРТ
а) Определения:
• Диффузное воспаление мозговой ткани, вызываемое различными патогенами (преимущественно вирусами)
• Локализация зависит от этиологии
б) Визуализация:
1. Общие характеристики вирусного энцефалита:
• Лучший диагностический критерий
о Повышение интенсивности сигнала на Т2 - ВИ от серого вещества (СВ) ± белого вещества (БВ) или глубоких ядер
о Часто встречаются крупные плохо очерченные зоны поражения ± участки кровоизлияний
о Картина при визуализации часто неспецифична
• Локализация:
о Вирус простого герпеса 1 типа (ВПГ1): лимбическая система
о Цитомегаловирус (ЦМВ): глубокое перивентрикулярное белое вещество
о Вирус Эпштейн-Барр (ВЭБ):
- Мультифокальное, диффузное поражение головного и спинного мозга
- Валик мозолистого тела
о Вирус Варицелла-Зостер (ВВЗ):
- Ветряная оспа: возможно наличие мультифокальных поражений коры больших полушарий
- Опоясывающий лишай: ствол мозга/кортикальное СВ, черепные нервы
о Церебеллит: двустороннее поражение полушарий мозжечка
о Восточный лошадиный энцефалит (ВЛЭ): БГ италамус
о Энтеровирусный энцефаломиелит:
- Энтеровирус (ЭВ) 71: задние отделы продолговатого мозга, мост, средний мозг, зубчатые ядра, спинной мозг
- Вирусы полиомиелита, Коксаки: средний мозг, передние отделы спинного мозга
о Хантавирус: кровоизлияние в гипофиз
о ВИЧ-1: БВ головного мозга, ствол мозга, таламус, БГ
о Японский энцефалит: двустороннее поражение таламуса, ствола мозга, мозжечка, спинного мозга, коры больших полушарий
о Энцефалит долины Муррея (ЭДМ): двустороннее поражение таламуса; возможно поражение среднего мозга, шейного отдела спинного мозга
о Вирусный энцефалит Нипах: мультифокальное поражение БВ
о Энцефалит при бешенстве: ствол мозга, гиппокамп, гипоталамус, БВ, СВ
о Ромбэнцефалит: ствол мозга и мозжечок
о Энцефалит Сент-Луис: черная субстанция
о Вирус Западного Нила (ВЗН): БГ и/или таламус; возможно поражение ствола мозга, БВ головного мозга, черной субстанции, мозжечка, спинного мозга
2. КТ признаки вирусного энцефалита:
• Бесконтрастная КТ: у большинства пациентов на начальных стадиях заболевания изменениий не наблюдаются:
о Японский энцефалит: возможно кровоизлияние в таламус
3. Рекомендации по визуализации:
• Советы по протоколу исследования
о Мультипланарная МРТ с контрастным усилением, FLAIR, ДВИ
в) Дифференциальная диагностика:
1. Острая ишемия:
• Соответствие типичным бассейнам кровоснабжения, ограничение диффузии на ДВИ
2. Аутоиммунный энцефалит:
• Часто обусловлен наличием антител к рецепторам NMDA; субкортикальное белое вещество
3. Герпетический энцефалит:
• Поражение лимбической системы и височных долей
4. Эпилептический статус:
• Активные судорожные приступы с гиперперфузией головного мозга, нарушением ГЭБ, что обусловливает изменения сигнала и патологическое контрастирование
5. Токсические/метаболические поражения:
• Часто наблюдается симметричное поражение БГ или таламуса
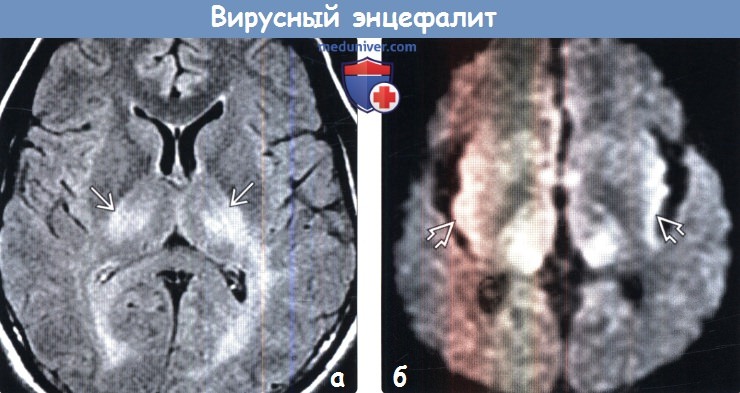
(а) MPT, FLAIR, аксиальный срез: у данного пациента с инфекционным мононуклеозом в анамнезе отмечается симметричное повышение интенсивности сигнала от таламуса билатерально. При ВЭБ обычно поражаются базальные ганглии, таламус, кора и/или ствол мозга.
(б) МРТ, ДВИ, аксиальный срез: у данного пациента с энцефалитом Западного Нила отмечается симметричное ограничение диффузии в области таламуса и коры островковых долей. Для энцефалита Западного Нила характерно поражение таламуса и базальных ганглиев. Д Патологические изменения на ДВИ могут определяться раньше, чем на традиционных МРТ-методиках
г) Патология:
1. Общие характеристики вирусного энцефалита:
• Этиология:
о В большинстве случаев (но не во всех) имеет вирусную этиологию:
- Вирусы служат облигатными внутриклеточными паразитами
- Реплицируются в клетках кожи, слизистых оболочек респираторного и пищеварительного тракта
- Проникает в ЦНС гематогенным или неврогенным путем
- В некоторых случаях-no ходу ЦНС (например, ВПГ1 проникает в ядро тройничного нерва через язычный нерв)
- Возможна реактивация латентной инфекции с распространением по оболочечным ветвям
о Вирусы герпеса: ВПГ1, ВПГ2, ЦМВ, ВЭБ, ВВЗ, В-вирус, ВПГб, ВПГ7:
- ВПГ2: энцефалит новорожденных
о Ветряная оспа: менингоэнцефалит, мозжечковая атаксия, асептический менингит (у < 1 % всех пациентов)
о Опоясывающий лишай: энцефалит, неврит, миелит или офтальмогерпес:
- Возможна реактивация вируса в латентном состоянии, локализующегося в ганглиях ЧН (часто ЧН V и ЧН VII) с распространением в ствол мозга
- Иммунокомпетентные пациенты: паралич черепных и периферических нервов
- Пациенты с иммунодефицитом: диффузный энцефалит
- Офтальмогерпес Зостер может вызывать некротизирующий ангиит внутренней сонной артерии
о ВЭБ: возбудитель инфекционного мононуклеоза:
- Диффузный энцефалит наблюдается у < 1 % пациентов
- Связан с менингоэнцефалитом, синдромом Гийена-Барре, поперечным миелитом
о Энтеровирусы: вирусы Коксаки типа А и В, вирус полиомиелита, эховирусы, энтеровирусы 86-71
о Арбовирусы (вирусы, передающиеся членистоногими): восточный, западный и венесуэльский лошадиный энцефалиты, энцефалит Сент-Луи, Японский энцефалит типа В, калифорнийский энцефалит, клещевой энцефалит
о Энцефалит Чипах: парамиксовирусная инфекция, возникающая при тесном контакте с инфицированными свиньями:
- Энцефалит Чипах: воспаление мелких кровеносных сосудов с развитием тромбоза и микроинфарктов
о Ромбэнцефалит: вирусная (наиболее часто), Listeria monocytogenes, болезнь легионеров, микоплазма, болезнь Лайма
2. Макроскопические и хирургические особенности:
• Застой крови в сосудах, генерализованный или локальный отек ± кровоизлияния, некроз
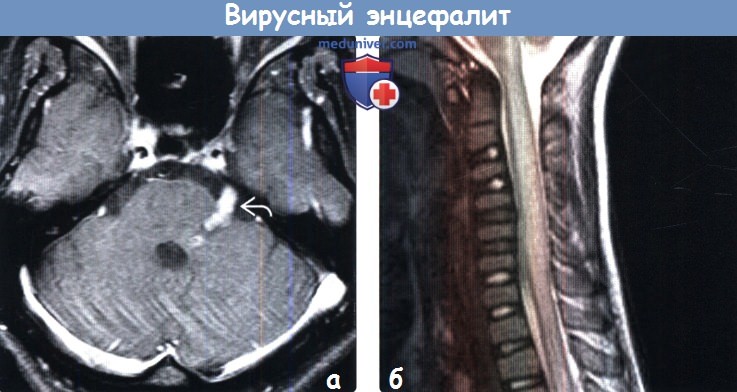
(а) МРТ, постконтрастное Т1 -ВИ, аксиальный срез: у пациента с невралгией тройничного нерва определяется контрастирование цистернального сегмента ЧН V и зоны входа его корешка, а также средней ножки мозжечка.
При опоясывающем лишае наиболее часто поражается зрительная ветвь (V1) нерва. У иммунокомпетентных пациентов при опоясывающем лишае часто поражаются черепные нервы. Энцефалит, вызванный ВВЗ, встречается редко.
(б) МРТ, Т2-ВИ, сагиттальный срез: у пациента с паралитическим бешенством определяется диффузное утолщение шейного отдела спинного мозга и повышение интенсивности сигнала от него. При паралитическом бешенстве часто поражается продолговатый и спинной мозг.
д) Клиническая картина:
1. Проявления вирусного энцефалита:
• Наиболее частые признаки/симптомы:
о Широкий спектр: от легких менингеальных симптомов до тяжелых энцефалических ± лихорадка, продромальный период
о Ветряная оспа и опоясывающий лишай: различные клинические проявления при инфекции одним вирусом (ВВЗ)
Ветряночный энцефалит: лихорадка, головная боль, рвота, судорожные приступы, изменения психического состояния через дни-недели после возникновения (ветряночной) сыпи Опоясывающий лишай: параличи ЧН и периферических нервов в дерматомах, соответствующих поражениям кожи, у иммунокомпетентных пациентов:
Наиболее часто поражается глазная ветвь ЧН V (офтальмический герпес Зостер)
о Опоясывающий лишай: лихорадка, менингизм, изменения психического состояния у пациентов с иммунодефицитом
о Церебеллит: внезапное появление атаксии конечностей и/или атаксическая походка после продромального периода
о Энтеровирусный энцефалит (ЭВ 71):
- Энтеровирусный везикулярный стоматит с экзантемой: лихорадка, везикулы на руках, ступнях, локтях, коленях, губах
- Невропатия черепных нервов, нарушения зрения, диспноэ, тахикардия при поражении ствола мозга
о Вирус Чипах: лихорадка, головная боль, сонливость, рвота; сегментарная миоклония, арефлексия, гипотония, гипертензия
о ЭДМ: лихорадка, головная боль, спутанность сознания, тремор; состояние может прогрессировать до паралича, комы, дыхательной недостаточности
о Бешенство (энцефалит): лихорадка, недомогание, изменения психического состояния, дисфункция лимбической системы, стимуляция автономной нервной системы:
- Паралитическая форма: мышечная слабость во всех конечностях
о Ромбэнцефалит: арефлексия, атаксия, офтальмоплегия
о Энцефалит Сент-Луи: тремор, лихорадка
2. Демография:
• Эпидемиология:
о Герпес: наиболее частая причина спорадического (неэпидемического) вирусного энцефалита
о Японский энцефалит: наиболее частый эндемический энцефалит в Азии
о Поражение ЦНС при ВЭБ встречается нечасто (< 10% случаев)
о ВВЗ: поражение ЦНС наблюдается в < 1 % случаев
о Заметная зависимость от сезона в США
3. Течение и прогноз:
• Для многих энцефалитов характерны высокие заболеваемость и смертность
• Снижения смертности и улучшения исхода заболевания можно добиться за счет быстрой диагностики и раннего начала терапии противовирусными или антибактериальными препаратами
е) Диагностическая памятка:
1. Обратите внимание:
• Картина при визуализации часто неспецифична и имитирует заболевания иной этиологии
• В диагностике помогает изучение клинического и эпидемиологического анамнеза
2. Совет по интерпретации изображений:
• Патологические изменения на ДВИ могут определяться раньше, чем на традиционных МРТ-методиках
ВЭБ вирус, или вирус Эпштейна-Барра – это вирус герпеса 4 типа, который вызывает высококонтагиозное инфекционное заболевание у взрослых и детей. По данным ВОЗ, вирус персистирует в организме 75-90% взрослого и детского населения. До 5% случаев заканчивается малигнизацией новообразований.
Рассказывает специалист ЦМРТ
Дата публикации: 25 Августа 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Причины Эпштейн-Барра
Вирус Эпштейна-Барра относится к группе герпесвирусов 4 типа.
В отличие от простого герпеса Эпштейн Барр приводит к пролиферации, или патологическому разрастанию, пораженных тканей с развитием образований. Вирус персистирует не в нервных клетках, а в клетках иммунной системы. Еще одно отличие – его постоянная трансформация.
Передаваться вирус Эпштейн Барр может:
- трансплацентарно
- контактно-бытовым путем
- половым способом
- воздушно-капельным путем
Заражение происходит только в острой стадии заболевания.
После перенесенной инфекции человек в течение 2 лет может оставаться возможным источником заражения. До 30% переболевших людей остаются вирусоносителями.
При воздушно-капельном типе заражения после выделения больным человеком ВЭБ попадает на слизистые оболочки дыхательной системы здоровых людей. Далее с током лимфы вирус попадает в организм.
Протекать болезнь может бессимптомно или по типу простуды. Острая фаза встречается при снижении иммунного ответа. Чаще развивается хронический процесс.
Симптомы Эпшетйна Барра
Ведущими признаками инфекции являются:
Симптомами вируса Эпштейна Барр у взрослых могут быть:
- слабость
- головокружение
- снижение работоспособности
- высокая температура
- боли в горле, насморк, кашель
- тяжесть в правом подреберье
- потемнение мочи
- желтушность кожного покрова и слизистой глаз
Характерные признаки заболевания длятся в среднем 7-14 дней, после чего наступает выздоровление. Слабость и увеличенные лимфоузлы сохраняются до 21 дня.
Для хронического течения заболевания характерно появление новообразований различной локализации.
Стадии развития болезни Эпштейн Барра
В стадии развития болезни Эпштейн Барра выделяют фазы: острую, или инфекционный мононуклеоз и хроническую.
Острая фаза занимает до 3 недель. Далее заболевание переходит в хронический процесс, который протекает с периодами обострения и ремиссий.
По тяжести течения выделяют 3 степени: легкая, средняя, тяжелая.
Эпштейн Барр при беременности
При первичном заражении вирусом Эпштейна Барр во время беременности могут развиваться осложнения со стороны матери и плода:
- самопроизвольный выкидыш
- преждевременные роды
- внутриутробное заражение плода
- поражение печени и селезенки матери.
Если будущая мать ранее имела контакт с возбудителем, то возможен переход инфекции из латентного состояния в период обострения.
Лечение инфекционного мононуклеоза у беременной обязательно проводится в стационаре под наблюдением специалистов.
Как диагностировать
Диагностика болезни Эпштейн Барра комплексная и состоит из сбора жалоб, осмотра и анализов.
При обращении пациентки к врачу отмечается характерная для простудных заболеваний симптоматика. При этом развивается регионарная лимфаденопатия и гепатоспленомегалия.
При осмотре определяются увеличенные до 2 см подвижные умеренно болезненные лимфоузлы. Поражаются обычно несколько групп лимфоузлов. При шейной лимаденопатии может возникать одутловатость лица.
Назначается общий анализ крови, для которого характерно повышение числа лейкоцитов, лимфоцитов и моноцитов, ускоренное СОЭ
В биохимическом анализе отмечается повышение значений печеночных ферментов: АлАТ, АсАТ, ЛДГ, билирубина.
Для верификации возбудителя используется серологическая диагностика:
- ПЦР: позволяет определить ДНК вируса
- ИФА: определяются количество и класс иммуноглобулинов, или антитела к Эпштейн Барру
- Для определения степени поражения печени и селезенки назначается УЗИ органов брюшной полости
- Дополнительно может назначаться иммунологическое исследование при тяжелых формах болезни.
К какому врачу обратиться
Лечением острой вирусной инфекции Эпштейн Барр занимается врач-инфекционист, терапевт или ВОП. Хроническую форму с развитием новообразований лечит онколог. При наличии показаний пациент направляется к смежным специалистам: ЛОР, иммунолог, гематолог.
Как лечить болезнь Эпштейн Барр
Лечение неспецифическое. Инфекционный мононуклеоз необходимо лечить в стационарных условиях.
Для снижения вирусной активности назначаются противовирусные препараты. По показаниям назначаются антибиотики, иммуномодуляторы.
Обязательно проводится симптоматическая терапия:
- при температуре назначаются жаропонижающие
- при кашле – отхаркивающие
- при заложенности носа – сосудосуживающие капли
Лечение патологии занимает от 2 недель до нескольких месяцев.
Последствия
Вирус Эпштейн Барра может приводить к развитию осложнений в виде:
- отита
- дыхательной недостаточности
- гепатита
- гемолитической анемии
- тромбоцитопенической пурпуры
- панкреатита
- малигнизации опухолей
Профилактика
Специфической профилактики заболевания не существует. Проводятся мероприятия по защите слизистых оболочек от проникновения вируса от больного человека: ношение маски при наличии симптомов простудной болезни, своевременное обращение к врачу для определения тактики ведения и лечения.
Лечение болезни Эпштейн Барра в клиниках ЦМРТ
В клинике ЦМРТ ведет прием терапевт. Специалист назначает необходимые виды лабораторно-диагностических исследований. При наличии жалоб можно записаться на прием по телефону, через онлайн-форму на сайте.
Источники
Инфекционные болезни: Уч. Пос / И.А. Бережнова. - М.: Риор, 2015.
Инфекционные болезни / Б.П. Богомолов. - М.: МГУ, 2006
Вирусные инфекционные заболевания и их этиотропная терапия: Метод. рек. для врачей, клин. ординаторов, интернов, студ. мед. вузов. / В. Л. Кокорев, Н. П. Куприна, Л. М. Коноплина и др.; Воронеж.мед.акад.;Сост.С.П.Кокорева и др. - Воронеж, 2003.
Эпштейна-Барр вирусная инфекция (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям человека. Антитела (Ат) к вирусу Эпштейна-Барр (ВЭБ) обнаруживают у 60% детей первых двух лет жизни и у 80–100% взрослых [3, 13]. Заболеваемость острой формой ЭБВИ (ОЭБВИ) в различных регионах мира колеблется от 40 до 80 случаев на 100 тыс. населения [2]. Хроническая форма ЭБВИ (ХЭБВИ) развивается у 15–25% лиц после ОЭБВИ [1, 5, 15]. Установлена роль ВЭБ в развитии злокачественных новообразований, аутоиммунных заболеваний и синдрома хронической усталости [3, 5, 14, 15]. Все это свидетельствует об актуальности проблемы ЭБВИ.
ВЭБ, открытый в 1964 г. M. Epstein и Y. Barr, относится к γ-герпес-вирусам [3]. ВЭБ имеет в своем составе 3 антигена: капсидный (VCA), ранний (EA) и ядерный (EBNA). Своеобразие патологического процесса при ЭБВИ определяется способностью ВЭБ к трансформации В-лимфоцитов, пожизненной персистенции в организме человека, индукции вторичного иммунодефицитного состояния (ИДС), аутоиммунных реакций, злокачественных опухолей [1, 3, 5, 12].
Источник заражения ВЭБ — больные манифестными и бессимптомными формами. 70–90% лиц, перенесших ОЭБВИ, выделяют вирус в последующие 1–18 мес. Пути передачи ВЭБ: воздушно-капельный, контактно-бытовой, парентеральный, половой, вертикальный. ОЭБВИ характеризуется эпидемическими подъемами 1 раз в 6–7 лет, чаще регистрируется в возрасте от 1 до 5 лет, в организованных коллективах [4, 7, 9].
Иммунный статус 109 больных ОЭБВИ в возрасте от 5 до 14 лет в нашей работе выявил признаки активации Т-клеточного звена иммунной системы — повышение количества Т-лимфоцитов (CD3), цитотоксических Т-лимфоцитов (CD8), клеток с маркерами поздней активации (HLA-DR); поликлональную активацию В-лимфоцитов — увеличение количества CD20-клеток, иммуноглобулинов (Ig) IgA, IgM, IgG, циркулирующих иммунных комплексов (ЦИК). Обнаружены признаки угнетения иммунной системы: нормальное содержание Т-хелперов (CD4), снижение иммунорегуляторного индекса CD4/CD8, количества естественных киллерных клеток NK (CD16), повышение готовности иммунокомпетентных клеток к апоптозу (CD95). Наблюдалась активация кислородзависимого метаболизма нейтрофилов и редукция его адаптационных возможностей.
У трети обследованных детей (33,9%) ОЭБВИ протекала в форме микст-инфекции с цитомегаловирусами (ЦМВ), вирусами простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2). При бактериологическом исследовании мазков из ротоглотки у 41,3% пациентов выделены Streptococcus (S.) viridans, у 11,9% — Candida albicans, у 8,2% — Staphilococcus (Staph.) epidermidis, у 6,4% — S. pyogenes, у 2,7% — Klebsiella (Kl.) pneumoniae, у 41,3% — ассоциация бактерий. У 43,1% пациентов — серологические маркеры активной формы хламидийной инфекции, у 30,3% — микоплазмоза.
Возможны следующие исходы ОЭБВИ: латентная инфекция, ХЭБВИ, ИДС, онкологические, аутоиммунные заболевания, синдром хронической усталости [5, 8, 10, 11]. Переход в ХЭБВИ связан с комплексом неблагоприятных факторов в анте-, интра- и постнатальном периодах, нарушением нейроиммунноэндокринной регуляции, генетической предрасположенностью.
Проведенное нами обследование 60 детей в возрасте от 5 до 14 лет с ХЭБВИ показало, что в этой группе у 86,7% матерей имел место отягощенный акушерский анамнез; у 83,3% детей обнаружены перинатальная и постнатальная патология ЦНС, ЛОР-органов и др.
Нарушения иммунного статуса приводили к активации условно-патогенной микрофлоры, вирусных и грибковых инфекций. В микробном спектре слизистой ротоглотки пациентов с ХЭБВИ выделены S. Viridans (30%), Candida albicans (28,3%), Staph. Epidermidis (25%), S. Pyogenes (20%), Kl. Pneumoniae (8,4%), ассоциация бактерий (41,7%); у 28,3% — серологические маркеры активной формы хламидиоза, у 26,7% — микоплазмоза. У 90% пациентов заболевание протекало в форме микст-инфекции с участием герпес-вирусов: ВЭБ + ЦМВ, ВЭБ + ВПГ-1, ВПГ-2.
Классификация. Общепринятая классификация заболевания отсутствует; рекомендуем использовать разработанную нами рабочую классификацию ЭБВИ.
- По периоду возникновения: врожденная, приобретенная.
- По форме: типичная (инфекционный мононуклеоз), атипичная: стертая, бессимптомная, висцеральная.
- По тяжести: легкая, среднетяжелая, тяжелая.
- По течению: острая, затяжная, хроническая.
- По фазе: активная, неактивная.
- Осложнения: гепатит, разрыв селезенки, менингоэнцефалит, полирадикулонейропатия, миокардит, синусит, отит, гемолитическая анемия, тромбоцитопения, нейтропения, панкреатит и др.
- Микст-инфекция.
Примеры оформления диагноза:
- Осн.: Приобретенная ЭБВИ, типичная тяжелая форма (инфекционный мононуклеоз), острое течение, активная фаза. Осл.: Острый гепатит.
- Осн.: Приобретенная ЭБВИ, висцеральная форма (менингоэнцефалит, гепатит, нефрит), тяжелое хроническое течение, активная фаза. Осл.: острая печеночно-почечная недостаточность. Сопp.: Респираторный хламидиоз (ринофарингит, бронхит, пневмония).
Клиническая картина острой ЭБВИ впервые была описана Н. Ф. Филатовым (1885) и Е. Пфейфером (1889). Инкубационный период длится от 4-х дней до 7 нед. Полный симптомокомплекс формируется к 4–10-му дням болезни [4, 7].
Нами обследованы 109 детей с ОЭБВИ. У большинства пациентов заболевание начинается остро, с повышения температуры тела и появления симптомов интоксикации; реже отмечается постепенное начало: несколько дней наблюдается недомогание, слабость, вялость, снижение аппетита. Температура тела субфебрильная или нормальная. Ко 2–4-му дням болезни температура достигает 39–40 °С; лихорадка и симптомы интоксикации могут сохраняться в течение 2–3 и более недель.
Тонзиллит — наиболее частый и ранний симптом ОЭБВИ, сопровождается увеличением миндалин до II-III степени. Лакунарный рисунок подчеркнут за счет инфильтрации ткани миндалин или сглажен из-за лимфостаза. На миндалинах — налеты желтовато-белого или грязно-серого цвета в виде островков, полосок. Они исходят из лакун, имеют шероховатую поверхность (напоминают кружево), легко снимаются без кровоточивости, растираются, не тонут в воде. Характерно несоответствие размера налета и степени увеличения регионарных ЛУ. При фибринозно-некротическом характере налетов в случае их распространения за пределы миндалин необходим дифференциальный диагноз с дифтерией. Налеты на миндалинах исчезают, как правило, через 5–10 дней.
Гепатомегалия может быть обнаружена с первых дней болезни, однако чаще выявляется на второй неделе. Нормализация размеров печени происходит в течение полугода. У 15–20% больных в качестве осложнения развивается гепатит.
Спленомегалия относится к поздним симптомам, встречается у большинства больных. Нормализация размеров селезенки происходит в течение 1–3 нед.
Экзантема при ОЭБВИ появляется на 3–14-й дни болезни, имеет полиморфный характер — пятнистая, папулезная, пятнисто-папулезная, розеолезная, мелкоточечная, геморрагическая. Определенной локализации нет. Сыпь наблюдается в течение 4–10 дней, иногда оставляет пигментацию. У детей, получавших ампициллин или амоксициллин, сыпь появляется чаще (90–100%).
Гематологические изменения включают лейкоцитоз (10–30 х 10 9 /л), нейтропению с палочкоядерным сдвигом влево, увеличение количества лимфоцитов, моноцитов, атипичных мононуклеаров до 50–80%, повышение СОЭ до 20–30 мм/час. Характерный гематологический признак — атипичные мононуклеары в количестве 10–50%: они появляются к концу первой недели заболевания, сохраняются в течение 1–3 нед.
Хроническая ЭБВИ является исходом ОЭБВИ или развивается как первично-хроническая форма [2, 5, 8, 10, 11, 15]. Нами обследовано 60 детей с ХЭБВИ, клиника которой включала хронический мононуклеозоподобный синдром и полиорганную патологию. У всех пациентов обнаружены лимфопролиферативный синдром (генерализованная лимфаденопатия, гипертрофия небных и глоточной миндалин, увеличение печени и селезенки) и признаки хронической интоксикации (длительный субфебрилитет, слабость, снижение аппетита и др.). Вследствие развития ИДС наблюдались острые инфекции респираторного тракта и ЛОР-органов с обострениями до 6–11 раз в год: ринофарингиты (28,3%), фаринготонзиллиты (91,7%), аденоидиты (56,7%), отиты (11,7%), синуситы (20%), ларинготрахеиты (18,3%), бронхиты (38,3%), пневмонии (25%). Обращала внимание высокая частота полиорганной патологии, обусловленная длительной репликацией ВЭБ, вторичным ИДС, аутоиммунными реакциями (патология ЦНС; хронический гастрит, дискинезия желчевыводящих путей; кардиальный синдром, артралгии).
В последние годы описана врожденная ЭБВИ. Установлено, что риск ее при первичной ЭБВИ во время беременности составляет 67%, при реактивации — 22%. Клиника врожденной ЭБВИ сходна с ЦМВИ.
Установлена роль ВЭБ в развитии онкологических заболеваний и паранеопластических процессов — лимфомы Беркетта, назофарингеальной карциномы, лимфогранулематоза, опухолей желудка, кишечника, слюнных желез, матки, лейкоплакии языка и слизистой ротовой полости, а также ряда аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена, лимфоидного интерстициального пневмонита, хронического гепатита, увеита и др. [3, 5, 14, 15]. ВЭБ, наряду с вирусами герпеса человека 6 и 7 типов, является этиологическим фактором синдрома хронической усталости и наиболее частой причиной (15%) развития длительной лихорадки неясного генеза.
Диагностика ЭБВИ основана на учете групп риска, ведущих клинических синдромов и данных лабораторного исследования [8–11]. К группам риска у матери относят отягощенный анамнез, маркеры герпес-вирусных инфекций и др., у ребенка — перинатальное поражение ЦНС, аллергический фенотип, ИДС, маркеры герпес-вирусных инфекций и др. Ведущими клиническими синдромами ЭБВИ являются мононуклеозоподобный, общеинфекционный синдромы, экзантема, синдром полиорганной патологии.
В обязательный стандарт диагностики ЭБВИ входят клинический анализ крови, общий анализ мочи, биохимическое исследование крови, бактериологическое исследование слизи ротоглотки и носа, серологические маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм, УЗИ органов брюшной полости, консультация ЛОР-врача, по показаниям — рентгенография придаточных пазух носа, органов грудной клетки, ЭКГ. Дополнительный стандарт диагностики (в специализированном лечебно-профилактическом учреждении): маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм методом полимеразной цепной реакции (ПЦР), иммунограмма второго уровня, консультация иммунолога, по показаниям — коагулограмма, морфологическая картина стернальной пункции, консультация гематолога, онколога.
Методом иммуноферментного анализа (ИФА) определяют Ат к антигенам ВЭБ, что позволяет осуществить лабораторную диагностику ЭБВИ и определить период инфекционного процесса.
Ат класса IgM к VCA появляются одновременно с клиникой ОЭБВИ, сохраняются в течение 2–3 мес, повторно синтезируются при реактивации ВЭБ. Длительная персистенция высоких титров этих Ат характерна для ХЭБВИ, ВЭБ-индуцированных опухолей, аутоиммунных заболеваний, ИДС.
Ат класса IgG к EA достигают высокого титра на 3–4-й нед ОЭБВИ, исчезают через 2–6 мес. Они появляются при реактивации, отсутствуют при атипичной форме ЭБВИ. Высокие титры Ат данного класса выявляют при ХЭБВИ, ВЭБ-индуцированных онкологических и аутоиммунных заболеваниях, ИДС.
Ат класса IgG к EBNA появляются через 1–6 мес после первичной инфекции. Затем их титр уменьшается и сохраняется в течение всей жизни. При реактивации ЭБВИ происходит повторное увеличение их титра.
Большое значение имеет исследование авидности Ат класса IgG (прочности связывания антигена с Ат). При первичной инфекции сначала синтезируются Ат с низкой авидностью (индекс авидности (ИА) менее 30%). Для поздней стадии первичной инфекции характерны Ат со средней авидностью (ИА — 30–49%). Высокоавидные Ат (ИА — более 50%) образуются через 1–7 мес после инфицирования ВЭБ.
Серологическими маркерами активной фазы ЭБВИ являются Ат IgM к VCA и Ат IgG к EA, низкая и средняя авидность Ат IgG к маркерам неактивной фазы, Ат IgG к EBNA.
Материалом для ПЦР служат кровь, ликвор, слюна, мазки со слизистой ротоглотки, биоптаты органов и др. Чувствительность ПЦР при ЭБВИ (70–75%) ниже, чем при других герпесвирусных инфекциях (95–100%). Это связано с появлением ВЭБ в биологических жидкостях лишь при иммуноопосредованном лизисе инфицированных В-лимфоцитов.
На основании опыта лечения 169 детей с ЭБВИ нами разработан стандарт лечения этого заболевания.
Базисная терапия: охранительный режим; лечебное питание; противовирусные препараты: вироцидные препараты — инозин пранобекс (Изопринозин), аномальные нуклеозиды (Валтрекс, Ацикловир), Арбидол; препараты ИФН — рекомбинантный ИФН α-2β (Виферон), Кипферон, Реаферон-ЕС-Липинт, интерфероны для в/м введения (Реаферон-EC, Реальдирон, Интрон А, Роферон А и др.); индукторы ИФН — Амиксин, сверхмалые дозы антител к γ-ИФН (Анаферон), Циклоферон, Неовир. По показаниям: локальные антибактериальные препараты (Биопарокс, Лизобакт, Стопангин и др.); системные антибактериальные препараты (цефалоспорины, макролиды, карбапенемы); иммуноглобулины для внутривенного введения (Иммуновенин, Габриглобин, Интраглобин, Пентаглобин и др.); витаминно-минеральные комплексы — Мульти-табс, Вибовит, Санасол, Киндер Биовиталь гель и др.
Интенсификация базисной терапии по показаниям:
Симптоматическая терапия.
При лихорадке — жаропонижающие препараты (парацетамол, ибупрофен и др.); при затруднении носового дыхания — назальные препараты (Изофра, Полидекса, Називин, Виброцил, Адрианол и др.); при сухом кашле — противокашлевые препараты (Глаувент, Либексин), при влажном кашле — отхаркивающие и муколитические препараты (АмброГЕКСАЛ, бромгексин, ацетилцистеин и др.).
Эффективность этиотропной терапии ОЭБВИ оценена в двух группах больных. Пациенты 1-й группы (52 человека) получали инозин пранобекс (Изопринозин) в сочетании с рекомбинантным ИФН α-2β (Вифероном), больные 2-й группы (57 детей) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Клинико-серологические показатели до начала лечения и через 3 мес терапии представлены в табл. 1. У пациентов обеих групп в динамике отмечалось достоверное уменьшение таких симптомов, как генерализованная лимфаденопатия, тонзиллит, аденоидит, гепатомегалия и спленомегалия. Вместе с тем на фоне комбинированной терапии, положительная динамика клинических показателей была более значительной; острые респираторные инфекции (ОРИ) лишь у 19,2% больных 1-й группы и у 40,3% больных 2-й группы (p < 0,05). На фоне комбинированной терапии наблюдалось более быстрое исчезновение серологических маркеров репликации.
Эффективность этиотропной терапии исследована у 60 больных ХЭБВИ. Пациенты 1-й группы (30 детей) получали инозина пранобекс (Изопринозин) и рекомбинантный ИФН α-2β (Виферон), 2-я группа (30 человек) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Независимо от схемы лечения через 3 мес после начала терапии отмечалось достоверное уменьшение частоты генерализованной лимфаденопатии, гипертрофии небных и глоточной миндалин, спленомегалии, интоксикационного, инфекционного и вегето-висцерального синдромов (табл. 2). Комбинация инозина пранобекса (Изопринозина) с рекомбинантным ИФН α-2β (Вифероном) способствовало более существенной динамике клинических показателей. Количество эпизодов ОРИ снизилось с 6–11 (7,9 ± 1,1) до 4–6 (5,2 ± 1,2) в год на фоне монотерапии рекомбинантным ИФН α-2β (Вифероном), и до 2–4 (2,5 ± 1,4) в год на фоне комбинированной терапии (p < 0,05). В обеих группах уменьшалась частота репликации ВЭБ, однако при сочетанном применении противовирусных препаратов этот эффект был более выраженным.
Побочных эффектов при использовании инозина пранобекса (Изопринозина) и рекомбинантного ИФН α-2β (Виферона) не было.
Результаты проведенного исследования свидетельствуют о потенцировании эффектов при комбинации инозина пранобекса (Изопринозина) с рекомбинантным ИФН a-2b (Вифероном) у больных ЭБВИ.
Потенцирование противовирусных, иммуномодулирующих и цитопротекторных эффектов этих препаратов приводит к более существенной, чем при монотерапии, положительной динамике проявлений клинических симптомов ЭБВИ, к исчезновению серологических маркеров активности инфекционного процесса. Следует отметить высокую эффективность и безопасность комбинированной терапии с использованием инозина пранобекса (Изопринозина) и рекомбинантного ИФН α-2β (Виферона).
Реабилитация. Ребенок наблюдается участковым врачом и инфекционистом, снимается с учета через 6–12 мес после исчезновения клинико-лабораторных показателей активности инфекционного процесса. Кратность осмотров — 1 раз в месяц. По показаниям рекомендуют консультацию ЛОР-врача, иммунолога, гематолога, онколога и др. Лабораторные и инструментальные исследования пациентов включают: клинический анализ крови 1 раз в месяц в течение 3 мес, затем 1 раз в 3 месяца, по показаниям — чаще; серологические маркеры ВЭБ методом ИФА один раз в три месяца, по показаниям — чаще; ПЦР крови, мазков из ротоглотки 1 раз в 3 месяца, по показаниям — чаще; иммунограмма — 1 раз в 3–6 мес; биохимическое и инструментальное исследования — по показаниям.
Реабилитационная терапия включает: охранительный режим, лечебное питание, противовирусные препараты по пролонгированным схемам. Под контролем иммунограммы осуществляют иммунокоррекцию. По показаниям назначают локальные антибактериальные препараты, курсы витаминно-минеральных комплексов, про- и пребиотиков, препаратов метаболической реабилитации, энтеросорбентов, антигистаминные препараты, гепато-, нейро- и ангиопротекторы, кардиотропные препараты, ферменты, гомеопатические средства, немедикаментозные методы лечения.
Таким образом, ЭБВИ характеризуется широким распространением, длительным течением с периодической реактивацией инфекционного процесса у части пациентов, возможностью развития осложнений и неблагоприятных исходов (онкозаболеваний, аутоиммунной патологии). Важную роль при ЭБВИ играет формирование вторичного ИДС. Ведущими клиническими синдромами ЭБВИ являются острый и хронический мононуклеозоподобный синдромы, интоксикационный, инфекционный, церебральный, гастроинтестинальный, кардиальный и артралгический синдромы. Диагностика ЭБВИ основана на анализе групп риска, выделении ведущих клинических синдромов и лабораторном исследовании. Лечение ЭБВИ является комплексным и включает этиотропные средства (виростатические препараты, интерферон и его индукторы), препараты патогенетической, иммуномодулирующей, симптоматической терапии. Сочетанное пролонгированное использование инозина пранобекс (Изопринозина) и рекомбинантного ИФН α-2β (Виферона), потенцирующих свои иммунокорригирующие и цитопротекторные эффекты, существенно повышает эффективность лечения. Больные ЭБВИ нуждаются в длительной реабилитации с обязательным контролем клинико-лабораторных показателей активности инфекционного процесса.
По вопросам литературы обращайтесь в редакцию.
Э. Н. Симованьян, доктор медицинских наук, профессор
В. Б. Денисенко, кандидат медицинских наук
Л. Ф. Бовтало, кандидат медицинских наук
А. В. Григорян
Ростовский ГМУ, Ростов-на-Дону

Вирус Эпштейна-Барр (ВЭБ) — ДНК-геномный герпесвирус человека из подсемейства Gammaherpesviridae. Он проявляет тропность к В-лимфоцитам (через специфический рецептор CD-21) и эпителиальным клеткам, а также онкогенные свойства.
Источником является больной человек. Пути заражения — воздушно-капельный (в подавляющем большинстве случаев), трансплацентарный, гемотрансфузионный.
Один из самых распространенных вирусов: инфицированность взрослого мирового населения составляет более 90 % и почти не варьируется в зависимости от этноса, условий жизни, доступности медицинской помощи и т. д.
Клинические проявления ВЭБ-инфекции различны. При заражении в раннем детском возрасте клиника может быть стертой, а при заражении в школьном и подростковом возрасте обычно развивается симптомокомплекс инфекционного мононуклеоза (ИМ): фебрильная лихорадка, тонзиллит, лимфаденопатия, гепатоспленомегалия и появление в крови атипичных мононуклеаров.
Этиологическую диагностику Эпштейна-Барр инфекции и оценку ее активности проводят при помощи определения антител к раннему антигену ЕА, к ядерному антигену VCA, EBNA, антител к EBV классов IgG и IgM, серологического профиля (IgMEA-IgG/EBNA-IgG), и, конечно, определения ДНК вируса методом ПЦР в слюне, сыворотке крови и ЦСЖ больного; согласно последним данным, серологические реакции Пауля-Буннеля, Томчика, Ловрика и т. д. показывают до 30 % ложноположительных реакций у лихорадочных больных, а потому их применимость сомнительна.
Если говорить о неврологических проявлениях ВЭБ-инфекции, то и этот список выглядит не менее впечатляющим: энцефалит, энцефаломиелит, поперечный миелит, асептический менингит, острая церебеллярная атаксия, синдром Алисы в стране чудес (аутометаморфопсия), синдром Гийена-Барре. Также доказана роль ВЭБ в развитии острого рассеянного энцефаломиелита, но для его развития могут послужить и другие инфекционные агенты.
Поражение центральной и периферической нервной систем при ВЭБ-инфекции может проявиться как на фоне симптомов мононуклеоза, так и изолированно, и протекать как в острой, так и в хронической форме.
Однако в процентном соотношении поражение ЦНС при мононуклеозе — явление нечастое, и выявляется примерно в 1 % случаев клинически явного ИМ.
Эпштейн-Барр энцефалит у иммунокомпетентных пациентов.
Клиническая картина
Типично развивается на фоне инфекционного мононуклеоза, чаще всего — на 3–7 день болезни. Специфические (исключая симптомы, и так характерные для ИМ) признаки включают в себя фокальные и генерализованные судорожные приступы, вплоть до развития эпилептического статуса, очаговые неврологические дефициты (обычно в виде слабости/спастичности в конечностях, атаксии, асимметрии рефлексов, нарушений слуха и зрения).
Возможно развитие симптоматики энцефалита или энцефаломиелита вне картины инфекционного мононуклеоза, в том числе у людей, перенесших ИМ в прошлом, как проявление реактивации латентной инфекции
Проведя ЭЭГ, можно увидеть диффузное или фокальное замедление ритма, эпилептиформные паттерны, или, в части случаев — нормальную картину.
Лучевые признаки
Радиологические проявления вариабельны (и также могут отсутствовать при наличии клиники). Методом выбора является МРТ.
Сигнальные характеристики энцефалитических очагов те же, что и при энцефалитах другой этиологии:
- одним из лучевых паттернов ВЭБ-энцефалита является симметричное поражение подкорковых структур: таламусов, базальных ядер, островковой доли
- симметричное или асимметричное поражение гиппокампов, коры височных и (реже) теменных областей, ножек мозга, понтинных структур, гемисфер мозжечка
- поражение структур ствола и спинного мозга (иногда в виде поперечного миелита).

Рисунок 1 | A. T1ВИ не выявляет никаких аномалий. B. T2-взвешенное изображение демонстрирует высокую интенсивность сигнала от валика мозолистого тела. С. последовательность FLAIR определила дополнительные области высокого сигнала в задних отделах обоих полушарий. D. все выявленные очаги демонстрировали повышение сигнала на DWI. Е. карта ИКД подтвердила ограничение диффузии в только в валике мозолистого тела. F. на постконтрастном T1ВИ не обнаруживается областей контрастного усиления.
Рисунок 2 | 5-летний мальчик с лихорадкой, судорогами и изменением психического статуса. Аксиальное FLAIR изображение показывает симметричные области гиперинтенсивного сигнала и признаки отека паренхимы мозга в области стриатума с вовлечением наружной капсулы (большие стрелки) и правой поясной извилины (маленькая стрелка).
Рисунок 3 | На аксиальном FLAIR изображении определяется аномально высокий МР-сигнал от тел хвостатых ядер, а также области поражения коры и субкортикального белого вещества головного мозга (стрелки).
Рисунок 4 | Мужчина 43 лет с синдромом приобретенного иммунодефицита, слабостью в нижних конечностях и расстройством мочеиспускания. МР-томограмма поясничного отдела позвоночника после введения контраста определила область гиперинтенсивного в Т2-взвешенных последовательностях сигнала от спинного мозга на уровне Th11–Th12 (миелит).
Поражения вирусом Эпштейна-Барр гематологических больных - диагностика, лечение
Вирусом Эпштейна — Барр (ЭБВ) инфицировано не менее 95 % взрослого населения во всех странах. У большинства людей первичная ЭБВ-инфекция протекает субклинически, а у меньшинства в виде инфекционного мононуклеоза. Случаи летального фульминантного мононуклеоза очень редки и чаще встречаются в группе больных одной из форм врожденного иммунодефицита — Х-сцепленным лимфопролиферативным синдромом (Х-ЛПС, или синдром Пуртильо). Главная особенность при это синдроме — отсутствие способности ограничивать пролиферацию ЭБВ-инфицированных В-лимфоцитов.
Второе по частоте проявление первичной ЭБВ-инфекции у больных с этим синдромом — лимфома Беркитта и, реже, лимфома Ходжкина. Соответственно у всех мальчиков с фульминантным мононуклеозом и семейными случаями лимфом Беркитта и Ходжкина необходимо заподозрить Х-ЛПС.
Резервуаром вируса Эпштейна — Барр (ЭБВ) являются В-лимфоциты и эпителиальные клетки слизистой оболочки носоглотки. Пожизненное латентное состояние вируса поддерживается цитотоксическими ЭБВ-специфическими Т-лимфоцитами, которые составляют около 1 % от всех циркулирующих лимфоцитов крови. При развитии длительного и глубокого дефицита Т-лимфоцитов возможна пролиферация ЭБВ-инфицированных В-лимфоцитов. Это состояние, описанное в конце 70-х годов XX в. у больных реципиентов донорской почки, названо В-клеточным лимфопролиферативным синдромом (В-ЛПС). Любая аллогенная трансплантация (почки, печени, сердца, легких, ГСК) может осложниться В-ЛПС.
Среди гематологических больных наивысший риск развития В-ЛПС отмечается у реципиентов аллогенного костного мозга, хотя отдельные случаи описаны после аутологичных трансплантаций и у реципиентов иммуносупрессивной терапии.
Риск развития В-ЛПС у реципиентов ТГСК оценивается как 1 % в течение 10 лет. В течение 1-го года он составляет 120 случаев на 10 000 пересадок и лишь 5 на 10 000 в последующие годы. Факторами риска развития В-ЛПС являются причины, способствующие возникновению или поддержанию Т-иммунодефицита.
Для клинической картины В-ЛПС характерны увеличение лимфатических узлов, печени, селезенки, высокая лихорадка и инфильтрация нелимфоидных органов. Вовлечение серозных оболочек приводит к развитию полисерозитов с массивными плевральными, перикардиальными выпотами и асцитом. При поражении лимфатических узлов средостения на первый план выступает синдром компрессии: нарушение притока крови к правому предсердию, сдавление трахеи. Нередко, как и при других В-клеточных пролиферациях у больных с Т-клеточным иммунодефицитом, при ЭБВ-ЛПС поражается ЦНС. Известны случаи развития тяжелого гемофагоцитарного синдрома в финальной стадии В-ЛПС.
Для лабораторной картины характерны наличие высокого моноклонального пика иммуноглобулинов класса М или G в сыворотке крови и подъем ЛДГ. Дискордантное восстановление репертуара В-лимфоцитов после аллотрансплантации иногда и в норме приводит к появлению высоких моноклональных пиков иммуноглобулинов, не связанных с В-ЛПС. Другие лабораторные признаки еще менее специфичны.
Патологическим субстратом при В-ЛПС являются ЭБВ-трансформированные В-лимфоциты, которые в подавляющем большинстве случаев имеют донорское происхождение. В связи с этим для профилактики В-ЛПС донорского происхождения на ранних стадиях после трансплантации гемопоэтических стволовых клеток (ТГСК) достаточно высокодозного миелоаблативного кондиционирования перед ТКМ, вызывающего глубокое истощение пула В-клеток донора.
Морфологически в отличие от реципиентов солидных органов, В-ЛПС которых имеют морфологию полиморфных крупноклеточных лимфом, В-ЛПС у реципиентов ТГСК примерно в половине случаев имеют морфологию иммунобластных лимфом. Еще одним отличием является олиго- или моноклональность В-ЛПС у реципиентов аллогенной ТКМ, хотя иногда удается проследить становление истинной моноклональной опухоли через стадии поликлональной и олигоклональной лимфопролиферации.
Интересно, что на стадии полиморфной лимфомы моноклональность обнаруживается менее чем в половине случаев, а при иммунобластных лимфомах — практически в 100 %.
Основными факторами риска развития В-ЛПС являются следующие: Т-деплеция трансплантата, лечение или профилактика РТПХ анти-CD3-моноклональными антителами, лечение или профилактика РТПХ антитимоцитарным глобулином, неродственный или родственный неполностью совместимый донор.
Самый высокий риск развития В-ЛПС, составляющий 64,8 ± 17,7 % через 4 года после трансплантации, присущ детям с тяжелыми комбинированными иммунодефицитными синдромами, получивших Т-деплетированный трансплантат от гаплоидентичного донора, тогда как у больных ТКИН, получивших HLA гено- или феноидентичный трансплантат без Т-деплеции, риск составляет 0,9 ± 0,2 %. Среди реципиентов неродственных трансплантаций с Т-деплецией частота посттрансплантационных В-ЛПС равна 5 %, без Т-деплеции — 1 %. Метод Т-деплеции значительно влияет на вероятность развития В-ЛПС.
В прошлом диагностика В-ЛПС основывалась на характерной патоморфологической картине биоптатов лимфатических узлов и пораженных органов и демонстрации наличия ДНК Эпштейна-Барр вируса (ЭБВ) в клетках опухоли. Важным лабораторным ориентиром служит появление моноклонального пика в глобулиновой фракции. Все эти данные являются, однако, поздними маркерами, которые констатируют заболевание на этапе, когда любая терапия малоэффективна. В настоящее время разработаны полуколичественные и количественные методы мониторинга ДНК Эпштейна-Барр вируса (ЭБВ) в крови, которые позволяют на ранних стадиях оценить риск развития В-ЛПС и назначить упреждающее лечение.
При исследовании частоты реактивации Эпштейна-Барр вируса (ЭБВ) в течение 180 дней после аллогенной ТГСК методом измерения количества копий ДНК Эпштейна-Барр вируса (ЭБВ) в крови выяснилось, что частота реактивации (количество копий генома в 1 мл крови более 50) составляет 39 % после трансплантации нативных ГСК и 65 % после Т-деплетированных трансплантаций. Среди больных, у которых количество копий генома Эпштейна-Барр вируса (ЭБВ) оказалось более 1000 в 1 мл, частота В-ЛПС составила 39 %, в то время как ни у кого из больных с показателем менее 1000 копий в 1 мл не развивался В-ЛПС. Таким образом, количественный мониторинг концентрации вирусной ДНК позволяет выявить популяцию высокого риска развития В-ЛПС. Возможно, что мониторинг вирусной ДНК не в цельной крови, а в плазме является еще более эффективным и специфичным методом ранней диагностики В-ЛПС.
Лечение уже развившегося В-ЛПС представляет сложную задачу. Химиотерапия и а-интерферон не показали воспроизводимой эффективности после ТГСК, хотя после трансплантации солидных органов их эффективность может быть выше, чем после ТГСК. Эпштейна-Барр вирус (ЭБВ) нечувствителен к ингибиторам тимидинкиназы типа ганцикловира и ацикловира, в то время как сидофовир может быть эффективен. Редукция иммуносупрессии, которая может быть предпринята после трансплантации солидных органов, чаще всего невозможна у реципиентов аллогенных ТГСК, поскольку может привести к вспышке РТПХ, которая, помимо того, что сама по себе может вызвать смерть пациента, способствует резкому усугублению иммунодефицита.
Несомненно, что в настоящее время мониторинг реактивации Эпштейна-Барр вируса в популяциях высокого риска и упреждающее лечение ритуксимабом являются методами выбора контроля В-ЛПС. Другой эффективный метод лечения В-ЛПС — клеточная терапия. Инфузии нативных донорских лимфоцитов в дозе более 1 * 106/кг высокоэффективны, однако чреваты высокой частотой развития тяжелой РТПХ. В некоторых самых передовых центрах используется введение ЭБВ-специфических Т-лимфоцитов донора, генерированных in vitro. Эффективность данного метода приближается к 80—90 %. Понятно, что клеточные технологии требуют высокого технологического уровня и доступны далеко не везде.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

