Псориатический артрит и гепатит с
Обновлено: 25.04.2024
Человек постоянно контактирует с окружающей средой, а значит и с населяющими ее микроорганизмами, многие из которых являются патогенными, способными вызвать воспалительный процесс. Инфекционный артрит развивается при попадании инфекции в сустав. Предупредить тяжелые осложнения этого заболевания может только своевременное обращение за медицинской помощью.
Общие сведения о заболевании
Инфекционный артрит – это воспаление сустава, вызванное местной или общей инфекцией. Симптомы болезни и ее течение во многом зависят от вызвавшей инфекционный процесс инфекции.
Коды инфекционных артритов по МКБ-10:
- стафилококковый - M00.0;
- пневмококковый - M00.1;
- стрептококковые - M00.2;
- вызванные другими уточненными бактериальными возбудителями - M00.8;
- пиогенный неуточненный - M00.9;
- туберкулезный – М01.1;
- гонококковый - M01.3;
- вирусный – М01.5.
Заболевание очень распространено и может стать причиной стойкого нарушения суставной функции. Четверть пациентов, обращающихся по поводу заболеваний суставов, страдают инфекционными артритами.
Причины инфекционного артрита
Причиной заболевания является инфекция – гнойная инфекция из расположенных рядом очагов (флегмон, абсцессов) или занесенная с током крови при холециститах тонзиллитах, а также общие инфекционные заболевания. При попадании инфекционных возбудителей в сустав иммунная система начинает с ними бороться, вызывая воспалительный процесс, течение которого напрямую связано с особенностями инфекционного возбудителя.
Воспаление может быть:
- неспецифическим – то есть, иметь общие симптомы, характерные для воспалительных процессов; вызываются такие процессы гноеродной патогенной и условно-патогенной микрофлорой – стафилококками, стрептококками, синегнойной и кишечной палочками и др.; вызываемые ими воспалительные процессы носят обычно острый гнойный характер и протекают остро, особенно, у детей;
- специфическим – при таком воспалении развиваются, как общие симптомы, характерные для всех артритов, так и симптомы, свойственные данной инфекции; к таким инфекциям относят туберкулезный, бруцеллезный, гонорейный, вирусный, грибковый, паразитарный воспалительные процессы.
Инфекционные артриты имеют два механизма развития:
- бактериально-метастатический – воспаление начинается из-за присутствия в суставе инфекции;
- токсико-аллергический – воспаление развивается за счет общей интоксикации и неадекватного иммунного ответа на внедрение в организм инфекции;
- смешанный – действуют оба механизма.
Факторы, предрасполагающие к развитию инфекционного артрита: вредные привычки, поднятие тяжестей, наличие лишней массы тела, сахарного диабета. Гнойные поражения суставов особенно часто развиваются у женщин, страдающих ревматоидным артритом.
Симптомы инфекционного атрита
Инфекционный артрит обычно начинается и протекает остро, иногда подостро. Но при некоторых специфических инфекциях он имеет незаметное начало и длительное течение.
Начало болезни и первые симптомы
При остром начале основными симптомами инфекционного артрита являются: выраженная лихорадка, озноб, летучие мышечно-суставные боли в сочетании с резкой болезненностью в пораженном суставе, отеком и гиперемией кожи над ним. Практически всегда остро протекает инфекционный артрит у детей.
Подострое течение имеет не такое заметное начало, температура тела нормальная или субфебрильная. Отек, гиперемия и боль в суставах умеренные.
Самым опасным является скрытое, незаметное течение, характерное для туберкулезного артрита. Характерны неопределенные боли в суставах, похрустывание, снижение двигательной активности. Болезнь протекает на фоне туберкулеза, небольшое повышение температуры также может не привлечь внимания, поэтому туберкулезный артрит редко выявляется на ранних стадиях.
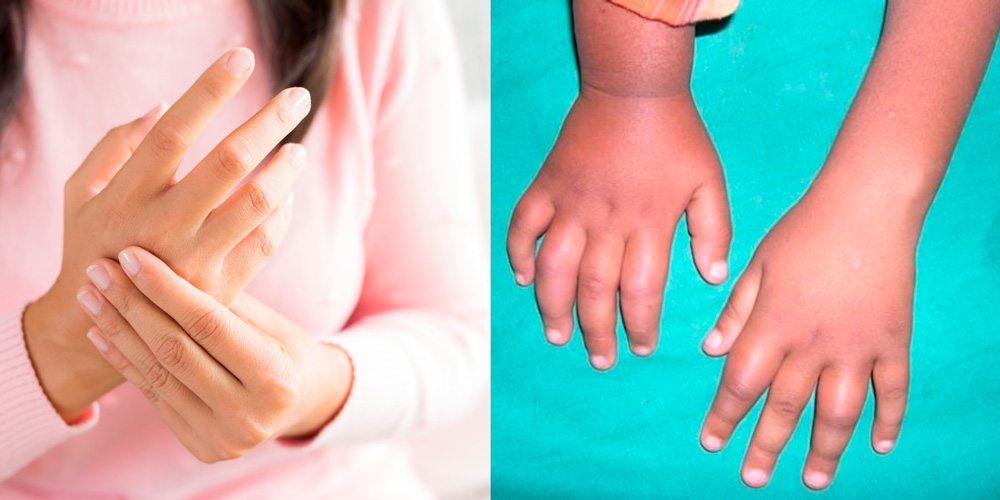
Боли и и отеки характерны для начальной стадии инфекционного токсико-аллергического артрита у детей и взрослых
Явные симптомы
Острый гнойный артрит развиваются очень быстро, состояние ухудшается с каждым днем, беспокоит лихорадка, отечность, гиперемия и боль нарастают. Не исключено, что больному потребуется хирургическая помощь.
При более медленном течении симптомы инфекционного артрита развиваются постепенно, появляется общее недомогание, слабость, суставные боли становятся постоянными, усиливаясь при движении. Постепенно нарушается функция конечностей: появляются трудности в их сгибании или разгибании.
Когда необходимо обращаться за медицинской помощью
К врачу нужно обращаться при появлении следующих симптомов:
- постоянных или регулярно повторяющихся болях в суставах;
- появлении лихорадки, недомогания в сочетании с болями в суставах;
- отека, гиперемии кожи над суставом в сочетании с лихорадкой у пациентов, уже страдающих хроническим артритом – возможно, к имеющемуся хроническому воспалению присоединилась инфекция;
- появление суставных болей при туберкулезе легких, гонорее, бруцеллезе и др. инфекционных заболеваниях.
Опасности
Заболевание часто протекает тяжело, с осложнениями.
Стадии заболевания
Течение болезни связано с ее клинической формой, поэтому стадии развития патологического процесса могут иметь значительные различия. Рассмотрим стадии развития острого гнойного артрита, разработанные НИИ им. Вишневского:
- Начальная – гнойный процесс без деструкции внутрисуставных тканей:
- А. - без поражения околосуставных тканей;
- В. – с развитием гнойных процессов в прилегающих тканях.
- Развернутая – гнойный артрит с деструкцией внутрисуставных тканей:
- А. - без поражения околосуставных тканей;
- В. – с гнойным поражением окружающих мягких тканей.
- Запущенная – с поражением костной и хрящевой ткани:
- А. - без поражения окружающих тканей;
- В. – с гнойным поражением данных тканей;
- С. – с выходом гноя на поверхность тела (свищами).
- Завершающая:
- при отсутствии адекватного лечения – деструкция, неподвижность сустава, инвалидизация;
- при правильном лечении – полное или частичное восстановление функции конечности.
Возможные осложнения
Инфекционный артрит может давать ранние и поздние осложнения. К ранним осложнениям относятся в основном осложнения гнойного артрита:
- нагноение околосуставных тканей;
- генерализация инфекции, сепсис.
Отдаленные последствия – это утрата функции конечности разной степени: от легкой до полной неподвижности.
Классификация
Происхождение и симптомы инфекционного артрита разных клинических форм имеют, как сходство, так и отличие. Рассмотрим наиболее распространенные формы.
Острый гнойный
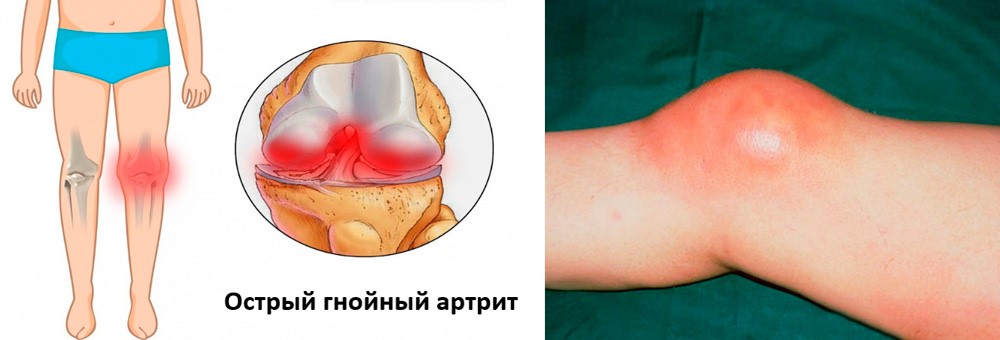
Острый гнойный артрит коленного сустава
Данная форма заболевания развивается при попадании в сустав гноеродной инфекции (синегнойной палочки, стафилококков, стрептококков и др.). Заражение может быть первичным при ранениях и вторичным – при переходе инфекции из окружающих тканей или отдаленных очагов инфекции. К группе риска относятся лица, страдающие ревматоидным артритом, особенно, женщины.
Начинается заболевание остро и протекает тяжело. Появляется лихорадка, головная боль, озноб. Пораженный сустав отекает, кожа над ним краснеет. Боль настолько сильная, что больной не может пошевелить конечностью и старается придать ей положение, вызывающее наименьшую болезненность.
Без оказания своевременной помощи суставные поверхности быстро разрушаются с ограничением подвижности конечности. При назначении адекватного лечения наступает полное выздоровление.
Септический
Развивается на фоне уже существующего сепсиса – генерализованного инфекционного процесса. Инфекция попадает в суставную полость гематогенным путем - с током крови. Заболевание может протекать в виде:
- бактериально-метастатической формы с симптомами острого гнойного артрита – состояние пациента может быть крайне тяжелым; прогноз заболевания зависит от своевременного лечения;
- токсико-аллергической формы – течение не всегда имеет острый характер, часто протекает подостро с множественным поражением суставов мигрирующего (чередующегося) характера; процесс носит негнойный характер и заканчивается выздоровлением на фоне излечения сепсиса.
Туберкулезный
Артрит в данном случае также протекает в виде бактериально-метастатической и токсико-аллергической форм. В первом случае поражаются в основном позвоночник и крупные суставы конечностей, а заболевание носит название костно-суставного туберкулеза. Протекает изначально хронически с нарастающими болями при движении, общим недомоганием. Основные изменения видны на рентгене в виде поражения суставной костной ткани от появления пятна с утратой костью кальция до разрушения кости. При отсутствии лечения приводит к инвалидности.
Токсико-аллергическая форма впервые описанная Понсе в начале 20-го века, протекает очень похоже на ревматоидный артрит с хроническим началом и поражением мелких суставов кисти и стоп. Возможна также их деструкция и инвалидизация. Поражение крупных суставов иногда протекает без последствий и проходит на фоне противотуберкулезной терапии.
Хондропротекторы что это как выбрать, насколько они эффективны
Боль в суставах в состоянии покоя
Гонорейный
Поражение суставов гонококковой инфекцией может иметь бактериально-метастатическую и токсико-аллергическую формы. В обоих случаях поражаются крупные суставы, чаще всего один коленный (голеностопный, лучезапястный). Протекает болезнь остро, с высокой температурой, интоксикацией и сильнейшими суставными болями. Колено отекает, краснеет, до него невозможно дотронуться из-за болей.
При проведении своевременного лечения болезнь имеет благоприятный исход. Если же не лечить, быстро наступает полная неподвижность конечности.
Боррелиозный
Боррелиоз или болезнь Лайма – это инфекция, вызываемая спиралевидными бактериями – спирохетами боррелиями. Передается она клещами и протекает в виде последовательной смены стадий:
- Через 1-2 недели после укуса клеща появляются повышение температуры тела, интоксикация, скованность мышц и появление на теле в месте укуса клеща покраснения - эритемы, окруженной концентрическими кольцами, распространяющейся на большие участки тела. При своевременном назначении антибактериальной терапии заболевание может закончиться на этой стадии.
- Развивается через 1 – 3 месяца после начала заболевания и проявляется в виде поражений нервной системы (менингитов, невритов с острыми болями) и сердца (сердечных блокад, миокардитов и др.).
- Поражение суставов начинается через полгода (иногда через 2 года) после начала заболевания у генетически предрасположенных людей и протекает в виде сильных суставных болей, доброкачественного рецидивирующего воспалительного процесса, протекающего по типу инфекционно-аллергического артрита с асимметричным поражением 1 – 2 суставов (чаще всего коленного) и заканчивающегося через несколько лет выздоровлением у большинства больных. Но у некоторых пациентов заболевание может переходить в хроническую форму с постепенным нарушением функции конечностей.
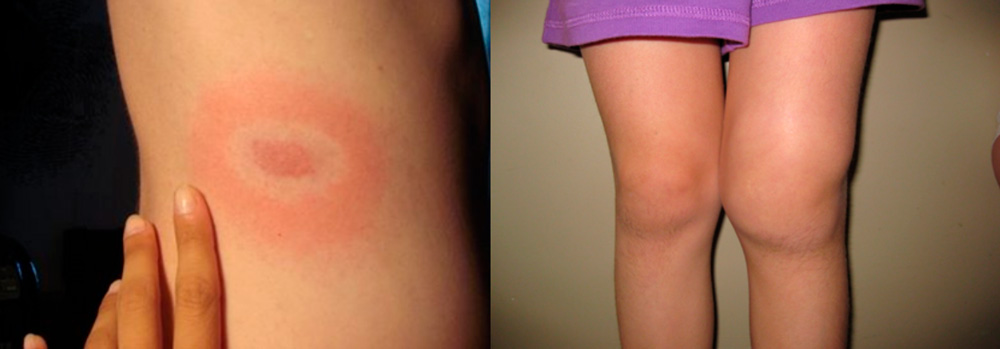
Начальная стадия боррелиоза – мигрирующая эритема и 3 стадия - хронический артрит колена
Вирусный
Развивается на фоне различных вирусных заболеваний:
- Парвовирусная инфекция, вызванная парвовирусом B19 – заболевание протекает с интоксикацией, лихорадкой, кожными проявлениями в виде красных пятен, возвышающихся над кожей папул и точечных подкожных кровоизлияний. Одновременно происходит симметричное поражение суставов. Могут вовлекаться мелкие суставчики кисти, лучезапястные, локтевые, коленные, голеностопные суставы. Симптомы похожи на ревматоидные поражения, но протекают от 3 месяцев до года и имеют благоприятный исход.
- Краснуха – артрит развивается чаще у взрослых женщин на фоне уже имеющихся симптомов краснухи или перед их появлением. У детей такие поражения встречаются редко. Околосуставные ткани отекают, краснеют, появляются сильные боли, нарушающие суставную функцию. Поражение асимметричное с вовлечением мелких суставов кисти, лучезапястных, коленных, локтевых суставов. Артрит продолжается две-три недели, после чего наступает полное выздоровление.
- Вирусные гепатиты В и С – артриты развиваются достаточно часто, но имеют доброкачественное течение и заканчиваются полным выздоровлением. Поражаются мелкие суставы кисти, локтевые, голеностопные и реже другие суставы. Воспаление в суставах обычно начинается до появления желтухи и заканчивается в период ее разгара.
Грибковый
Чаще всего грибковые поражения суставов развиваются при актиномикозе, но встречаются и при другой грибковой инфекции. Патогенные грибки попадают в суставную полость из расположенного рядом костного очага поражения или из отдаленных очагов (кариозные зубы) с током крови. Течение хроническое, с рецидивами и возможным присоединением бактериальной инфекции. Очень часто возникают свищи – ходы, по которым гной из сустава выделяется на поверхность кожи. При отсутствии адекватного лечения приводит к постепенной утрате суставной функции.
Паразитарный
Причиной артрита обычно является эхинококкоз, поражающий костную ткань позвонков, костей таза и длинных костей конечностей. В суставах обычно развивается токсико-аллергический воспалительный процесс. Часто вовлекаются суставы позвоночника, тазобедренные, коленные и локтевые суставы. Течение доброкачественное, но сопровождается сильными суставными болями. Выздоровление наступает при назначении полноценного лечения эхинококкоза.
Инфекционно-аллергический артрит
Инфекционно-аллергический артрит возникает, когда есть аллергия, на фоне которой развивается при неблагоприятных условиях воспалительный процесс в суставах. Заболевание протекает в бурной форме, сопровождается высокой температурой и сильными болевыми признаками. В области поражения наблюдается покраснение, отечность, припухлость. На разных участках кожи – кольцеобразная аллергическая сыпь. Лечением инфекционно-аллергического артрита занимаются ревматолог и аллерголог.
Локализация инфекционного артрита
При инфекционном поражении суставов локализация патологического процесса зависит от особенностей инфекции и ее клинической формы. При острых гнойных артритах – это в основном крупные суставы – коленный, голеностопный, локтевой. Мелкие суставы кисти и стопы поражаются при токсико-аллергической форме туберкулезного и некоторых вирусных артритах.
Асимметричное поражение одного-двух крупных суставов характерно для боррелиоза, чаще всего при этой инфекции в процесс вовлекаются коленные суставы.
В статье приводятся данные о нарушениях функции гепатобилиарной системы у больных псориазом. Раскрываются результаты проведенных исследований зарубежных и отечественных авторов, показавшие значимые связи наличия и тяжести поражения печени, билиарного трак
The article provides information about disorders of the hepatobiliary system in patients with psoriasis. The research results of foreign and domestic authors, which showed a significant correlation with the presence and severity of liver damage, biliary tract severity and clinical forms of psoriasis are described.
Псориаз — это иммуноассоциированный, генетически детерминированный, органоспецифический хронический эритематозно-сквамозный дерматоз многофакториальной природы. Характеризуется гиперпролиферацией эпидермальных клеток, нарушением процесса кератинизации, воспалительной реакцией в дерме и изменениями в различных органах и системах [1, 2]. Псориаз приводит к эмоциональной, социальной дезадаптации, а в ряде случаев к инвалидизации. Показатель заболеваемости псориазом на территории Российской Федерации составляет у взрослых 65,9 на 100 тыс. населения. Частота встречаемости псориаза в мире достигает от 2% до 5% всего населения. Наиболее часто псориаз регистрируется в Скандинавии и странах Северной Европы (3-5% от популяции). Средний уровень выявляется в Европе, США и России (1-3%). Низкий уровень встречаемости псориаза наблюдается у коренных северо- и латиноамериканских индейцев, монголоидных и западных африканцев (0-0,3%). У 25% больных псориазом заболевание сопровождается потерей или временной утратой трудоспособности. Псориазом одинаково часто болеют как мужчины, так и женщины. В детском возрасте заболевание несколько чаще встречается у девочек. Дебют заболевания наблюдается в любом возрасте. В целом чаще в третьей декаде жизни, хотя в последние годы нередки случаи диагностики псориаза у детей и даже младенцев [1].
В настоящее время псориаз рассматривается как системное заболевание с поражением не только кожных покровов, но и функциональных и морфологических нарушений других органов. Важное значение в поддержании и рецидивировании дерматоза придают нарушениям функции гепатобилиарной системы, поскольку патология печени и желчных путей может инициировать и усугублять выраженность эндотоксикоза, воспаления, иммунный дисбаланс, поддерживает нарушения процессов регенерации во всех системах в целом, в коже в частности [3]. К причинам развития псориаза относят и иммунологические нарушения, которые, как правило, возникают у лиц с генетической предрасположенностью к их развитию под воздействием провоцирующих факторов. Гены (PSORS 1 — PSORS 9), по отдельности или в комбинации, под воздействием инициирующего фактора способствуют развитию временных или стойких псориатических изменений кожи самых разных видов, степени выраженности и локализации [1, 4, 5]. Провоцирующими факторами риска могут быть инфекционные процессы (особенно вызванные стрептококками), травматизация кожи (парезы, царапины, ушибы и т. д.), избыточная инсоляция, токсические факторы (алкоголь, курение, наркотики, некоторые лекарственные средства: β-блокаторы, аминохинолиновые препараты, препараты лития, пероральные контрацептивы, интерфероны и т. д.), синдром отмены кортикостероидной терапии. Изменения клеточного метаболизма кератиноцитов и их патологическая пролиферация являются результатом структурно-органических нарушений, таких как метаболические нарушения (абдоминальное ожирение, инсулинорезистентность, сахарный диабет 2-го типа, нарушение липидного спектра, атеросклероз, гипертоническая болезнь); психические расстройства; болезни сердечно-сосудистой системы, где общие генетические факторы определяют высокий кардиоваскулярный риск; заболевания пищеварительной и особенно гепатобилиарной системы [1, 2, 6].
В последние годы у больных псориазом значимое внимание уделяется сопутствующей патологии неалкогольной жировой болезни печени (НАЖБП). НАЖБП в анамнезе у больных псориазом определяется как избыточное накопление триглицеридов в печени пациентов при отсутствии сопутствующих заболеваний [8]. По данным Национальной образовательной программы по холестерину, пациент подвержен метаболическому синдрому, если он имеет по крайней мере три из следующих критериев [9]:
- абдоминальное ожирение, определяемое как окружность талии ≥ 102 см у мужчин и ≥ 88 см у женщин;
- триглицериды в сыворотке крови ≥ 150 мг/дл;
- липопротеиды высокой плотности холестерина в сыворотке крови не более 40 мг/дл у мужчин и 50 мг/дл у женщин;
- артериальное давление более 130 мм рт. ст. (систолическое) и 85 мм рт. ст. (диастолическое);
- уровень глюкозы в сыворотке крови натощак более чем 100 мг/дл.
Неалкогольная жировая болезнь печени в настоящее время является наиболее распространенным хроническим заболеванием печени, достигая 10-25%, особенно у тучных людей [10]. Известно, что метаболический синдром чаще связан с псориазом и НАЖБП, которые могут присутствовать у одного пациента одновременно [11]. НАЖБП может включать разнообразные поражения печени, начиная от относительно доброкачественного стеатоза, состоящего из жировой инфильтрации, безалкогольного стеатогепатита с жировой инфильтрацией, лобулярного воспаления до цирроза печени и гепатоцеллюлярной карциномы [12].
Наиболее часто встречаемые у больных псориазом неблагоприятные факторы, способствующие повреждению печени, включают окислительный стресс внутри клеток печени, инсулинорезистентность, выброс токсичных воспалительных белков тучными клетками и цитокинами. В жировой ткани инсулин способствует этерификации свободных жирных триглицеридов и хранению жира. Когда развивается инсулинорезистентность, свободные жирные кислоты смещаются в такие нежировые ткани, как печень. Кроме того, печеночный липогенез и активация профиброзных цитокинов опосредует гиперинсулинемия [13]. Накопление ТГ в печени приводит к развитию окислительного стресса, липотоксичности и, следовательно, к митохондриальной дисфункции, которые представляют собой дальнейшее повреждение печени [14].
Последние данные зарубежных исследователей показали, что НАЖБП может быть связана с повышенным риском сердечно-сосудистых заболеваний независимо от традиционных факторов риска [15]. Дислипидемический профиль предшествует развитию псориаза. Повышенные уровни липопротеидов низкой плотности и снижение уровня холестерина, липопротеидов высокой плотности коррелируют с ишемической болезнью сердца и смертностью от сердечно-сосудистых заболеваний [16]. Недавно проведенные исследования направлены на возможную связь между псориазом, ожирением и метаболическим синдромом, являющимися известными факторами риска для НАЖБП [17].
Известно, что в возрасте после 40 лет пациенты с псориазом имеют более высокую распространенность метаболического синдрома и повышенный риск для каждого из компонентов метаболического синдрома [11, 18]. Также по данным A. Campanati с соавт. (2013) у пациентов с псориазом и НАЖБП отмечается увеличение риска развития псориатического артрита, что отражает активность провоспалительных цитокинов при обоих заболеваниях. Пациенты с псориазом с НАЖБП имеют значительное увеличение концентрации АСТ/АЛТ и показателей фиброза по сравнению с контрольной группой больных НАЖБП, не связанных с псориазом. Показатели АСТ/АЛТ стали независимыми прогностическими факторами фиброза печени у пациентов с НАЖБП [13]. Проведенные исследования ряда авторов показали, что риск тяжелого фиброза печени выше у пациентов с НАЖБП, коморбидных с псориазом, чем только у пациентов с НАЖБП. Эти два параметра считаются независимыми прогностическими факторами фиброза печени у пациентов с НАЖБП [20].
E. A. van der Voort с соавт. в 2013 г. проведено большое проспективное популяционное когортное исследование пациентов в возрастной группе от 18 до 55 лет. Среди участников исследования регистрировались 2292 (5,1%) пациента с псориазом. Частота встречаемости НАЖБП составила 46,2% у пациентов с псориазом по сравнению с 33,3% пациентов без псориаза [21]. По данным P. Gisondi (2009) из 130 обследованных человек признаки НАЖБП были обнаружены у 47% больных псориазом, в то время как у 260 обследованных контрольной группы — только у 28%. Больные псориазом с признаками НАЖБП имеют более высокий индекс тяжести псориаза PASI (14,2 против 9,6), в сравнении с пациентами с псориазом без признаков НАЖБП [22]. Пациенты с псориазом, метаболическим синдромом и НАЖБП показали более высокий уровень С-реактивного белка. Следует также отметить, что проявление НАЖБП может быть связано с нарушением циркуляции и транспортировки желчных кислот. В связи с этим можно констатировать, что имеющиеся болезни печени усугубляют течение псориаза и осложняют его лечение [20]. Результаты многочисленных исследований показывают, что на уровне таких неблагоприятных факторов, как потребление алкоголя, статус курения, нарушения показателей метаболического эквивалента Mets и аланинаминотрансферазы, псориаз остается значимым прогностическим параметром НАЖБП [22, 23].
Патогенез НАЖБП, как и псориаза, многофакторный и сложный. Стойкое хроническое воспалительное состояние может быть первичной связью между НАЖБП и псориазом. Известно, что псориаз и ожирение значимо связаны (ожирение предрасполагает к развитию псориаза, и псориаз увеличивает риск ожирения). Псориаз и НАЖБП также связаны с ожирением, которое в результате может способствовать развитию дальнейшего изменения показателей метаболического эквивалента Mets и сопутствующих заболеваний [23]. Накопление жировой ткани может привести к гипертрофии и гиперплазии адипоцитов вследствие воспалительного процесса, высвобождения провоспалительных хемокинов, а также вовлечения макрофагов, которые усиливают распространение воспалительного процесса в соседние адипоциты. Избыток жировой ткани приводит к дисбалансу между про- и противовоспалительными цитокинами и увеличению воспалительных компонентов, отвечающих за запуск стойкого воспаления. Адипоцитокины являются биологически активными молекулами, способными модулировать энергетический баланс, иммунитет, чувствительность к инсулину, ангиогенез, кровяное давление и липидный метаболизм путем аутокринной, паракринной и эндокринной систем. Кроме того, они играют решающую роль в патогенезе метаболического синдрома. Адипоцитокины фактора некроза опухоли α (ФНО-α), лептина, висфатина, резистина оказывают провоспалительный эффект, тогда как адипонектин обладает противовоспалительными свойствами. Производство адипонектина тормозится ФНО-α. Положительная корреляция между ФНО-α и индексом массы тела, а также их более высокие сывороточные уровни наблюдаются у пациентов с НАЖБП. ФНО-α играет ключевую роль в патогенезе псориаза: у больных значимо повышенное содержание ФНО-α в сыворотке крови положительно коррелирует с индексом тяжести псориаза PASI и негативно коррелирует с уровнем сывороточного адипонектина. При псориазе ФНО-α повышает пролиферацию кератиноцитов, производство провоспалительных цитокинов, сосудистых эндотелиальных клеток молекул адгезии, ангиогенеза. Происходит высвобождение ФНО-α, непосредственно участвуют макрофаги и липолиз, создавая порочный круг [24, 25].
В проведенном исследовании А. А. Иблияминовой (2011) у пациентов вне зависимости от степени тяжести заболевания установлена прямая корреляционная взаимосвязь индекса тяжести псориаза PASI и концентрации общего билирубина, активности щелочной фосфатазы в сыворотке крови, степени выраженности холестаза (г = 0,56-0,64 при р < 0,01), а также повышения литогенности желчи, определяемой по снижению холатохолестеринового и фосфолипидно-холестеринового коэффициентов (г = -0,55-0,52 при р < 0,05) [26].
По мнению ряда российских авторов, обычный псориаз, коморбидный с некалькулезным холециститом, имеет особенности в клиническом течении, нарушении пигментного обмена, ферментов сыворотки крови и метаболизме холестерина, фосфолипидов и холевой кислоты на печеночном уровне, что проявляется холестазом, более высоким литогенным потенциалом желчи. При снижении показателей коэффициентов литогенности холато-холестеринового коэффициента и фосфолипидно-холестеринового коэффициента пузырной желчи прогнозируют возможность нарушения коллоидного состояния желчи, ухудшающего течение билиарной патологии, обострение которой оказывает отрицательное влияние на псориатический процесс [27].
По данным Матусевича с соавт. (2000) хроническая эндотоксинемия при псориазе может приводить к функциональным нарушениям в работе печени, тяжесть которых зависит от ее уровня и длительности, а также от наличия сопутствующих заболеваний [28]. Органическая патология билиарного тракта и/или его функциональные расстройства отягощают течение псориаза, а степень холестаза коррелирует с величиной индекса тяжести псориаза PASI [22, 26].
По данным полученных результатов Л. П. Розумбаевой с соавт. у пациентов с распространенными формами псориаза высока частота неалкогольной жировой болезни печени, начальных признаков фиброза печени в сочетании с патологией билиарной системы. Патология билиарной системы разнообразна и характеризуется признаками дисфункциональных расстройств, симптомами бескаменной и желчнокаменной болезни. Установлены значимые связи наличия и тяжести поражения печени и билиарного тракта с клинической формой псориаза: при распространенном поражении кожи достоверно чаще встречаются признаки не только стеатоза, стеатогепатита, но и признаки продвинутого фиброза печени. Указанные обстоятельства необходимо учитывать при назначении терапии обострения распространенного псориаза, особенно при применении препаратов с потенциальным гепатотоксическим эффектом [3].
Таким образом, учитывая высокую распространенность сопутствующих функциональных расстройств патологии печени у пациентов с псориазом, патогенетическая роль патологии печени при псориазе не вызывает сомнений, и углубленное комплексное обследование нарушений функционального состояния гепатобилиарной системы у больных псориазом (ультразвуковое и биохимическое) позволит лучше понять роль и место этих нарушений в механизме псориаза и, возможно, разработать новые персонализированные подходы к терапии дерматоза, что в конечном итоге будет способствовать повышению качества жизни этих больных.
Литература
Л. А. Юсупова, доктор медицинских наук, профессор
Своеобразие псориатического артрита (ПА) состоит в сочетанном поражении суставов конечностей и позвоночника, большом разнообразии клинических симптомов, вариабельности начальных проявлений, серологической и рентгенологической негативности на ранних стадия
Своеобразие псориатического артрита (ПА) состоит в сочетанном поражении суставов конечностей и позвоночника, большом разнообразии клинических симптомов, вариабельности начальных проявлений, серологической и рентгенологической негативности на ранних стадиях. Являясь одной из форм заболевания суставов и позвоночника, ПА наряду с болезнью Бехтерева, болезнью Рейтера и другими реактивными артритами относится к группе серонегативных артритов [2, 17].
В основном заболевание начинается в возрасте от 20 до 50 лет, хотя нередки случаи ПА у детей. Бадокин В. В. (2005) указывает, что предикторами неблагоприятного течения ПА являются молодой возраст и мужской пол.
Причины развития ПА остаются невыясненными, среди факторов формирования можно выделить генетические, иммунологические и факторы внешней среды. Однако основой патогенетического механизма является активизация клеточного иммунитета у лиц с врожденной предрасположенностью. Участие иммунологических факторов в патогенезе ПА подтверждается обнаружением клеточных инфильтратов как в коже, так и в ткани пораженных суставов, отложением иммуноглобулинов в эпидермисе и синовиальной мембране. В сыворотке в первую очередь определяется повышение иммуноглобулинов класса А (Ig A) (у 90%) и G (IgG), циркулирующих иммунных комплексов (ЦИК), выявляются антитела к компонентам кожи и антинуклеарные антитела [2, 12, 18]. Достаточно отчетливы признаки нарушения не только гуморального, но и клеточного иммунитета (снижение ответа Т-лимфоцитов, уменьшение супрессорной клеточной функции). В настоящее время доказано, что в воспалительной реакции при псориазе ключевым моментом является экспрессия фактора некроза опухоли-a (ФНО-α) [2, 12, 17].
Нельзя не учитывать влияние таких факторов, как бактериальная, вирусная и другие виды инфекции (хламидийная и т. д.). В качестве патогенетических факторов обсуждается возможная роль в этиологии ПА инфекции, в том числе и вирусной [12, 14, 20]. Нередко наблюдается обострение или даже дебют ПА после травмы сустава [12, 14, 15].
Выраженность морфологических изменений при ПА зависит от локализации суставного процесса и длительности течения болезни. Доказано, что чем более выражен синовиит при ПА, тем более морфологически он отличается от ревматоидного артрита. Исходом заболевания может быть фиброзный и костный анкилоз. Продолжительная пролиферация приводит к костной деструкции, вызывая в конечном итоге формирование вновь образуемой кости и впоследствии извращенное ремоделирование сустава [3, 5, 7, 9, 10, 11, 12, 20].
При постановке диагноза ПА дерматологи чаще всего ориентируются на один-единственный признак — наличие псориатических высыпаний в сочетании с артритом. Однако ПА имеет свой характерный симптомокомплекс:
артрит дистальных межфаланговых суставов кистей (при дебюте ПА редко поражаются более крупные суставы);
поражение пястно-фалангового, проксимального и дистального межфаланговых суставов (осевое поражение);
Имеют значение асимметричность рентгенологической симптоматики, выраженные явления вторичного остеоартроза; кистовидные просветления в сочетании со склеротическими изменениями, очаговым уплотнением костной структуры, краевыми выростами. Характерная для ПА асимметричность поражения суставов может быть выражена не только в право- или левосторонности поражения, но и в степени пораженности суставов.
Степень выраженности ПА почти всегда коррелирует с тяжестью кожного процесса. Так, очаговый вульгарный псориаз обычно ассоциируется с развитием дистального или моноолигоартритического вариантов суставного синдрома и длительным сохранением функциональной способности опорно-двигательного аппарата. В то же время экссудативный и особенно атипичный дерматоз наиболее часто сопровождается развитием генерализованного артрита, остеолитического и спондилоартритического вариантов, быстропрогрессирующего течения. Что же касается злокачественной формы ПА, протекающей по типу псевдосепсиса с яркой общей и висцеральной патологией, то она встречается исключительно редко в случаях тяжелых форм псориаза с постоянно рецидивирующим течением.
Обострения ПА могут сопровождаться изменениями лабораторных показателей — ускоряется СОЭ (до 60 мм/час и более), развивается анемия (Нb до 50 г/л и ниже), резистентная к терапии. Возможна выраженная диспротеинемия с уменьшением альбуминов и гипергаммаглобулинемией (до 35% и более).
Обострение заболевания почти всегда сопровождается повышением температуры тела до фебрильной. Вместе со стиханием активности процесса и разрешением экссудативных явлений в суставах нормализуется и температура. Иногда, при злокачественных формах ПА, лихорадка носит интермитирующий характер, сопровождается ознобом и проливным потом, напоминая картину сепсиса.
Проблема дифференциальной диагностики ПА в настоящее время не утратила своей актуальности. Это объясняется тем, что ПА — заболевание чрезвычайно разнообразное по своим клиническим проявлениям и не всегда укладывается в разработанные критерии. Обязательно следует обращать внимание на признаки, не свойственные ПА:
Иногда дерматологи упускают из виду поражения позвоночника при ПА. Более чем у 50% больных псориазом спондилоартриты не диагностируются. Хотя наличие спондилоартрита и определенного сакроилеита является дифференциальным признаком ПА. Особенное значение это имеет у женщин в возрасте 20–30 лет при симметричном поражении проксимальных суставов кистей и стоп, когда усложняется дифференциальная диагностика ПА и ревматоидного артрита (РА). Дополнительным диагностическим признаком РА является положительная реакция Валера–Роузе. Из истории известно, что сначала спондилоартрит при псориазе диагностировался как атипичный вариант РА. Открытие ревматоидного фактора позволило выделить ПА как самостоятельное заболевание, а спондилоартрит при псориазе отнести к вторичным поражениям суставов.
Также к вторичным спондилоартритам относят синдром Рейтера, синдром Бехчета, артриты при неспецифическом язвенном колите и болезни Крона. Были отмечены некоторые характерные общие черты для всех заболеваний этой группы: инфекционный триггерный фактор, семейный анамнез, генетическая предрасположенность. Часто у одного больного можно найти клинические проявления ПА и болезни Рейтера, болезни Рейтера и воспалительных поражений кишечника (болезнь Крона, Уипля), острые кишечные инфекции и проявления болезни Рейтера.
Для болезни Бехтерева (анкилозирующий спондилоартрит) характерны:
ночные боли в покое, особенно во второй половине ночи и утром, часто сочетающиеся со скованностью и напряжением прямых мышц спины;
При объективном исследовании выявляется клинический синдром сакроилеита и нестойкий артрит, особенно суставов нижних конечностей; наличие белков острой фазы воспаления (повышение АЛТ, АСТ, общего белка, серомукоида, увеличение тимоловой пробы и т. д.); наличие антигена HLA-B-27; рентгенологические признаки поражения крестцово-подвздошных суставов (двусторонний сакроилеит) [8, 19].
Лечение
Лечение ПА должно быть направлено на решение следующих задач: уменьшение боли и воспаления, снижение частоты обострений и поражения новых суставов, улучшение качества жизни, замедление прогрессирования патологического процесса и предотвращение инвалидности. Таким образом, основываясь на патоморфологических изменениях в суставах при ПА и собственном опыте, лечение ПА должно быть длительным, комплексным, включающим наряду с противовоспалительной терапией, сосудистые средства, улучшающие микроциркуляцию, миорелаксанты, хондропротекторы; средства для лечения остеопороза; физиотерапевтические методы и реабилитационные мероприятия.
НПВП сходны по фармакологическим свойствам, биологической активности и механизмам действия, которые в первую очередь связаны с блокадой синтеза циклооксигеназы — ключевого бифункционального фермента, участвующего в регуляции синтеза простогландинов. Таким образом, они оказывают двойной эффект — устраняют боль и ослабляют воспалительный процесс. Без них трудно представить себе лечение ПА.
Объективные: эрозии и язвы, выявляемые с помощью эндоскопического (или рентгенологического) исследования.
Желательно, чтобы базисный препарат при лечении ПА, которым являются НПВП, соответствовал нескольким критериям: препарат должен давать клиническое и лабораторное улучшение, которое должно держаться некоторое время после его отмены, должен тормозить костную и хрящевую деструкцию и обладать меньшими побочными эффектами. Поэтому на современном этапе в медицине появилась новая серия препаратов: нимесулид, целекоксиб, лорноксикам, мелоксикам, инфликсимаб.
Нимесулид, целекоксиб, мелоксикам являются прямыми потомками НПВП, но только по одной линии: направленно действуют на ЦОГ-2, но не затрагивают ЦОГ-1. ЦОГ-1 конституциональный фермент, т. е. постоянно в норме функционирующий в организме, главным образом, влияет на продукцию простогландинов, которые защищают и регулируют нормальные клеточные процессы в ЖКТ и тромбоцитах. В результате, сохраняя лечебное действие, эти препараты не оказывают вредных эффектов на многие органы, в том числе и на желудок. Данные препараты снижают риск и частоту тяжелых поражений желудка — гастритов, язв и кровотечений. Особенно важно применение этих препаратов у больных пожилого и старческого возраста.
Инфликсимаб — относится к принципиально новой группе так называемых биологически активных препаратов иммуномодуляторов. Механизм их действия связан с антагонизмом одного из центральных медиаторов воспаления — ФНО-a. Препарат представляет собой химерные мышино-человеческие IgG1 моноклональные антитела, состоящие из высокоаффинных нейтрализующих мышиных моноклональных антител к ФНО-a и фрагмента молекулы IgGlk человека. Образует устойчивый комплекс как с растворимой, так и с мембран-ассоциированной формами человеческого ФНО-a, снижая его функциональную активность. Понижает концентрацию (связывает и ингибирует синтез) интерлейкина-1 (ИЛ-1); интерлейкина-6, интерлейкина-8 и других индукторов воспаления и тканевой деструкции. Инфликсимаб элиминируется из организма в течение 6 мес. Основными критериями выбора инфликсимаба для проведения терапии у конкретного больного являются: тяжелое течение псориаза, резистентного к обычной терапии, площадь поражения кожного покрова более 50%, продолжительность заболевания не менее 6 месяцев, тяжелый олиго- или полиартрит [13, 19, 20].
Возможно назначение комбинированного препарата диклофенака натрия (50 мг) и мизопростола (200 мкг). При этом мизопростол предупреждает негативное воздействие диклофенака на слизистую оболочку и развитие НПВП-гастропатии.
Хондропротекторы. Одним из патологических проявлений ПА является разрушение суставного хряща. Хрящ, подобно другим тканям, ремодулируется в течение роста и развития, иными словами, в нем происходят процессы синтеза и деградации. Напомним, суставной хрящ состоит из двух основных компонентов: межклеточного вещества (матрикса), составляющего 98% объема хрящевой ткани, и клеток: хондроцитов и хондроблатов (2%). Для целостности хряща в течение всей жизни необходимо, чтобы постоянный синтез гликозоаминогликанов, коллагенов и гиалуроновой кислоты был равен теряемому их количеству в результате естественного обмена. ИЛ-1 угнетает катаболизм матрикса [1]. Постоянный синтез гликозоаминогликанов и коллагена зависит от наличия таких веществ, но при очень малых количествах ИЛ-1 их активность угнетается. Воздействовать на хрящ можно на разных стадиях его поражения: первичная профилактика, скрининг асимптомной стадии и профилактическое лечение (например, при остеопорозе) или лечение уже развившейся болезни. Эффективность ряда препаратов из хондропротекторов уже доказана — это хондроитин сульфат, гликозамин сульфат, диацереин, натрия гиалуронат (содержит высокомолекулярную гиалуроновую кислоту), гиалуроновая кислота, вводимая внутрисуставно, и т. д. Следует обратить внимание, что в основном эти препараты являются биологически активными добавками. Отличительной особенностью данной группы препаратов является время наступления эффекта, обычно спустя 2–8 недель от начала лечения, и сохранение эффекта в течение 2–3 месяцев после прекращения терапии [1].
Лечение остеопороза. Для ПА характерно наличие остепороза метафизов. Количество потери костной массы увеличивается с возрастом больного и чаще встречается у лиц женского пола. Рентгенологические методы являются наиболее доступными и широко используются в клинической практике при исследовании костей. Однако при рентгенографии можно обнаружить наличие остеопении только при потере более 30% костной массы, поэтому этим методом чаще всего выявляются поздние признаки остеопороза. Современный метод измерения плотности костной ткани — денситометрия — основан на измерении минерального компонента костной ткани — кальция. Это наиболее чувствительный метод для выявления остеопороза и оценки степени его тяжести. Денситометрия необходима для подтверждения диагноза остеопороза, оценки риска переломов, а также контроля адекватности лечения. При выборе метода лечения остепороза должна быть твердая уверенность в его эффективности в плане предотвращения переломов и их последствий. Ожидаемый результат должен значительно перекрывать потенциальную опасность терапии, ассоциирующуюся с возможными побочными эффектами.
Физиотерапевтические методы и реабилитационные мероприятия. Немаловажным условием успеха лечения больных с ПА является также физиотерапия и комплексные реабилитационные мероприятия. Широко применяемые физиотерапевтические методы лечения ПА уменьшают болевой синдром, мышечный спазм, воспалительные процессы, улучшают микроциркуляцию и трофику, благоприятно воздействуют на метаболические процессы в тканях сустава.
Используют ультрафиолетовое облучение, электрическое поле УВЧ, переменные магнитные поля низкой частоты, электрофорез Анальгина, Новокаина, Тримекаина, Димексида на область пораженного сустава. В период стихания обострения, а также в начальной стадии заболевания, когда явления синовиита слабо выражены или отсутствуют, показаны воздействия электромагнитными полями высоких и сверхвысоких частот (индуктотермия, дециметровая и сантиметровая волновая терапия), импульсные токи низкой частоты — синусоидальные модулированные и диадинамические, магнитотерапия, лазерное воздействие, фонофорез гидрокортизона. Для стимуляции трофики суставного хряща проводят электрофорез лития, кальция, серы, цинка, Гумизоля.
Из различных физиотерапевтических методов хорошо зарекомендовал себя лекарственный электрофорез, сочетающий терапевтическое воздействие постоянного электрического тока и медикаментозного средства, вводимого с его помощью.
При ПА с болевым синдромом без клиники синовиита, пролиферативных явлениях, вазотрофических расстройствах, контрактурах показаны тепловые процедуры, включая аппликации парафина, озокерита, иловой, торфяной грязи. В стадии ремиссии эффективны морские, радоновые, сульфидные, йодобромные, бишофитные ванны. Не следует забывать о благоприятном воздействии на мышечно-суставную ткань лечебного массажа, который уменьшает мышечный спазм, повышает тонус ослабленных мышц, стимулирует трофику пораженных суставов и улучшает функциональные способности больного. Массаж, проводящийся вне обострения ПА, должен быть щадящим по отношению к пораженным суставам; необходимо избегать механического раздражения суставной капсулы; особое внимание следует обращать на работу с прилегающими к суставу мышцами.
По вопросам литературы обращайтесь в редакцию.
Ю. А. Галлямова, доктор медицинских наук, доцент
РМАПО, Москва
Приводятся сведения о псориатическом артрите как хроническом системном заболевании. Изложены клинические проявления псориатического артрита. Псориатический артрит ассоциируется с псориазом, сопровождается патологией разных суставов с различной степенью тя
The article provides information on psoriatic arthritis, a chronic systemic disease. Detailed clinical manifestations of psoriatic arthritis. Psoriatic arthritis associated with psoriasis, accompanied by various pathologies of joints with varying degrees of severity. The information about the methods of diagnosis and treatment of patients.
Псориатический артрит — это хроническое системное прогрессирующее заболевание, ассоциированное с псориазом, относится к группе серонегативных спондилоартропатий, сопровождающихся синовиитом различной степени выраженности, включающим пролиферацию синовиальной оболочки в сочетании с суставным выпотом [1–3].
Характерная клиника для псориатического артрита формируется за счет развития эрозивного артрита, костной резорбции, множественных энтезитов и спондилоартрита [4].
Распространенность псориаза в популяции составляет от 2% до 8%, а псориатического артрита у больных псориазом колеблется от 13,5% до 47%. Псориатический артрит развивается в возрасте 20–50 лет, с равной частотой как у мужчин, так и у женщин [1, 5].
По данным современной литературы современное течение псориатического артрита характеризуется торпидным, резистентным к проводимой терапии течением, с формированием инвалидизирующих форм, с утратой трудоспособности в 30% случаев [1, 6, 7].
В настоящее время в патогенезе как псориаза, так и псориатического артрита ведущая роль отводится иммунной системе и генетической предрасположенности. Так, основным феноменом является формирование сложной сети взаимодействий иммунокомпетентных клеток, кератиноцитов, клеток синовиальной оболочки и цитокинов, относящихся к наиболее значимым маркерам нарушения процессов иммунорегуляции при воспалительных заболеваниях [1, 8]. При псориатическом артрите, как и при других спондилоартритах, наблюдаются разнообразные изменения профиля про- и противовоспалительных цитокинов, которые образуют регуляторную сеть и, оказывая плейотропное действие, участвуют в патогенетических механизмах данного вида артрита, являясь индукторами воспаления и тканевой деструкции [1, 2, 9].
Генетическая детерминанта псориатического артрита, по данным отечественных и зарубежных исследователей, чаще всего определяется комплексом антигенов гистосовместимости и его определенными гаплотипами [10]. Кроме того, при псориатическом поражении суставов большое значение придается антигенам B27, B38, DR7, DR4, Cw6 и другим. Считается, что наличие антигена В38 ассоциируется с быстрым прогрессированием костно-хрящевой деструкции уже в ранний период развития заболевания, антигены В17 и Cw6 являются прогностическим фактором ограниченного числа пораженных суставов, антигенная структура В57 — множественного количества суставов, DR4 ассоциируется с деструктивным полиартритом [2, 4, 11].
Полиморфизм псориатических изменений кожи в сочетании с разнообразными формами поражения суставов, позвоночника и зачастую внутренних органов явился причиной разнообразной терминологии, встречающейся в научной литературе: псориатическая артропатия, псориатический артрит с системными и внесуставными проявлениями, псориатическая болезнь и др. [12, 13]. Однако при постановке диагноза следует помнить, что по МКБ-10 данная патология определяется как псориатический артрит (L 40.5). Выделяют следующие клинико-анатомические варианты суставного синдрома псориатического артрита [14]:
- дистальный;
- моноолигоартрический;
- остеолитический;
- спондилоартритический.
Степень активности псориатического артрита характеризуется следующими номинациями:
- минимальная — характеризуется незначительными болями при движении. Утренняя скованность либо отсутствует, либо не превышает 30 минут. Температура тела соответствует физиологическим показателям, скорость оседания эритроцитов (СОЭ) не более 20 мм/час;
- умеренная — характеризуется болевым синдромом как в покое, так и при движении. Утренняя скованность достигает 3 часов, кроме того, в области суставов возможен умеренный экссудативный отек. Температура тела субфебрильная, СОЭ до 40 мм/час, возможен лейкоцитоз и палочкоядерный сдвиг;
- максимальная — характеризуется сильными болями в покое и при движении. Утренняя скованность превышает 3 часа. В области периартикулярных тканей отмечается стойкий отек. Температура фебрильная, выявляется значительное превышение биохимических лабораторных показателей [14].
Клинико-анатомический вариант поражения суставов устанавливается по преобладанию одного из симптомокомплексов в клинической картине заболевания. Так, например, при дистальном варианте будут преобладать изолированные поражения дистальных межфаланговых суставов [15, 16]. Асиметричное поражение будет наблюдаться при олигоартрической локализации процесса. Характерная локализация — это крупные суставы, чаще всего коленные. При полиартрическом варианте процесс будет носить симметричный характер и поражаться будут как крупные, так и мелкие суставы. Для остеолитического варианта псориатического поражения суставов будет характерна костная резорбция: внутрисуставная, акральный остеолиз, истинная костная атрофия. Для спондилоартрического варианта характерно развитие сакроилеита и анкилозирующего спондилоартрита [14].
Помимо типичных форм, существуют атипичные варианты течения острого псориатического артрита:
- ревматоидноподобная форма, характеризуется поражением мелких суставов кистей, лучезапястных суставов и длительным течением;
- псевдофлегманозная форма, проявляется моноартритом с резко выраженным воспалительным процессом в области сустава и окружающих тканей, сопровождается высокой температурной реакцией, ознобом, лейкоцитозом, увеличением СОЭ;
- подострая форма моноартрита типичной локализации с незначительной болью;
- первичное поражение сухожилий, суставных сумок, чаще всего ахиллобурсит.
При псориатическом артрите могут регистрироваться различные коморбидные состояния. Наиболее часто наблюдаются артериальная гипертензия, ишемическая болезнь сердца, ожирение и сахарный диабет.
Для диагностики псориатического артрита актуальными являются биохимические исследования крови и рентгенологические исследования суставов и позвоночника. Рентгенологические изменения при псориатическом артрите будут представлены следующими изменениями [14]:
- неравномерное сужение суставной щели;
- истончение, нечеткость, частичное или полное разрушение замыкающих пластинок;
- краевая деструкция в виде узур;
- остеопороз эпиметафизов;
- периостальные наслоения в области метафизов, вывихи и подвывихи;
- анкилозы;
- повышение интенсивности и потеря структуры периартикулярных мягких тканей;
- остеолиз эпифизов мелких костей.
- псориатические высыпания на коже;
- псориаз ногтевых пластинок;
- псориаз кожи у близких родственников;
- артрит трех суставов одного и того же пальца кистей;
- подвывих пальцев рук;
- асиметричный хронический артрит;
- параартикулярные явления;
- сосискообразная конфигурация пальцев стоп и кистей;
- параллелизм течения кожного и суставного синдромов;
- боль и утренняя скованность в позвоночнике, сохраняется на протяжении не менее трех месяцев;
- серонегативность по ревматоидному фактору;
- акральный остеолиз;
- анкилоз дистальных межфаланговых суставов кистей и/или межфаланговых суставов стоп;
- рентгенологические признаки сакроилеита;
- синдесмофиты или паравертебральные оссификаты.
Критерии исключения псориатического артрита:
- отсутствие псориаза;
- серопозитивность по ревматоидному фактору;
- ревматоидные узелки;
- тофусы;
- тесная связь суставного синдрома с урогенитальной и кишечной инфекцией.
Дифференциальную диагностику при псориатическом артрите проводят с болезнью Бехтерева, реактивным артритом, подагрой, недифференцированной спондилоартропатией.
Лечебный маршрут псориатического артрита должен быть комплексным, так как при отсутствии адекватной терапии возможна деформация суставов с последующей инвалидизацией пациента. Основные цели лечения при псориатическом артрите: снижение активности воспалительного процесса в суставах, позвоночнике и энтезисах — местах прикрепления сухожилий; уменьшение проявлений псориаза кожи и ногтей; замедление прогрессирования разрушения суставов; сохранение качества жизни и активности пациентов [16, 17]. Несмотря на то, что в настоящее время не существует лекарственных средств для полного излечения псориатического артрита, современные препараты позволяют управлять болезнью, снимая симптомы заболевания. В качестве симптоммодифицирующих препаратов используются нестероидные противовоспалительные препараты (мелоксикам, нимесулид, целекоксиб, диклофенак и др.), глюкокортикостероидные средства (преднизолон, бетаметазон, триамцинолон). Препаратами выбора болезньмодифицирующих лекарственных средств являются метотрексат, циклоспорин, сульфасалазин, лефлуномид [14].
В период ремиссии или минимальной выраженности псориатического артрита показано санаторно-курортное лечение (Сочи, Мацеста, Пятигорск, Кемери, Кисловодск, Талги, Немиров, Краинка, Миргород) и бальнеотерапия (сероводородные, радоновые, сульфидные ванны). Бальнеотерапия используется крайне осторожно и только под наблюдением врача, в противном случае возможно обострение суставного синдрома.
Пациентам с псориатическим артритом в период ремиссиии рекомендуют вести подвижный образ жизни и ежедневно заниматься лечебной физкультурой.
Таким образом, современное течение псориатического артрита проявляет тенденцию к более раннему началу заболевания, с малопредсказуемым течением и склонностью к формированию инвалидизирующих форм. Однако улучшить прогноз течения псориатического артрита позволяет систематический врачебный контроль и целенаправленная терапия с контролем лабораторных показателей.
Литература
- Бадокин В. В. Перспективы применения ингибиторов ФНО-а при псориазе и псориатическом артрите // Клиническая фармакология и терапия. 2005. № 14. С. 76–80.
- Кунгуров Н. В. и соавт. Генетические факторы этиологии и патогенеза псориаза // Вестник дерматологии и венерологии. 2011. № 1. С. 23–27.
- Юсупова Л. А., Филатова М. А. Современное состояние проблемы псориатического артрита // Практическая медицина. 2013. № 3. С. 24–28.
- Беляев Г. М. Псориаз. Псориатическая артропатия (этиология, патогенез, диагностика, лечение, профилактика). М.: МЕД-пресс-информ. 2005. 272 с.
- Бадокин В. В. Современная терапия псориатического артрита // Consilium Medicum. 2005. Т. 7. № 3.
- Довжанский С. И. Генетические и иммунологические факторы в патогенезе псориаза // Российский журнал кожных и венерических болезней. 2006. № 1. С. 14–18.
- Коноваленко A. A. Состояние иммунной системы у больных осложненными формами псориаза // Медицинская панорама. 2008. № 2. С. 64–66.
- Мельников А. Б. Псориатический артрит: клиническая картина, диагностика и терапия // Клиническая дерматология и венерология. 2010. № 5. С. 17–24.
- Коротаева Т. В. Лефлуномид в терапии псориатического артрита (ПсА) // Фарматека. 2007. № 6. С. 24–28.
- Кубанова A. A. с соавт. Иммунные механизмы псориаза. Новые стратегии биологической терапии // Вестник дерматологии и венерологии. 2010. № 1. С. 35–47.
- Бакулев А. Л. Применение гепатопротекторов при псориазе: сравнительная клинико-лабораторная и ультрасонографическая оценка эффективности // Вестник дерматологии и венерологии. 2010. № 1. С. 112–117.
- Кочергин Н. Г. Итоги работы Первой всемирной конференции по псориазу и псориатическому артриту // Русский медицинский журнал. Дерматология. 2006. Т. 14, № 15. С. 1151–1155.
- Пирузян А. Л. Молекулярная генетика псориаза // Вестник РАМН. 2006. № 3. С. 33–43.
- Клинические рекомендации. Дерматовенерология. Под ред. А. А. Кубановой. М.: ДЭКС-Пресс, 2010. 428 с.
- Коротаева Т. В. Стандарты терапии псориатического артрита // Научно-практическая ревматология. 2009. № 3. С. 29–38.
- Аковбян В. А. с соавт. Применение кальципотриола в терапии псориаза // Вестник дерматологии и венерологии. 2007. № 3. С. 45–46.
- Шостак Н. А. Псориатический артрит: новые подходы к лечению // Клиницист. 2008. № 2. С. 41–45.
З. Ш. Гараева 1 , кандидат медицинских наук
Л. А. Юсупова, доктор медицинских наук, профессор
Г. И. Мавлютова, кандидат медицинских наук
Е. И. Юнусова, кандидат медицинских наук
Читайте также:

