Сахароснижающие препараты при гепатите в
Обновлено: 11.05.2024
Печень самая большая биохимическая лаборатория в нашем организме. Она участвует более чем в 500 реакциях. Поэтому любые изменения в её состоянии могут отразиться на самочувствии. Все знают ее важную роль и наслышаны о таком грозном диагнозе, как цирроз, многие хотят её почистить, попить специальные лекарства. Кто-то ищет народные средства, другие больше доверяют разработкам фармацевтической промышленности. Остается вопрос, что будет эффективно на самом деле?
А что же печень?
Можно подумать, что печень только и ждет, когда же мы ей поможем. Это не так. Компенсаторные и регенераторные возможности печени огромны. При сохранении 25% здорового органа она может сама восстановиться. Как работает здоровая печень, мы никогда не почувствуем. В ней нет нервных окончаний, поэтому она никогда не болит. Клетки печени — гепатоциты. Если гибнет клетка, её нагрузку перераспределяют между собой оставшиеся. Так, при разрушении значительной части печени, может не быть никаких симптомов и даже изменений в анализах.
С одной стороны, это хорошо, печень не беспокоит нас по пустякам как желудок, который может скрутить после плохой пищи, а через 3 дня мы уже и забыли об этом. Но если симптомы появились, это может свидетельствовать уже о серьезных проблемах, просто так от которых не избавиться. При проблемах с печенью могут страдать следующие функции:
- фильтрация и переработка токсичных продуктов, поступающих из желудочно-кишечного тракта;
- производство молекул белка, их накопление, преобразование аминокислот, образование мочевины и синтез креатина;
- образование и хранение гликогена;
- хранение и трансформация многих витаминов (A, PP, B, D, K), ионов металлов железа, меди, цинка, марганца, молибдена и др.;
- производство ферментов, участвующих в обменных процессах;
- поддержание баланса между свертывающей и антисвертывающей системами крови, образование гепарина;
- депонирование плазмы крови и форменных элементов, регуляция системы крови.
Ошибочно за проблемы с печенью принимают проблемы с желчным пузырем, поджелудочной железой, позвоночником и многие другие. Боль в печени может появиться, когда она увеличена и растягивает собственную капсулу, но обычно это уже запущенные проблемы.

Часто за проблемы с печенью принимают проблемы с желчным пузырем, поджелудочной или позвоночником.
Препараты
Проблемы с печенью могут развиваться более 10 лет и никак не беспокоить. Средняя продолжительность жизни с диагнозом цирроз — 9 лет. Поэтому даже имея проблемы с печенью, можно с ними бороться. Одних наименований средств, применяемых в гепатологии около 1000. При терапии не только лечат само заболевание, но и поддерживают печень, чтобы создать ей максимально благоприятные условия для восстановления. Одной из таких групп препаратов являются гепатопротекторы. Гепатопротекторы помогают восстановлению обменных процессов в печени, повышают устойчивость органа к действию разрушающих факторов, нормализуют функциональную активность и стимулируют регенеративные процессы в печени.
Требования к гепатопротекторам
Так как печень является тем органом, через который происходит обмен многих веществ, препараты должны быть не только мощными, но и отвечать определенным требованиям безопасности, а также:
Несмотря на то, что требования известны, идеального препарата еще не создано. Более половины представленных средств растительного происхождения, оставшуюся часть делят между собой фосфолипиды, синтетические производные, органопрепараты и аминокислоты.

Несмотря на то, что требования к препаратам для печени известны, идеального еще не создано.
Список лекарств
Группы гепатопротекторов разделяются в зависимости от состава.
Группа I: флавоноиды расторопши могут входить как натуральная вытяжка из растений, так и произведенные синтетическим способом:
Эти продукты содержат в себе вещество из расторопши пятнистой – силимарин (силибинин). Он защищает и стабилизирует мембраны клеток. Расторопша пятнистая обладает мощным антитоксическим действием, способна помочь при отравлениях бледной поганкой. Правда, в этом случае используют модификацию с внутривенным введением. Также имеется антиоксидантный и метаболический эффекты, ускоряет регенерацию гепатоцитов. Замедляется образование рубцовой ткани в органе.
Холестаз, то есть затрудненный отток желчи может быть противопоказанием к приему. Если это игнорировать, застой от приема препаратов может усилиться.
Обычно курс приема составляет около 4 недель, затем делают перерыв.
Группа II: остальные флавоноиды, кроме расторопши:
Лив 52 помогает усилить защиту печени от токсинов, имеет в составе компоненты широко используемые в индийской медицине. Но применение препарата в острой воспалительной фазе небезопасно и может усилить воспаление. Поэтому рекомендуется применять препарат, когда активна фаза регенерации и печень нуждается в поддержке.
Группа III: гепатопротекторы из органов животных:
Гепатносан – высушенные гепатоциты животных. В кишечнике он абсорбирует токсины. Перевариваясь, питательные компоненты клеток всасываются и доставляются в печень. Они работают как защитные факторы на уровне клеток печени, восстанавливают активность гепатоцитов. Препарат способствует ускорению репаративных процессов.
Сирепар — гидролизат экстракта печени крупного рогатого скота. Содержит в 1 мл 10 мг цианокобаламина. Способствует регенерации печени, оказывает очищающее действие. Не следует использовать в активную фазу болезни, так как может усилиться воспалительный процесс. Принимается при хронических гепатитах и циррозах, отравлениях токсинами и лекарствами.

Некоторые препараты не следует использовать в активную фазу болезни, так как может усилиться воспалительный процесс.
Группа IV: лекарства, имеющие в своем составе эссенциальные фосфолипиды:
Фосфолипиды, в том числе фосфатидилхолин, важнейший компонент, из которого как из кирпичиков состоит большая часть мембран самих клеток печени. Фосфолипиды выделены и изучаются почти 50 лет, проведены различные опыты и эксперименты. Восстанавливая мембраны клеток, печень нормализует свою функцию. Применяются при очень широком спектре заболеваний. Курс приема обычно длится около 3 месяцев при отсутствии противопоказаний и нежелательных эффектов.
Средства из других групп, не вошедшие в первые четыре:
-
; ;
- Нестероидные анаболики (метилурацил, натрия нуклеинат); ; .
Из этой группы разберем подробно Урсофальк, как препарат, имеющий широкое назначение среди врачей. Действующее вещество (урсодезоксихолевая кислота) помогает защитить орган и обладает желчегонным действием. Используется для растворения желчных камней. Снижает токсические эффекты на эпителий желчных протоков в печени и мембраны гепатоцитов. Облегчает выведение желчи из протоков, вследствие чего облегчает выведение токсинов.
Имеет противопоказания в виде неработающего желчного пузыря, воспалительных болезней кишечника, желчных протоков, желчные камни с высоким содержанием кальция (видны на рентгене), в общем любые состояния, которые будут препятствовать усиленному оттоку желчи из печени. Также цирроз в стадии декомпенсации.
Вывод
Гепатопротекторов множество, они отличаются составом, механизмом действия. У врачей отношение к ним неоднозначное, многие из них применяются и выпускаются только для территории постсоветских стран. Иногда можно встретить, отзывы, что человек после выхода из алкогольного запоя пропил некий препарат в течение 3 месяцев и его анализы улучшились. Это могло случиться и не из-за препарата, а от того, что токсины перестали действовать на печень, и она смогла в определенной мере восстановиться.

При прекращении воздействия токсинов, печень может сама в определенной мере восстановиться.
Главное в лечении печени не прием лекарств для компенсации вреда, который мы наносим сами, а прекращение воздействия токсинов и других разрушающих факторов. То есть нужно отказаться от алкоголя, курения и лишних килограммов (риск неалкогольного жирового гепатоза). Так как чередуя курсы препаратов с неправильным образом жизни мы создаем иллюзию благополучия. Если есть подозрения, что с печенью что-то не так, — обязательно обратитесь к врачу. Неправильное самолечение при проблемах с печенью может только навредить.
Рассмотрены подходы к сахароснижающей терапии у больных сахарным диабетом 2-го типа. Проведено сравнение препаратов — преимущества, побочные эффекты, противопоказания. Даются рекомендации по выбору терапии с учетом различных факторов.
Approaches to hypoglycemic therapy in patients with 2nd type diabetes mellitus were considered. The preparations were compared in terms of advantages, side effects, contraindications. The recommendations on therapy selection regarding different factors were given.
В настоящее время имеется широкий арсенал стационарных и амбулаторных средств, способных воздействовать практически на все известные звенья патогенеза сахарного диабета (СД) 2-го типа. Существует множество их классификаций, среди которых разделение по основному эффекту, по точкам приложения, по механизму действия, по длительности и т. д.
Выделяют гипогликемические средства и антигипергликемические средства. Целью гипогликемических препаратов (производные сульфонилмочевины и меглитиниды) является стимуляция синтеза эндогенного инсулина, в результате чего среди положительных сторон лечения происходят и отрицательные события: прибавка в весе и увеличение риска развития гипогликемических состояний.
Антигипергликемические препараты (ингибиторы α-глюкозидаз, бигуаниды, тиазолидиндионы, инкретиномиметики) улучшают периферическую утилизацию глюкозы, но не оказывают стимулирующего действия на β-клетки поджелудочной железы. Благодаря этому уровень инсулина в крови не повышается и снижения глюкозы в крови ниже нормы не происходит [1].
.jpg)
Сахароснижающие средства, влияющие на тонкую кишку, препятствуют полному всасыванию углеводов в кишечнике за счет ингибирования ферментов α-глюкозидаз, влияющих на поджелудочную железу (секретогены), — заставляют ее β-клетки выделять эндогенный инсулин, а влияющие на гепатоциты, жировую и другие периферические ткани (сенситайзеры) — увеличивают чувствительность органов-мишеней к инсулину.
Примерами секретогенных сахароснижающих лекарственных средств являются препараты сульфонилмочевины (глибенкламид, гликлазид, глимепирид) и прандиальные регуляторы глюкозы — меглитиниды (натеглинид, репаглинид). Сенситайзеры представлены бигуанидами (метформин) и тиазолидиндионами (пиоглитазон, росиглитазон).
Относительно новым классом сахароснижающих препаратов являются инкретиномиметики (вилдаглиптин, саксаглиптин, эксенатид, лираглутид), инсулинотропное действие которых является глюкозозависимым и реализуется только при повышенном уровне гликемии. При достижении нормогликемии концентрация инсулина возвращается к базальному уровню, что способствует снижению риска развития гипогликемии на фоне приема данных лекарственных средств. Механизм действия этих препаратов является глюкозозависимым и не нарушает нормального глюкагонового ответа на гипогликемию [2]. Основные классы пероральных сахароснижающих препаратов и механизмы их действия представлены в табл. 1 и на рис. 1.
Перед читателем десятки наименований лекарственных средств, принадлежащих к разным фармакологическим группам, обладающим своим механизмом действия, доказательной базой и стоимостью. При таком обилии лекарств, в рамках короткого режима общения с пациентом, а также в условиях коморбидности и вынужденной полипрагмазии, выбор нужного медикамента в адекватном режиме дозирования сделать очень нелегко — практически невозможно, что диктует необходимость в обозначении клинико-фармакологических ниш данных препаратов, а также их преимуществ и недостатков (рис. 2–8).
Ингибиторы a-глюкозидазы должны применяться в основном с целью профилактики сахарного диабета 2-го типа у пациентов с начальными проявлениями инсулинорезистентности. Кроме того, они являются препаратами выбора для лиц с предиабетом, сопровождающимся именно постпрандиальной гипергликемией при нормальных тощаковых уровнях (снижение уровня HbA1c на 0,5–0,8%).
Показаниями для назначения глинидов являются сахарный диабет 2-го типа при неэффективности диеты и физических нагрузок. Также они предназначены для преимущественного снижения постпрандиальной гипергликемии (снижение уровня HbA1c на 0,5–1,5%).
Клиническая ниша для назначения глитазонов (тиазолидиндионов) сводится к сахарному диабету 2-го типа, в качестве монотерапии или в комбинации с препаратом сульфонилмочевины, бигуанидами или инсулином при отсутствии эффекта от диетотерапии, физических упражнений и монотерапии одним из вышеперечисленных средств (снижение уровня HbA1c на 0,5–1,4%).
Бигуаниды являются препаратами выбора как для лиц с предиабетом, сопровождающимся тощаковой гипергликемией и с нормальным уровнем сахара после еды, что косвенно свидетельствует об инсулинорезистентности, так и для пациентов с сахарным диабетом 2-го типа. Их назначение возможно в виде монотерапии и в комбинациях прежде всего с секретогенами (когда последние не дают полной коррекции гипергликемии) и с инсулином (при наличии инсулинорезистентности) (снижение уровня HbA1c на 1–2%).
Назначение производных сульфанилмочевины, как правило, ассоциировано с наличием СД 2-го типа в тех случаях, когда диета и физические нагрузки, назначение ингибиторов α-глюкозидаз и бигуанидов оказались неэффективными (снижение уровня HbA1c на 1–2%).
Препараты с инкретиновой активностью (рис. 7), влияющие преимущественно на ГПП1, назначаются при СД 2-го типа в качестве дополнения к терапии бигуанидами, производными сульфонилмочевины, тиазолидиндионами в случае неадекватного гликемического контроля (снижение уровня HbA1c на 0,8–1,8%).
Другая разновидность инкретиномиметиков — препараты, влияющие на ДПП4 (рис. 8), которые целесообразно назначать при сахарном диабете 2-го типа в качестве монотерапии в сочетании с диетотерапией и физическими упражнениями; в комбинации с бигуанидами в качестве начальной медикаментозной терапии при недостаточной эффективности диетотерапии и физических упражнений; а также в составе двухкомпонентной комбинированной терапии с бигуанидами, производными сульфонилмочевины, тиазолидиндионами или инсулином в случае неэффективности диетотерапии, физических упражнений и монотерапии этими препаратами (снижение уровня HbA1c на 0,5–1,0%).
Механизм действия ингибиторов ДПП4 максимально приближен к естественным процессам, происходящим в здоровом человеческом организме. Под их действием происходит уменьшение частоты защитных перекусов, которые пациенты употребляют во избежание гипогликемий, уменьшение всасывания жира из кишечника, повышение расхода энергии, а также повышение окисления липидов во время приема пищи [3]. Кроме того, при СД в результате повышенного апоптоза β-клетки теряют свою массу, что выражается в значительных нарушениях их функций, основной из которых является синтез инсулина. Физиологичное действие данной группы препаратов поддерживает жизнеспособность β-клеток поджелудочной железы, увеличивает их массу на 75% и на 65% уменьшает апоптоз [4]. Сравнение основных представителей ингибиторов ДПП4 представлено в табл. 2.
Сердечно-сосудистые эффекты ингибиторов ДПП4 сводятся к уменьшению ремоделирования миокарда, улучшению функции эндотелия, снижению атерогенных фракций липопротеидов, снижению артериального давления (АД), уменьшению симптомов недостаточности кровообращения, защите миокарда от ишемии, а также к функциональному восстановлению миокарда после ишемии и увеличению числа рецепторов к инсулину в кардиомиоцитах [5]. Кардиометаболизм ингибиторов ДПП4 представлен в табл. 3.
Сводные данные, отражающие преимущества и недостатки основных классов сахароснижающих препаратов, представлены в табл. 4.
Как видно из представленной таблицы:
- при сердечно-сосудистых заболеваниях пациентам следует избегать препаратов с высокой вероятностью развития гипогликемии, которая может оказаться весьма опасной для них;
- больным с избыточной массой тела необходимо назначать сахароснижающие препараты, не способствующие дальнейшей прибавке веса;
- при лечении женщин детородного возраста следует принимать во внимание возможность беременности, при которой таблетированные сахароснижающие препараты противопоказаны;
- все таблетированные сахароснижающие препараты противопоказаны лицам с диабетическим кетоацидозом;
- у больных алкогольной висцеропатией и циррозом печени выбор сахароснижающей терапии должен основываться на особенностях метаболизма препарата, а также длительности его действия;
- у пациентов с ХБП (в т. ч. в результате диабетической нефропатии) коррекцию гликемии следует осуществлять под контролем скорости клубочковой фильтрации (СКФ).
Невозможность поддержания компенсации углеводного обмена у пациентов на монотерапии, а также высокий риск развития острых и хронических осложнений сахарного диабета у коморбидных больных являются достаточными основаниями для проведения комбинированного лечения. В случае комбинированной сахароснижающей терапии улучшение эффективности лечения является следствием сложения механизмов действия препаратов (например, секретогенов и сенситайзеров) [6]. Комбинированная терапия сопровождается улучшением качества жизни больных и хорошо переносится ими, что связано с параллельным воздействием на разные звенья патогенеза СД и с уменьшением количества одномоментного приема таблетированных препаратов при одновременном улучшении компенсации углеводного обмена (рис. 9).
Однако эволюция пероральных сахароснижающих средств продолжается — еще в ноябре 2012 г. в Европе был одобрен первый представитель новейшего класса пероральных ингибиторов натрий-глюкозного котранспортера 2-го типа (SGLT2) — дапаглифлозин, а в марте 2013 г. Управление по контролю за продуктами питания и лекарственными средствами (Food and Drug Administration, FDA) одобрило канаглифлозин для лечения взрослых пациентов с сахарным диабетом 2-го типа. В американские, европейские и азиатские регуляторные органы также поданы заявки на регистрацию эмпаглифлозина, ипраглифлозина и лузеоглифлозина, масштабные исследования которых продолжаются в настоящее время.
Механизм их действия заключается в следующем. Из-за активной системы реабсорбции эта глюкоза практически полностью реабсорбируется в проксимальном канальце нефрона. Моча, поступающая в петлю Генле, свободна от глюкозы. Повышение концентрации глюкозы в плазме крови приводит к увеличению ее фильтрации в клубочках. При увеличении скорости поступления глюкозы в проксимальный каналец выше 260–350 мг/мин/1,73 м 2 , например у пациентов с СД, избыток глюкозы превышает реабсорбтивный потенциал, и она начинает выделяться с мочой. У здорового взрослого человека это соответствует концентрации глюкозы в крови около 10–11 ммоль/л (180–200 мг/дл). Поскольку глюкоза не способна свободно проникать через клеточную мембрану, то во всасывании ее в кишечнике и реабсорбции в почках участвуют натрийзависимые переносчики глюкозы (SGLT1 и 2) [7]. Соответственно, ингибиторы SGLT снижают концентрацию глюкозы в крови за счет стимуляции ее выведения с мочой.
Клинико-фармакологические ниши данного класса препаратов расставит время, а ответы на многие вопросы должны развеять результаты клинических исследований этих лекарств, однако уже сегодня не вызывает сомнений постулат, гласящий о том, что, выбирая сахароснижающий препарат, врачу необходимо помнить, что в каждом конкретном случае адекватная терапия СД возможна только при учете возраста, пола, гендерных особенностей, массы тела пациента, а также этиологических и патогенетических механизмов развития заболевания.
Литература
А. С. Скотников* , 1 , кандидат медицинских наук
М. Г. Селезнёва**
* ГБОУ ВПО Первый МГМУ им. И. М. Сеченова, Москва
** ГБУЗ ГКБ № 5 ДЗМ, Москва
Печень - это самый большой паренхиматозный внутренний орган, выполняющий жизненно важные функции и содействующий функциям многих систем организма. Печень участвует в метаболизме всех питательных веществ, в пищеварении, синтезе и резервировании необходимых организму веществ, в расщеплении, детоксикации и экскреции ненужных или вредных веществ, в кроветворении и осуществлении ряда других функций.
Учитывая роль печени в метаболизме химических веществ, можно априорно утверждать, что не существует лекарств, которые в определенных условиях не вызывали бы повреждение печени. Непрерывно возрастающий поток сведений о гепатотоксическом действии многих лекарственных препаратов свидетельствует о том, что медикаментозные поражения печени - одна из важнейших проблем гепатологии. Это в значительной степени обусловлено тем, что непросто отличить симптомы основного заболевания от побочных эффектов лечения. По данным литературы, частота лекарственных гепатитов составляет от 1 до 28% всех побочных действий, связанных с медикаментозной терапией. Примерно у 2% больных, госпитализируемых по поводу желтухи, причиной ее оказываются лекарства. В США в 25% случаев фульминантная печеночная недостаточность обусловлена лекарствами.
В настоящее время исследователи выделяют три механизма медикаментозного поражения печени:
циты в настоящее время встречается крайне редко вследствие ужесточения контроля за побочным действием лекарственных препаратов. В качестве такого примера можно привести препарат галотан.
Токсическое действие метаболитов лекарственных средств можно представить следующей последовательностью (рис. 1):
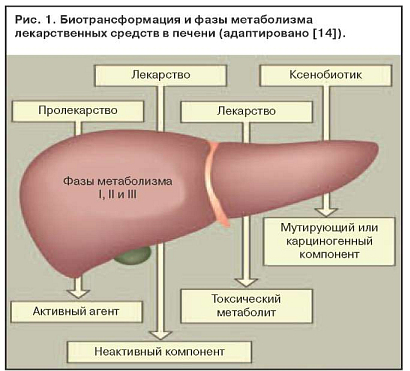
Фаза I. Основная система, метаболизирующая лекарства, расположена в микросомальной фракции гепатоцитов гладкой эндоплазматической сети. К ней относятся монооксигеназы со смешанной функцией, цитохром С-редуктаза, цитохром Р-450. Кофактором служит восстановленный никотинамидадениндинуклеотидфосфат в цитозоле. Лекарства подвергаются гидроксилированию или окислению, которые обеспечивают усиление их поляризации.
Система гемопротеинов Р-450, расположенная в эндоплазматической сети гепатоцитов, обеспечивает метаболизм лекарств. При этом образуются токсичные метаболиты. Идентифицировано по меньшей мере 50 изоферментов системы Р-450, и нет сомнений, что их еще больше. У человека метаболизм лекарств обеспечивают цитохромы, относящиеся к трем семействам: P-450-I, P-450-II, P-450-III.
Увеличение содержания ферментов системы цитохрома Р-450 в результате индукции приводит к повышению выработки токсичных метаболитов. Когда два активных препарата конкурируют за один участок связывания на ферменте, метаболизм препарата с меньшей аффинностью замедляется и срок его действия увеличивается. Этанол индуцирует синтез P-450-II-E1 и тем самым увеличивает токсичность парацетамола. Повреждение клеток печени редко бывает обусловлено самим лекарственным препаратом. Токсичность парацетамола увеличивается и при лечении изониазидом, который также индуцирует синтез P-450-II-E1 (рис. 2). Некроз наиболее выражен в зоне 3, где отмечается самая высокая концентрация ферментов, метаболизирующих лекарства (рис. 3).
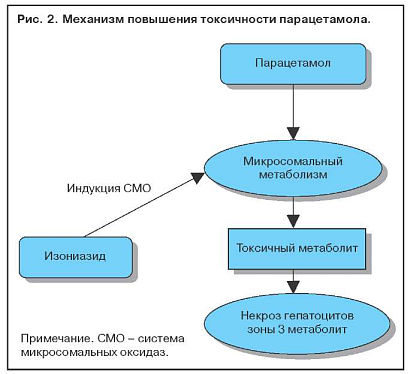
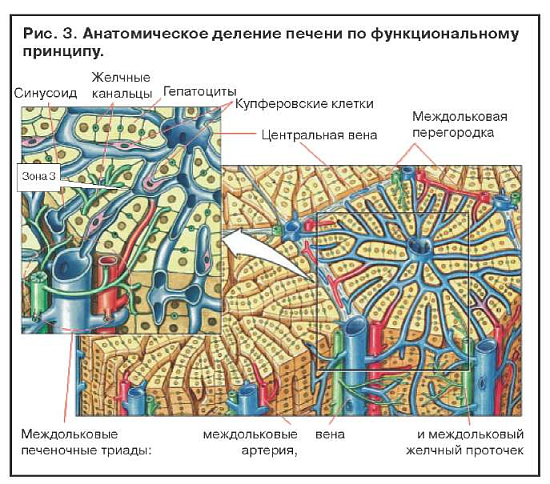
Фаза II. Механизм действия биотрансформации состоит в конъюгации метаболитов лекарственных препаратов с мелкими эндогенными молекулами. Обеспечивающие ее ферменты неспецифичны для печени, но обнаруживаются в ней в высоких концентрациях.
Фаза III. Продукты биотрансформации лекарств могут выделяться с желчью или мочой. Способ выделения определятся многими факторами, некоторые из них еще не изучены. Высокополярные вещества, а также метаболиты, ставшие полярными после конъюгации, выделяются с желчью в неизмененном виде.
Иммуноаллергические поражения печени связывают с метаболитом, который может оказаться гаптеном для белков клеток печени и вызвать их иммунное повреждение (рис. 4). При наличии генетического дефекта в печени лекарство превращается в токсический метаболит, ковалентно связывается с клеточным белком (глутатионом), приводя к некрозу гепатоцита, а также стимулирует образование антигена (гаптена) и сенсибилизирует Т-лимфоцит, который запускает иммунную гепатотоксичность. Повторная экспозиция (назначение лекарственного препарата) приводит к усилению иммунной реакции.
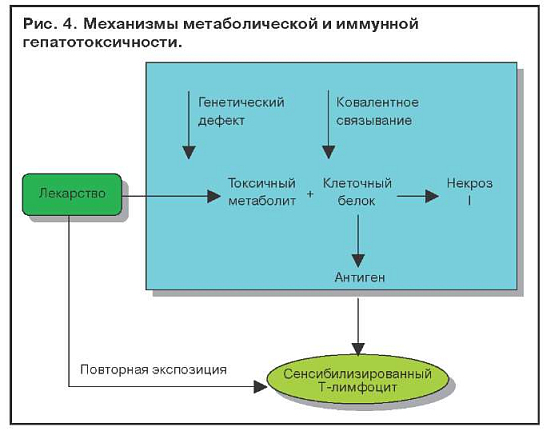
В этом процессе могут участвовать ферменты системы Р-450. На мембране гепатоцитов имеется несколько изоферментов Р-450, индукция которых может привести к образованию специфичеких антител к иммунному повреждению гепатоцита.
Идиосинкразия к диуретикам и тиениловой кислоте сопровождается появлением аутоантител, взаимодействующих с микросомами печени.
Известно шесть механизмов поражения гепатоцита (рис. 5):
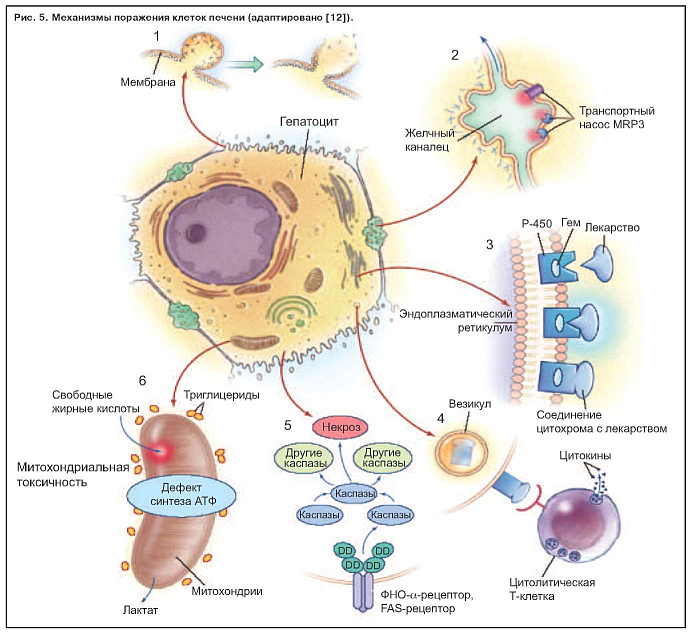
Повреждение клеток печени происходит в специфических структурах пораженных внутриклеточных органелл. Нормальный гепатоцит, показанный в центре рис. 5, может быть поврежден по крайней мере шестью способами, обозначенными цифрами от 1 до 6. Нарушение внутриклеточного гомеостаза кальция приводит к разрушению фибрилл актина на поверхности гепатоцита. Это приводит к вздутию мембраны клетки (1), а в дальнейшем к ее разрушению и лизису. При холестатических заболеваниях разрушение ворсинок актина (2) может происходить рядом с канальцем специфичной части клетки, ответственной за желчную экскрецию. Нарушение передачи в ворсинках актина мультирезистентного белка (MRP3) предотвращает экскрецию в билирубин органических соединений лекарственного препарата.
Многие гепатоцеллюлярные реакции активизируют гемсодержащий цитохром P-450 (3), производя при этом высокоэнергетические реакции, которые могут привести к ковалентной связи лекарственного средства с ферментом, таким образом создавая неактивные продукты метаболизма. Эти неактивные продукты метаболизма в виде пузырьков (4) мигрируют к поверхности клетки и могут быть причинами многогранного иммунного ответа, включающего цитолитические Т-лимфоциты и цитокины. Активация фактора некроза опухоли a (ФНО-a) является триггерным фактором для запуска каскад межклеточных каспаз (5), который заканчивается программированным апоптозом клеток с потерей ядерного хроматина.
Определенные препараты ингибируют функцию митохондрий гепатоцита двойным эффектом, снижая продукцию аденозинтрифосфата (АТФ) и ферментов дыхательной цепи (6). Свободные жирные кислоты не метаболизируются из-за нехватки аэробного дыхания в накоплении лактата и реактивных продуктов окисления. Их накопление приводит к повреждению митохондриальной ДНК. Эта структура повреждения характерна для множества средств, включая ингибиторы обратной транскриптазы нуклеозида, вальпроевой кислоты, тетрациклина, ацетилсалициловой кислоты. Они экскретируются в желчь и могут повредить эпителий желчного протока. DD обозначает смертельный домен.
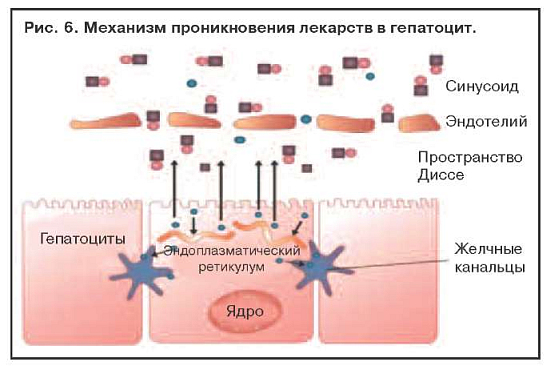
Проникновение лекарств в гепатоцит зависит от липофильности медикаментов. Жировая растворимость является важнейшим фактором при назначении медикаментов и попадании в системную циркуляцию с диффузным проникновением в энтероцит. Лекарства с незначительной липофильностью плохо абсорбируются и экскретируются с каловыми массами. В противоположность им лекарства, соединяющиеся в комплексе с протеином, обычно альбумином, обладают высокой проницаемостью в разные ткани, исключая жир. Практически все лекарственные препараты, назначенные per os, попадают в печень. Степень печеночной экскреции лекарств зависит от печеночного кровотока и активности метаболитов лекарственных энзимов. В печеночных синусоидах белки диффундируют к эндотелиальному ретикулуму, в дальнейшем к пространству Диссе, а далее - в гепатоциты, связанные ферментами как полярные компоненты. Некоторые водорастворимые молекулы возвращаются к синусоидам, другие - в билиарные канальцы (рис. 6).
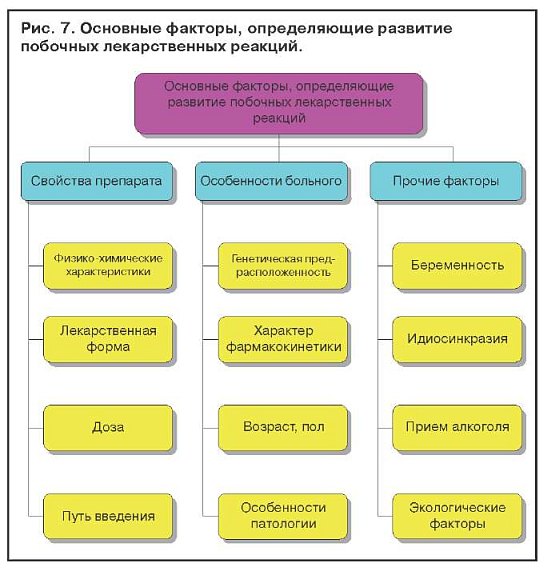
Лекарственные поражения печени зависят от свойств лекарственного препарата, особенности больного и прочих факторов (рис. 7). Известно, что вероятность побочных реакций возрастает с увеличением количества одновременно принимаемых лекарств. Установлено, что, если больной принимает одновременно шесть или более препаратов, вероятность побочного действия у него достигает 80%.
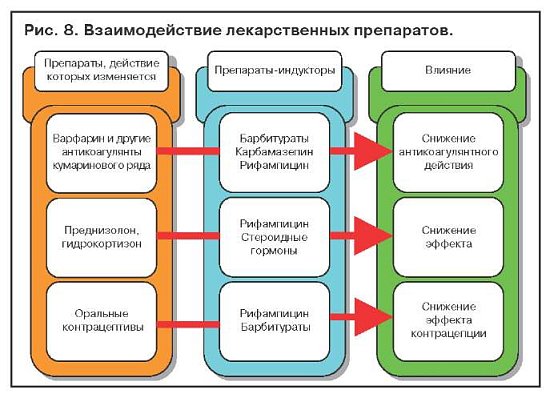
Беременность, стресс, бедное белками питание увеличивают риск токсичности медикаментов. Медикаменты, которые являются энзиматическими индукторами, могут потенцировать действие другого препарата.
Примеры взаимодействия лекарственных препаратов, обусловленного индукцией ферментов печени, представлены на рис. 8.
Гепатотоксический эффект лекарственных препаратов подразделяется на дозозависимый, который проявляется при приеме большого количества того или иного препарата, дозонезависимый, связанный с идиосинкразией, и поражения печени без нарушения пигментного обмена. На рис. 9 представлены фармакотерапевтические группы лекарственных препаратов, которые способны вызывать желтухи. Применение препаратов из представленных фармакотерапевтических групп при определенных условиях может вызывать поражения печени без желтухи.
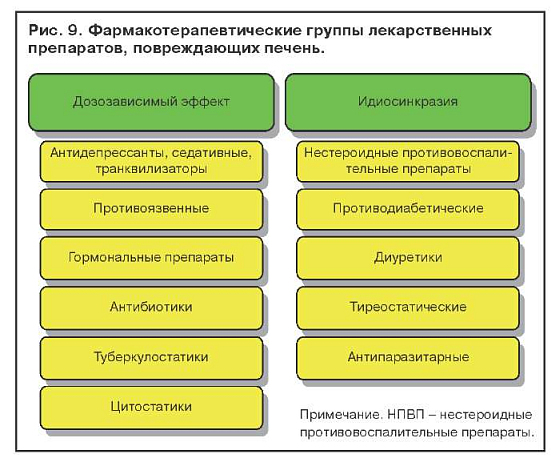
Острые медикаментозные гепатиты подразделяются на цитолитические, холестатические и смешанные формы, сочетающие признаки холестаза и цитолиза. Фактором, способствующим переходу гепатита в хронический, является длительный прием лекарств.
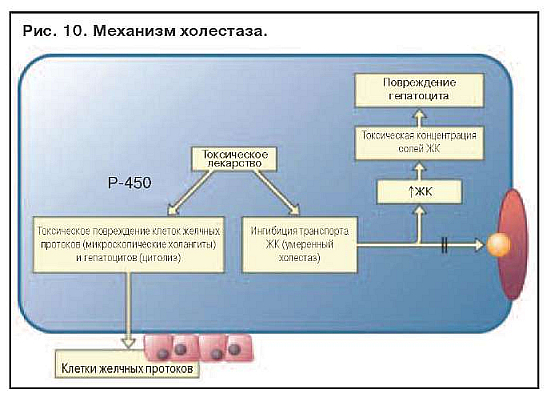
На рис. 10 представлен пример лекарственного повреждения печени. Токсическое лекарственное средство блокирует транспорт желчных кислот (ЖК) и
повреждает клетки желчных протоков и гепатоцитов, вызывая легкий холестаз. Аккумуляция ЖК ведет к повреждению гепатоцита, что приводит к смешанной реакции, включающей холестаз и цитолиз. Особенностью лекарственного холестаза является микроскопический холангит, проявляющийся поражением клеток мелких желчных ходов.
Современную классификацию лекарственных реакций печени представляет Ш.Шерлок (табл. 1).
Таблица 1. Классификация лекарственных реакций печени
Тип реакции
Особенности гепатотоксического действия
Клинико-фармакологическая группа
Холестаз
Антибиотики Гормоны Противоязвенные
Обратимая желтуха средней степени тяжести
Антибиотики. Уроанитисептики Цитостатики Пероральные сахароснижающие препараты
Бессимптомное течение Возможен приступ желчной колики
Антибиотики цефалоспоринового ряда
Цитолиз
Зависимая от дозы. Безжелтушная форма течения
Антибиотики Гормоны Противорвотные Активаторы образования тромбопластины
Дозозависимый, обратим. Желтуха средней тяжести
Гормоны Антибиотики Противопротозойные
Мостовидные некрозы. Различные нарушения пигментного обмена
Статины Противотуберкулезные Нейролептики Противогрибковые Транквилизаторы и антидепрессанты Нейролептики Мочегонные
Часто сопровождаются гранулематозом
Портальная гипертензия. Цирроз
Антитиреоидные Противоподагрические Антихолинэстеразные
Сосудистые реакции
Половые гормоны Антиандрогены Антиэстрогены Антигонадотропные
Неопластические реакции
Носит доброкачественный характер
Антигонадотропные Половые и анаболические гормоны
Особенности гепатотоксического действия
Холестаз
Антибиотики Гормоны Противоязвенные
Обратимая желтуха средней степени тяжести
Антибиотики. Уроанитисептики Цитостатики Пероральные сахароснижающие препараты
Бессимптомное течение Возможен приступ желчной колики
Антибиотики цефалоспоринового ряда
Цитолиз
Зависимая от дозы. Безжелтушная форма течения
Антибиотики Гормоны Противорвотные Активаторы образования тромбопластины
Дозозависимый, обратим. Желтуха средней тяжести
Гормоны Антибиотики Противопротозойные
Мостовидные некрозы. Различные нарушения пигментного обмена
Статины Противотуберкулезные Нейролептики Противогрибковые Транквилизаторы и антидепрессанты Нейролептики Мочегонные
Часто сопровождаются гранулематозом
Портальная гипертензия. Цирроз
Антитиреоидные Противоподагрические Антихолинэстеразные
Сосудистые реакции
Половые гормоны Антиандрогены Антиэстрогены Антигонадотропные
Неопластические реакции
Носит доброкачественный характер
Антигонадотропные Половые и анаболические гормоны
В большинстве случаев осложнения со стороны печени реализуются изолированным повышением уровня аминотрансфераз, без отчетливых клинических проявлений или сопровождаются астеническим синдромом. Бессимптомное повышение уровня аминотрансфераз может наблюдаться при использовании таких лекарственных средств, как изониазид, допегит, амиодарон. При повторном приеме перечисленных препаратов могут развиться тяжелые гепатиты со смертельным исходом. Поэтому на изолированное повышение активности аминотрасфераз необходимо обращать внимание, так как оно может свидетельствовать о развитии лекарственной патологии печени. Диапазон клинических проявлений лекарственных гепатитов разнообразен - от небольшого повышения уровня аминотрансферез, не сопровождающегося клинической симптоматикой, до молниеносных гепатитов и развития циррозов. У человека лекарственные поражения могут напоминать почти все существующие заболевания печени.
Лекарственные гепатиты, сопровождающиеся желтухой, могут протекать по цитолитическому, холестатическому или смешанному варианту. В ряде случаев может развиваться псевдохирургическая симптоматика (боли в животе, лихорадка, желтуха, увеличенный желчный пузырь). К лекарствам, способным вызвать острую псевдохирургическую симптоматику, относятся цитостатики, антидепрессанты, антиаритмические препараты.
Диагностика медикаментозных гепатитов представляет сложную проблему. Предлагается несколько критериев, позволяющих уточнить диагноз и подтвердить ее лекарственный характер:
Хронологический критерий очень показателен, хотя время появления осложнений после приема лекарства крайне разнообразно - от нескольких дней (иногда нескольких часов) до нескольких недель и месяцев. В случае полипрагмазии хронологический фактор очень трудно оценить.
Регресс клинических признаков осложнения после отмены лечения - довольно четкий диагностический признак. Регресс может быть длительным (более месяца), при этом учитывается нормализация уровня аминотрансфераз. При повторном применении лекарства, ранее уже вызвавшего гепатит, рецидив осложнения рассматривается как результат действия данного лекарства.
В ряде работ указывается на необходимость дифференциальной диагностики между медикаментозными гепатитами и вирусными гепатитами, гепатомой, первичным билиарным циррозом печени, алкогольным гепатитом. Кроме того, важно исключить поражение печени вследствие тяжелого инфекционного заболевания, шока, сердечно-сосудистой недостаточности, глистных инвазий, заболеваний желчных путей.
К исследованиям, позволяющим проводить дифференциальную диагностику лекарственного гепатита с другой возможной патологией печени, относятся биохимические исследования сыворотки крови (спектрпеченочных ферментов), иммуноферментный анализ (маркеры вирусных гепатитов и опухолевого процесса) и инструментальные методы исследования (ультразвуковое исследование, компьютерная томография, лапароскопия с биопсией печени, эндоскопическая ретроградная холангиопанкреатография).
Для коррекции лекарственных поражений печени рекомендовано использовать адеметионин (Гептрал).
Адеметионин (Гептрал) относится к аминокислотам или их производным. Это соединение играет важнейшую роль в биохимических реакциях трансметилирования, транссульфатирования и аминопропилирования, участвует в биосинтезе фосфолипидов, глутатиона, таурина и других биологически активных соединений (рис. 11). При применении адеметионина повышается элиминация свободных радикалов и других токсических метаболитов из гепатоцитов, стимулируются процессы регенерации. В эксперименте показана антифибротическая активность адеметионина. Препарат также оказывает антидепрессивное действие.
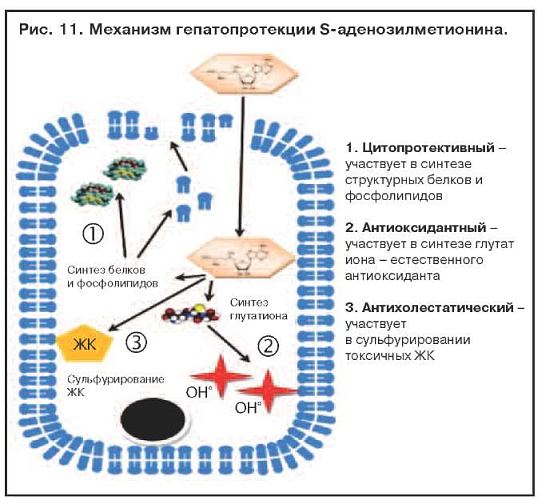
Наличие отчетливого гепатопротекторного действия практически при любой патологии печени, в томчисле при высоких показателях цитолиза и синдроме холестаза, является несомненным преимуществом адеметионина. Наилучшие показатели при лечении адеметионином наблюдаются при токсических гепатитах, в том числе алкогольных. Препарат максимально эффективен при парентеральном введении, так как обладает следующими эффектами:
Это позволяет компенсировать функции печени и увеличивает выживаемость пациентов даже при выраженных изменениях, включая цирроз;
Таким образом, диагностика медикаментозных поражений печени осуществляется на стадии, проявляющейся желтухой, гепатомегалией. Отсюда возникает настоятельная необходимость выявления лекарственных препаратов, применяемых в России и обладающих гепатотоксическим эффектом, описания клинических вариантов течения лекарственных поражений печени, усовершенствования алгоритма дифференциальной диагностики лекарственных гепатитов.
Список использованной литературы
Ключевые слова: лекарственные поражения печени, гепатопротекторы, силибинин, Легалон.
Для цитирования: Логинов А.Ф., Буторова Л.И., Логинов В.А. Лекарственные поражения печени: диагностика, лечение // РМЖ. Гастроэнтерология. 2016. № 11. С. 721–727.
Для цитирования: Логинов А.Ф., Буторова Л.И., Логинов В.А. Лекарственные поражения печени: диагностика, лечение. РМЖ. 2016;11:721-727.
Drug-induced liver injury: diagnosis and treatment
Loginov A.F. 1 , Butorova L.I. 2 , Loginov V.A. 3
1 Faculty of Postgraduate Education, N.I. Pirogov National Medical Surgical Center, Moscow, Russia
2 I.M. Sechenov First Moscow State Medical University, Russia
3 Outpatient Clinic No. 2 of the Department of Presidential Affairs, Moscow, Russia
Drug-induced liver injury (DILI) is a heterogeneous group of clinical morphological variants of liver damage caused by the drugs in recommended standard therapeutic doses due to the direct toxic (usually predictable), toxic immunological (idiosyncratic) or allergic effect. The range of clinical presentations is wide and often similar to "classic" liver disorders. The diagnosis is based on a detailed history of the drugs used by a patient. Patients with moderate liver damage undergoing long-term treatment with hepatotoxic drugs in outpatient care units should take silymarin to protect their liver against pharmaceuticals as early as possible.
In most cases, hepatoprotective silymarin-containing drug with high bioavailability (Legalon) effectively prevents liver damage (in patients receiving drugs with known hepatotoxic properties) or treats verified mild-to-moderate DILI. This agent inhibits liver fibrosis, recovers intrinsic liver antioxidant systems, and provides anti-inflammatory, regenerative, and metabolic effects. Legalon should be taken throughout the treatment with hepatotoxic drug.
Key words: drug-induced liver injury, hepatoprotector, silybin, Legalon.
For citation: Loginov A.F., Butorova L.I., Loginov V.A. Drug-induced liver injury: diagnosis and treatment // RMJ. Gastroenterology. 2016. № 11. P. 721–727.
В статье освещены вопросы диагностики и лечения лекарственных поражений печени



Диагностика лекарственных поражений печени
Ранняя диагностика ЛПП представляет особую важность из-за высокого риска прогрессирования заболевания без отмены препарата. Возможность поражений такого рода учитывается при нарушении функции печени у пациентов, принимающих различные лекарственные препараты и препараты альтернативной медицины.
В связи с большим количеством малосимптомных лекарственно-ассоциированных заболеваний печени у больных, получающих гепатотоксичные лекарственные препараты, и при полипрагмазии целесообразно регулярно (не реже 1 р./2 нед., а при длительной терапии – 1 р./мес.) определять активность аминотрансфераз, ЩФ и уровень билирубина в сыворотке крови. Если активность трансаминаз повышена более чем в 3 раза, препарат отменяют. Альтернативой отмены препарата, а также при необходимости продолжения лечения гепатотоксичным препаратом, является снижение дозы гепатотоксиканта с приемом перорального гепатопротектора. Препаратом выбора в такой ситуации являются лекарства на основе силимарина (Легалон). Показание к немедленной отмене препарата – появление у больного лихорадки, сыпи или зуда.
Основу диагностики ЛПП составляет тщательно собранный анамнез о применяющихся лекарственных препаратах с оценкой длительности и дозы получаемых средств, выяснением возможности их приема в прошлом. Следует обязательно уточнить ближайший анамнез, узнать, не имел ли место прием биологических активных добавок к пище. Они формально не являются лекарственными препаратами, однако обычно позиционируются в качестве средств лечения широкого спектра заболеваний, в т. ч. и болезней печени, при этом субстанции, входящие в состав подобных средств, нередко обладают выраженными гепатотоксичными свойствами (табл. 4).

Диагноз поражений печени, ассоциированных с лекарственными средствами, является в большинстве случаев диагнозом исключения. Вариант диагностического алгоритма представлен в таблице 5.


Легалоном следует сопровождать лекарственную терапию с первых дней лечения, т. к., по данным многочисленных исследований, более ранний старт гепатопротективной защиты значительно снижает риск хронизации заболевания.
Препарат целесообразно применять у больных с ЛПП с клиническими и биохимическими признаками активности профилактическими курсами при необходимости длительного приема гепатотоксичных препаратов (например, цитостатиков, НПВП, антиаритмических средств, антидепрессантов, контрацептивов и т. д.), при вынужденной полипрагмазии (особая группа риска – женщины после 40 лет). Лекарственную терапию пациентам с указанием в анамнезе на диффузные заболевания печени любой этиологии или страдающим алкогольной и никотиновой зависимостью следует также проводить в сочетании с приемом Легалона. Работникам вредных химических производств рекомендуется профилактический прием препарата.
Способы применения:
1. При ЛПП с умеренно выраженным цитолитическим синдромом: по 70 мг 3 р./сут в течение 3–4 мес.
2. При тяжелых ЛПП: 140 мг 3 р./сут 3–4 нед., с переходом на поддерживающие дозы 70 мг 3 р./сут 3–4 мес.
3. При хронических интоксикациях печени (лекарствами, промышленными, бытовыми гепатотоксичными соединениями): по 70 мг 3 р./сут курсами по 3–4 мес. 2–3 р./год.
4. При необходимости медикаментозной терапии пациентам с диффузными заболеваниями печени любой этиологии: 140 мг 3 раза на время проведения лечения и далее по 70 мг в течение 3–4 мес.
5. Для профилактики ЛПП работникам вредных производств: по 70 мг длительно.
Лечение ЛПП остается традиционно трудной проблемой для практических врачей. Отмена гепатотоксичного препарата зачастую невозможна без создания непосредственной или отсроченной угрозы для жизни пациента, либо без существенного ухудшения качества его жизни. Вместе с тем широко известные данные о способности ткани печени к регенерации позволяют достаточно оптимистично оценивать перспективы и потенциальные возможности патогенетической терапии лекарственно-индуцированных повреждений печени гепатопротекторами.
1 Управление по контролю за качеством пищевых продуктов и ле-
карственных препаратов (FDA, Food and Drug Administration) – пра-
вительственное агенство, подчиненное Министерству здравоохра-
нения США.
2 Европейское агентство лекарственных средств (EMEA, European
Medicines Agency) – агентство по оценке лекарственных препара-
тов на их соответствие требованиям, изложенным в Европейской
фармакопее.
Представлен литературный обзор по проблеме неалкогольной жировой болезни печени (НАЖБП), включающий данные об эпидемиологии, патогенезе, клинических особенностях, диагностике и лечении при сахарном диабете. Приведены данные о влиянии сахароснижающей терапии на прогрессирование или обратное развитие НАЖБП.
В течение последнего десятилетия жировая болезнь печени (НАЖБП) стала одной из наиболее обсуждаемых тем гастроэнтерологической и терапевтической практики. Этот термин обозначает феномен, при котором в печени происходит накопление жира, преимущественно триглицеридов и ЛПОНП, в меньшей степени холестерина и ЛПНП. Жировая болезнь печени не имеет шифра в МКБ-10 и, по сути, является клинико-морфологическим понятием, объединяющим целый ряд социально значимых заболеваний, при которых жировая инфильтрация является ранним и чувствительным маркером глубоких нарушений метаболизма [2].
Наиболее частыми причинами являются злоупотребление алкоголем, сахарный диабет и морбидное ожирение с нарушением толерантности к глюкозе [2]. Бессимптомное течение заболевания, трудности его диагностики, отсутствие единой концепции лечения НАЖБП актуальные проблемы, требующие более углубленного изучения и заслуживающие пристального внимания широкого круга специалистов.
Определение
Неалкогольная жировая болезнь печени распространенное хроническое заболевание печени, характеризующееся патологическим накоплением жировых капель, не связанное с употреблением алкоголя.
НАЖБП включает спектр состояний, начиная от простого стеатоза через воспалительный стеатогепатит (НАСГ) с повышенным фиброзом, затем к развитию цирроза и печеночной недостаточности в финале [1].
Безопасным количеством алкоголя в сутки считается:
• 30 г алкоголя для мужчин и 20 г для женщин
• 350 мл пива
• 120 мл вина
• 45 мл крепких напитков
Современное понятие НАЖБП охватывает спектр поражений печени, включающий в себя три ее основные формы: жировой гепатоз (ЖГ), неалкогольный (метаболический) стеатогепатит (НАСГ) и цирроз (как исход прогрессирующего НАСГ). Редко исходом НАСГ может являться гепатоцеллюлярная карцинома. Морфологическим критерием жирового гепатоза является содержание триглицеридов в печени свыше 510% сухой массы. Содержание ТГ при НАЖБП может достигать 40% от массы печени (при норме около 5%).
НАЖБП зачастую является компонентом других заболеваний, таких как метаболический синдром, сахарный диабет, ожирение, и вносит свой вклад в распространенность сердечно-сосудистых заболеваний (ССЗ) среди населения.
Эпидемиология
НАЖБП самая частая причина нарушения печеночных проб; у взрослых лиц в США данное заболевание является причиной 70% бессимптомного повышения уровня трансаминаз. В популяционном исследовании, в котором использовалась высокочувствительная методика - МР-спектроскопия, с включением 2 287 пациентов (США) было показано, что распространенность НАЖБП составляет 32%.
Менее чувствительные методы, такие как ультразвуковое обследование, в популяционных исследованиях в Японии, Китае и Италии выявили показатель распространенности на уровне от 13% до 25%. НАЖБП не ограничивается только взрослыми; 10% детей и подростков в США также страдают НАЖБП.
Распространенность ожирения среди пациентов с НАЖБП находится в диапазоне 61-100%, а дислипидемии - 27-67%. Среди тяжело больных пациентов с ожирением, которым планируется проведение бариатрических вмешательств, НАЖБП выявляется в 90% случаев. Истинная распространенность НАЖБП неизвестна, однако, по оценкам последних исследований, распространенность НАЖБП и НАСГ среди общего числа населения может достигать 20-24 и 3% соответственно. Проведенные исследования показали, что при заболеваниях, сочетающихся с инсулинорезистентностью, характерные изменения со стороны печени выявляются в 74% случаев.
Неалкогольный стеатогепатит (НАСГ) – заболевание, для которого характерны повышение активности ферментов печени в крови и морфологические изменения в биоптатах печени, подобные изменениям при алкогольном гепатите, – жировая дистрофия (ЖД) с воспалительной реакцией и фиброзом; однако больные с НАСГ не употребляют алкоголь в количествах, способных вызывать повреждение печени. До сих пор не выяснены точные механизмы фиброгенеза печени. Фиброз выявляется у 20–37% пациентов с НАЖБП. У 20% из них в течение 20 лет формируется цирроз с развитием печеночно-клеточной недостаточности. Популяционные исследования позволяют предположить, что 60–80% криптогенных циррозов печени являются исходами НАСГ. Установлено, что сочетание сахарного диабета 2-го типа (СД 2) и неалкогольного стеатогепатита в 2–2,5 раза увеличивает риск развития цирроза печени и гепатоцеллюлярной карциномы. Кроме того, у больных с НАЖБП в сочетании с СД и без диабета установлена более высокая распространенность ССЗ, чем у пациентов без НАЖБП вне зависимости от тучности и традиционных факторов риска ССЗ.
Вторичное поражение печени возможно под воздействием многих причин: приема ряда лекарственных препаратов, нутрициологических факторов, хирургических вмешательств, метаболических или генетических, токсических и др.
В норме печень только перерабатывает поступающие с пищей ингредиенты и осуществляет их разрушение, синтез новых соединений и выделение (рис. 1).
У здоровых в печени не должно задерживаться более 5% триглицеридов. Однако при патологии происходит отложение избыточного количества липидов в печени.
Клиническая картина
Клиническая картина обычно скудная. Жалобы на дискомфорт в области эпигастрия. Выявляется бессимптомное повышение уровней аминотрансфераз. Необъяснимое существование постоянной гепатомегалии. Обращает на себя внимание наличие ожирения, acanthosis nigracans (обязательный признак инсулинорезистентности).
У небольшого количества могут быть признаки цирроза печени в виде спленомегалии, варикозного расширения вен и т. п.
Для постановки диагноза НАЖБП необходимо исключение всех других причин, приводящих к гепатомегалии (алкоголь, лекарства, недостаток белкового питания, ядовитые грибы, органические растворители и др.).
Главными в постановке диагноза НАЖБП являются лабораторные данные (показатели цитолиза) и инструментальные методы исследования.
Лабораторные данные
Показатели синдромов цитолиза:
• повышение активности АЛТ и АСТ аминотрансфераз не более чем в 4–5 раз, индекс АСТ/АЛТ не более 1, чаще повышена активность АЛТ; более высокие уровни могут наблюдаться при некровоспалительных формах
Показатели холестаза
• Повышение активности щелочной фосфатазы и γ-глутамилтранспептидазы обычно не более чем до 2 норм
• Повышение прямого билирубина
Показатели обмена железа
• Повышение ферритина у 20–50% больных
• Повышение трансферрина в 5–10% случаев
Другие изменения
• Гипертриглицеридемия, гиперхолестеринемия
• Гипергликемия (НТГ или СД 2)
• Гипоальбуминемия, тромбоцитопения, увеличение протромбинового времени у пациентов с далеко зашедшей стадией НАЖБП
Методы визуализации печени
• Ультразвуковая диагностика
• Компьютерная томография
• Магниторезонансная томография
• Магниторезонансная спектроскопия
• Биопсия печени
Золотым стандартом диагностики и определения стадии развития НАЖБП по-прежнему является пункционная биопсия печени.
Показаниями для выполнения биопсии печени являются: возраст старше 45 лет и хронический цитолиз неустановленной этиологии; сочетание хронического цитолиза неустановленной этиологии по крайней мере с двумя проявлениями МС, независимо от возраста [4].
• Биопсия печени не показана в тех случаях, когда уровень сывороточных аминотрансфераз в норме [5].
Лица с НАЖБП имеют более высокий риск смерти по сравнению с общей популяцией (относительный риск выше на 34%). Прогноз у лиц с НАЖБП зависит от подтипа болезни. Отмечают более низкую смертность при установленном при биопсии стеатозе без воспаления и фиброза. НАСГ, в противоположность этому, более часто прогрессирует с исходом в цирроз или гепатоцеллюлярную карциному, печеночную недостаточность, требующую трансплантации печени. Лица с НАСГ имеют повышенный риск заболеваний сердца и сердечной смертности [6].
Лечение НАЖБП
Многочисленные данные о влиянии снижения массы тела на состояние печени весьма противоречивы. Показано, что быстрая потеря массы тела закономерно приводит к нарастанию активности воспаления и прогрессии фиброза. В то же время ее снижение на 1120 кг/год положительно влияет на выраженность стеатоза и воспаления, степень фиброза печени. Безопасной считается потеря веса до 1 600 г в неделю для взрослых и до 500 г в неделю для детей, достигаемое при суточном калораже 25 кал/кг и активных физических упражнениях. Необходимыми условиями для устранения главного патогенетического фактора НАЖБП инсулинорезистентности, также являются действия, направленные на снижение веса: изменение образа жизни, гипокалорийное питание, расширение двигательной активности. Для лиц с избыточной массой тела и ожирением реально достижимая цель – снижение массы тела примерно на 7–10% за 6–12 мес.
Физическая нагрузка играет определенную роль в лечении и метаболического синдрома (МетС), и НАЖБП. Тренировки на кардиореспираторную выносливость модулируют взаимоотношения между МетС и фатальными состояниями, обеспечивая мощный защитный эффект против общей смертности и смертности вследствие сердечно-сосудистых осложнений, а также накопления жиров в печени и степенью его выраженности [7, 8].
Хирургическое лечение
Бариатрическая хирургия как метод снижения веса у пациентов с НАЖБП показала снижение смертности в долгосрочной перспективе, в частности у пациентов с СД 2. Снижение веса после бариатрических операций также связывается с улучшением проявлений гепатостеатоза и воспаления; однако не было показано, что при этом достигается улучшение показателей фиброза. Опубликован метаанализ 15 рандомизированных исследований, включавших 766 пар биопсий печени у больных с НАЖБП, опубликованных до 2008 г. Улучшение гистологической картины отмечено по стеатозу – у 92%, по стеатогепатиту – у 81%, фиброзу – у 65,5%. Полное разрешение НАСГ было достигнуто у 69,5% пациентов. Однако при наблюдении через 1 год и 5 лет после бариатрической операции было доказано на биопсии улучшение картины стеатоза, но не было достоверного улучшения показателей воспаления или фиброза [9].
Фармакотерапия
Особый интерес представляют данные о влиянии на развитие НАЖБП пероральных сахароснижающих препаратов-сенситайзеров, снижающих инсулинорезистентность.
Тиазолидиндионы (пиоглитазон и розиглитазон) - это агонисты γ-рецепторов, активируемых пролифераторами пероксисом, которые обеспечивают перераспределение жира из мышц и печени в периферическую жировую ткань и, таким образом, снижают проявления инсулинорезистентности, однако стимулируют набор веса. В пяти относительно небольших рандомизированных контролируемых исследованиях длительностью от 6 до 24 мес. была показана эффективность тиазолидиндионов у пациентов с НАСГ. Эта группа препаратов имеет сегодня ограниченное применение в силу ряда причин: высокий риск развития сердечной недостаточности, выраженные отеки и риск переломов.
Эффекты бигуанидов [10] обусловлены уменьшением глюконеогенеза и синтеза липидов в печени, реализуемого через активацию цАМФ-зависимой протеинкиназы печени, что приводит к снижению синтеза ТГ из жирных кислот и митохондриального β-окисления. Кроме того, бигуаниды подавляют экспрессию ФНО-α в печени и индуцированных этим цитокином механизмов, приводящих к стеатозу, а также экспрессию SREBP-1 в гепатоцитах. Основным механизмом действия метформина на повышение фибринолиза является снижение уровня PAI-1, что имеет место у больных СД 2 вне зависимости от его дозы. Помимо снижения PAI-1, метформин уменьшает также и пролиферацию гладкомышечных клеток в сосудистой стенке in vitro и скорость атерогенеза у животных [10]. Потенциальные эффекты метформина представлены в таблице 1.
Проведены исследования, сравнивающие эффективность применения метформина и диетотерапии. В исследование было включено 20 пациентов (без СД и ожирения). Проводилась оценка функции печени и уровня инсулина и инсулинорезистентности (в эугликемии и гиперинсулинемии при проведении клэмп-теста). Биопсия печени была проведена 14 больным, которые получали метформин (500 мг х 2 р/д), и шести пациентам, находившимся на диетотерапии в течение четырех месяцев. Оценка гистологического улучшения не проводилась. Единственное существенное различие между двумя группами было в уровне АЛТ. Группы пациентов не отличались значимо по показателям снижения веса. Хотя проводимое активное лечение вызвало повышение уровня молочной кислоты (до 30% активно леченых пациентов), но только у одного пациента показатель лактата выходил за рамки нормального диапазона более 2 ммоль/л (2,2 ммоль/л). Uygun с соавт. проводили исследования, включавшие 36 пациентов с НАСГ, разделенных на 2 группы: одна группа получала метформин в дозе 850 мг вместе с диетой, контрольная группа была ограничена в питании (1 6001 800 калорий в день). По сравнению с группой контроля, в первой группе были выявлены улучшения по следующим показателям: снижение уровня АЛТ (с 83,5 ± 24,6 до 46,4 ± 23,3 Ед/л, соответственно p = 0,0001) и АСТ (57,9 ± 17,3 против 35,8 ± 10,5 Ед/л, р = 0,0001). В контрольной же группе: АЛТ (с 72,8 ± 31,2 до 55,4 ± 16,3 Ед/л, р = 0,001) и АСТ (с 48,1 ± 26,3 до 41,3 ± 13,5 Ед/л, p = 0,06). Изменений в печени, при биопсии у пациентов после лечения не наблюдалось [10]. В других исследованиях по оценке эффективности метформина было показано улучшение показателей индекса инсулинорезистентности (по оценке QUICKI, HOMA или KITT методов). В трех исследованиях сообщалось о снижении показателей функции печени и одно исследование показало незначительное увеличение этих показателей. Изучение эффективности метформина (1 500 мг/сут или 20 мг/кг/сут) в терапии (46 мес.) больных НАСГ показало, что на фоне снижения массы тела (около 1,5 кг/мес) происходит нормализация трансаминаз, уменьшаются гиперхолестеринемия, гипертриглицеридемия и гепатомегалия. Верифицирована аналогичная экспериментальным данным положительная гистологическая динамика [10].
Агонисты ГПП-1 разрешены к применению как препараты 1 и 2 ряда при диабете 2-го типа. Они работают не как препараты, непосредственно повышающие чувствительность к инсулину, но, нормализуя уровень глюкозы и индуцируя клинически значимое снижение веса, они в итоге позволяют повысить чувствительность к инсулину.
С учетом таких благоприятных эффектов агонисты ГПП-1 могут быть отличными кандидатами на роль препарата, применяемого для лечения и НАЖБП. В исследованиях на животных было показано, что агонисты ГПП-1 обладают прямым действием на метаболизм липидов в гепатоцитах. В клинических условиях в рамках открытого клинического исследования эксенатида у больных СД был показан благоприятный эффект в отношении чувствительности к инсулину и возврат повышенных показателей аминотрансфераз к нормальным значениям в 41% случаев [11].
НАЖБП развивается у значительной доли пациентов с СД 2; при этом данное состояние зачастую остается недиагностированным. У пациентов с СД 2 и НАЖБП заболевание протекает более агрессивно по сравнению с пациентами с НАЖБП, но без СД 2, и у них выше риск развития цирроза печени, терминальной стадии печеночной недостаточности и гепатоцеллюлярной карциномы. У пациентов с диабетом и НАЖБП выше риски смерти от сердечно-сосудистых и онкологических заболеваний, что может говорить о присутствии системной воспалительной реакции.
Выявление и четкий контроль метаболических факторов риска остается основным направлением для терапевтических мероприятий. Хотя фармакотерапия и имеет некоторые перспективы, необходимо проведение дальнейших клинических исследований для оценки эффективности разных препаратов и их возможности повлиять на течение НАЖБП. В связи с отмечающимся неуклонным ростом распространенности среди населения ожирения, метаболического синдрома и сахарного диабета проблема диагностики и лечения НАЖБП будет приобретать еще большую актуальность. Слабое освещение в медицинской литературе приводит к малой информированности врачей о возможных исходах этого состояния и представляет огромную проблему. Сложность верификации диагноза, поиск достоверных и высокоинформативных маркеров заболевания и новых неинвазивных методов диагностики делает необходимым проведение дальнейших многоцентровых исследований, которые планируются в настоящее время.
Читайте также:

