Вирус герпеса биохимический анализ крови
Обновлено: 26.04.2024
Вирус простого герпеса I и II типа
В качестве биологического материала для данного исследования используется кровь с ЭДТА. Для подготовки к анализу нужно за 3 часа до проведения манипуляции отказаться от употребления пищи. Можно пить только негазированную очищенную воду.
Вирус простого герпеса – вирус с содержанием ДНК. Существует 2 серотипа патогена – вирус простого герпеса 1 и 2 типа.
ВПГ-1 часто становится причиной развития поражений слизистой оболочки полости рта, глаз и кожи. В редких случаях может развиться поражение гениталий. Также вирус простого герпеса 1 может вызвать герпетический энцефалит и пневмонит. Вирус простого герпеса 2 типа в большинстве случаев вызывает поражение гениталий, герпес у новорожденных детей, диссеминированный герпес.
Вирус простого герпеса очень опасен во время беременности. Если патоген циркулирует в крови, велика вероятность самопроизвольного выкидыша, развития тяжелых поражений плода и младенца, формирования врожденных уродств.
В лабораторных условиях несложно обнаружить ДНК вируса простого герпеса в биологическом материале пациента. С помощью исследования можно обнаружить оба типа вируса.
Направление на анализ выдается в следующих случаях:
- Наличие характерной симптоматики заболевания (специфические высыпания на любой части тела);
- Отягощенный акушерский анамнез (потеря ребенка во время родов, рождение младенца с серьезными пороками развития);
- Подозрение на герпес в период беременности (те женщины, у которых во время ультразвукового исследования обнаруживаются признаки внутриутробной инфекции, лимфоаденопатии, а также с подозрением на гепатит и гепатоспленомегалию неясного происхождения)
- Признаки внутриутробной инфекции у детей, а также наличие врожденных пороков развития, везикулы или корочки на коже или слизистых оболочках;
- Новорожденные младенцы с сепсисом, гепатитами, пневмонией, поражением глаз или желудочно-кишечного тракта;
- Комплексное обследование пациентов, у которых наблюдается иммунодефицитное состояние.
Допустимого значения в интерпретации результатов анализа не существует. Если ДНК вируса простого герпеса в биологическом материале обнаружен, это говорит о том, что человек является носителем патогена.
Расшифровка анализа на вирус простого Герпеса
Антитела к вирусу простого герпеса 1 и 2 типа
Повышенная концентрация специфических иммуноглобулинов класса G свидетельствует о том, что вирус в организме пациента однозначно присутствует и уже давно. Однако данный анализ никогда не проводится однократно – для определения динамики развития заболевания его необходимо повторить через 10 дней с момента первой сдачи биологического материала. И вот если к тому времени концентрация вирусных клеток в организме повысится более, чем на 30%, это говорит о том, что инфекция активно прогрессирует и скоро даст о себе знать.
Кроме того, повышение концентрации специфических антител класса G в крови беременной женщины может говорить о том, что у плода присутствует внутриутробная инфекция. Здесь необходимо смотреть по состоянию пациентки, изучать показатели других анализов, а также результаты ультразвукового исследования плода. Также в случае, если у пациентки вирус герпеса присутствовал еще до беременности, вероятность развития внутриутробной инфекции у плода значительно снижается.
При обнаружении в крови антител класса А нельзя точно сказать, в какой фазе на данный момент находится заболевание. Но с высокой долей вероятности медик может судить, что пациент заражен.
Если же обнаружены антитела класса М, это говорит о том, что на момент забора биологического материала инфекция находилась в активной фазе. Выработка специфических иммуноглобулинов данного класса говорит о том, что с момента инфицирования прошло минимум 2 недели. Диагноз зависит от концентрации данных иммуноглобулинов – чем их больше, тем агрессивней ведет себя инфекция в организме.
Если же результат анализа на герпес оказался отрицательным, это свидетельствует о том, что пациент с данным патогеном не сталкивался. Есть ряд условий, при которых исследование может быть ложноположительным, однако такое случается крайне редко.
За последние пять лет увеличилось число детей в возрасте до одного года, умерших от генерализованных вирусных инфекций [4]. Велика роль герпес-вирусных инфекций, особенно цитомегаловирусной, в формировании перинатальной патологии и младенческой смертности. Риск развития внутриутробной инфекции зависит от характера взаимоотношений между организмом беременной женщины и микроорганизмом (первичное заражение во время беременности или реактивация ранее приобретенной инфекции).
Проблема врожденной инфекционной патологии является приоритетной для России [5].
Иммуногенез герпес-вирусной инфекции. Длительное нахождение герпес-вируса в организме человека становится возможным благодаря сложной стратегии противоборства и ускользания от иммунной системы хозяина. В достижении этого состояния можно выделить три пути стратегии возбудителя:
Вирус простого герпеса. В инфицированных клетках вирус простого герпеса образует внутриядерные включения и гигантские клетки, оказывает выраженное цитопатическое действие, проявляющееся округлением и образованием многоядерных клеток. Вирус является слабым индуктором интерферона, в связи с чем инактивация вирусной ДНК внутри клеток не наступает и он сохраняется внутри клеток длительное время, периодически вызывая рецидивы заболевания.
ЦМВ. Сущность проблемы ЦМВ-инфекции в том, что последняя относится к так называемым оппортунистическим инфекциям, клинические проявления которых возможно в условиях первичного или вторичного иммунодефицита.
ЦМВ поражает разнообразные клетки, чаще всего лейкоциты (лимфоциты, моноциты), эпителиальные клетки (дыхательных путей, слюнных желез, почек). С клеток крови ЦМВ с большим постоянством переходит на эндотелий, тропизм к которому у него весьма выражен. Поврежденные эндотелиальные клетки постоянно обнаруживаются в токе крови при активной/реактивированной ЦМВ-инфекции. Повреждение эндотелия сосудов имеет собственное патогенетическое значение в формировании органных поражений, так как вызывает ишемию или кровоизлияния в различные ткани [6].
В раннем неонатальном периоде (0–7 дней) у детей с ЦМВ-инфекцией наблюдались симптомы интоксикации, серый колорит кожи, выраженная мышечная гипотония, большая первоначальная потеря массы тела, синдром рвоты или срыгиваний, признаки угнетения ЦНС. В позднем неонатальном периоде (от 7 дней до одного мессяца) анализ клинических проявлений острой ЦМВ-инфекции выявляет поражение многих органов и систем. Так, у всех детей обнаруживаются гипоксически-ишемическая энцефалопатия с трансформацией синдрома угнетения в синдром гипервозбудимости, проявления анемии, патологическая гипербилирубинемия, увеличение печени и селезенки.
ВЭБ относится к подсемейству бета-герпес-вирусов. Вирусный геном заключен в нуклеокапсид, который покрыт гликопротеидным тегументом gp350, являющимся фактором рецепторного взаимодействия [7]. Проникновение вируса в В-лифоциты осуществляется через рецептор этих клеток CD21-рецептор к C3d-компоненту комплемента. ВЭБ-инфекция широко распространена среди людей, причем первичное инфицирование, как правило, происходит в антенатальном или детском возрасте, но манифестация ВЭБ-инфекции в виде отчетливых клинических проявлений инфекционного мононуклеоза в большинстве случаев происходит в школьном возрасте при различного рода иммунопатологических реакциях. Манифестация инфекции в виде инфекционного мононуклеоза может осложняться поражением печени, слизистой оболочки желудка, ткани почек, лимфоидного аппарата.
Особый характер взаимодействия микро- и макроорганизма при хронических персистирующих инфекциях обусловливают трудности лабораторной диагностики. Обнаружение возбудителя не может быть единственным критерием подтверждения диагноза. Необходима комплексная оценка клинических и лабораторных данных для постановки диагноза.
Цель исследования. Определить клинические особенности течения персистирующих герпес-вирусных инфекций у детей и оценить значимость комплекса лабораторных исследований, в том числе показателей общей иммунологической реактивности у больных при персистирующем у них инфекционном процессе.
Материал и методы исследований. Под наблюдением находилось 63 пациента в возрасте от одного месяца до 7 лет, из них детей до одного года было 25, от одного года до трех лет — 22 и старше трех лет — 15 больных. Среди обследованных детей преобладали пациенты первых двух лет жизни — 47 детей (74,6%) и старше двух лет было 15 больных (25,4%).
Результаты. В клинической диагностике персистирующих инфекций у детей следует отводить первостепенное значение неблагополучию акушерского анамнеза матерей больных детей.
Беременность и роды были осложненными у большинства матерей наблюдаемых детей, чаще всего у них отмечались гестозы и угроза выкидыша, рождение недоношенных, в родах гипоксия плода, преждевременная отслойка плаценты, кесарево сечение и др. У 32 женщин из 63 (50,7%) были различные соматические заболевания (хронический пиелонефрит, кольпит, анемия, аутоиммунный тиреоидит и др.). При обследовании беременных женщин было выявлено как моноинфицирование (у 30 из 63–47,6%), так и сочетания инфекций (у 16 из 63–25,4%). Наиболее часто обнаруживались герпес-вирусы и цитомегаловирусы (суммарно у 27 женщин из 63–43%) и реже другие возбудители — хламидии, микоплазмы (у 11 беременных — 17,4%). Высокая частота вышеуказанных осложнений свидетельствует о несомненной роли инфекции как отягощающего фактора в течение гестационного периода и родов.
Заподозрить внутриутробную или персистирующую инфекцию у детей можно было по высокой степени поражения у детей различных органов и систем: ЦНС (71,4%), органов дыхания (88,8%), желудочно-кишечного тракта (95,2%), поражению глаз (31,7%), лимфатического аппарата (15,9%).
В процессе наблюдения за детьми в недалеком прошлом все дети обследовались на состояние микробиоценоза кишечника.
У всех детей обнаруживались нарушения как в основных компонентах биоценоза, так и в составе условно-патогенной флоры. Следует отметить, что у всех пациентов проводилась коррекция микробиоценоза повторными курсами пре- и пробиотиков, однако восстановления микрофлоры до нормобиоценоза не наблюдалось ни у одного пациента. Следовательно, без выявления и адекватного лечения основного заболевания не удается курировать дисбиотические нарушения в организме ребенка.
Закономерен вопрос о правильности выбора комплекса диагностики внутриутробной и персистирующей инфекции у детей. В зависимости от возраста пользуются разными методами диагностики. Важное значение отводится сбору семейного анамнеза. Диагностика внутриутробных инфекций у детей должна опираться на клинические проявления как общего характера, так и на типоспецифические ее признаки, а также основываться на анализе комплекса лабораторных методов обследования [8].
При оценке клинических анализов крови у наблюдаемых детей обращали на себя внимание значительные отклонения в различных показателях гемограммы: выраженная анемизация (у 31,7% пациентов), нейтропения (у 19%), лимфоцитоз (у 27%), лейкопения с лимфоцитопенией (36,5%), ускорение СОЭ (у 27%), что в совокупности свидетельствовало о наличии воспалительного процесса в организме с выраженным снижением иммунореактивности у детей.
При скрининговом серологическом обследовании методом ИФА на внутриутробные инфекции у детей наиболее часто выявлялись положительные титры типоспецифических антител класса IgM и/или IgG к герпес-вирусам. Диагностические титры антител класса IgM и IgG определялись к ЦМВ (у 9 детей), к HV 1-го, 2-го типа (у 9 детей). Антитела к антигенам ВЭБ обнаруживались у 20 детей, из них у 10 детей были антитела класса IgG к раннему антигену ВЭБ и антитела класса IgM к капсидному антигену ВЭБ, что свидетельствовало об активной фазе ВЭБ-инфекции. Остальные 10 пациентов имели антитела класса IgG к нуклеарному (ядерному) антигену ВЭБ, что расценивалось как поздняя стадия инфекции.
У детей при персистирующем течении с реактивацией инфекции, которое чаще возникало после провоцирующих воздействий (ротавирусные диареи, ОРВИ, профилактические прививки) ПЦР-тесты при исследовании биосубстратов: кровь, осадок мочи, секрет из зева давали положительные результаты с последующим нарастанием титра типоспецифических антител по данным ИФА.
Совокупность проведенных исследований позволила выделить у обследованных больных следующие формы инфекций: моноинфекции были у 21 пациента — 31,8% (ЦМВ — у 5 детей, HV 1-го, 2-го типа — у 6 детей и ВЭБ — у 10), у 42 детей из 63 (68,2%) обнаруживались микст-инфекции. У 23 детей была ассоциация ЦМВ с герпес-вирусами (у 9 детей с HV 1-го, 2-го типа, у 3 детей — с HV 6-го типа и у 11 детей — с C. albicans и хламидиями). Микст-формы герпеса 1-го, 2-го типа были выявлены у 9 больных, у них были ассоциации с микоплазмами и хламидиями. Ассоциации ВЭБ были обнаружены у 10 детей (5 больных имели ассоциацию с ЦМВ, пациента — с HV 6-го типа и 2 больных — с Yersinia pseudotuberculosis).
Из 63 больных у 21 (33,3%) с моноинфекцией течение заболевания расценивалось как латентное (с ЦМВ-инфекцией у 5 и HV 1-го, 2-го типа у 6) и как персистирующее (у 10 детей с ВЭБ-инфекцией). У 14 детей из 42 с микст-инфицированием (у 1/3) было персистирующее течение инфекционного процесса (у 3 детей с ЦМВ-инфекцией в ассоциации с HV 6-го типа и у 11 детей с ЦМВ-инфекцией в ассоциации с C. albicans и хламидиями). У 28 детей из 43 (у 2/3) наблюдалось персистирующее течение с реактивацией инфекции (у 9 детей с ЦМВ-инфекцией в ассоциации с HV 1-го, 2-го типа; у 9 детей с HV 1-го, 2-го типа в ассоциации с хламидиями или микоплазмами и у 10 детей с ВЭБ инфекцией в ассоциации с ЦМВ, HV 6-го типа и ВЭБ в ассоциации с Y. pseudotuberculosis).
Коэффициент фагоцитарной защиты у детей с моноинфицированием и микст-формами герпесвирусной инфекции оказался достоверно сниженным по сравнению со средневозрастной нормой для здоровых детей (0,634 ± 0,05 усл. ед. и 0,540 ± 0,03 усл. ед. соответственно при норме 0,946 ± 0,03, Р1–2 и Р2–3 < 0,001 и < 0,001 соответственно). При микст-инфицировании герпес-вирусами КФЗ имел более низкие значения по сравнению с таковым у детей с -моноинфекцией, однако разница недостоверна (Р1–2 > 0,05). Недостаточность защиты клеточно-фагоцитарного звена иммунитета играет важную роль в патогенезе герпес-вирусных инфекций, что должно учитываться в лечении этих заболеваний.
Отклонение величины показателя ИЛМП имело противоположную направленность, она оказывалась достоверно повышенной как при моноинфекции, так и при микст-формах герпес-вирусных инфекций по сравнению с контролем (Р1–3 и Р2–3 < 0,001 и < 0,001 соответственно). Величины показателя ИЛМП у детей с микст-инфицированием была большей по сравнению с таковой при моноинфекции, однако разница недостоверна Р1–2 > 0,05. Увеличение показателя ИЛМП у детей с герпес-вирусной инфекцией еще раз подтверждает лимфотропность вирусных антигенов.
ЛИИ оказался достоверно повышенным у больных с микст-формами герпес-вирусной инфекции по сравнению со средневозрастной нормой в контроле (Р2–3 < 0,001). Средние значения ЛИИ у детей с моноинфекцией достоверно не отличались от норматива (Р1–3 > 0,05), они имели лишь тенденцию к повышению. Однако при оценке индивидуальных показателей ЛИИ у детей с моноинфицированием герпес-вирусами выявились существенные особенности. У 13 детей из 21 (61,9%) ЛИИ был ниже возрастной нормы, что отражало фазу положительной анергии к совершенно определенному антигену. Это свидетельствует, что организм защищен сейчас только от специфических антигенов, однако он остается уязвимым в отношении других патогенов, то есть низкий индекс интоксикации отнюдь не указывает на полное благополучие организма.
Полученные результаты исследований подтверждают выраженность иммунного дисбаланса как в клеточно-фагоцитарном звене иммунитета, так и в гуморальном, а также свидетельствуют о значимости эндогенной интоксикации у больных с микст-формами герпес-вирусной инфекции и уязвимости иммунной защиты у детей и при моноинфицировании.
Клинический пример. Андрей С., 2 года 5 мес., поступил в стационар с жалобами на высокую температуру — 39 °С, однократную рвоту, сниженный аппетит и жидкий стул 5 раз в сутки. Болен в течение двух недель ОРВИ, получил амбулаторно симптоматическое лечение. К концу второй недели ухудшилось состояние, рецидив лихорадки — 39 °C и дисфункция кишечника. Направлен на госпитализацию.
Анамнез жизни. От первой беременности, протекала с угрозой выкидыша, нефропатией, преэклампсией в родах. Во время беременности перенесла ОPВИ с лимфаденитом. Обследование на пренатальные инфекции, обнаруживались антитела класса IgG к антигенам ЦМВ и вирусу герпеса 1-го, 2-го типа. Лечение не проводилось. Роды в срок, масса при рождении 3500 г, длина 51 см. К груди приложен сразу, сосал активно, грудное вскармливание до года, прикормы вводились в 5 и 6 месяцев. Адаптация к пище нормальная. В массе прибавки достаточные, в 2 г. 5 мес — масса 14 кг 810 г, рост 93 см.
Состояние здоровья в течение первого года жизни неблагополучное. Длительно держалась желтуха, в возрасте 3 недель: общий билирубин — 315,1 мкмоль/л, непрямой — 297,3 мкмоль/л, прямой — 17,8 мкмоль/л. Одновременно с желтухой был неустойчивый стул. В 1-месячном возрасте неврологом установлен диагноз перинатального поражения ЦНС, гипоксическо-ишемического генеза, гипертензионный синдром.
К возрасту 6 мес были обнаружены изменения в гемограмме: гемоглобин — 112 г/л, эритроциты — 4,2 × 10 12 /л, лейкоциты — 7,8 × 10 9 /л, сегментоядерные нейтрофилы — 12%, лимфоциты — 67%, моноциты — 12%, эозинофилы — 8%, базофилы — 1%, СОЭ — 3 мм/час. В повторных анализах крови во 2-м полугодии продолжала выявляться нейтропения. Консультирован гематологом, установлен диагноз доброкачественной нейтропении детского возраста. В 10 мес в анализе крови выявлена анемия (гемоглобин — 107 г/л, эритроциты — 3,81 × 10 12 /л, цветовой показатель — 0,84, тромбоциты — 280 × 10 9 /л, сегментоядерные нейтрофилы — 11%, лимфоциты — 76%, моноциты — 90%, эозинофилы — 3%, базофилы — 1%). Гематологом назначено лечение Сорбифером дурулесом, курс 1 месяц.
Осмотрен ортопедом: отмечено ограниченное отведение бедер. В один год на УЗИ органов брюшной полости определялся перегиб в области шейки желчного пузыря, холестаз. Осмотр генетика: диагностирована недифференцированная дисплазия соединительной ткани с поражением костно-мышечной системы. В 1 г. 5 мес перенес острый энтероколит неуточненной этиологии, госпитализировался в стационар на 10 дней, получал лечение метронидазолом и Энтеролом. В течение 1,5 лет переносит частые ОРВИ с повышением температуры до 38,8 °С в течение 3–4 дней и катаральными явлениями.
Объективные данные. При последней госпитализации отмечались явления назофарингита в течение 5 дней, лихорадка до 39 °С 2 дня, кожные покровы без сыпи. При осмотре — гиперемия зева и увеличение подчелюстных, передних и заднешейных лимфоузлов, стул учащенный до 3 раз в сутки, с 5 дня лечения — оформленный. ЛОР-врачом диагностирован хронический тонзиллит и аденоидит, в фазе обострения.
Обследование. В мазке из зева — высев гемолитического стрептококка. Посевы на патогенную кишечную флору отрицательные. ИФА на ротавирус — отрицательный. Реакция непрямой гемагглютинации (РНГА) с кишечными диагностикумами — отрицательные.
Гемограмма при поступлении: гемоглобин 104 г/л, эритроциты — 3,7 × 10 12 /л, цветовой показатель — 0,85, лейкоциты — 6,4 × 10 9 /л, палочкоядерные нейтрофилы — 4%, сегментоядерные — 72%, лимфоциты — 18%, моноциты — 4%, эозинофилы — 2%, СОЭ — 4 мм/час.
Гемограмма в динамике: гемоглобин — 109 г/л, эритроциты — 3,4 × 10 12 /л, лейкоциты — 7,8 × 10 9 /л, палочкоядерные нейтрофилы — 19%, сегментоядерные — 42%, лимфоциты — 28% (широкоплазменные лимфоциты), моноциты — 8%, плазматические клетки — 1%, эозинофилы — 2%, СОЭ — 13 мм/час. В дальнейшем — красная кровь оставалась без динамики, число лейкоцитов не изменялось, нарастал лимфоцитоз до 43% (широкоплазменные формы), моноцитов до 12%, СОЭ повысилась до 20 мм/час.
Анализ мочи без отклонений от нормы (пятикратно). В биохимическом анализе крови — умеренная гипоальбуминемия, печеночные пробы — в норме. ИФА на специфические антитела к антигенам ЦМВ класса IgM — отрицательный, класса IgG — положительный. Маркеры ДНК-ЦМВ в осадке мочи и в секрете из зева методом ПЦР не найдены. ИФА на специфические антитела к хламидийному антигену (Chlamydia pneumoniae) — положительный в титре 1:80. Маркеры ДНК Ch. pneumoniae в мазке из носоглотки методом ПЦР — положительный. ИФА с микоплазменным антигеном — IgM и IgG — отрицательные, с герпес-вирусами 1-го, 2-го типа — IgM и IgG отрицательные. ИФА на специфические антитела к антигенам ВЭБ: IgM к капсидному антигену — отрицательный, IgG к раннему антигену — положительный и IgG к ядерному антигену (IgGNA) — положительный (> 0,5 ед.). Совокупность данного анализа была индикатором активной фазы мононуклеозной инфекции.
После проведенного обследования ребенку была назначена адекватная комплексная терапия (Cумамед, Ликопид с последующим переходом на Виферон, витамины А, Е, Пиридоксин, пробиотики — курс Примадофилуса). Наблюдение за ним продолжается.
Выводы
- В пользу диагностики персистирующих инфекций у детей свидетельствует отягощенный акушерско-гинекологический и соматический анамнез, а также инфекционный фактор беременных женщин.
- Заподозрить внутриутробное инфицирование у детей раннего возраста можно по высокой степени поражения различных органов и систем: ЦНС, органов дыхания, пищеварения, лимфатического аппарата.
- Диагностика внутриутробных инфекций должна базироваться на клинических проявлениях болезни и основываться на комплексе лабораторных и иммунологических методов исследования с их оценкой в динамике (в 1 мес, 3 мес, 6 мес и в 1 год жизни).
- Правильность выбора комплекса клинических и лабораторных тестов (ИФА в динамике, ПЦР-тесты с различными биосубстратами) приводит к своевременной диагностике внутриутробных инфекций и позволяет выявить моноинфицирование или микст-формы при их длительной персистенции.
- Для суждения о состоянии общей иммунологической реактивности детей с персистирующими герпесвирусными инфекциями может использоваться оценка интегральных показателей (КФЗ и ИЛМП): чем меньше величина КФЗ, тем больше выражен риск прорыва защитного барьера на пути инфекции.
- Наиболее неблагоприятное персистирующее течение имеют микст-формы герпесвирусной инфекции (ЦМВ, герпес, ВЭБ) или их сочетания с внутриклеточными возбудителями.
Литература
Ф. Н. Рябчук, кандидат медицинских наук, доцент
З. И. Пирогова, кандидат медицинских наук, доцент
СПбМАПО, Санкт-Петербург
Биоматериал: Соскоб из: церв. канала,из уретры, из влагалища, секрет простаты, соскоб с эрозивно-язвенных элементов, поверхность миндалин, мазок из носоглотки и ротоглотки, отделяемое конъюнктивы, мокрота, моча, слюна, сперма
Время выполнения: 2-3 дня

Анализ крови на герпес в Москве - цены
Герпес — одна из самых распространенных вирусных инфекций, которая с легкостью передается при половом контакте. На сегодняшний день известно о восьми типах герпеса. Каждый из них вызывает различные заболевания.

Симптомы инфицирования – высыпания на коже, слизистой оболочке, поражение нервных клеток, сопровождающиеся болями, жжением, зудом и т. д. Все это свидетельствует о неспособности иммунной системы полностью исполнять защитные функции.
Что показывает анализ
Герпес, относящийся к первому типу, проявляет себя пузырьками, наполненными жидкостью с локализацией на слизистых, губах и языке. Второй тип поражает слизистые половых органов. Третий тип — вызывает ветряную оспу и опоясывающий лишай.
Четвертый тип поражает миндалины, вызывая тяжелые формы ангины.
Пятый тип опасен тем, что долгое время находится в организме в спящем состоянии, при активизации поражает внутренние органы.
Шестой тип — провоцирует развитие лимфосаркомы и лимфомы. Седьмой тип проявляется симптомами хронической усталости. Восьмой тип — сопровождает саркому Капоши у ВИЧ инфицированных.
В ходе исследование подтверждается наличие или отсутствие вируса герпеса в организме. Кровь исследуется на наличие антител и частей вируса.
Показания к анализу
Анализ крови на герпес назначается в диагностических целях, даже в случаях, когда внешние проявления полностью отсутствуют.
- При подготовке женщины к зачатию и во время беременности.
- При подготовке пациента к пересадке органов.
- При появлении видимых признаков присутствия вируса герпеса в организме.
Сдать анализ крови на герпес рекомендуют при появлении симптомов патологии, среди которых характерные высыпания в виде шариков с жидкостью. Они зудящие и болезненные, появляются на губах, половых органах, реже на кожных покровах в различных участках тела. Со временем пузырьки вскрываются и образуются корочки. Герпес заразен, поэтому обследоваться рекомендуется людям, которые вступали в тесный контакт с зараженными.
Подготовка к анализу
Обследование женского организма лучше проводить в первой половине менструального цикла, но не раньше 5 дня. Допускается исследование во 2 половине менструального цикла, но не позднее чем за пять дней до начала менструации.
Если присутствуют выраженные признаки воспалительных процессов, забор биоматериала следует проводить в день обращения. Накануне исследований и в день обследования женщине нельзя проводить процедуру спринцевания влагалища.
Специалисты не рекомендуют производить взятие материала при проведении терапии антибактериального характера вне зависимости от того, местная она или общая. Также нельзя проводить важную процедуру во время menses, ранее 1-2 суток после сексуального контакта, кольпоскопии и интравагинального УЗИ.
Рекомендовано взятие биоматериала не раньше, чем через 2 недели после использования местных антисептиков и антибактериальных средств, и не раньше, чем за 30 дней после использования пероральным способом антибиотических препаратов.
При взятии соскоба для исследования из уретры, забор биоматериала следует проводить до мочеиспускания или только по истечении 2-3 часов после мочеиспускания.
Причины ложных результатов
Исказить результат могут многие факторы, в том числе:
- Забор материала в период, когда заражение только состоялось, и в крови отсутствуют следы вируса.
- При проведении исследования в момент наличия очагов инфекции и проведения связанного с ними курса лечения.
- При нарушении стерильности образца и попадании вируса извне.
В этом случае проводят повторный забор материала.
Как проводится анализ
Существует сразу несколько методов исследования материала на наличие вируса герпеса.
ПЦР. Имеет свои преимущества и недостатки, и его использование возможно не во всех случаях, а только тогда, когда прошел инкубационный период. Итогом такого исследования становится обнаружение частей вируса в сыворотке и определение уровня их концентрации.
ИФА. Позволяет не только обнаружить вирус, но и получить примерное представление о степени развития процесса. Метод может быть использован на первых этапах развития заболевания. В плазме выявляют наличие антител ко всем известным типам вируса данного вида.
Посев на питательную среду. Проводится крайне редко, хотя и не дает ложных данных. Не используется, несмотря на всю эффективность, из–за высокой стоимости исследования и большого промежутка времени, необходимого для его завершения. Для анализу используют куриные эмбрионы. Такая особенность связана с тем, что вирус способен развиваться и размножаться только в живых тканях, отсюда и высокая стоимость проведения диагностики. Результат определяется по степени повреждения эмбриона. Возбудитель для посева берется из образцов венозной крови.
Нормы и расшифровка результата
При использовании ПЦР в бланке указывается одно из двух значений — положительное или отрицательное.
Результат отрицательный. В крови нет следов вируса. Но их отсутствие не доказывает, что его вовсе нет в организме. Для получения более достоверного результата обследование повторяют. При повторном отрицательном значении пациент считается здоровым.
Результат положительный. Это значит, что в крови обнаружены части вируса, что доказывает состоявшееся заражение.
При обследовании образца методом ИФА указывают один из четырех вариантов полученных данных:
- В пробе обнаружено только присутствие иммуноглобулинов IgG.
- Это означает, что пациент на данный момент является носителем. Сам вирус на этом этапе заболевания не проявляет активности. Такой результат исследования свидетельствует о достаточно высоком уровне иммунитета и подавлении процессов распространения возбудителя.
- В сыворотке обнаружено наличие иммуноглобулинов типа IgM. Их присутствие означает, что заражение состоялось недавно. Произошло первичное инфицирование и вирус активен.
- Отсутствии антител обоих видов, говорит о возможности заражения при контакте с вирусом, так как пациент не имеет сформированного иммунитета.
- При обнаружении иммуноглобулинов обоих типов, врачи говорят, о наличии хронического поражения вирусом. На данном этапе, идет обострение инфекции, поскольку присутствуют антитела обоих типов. Степень развития процесса определяется в зависимости от количества имеющихся в крови клеток вируса.
Данная статья размещена исключительно с целью ознакомления в познавательных целях и не является научным материалом или профессиональным медицинским советом. За диагностикой и лечением обратитесь к врачу.

уролог / Стаж: 28 лет
Дата публикации: 2019-07-05
уролог / Стаж: 29 лет
Дата обновления: 2021-12-01
Хотите записаться или получить подробную консультацию?
Наши специалисты работают круглосуточно и без выходных!
Анализ на герпес позволяет определить присутствие в организме вируса герпеса.
Герпес может передаваться различными путями – при непосредственном контакте (бытовым путем), воздушно-капельным путем; возможно внутриутробное заражение. В то же время типично заражение герпесом при половом контакте, поэтому герпес включается в число ЗППП (заболеваний, передающихся половым путем). Также герпес входит в число ToRCH-инфекций, объединяющих заболевания, способные причинить вред плоду во время беременности.
Вирус герпеса не всегда активен. Он может годами присутствовать в организме, не приводя к проявлению каких-либо явных симптомов и активизируясь лишь при снижении иммунитета.
Считается, что вирусом герпеса заражено большинство жителей Земли (по некоторым оценкам – до 90%). Поэтому так важно определить, являетесь ли Вы носителем вируса. Если нет, Вам следует быть особенно внимательным к угрозам возможного заражения, - это позволит Вам сохранить тот потенциал здоровья, которым Вы обладаете.
Анализ на герпес проводится для каждого конкретного типа вируса. Зная, присутствует ли данный тип вируса герпеса в организме или нет, врач получает необходимую информацию для диагностики заболеваний и оценки общего состояния организма.
На сегодняшний день медицина еще не располагает средствами, способными полностью победить герпес. Но подавить активность вируса или предотвратить его переход в активное состояние вполне возможно. Поэтому анализ на герпес является составляющей многих комплексных обследований, а в случае подозрения на герпес он необходим для точной диагностики и назначения адекватного курса лечения.
Когда назначается анализ на герпес
Анализ на герпес обычно назначается:
- при наличии симптомов, характерных для герпесной инфекции – для того, чтобы подтвердить их герпесную природу, а также для того, чтобы определить, каким именно типом вируса они вызваны;
- при планировании беременности – обоим партнерам;
- во время беременности;
- новоророжденным при инфицированности матери;
- для того чтобы установить, передалась ли герпесная инфекция при контакте с зараженным партнером.
Методы проведения
Основными методами анализа на герпес являются иммуноферментный анализ (ИФА) и ПЦР-диагностика.
Анализ крови на герпес иммуноферментным методом (ИФА)
Для иммуноферментного анализа на герпес биологическим материалом является кровь.
Организм отвечает на проникновение вируса тем, что вырабатывает для борьбы с ним специфические иммунные тела. Эти тела могут быть обнаружены в крови с помощью серологического исследования. Иммуноферментный анализ показывает наличие в крови антител к вирусу герепеса (Ig G и Ig M).
ПЦР-диагностика герпеса
Метод ПЦР (полимеразной цепной реакции) строится на анализе ДНК во взятом образце биологического материала. Выделяются фрагменты ДНК, характерные для данного типа вируса и многократно воспроизводятся. Умножение позволяет обнаружить вирус, присутствующий даже в незначительных количествах.
Биологическим материалом для ПЦР-диагностики обычно является соскоб (проба, взятая непосредственно с места высыпания), моча, кровь или слюна.
Подготовка к анализу на герпес
Где сдать анализ на герпес в Москве
Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
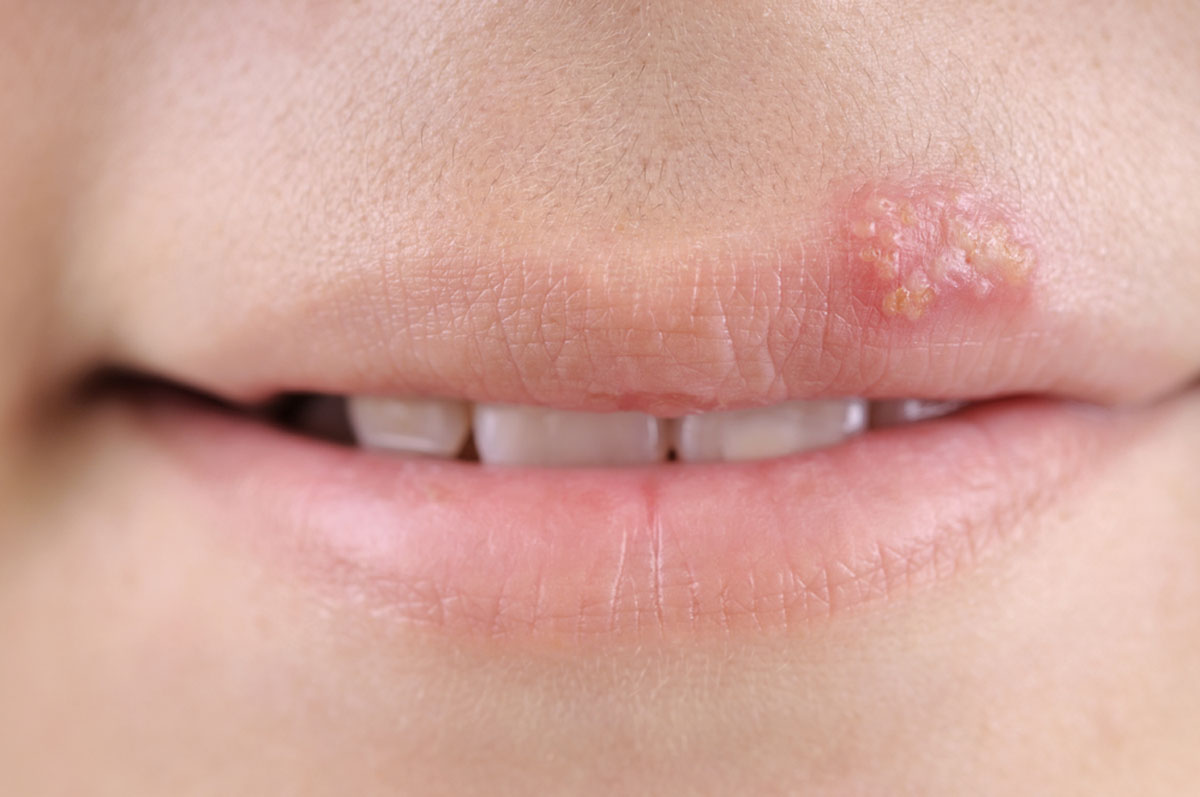
Однако семейство вирусов герпеса довольно обширно. Существует несколько типов вируса герпеса, способных поражать организм человека. Самые изученные типы это:
- вирус простого герпеса 1-го типа (ВПГ-1). Именно он ответственен за прыщики на губе. ВПГ-1 поражает, прежде всего, слизистую губ, ротовой полости и носоглотки. Герпетические высыпания также могут появиться в пределах носогубного треугольника (в частности, на крыльях носа), реже – на щёках и других участках лица. В последнее время ВПГ-1 довольно часто становится причиной герпетического поражения генитальной области, куда заносится посредством орального секса;
- вирус простого герпеса 2-го типа (ВПГ-2) – генитальный герпес. Основные проявления: покраснения, появление в области покраснения пузырьков, заполненных жидкостью, тяготеющих к слиянию, возникновение эрозий и корочек на месте пузырьков, зуд, головная и мышечная боль, учащение мочеиспускания;
- вирус ветряной оспы (varicella) – вирус герпеса 3-го типа. У людей, уже переболевших ветрянкой, этот тип вируса вызывает опоясывающий лишай (zoster). Поэтому данный тип герпеса также называется Varicella-Zoster;
- вирус Эпштейна-Барр (Эпштейн-Барр вирусная иинфекция – ЭБВИ) – вирус герпеса 4-го типа. Является возбудителем мононуклеоза , вызывает злокачественные заболевания лимфоидной ткани, считается причиной синдрома хронической усталости;
- цитомегаловирус – вирус герпеса 5-го типа. Вирус представляет угрозу для детей в период внутриутробного развития. Может поражать внутренние органы.
Причины герпеса
Вирус простого герпеса 1-го типа (ВПГ-1) может передаваться контактно-бытовым путём. Возможен также воздушно-капельный путь передачи.
Воздушно-капельный путь является основным при заражении вирусом ветряной оспы.
Генитальный герпес и цитомегаловирус передаются половым путём.
Также заразиться герпесом можно через кровь или слюну. Со слюной вирус может передаться при поцелуе. Маленькие дети, то и дело что-то берущие в рот, также весьма уязвимы. Если в детском коллективе инфицирован хотя бы один ребенок, можно ожидать быстрого распространения инфекции.
Симптомы герпеса
В настоящее время большинство людей инфицировано тем или иным типом вируса герпеса. Считается, что антитела к вирусу Эпштейна-Барр могут быть выявлены практически у каждого взрослого (до 98% взрослого населения Земли). Антитела к вирусу простого герпеса 1-го типа выявляются у 90% взрослого населения крупных городов.
Однако, как правило, носительство герпетической инфекции не приводит к развитию заболевания. Вирус герпеса активизируется при снижении защитных сил организма. Чем слабее иммунитет, тем вероятнее переход вируса из спящего в активное состояние.
При заражении вирусом простого герпеса 1-го типа инкубационный период составляет от 1 до 8 дней. Типичные симптомы: озноб, повышение температуры до 39-40°C, головная боль, общая слабость и сонливость. Затем появляются покраснения, на месте которых образуются характерные пузырьки. При поражении слизистой рта пузырьки, как правило, обнаруживаются на внутренней стороне губ, языке, реже – на нёбе, нёбных дужках и миндалинах. Пузырьки возникают в месте внедрения вируса в слизистую. В дальнейшем пузырьки лопаются, оставляя после себя болезненные эрозии.
Исчезновение симптомов не означает окончательного выздоровления. Вирус остаётся в организме и через какое-то время (в условиях снижения иммунитета) возможен рецидив заболевания. Рецидивы могут наблюдаться от 1-3 раз в год на протяжении нескольких лет и даже десятилетий.
Инкубационный период генитального герпеса длится от 1 до 10 дней, после чего могут наблюдаться зуд (жжение) в местах будущих высыпаний. После чего появляются отеки, а затем группы пузырьков на слизистых половых органов. Увеличиваются паховые лимфоузлы. Пузырьки лопаются и на их месте образуются эрозии и язвы. Процесс может продолжаться от двух до пяти недель.
Рецидив болезни возможен уже через две недели после первичного поражения. Рецидивы встречаются не менее, чем у половины переболевших.
Методы диагностики герпеса
Диагностика герпеса проводится, прежде всего, на основании осмотра пациента, поскольку герпетические высыпания имеют определённую специфичность. Однако врач может назначить лабораторные исследования. Лабораторные исследования позволяют выявить инфекцию даже при отсутствии явных проявлений.
Будьте готовы, что при подозрении на герпетическую инфекцию, врач выпишет направление на сдачу анализа крови, который позволит установить наличие антител к вирусу герпеса в крови. По результатам анализа можно будет судить не только о наличии возбудителя, но и о его активности.
Методы лечения герпеса
Лечение герпеса направлено на подавление вирусной активности, а также на повышение иммунитета. Могут быть назначены препараты для приема внутрь, а также средства местного действия.
Подбор препаратов осуществляется врачом в зависимости от вида заболевания (типа инфекции), а также от локализации поражения.
Полностью элиминировать вирус герпеса из организма нельзя. Именно поэтому важно всегда поддерживать защитные силы организма на достаточно высоком уровне, а также не допускать повторного проникновения вируса.
- пользуйтесь индивидуальным полотенцем и средствами личной гигиены (мылом, зубной щеткой и т.д.);
- будьте осторожны с косметикой: не пользуйтесь помадой заболевшего человека;
- при генитальном герпесе исключите половые контакты.
Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
Читайте также:

