Вирус папилломы человека лечение аюрведа
Обновлено: 05.05.2024
Статья посвящена папилломавирусной инфекции (ПВИ) - одной из самых распространенных вирусных инфекций, передаваемых половым путем. Представлены сведения о биологии вируса, путях заражения, патогенезе, клинических проявлениях инфекции. Рассматриваются различные клинические формы заболевания: манифестные - остроконечные кондиломы (аногенитальные бородавки), субклинические (интраэпителиальная неоплазия) и латентные. Обсуждаются подходы к лечению лечения ПВИ, включающие деструктивные (физические, химические), хирургические, иммунологические и комбинированные методы. Приводятся доказательства эффективности применения препарата Изопринозина - иммуномодулятора с противовирусной активностью при различных формах ПВИ, изученного в многочисленных зарубежных и отечественных исследованиях.
Ключевые слова: папилломавирусная инфекция, остроконечные кондиломы, деструктивные методы лечения, иммунокорригирующая терапия, Изопринозин
Папилломавирусная инфекция (ПВИ) относится к наиболее распространенным инфекциям, передаваемым половым путем. В США ежегодно выявляют около 5 млн новых случаев этого заболевания. По данным зарубежных исследований, практически каждый человек, живущий половой жизнью, инфицирован вирусом папилломы человека (ВПЧ). Заражение ВПЧ может произойти даже при однократном половом контакте вследствие высокой контагиозности вируса. Более половины женщин и мужчин приобретают эту инфекцию в течение первых двух лет сексуально активной жизни. Риск заражения значительно возрастает при наличии многочисленных половых партнеров и раннем начале половой жизни. По данным отечественных исследований, разные формы ПВИ гениталий встречаются у 44,3 % пациенток, обращающихся в гинекологические учреждения по различным причинам. По данным биопсий шейки матки, субклинические формы инфекции выявляются у 8,1 % женщин.
Этиопатогенез папилломавирусной инфекции
ВПЧ относится к безоболочечным вирусам, содержит двухцепочечную ДНК, имеет икосаэдрическую форму. Он является строго эпителиотропным, т. к. вначале поражает базальный слой эпителия кожи и слизистых оболочек гениталий и других органов (гортани, ротовой полости, глаз и др.), а его жизненный цикл связан с дифференциацией эпителиальных клеток. Репликация ДНК ВПЧ происходит только в клетках базального слоя, а в клетках других слоев эпидермиса вирусные частицы лишь персистируют. При заражении ВПЧ в клетках эпидермиса нарушается нормальный процесс дифференцировки. Происходит клональная экспансия инфицированных ВПЧ-клеток базального слоя с их трансформацией и последующей малигнизацией. Этот процесс контролируют гены ВПЧ, кодирующие ранние белки Е6 и Е7. Морфологически при этом наблюдаются деформация слоев эпидермиса, общее утолщение кожи и слизистых оболочек. В стадии развитой инфекции клетки шиповатого слоя при переходе в зернистый оказываются наиболее активными в синтезе вирусной ДНК. Эта фаза жизненного цикла ВПЧ характеризует второй этап экспансии вирусной инфекции внутри эпидермиса. Экспрессия поздних генов L1 и L2 наступает на конечной стадии дифференцировки в роговом слое, где наблюдаются активная сборка зрелых вирусных частиц и их выделение из клеток на поверхности кожи. Участки кожи и слизистых оболочек, на поверхности которых происходит активное выделение и почкование вируса, представляют наибольшую опасность для контактного заражения [1, 15].
Типы ВПЧ "высокого риска", особенно 16-й, 18, 31 и 45-й, ассоциируются с дисплазией шейки матки, а также с раком шейки матки, заднего прохода, вульвы и полового члена. Типы ВПЧ "низкого риска", прежде всего 6-й и 11-й, вызывают развитие остроконечных кондилом. Пациенты с остроконечными кондиломами могут быть одновременно инфицированы вирусами нескольких типов. Определение типа ВПЧ помогает оценить риск малигнизации [2].
Сексуальные контакты — основной путь заражения ВПЧ. Аутоинокуляция, контактнобытовой путь передачи инфекции допускаются, но изучены мало. Заражению способствуют микротравмы кожи и слизистых оболочек. Возможен вертикальный способ заражения, т. е. вирус может передаться новорожденному во время прохождения по родовым путям и послужить причиной развития рецидивирующего респираторного папилломатоза.
Клинические проявления ПВИ
В большинстве случаев инфекция ВПЧ протекает бессимптомно. Наиболее известными практическим врачам проявлениями этой инфекции являются остроконечные кондиломы, которые возникают в среднем через 1—3 месяца после заражения. С момента инфицирования и до развития предраковых заболеваний или рака in situ обычно проходит от 5 до 30 лет и очень редко - менее года. У 40 % больных отмечены субклинические, малосимптомные проявления заболевания в виде мелких плоских бородавок.
Манифестация инфекции ВПЧ наиболее часто сопровождается появлением остроконечных кондилом (аногенитальных бородавок). Они возникают, как правило, на коже и слизистых оболочках половых органов или в анальной области в местах трения и травматизации при половом акте. У лиц, практикующих орально-генитальные контакты, кондиломы могут возникнуть на губах, языке, небе. Чаще высыпания представлены узелковыми образованиями, сгруппированными по 5-15 элементов, иногда сливающимися в бляшки; реже высыпания бывают единичными. Слияние в крупные бляшки происходит при иммуносупрессии, соматических заболеваниях, метаболических нарушениях, интоксикациях. У некоторых больных с выраженными нарушениями клеточного иммунитета (ВИЧ-инфекцией, на фоне иммуносупрессивной терапии), при беременности развиваются очень крупные генитальные бородавки - гигантские кондиломы Бушке-Левенштейна. Эта предраковая инвазивная и деструктирующая опухоль ассоциируется с ВПЧ-6 и ВПЧ-11. Кондиломы могут быть плоской, конической или напоминающей цветную капусту форм. Цвет образований варьируется от беловато-телесного до розовато-синюшного, реже - красновато-коричневого.
Клинически выделяют четыре типа остроконечных кондилом:
Остроконечные кондиломы обычно бессимптомны и часто случайно выявляются самим больным или врачом при осмотре. Однако крупные или травмированные, изъязвленные или подвергшиеся вторичной инфекции бородавки сопровождаются зудом, болью, неприятным запахом и гнойным отделяемым. При локализации кондилом в уретре могут развиться признаки вялотекущего уретрита, кондиломы могут вызвать раздвоение струи мочи или даже обструкцию уретрального отверстия [3].
Диагностика и принципы лечения
Для диагностики ВПЧ-инфекции помимо клинического осмотра проводят лабораторные методы исследования: цитологические, гистологические, а также молекулярно-генетические, получившие в последнее время широкое распространение. ПЦР является более чувствительным методом диагностики, чем цитологическое исследование, и способна выявить субклинические и латентные формы заболевания. Метод имеет не только важную диагностическую ценность, но и прогностическое значение, т. к. позволяет идентифицировать отдельные типы ВПЧ [2].
Лечение ВПЧ-инфекции направлено на устранение ее клинических проявлений - остроконечных кондилом.
Для этого применяют различные методы наружной терапии:
Эффективность этих методов лечения составляет от 30 до 70 %. Активность ВПЧ зависит прежде всего от иммунного статуса и реакции организма на инфекцию. Для повышения эффективности терапии в лечебный комплекс необходимо включать противовирусные препараты и иммуномодуляторы для стимуляции иммунного ответа пациента [4, 16].
Показано, что иммунный ответ хозяина имеет большое значение в предотвращении клинической манифестации ВПЧ-инфекции. Клеточный иммунитет играет основную роль как в персистенции, так и в спонтанном регрессе кондилом, который может наступить через 6-8 месяцев. Это подтверждается данными о более высокой частоте ВПЧ-ассоциированных заболеваний у реципиентов трансплантата внутренних органов и ВИЧ-инфицированных. Нарушение Т-клеточного иммунитета у больных кондиломами проявляется снижением количества клеток Лангерганса в очагах поражения и большом числе CD4+- и CD8+-T-лимфоцитов в инфильтрате регрессирующих генитальных бородавок [1].
Изопринозин в лечении ПВИ
Иммуномодулирующее действие Изопринозина заключается в усилении пролиферации и стимулировании функций Т-лимфоцитов: Т-хелперов, естественных клеток-киллеров; увеличении продукции интерлейкинов и нормализации продукции интерферона. Препарат стимулирует биохимические процессы в макрофагах, повышает хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфноядерных клеток. Иммуномодулирующие потенции Изопринозина более активно проявляются в стимулировании клеточного, чем гуморального, иммунитета. Опытным путем было показано, что его действие в большей степени проявляется при иммуносупрессии по сравнению со здоровым организмом. Изопринозин восстанавливает и усиливает деятельность клеток иммунной системы, тем самым повышает способность организма эффективно противостоять инфекциям.
Препарат отличается от других иммуномодуляторов тем, что обладает не только иммуномодулирующим, но и противовирусным (подтвержденным in vivo и in vitro) действием. Противовирусное действие Изопринозина заключается в подавлении репликации ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Фармакокинетика препарата хорошо изучена. Максимальная концентрация Изопринозина достигается через час после приема 1,5 г препарата. Первый период полувыведения (50 минут) связан в выведением инозина и проходит с образованием мочевой кислоты. Второй период полувыведения диметиламино-2-пропанол β-ацетамидо-бензоата равен 3—5 часам, при этом метаболиты выводятся почками. Во время приема Изопринозина не рекомендуется применять иммунодепрессанты, а также лекарственные препараты, обладающие нефротоксичным действием [5, 6].
Благодаря своему комплексному действию Изопринозин более 35 лет успешно применяется при лечении различных, в т. ч. трудно поддающихся терапии, инфекционных заболеваниях кожи и слизистых оболочек. Основными показаниями к применению препарата в дерматовенерологии служат вирусные дерматозы: ПВИ, простой герпес, опоясывающий лишай. Многочисленные исследования подтвердили высокую клиническую эффективность Изопринозина в лечении персистирующих герпес-вирусных инфекций. Антивирусная активность препарата проявляется не только в области клинических проявлений (везикулы, эрозии), но и в нервных ганглиях. Поэтому он оказывает свое лечебное действие как в фазе обострения герпетической инфекции, так и в межрецидивный период. Препарат можно назначать в поддерживающей дозе на период до 6 месяцев [7, 14, 18].
Проведенные исследования показали, что применение инозиплекса в комплексе с деструктивными методами у пациентов с остроконечными кондиломами способствует более активному их разрешению и уменьшает частоту рецидивов, что объясняется активным иммунокорригирующим и противовирусным действиями препарата во всех зонах инвазии ВПЧ в коже [10, 17]. Препарат применяли по 1000 мг три раза в сутки в течение 28 дней.
В настоящее время несомненной представляется ведущая роль ВПЧ в генезе рака шейки матки. ВПЧ также может инициировать и поддерживать хронические воспалительные процессы в нижних отделах гениталий, поскольку при ВПЧ-индуцированном изменении структуры эпителия создаются предпосылки к заражению различными вирусными, бактериальными, протозойными, грибковыми и другими инфекциями. Показано, что одновременное инфицирование ВПЧ и вирусом простого герпеса II типа в два раза повышает риск развития плоскоклеточного рака шейки матки [19]. Имеются данные об успешном применении Изопринозина в лечении ПВИ шейки матки, цервикальной интраэпителиальной неоплазии и даже преинвазивного рака шейки матки.
В поликлиническом отделении Центра охраны здоровья матери и ребенка была изучена эффективность комбинированного лечения (этиотропный препарат, Изопринозин и абляция) 64 больных с гистологически подтвержденными субклиническими формами ПВИ на фоне хронического цервицита. Все пациентки были разделены на основную группу, в которой применяли комбинированное лечение с Изопринозином и этиотропным средством, и контрольную группу, где после курса этиологического лечения проводили только локальную монодеструкцию очагов плоскоклеточного интраэпителиального поражения. Изопринозин назначали по 2 таблетки (1000 мг) 3 раза в сутки на протяжении 5 дней за 7-10 дней до деструкции очагов. Анализ результатов проведенного лечения и последующее наблюдение за пациентками показали, что эффективность комбинированного лечения с применением Изопринозина была выше и составила 87,5 %, а при монодеструкции - 65,6 %. Рецидивирование ПВИ к 6-му месяцу наблюдения было выявлено лишь у 9,4 % женщин, принимавших Изопринозин, а в контрольной группе - у 28,1 % пациенток. Симптоматика воспалительного процесса на шейке матки наблюдалась только при рецидиве ВПЧ-инфекции. Кроме того, на фоне комплексного лечения через 6 месяцев чаще наблюдалась элиминация ВПЧ (65,6 и 46,9 % соответственно) и более качественная эпителизация. На основании полученных данных авторы пришли к выводу, что адекватная иммунотерапия способствует более полной элиминации ПВЧ, т. к. позволяет воздействовать не только на участок эпителия, где произошла клиническая манифестация, но и на резервуары ВПЧ в эпителии, находящиеся в латентном состоянии. Поэтому включение антивирусного иммуномодулирующего препарата Изопринозин в курс лечения больных хроническим цервицитом и ПВИ является обоснованным и перспективным [5].
Заключение
ПВИ вследствие ее широкой распространенности и отсутствия надежных методов лечения на сегодняшний день является актуальной проблемой в клинической практике. Терапевтическая стратегия при этом заболевании должна быть направлена не только на удаление локальных очагов инфекции — остроконечных кондилом, но и на воздействие на субклинические и латентные формы ВПЧ-инфекции. При этом большое значение в предотвращении рецидива и процесса канцерогенеза имеет элиминация ВПЧ. Поэтому в терапевтический комплекс необходимо включать препараты с противовирусным и иммуномодулирующим действиями для активации иммунной системы организма и подавления вирусной активности. Изопринозин является одним из наиболее изученных и эффективных иммунных препаратов с противовирусным действием. Более 35 лет его с успехом применяют в широкой клинической практике для лечения ПВИ и других вирус-ассоциированных заболеваний кожи и слизистых оболочек. Хорошая переносимость препарата, минимум побочных эффектов, возможность применять его в индивидуальной дозировке и в комбинации с другими методами лечения позволяют использовать его в лечении ВПЧ как у детей, так и у взрослых.
Остроконечные кондиломы (синонимы: condylomata acuminate, вирусные кондиломы, остроконечные бородавки, генитальные бородавки) относятся к заболеваниям, вызываемым вирусом папилломы человека (ВПЧ). Заболевания, обусловленные ВПЧ, являются одними из на

Остроконечные кондиломы (синонимы: condylomata acuminate, вирусные кондиломы, остроконечные бородавки, генитальные бородавки) относятся к заболеваниям, вызываемым вирусом папилломы человека (ВПЧ). Заболевания, обусловленные ВПЧ, являются одними из наиболее распространенных заразных вирусных инфекций человека. ВПЧ представляет собой небольшой округлый двухспиральный ДНК-вирус диаметром от 50 до 55 нм. На сегодняшний день описано более 80 типов ВПЧ (табл. 1). Инфекции, вызываемые ВПЧ, высокоспецифичны для эпидермиса, так как ВПЧ обладает тропизмом к эпителиальным клеткам кожи и слизистых оболочек.
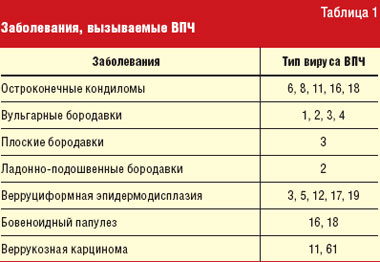
За последние 20 лет отмечается рост заболеваемости остроконечными кондиломами. В США остроконечные кондиломы (или генитальные бородавки) относятся к наиболее часто встречающимся заболеваниям, передающимся преимущественно половым путем. Заболеваемость остроконечными кондиломами превышает 106,5 случая на 100 тыс. населения США, что составляет около 0,1% всей популяции [1]. Пристальное внимание к этому заболеванию объясняется тем, что некоторые из типов ВПЧ, которые вызывают остроконечные кондиломы, могут приводить к малигнизации процесса. Наиболее потенциально опасными являются типы 16 и 18. Неслучайно важно своевременно диагностировать и лечить остроконечные кондиломы. Рецидив остроконечных кондилом не всегда связан с повторным заражением, а может быть вызван реактивацией вируса.
Клиническая картина. Инкубационный период продолжается от 3 нед до 6 мес и в среднем составляет около 2,8 мес. Мужчины и женщины одинаково подвержены этому заболеванию. Средний возраст заболевших колеблется от 22 до 25 лет.
Обычно остроконечные кондиломы локализуются на половых органах и в перианальной области. У ВИЧ-инфицированных пациентов остроконечные кондиломы могут локализоваться в необычных местах, например на лице, веках и ушных раковинах. У мужчин наиболее частая локализация — пенис, уретра, мошонка, перианальная, анальная и ректальная области [2]. Элементы сыпи имеют телесный цвет, могут быть представлены гладкими папулами размером с булавочную головку и на начальных этапах развития не всегда заметны на половом члене. Для их выявления проводят пробу с 5% уксусной кислотой. После обработки кожи окраска папул становится белесоватой. В дальнейшем папулы разрастаются и приобретают бородавчатую или нитевидную форму, напоминая цветную капусту или петушиный гребень. Как правило, остроконечные кондиломы множественные и располагаются группами.
У женщин клиническая картина остроконечных кондилом может быть разнообразной. Классические экзофитные поражения на наружных половых органах носят распространенный характер и легко выявляются при осмотре, однако могут быть и случайными находками при проведении кольпоскопии или ректороманоскопии. На малых половых губах и в преддверии влагалища кондиломы представляют собой влажные, бархатистые или множественные пальцеобразные разрастания и занимают значительную площадь. Кондиломы в цервикальном канале обнаруживаются у 20% женщин, инфицированных ВПЧ и с локализацией остроконечных кондилом на наружных половых органах. Локализация остроконечных кондилом на шейке матки или в цервикальном канале считается неблагоприятным фактором, так как может способствовать развитию рака шейки матки [3].
Даже при своевременном и рациональном лечении остроконечные кондиломы часто рецидивируют. Это связано с тем, что вирус длительное время может сохраняться в инактивированном состоянии во внешне здоровых участках кожи и слизистых оболочках.
Дифференциальный диагноз остроконечных кондилом проводится со вторичным сифилисом (широкие кондиломы), контагиозным моллюском, бовеноидным папулезом, блестящим лишаем, красным плоским лишаем, ангиокератомами, ангиофибромами на венечной борозде головки полового члена, фолликулитами, мягкой фибромой, волосяной кистой (табл. 2).
Диагностика остроконечных кондилом, как правило, клинически не представляет трудности. Дополнительно в некоторых случаях проводят пробу с 5% уксусной кислотой. Для этого смоченную раствором медицинскую салфетку располагают в зоне предполагаемой локализации остроконечных кондилом на 5–10 мин, после чего высыпания приобретают белесоватый оттенок [4].
При установлении диагноза остроконечных кондилом необходимо проводить обследование на сифилис и ВИЧ-инфекцию.
Проведение биопсии показано тем больным, у которых возникает подозрение на предраковые заболевания или плоскоклеточный рак. Удаление остроконечных кондилом не снижает риск развития рака шейки матки. Поэтому всем женщинам, у которых в анамнезе имелись сведения об остроконечных кондиломах, необходимо ежегодно проводить цитологическое исследование мазков с шейки матки с целью своевременного выявления онкологического процесса.
Лечение и профилактика
Использование презервативов снижает риск заражения половых партнеров. Полностью удалить ВПЧ невозможно — можно лишь удалить остроконечные кондиломы, облегчив состояние больного и снизив риск заражения полового партнера. Существует несколько методов лечения остроконечных кондилом. Все они имеют определенные недостатки.
Криодеструкция — один из наиболее часто применяемых методов лечения. Пораженную поверхность обрабатывают жидким азотом с помощью ватного тампона или распылителя. Обработку повторяют каждые 1–2 нед до полного удаления всех кондилом. Метод редко приводит к рубцеванию, отличается невысокой стоимостью. Криодеструкция может вызывать сильную боль. Не всегда можно одномоментно обработать всю пораженную поверхность. В некоторых случаях после криодеструкции может развиваться гиперпигментация или гипопигментация.
Диатермокоагуляция является болезненным методом лечения и оставляет после себя стойкие рубцы, поэтому применяется только для удаления одиночных кондилом.
Удаление лазером осуществляется с помощью углекислотного и неодимового ИАГ-лазеров (лазеров на иттрий-алюминиевом гранате). После удаления могут оставаться рубцы.
Медикаментозные методы лечения. Кондилин (подофиллотоксин) — 0,5% раствор во флаконах по 3,5 мл с аппликатором. Компонент Кондилина подофиллотоксин — наиболее активный в составе растительного экстракта подофиллина, при местном применении он приводит к некрозу и деструкции остроконечных кондилом. Преимущество данного метода лечения состоит в том, что больной может самостоятельно обрабатывать пораженные участки кожи в доступных местах. С помощью пластикового аппликатора препарат наносится на кондилому; постепенно смачиваются все кондиломы, но не более 50 штук за 1 раз (по площади не более 10 см2). Препарат нужно наносить с осторожностью, избегая здоровых участков кожи. Первый раз обработку проводит врач или медсестра, обучая пациента правильно наносить препарат. После обработки препарат должен высохнуть, чтобы не возникло раздражения окружающей кожи или ее изъязвления. Кондилин наносят 2 раза в день в течение 3 дней, а затем делают 4-дневный перерыв. Продолжительность лечения не должна превышать 5 нед. Противопоказанием для применения препарата являются беременность, лактация, детский возраст, применение других препаратов, содержащих подофиллин.
Солкодерм представляет собой смесь кислот: 65% азотной, 98% уксусной, а также молочной и щавелевой кислоты и нитрата меди; выпускается в виде раствора (ампулы по 0,2 мл). После его нанесения на поверхность кожи она окрашивается в желтый цвет, после чего происходит мумификация обработанных тканей. Обработку должен осуществлять медицинский персонал. Препарат наносится на поверхность с помощью стеклянного капилляра или аппликатора, после чего препарат должен высохнуть. Одномоментно допускается обработка площади не более 4–5 см2. При необходимости обработку можно повторить через 4 нед. Нанесение препарата может сопровождаться сильным жжением и болью, в некоторых случаях может возникнуть гиперпигментация и образование рубцов.
Препараты интерферона вводят непосредственно в остроконечные кондиломы. Процедура болезненна и требует проведения повторной обработки.
Трихлоруксусная кислота в концентрации 80–90% наносится непосредственно на кондиломы. Остатки ее удаляют с помощью талька или бикарбоната натрия. При необходимости лечение повторяют с интервалом в 1 нед. Если после 6-кратной обработки остаются остроконечные кондиломы, то необходимо сменить метод лечения.
Литература
Л. П. Котрехова, кандидат медицинских наук, доцент
К. И. Разнатовский, доктор медицинских наук, профессор
СПбМАПО, Москва
Е.В. Файзуллина
Казанский государственный медицинский университет
Генитальная папилломавирусная инфекция является распространенным заболеванием, передающимся половым путем. Вирус папилломы человека (ВПЧ) — высокоспецифичная в отношении человека инфекция, обладающая способностью инфицировать эпителиальные клетки, вызываемая вирусом из семейства Papovaviridea. Инфицирование ВПЧ половых органов, так же как и кожных покровов, происходит при наличии микротравм, при этом резервуаром ВПЧ-инфекции служат уретра, бартолиниевы железы, семенная жидкость. Идентифицировано более ста видов ВПЧ, из которых 35 инфицируют урогенитальный тракт человека, вызывая поражение покровного эпителия кожи и слизистых оболочек половых органов. ВПЧ-инфекция является наиболее распространенной инфекцией, передаваемой половым путем (ИППП), которой инфицирована большая часть сексуально активного населения. Кроме этого, папилломавирусы — единственная группа вирусов, для которых доказана индукция опухолей у человека. Число инфицированных в мире за последнее десятилетие увеличилось в 12 раз (Молочков В.А., 2004).
МКБ X пересмотра, раздел А 63. Аногенитальные бородавки.
Этиология
Вирус, относящийся к роду А семейства Papovaviridea, сохраняется при температуре 50?С в течение 30 минут. В процессе репликационного цикла геном вируса экспрессирует от 8 до 10 белковых продуктов; за онкогенные свойства вируса ответственны онкопротеины Е6 и Е7. По онкогенной активности различают ВПЧ низкой степени риска — HPV6, 11,42,43,44; средней – HPV31,33,35, 51,52, 58 и высокой — HPV16, 18,45,56 степени риска. Одним или более типами ВПЧ инфицировано не менее 50% взрослого населения, живущего активной половой жизнью, в большинстве случаев генитальная ВПЧ-инфекция у них является нераспознанной, протекающей субклинически или асимптомно. Генитальная ВПЧ-инфекция имеет высокую контагиозность; заражение при однократном половом контакте происходит примерно в 60% случаев.
Патогенез
Инвазия вируса происходит через микроповреждения тканей. ВПЧ инфицирует стволовые клетки базального слоя, которые затем являются постоянным источником инфицирования эпителиальных клеток. Вирусы инфицируют делящиеся незрелые клетки базально-клеточного слоя, находящиеся близко к поверхности, что во многом объясняет частоту инфицирования шейки матки и нижней трети влагалища и вульвы.
Вирусная ДНК включается в ядерный материал клетки хозяина. Интегрированная форма ВПЧ способна к злокачественной трансформации, поскольку вирусная ДНК начинает контролировать клеточный генетический материал для воспроизводства ВПЧ-кодированных белков. Интеграция ВПЧ высокого риска в клеточный геном хозяина усиливает продукцию двух онкопротеинов — Е6 и Е7, взаимодействующих с эндогенными клеточными регуляторными белками, ведущими к дерегуляции цикла клеточной прогрессии, что является разрешающим моментом в формировании цервикальной неоплазии, образованию плоских кондилом, невидимых вооруженным глазом (Прилепская В.Н., 1997).
Однако по мнению В.А. Молочкова и соавт. (2004), инфицирование эпителиальных клеток ВПЧ является необходимым, но не достаточным событием для развития рака. Для формирования необратимой неоплазии необходимы следующие факторы: во-первых, активная экспрессия генов Е6 и Е7, причем высокоонкогенных типов ВПЧ-16 и 18; во-вторых, индукция метаболических механизмов конверсии эстрадиола в 16-ОН; в третьих, индукция множественных повреждений хромосомной ДНК в инфицированной клетке, которая завершает процесс перерождения.
Первая стадия неоплазии CIN I характеризуется активной репликацией вируса и его бессимптомным выделением. Опухолевая трансформация возникает с большей вероятностью при взаимодействии ВПЧ с другими инфекционными агентами (цитомегаловирусы, вирус простого герпеса 2 типа, С. trachomatis, микоплазма и уреаплазма).
Факторы риска
ВПЧ является необходимым, но не достаточным фактором цервикальной неоплазии. Предрасполагающими факторами риска для развития заболевания могут быть: неблагополучный социально-экономический статус и сексуальное поведение, нарушения клеточного и гуморального иммунитета, сопутствующие сексуально-трансмиссивные заболевания (гонорея, сифилис герпес, трихомониаз хламидиоз и т.д.), молодой возраст, курение, беременность, дисбиоз вагинального биотопа, гипо- и авитаминозы (Марченко Л.А., 2001).
Риск ВПЧ-инфекции наиболее высок у гомосексуалистов. Не исключены случаи перинатальной передачи инфекции младенцам, рожденным от инфицированных матерей во время родоразрешения через естественные родовые пути, за счет аспирации околоплодных вод, цервикального или вагинального секрета; случаи папилломатоза гортани, трахеи, бронхов у детей, рожденных с применением операции кесарева сечения, что, по мнению ряда авторов, свидетельствует о возможности трансплацентарной передачи инфекции и нецелесообразности применения кесарева сечения с единственной целью — предупреждения заражения новорожденного ВПЧ (Koutsky L.A., Kiviar N.B.,1999).
Течение заболевания и клинические разновидности
Инкубационный период при аногенитальных бородавках составляет от 1 до 3 месяцев. В большинстве случаев ВПЧ-инфекция не манифестирует сразу, оставаясь некоторое время асимптомной. Прогрессия ВПЧ-инфекции высокого онкогенного риска в цервикальную интраэпителиальную неоплазию и рак in situ обычно происходит в сроки от 5 до 30 лет.
1. Клинические формы (видимые невооруженным взглядом):
1.1. Экзофитные кондиломы (остроконечные типичные, паппилярные, папуловидные);
1.2. Вестибулярный паппиломатоз ( мелкие паппиломовидные образования преддверья влагалища).
2. Субклинические формы (не видимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/ или цитологическом или гистологическом исследовании):
Плоские кондиломы (типичная структура с множеством койлоцитов);
Малые формы (различные поражения метапластического эпителия с единичными койлоцитами);
Кондиломатозный цервицит/вагинит.
3. Латентные формы (отсутствие клинических, морфологических или гистологических изменений при обнаружении ДНК ВПЧ);
4. Цервикальная интраэпителиальная неоплазия (плоскоклеточные интраэпителиальные поражения):
CIN - CIN 1 — слабо выраженная дисплазия +/- койлоцитоз, дискератоз;
4.2 CIN II — выраженная дисплазия +/- койлоцитоз, дискератоз;
4.3 CIN III или CIS - тяжелая дисплазия или карцинома in situ+/- койлоцитоз, дискератоз;
4.4 Микроинвазивная плоскоклеточная карцинома.
Поверхность покрыта многослойным плоским эпителием по типу дискератоза. В подлежащей строме имеются атипичные сосуды, явления воспаления. Локализация ОК различна, в основном, в местах возможной мацерации: клитор, малые половые губы, устье уретры, влагалище, шейка матки, анус.
Манифестация генитальной ВПЧ-инфекции сопровождается появлением генитальных бородавок. Экзофитные формы остроконечных кондилом представляют из себя типичное проявление инфекции, обусловленной доброкачественными типами вируса ВПЧ6 и ВПЧ11. Эндофитные кондиломы могут быть плоскими и инвертированными, располагаются на шейке матки и имеют вид плоских или слегка возвышающихся бляшек, определяются при расширенной кольпоскопии.
Субклиническая форма болезни обнаруживается только при кольпоскопии в виде мелких плоских бородавок или устанавливается на основании характерной гистологической картины в виде койлоцитоза. Отсутствие клинических и гистологических признаков инфекции при выявлении ДНК ВПЧ свидетельствует о латентной или асимптомной инфекции.
Наружное отверстие уретры у женщин поражается в 4-8% случаев, более глубокое поражение мочеиспускательного канала вызывает явления вялотекущего уретрита.
Анальные бородавки чаще встречаются у лиц, практикующих анальный секс, и редко располагаются выше зубчатой линии прямой кишки. У лиц, практикующих орально-генитальные контакты, генитальные бородавки могут поражать губы, язык, небо.
Генитальные бородавки, как правило, бессимптомны, и часто случайно выявляются при осмотре или на основании Pap-мазка. В связи с этим вначале больные не предъявляют жалоб на связанный с ними дискомфорт. Однако, крупные, травмированные, изъязвленные или подвергшиеся вторичной инфекции бородавки сопровождаются зудом, болью, неприятным запахом. Уретральные бородавки у мужчин могут вызывать раздвоение струи мочи, обструкцию уретрального отверстия.
У больных с нарушением клеточного иммунитета (ВИЧ-инфекция, иммуносупрессивная терапия, беременность), — развиваются очень крупные генитальные бородавки — гигантская кондилома Бушке-Левенштейна, инвазивная и деструирующая опухоль, ассоциирующаяся с ВПЧ 6 и 1 1 типа.
ВПЧ-инфекция, обусловленная типами вируса высокого онкогенного риска (ВПЧ-16 и 18), является этиологическими агентами довольно гетерогенной группы заболеваний: бовеноидный папулез, цервикальная интраэпителиальная неоплазия, рак шейки матки, реже - рак влагалища, вульвы, ануса (Баткаев Э.А. с соавт., 2001; Киселев В.И., Киселев О.И., 2003).
Бовеноидный папулез ассоциируется с ВПЧ-16, а также с другими типами ВПЧ - 1, 6, 11, 18, 31-35, 39, 42, 48, 51-54 и проявляется плоскими папулами и пятнами с гладкой, бархатистой поверхностью. Заболевание обычно развивается у мужчин, имеющих много половых партнеров. У партнерш таких пациентов выявляется инфекция ВПЧ шейки матки и цервикальной интраэпителиальной неоплазии. Течение бовеноидного папулеза обычно доброкачественное. У некоторых больных бовеноидный папулез может персистировать годами, трансформируясь (особенно у лиц пожилого возраста) в плоскоклеточный рак.
Диагностика папилломавирусной инфекции
Лабораторная диагностика ВПЧ-инфекции проводится на основании цитологического, гистологического исследования биоптатов, определения антител к ВПЧ, обнаружения ДНК ВПЧ и онкобелка Е7.
Клинический осмотр наружных половых органов, вульвы, влагалища следует проводить при хорошем освещении. Для выявления субклинической генитальной ВПЧ-инфекции проводится расширенная кольпоскопия. Ложноположительные результаты при этом методе обычно являются следствием воспалительных и дискератических процессов вульвы и влагалища.
Кольпоскопия и биопсия показаны всем женщинам с цервикальной интраэпителиальной неоплазией класса II (CIN II) или класса III (CINIII), независимо от подтверждения у них наличия ВПЧ-инфекции.
Наиболее простые методы для идентификации ВПЧ — иммунологические методы: РСК, ИФА, ПИФ.
Диагностика ВПЧ-инфекции шейки матки включает тестирование по Папониколау (РАР-тест). Молекулярно-биологические методы реакция гибридизации in situ, ПЦР, ДНК-зонд. Гистологическое исследование биоптатов тканей эпителия и эпидермиса используются и при малосимптомных или асимптомных формах вирусных заболеваний гениталий. Использование молекулярно-биологических методов исследования целесообразно для доказательства наличия ВПЧ с его типированием, так как и ДНК-гибридизация, и полимеразная цепная реакция позволяют выявить онкогенные типы вируса 16 и 18.
Основным методом диагностики ВПЧ является цитологический — обнаружение койлоцитарных клеток в биоптате эпителия шейки матки (клетки МПЭ промежуточного и поверхностного типа с многоядерным строением), патогномоничные для ВПЧ.
При гистологическом исследовании генитальных бородавок обнаруживается умеренное утолщение рогового слоя с папилломатозом, паракератозом и акантозом; могут присутствовать фигуры митоза. Диагностически важным считается наличие в глубоких участках мальпигиева слоя койлоцитов — больших эпителиальных клеток с круглыми гиперхромными ядрами и выраженной перинуклеарной вакуолизацией.
Лечение
При выборе метода лечения ВПЧ-инфекции учитывается анамнез, соматический статус, предшествующая противовирусная терапия, локализация, количество, размеры остроконечных и плоских кондилом. Тактика лечения должна быть индивидуальной с учетом переносимости тех или иных методов лечения. Местное лечение АБ направлено на удаление кондилом и атипически измененного эпителия, с применением различных видов химических коагулянтов, цитостатиков и физиохирургических методов лечения. После удаления папилломатозных разрастаний для профилактики рецидива АБ необходима местная и общая терапия противовирусными препаратами, индукторами интерферона, неспецифическими иммуномодуляторами. Больных с папилломавирусной инфекцией следует предупредить, что данное заболевание является сексуально трансмиссивным, поэтому обследование и лечение необходимо проводить обоим партнерам, а на период терапии и ближайшие 6-9 месяцев рекомендовать барьерные методы контрацепции.
Местное лечение ВПЧ (данные приведены по Подзолковой Н.М. с соавт, 2007).
В течение трех лет (2006-2008 гг.) нами были обследованы и пролечены 650 женщин с аногенитальными бородавками (АБ). Данные представлены в таблице 1.
Таблица 1.
Группы пациенток по локализации и распространенности АБ
| Группа | Локализация ОК | Количество пациенток | % |
|---|---|---|---|
| 1. | Влагалище | 17 | 2,6 |
| 2. | Вульва | 173 | 23,6 |
| 3. | Влагалище + вульва | 258 | 39,7 |
| 4. | Влагалище + большие половые губы | 126 | 19,4 |
| 5. | Влагалище + вульва + большие половые губы | 76 | 11,7 |
| Всего | 650 | 100 | |
Таблица 2.
Число сеансов радиоволновой деструкции АБ, требующихся для достижения стойкой ремиссии заболевания у женщин
| Группа | 1 сеанс | 2 сеанс (10-12 дней) | 3 сеанс (14-21 день) | Более 3 сеансов | Всего | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| Чел. | % | Чел. | % | Чел. | % | Чел. | % | Чел. | % | |
| 1 | 7 | 41,2 | 10 | 58,82352941 | 0 | 0 | 0 | 0 | 17 | 100 |
| 2 | 121 | 69,9 | 41 | 23,69942197 | 11 | 6,4 | 0 | 0 | 173 | 100 |
| 3 | 118 | 45,7 | 112 | 43,41085271 | 25 | 9,7 | 3 | 1,2 | 258 | 100 |
| 4 | 13 | 10,3 | 77 | 61,11111111 | 29 | 23,0 | 7 | 5,6 | 126 | 100 |
| 5 | 0 | 0,0 | 23 | 30,26315789 | 41 | 53,9 | 12 | 15,8 | 76 | 100 |
| Итого: | 650 | |||||||||
М.А.Гомберг, д.м.н., профессор, А.М.Соловьев, к.м.н., доцент, МГМСУ, Москва
В последнее время папилломавирусная инфекция привлекает особое внимание в связи с ролью этой группы вирусов в развитии рака. В 2008 г. Нобелевской премией по медицине было отмечено доказательство того, что некоторые типы вируса папилломы человека (ВПЧ) способны вызывать рак шейки матки. По Handley J.M., et al. (1994), к ВПЧ-поражениям относят: клинические формы — аногенитальные бородавки (остроконечные кондиломы, вульгарные бородавки), симптоматические внутриэпителиальные неоплазии на ранних стадиях при отсутствии дисплазии (плоские кондиломы); субклинические формы — бессимптомные внутриэпителиальные неоплазии при отсутствии дисплазии; латентные формы (отсутствие морфологических или гистологических изменений на фоне обнаружения ДНК ВПЧ).
Лечение аногенитальных ВПЧ-поражений, согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, должно быть направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией — CDC, Европейских рекомендациях, рекомендациях ВОЗ, и в том числе в рекомендациях РОДВ, приведен именно такой подход.
Роль вирусов папилломы человека (ВПЧ) в развитии множества доброкачественных и злокачественных новообразований кожи и слизистых оболочек не вызывает сомнений. Полагают, что все 500тыс. случаев рака шейки матки, ежегодно диагностируемые в мире, вызваны генитальной ВПЧ-инфекцией (Bulletin Word Health Organization, 2007).
В различных клинических рекомендациях и протоколах подробно описываются методы лечения именно клинических проявлений ВПЧ, но обходится стороной вопрос так называемого вирусоносительства или бессимптомного выделения вируса. Причем вопросу тактики врача при бессимптомном выделении вируса у пациента ВПЧ уделяется мало внимания не только в практических рекомендациях, но и в научно-исследовательской литературе.
Мы предлагаем свой подход к этой проблеме.
Прежде всего мы исходим из того, что наш долг — ставить во главу угла интересы пациента. Если он встревожен наличием ВПЧ и желает избавиться от этой инфекции, мы должны постараться успокоить его и обсудить все имеющиеся в настоящее время возможности лечения. В противном случае нам будет трудно рассчитывать на доверие с его стороны.
Мы считаем, что такое обсуждение должно состоять из 3 частей.
1. Информирование пациента относительно характера течения и последствий инфекции.
2. Методы профилактики рака шейки матки (при выявлении вируса у женщин).
3. Возможности воздействия на ВПЧ с целью его элиминации.
1. ИНФОРМИРОВАНИЕ ПАЦИЕНТА
При первом же визите необходимо рассказать человеку о возможных рисках, связанных с инфицированием ВПЧ. Однако консультирование нужно проводить очень осторожно, чтобы не спровоцировать у человека развитие психоневроза и канцерофобии.
Пациент с выявленным ВПЧ должен знать о своей потенциальной заразности для неинфицированных лиц, поэтому ему надо рекомендовать использовать презерватив при половых контактах и обязательно информировать своего полового партнера о вирусоносительстве.
Следует проинформировать пациентов о том, что возможно самостоятельное исчезновение ВПЧ. Известно, что у лиц более молодого возраста вероятность исчезновения вируса с течением времени выше, чем у лиц старше 25 лет.
2. ПРОФИЛАКТИКА РАКА ШЕЙКИ МАТКИ (ПРИ ВЫЯВЛЕНИИ ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА У ЖЕНЩИН)
Всем женщинам, инфицированным ВПЧ, следует провести кольпоскопическое исследование, в том числе с окраской раствором Люголя или раствором уксусной кислоты, а также цитологические тесты по Папаниколау. Периодичность обследований обсуждается с гинекологом в зависимости от степени онкогенности выявленных вирусов и результатов кольпоскопии и цитологии. Цитологические исследования следует проводить не реже, чем 1 раз в 6 месяцев. Для женщин старше 26 лет этот подход является практически единственным способом профилактики рака шейки матки.
Имеются публикации об эффективности российского препарата индинол для профилактики рака шейки матки у женщин, инфицированных ВПЧ. Однако контролированных плацебо-исследований не проводилось.
3.ВОЗДЕЙСТВИЕ НА ВПЧ
Наиболее дискуссионным является вопрос о воздействии на выделение вируса, поэтому остановимся на нем подробнее. Врач, безусловно, должен информировать пациента о том, что в настоящее время нет методов, позволяющих достоверно и с высокой степенью вероятности устранить вирус из организма.
Необходимость проведения лечебных мероприятий обсуждается индивидуально с каждым пациентом. Желательно, чтобы врач принимал решение о проведении лечения с целью устранения ВПЧ в отсутствие клинических проявлений только после подписания пациентом информированного согласия, во избежание возможных последующих недоразумений.
Теоретически, учитывая локализацию вируса в эпителиальных клетках и то, что происходит постоянное слущивание эпителия, можно предположить, что ВПЧ может исчезнуть вместе со старыми эпителиальными клетками. Видимо, именно этим объясняются случаи самопроизвольного исчезновения ВПЧ. Между тем очевидно, что элиминации ВПЧ из организма с гораздо большей эффективностью можно добиться при активизации противовирусного иммунитета, ингибирующего размножение ВПЧ и его внедрение в другие клетки. Доказать возможность достижения такого результата на практике можно только путем проведения соответствующих специальных исследований.
Потенциально возможны 3 способа инфицирования: от матери к ребенку (трансплацентарно; во время родов, в том числе путем кесарева сечения; возможно — через слюну или грудное молоко), посредством передачи вируса воздушно-капельным или контактно-бытовым путями. Cчитается, что ВПЧ-инфекция передается в основном половым путем, что объясняет ее широкую распространенность среди сексуально активного населения. В частности, в США ежегодно диагностируют 6,2 млн новых случаев генитальной ВПЧ-инфекции (Steinbrook R., 2006).
Повышение функциональной эффективности противовирусного иммунитета является основным способом, который предположительно может помочь в устранении вируса из организма или уменьшить его активность. Этого можно достичь как неспецифическими, так и специфическими методами.
К неспецифическим относят различные способы укрепления защитных сил организма, так называемый здоровый образ жизни: правильное питание, профилактический прием витаминов, биологически активных добавок.
Отдельный вопрос — проведение гомеопатического лечения. Но поскольку об этих способах часто упоминается в научно-популярной литературе, в рамках данной статьи мы их комментировать не будем.
Установлено, что при применении интерферонов снижается количество вирусной ДНК (по данным ПЦР) у пациентов в очагах поражения [Arany I., et al., 1995].
Интерферон применяют местно и системно (подкожно, внутримышечно, внутривенно или ректально).
В большинстве исследований была показана невысокая эффективность наружного применения интерферона [Keay S., et al, 1988] при наличии клинических проявлений, а при лечении больных с субклиническими очагами ВПЧ-инфекции и цервикальных неоплазиях (ЦИН) были получены обнадеживающие результаты [Gross G., 1996].
По данным различных авторов, при системном применении альфа-интерферона в дозе от 1,5 до 3 млн МЕ внутримышечно или подкожно через день в течение 4 недель в качестве монотерапии у 11—100% пациентов наблюдается полное исчезновение бородавок [Gross G., et al., 1986; Zwiorek L., et al., 1989], что свидетельствует о возможном ингибирующем влиянии препаратов интерферонов на ВПЧ.
При системном применении интерферонов побочными эффектами обычно являются гриппоподобные состояния, выраженность которых зависит от полученной дозы [Handley, et al., 1994]. Эти побочные явления можно ослабить приемом нестероидных противовоспалительных препаратов.
Считается возможным самостоятельное исчезновение ВПЧ. Известно, что у лиц более молодого возраста вероятность исчезновения вируса с течением времени выше, чем у лиц старше 25 лет.
На российском рынке представлен широкий выбор интерферонов различных производителей, как отечественных, так и зарубежных, — генферон, виферон, кипферон, реаферон, роферон-А, интрон А, реальдирон и т.д. Предпочтительнее назначать рекомбинантные, а не человеческие интерфероны.
При назначении интерферонов надо учитывать не только частые побочные реакции, но и то, что их введение может подавлять синтез собственных эндогенных интерферонов. Поэтому в отсутствие клинических проявлений интерфероны применяют только в том случае, когда о целесообразности такого назначения свидетельствуют результы исследования иммунного статуса. Следует также отметить и высокую стоимость качественных препаратов интерферона.
Воздействовать на противовирусный иммунитет можно с помощью индукторов эндогенного интерферона и других активаторов иммунитета. На российском фармацевтическом рынке представлено много иммуноактивных препаратов, которые, согласно инструкции производителя или рекомендациям исследователей, можно применять для комбинированного лечения аногенитальных бородавок (в сочетании с различными деструктивными методами). На основании этого их можно рекомендовать для противовирусной терапии при отсутствии клинических проявлений.
Гепон — синтетический олигопептид, состоящий из 14 аминокислотных остатков, относится к группе иммуномодуляторов. Препарат показан для повышения эффективности иммунной защиты от инфекций, лечения и профилактики оппортунистических инфекций, вызванных бактериями, вирусами или грибами. Гепон оказывает иммунофармакологическое и противовирусное действие:
У больных с ослабленной иммунной системой гепон:
Так, например, после удаления очагов ВПЧ-поражений любым деструктивным методом, аппликации гепона (от 3 до 6 аппликаций через день) позволяют ускорить процесс заживления и снизить уровень рецидивирования. Системно препарат применяют по 2 мг перорально 3 раза в неделю. Курс можно повторять с интервалом в 1 неделю [Соловьев А.М., 2003].
Изопринозин (инозин пранобекс) — противовирусное средство с иммуномодулирующими свойствами. Препарат, индуцируя созревание и дифференцирование Т-лимфоцитов и Т1-хелперов, потенцируя индукцию лимфопролиферативного ответа в митогенных или антиген-активных клетках, нормализует дефицит или дисфункцию клеточного иммунитета. Изопринозин моделирует цитотоксичность Т-лимфоцитов и натуральных киллеров, функцию Т8-супрессоров и Т4-хелперов, а также повышает количество иммуноглобулина G и поверхностных маркеров комплемента. Препарат повышает синтез интерлейкина-1 (ИЛ-1) и интерлейкина-2 (IL-2), регулирует экспрессию рецепторов IL-2, существенно увеличивает секрецию эндогенного γ-интерферона и уменьшает продукцию интерлейкина-4 в организме. Изопринозин усиливает действие нейтрофильных гранулоцитов, хемотаксис и фагоцитоз моноцитов и макрофагов. Кроме этого, он оказывает прямое противовирусное действие, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной и-РНК. Одним из показаний для применения препарата являются инфекции, вызванные вирусом папилломы человека: остроконечные кондиломы, папилломавирусная инфекция вульвы, вагины и шейки матки (в составе комплексной терапии).
Для женщин старше 26 лет цитологическое исследование слизистой шейки матки, проводимое 2 раза в год, является практически единственным способом профилактики рака шейки матки.
В литературе описаны различные схемы и результаты применения изопринозина.
При инфекциях, вызванных ВПЧ, изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству на протяжении 14—28 дней для пациентов с низкой степенью риска или 5 дней в неделю последовательно в течение 1—2 недель в месяц в течение 3 мес для пациентов с высокой степенью риска.
Известно о зарубежном опыте применения инозин пранобекса в качестве терапии, дополняющей деструкцию аногенитальных бородавок [Davidson-Parker J., et al., 1988]. Препарат назначали по 1 г 3 раза в сутки в течение 14—28 дней.
В работе Забелева А.В. и соавт. (2005) показано исчезновение атипичного эпителия у женщин с ВПЧ-ассоциированными плоскоклеточными интраэпителиальными поражениями низкой степени после проведения курсов лечения изопринозином. Препарат назначали по 1 грамму 3 раза в сутки в течение 5 дней, 3 курса с интервалом в 1 месяц. В исследовании, проведенном Sun Kuie Tay (1996), показаны аналогичные результаты — улучшение морфологической картины эпителия вульвы. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, тогда как в группе, принимавшей плацебо, только у 16,7%. О прекращении выделения ВПЧ у 65,6% больных после проведения комбинированной терапии (изопринозин + деструкция очагов) ЦИН низкой степени сообщает Прилепская В.Н. (2007). При использовании только деструкции очагов этот результат был достигнут у 46,9% больных. Изопринозин назначали за 7—10 дней до проведения деструкции по 1 г 3 раза в сутки в течение 5 дней. В исследовании Шевниной И.В. (2009) показаны похожие результаты — прекращение выделения ВПЧ у 77% больных при комбинированной терапии женщин с ЦИН и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 г 3 раза в сутки в течение 20 дней.
Для решения поднятой в этой статье проблемы интересным является факт прекращения обнаружения ВПЧ из очагов поражения в ходе проводимой комбинированной терапии с применением иммуномакса. При проведении вирусологического обследования пациентов до лечения в среднем у 70% выявлялся ВПЧ в очагах поражения. После проведенного комбинированного лечения в ходе контрольного наблюдения у 45% больных было отмечено прекращение выделения ВПЧ [Перламутров Ю.Н. и соавт., 2003]. Полученные результаты свидетельствуют, что проведение терапии иммуномаксом влияет на противовирусный иммунитет и приводит к прекращению не только рецидивов, но и выделения ВПЧ из очагов поражения. В связи с этим в перспективе иммуномакс можно будет использовать не только для лечения остроконечных кондилом, но и для предотвращения вирусовыделения у больных без клинических проявлений инфекции.
ПРОТИВОВИРУСНЫЕ ПРЕПАРАТЫ С ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ
Панавир — растительный полисахарид, полученный из растения Solanum tuberosum, относится к классу высокомолекулярных гексозных гликозидов сложного строения с молекулярной массой 1000 кД. В настоящее время в России он является одним из самых популярных препаратов, использующихся для противовирусной терапии. Причем лечение папилломавирусной инфекции является лишь одним из показаний к его применению.
После однократной инъекции панавира в 2,7—3 раза повышается уровень лейкоцитарного интерферона, что соответствует воздействию терапевтических доз интерферона [Колобухина и соавт., 2005].
Повышение функциональной эффективности противовирусного иммунитета является основным способом, который предположительно может помочь в устранении вируса из организма или уменьшить его активность.
Со степенью распространенности неопластического процесса связывают эффективность препарата в отношении прекращения вирусовыделения [Иванян А.Н. и соавт., 2004]. Так, после проведения комплексного лечения у пациенток с 1-й степенью распространенности процесса вирус не выявлялся в 90,5%, при 2-й степени — в 71,1%, при 3-й степени — в 39,6%, при 4-й степени — в 9,4% случаев. Достоверное снижение вирусной нагрузки с 398,2 RLU до 176,2 RLU (p<0,05) через 1 месяц после окончания монотерапии панавиром ВПЧ-инфекции отмечает Мелехова Н.Ю. (2005).
Продолжаются исследования противовирусной активности панавира с целью установления мишени, объясняющей его высокую противовирусную активность, а также по расширению показаний к его применению. Но уже сейчас можно говорить о том, что он является одним из наиболее перспективных противовирусных агентов с доказанным иммуномодулирующим действием.
В этой статьей мы начали дискуссию о целесообразности попытки устранения папилломавирусной инфекции при отсутствии ее клинических проявлений. Существующие рекомендации по наблюдению таких пациентов могут не удовлетворить тех из них, которые хотели бы получить квалифицированную помощь в устранении этой инфекции. Поэтому мы предлагаем 3-х этапную тактику ведения таких больных: консультирование, цитологический контроль у женщин и использование противовирусных препаратов с иммуномодулирующим действием.
Читайте также:

