Вирус зита что это такое
Обновлено: 26.04.2024
Как комары передают вирус Зика
Людей кусают только самки комаров — им необходима кровь для того, чтобы отложить яйца. Они всасывают вирус вместе с кровью. Он перемещается из кишечника через кровеносную систему в слюнные железы и вводится в организм следующей человеческой жертвы. Слюна комаров содержит белки, которые предотвращают свертывание крови. Когда комар кусает человека, он сперва вводит свою слюну, чтобы кровь не сворачивалась в его хоботке. Вместе со слюной в организм человека попадает и вирус. Вирус Зика передается комарами рода Aedes, которые могут размножаться в небольших источниках воды (например, в колпачке от бутылки) и кусают людей, как правило, в дневное время. В большинстве случаев вирус Зика распространяет комар, передающий желтую лихорадку — Aedes aegypti. Также передавать вирус могут комары Aedes albopictus (его еще называют Азиатским тигром), но в настоящее время неизвестно, насколько эффективно они это делают.
Какой инкубационный период при заражении?
Инкубационный период для вируса Зика составляет примерно 3–12 дней после укуса комара. Симптомы могут длиться около 4–7 дней. Примерно 60–80% зараженных людей не испытывают никаких симптомов и признаков. Является ли вирус Зика заразным? В целом, вирус не передается от человека к человеку; ему необходим переносчик (комар), который передаст вирус другому пациенту. Теоретически, донорская кровь и органы для трансплантации могут стать причиной редкой передачи возбудителя от человека к человеку. Другие возможные пути: передача от матери к плоду, половым путем.
Каковы симптомы заражения вирусом Зика?
Заболевание может вызвать развитие повышения температуры, кожной сыпи, боли в суставах, конъюнктивита, мышечной и головной боли, реже — дискомфорта в пищеварительном тракте, рвоты. Но большинство из пациентов не знают, что заразились вирусом Зика. По словам представителя Американского Общества Инфекционных Заболеваний (США), Амеш Адалья, только примерно каждый пятый инфицированный человек испытывает какие-либо симптомы, а у большинства людей вообще нет никаких признаков. Она также говорит, что вирус редко приводит к развитию тяжелых осложнений, и до настоящего времени вообще не считался серьезным инфекционным заболеванием. Но в редких случаях вирус Зика связан с развитием синдрома Гийена-Баре — заболевания, которое может стать причиной частичного или полного паралича, который в большинстве случаев носит временный характер. Увеличение частоты этого заболевания было обнаружено в таких регионах, как Французская Полинезия и Бразилия, Где наблюдается эпидемия вируса Зика. Однако научные исследования не смогли установить наличие прямой связи между этими двумя болезнями. Об одном случае синдрома Гийена-Баре, который можно связать с вирусом Зика, сообщили Центры контроля и профилактики заболеваний. Но обнаружить такую связь в каждом индивидуальном случае проблематично, так как синдром Гийена-Баре также может развиваться после гриппа или других инфекционных заболеваний. Подобен ли вирус Зика другим заболеваниям, передаваемым комарами (лихорадка денге, чикунгунья, вирус Западного Нила)? Все эти заболевания могут вызвать различные гриппоподобные симптомы, которые варьируют по тяжести и могут длиться от нескольких дней до недели и больше. Как и при инфицировании вирусом Зика, при заражении лихорадкой денге или вирусом Западного Нила некоторые люди не имеют никаких симптомов. Как установить диагноз инфекции? Врачи начинают диагностический процесс с опроса и осмотра пациента. Человек должен рассказать медицинским работникам о любом путешествии в те страны, в которых есть опасность заражения вирусом. При подозрении на инфицирование вирусом Зика можно провести полимеразно-цепную реакцию с обратной транскрипцией, с помощью которой можно обнаружить возбудителя и отличить это заболевание от подобных вирусных инфекций — лихорадки денге или чикунгуньи.
Какие осложнения заболевания?
Хотя осложнения при инфицировании вирусом Зика развиваются редко, некоторые из них могут угрожать жизни пациента (например, тяжелое обезвоживание). Может развиться также синдром Гийена-Барре. Кроме того, в Бразилии с инфицированием вирусом Зика было связано увеличение распространенности врожденных пороков развития у детей (в основном — микроцефалии). Новое научное исследование показало, что аномалии глаз у детей с микроцефалией также могут быть связаны с вирусной инфекцией.
Какова опасность заражения вирусом Зика во время беременности?
Риск женщины заразиться вирусом Зика во время беременности такой же, как и у небеременной женщины. Но у инфицированных беременных повышался риск рождения ребенка с пороками развития (чаще всего — микроцефалией), особенно в Бразилии. Тем не менее, окончательно причинно-следственная связь еще не доказана. Тем не менее, эпидемиологические данные из Бразилии подтверждают взаимосвязь инфицирования вирусом Зика беременных женщин и врожденной микроцефалией. Беременным женщинам, особенно в первом и начале второго триместра, находящимся в регионах распространения этого заболевания, следует остерегаться любых укусов комаров. В Бразилии с мая 2015 года родилось почти 4000 детей с микроцефалией, тогда как за такой же период времени в прошлом диагностировали только 150 случаев этого порока. Кроме этого, в амниотической жидкости двух женщин и тканях одного ребенка (головном мозге и сердце) удалось выделить вирус Зика, на основании чего можно придти к выводу, что этот вирус может быть связан с развитием микроцефалии. В Бразилии рекомендовали даже женщинам избегать беременности, пока окончательно не установят причину врожденных пороков у младенцев. Несколько научных организаций интенсивно изучают эту проблему. Кроме этого, новое исследование детей с микроцефалией и предполагаемой врожденной инфекцией вируса Зика показало, что 10 из 29 изученных младенцев (34,5%) имели различные нарушения зрения — от легких до тяжелых. Исследователи указывают, что между вирусной инфекцией и нарушениями зрения нет окончательно установленной связи. Однако, так как другие заболевания были исключены, они считают, что вирус Зика может быть связан с развитием этих нарушений зрения.
Профилактика заражения вирусом Зика
Поскольку в настоящее время вакцины от этого заболевания не существует, предотвращение укусов комаров — самая важная часть профилактики заражения вирусом Зика. Рекомендуется использовать репелленты, носить одежду с длинными рукавами и длинные брюки, использовать защитные сетки на окнах и дверях, избегать области со стоячей водой, в которой комары могут откладывать свои яйца. В некоторых случаях рекомендуют использовать защищающую от комаров сеть над кроватью. Это, как правило, советуют женщинам, которые путешествуют в страны с опасностью заражения вирусом Зика. При выборе репеллентов советуется покупать средства с диэтилтолуамидом, пикаридином и IR335. Длительную защиту также могут обеспечить средства, содержащие масло лимонного эвкалипта и параметандиол. Рекомендуется наносить репеллент после использования солнцезащитного крема, одевания одежды, обработанной перметрином. Не следует использовать репеллент под одеждой. Всегда нужно читать инструкцию к каждому конкретному средству. Если человек все же заразился вирусом Зика, важно избегать любых укусов комаров в течение первой недели заболевания. Вирус может передавать от человека к комарам через кровь, повышая риск распространения другим людям. Так как вирус Зика может передаваться половым путем от мужчины к своему партнеру, рекомендуется использовать презервативы во время и после путешествия в страны, пораженные этим заболеванием.
Рекомендации женщинам, планирующим беременность, которые посещали страны с активным вирусом Зика
После того, как женщина покинула регион с возможностью заражения вирусом Зика, ей рекомендуется не пытаться забеременеть в течение 28 дней (это перекрывает возможный 14-дневный инкубационный период и возможный 14-дневный период пребывания вируса в крови).
Рекомендации беременным женщинам, которые посещали или проживали в странах с возможным заражением вирусом
Научные данные о инфицировании вирусом Зика и беременности в настоящее время ограничены и продолжают пополняться. Рекомендации основаны на текущей информации и периодически могут пересматриваться с учетом новых данных. Беременные женщины, посещавшие во время беременности регион с возможностью заражения вирусом Зика, у которых развились клинические симптомы, позволяющие заподозрить инфицирование в течение двух недель после путешествия или в его время, и у которых в настоящее время есть эти признаки, должны пройти тестирование на наличие вируса Зика и ультразвуковое исследование плода. Все другие беременные женщины, посещавшие эти страны во время беременности, должны проходить ультразвуковое исследование плода.

Обзор
Реконструкция оболочки вируса Зика. Карта поверхности вириона (разрешение — 3,8 Å), полученная с помощью программной обработки криоэлектронных микрофотографий, позволяет предположить, как именно вирус поражает те или иные клетки, и вычислить потенциальные мишени для терапии или компоненты для вакцины. Симметрически неэквивалентные мономеры вирусного гликопротеина Е окрашены разными цветами.
Автор
Редакторы
В эпоху глобализации из-за свободного перемещения людей по миру проникновение ZIKV в новые регионы становится неизбежным. Там он может длительно сохраняться, передаваясь от животных к животным и изредка вызывая мелкие вспышки болезни у людей, либо циркулировать в человеческой популяции. Угроза, исходящая от любого нового заболевания, зависит от его эпидемиологии, клинических особенностей и способности медицинского сообщества эффективно его контролировать (рис. 1). И сейчас огромные усилия брошены на изучение особенностей вируса Зика и механизмов его воздействия на человеческое здоровье, в особенности — на здоровье беременных [1].

Рисунок 1. Сотрудник муниципальной службы города Ресифи (Бразилия) во время операции по уничтожению комаров Aedes aegypti, переносящих вирус Зика.
Хронология событий в Зика-эпопее

Рисунок 2. Микрофотография вируса Зика, полученная с помощью трансмиссионного электронного микроскопа (ТЭМ). Вирусные частицы размером 40 нм окрашены синим цветом.
В Энтеббе расположен Угандийский исследовательский институт вирусологии (Uganda Virus Research Institute, UVRI), чьи сотрудники в 1947 году при изучении желтой лихорадки в лесу Зика выделили из крови макаки до тех пор неизвестный флавивирус. Ученые описали его как вирус Зика (рис. 2). А на следующий год обнаружили вирус в комарах Aedes africanus [3].
В 1952 году вирус выявили уже у людей — в Уганде и Танзании, а в 1954 году — в Нигерии. ZIKV четко ассоциировался с лихорадкой и кожной сыпью, в связи с чем его окончательно объявили патогенным для человека. Тогда же, в 50-е, экспериментальным путем с участием добровольцев установили основного переносчика вируса — комара Aedes aegypti, обычного переносчика желтой лихорадки, лихорадки денге и чикунгуньи. Позже компанию ему составили и другие виды, в том числе Aedes albopictus [1].
В 60–80-е годы легкие формы инфекции выявляли в странах Африки, Азии и в Индии. Длительное присутствие ZIKV в этих регионах подтверждалось обнаружением вируса в комарах и нечеловекообразных обезьянах. У людей до 2007 года фиксировали не так много клинических случаев, и потому система здравоохранения не спешила бить тревогу [4].
Первую крупную вспышку лихорадки Зика зарегистрировали в 2007 году на острове Яп в тихоокеанских Федеративных штатах Микронезии, где инфицированными оказались 73% населения, однако симптомы у подавляющего большинства были умеренными и недолгими. Следующая вспышка охватила в 2013–2014 годах Французскую Полинезию, где заразились 66% жителей. Одновременная волна заболеваемости синдромом Гийена-Барре подняла вопрос о его ассоциации с вирусом Зика: тогда зафиксировали 42 случая — а это на порядок больше, чем в 2012 году, когда синдром диагностировали у троих [1].
К 27 июля ZIKV циркулировал уже в 67 странах и территориях (рис. 3). Крупная вспышка заболевания произошла в Колумбии — там заразились 65 000 человек. У многих из них выявлялись неврологические синдромы, отмечались и случаи микроцефалии [1].
В июле 2016 зафиксировали две смерти, связанные с заражением ZIKV: в США и Пуэрто-Рико. Предполагают, что смерти вызвал не сам вирус, а обострившиеся во время лихорадки симптомы хронических заболеваний.
В середине августа 2016 года в Пуэрто-Рико ввели режим чрезвычайной ситуации, поскольку распространение вируса набирало обороты слишком быстро: за полгода (с декабря 2015 по 12 августа 2016) число заразившихся возросло с одного до 10 000 человек.
К 1 сентября в американской Флориде зарегистрировали 47 случаев заболевания, а в Майами-Бич впервые в США обнаружили трех комаров — переносчиков вируса Зика.

Рисунок 3. История распространения вируса Зика по миру.
В Россию впервые вирус завезли в феврале 2016 года из Доминиканской республики. За прошедшие месяцы отмечены еще 7 случаев. Все — у туристов, вернувшихся из стран, где распространяется ZIKV: большинство — из Доминиканской республики, один — с Карибских островов. Все пациенты благополучно перенесли лихорадку.
Патогенез лихорадки Зика
Передача вируса и развитие болезни
Какие-то симптомы появляются у меньшинства инфицированных: на острове Яп лишь 19% заразившихся сообщили о симптомах, а во Французской Полинезии — 26%. Если признаки лихорадки развиваются, то в 95% случаев это происходит через 6–11 суток после заражения (рис. 4). Симптомы сходны с проявлениями других подобных инфекций [1], [4]:
- повышенная температура тела;
- кожная сыпь;
- боль в суставах и мышцах;
- головная боль;
- конъюнктивит;
- отеки;
- иногда рвота;
- общее недомогание.

Рисунок 4. Схема протекания инфекции у человека и комара. В среднем признаки развиваются на шестой день после инфицирования. Примерно на девятый день начинается выработка иммуноглобулинов (антител): первым обнаруживают IgM, количество которого позже снижается одновременно с ростом концентрации IgG. Последний сохраняется в крови неопределенное время. Виремия, вероятно, возникает до появления симптомов, и ее продолжительность сказывается на риске инфицирования восприимчивых комаров, кусающих зараженного человека. После определенного инкубационного периода комар приобретает способность передавать возбудителя другим людям. Tg — интервал между эпизодами инфицирования первого и второго человека.
Виремия, или вирусемия — медицинское состояние, когда вирусы попадают в кровоток и могут распространяться по всему телу, — аналогично бактериемии, при которой в кровь попадают бактерии [9]. — Ред.
В клетку вирус Зика проникает, взаимодействуя с определенными рецепторами на ее поверхности. Основной из них — AXL. А посредником выступает рецептор TIM-1, который связывает вирусные частицы и транспортирует их к AXL, способствующему проникновению вируса в клетку. Однако TIM-1 не необходимое звено, он лишь повышает концентрацию вирионов на поверхности клетки и ускоряет их взаимодействие с AXL [10].
Когда вирус оказывается внутри клетки, она отвечает повышенной продукцией интерферонов IFN-α и IFN-β, а также хемокинов CXCL10 и CXCL11, которые играют важную роль во врожденном и адаптивном иммунитете. Эти хемокины привлекают Т-клетки и другие лейкоциты к месту воспаления и даже оказывают прямое антимикробное действие, когда их концентрация в кожных фибробластах сильно повышается [10].
Антитела к вирусу обнаруживают в крови уже на девятый день после заражения. Продолжительность иммунитета против ZIKV пока не известна, но, судя по другим флавивирусам, можно предположить, что он пожизненный [1].
Вирус Зика и беременность
Однако установить связь между ZIKV и микроцефалией оказалось достаточно сложно из-за нескольких обстоятельств:
- остается неясным, сколько беременностей затронул вирус — инфекция ведь часто бессимптомна;
- до сих пор нет четкого определения микроцефалии;
- существуют другие инфекционные агенты, вызывающие микроцефалию: цитомегаловирус и Rubella virus (вирус краснухи).
Симптомы инфекции у беременных женщин такие же, как и у остальных, но пока не известно, влияет ли на частоту их проявления иммунодефицит, характерный для этого периода. Результаты исследований, касающихся неблагоприятных последствий заболевания для эмбриона, очень разнородны: где-то у 29% беременных с симптомами болезни развивался эмбрион с микроцефалией, а где-то и у 74%. Возможно, такие расхождения возникли потому, что в исследованиях участвовало недостаточное количество пациентов — меньше 50 человек. С определенной уверенностью можно утверждать лишь то, что ZIKV-ассоциированная микроцефалия разовьется у плода одной из ста инфицированных в первый триместр женщин независимо от наличия симптомов, и этот риск становится незначительным во второй и третий триместры [1].
Помимо микроцефалии с вирусом Зика сейчас связывают и другие эмбриональные патологии [1]:
- внутричерепной кальциноз; ;
- дефекты органа зрения;
- гипоплазию ствола мозга; ; .
Устройство вируса Зика
Организация генома
К концу августа 2016 года в GenBank хранилось 67 полных последовательностей генома ZIKV. Вирус Зика содержит кодирующую молекулу РНК длиной 10,8 т.н. с одной ORF (открытой рамкой считывания), фланкированной нетранслируемыми участками (UTR) — 5′-UTR длиной 106 н. и 3′-UTR длиной 428 н. (рис. 5). ORF кодирует полипротеиновый предшественник, который впоследствии разделяется на три структурных белка (капсидный [С], премембранный [prM] и оболочечный [E]) и семь неструктурных (NS1, NS2A, NS2B, NS3, NS4A, NS4B и NS5). Вирусный полипротеин во время трансляции и/или после нее расщепляется вирусной протеазой, сигнальной пептидазой и неизвестной протеазой клетки-хозяина. Фрагмент pr затем, при производстве зрелых вирионов, обычно отсекается в аппарате Гольджи фурином [17].

Рисунок 5. Геном вируса (представлен в виде последовательности кодируемых РНК белковых продуктов). Структурные белки окрашены серым цветом, неструктурные синим. Цифрами обозначены длины белков (число аминокислотных остатков). Стрелки указывают на места расщепления полипротеина.
Основные белки
Белок E — главный поверхностный гликопротеин флавивирусов, а неструктурные белки NS3 и NS5 — основные ферменты вирусной репродукции [17]. Структура этих белков показана на рисунке 6.

Рисунок 6. Структура главных белков ZIKV.
Белок Е разделен на два структурных региона — стволовой и трансмембранный (на рис. 6 — stem и ТМ) — и три функциональных домена: домен I участвует в организации оболочки (рис. 7), домен II отвечает за взаимодействие мономеров, а домен III связывает клеточный рецептор.
NS3 состоит из протеазного и хеликазо-НТФазного доменов, которые осуществляют процессинг вирусного полипротеина и раскручивание структурированных участков во время синтеза вирусной РНК.
NS5 содержит метилтрансферазный домен, который метилирует 5’-CAP-участок геномной РНК, и домен РНК-зависимой-РНК-полимеразы (RNA dependent RNA polymerase, RdRp).

Рисунок 7. Трехмерная модель вируса Зика в атомном разрешении, созданная в студии биомедицинской визуализации Visual Science. Модель построена по данным научных публикаций об организации вируса Зика и родственных вирусов и считается наиболее достоверной на текущий момент.
Известно, что гликозилирование играет важную роль в инфекционности, созревании и вирулентности флавивирусов [18], [19]. Для вируса Зика предсказаны потенциальные участки для N- и O-гликозилирования в белках prM, E, NS1 и NS4B, которые гликозилируются и в других флавивирусах. Исследования, посвященные роли этих сайтов в жизненном цикле вируса Зика, еще только планируются [17]. Правда, уже обнаружено одно структурное отличие белка Е ZIKV от подобных белков других флавивирусов — выставленная на поверхность вирусной частицы аминокислотная петля, с которой в позиции Asn154 связывается гликан (см. видео). Предполагают, что именно эта петля вместе с прикрепленным сахаром может отвечать за тропизм вируса (взаимодействие с рецепторами определенной группы клеток) и патогенез болезни [20].
Отличие в структуре белка Е ZIKV от гомологичных белков других флавивирусов.
исследовательская группа Университета Пердью, США
Борьба с вирусом Зика
Диагностика
Основные проблемы диагностики ZIKV-инфекции — это значительное количество бессимптомных случаев и неспецифичность симптомов: лихорадка денге и чикунгунья, которые тоже переносятся комарами рода Aedes, проявляются подобным образом. Предположить заражение вирусом Зика можно, если симптомы появляются у человека, который недавно побывал или длительно проживал в районе циркуляции ZIKV [1], [4].
Лучшим решением был бы высокоспецифичный тест на антитела, который можно использовать не только для подтверждения инфицированности, но и для проверки иммунитета против вируса Зика в самом начале беременности, что позволило бы женщинам понять степень риска. Однако такое тестирование осложняется кросс-реактивностью с другими флавивирусами. Определенные надежды дает тест ELISA. Например, IgG-ELISA, применяемый во Французской Полинезии, где циркулирует вирус денге, еще до основной вспышки лихорадки Зика выявлял ZIKV-позитивных доноров крови (тогда их было <1%) [1].
Профилактика
Основной способ — это защита от укусов комаров, в том числе и с помощью контроля их распространения.
В регионах циркуляции вируса Зика и потенциально опасных зонах людям рекомендуют носить светлую одежду, закрывающую как можно больше поверхности тела, устанавливать на окна и двери домов противомоскитные сетки, использовать сетку во время сна, а также применять репелленты с ДЭТА, IR3535 или икаридином [4].
Самки комаров Aedes после насыщения кровью откладывают яйца, которые в безводной среде могут сохраняться до года. Даже в минимальном количестве воды из яиц выходят личинки и дальше развиваются во взрослых особей. Потому для контроля численности и распространения комаров необходимо постоянно отслеживать и ликвидировать места их размножения: ведра, бочки, горшки с водой, сточные канавы, использованные автомобильные покрышки. В особых случаях прибегают к распылению инсектицидов [4].
Пример эффективного контроля численности переносчика вирусов — действия Уильяма Горгаса по ликвидации эпидемии желтой лихорадки в Гаване и регионе Панамского канала в начале XX века. Этот американский военврач и его команда устроили жестокую борьбу с антисанитарией и обработали все здания и улицы инсектицидами (от которых, к слову, пострадало и немало жителей). В результате желтая лихорадка была полностью побеждена [21].
В 50-х и 60-х годах в государствах Америки применяли интенсивные меры по контролю переноса возбудителя желтой лихорадки, включая повсеместное распыление ДДТ. Это привело к устранению Aedes aegypti из 18 стран и значительно сократило область распространения заболевания. Позже подобные программы успешно осуществили Сингапур и Куба. Конечно, через некоторое время лихорадка вернулась, но даже краткосрочный период без инфекции имел большое значение для населения [1].
Чтобы сократить риск передачи ZIKV половым путем (особенно во время беременности), мужчинам, проживающим в зонах циркуляции вируса или недавно побывавшим там, ВОЗ рекомендует пользоваться презервативами или воздерживаться от половой активности на всём протяжении беременности партнерши [4].
Лечение
Обычно заболевание протекает в легкой форме и не требует специального лечения. Во время лихорадки необходим отдых и обильное питье, иногда — прием препаратов для устранения боли и других неприятных симптомов [4].
Тем не менее существуют вещества, которые оказывают воздействие и на сам вирус Зика. Например, эффективно подавляет репродукцию вируса in vitro 2′-C-метиладенозин, а 7-деаза-2′-C-метиладенозин (МК-608) ингибирует репликацию ZIKV in vitro и затормаживает развитие болезни в экспериментах на мышах. Препараты 2′-C-метилцитидин, рибавирин, фавипиравир и T-1105 ослабляют цитопатическое действие вируса и снижают его урожай [22], [23].
Разумеется, вакцина решила бы проблему кардинально, но она до сих пор не разработана. Сейчас исследованиями занимаются 18 коммерческих компаний и исследовательских институтов [24–26]. Однако первая фаза клинических испытаний стартует не раньше конца 2016 года, а значит, готовая вакцина появится еще не скоро, и распространение инфекции по миру продолжится [1].
Заключение
Хотя всевозможные случайности в эволюции вирусов делают точный прогноз пандемий практически невозможным, научный мир пытается повышать скорость реакции на новые угрозы. В ближайшее время усилия биологов и медиков сосредоточатся на разработке единой стратегии, которую в любой момент можно было бы применить к той или иной вспышке заболевания. Такая стратегия позволит быстро разобраться в путях передачи, патогенезе и способах контроля инфекции, чтобы предотвратить ее глобальное распространение.

Обзор
Zika Virus — эмерджентная инфекция, распространение которой не на шутку взволновало ВОЗ и мировые СМИ.
Автор
Редактор

Генеральным спонсором конкурса, согласно нашему краудфандингу, стал предприниматель Константин Синюшин, за что ему огромный человеческий респект!
Лихорадка Зика: что за зверь и откуда он взялся?

Рисунок 1. История распространения вируса Зика.
Вирус Зика имеет типичное для семейства Flaviviridae строение: геном РНК+ (РНК вируса в зараженной клетке играет роль иРНК), нуклеокапсид и гликопротеидный суперкапсид, икосаэдральный тип симметрии (рис. 2). Основу суперкапсида составляет гликопротеид Е, который является основным фактором адгезии вируса, принимает участие в объединении оболочки вируса с мембраной клетки. Кроме того, в состав вириона входят высокомолекулярные белки НС1, NS3, NS5 и низкомолекулярные NS2A, NS2B, NS4A и NS4B. Их роль на данный момент является малоизученной [3].

Рисунок 2. Модель вируса Зика. Модель сделана компанией Visual Science.
Где и как распространяется вирус Зика?
Вирус Зика долгое время считался классическим примером арбовирусной инфекции. Грубо говоря, группы вирусных инфекций совершенно разной генетической природы, которые объединяет лишь одно — членистоногие в качестве переносчиков. Специфическими переносчиками вируса Зика являются комары Aedes aegypti (рис. 3) и Aedes albopictus [2]. Ареал обитания этих видов ограничен экваториальной и тропической областями. Соответственно, вирус может активно распространяться только в этих регионах. Так было принято считать до недавнего времени.

Рисунок 3. Aedes aegypti — переносчик вируса Зика.
В связи с быстрым распространением лихорадки Зика в Центральной и Южной Америках, подтверждением трансплацентарного пути передачи, а также возникновением неэндемичных случаев заболевания вне границы обитания комаров-переносчиков, ученые принялись более подробно изучать пути передачи вируса. Понятно, что кто ищет, тот всегда найдет — это и произошло в результате исследования. Все гипотезы имеют косвенные или малочисленные доказательства, но от этого являются не менее интересными. Предполагается возможность передачи вируса во время гемотрансфузий, также совсем недавно было установлено, что самки комаров Aedes могут заражать свое потомство. Особо опасной считается возможность полового пути передачи, ведь именно он стирает границы эндемичности лихорадки Зика и наделяет это заболевание высоким уровнем социальной опасности [4].
Почему так много шума?
В научной литературе клиническую картину лихорадки называют облегченной версией лихорадки денге, не отягощенной геморрагическим синдромом и летальностью [5]. Правда, для того, чтобы приблизительно понять, что это значит, нужно еще найти человека, который хотя бы один раз видел вживую пациента, зараженного вирусом лихорадки денге. Если говорить проще, то лихорадка Зика проявляется точно так же, как многие другие инфекционные заболевания (рис. 4). Подтвердить диагноз возможно только лабораторно.

Рисунок 4. Клиническая картина лихорадки Зика.
Важно отметить, что лабораторная диагностика вируса Зика весьма затруднительна и не всегда точна. Исследование методом иммуноферментного анализа (ИФА) может давать ложноположительные результаты, поскольку вирус Зика содержит антигены, перекрестно реагирующие с антителами вируса лихорадки денге. Более-менее надежный способ диагностики на данный момент — полимеразная цепная реакция (ПЦР) [6].
Перспективным направлением в лабораторной диагностике является использование нанотехнологий. Яркий пример — метод спектроскопии с использованием серебряных наночастиц, усиливающих сигнал. Методика основана на SERS — комбинационном рассеивании света. Благодаря такому виду диагностики менее чем за 1 минуту можно выявить следовые частицы вируса в биологическом материале, а также идентифицировать штаммы репродуцирующихся вирусов, выявляя даже наименьшие спектральные различия в строении белков [7].

Рисунок 5. Схема работы атомно-силового микроскопа.

Рисунок 6. Сравнение размера головы ребенка с синдромом микроцефалии с физиологической нормой.
Что касается осложнений у взрослых, то это тот самый случай, когда редко, но метко. Синдром Гийена-Барре проявляется неврологическими расстройствами, которые имеют патогенез вялых параличей. У пациентов наблюдаются мышечная слабость, паралич лицевого нерва и бульбарный паралич. Последний становится причиной смерти 5% пациентов. Еще 20% вследствие патологии становится инвалидами, что пугает даже больше. Прямых доказательств связи синдрома Гийена-Барре с заражением вирусом Зика пока нет, но тот факт, что об этом говорит ВОЗ, как бы намекает [11].
Так много букв, но что делать?

Неспецифическую профилактику проще всего обеспечить туристам: ну не ездите вы в беременном состоянии в регионы эпидемии! Во всех остальных случаях отменять поездки не обязательно, но меры предосторожности лучше соблюдать. Они включают применение репеллентов, москитных сеток, защищенные половые контакты. Власти стран с наличием эпидемии либо риска ее возникновения должны проводить профилактическую дезинсекцию и уничтожение потомства комаров рода Aedes (рис. 8).

Рисунок 8. Уничтожение комаров-переносчиков необходимо для предотвращения распространения вируса Зика.
Как эпидемия вируса Зика влияет на мир?
Распространение лихорадки Зика по земному шару стало причиной значительного резонанса в обществе именно благодаря тератогенному действию вируса. Дело в том, что наиболее серьезная эпидемическая ситуация в связи с этим заболеванием сложилась в странах Африки, Центральной и Южной Америки. Очень часто это страны с резко патриархальной культурой (особенно африканские), где не то, что аборты не разрешены, там до сих пор популярна традиция женского обрезания (Нигерия, Камерун, Конго и т.д.) [15]! В Латинской Америке, в первую очередь, в Бразилии, ситуация немногим лучше: возможность искусственно прервать беременность — это всего лишь редкие исключения, подтверждающие правило. Из-за страха врожденной патологии у ребенка женщины этих стран очень часто идут на незаконный аборт, который чреват летальным исходом. Такое положение дел не может не волновать общество, поэтому во многих странах Латинской Америки впервые за много лет был поднят вопрос легализации абортов (рис. 9). Впрочем, на данный момент никакого решения не последовало даже в Бразилии, где резонанс был особо высоким [16].

Рисунок 9. Демонстрация в поддержку права женщин на свободный аборт.
Кроме того, эпидемия лихорадки Зика некоторое время угрожала проведению Олимпийских игр 2016 в Рио-де-Жанейро. Несколько команд даже отказались от участия в соревнованиях из-за опасности заражения. Однако сейчас, когда игры уже завершились, можно смело сказать, что вирус Зика на Олимпиаду никак не повлиял.
В заключение
Сложно сказать, насколько сильным будет распространение вируса Зика, останется ли за ним статус пандемии, который заболеванию приписывает часть научного сообщества. Во многом все зависит от того, подтвердится ли половой путь передачи инфекции, не возникнет ли адаптации возбудителя к новым переносчикам, в частности, другим представителям рода Aedes. Возможно, позже будет создана эффективная и безопасная вакцина — тогда опасность заболевания будет полностью нивелирована. А пока остается расслабиться, следить за новостями и не паниковать раньше времени.
Лихорадка Зика – острое инфекционное заболевание с преимущественно трансмиссивным механизмом передачи. Заболевание протекает бессимптомно либо проявляется повышением температуры тела, общеинтоксикационным синдромом, болями в мышцах, суставах, конъюнктивитом, сыпью. Основной опасностью инфекции является формирование микроцефалии и различных неврологических нарушений у плода в случае инфицирования беременных женщин, а также стойких патологий ЦНС у взрослых. Диагностика основана на обнаружении самого вируса в биологическом материале, а также специфических антител в сыворотке крови человека. Этиотропное лечение не разработано. Проводится симптоматическая терапия.
МКБ-10
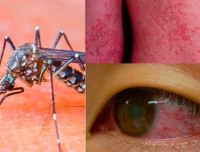
Общие сведения
Восприимчивость всеобщая. Сезонность не выражена, однако наблюдается учащение случаев инфицирования в период проливных дождей, что связано с увеличением активности комаров–переносчиков. С развитием глобального потепления ареал распространения соответствующих насекомых увеличивается, что создает еще большую опасность для человека. Однако вирус не выносит низких температур. Поэтому формирование стойких очагов лихорадки в странах с умеренным климатом невозможно, но завозные случаи могут способствовать развитию вспышек заболеваемости в летнее время.

Причины лихорадки Зика
Возбудитель заболевания – РНК-содержащий вирус из семейства Flaviviridae. Относится к арбовирусам. Патоген достаточно устойчив в окружающей среде. В лиофилизированном состоянии сохраняется до 30 месяцев. Фенол и низкопроцентный этиловый спирт не убивают микроорганизм, однако он быстро инактивируется при контакте с эфиром, раствором калия перманганата. Существует две линии вируса: азиатская и африканская. Считается, что африканская форма паразитирует у обезьян, а человек является случайным хозяином. Азиатская линия выделена от большинства больных во время эпидемий в эндемичных районах.
Источником инфекции являются обезьяны и больной человек. Передача заболевания реализуется через трансмиссивный механизм с помощью комаров вида Aedes. Возможны половой, парентеральный (при переливании компонентов крови), трансплацентарный, контактный (со слюной) пути заражения. Половой путь реализуется только у мужчин. Некоторые авторы высказывают возможность аспирационного инфицирования у лиц с иммунодефицитом. Вирус обнаруживается в крови, слюне, моче, сперме, грудном молоке, околоплодных водах при внутриутробном заражении. Опасность представляет передача вируса Зика при гемотрансфузиях и трансплантациях органов и тканей, т. к. в большинстве случаев заболевание проходит бессимптомно, отсутствует специфический скрининг доноров, что может привести к ятрогенному заражению реципиентов.
Патогенез
Механизм развития данного инфекционного заболевания до конца не изучен. Считается, что первыми в месте укуса поражаются дендритные клетка. Далее вирус с током крови разносится в различные органы и ткани. В инфицированных клетках организма человека происходит репликация РНК. Во время выхода новых вирионных частиц из клетки развивается цитолиз пораженных структур. При изучении микропрепаратов обнаружены морфологические изменения в скелетной мускулатуре, миокарде (набухание волокон, некроз, пролиферация ядер, исчезновение поперечной исчерченности). В экспериментах на лабораторных животных доказана высокая тропность вируса к клеткам нервной системы. В случае внутриутробного инфицирования патоген поражает ворсины хориона, сосуды плаценты. Возникает стойкая ишемия плода. Кроме того, вирус Зика воздействует на митотическую активность клеток, что в свою очередь ведет к формированию пороков развития.
Симптомы лихорадки Зика
В четырех из пяти случаев инфекция протекает бессимптомно. Инкубационный период составляет от 3 дней до 2 недель. Человек становится заразным за несколько дней до появления первых симптомов. Характерно наличие субфебрильной лихорадки, которая держится до 5 дней. Отмечается слабость, вялость, сонливость, чувство недомогания. Типично наличие миалгий, артралгий, боли в глазных яблоках, светобоязни. Нередко развивается конъюнктивит, отек мелких суставов.
С первого дня заболевания появляется мелкая зудящая пятнисто-папулезная сыпь на лице, туловище с последующим возможным распространением по всему телу. Элементы могут увеличиваться в размере, сливаться. Иногда формируются волдыри с прозрачным содержимым. Очень редко возникают диспепсические явления в виде тошноты, рвоты, диареи, чувства тяжести, болей в эпигастрии. Длительность заболевания составляет около 7 дней.
У беременных женщин и детей, инфицированных не трансплацентарным путем, заболевание протекает с типичной клинической симптоматикой. Считается, что после перенесенной инфекции, формируется стойкий иммунитет, повторное заражение маловероятно.
Осложнения
Наиболее грозным осложнением у взрослых, переболевших лихорадкой Зика, является развитие синдрома Гийена–Барре. Прямых доказательств связи данного неврологического нарушения с инфицированием нет, однако, по данным исследований в странах риска, более чем у 90% пациентов с синдромом Гийена–Барре обнаруживались антитела к вирусу Зика.
Наибольшую опасность представляет инфицирование женщин во время беременности, особенно в критические периоды развития плода. Характерно прерывание гестации на ранних сроках, формирование фетоплацентарной недостаточности, пороков развития, поражение ЦНС с развитием микроцефалии и мальформации головного мозга. В некоторых случаях отмечается возникновение патологии зрительного нерва. Многие авторы ассоциируют вирус Зика с развитием менингоэнцефалита, миелита, геморрагических осложнений.
Диагностика
Во время объективного осмотра специфических симптомов не выявляется. Отмечается наличие сыпи, конъюнктивита, возможно ‒ отеков мелких суставов. Данное заболевание протекает чаще всего в легкой форме, поэтому инфицированные за медицинской помощью обращаются редко. При подозрении на лихорадку Зика необходима консультация инфекциониста. В диагностике используются следующие клинико-лабораторные методы:
- Обнаружение вируса. Проводят идентификацию РНК вируса методом ПЦР с обратной транскрипцией. Данный способ наиболее информативен с 3 по 7 день от начала заболевания. В качестве исследуемого материала используют сыворотку крови. В научных исследованиях также изучают мочу и сперму.
- Серологические методы. Определяют в динамике нарастание титра специфических IgM антител методом ИФА. Данный метод может давать ложноположительные результаты из-за возможности перекрестных реакций с другими представителями флавивирусов.
- УЗИ плода. Сонография позволяет на антенатальной стадии выявить пороки развития плода. Определяются признаки микроцефалии с уменьшением окружности головы, наличие интракраниальных кальцификатов, вентрикуломегалия.
- Амниоцентез. Не существует единого мнения о необходимости проведения исследования зараженным беременным женщинам. В околоплодных водах вирус Зика обнаруживается спустя 6-8 недель после инфицирования матери. Кроме того, степень выделения патогена в амниотическую жидкость зависит от зрелости почек плода.
ВОЗ выделяет следующие критерии в диагностике лихорадки Зика: предполагаемый, возможный и подтвержденный случаи. Предполагаемый случай основывается лишь на наличии клинической симптоматики. Возможный случай включает отсутствие клиники, обнаружение IgM в крови, отягощенный эпидемиологический анамнез. Для подтвержденного варианта характерно обнаружение РНК вируса, IgM в диагностически значимом титре, исключение заражения другими флавивирусами. Дифференциальный диагноз проводится с желтой лихорадкой, лихорадкой денге, чикунгунья, краснухой, малярией, ВИЧ-инфекцией, лептоспирозом, корью, риккетсиозом, заражением парвовирусом, энтеровирусом, аденовирусом, стрептококковой инфекцией.
Лечение лихорадки Зика
Специфические препараты для терапии Зика-вирусной инфекции на сегодняшний день не разработаны. Проводится симптоматическое лечение. Пациентам рекомендуется обильное питье с целью детоксикации. При выраженном интоксикационном синдроме назначаются инфузионные растворы. До исключения лихорадки денге следует избегать приема НПВС с целью предотвращения геморрагических осложнений. Использование нестероидных препаратов у беременных до 32 недель может вызвать преждевременное закрытие боталова протока у плода. Для уменьшения зуда возможно назначение антигистаминных препаратов. Отдельные авторы рекомендуют прием средств, активизирующих иммунитет (женьшень, элеутерококк).
Прогноз и профилактика
Прогноз относительно благоприятный. В большинстве случаев данная вирусная инфекция протекает в легких формах. Однако отдаленные последствия связаны с развитием тяжелых неврологических осложнений. Также вирус ассоциирован с формированием пороков развития у плода и прерыванием беременности на ранних стадиях развития. Подобную связь демонстрируют статистические исследования.
Специфическая профилактика не разработана. Мероприятия неспецифической защиты включают в себя использование репеллентов, антимоскитных сеток в проветриваемых помещениях, одежды с длинным рукавом, уничтожение мест выплода комаров, использование кондиционеров. Беременным женщинам и женщинам, планирующим беременность, не рекомендуется посещать страны распространения инфекции. Разрабатывается алгоритм по скринингу всех беременных, вернувшихся из стран риска по лихорадке Зика. Мужчинам следует использовать барьерные методы контрацепции при возращении из путешествий по эндемичным районам как минимум в течение месяца, хотя имеются данные о выделении вируса из спермы до 60 дней.
1. Вирус Зика: новый фактор внутриутробного инфицирования плода/ Боровикова Е.И// MEDICUS. - 2016 - №3 (9).
2. Болезнь Зика - новая угроза XXI века/ Лобзин Ю.В. Бабаченко И.В.// Медицина экстремальных ситуаций. - 2016.
3. Лихорадка Зика как глобальная угроза общественному здоровью/ Козлов А.Е., Казанцев А.В., Ляпина Е.П. - 2016 - Т.6, №5.
4. Глобальные и педиатрические аспекты лихорадки Зика/ Д.О. Иванов, В.В. Малиновская, В.Н. Тимченко, Т.А. Каплина, Ж.-К. Хакизимана// Педиатр. - 2016.
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
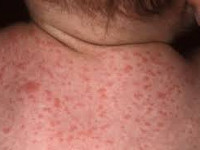
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Читайте также:

