Внутриутробный гепатит у новорожденного
Обновлено: 25.04.2024
Пример врожденного сифилиса и гепатита у новорожденного
Запоздалая диагностика раннего врожденного сифилиса может быть обусловлена смешанной этиологией гепатита при перинатальной инфекции. В качестве примера приводим сведения о ребенке, направленном в Центр гепатологии по поводу повышения активности аминотрансфераз и обнаружения у мамы до наступления беременности маркеров вируса гепатита С — anti-HCV.
Девочка Я. поступила под наблюдение Центра гепатологии в возрасте трех с половиной месяцев. Проживает в сельской местности. Направлена для решения вопроса о календаре прививок в связи с обнаружением у матери до и во время беременности anti-HCV.
Ребенок от 1 беренности, протекавшей с гестозом, угрозой прерывания. Девочка родилась в срок с весом 2 900,0, закричала сразу, к груди приложена на 2 сутки. Отмечалась желтуха, расцененная как конъюгационная. При обследовании ребенка по месту жительства в возрасте одного, двух и трех месяцев обнаруживали anti-HCV, повышение активности АЛТ до трех норм, ACT более трех норм.
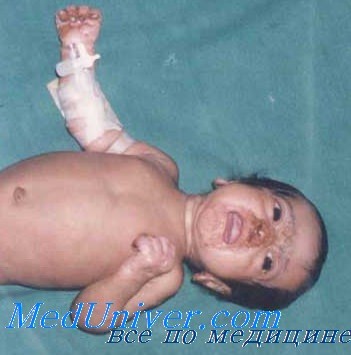
При поступлении состояние ребенка расценено как средней тяжести — бледна, беспокойна, пониженного питания. Находится на грудном вскармливании. Печень на 2—3—2 см выступает из подреберья, плотновата, чувствительна при пальпации. Селезенка до 1 см выступает из подреберья, мягкая. Бабушка и мать считают девочку здоровой, с трудом соглашаются на обследование. Билирубин — 22,0 мкмоль/л, непрямой, тимоловая проба 4,5 ед, сулемовая — 2,0 мл, АЛТ — 2 нормы, ACT — 2,5 нормы, anti-HCV положительны, anti-IgG cor— 11,2, IgG NS — 9,7 о. е.
У матери билирубин — 26,7 мкмоль/л, прямой — 4,9 мкмоль/л, тимоловая проба— 6,7 ед, сулемовая— 1,6 мл, АЛТ—7 норм, ACT — 6 норм, anti-HCV обнаружены: IgG cor— 10,2, IgG NS — 9,4 о. е. У матери и у ребенка при исследовании в Центре молекулярной диагностики ЦНИИЭ МЗ РФ обнаружена RNA HCV, генотип За. Назначены виферон на 3 месяца с последующей коррекцией дозы по возрасту, ликопид, метилурацил, галстена, ферменты, глюкоза.
Обговорена необходимость регулярного наблюдения в Центре гепатологии, постоянной информации лечащего врача о состоянии ребенка. При иследовании сывороток матери и ребенка в специализированной лаборатории реакции RW, Кана, цитохолевая положительны. После получения результатов мать и ребенок направлены под наблюдение специалиста в Областной кожно-венерологический диспансер. Выяснено, что мать ранее, до наступления беременности, получала специфическую терапию по поводу сифилиса, ребенок не обследован, не пролечен.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Врожденные гепатиты у детей – это группа гетерогенных заболеваний, возникающих в результате внутриутробного воздействия патогенных факторов на печень плода. Клинически такие патологии могут проявляться холестатическим синдромом, гепатоспленомегалией, отставанием в психофизическом развитии, неврологической симптоматикой. Лабораторная диагностика основывается на определении уровня АлАТ, АсАТ, билирубина, щелочной фосфатазы, HBs- HBe- HBc-антигенов, РСК, ПЦР, ИФА. Основное лечение – этиотропная терапия, коррекция рациона и водно-электролитного баланса. При необходимости проводится патогенетическая фармакотерапия, хирургическая коррекция или трансплантация печени.
Общие сведения
Врожденные гепатиты у детей – это полиэтиологическая группа острых или хронических воспалительных, дистрофических и пролиферативных заболеваний печени, возникающих во внутриутробном периоде либо во время родов. Суммарная распространенность всех форм составляет 1:5 000-10 000. Среди всех новорожденных порядка 15% инфицируются трансплацентарно и 10% – непосредственно во время родов. Вероятность развития врожденного гепатита у детей зависит от этиологического фактора. При остром вирусном гепатите В она составляет до 90%, при HCV-инфекции – около 5%. Прогностически благоприятными формами врожденных гепатитов у детей считаются холестатические, неблагоприятными – с выраженной гепатоцеллюлярной недостаточностью. Во втором случае летальность на первом году жизни достигает 40%.

Причины врожденных гепатитов у детей
Ведущую роль в этиологии врожденных гепатитов у детей играют вирусные инфекции из группы TORCH: цитомегаловирус, вирусы гепатита В и простого герпеса человека, вирусы Эпштейна-Барр, ECHO, краснухи. Также развитие этой группы патологий могут вызывать перенесенные во время беременности бактериальные и паразитарные заболевания: сифилис, листериоз, туберкулез, токсоплазмоз. К факторам риска со стороны матери относятся бесконтрольный прием медикаментов с гепатотоксическими свойствами, употребление алкоголя, табачных изделий, наркотических веществ. Со стороны ребенка спровоцировать развитие врожденного гепатита у детей могут наследственные ферментопатии: муковисцидоз, галактоземия, дефицит α1-антитрипсина и тирозина. Довольно часто точную этиологию определить не удается. В таком случае устанавливается диагноз идиопатический врожденный гепатит.
Механизм заражения при врожденных гепатитах у детей основывается на трансплацентарной (вертикальной) передаче вирусных или инфекционных агентов от матери к ребенку или их интранатальной аспирации вместе с околоплодными водами. Реже заражение происходит при контакте кожи и слизистых оболочек ребенка с инфицированными родовыми путями. Развитие врожденного гепатита во внутриутробном периоде обычно происходит в III триместре. Риск заражения ребенка в первой половине беременности при остром гепатите В или С составляет до 10%. Воздействие TORCH-инфекций на плод в I-II триместре может привести к спонтанному аборту.
В основе патогенеза врожденных гепатитов у детей помимо структурных изменений гепатоцитов (баллонной или вакуольной дистрофии и др.) лежит холестатический синдром. Его главное морфологическое проявление – имбибиция цитоплазмы желчными пигментами и образование желчных тромбов в начальных отделах внутрипеченочных ходов. Также при врожденных гепатитах у детей возможна гипо- или аплазия внепеченочных отделов желчевыводящих путей, что еще больше усугубляет холестаз.
Симптомы врожденных гепатитов у детей
Первые симптомы бактериальных врожденных гепатитов у детей возникают на 2-3 сутки после рождения. Как правило, отмечается субфебрильная или фебрильная температура тела, диарея, увеличение печени. Часто развиваются пневмонии и инфекционно-токсический шок, появляются признаки энцефалита. В зависимости от возбудителя наблюдаются характерные клинические особенности. Для ЦМВ характерны геморрагии, микроцефалия или гидроцефалия, поражения сетчатки, легких и почек. При краснухе отмечается незаращение артериальной протоки, поражение хрусталика и внутреннего уха. Токсоплазмозный врожденный гепатит у детей сопровождается кожными высыпаниями, гидро- и микроцефалией, хориоретинитом. При герпес-вирусном гепатите, помимо других симптомов, возникают высыпания на коже, слизистых оболочках рта и конъюнктивы, а также геморрагический синдром и ДВС-синдром. При заболевании сифилитической этиологии формируется специфическая сыпь на коже и слизистых, обнаруживается периостит.
Диагностика и лечение врожденных гепатитов у детей
Диагностика врожденных гепатитов у детей включает в себя сбор анамнеза, объективное обследование ребенка, лабораторные анализы и инструментальные методы исследования. Анамнестические данные дают возможность определить, в каком возрасте возникли первые признаки заболевания и какими они были. Также они могут указывать на потенциальные этиологические факторы. При физикальном обследовании педиатром внимательно осматриваются все кожные покровы и видимые слизистые оболочки на предмет желтухи и высыпаний. Оцениваются размеры печени и селезенки, размеры живота, определяются возможные неврологические расстройства.
При врожденных гепатитах у детей наблюдаются неспецифические изменения лабораторных анализов. Наиболее информативными являются печеночные трансаминазы – АлАТ и АсАТ, уровень которых значительно повышается. Также отмечается повышение уровня билирубина (как прямой, так и непрямой фракций), щелочной фосфатазы. При исследовании кала удается выявить отсутствие в нем желчи (ахолия), в моче определяется наличие уробилина. В диагностике врожденных гепатитов у детей крайне важными являются вирусологические и иммунологические исследования, которые позволяют установить этиологию заболевания. Среди них используются определение HBs- HBe- HBc-антигенов в крови, Ig M и G при ИФА, бактериальные посевы крови и ликвора, ПЦР и РСК.
Среди инструментальных методов исследования при врожденных гепатитах у детей информативными могут быть УЗИ и биопсия. При ультразвуковом исследовании определяются структурные изменения паренхимы печени, желчного пузыря и желчевыводящих путей. Пункционная биопсия печени используется с целью подтверждения диагноза на фоне нечеткости клинической картины и лабораторных результатов. По данным цитологического исследования тканей печени при врожденных гепатитах у детей может выявляться фиброз, склероз или некроз печеночных ацинусов, наличие гигантских клеток, лимфо- и плазмоцитарная инфильтрация, имбибиция цитоплазмы желчными пигментами.
Специфическое этиотропное лечение врожденных гепатитов у детей осуществляется в соответствии с их этиологией. При идиопатических формах применяется только патогенетическая и симптоматическая терапия. Проводится коррекция рациона ребенка, при подтверждении острой патологии у матери показан перевод на искусственные смеси, в других случаях – грудное вскармливание, нормализация водно-электролитного баланса. Смеси, применяемые у таких детей, должны быть богатыми на триглицериды, кальций, фосфор, цинк и водорастворимые витамины. При наличии холестатического синдрома в рацион ребенка также включают витамины A и E. Помимо коррекции питания могут назначаться гепатопротекторы, желчегонные, глюкокортикостероиды, интерфероны в зависимости от клинической ситуации. При наличии структурных аномалий или атрезии желчевыводящих путей выполняется их хирургическая коррекция. В тяжелых случаях врожденного гепатита у детей показана трансплантация печени.
Прогноз и профилактика врожденных гепатитов у детей
Прогноз при врожденном гепатите у детей зависит от этиологии, тяжести состояния ребенка и эффективности лечения. Показатель смертности на первом году жизни составляет 25-40%. Сюда преимущественно относятся формы, которые сопровождаются выраженной гепатоцеллюлярной недостаточностью. Еще у 35-40% детей формируются хронические заболевания печени и различные осложнения. Наиболее распространенными среди них являются холестатический синдром, синдромы недостаточности витаминов D, E и K, цирроз печени и фиброзирующий хронический гепатит, портальная гипертензия и острая печеночная недостаточность, энцефалопатия, задержка физического развития.
Специфическая профилактика врожденных гепатитов у детей проводится при выявлении у матери в крови HBs-антигенов или подтверждении диагноза острого гепатита. Таким детям уже в первый день жизни осуществляется вакцинация донорскими иммуноглобулинами и рекомбинантной вакциной. В 1 и 6 месяцев показана повторная вакцинация без иммуноглобулинов. Неспецифические профилактические меры включают в себя контроль над используемой донорской кровью и медицинским инструментарием, антенатальную охрану плода, регулярное посещение женской консультации и прохождение соответствующих обследований во время беременности.
Гепатит В у детей – инфекционное поражение печеночной паренхимы, вызываемое гепатотропным вирусом типа В. Специфические проявления гепатита В у детей развиваются в желтушном периоде, когда появляется потемнение мочи, обесцвечивание кала, желтая окраска глазных склер, слизистых и кожных покровов, тяжесть и боль в правом подреберье. Диагностика гепатита В у детей проводится на основании клинико-лабораторных данных (симптоматики, биохимического анализа крови, определения маркеров). Базовая терапия гепатита В у детей включает диету, интерферонотерапию, дезинтоксикационную терапию, назначение гепатопротекторов, сорбентов, витаминов; в тяжелых случаях – плазмаферез и гемосорбцию.
Общие сведения
Гепатит В у детей (парентеральный или сывороточный гепатит) – специфическое вирусное воспаление печени, протекающее в острой или хронической форме. Возбудителем гепатита В у детей является ДНК-содержащий вирус, высоко патогенный и чрезвычайно устойчивый к воздействиям окружающей среды. При инфицировании ребенка вирусом гепатита В в перинатальном периоде или грудном возрасте вероятность хронического поражения печени возрастает до 70-90%. У 20-35% людей, инфицированных гепатитом В в детстве, в дальнейшем развивается цирроз печени или первичная гепатоцеллюлярная карцинома. Профилактика и повышение эффективности лечения гепатита В у детей служит одной из приоритетных задач педиатрии.

Причины гепатита В у детей
Гепатит В у детей является типичной антропонозной инфекцией; источником заражения выступают как больные люди, так и вирусоносители. Основными путями инфицирования детей гепатитом В служат трансплацентарный (внутриутробное заражение), интранатальный (в процессе родов), постнатальный (послеродовый).
Трансплацентарный путь передачи реализуется в 6-8 % всех зафиксированных случаев. Особенно часто инфицирование плода происходит на фоне фетоплацентарной недостаточности и отслойки плаценты. Внутриутробное инфицирование плода вирусом гепатита В грозит преждевременными родами. Интранатальная передача вируса гепатита В у детей (около 90%) обусловлена контактом ребенка с биологическими жидкостями и кровью инфицированной матери при прохождении по родовым путям. Постнатальное заражение ребенка происходит в процессе кормления грудью или ухода за младенцем: при нарушении целостности кожи и слизистых оболочек у ребенка, тесном контакте с инфицированной матерью, выделении вируса с кровью из трещин сосков.
В более старшем возрасте заражение детей гепатитом В может происходить при использовании общих полотенец, мочалок, зубных щеток и др. предметов гигиены, а также половым путем (у подростков). Не исключается возможность инфицирования детей гепатитом В при проведении гемотрансфузии, инвазивных лечебно-диагностических процедур. Риск развития гепатита В повышен у детей, находящихся на почечном диализе. Высока вероятность инфицирования среди подростков-наркоманов, использующих общие иглы и шприцы.
Незрелость иммунной системы детей обусловливает быстрое распространение вируса гепатита В через жидкие среды организма и поражение паренхимы печени. Обычно острая форма гепатита В у детей протекает быстро и заканчивается выздоровлением с выработкой стойкого пожизненного иммунитета к вирусу. При латентном, бессимптомном течении гепатита В у детей во взрослом возрасте может быть случайно выявлено рубцовое изменение ткани печени. Дети с хроническим гепатитом В являются пожизненными вирусоносителями.
Симптомы гепатита В у детей
Циклическое течение гепатита В у детей включает инкубационный (латентный), преджелтушный, желтушный периоды и период реконвалесценции.
Продолжительность инкубационного периода составляет 2-4 месяца и определяется инфицирующей дозой, путем заражения и возрастом ребенка. В случае переливания инфицированных компонентов крови длительность латентного течения гепатита В у ребенка уменьшается до 1,5-2 месяцев, при других путях заражения может увеличиваться до 4-6 месяцев. Чем меньше возраст ребенка, тем непродолжительнее инкубационный период. На данном этапе клинические проявления гепатита отсутствуют, однако в конце периода в крови обнаруживаются маркеры гепатита В (НВsAg, НВeAg, анти-НВсAg IgM) и высокая активность печеночных ферментов.
В преджелтушном периоде, который длится от нескольких часов до 2-3 недель, преобладает общая инфекционная астения (слабость, вялость), миалгии и артралгии, кожные высыпания, абдоминальный синдром, срыгивания, рвота, снижение аппетита, метеоризм, понос. Иногда первыми клиническими признаками гепатита В у детей служат потемнение мочи и обесцвечивание кала. В крови отмечается повышенный уровень трансаминаз и прямого билирубина, обнаруживается ДНК вируса.
Период желтухи при гепатите В у детей может длиться от 7-10 дней до 1,5-2 месяцев. Появлению желтухи во всех случаях предшествует изменение цвета мочи и кала. Интенсивность желтушного окрашивания кожи и видимых слизистых оболочек нарастает в течение 7 дней и сохраняется еще 1-2 недели. В отличие от гепатита А, при гепатите В с появлением желтухи обще состояние не улучшается, а интоксикационный синдром, напротив, усиливается: температура тела повышается до 38°С, нарастает вялость, заторможенность, адинамия. У детей с гепатитом В может отмечаться появление пятнисто-папулезной сыпи на коже, артериальная гипотония, увеличение размеров печени, иногда – селезенки. На высоте желтушного периода в крови регистрируется максимальная активность трансаминаз, снижение ПТИ, гипоальбуминемия.
При благоприятном течении гепатита В у детей заболевание оканчивается периодом реконвалесценции, который продолжается 3-4 месяца. Постепенно исчезает желтуха, нормализуется аппетит, сон, активность, показатели крови. Гепатит В у детей может иметь острое (до 3 мес.), затяжное (до 6 мес.) и хроническое (более 6 мес.) течение.
У грудных детей преобладают среднетяжелые и тяжелые формы гепатита В, возможны летальные исходы вследствие злокачественного течения заболевания. В последнем случае у детей быстро нарастает картина печеночной энцефалопатии, печеночной недостаточности, развивается печеночная кома.
Диагностика гепатита В у детей
Постановке обоснованного диагноза способствует осмотр ребенка педиатром и детским инфекционистом, анализ сведений о развитии и течении заболевания (цикличность, характерная симптоматика), эпидемиологический анамнез (предшествующие гемотрансфузии, инъекции, инвазивные манипуляции, операции) и т. п.
Основная роль в диагностике гепатита В у детей принадлежит лабораторным методам: обнаружению маркеров (HBsAg, HBeAg, анти-HBs, анти-НВе, анти-НВс), изменению биохимических показателей крови (повышению уровня билирубина и увеличению активности трансфераз).
При подозрении на гепатит В у детей в преджелтушном периоде следует исключить грипп, ОРВИ, пищевые токсикоинфекции, артрит; в желтушном периоде - вирусные гепатиты А, С, Е, желтую лихорадку, инфекционный мононуклеоз, цитомегаловирусную инфекцию, синдром Жильбера, ЖКБ, холангит, панкреатит, цирроз печени и пр. С целью дифференциальной диагностики дополнительно проводятся МР холангиография, УЗИ печени и желчного пузыря, сцинтиграфия печени, пункционная биопсия печени.
Лечение гепатита В у детей
Дети с диагностированным гепатитом В подлежат госпитализации в инфекционное отделение. В течение всего желтушного периода показан постельный режим, затем – щадящий режим. Назначается диета (стол №5 по Певзнеру) с преобладанием молочно-растительной, механически и химически щадящей пищей, обильное питье.
Базисная лекарственная терапия гепатита В у детей включает витамины групп В, С, А, Е; спазмолитики (папаверин, дротаверин), гепатопротекторы, желчегонные средства. При тяжелых формах гепатита В у детей показаны интерфероны, дезинтоксикационная терапия, трансфузии плазмы и альбумина, при необходимости - глюкокортикоиды, гепарин, мочегонные препараты, плазмаферез, гемосорбция.
Диспансерное наблюдение реконвалесцентов проводится в течение 1 года (каждые 3 месяца) с осмотром кожи и видимых слизистых, определением размеров печени и селезенки, оценкой цвета мочи и кала, определением лабораторных показателей. Детям, перенесшим гепатит В, рекомендуется санаторное лечение в учреждениях гастроэнтерологического профиля.
Прогноз и профилактика гепатита В у детей
Типичные формы гепатита В у детей, как правило, заканчиваются выздоровлением. Переход в хроническую форму отмечается в 2-18% случаев. Перенесенный в детстве гепатит В сопровождается формированием стойкого пожизненного иммунитета.
Осложнениями гепатита В у детей могут являться хронический гепатит или цирроз печени, резко повышающие риски развития гепатоцеллюлярной карциномы во взрослом возрасте. При злокачественном течении гепатита В у детей летальность крайне высока (75%).
Самым надежным способом профилактики гепатита В у детей является вакцинация, которая осуществляется трехкратно: в первые сутки после рождения ребенка, 1 и 6 месяцев жизни рекомбинантными вакцинами Регевак, Энджерикс В, Эувакс В, Комбиотех и др. Вакцинация против гепатита В обеспечивает 95% защиту от инфекции на 15 лет.
Неспецифическая профилактика гепатита В у детей предполагает использование одноразового медицинского инструментария, тщательную обработку и стерилизацию многоразовых инструментов, обследование доноров, проведение трансфузионной терапии по строгим показаниям.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Неонатальный гепатит у детей: причины, диагностика
Заболевание характеризуется развитием воспаления в печени. Во многих случаях какой-либо причины выявить не удаётся. В отличие от билиарной атрезии у детей с неонатальным гепатитом часто наблюдают ЗВУР и гепатоспленомегалию при рождении. При биопсии печени в ряде случаев выявляют только неспецифические изменения.
Недостаточность а1-антитрипсина как причина неонатального гепатита. Недостаточность a1-антитрипсина может проявляться поражением печени у детей (в том числе грудного возраста) и эмфиземой лёгких у взрослых. Это аутосомно-рецессивное заболевание, частота которого в Великобритании составляет 1 случай на 1000-2000. Существует несколько фенотипов ингибитора протеаз (Pi), кодирующий их ген локализуется на хромосоме 14. Болезнь печени ассоциирована с фенотипом PiZZ.
У детей заболевание чаще всего проявляется затяжной неонатальной желтухой, в некоторых случаях также развивается геморрагический синдром (в том числе внутричерепные кровоизлияния), обусловленный дефицитом витамина К (особенно у детей, находящихся на грудном вскармливании). Выявляют гепатомегалию, по мере развития цирроза печени и портальной гипертензии развивается спленомегалия. Для подтверждения диагноза определяют концентрацию а1-антитрипсина в плазме крови и его фенотип.
Приблизительно у 30% детей симптоматика разрешается, у остальных развивается хроническое поражение печени, которое в части случаев приводит к циррозу печени и портальной гипертензии, что обусловливает необходимость трансплантации печени. Значимые поражения лёгких у детей не наблюдают. Недостаточность а1-антитрипсина можно диагностировать в антенатальном периоде.

Галактоземия как причина неонатального гепатита. Заболевание наблюдают редко (1 случай на 40 000). Характерны недостаточная прибавка массы тела, рвота, желтуха и гепатомегалия при грудном вскармливании. При отсутствии лечения неизбежно развиваются хроническая печёночная недостаточность, катаракта и задержка развития. В некоторых случаях наблюдают быстро прогрессирующее течение заболевания с летальным исходом, характеризующееся развитием шока, геморрагического и ДВС-синдрома, часто вследствие сепсиса, вызванного грамотрицательными бактериями.
В качестве скрининга на галактоземию у новорождённых с затяжной желтухой используют тест-восстанавливающие субстанции в моче. Диагноз подтверждают с помощью определения активности галактозо-1-фосфатуридилтрансферазы в эритроцитах. Диета с исключением галактозы позволяет предупредить прогрессирование поражения печени, но в дальнейшем могут развиться яичниковая недостаточность и нарушения обучения.
Другие причины кнеонатального гепатита. Неонатальный гепатит может развиваться при тирозинемии 1-го типа, муковисцидозе, болезнях накопления липидов и гликогена, пероксисомных болезнях, а также иногда ассоциируется с парентеральным питанием.
Синдром Аладжила — аутосомно-доминантное заболевание. Характерные признаки включают треугольное лицо, аномалии скелета, периферический стеноз лёгочной артерии, почечные тубулярные нарушения, аномалии глаз, гипоплазию внутрипечёночных жёлчных протоков, проявляющуюся выраженным зудом и нарушением физического развития. Прогноз вариабельный, 50% детей доживают до зрелого возраста без трансплантации печени.
Прогрессирующий семейный внутрипечёночный холестаз (PFIC) — гетерогенная группа холестатических расстройств, связанных с дефектами переносчика жёлчных кислот. Клинические проявления включают желтуху, зуд, нарушение физического развития, диарею и поражение печени. Прогноз вариабельный, в части случаев может потребоваться трансплантация печени.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

