Вынашивание ребенка с вирусом
Обновлено: 13.05.2024
Вирусы гепатита В и С, попав в организм человека, вызывают воспаление в печени – гепатит. Вначале оно протекает бурно и называется острым гепатитом, затем, если организм справляется с инфекцией, наступает выздоровление. В случае с гепатитом В это происходит гораздо чаще. До 95% взрослых выздоравливают от острого гепатита В самостоятельно, от острого гепатита С – лишь 20% людей. Часто человек даже не знает о том, что он заразился вирусом гепатита, так как симптомы болезни в обоих случаях могут быть слабозаметными или отсутствовать вовсе.
Если в течение 6 месяцев острый гепатит не проходит самостоятельно, наступает хронический гепатит. Это означает, что с этого времени вирус существует в клетках печени постоянно, а значит, в ней происходит постоянное воспаление. С годами это может привести к тяжелым последствиям – циррозу и раку печени. Поэтому проблеме вирусных гепатитов В и С уделяют столько внимания.
Как передаются вирусы гепатита В и С?
Вирусы гепатита В и С содержатся в крови и биологических жидкостях больного человека. Заражение происходит, когда его кровь, слюна, сперма или отделяемое из влагалища попадают в кровь или на поврежденные кожу и слизистые другого человека. Оба вируса могут передаваться от матери ребенку, это называется перинатальным путем заражения.
Вирус гепатита В гораздо более заразный, чем вирус гепатита С, поэтому довольно часто передается при половых контактах и от матери ребенку. Риск заражения выше, в случае если болезнь протекает активно и в крови обнаруживается высокая концентрация вируса.
Риск передачи вируса гепатита С при половых контактах и от матери ребенку очень мал, он не превышает 5%. В основном этот вирус передается при прямом контакте с инфицированной кровью.
Искаженное представление о вирусных гепатитах В и С
К сожалению, такое искаженное восприятие нередко встречается даже среди врачей.
Этот подход к болезни заставляет больных людей стыдиться ее, скрывать свои переживания даже от близких, бояться осуждения окружающих.
На самом деле все обстоит далеко не так. Конечно, у людей, употребляющих наркотики или занимающихся проституцией, риск заразиться гепатитами очень высок, но важно помнить, что вирусы гепатита В и С передаются далеко не только при использовании общих шприцев или беспорядочных половых связях. Ситуаций, при которых происходит контакт с инфицированной кровью, очень много, это, например, переливание крови, операции, выполнение таких, казалось бы безобидных процедур, как маникюра, педикюра, татуировок.
Существует еще много неверной или сильно искаженной информации о вирусных гепатитах В и С, и один из центральных вопросов – вопрос о возможности зачать здорового ребенка.
Если выявлен гепатит В или С, возможна ли беременность?
Итак, болеющих хроническими гепатитами В и С довольно много, среди них – масса молодых женщин и мужчин, готовых создать семью и иметь детей. Однако бытующее по сей день в обществе опасное заблуждение о том, что эти болезни чуть ли ни смертельно опасны, мешает многим осуществить свое желание.
Важно помнить, что вирусы гепатита В и С не влияют на развитие плода. Яйцеклетки и сперматозоиды, которые участвуют в формировании ребенка, не инфицированы этими вирусами. Если в семье кто-то из будущих родителей болен гепатитом В или С, они могут планировать детей. Важно лишь помнить некоторые детали, о которых речь пойдет дальше.
Что делать, если во время беременности впервые выявлен гепатит В или С?
Как правило, в 1-м и 3-м триместрах беременности женщин обследуют на гепатиты В и С. Нередко именно тогда впервые выявляются эти инфекции. Далее необходимо провести дополнительное обследование, чтобы правильно поставить диагноз и понять, как поступать дальше. В этом случае лучше обратиться к гепатологу – врачу, который занимается гепатитами.
В случае в гепатитом В определяют наличие HBeAg в крови, количественный анализ на ДНК вируса гепатита В, некоторые биохимические показатели крови, основные среди них – АЛТ, АСТ, билирубин. При положительном анализе на гепатит С проводят уточняющий анализ на РНК вируса гепатита С (качественный и количественный), а также исследуют биохимические показатели крови. И при гепатите В, и при гепатите С определяют стадию болезни, чаще всего при помощи безопасного исследования – эластометрии печени.
Как уже сказано, эти вирусы не влияют на развитие плода, поэтому необходимости прерывать беременность нет.
Как нужно обследоваться во время беременности?
Если диагностирован хронический гепатит В или С, и не обнаружен цирроз печени (он бывает крайне редко среди молодых женщин), обследование во время беременности во многом носит формальный характер, так как активных действий, как, например, лечение, проводить нельзя (в случае с гепатитом С) или с осторожностью (в случае с гепатитом В). Как правило, контролируются биохимические показатели крови и вирусная нагрузка (количественное определение ДНК вируса гепатита В и РНК вируса гепатита С).
Нужно ли лечение гепатита во время беременности?
Лечение гепатита С во время беременности строго запрещено, гепатита В – допустимо некоторыми препаратами, но при условии крайней необходимости. Поэтому, если у будущей мамы вируса гепатита В в крови очень много, некоторые врачи иногда назначают противовирусные препараты, чтобы снизить риск передачи инфекции ребенку. Но такое решение принимается в каждом случае индивидуально.
Где проводят роды у инфицированных вирусными гепатитами В и С?
Прием родов у таких будущих мам производят в специально выделенной палате, предпочтительно в боксе. Для подтверждения и уточнения диагноза в роддомах требуют заключение гепатолога.
При выборе роддома необходимо поинтересоваться, есть ли у него возможности принимать роды у инфицированных вирусами гепатита.
Имеет ли смысл применить кесарево сечение для того, чтобы снизить риск заражения ребенка?
Нет, вариант родоразрешения не имеет какого-либо предпочтения. Гепатит В или С у беременной не является противопоказанием для естественных родов.
Обязательно ли заразится ребенок?
Заражение ребенка может произойти только от инфицированной матери, как правило, это происходит во время родов. То есть если в семье болен только отец, инфекция ребенку не передастся.
Риск передачи вируса гепатита C от матери ребенку очень мал, от 1 до 5%. Он возрастает при высоких концентрациях вируса гепатита C в крови будущей мамы, а также при наличии у нее ВИЧ-инфекции.
Риск передачи вируса гепатита В значительно выше и зависит от активности болезни у мамы, то есть от концентрации вируса в ее крови и от наличия HBeAg. При очень высокой активности болезни вероятность заражения ребенка доходит до 85-100%. У детей, заразившихся вирусом гепатита В от инфицированных мам, гораздо чаще, чем у взрослых, возникает хронический гепатит В. Это происходит в 90% случаев (а у взрослых, как уже говорилось, всего в 5%, так как 95% выздоравливают самостоятельно). Поэтому так важно провести вакцинацию ребенка против гепатита В в первые часы жизни, о чем пойдет речь дальше.
Можно ли кормить грудью ребенка?
Да, ребенка можно кормить грудью.
Случаев передачи вируса гепатита C от матери ребенку при грудном вскармливании не выявлено.
Вирус гепатита В может передаваться при кормлении грудью, но если ребенку была вовремя сделана вакцина против гепатита В, кормить можно.
Вакцины против гепатитов
Вакцины против гепатита С нет.
Вакцина против гепатита В существует, она безопасна, так как не содержит вирус, и очень важна, потому что позволяет сильно снизить риск заражения гепатитом В. Это особенно актуально для новорожденного, если мама болеет хроническим гепатитом В. Если ребенок рождается от инфицированной мамы, ему должны ввести вакцину в первые часы жизни. Промедление опасно, с каждым пропущенным днем эффективность вакцины будет снижаться.
Что делать, если ребенок заразился от мамы гепатитом В или С?
Информация о центрах с консультацией гепатологов
Врачи, которые занимаются хроническими гепатитами В и С, называются гепатологами. По специальности это либо гастроэнтерологи, либо инфекционисты. В каждом субъекте страны есть городские или областные инфекционные больницы, в которых, как правило, консультируют гепатологи. Кроме того, в некоторых городах есть частные центры, специализирующиеся на вирусных гепатитах.
Вот список основных центров Москвы, куда можно обратиться за консультацией гепатолога:
Школа для пациентов с хроническими вирусными гепатитами
В Центральном НИИ эпидемиологии с 2009 г. проводится школа для людей, больных гепатитами. На занятиях обсуждаются все вопросы, связанные с этими болезнями, есть возможность задать вопрос специалистам.
Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Врождённый токсоплазмоз
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Врождённая краснуха
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Врождённая цитомегалия
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Врождённая герпетическая инфекция
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
ВИЧ-инфекция у детей – это патологическое состояние, вызванное вирусом иммунодефицита человека (ВИЧ) и характеризующееся прогрессирующим снижением иммунитета ребенка. Специфических клинических симптомов нет, основные проявления – лихорадка, диарея неясной этиологии, лимфаденопатия, частые инфекционные и бактериальные заболевания, СПИД-ассоциированные и оппортунистические патологии. Основные методы лабораторной диагностики ВИЧ-инфекции у детей – ИФА, иммуноблоттинг, ПЦР. Специфическое лечение включает в себя схемы антиретровирусных препаратов (ингибиторов обратной транскриптазы и протеазы).

Общие сведения
ВИЧ-инфекция у детей – это заболевание, которое развивается в результате длительной персистенции вируса иммунодефицита человека в лимфоцитах и клетках нервной системы и характеризуется медленно прогрессирующей дисфункцией иммунной системы. Впервые данный вирус был описан французским вирусологом профессором Люком Монтанье в 1983 году. ВИЧ – это РНК-содержащий ретровирус, имеющий сложное строение и высокую изменчивость, что обеспечивает его выраженную способность к репликации и стойкости в организме человека. Распространенность ВИЧ-инфекции у детей за последние 15 лет уменьшилась более чем на 50%. Ежегодно в мире фиксируется порядка 250 тысяч случаев, из них в России около 6,5-7,5 тысяч. Правильное проведение профилактики вертикальной трансмиссии вируса позволило снизить частоту инфицирования с 30% до 1-3% беременностей ВИЧ-позитивных матерей.

Причины ВИЧ-инфекции у детей
ВИЧ-инфекция у детей имеет несколько механизмов передачи. Вирус может быть получен ребенком гематогенным путем от матери во время беременности. Также инфицирование может произойти во время использования необработанного медицинского инструментария, гемотрансфузий, трансплантации органов, у старших детей – при незащищенном половом акте. Все эти пути реализуются за счет содержания вируса в биологических жидкостях (кровь, спинномозговая жидкость, сперма, влагалищные выделения), тканях и органах инфицированного человека.
Основная причина (примерно 80%) ВИЧ-инфекции у детей – вертикальная передача вируса от матери к ребенку. Выделяют 3 периода, в которых потенциально возможно заражение – перинатальный (через систему плацентарного кровообращения), интранатальный (при контакте кожных покровов ребенка с кровью и секретом влагалища матери) и постнатальный (через грудное молоко). Риск инфицирования указанными путями составляет 20%, 60% и 20% соответственно. К факторам, повышающим риск передачи, относятся отсутствие профилактического лечения матери во время вынашивания ребенка, многоплодная беременность, преждевременные роды и роды через естественные половые пути, маточные кровотечения и аспирация крови ребенком, прием наркотических веществ и алкоголя во время беременности, вскармливание грудным молоком, экстрагенитальная патология и коинфекция.
Патогенез ВИЧ-инфекции у детей основан на связывании вируса с CD4+ Т-лимфоцитами, в которых он модифицирует ДНК клетки. В результате этого начинается синтез новых вирусных частичек, а затем – вирионов. После полной репродукции вируса происходит гибель Т-лимфоцитов, однако инфицированные клетки остаются в системном кровотоке, служа резервуаром. Как результат отсутствия функционально полноценных иммунокомпетентных клеток развивается иммунодефицит. Характерной особенностью ВИЧ-инфекции у детей является сопутствующий дефицит В-лимфоцитов и тропность вируса к тканям ЦНС. Проходя сквозь гематоэнцефалический барьер, вирус вызывает аномалию расположения глиальных клеток, задержку развития головного мозга, дистрофию и атрофию нервной ткани и определенных нервов (чаще всего – зрительного). В педиатрии поражение ЦНС является одним из первых маркеров наличия ВИЧ.
Симптомы ВИЧ-инфекции у детей
Клиническая картина ВИЧ-инфекции у детей может существенно отличаться в зависимости от периода и способа передачи вируса. При инфицировании парентеральным или половым путем присутствует острый ретровирусный синдром, после чего заболевание протекает в 4 стадии: два латентных этапа и два периода развернутых клинических симптомов. При вертикальном пути заражения острый ретровирусный синдром и бессимптомная стадия не выявляются. Острый ретровирусный синдром наблюдается у 30-35% детей после окончания инкубационного периода (от 2 недель до 3 месяцев с момента инфицирования). Клинически ВИЧ-инфекция у детей на этом этапе может проявляться фарингитом, лимфоаденопатией, гепатоспленомегалией, субфебрилитетом, уртикарной или папулезной сыпью, редко – менингеальными симптомами. Ее длительность колеблется от 2 суток до 2 месяцев, в среднем составляет 21 день.
Следующая стадия – бессимптомного носительства и персистирующей лимфаденопатии. Возможное проявление ВИЧ-инфекции у детей на этой стадии – увеличение двух групп лимфоузлов. Ее длительность – от 2 до 10 лет. Вторая стадия характеризуется потерей массы тела (порядка 10%), поражением кожных покровов и слизистых оболочек (дерматиты, микозы придатков кожи, рецидивные заболевания слизистых ротовой полости и губ), рецидивирующим опоясывающим герпесом. Общее состояние, как правило, не нарушается. Третья стадия включает в себя выраженные проявления иммунодефицита: общее недомогание, диарею невыясненной этиологии, анорексию, лихорадку, головную боль, потливость по ночам, спленомегалию. ВИЧ-инфекция у детей на данном этапе сопровождается неврологическими нарушениями, отмечаются периферическая невропатия, ухудшение памяти. Также она характеризуется рецидивирующим кандидозом полости рта, простым и опоясывающим герпесом, ЦМВ-паротитом. При четвертой стадии (стадия СПИДа) на первый план выходят клинические проявления тяжелых оппортунистических заболеваний и опухолей.
У младенцев и детей в возрасте до 3 лет типичной особенностью является высокая частота тяжелых бактериальных инфекций. Практически в 50% случаев ВИЧ-инфекции у детей возникают гнойные отиты, менингиты, поражения кожи, бактериальные пневмонии со склонностью к абсцедированию и появлению плеврального выпота, бактериальный сепсис, поражения суставов и костей. Как правило, в роли возбудителей выступают S. pneumoniae, S. aureus, H. influenzae, E. coli и некоторые виды сальмонелл.
Диагностика ВИЧ-инфекции у детей
Диагностика ВИЧ-инфекции у детей основывается на данных анамнеза и лабораторных тестах. Объективный осмотр и инструментальные методы исследования информативны только в случае развития бактериальных инфекций или СПИД-ассоциированных заболеваний. Подозрение на ВИЧ-инфекцию у детей возникает при выявлении педиатром хотя бы четырех из следующих симптомов: отягощенный эпидемиологический анамнез, генерализованная гиперплазия лимфоузлов, потеря массы тела (свыше 10% от исходной), необоснованная диарея (более 1 месяца), стойкая или перемежающаяся гипертермия (более 1 месяца), частые бактериальные, вирусные, грибковые или паразитарные заболевания, СПИД-ассоциированные и оппортунистические патологии и т. д.
Ведущее место в диагностике ВИЧ-инфекции у детей занимают лабораторные тесты. Среди неспецифических изменений в общем и биохимическом анализах крови могут присутствовать анемия, лейкопения, тромбоцитоз или тромбоцитопения, повышение уровня АлТ и/или АсТ. При иммунологических исследованиях у таких детей можно выявить повышение уровня иммуноглобулинов, падение уровня CD4 и соотношения CD4/CD8, уменьшение продукции цитокинов, повышение уровня циркулирующих иммунокомплексов, у новорожденных возможна гипо-γ-глобулинемия. Специфическая диагностика ВИЧ-инфекции у детей подразумевает проведение ИФА с определением антител к вирусу. При его позитивном результате осуществляется иммуноблоттинг с идентификацией иммуноглобулинов к некоторым белкам вируса (gp 41, gp 120, gp 160). В последнее время широко используются тесты для определения вирусной нагрузки (количества копий вирусной РНК).
Лечение ВИЧ-инфекции у детей
Лечение ВИЧ-инфекции у детей заключается в проведении специфической антиретровирусной терапии, профилактике или лечении оппортунистических заболеваний и устранении симптомов патологии. В современной медицинской практике используются противовирусные препараты, ингибирующие обратную транскриптазу (нуклеозидные и ненуклеозидные аналоги) и протеазу. Наиболее эффективной считается схема, состоящая их трех препаратов – два нуклеозидных аналога и один ингибитор протеазы. Выбор конкретных медикаментов, схема их употребления подбираются индивидуально для каждого ребенка. В зависимости от имеющихся оппортунистических заболеваний используются специфические этиотропные (антибиотики, противотуберкулезные, противовирусные, противогрибковые препараты и пр.) и симптоматические (жаропонижающие, антигистаминные, пробиотики, витаминные комплексы, дезинтоксикационная терапия) средства.
Прогноз и профилактика ВИЧ-инфекции у детей
Прогноз при ВИЧ-инфекции у детей серьезный. Как правило, правильно подобранная антиретровирусная терапия позволяет добиться замедления репликации вируса на долгие годы, однако на данный момент ВИЧ остается неизлечимым заболеванием. На фоне проводимого лечения удается достичь высокого качества и удовлетворительной продолжительности жизни и полной адаптации ребенка в социуме.
Профилактика ВИЧ-инфекции у детей включает в себя исключение всех возможных путей передачи вируса: контроль переливаемой крови и трансплантируемых органов, медицинского инструментария, избежание незащищенных половых актов. Отдельное место занимает профилактика вертикальной трансмиссии. Согласно рекомендациям UNICEF, она включает в себя помещение беременной ВИЧ-позитивной женщины на учет у гинеколога, прием противовирусных средств с 24-28 недели, рациональный выбор способа родоразрешения, исключение грудного вскармливания, назначение противовирусных средств ребенку с момента рождения. Данные меры позволяют снизить риск развития ВИЧ-инфекции у детей до 1-3%.
Что такое перенашивание беременности? Причины возникновения, диагностику и методы лечения разберем в статье доктора Коротковой Оксаны Владимировны, гинеколога со стажем в 9 лет.
Над статьей доктора Коротковой Оксаны Владимировны работали литературный редактор Маргарита Тихонова , научный редактор Светлана Симанина и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Процесс беременности, задуманный природой, рассчитан на 287 дней. Отклонения от этих сроков возможны, но для них всегда существует веская причина. Если дата родов, рассчитанная доктором, уже прошла, а роды так и не наступили, следует предполагать перенашивание беременности.

Переношенная беременность — это беременность, длящаяся более 42 недель или более 294 дней [12] . Она встречается примерно в 4-14 % случаев [1] [5] [7] . Чаще с ней сталкиваются первородящие женщины после 30 лет [3] . Причём каждая беременность, закончившаяся запоздалыми родами, увеличивает риск переношенности при последующей беременности.
Все изменения в плаценте, которые происходят при перенашивании, приводят к длительным затяжным родам и могут стать причиной родовых травм плода (переломов ключиц, различных гематом) и других осложнений. Все они опасны для новорождённого и нарушают процесс его адаптации к внеутробной жизни.
Причины перенашивания многообразны. В большинстве случаев оно развивается при сочетании причин, факторов риска, особенностей организма беременной и самого плода. К ним относятся:
- недостаточная перестройка нервной системы женщины к родам — неправильное соотношение в работе симпатической и парасимпатической нервной системы, недостаточно сформированная родовая доминанта (особая рефлекторная система, отвечающая за своевременное наступление родов);
- эндокринные патологии — сахарный диабет, ожирение , гипотиреоз ;
- гормональный дисбаланс, в частности снижение уровня эстриола, отвечающего за готовность матки и половых путей к родам;
- осложнения беременности — маловодие или хроническая плацентарная недостаточность;
- психические травмы.
Причинами перенашивания беременности могут стать нарушения женской репродуктивной системы:
- генитальный инфантилизм (недоразвитие полового аппарата);
- аномалии развития репродуктивной системы — дисфункция яичников, нарушения менструального цикла;
- перенесённые гинекологические инфекции;
- травмы половых органов;
- искусственные или самопроизвольные аборты в анамнезе.
Причинами перенашивания со стороны плода могут быть его хромосомные аномалии (синдром Дауна, поликистоз почек) или тяжёлые пороки развития:
- анэнцефалия (отсутствие головного мозга); (увеличение объёма жидкости в головном мозге);
- микроцефалия (маленький головной мозг) [2][8] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы перенашивания беременности
К симптомам перенашивания беременности относят уплотнение матки за счёт маловодия, уменьшение размера живота, снижение веса беременной относительно последних измерений, выделения из молочных желёз. При этом шейка матки не указывает на биологическую готовность родовых путей к родоразрешению. Также выявляются признаки ухудшения состояния плода:
- по данным УЗИ — маловодие, структурные изменения в плаценте, её преждевременное созревание, нарушение кровотока в артериях пуповины или маточных артериях;
- по данным кардиотокографического исследования (КТГ) — снижение компенсаторных возможностей плода, признаки его гипоксии (нехватки кислорода).
При рождении переношенный младенец отличается характерным внешним видом. Его кожа и слизистые оболочки, а также пуповина и плацента окрашены в зелёный или жёлтый цвет. Если количество защитной сыровидной смазки снижено, то кожа и слизистые покровы плода становятся сухими. При отсутствии смазки они сморщиваются из-за контакта с околоплодными водами. Кожа стоп и ладоней новорождённого выглядит распаренной, как после бани. На руках и ногах видны длинные ногти [1] [5] [6] [11] .
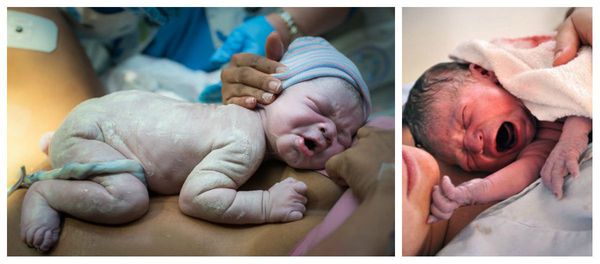
При перенашивании ребёнок, как правило, крупный, его рост и головка увеличены. Но возможен и другой вариант, когда рождается небольшой по весу малыш с уменьшенным количеством подкожно-жировой клетчатки (в связи с задержкой роста плода), но с вышеописанными признаками перезрелости. Плотность костей черепа новорождённого повышена, роднички маленькие, а швы узкие, что затрудняет процесс приспособления головки плода к родовым путям матери — как следствие, это становится причиной травм матери во время родов.
Патогенез перенашивания беременности
Основное звено патогенеза переношенной беременности — это изменения со стороны плаценты (плацентарная недостаточность). Они вызывают внутриутробный дефицит кислорода у плода. Такое отклонение приводит к выраженным изменениям и нарушению состояния ребёнка. При этом плацентарная дисфункция, дисбаланс эндокринной системы плода, наличие факторов риска перенашивания не позволяют родам начаться в срок, усугубляя уже имеющиеся нарушения.
При беременности плацентарная дисфункция проявляется нарушением кровотока в маточных артериях и/или артериях пуповины [1] [8] . При морфологическом исследовании плаценты диагностируются признаки сниженной циркуляции крови, образование мелких тромбов, склероз ворсин и сосудов и снижение количества капилляров. Также в ней могут быть обнаружены кальцинаты — локальные скопления кальция в очаге нарушенного кровотока.
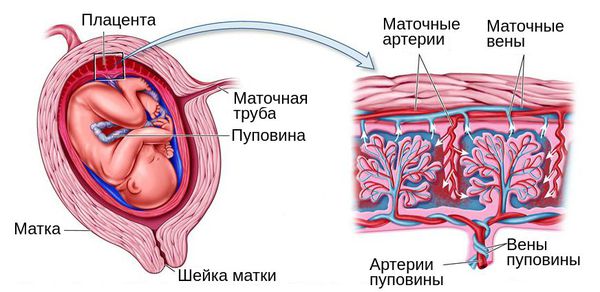
Для выживания плода при дефиците поступающего к нему кислорода организм запускает процесс централизации кровообращения. При этом в жизненно важных органах малыша, таких как мозг, сердце и печень, кровоток сохраняется, а в мышцах, кишечнике, почках и остальных органах уменьшается.
Из-за снижения кровотока в почках плода выделение мочи значительно уменьшается, развивается маловодие. Также изменяется характер околоплодных вод: они теряют прозрачность, становятся мутными, приобретают желтоватый или зеленоватый оттенок из-за примеси мекония — первых фекалий ребёнка.
За счёт изменения состава околоплодных вод нарушается выработка сурфактанта — вещества, которое не даёт альвеолам слипаться во время выдоха. Это вызывает патологию лёгочной ткани и нарушение дыхания после рождения. Также снижается защитная функция лёгких: в водах увеличивается число бактерий, что повышает риск инфицирования лёгочной ткани [1] [8] [11] .
На фоне плацентарной недостаточности пуповина становится тонкой. Из-за этого повышается риск сдавления пуповины, возникновения гипоксии или асфиксии в ходе родов. Сниженное поступление кислорода в организм малыша приводит к накоплению продуктов обмена веществ — развивается закисление внутренней среды плода (метаболический ацидоз), на фоне которого возникает кислородная недостаточность в тканях.
Тканевая гипоксия повышает проницаемость сосудистых стенок у плода, что приводит к задержке жидкости в тканях. В случае скопления жидкости в головном мозге может развиться отёк мозга. Такое состояние является неблагоприятным фактором во время родов: оно повышает чувствительность мозга к воздействию кислородной недостаточности и увеличивает риск развития осложнений при возможной родовой травме.
Следствием внутриутробной гипоксии также является нарушение сокращения миокарда у плода. Оно влияет на обмен веществ, что в итоге затрудняет адаптацию новорождённого к новым внеутробным условиям жизни.
Классификация и стадии развития перенашивания беременности
В зависимости от состояния ребёнка выделяют два типа переношенной беременности:
- Запоздалые роды плодом без признаков перезрелости (пролонгированная беременность). Характерны для женщин с дисфункцией яичников младше 30 лет. Ребёнок рождается крупным, но без признаков переношенности. Шейка матки зрелая. По данным УЗИ и КТГ нет признаков изменения плаценты и нарушений плода. Околоплодные воды прозрачные, нормальной окраски. При гистологии плаценты отсутствуют характерные изменения. Нередко такие роды являются результатом неверно определённого срока беременности.
- Запоздалые роды перезрелым плодом (истинное перенашивание). Характерны для первой беременности у женщин старше 30 лет с инфекциями, передающимися половым путём, хроническими воспалительными заболеваниями гениталий и запоздалыми родами в анамнезе. Шейка матки незрелая или недостаточно зрелая. По данным УЗИ выявляют изменения в плаценте и маловодие, по данным КТГ отмечают признаки гипоксии плода. После рождения плод имеет признаки переношенности: большой или малый вес новорождённого, сморщенная желтоватая или зеленоватая кожа с отсутствием сыровидной смазки на ней, плотные кости черепа, длинные ногти. Гистология плаценты выявляет её структурные изменения [1][7][8] .
Чем больше срок истинного перенашивания, тем выше риск осложнений и неблагоприятного исхода данной беременности. Возможны:
- травмы половых органов матери во время родов из-за большого размера плода и плотности костей его черепа;
- травмы ребёнка, гипоксическое поражение его нервной системы и проблемы с дыханием [1][6][10] .
Осложнения перенашивания беременности
Для плода большую опасность представляет асфиксия (острая гипоксия) и отслойка плаценты. Нехватка кислорода внутри утробы стимулирует плод выполнить несвоевременные дыхательных движения. Они приводят к заглатыванию вод и возможному воспалению лёгочной ткани — пневмониту. Если в водах есть примесь мекония (первородного кала), то велика вероятность мекониальной аспирации — проникновения содержимого кишечника новорождённого в его лёгкие.
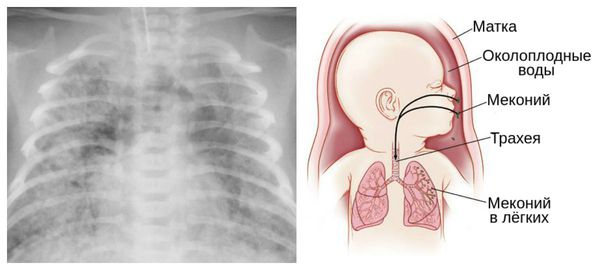
В результате гипоксии и централизации кровообращения во время внутриутробного развития возможны ишемические поражения миокарда, почек и кишечника плода — развивается кислородное голодание клеток этих органов и нарушаются процессы тканевого дыхания. При длительной ишемии возможно стойкое нарушение работы органов, вплоть до их отмирания (некроз кишечника, почечная недостаточность и др.).
Центральная нервная система переношенного плода также становится очень чувствительной к недостатку кислорода и возможным травмам. Поэтому гипоксия может нарушить работу нервной системы и привести к отставанию ребёнка в физическом и нервно-психическом развитии [1] [5] [6] .
Помимо прочего возможны травмы плода во время родов. Они связаны с большим размером головки малыша, узкими родничками и плотностью костей его черепа [1] [4] [10] .
У матери часто наблюдается клиническая картина узкого таза, возникают травмы половых органов (разрывы шейки матки, влагалища или промежности), послеродовые кровотечения (как результат перерастянутой матки), септические и эмболические осложнения.
При клинически узком тазе возникает диспропорция размеров плода и таза матери. Роды через естественные родовые пути в этом случае невозможны. Как правило, проводится оперативное родоразрешение.
Возникновение септических осложнений связано с инфекцией, которая приобретает системный характер. Возможно развитие хориоамнионита (воспаления хориона и инфекции в амниотической жидкости), послеродового эндометрита , сепсиса (заражения крови) и септического шока.
Эмболические осложнения возникают при появлении в кровотоке женщины фрагментов инородных тканей (тромбов, амниотической жидкости и др.). При этом возникают чрезвычайно опасные процессы, такие как ТЭЛА , эмболия околоплодными водами и септическая эмболия с высокой вероятностью смертельного исхода.
Диагностика перенашивания беременности
Диагноз переношенной беременности устанавливают на основании данных анамнеза (истории болезни) и совокупности результатов обследования:
- выявление факторов, которые относят беременную к группе риска (дисфункции яичников, заболевания гениталий, аборты и самопроизвольные выкидыши);
- правильный подсчёт даты родов, УЗИ в первом триместре беременности ;
- ультразвуковая фетометрия (измерение плода) — отсутствие увеличения плода при осмотре в динамике, выявление синдрома задержки роста (симметричное или асимметричное уменьшение окружности головки и живота плода) [1][5] ;
- оценка объёма и структуры околоплодных вод — появление взвеси из-за наличия сыровидной смазки, пушковых волос, эпидермиса и мекония, уменьшение объёма околоплодных вод (чем меньше их объём, тем выше риск истинного перенашивания беременности);
- ультразвуковая оценка зрелости плаценты : снижение её толщины, обратное развитие плаценты с комплексом её структурных изменений (кальцинаты, кисты);
- кардиотокография (КТГ) — при гипоксии плода отмечается изменение подвижности плода (от усиления до полной неподвижности), изменение числа сердечных сокращений, снижение компенсаторных возможностей плода при физической нагрузке;
- допплерометрия в маточных артериях и артериях пуповины — регистрируется нарушение кровотока разной степени выраженности;
- оценка гемодинамики плода — скорость кровотока в средней мозговой артерии, аорте, венозном протоке и нижней полой вене плода снижена (говорит о степени централизации кровотока у плода);
- оценка зрелости шейки матки ;
- амниоскопия — осмотр нижнего полюса плодного пузыря с помощью амниоскопа (отмечается уменьшение прозрачности и изменение цвета околоплодных вод).
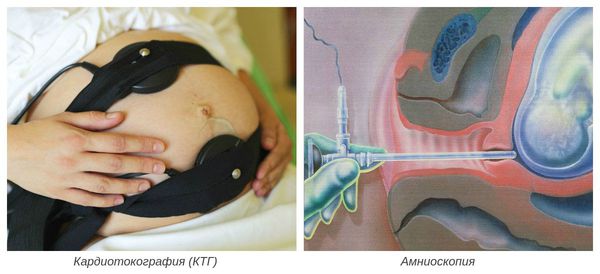
Окончательный диагноз устанавливается после рождения и осмотра ребёнка и плаценты. При патогистологическом исследовании плаценты наблюдается жировая инволюция (замещение биологически активной ткани на нефункционирующую жировую ткань), кальцинаты и жёлто-зелёное окрашивание оболочек.
Дифференциальная диагностика:
- запоздалые роды плодом без признаков перезрелости — характерна задержка наступления родов, отсутствие патологии по результатам УЗИ и КТГ, рождение ребёнка без признаков переношенности, отсутствие характерных изменений в плаценте по результатам гистологии.
- своевременное рождение ребёнка с признаками перезрелости — может быть связано с особенностями созревания плаценты и организма беременной;
- рождение крупного плода пригестационном сахарном диабете — у новорождённого нет признаков переношенности.
Лечение перенашивания беременности
Ведение беременности при перенашивании имеет свои особенности. Пристальное внимание должно уделяться беременным с факторами риска. Своевременная госпитализация в роддом необходима для обследования беременной и решения вопроса о способе ведения родов. Выбор метода зависит от многих факторов: данных анамнеза, готовности к родам, состояния и предполагаемого веса плода, сопутствующих заболеваний женщины.
Проведение оперативного родоразрешения показано при сочетании факта перенашивания с такими осложняющими факторами, как:
- возраст матери (30 лет и старше);
- очень крупный или очень маленький плод;
- отсутствие готовности к родам — незрелая шейка матки, неправильное положение плода;
- гипоксия плода;
- беременность после ЭКО;
- неудачи при предыдущих беременностях и родах в анамнезе.
При более благоприятной ситуации, но неготовности родовых путей, необходимо дополнительно подготовить шейку матки к родам. Для этого применяют различные методы:
- отслоение нижнего полюса плодного пузыря от стенок матки;
- баллонная дилатация шейки матки с помощью катетера Фолея — позволяет механически расширить шейку матки;
- дилататоры природного (ламинарии) и синтетического происхождения — оказывают расслабляющее действие, способствуют выработке эндогенных простагландинов в шейке матки;
- возможно использование простагландина Е либо антипрогестагенов ( Мифепристона ) [1][5][6][11] .
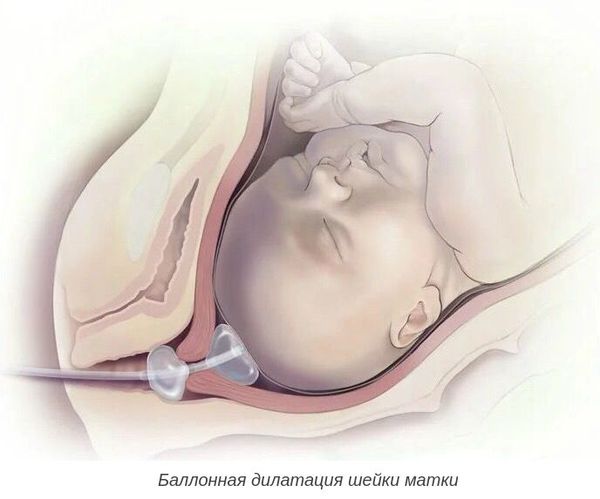
Роды при пролонгированной беременности без признаков перезрелости плода чаще всего протекают без выраженных осложнений, но требуют пристального наблюдения за их ходом.
Запоздалые роды с признакам перезрелости плода часто осложняются. Поэтому для своевременного решения вопроса о выборе способа родоразрешения важна оценка каждого периода беременности. Во время консервативных родов (через естественные родовые пути) необходимо проводить постоянный мониторинг за состоянием плода [1] [9] .
Для родовозбуждения можно использовать амниотомию — искусственный разрыв оболочек плодного пузыря. Она проводится исключительно при зрелой шейке матки и хорошем состоянии плода.
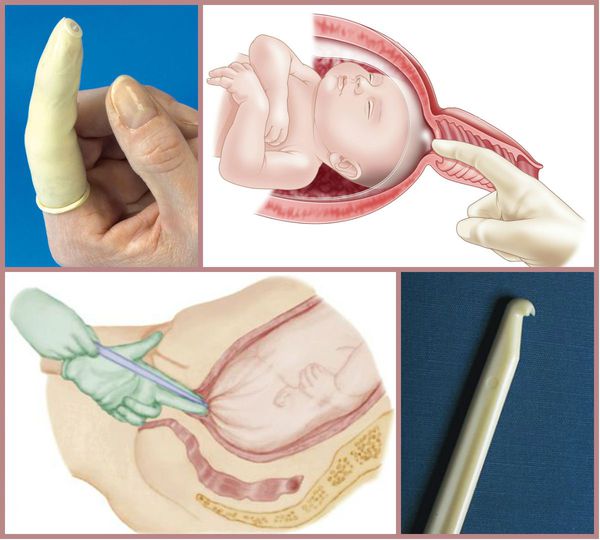
В послеродовом периоде очень важно принимать профилактические меры для предупреждения кровотечения, которое может возникнуть в связи с особенностью строения матки, задержкой частей плаценты, разрывом мягких тканей и нарушением гемостаза (свёртывающей системы крови). Для этого проводится тщательный осмотр родовых путей на выявление разрывов, учёт кровопотери, клинический и лабораторный контроль анализов крови и применение утеротоников, которые стимулируют сокращение матки.
Прогноз. Профилактика
При своевременной и адекватной оценке состояния плода, а также правильном выборе тактики родоразрешения прогноз благоприятный [13] . По наблюдениям врачей, показатели физического, неврологического и психического развития переношенных детей не отличаются от состояния детей, рождённых при неосложнённых своевременных родах. Менее благоприятный прогноз возможен при тяжёлой гипоксии плода, родовой травме и мекониальной аспирации.
Взрывная пандемия вируса Зика охватила Центральную и Южную Америку, Карибские острова, а теперь потенциально угрожает США. На сегодняшний день вирусу присвоен статус пандемии, что отражает степень его распространения и массовый повальный характер, поражающий значительную часть населения. И, хотя вирус Зика не циркулирует на территории России, отправляясь в эндемичные страны, необходимо знать о последствиях этой болезни.
Вирус Зика – это последняя из четырёх распространяемых членистоногими вирусных инфекций, которые неожиданно вспыхнули в западном полушарии за последние 20 лет. Незаметно циркулировавшая лихорадка денге агрессивно проявила себя в 1990-е гг., затем вирус Западного Нила в 1999 году и вирус Чикугунья в 2013 году. Связаны ли эти эпидемии между собой, отражая новые модели возникновения и распространения инфекционных заболеваний? Имеют ли такие пандемии последствия, отличные от последствий других арбовирусных пандемий?
Почему, проживая в России, необходимо знать об особенностях распространения вируса
Заявления специалистов сводятся к тому, что вирус вряд ли получит распространение на территории РФ, так как отсутствует главное звено передачи болезни – комары Aedes, являющиеся основными переносчиками. Такие комары обитают в тропиках и субтропиках, их популяция есть и в Сочи, хотя пока что циркуляции вируса среди них не обнаружено.
Серьезность пандемии Зика ещё и в том, что активное распространение вируса началось только в прошлом году и он недостаточно изучен. Под вопросом до сих пор остаются пути передачи Зика. Ранее считалось, что вирус распространяется непосредственно через укусы, но в январе этого года бразильские ученые подтвердили факт передачи вируса от матери – плоду. Сомнения вызывала и возможность передачи Зика половым путём, тем не менее в феврале 2015 года министр здравоохранения Франции сообщила о зафиксированном случае заражения женщины от своего партнёра, который вернулся из Бразилии. Если передача вируса действительно реализуется половым путём, то его распространение станет повсеместным, в том числе и на территории России.
Количество заболевших постоянно растёт, и случаи заражения регистрируются уже в Европе. Так, в Словении инфицированной беременной женщине был сделан аборт по причине обнаружения у плода микроцефалии.
История обнаружения и распространения вируса
К арбовирусам относятся вирусы, переносчиками которых выступают членистоногие. Вирус Зика также относится к роду арбовирусов, семейству флавивирусов. Флавивирусы, как и другие арбовирусы, вызывают природно-очаговые заболевания, распространяемые кровососущими насекомыми. Комариные флавивирусные инфекции (как в случае с вирусом Зика) распространены преимущественно в южных широтах, в то время как клещевые встречаются повсеместно. Важную роль в поддержании таких вирусов играют теплокровные животные, которых кусают комары-переносчики. У животных болезнь протекает бессимптомно, но сопровождается выраженным инфицированием крови, что способствует трансмиссивному механизму заражения. Человек, как правило, является случайным, тупиковым звеном в экологии флавивирусов. До недавнего времени лишь несколько арбовирусов были причиной клинически важных заболеваний человека: вирус Чикугунья, лихорадка денге и лихорадка Западного Нила. Наиболее исторически значимой оказалась желтая лихорадка, первая геморрагическая лихорадка, ставшая причиной смертельной эпидемии.
Вирус Зика получил своё название благодаря лесу в Уганде, где впервые был выявлен у макак в 1947 г. Год спустя он был идентифицирован у комаров Aedes africanus, обитавших в том же лесу. Именно комары Aedes и являются переносчиком вируса Зика. Позднее, в 1968 г. вирус был впервые обнаружен у людей в Нигерии. И, хотя в последующие годы вирус неоднократно идентифицировали у комаров и людей из Египта, Индии и Индонезии, первая крупная вспышка эпидемии случилась только в 2007 году на острове Яп, в результате которой было инфицировано 75% населения. А с 2015 года началось активное распространение вируса в Центральной и Южной Америке. Американские и канадские учёные смоделировали карту распространения вируса, что позволило предположить: в конце концов вирус Зика расселится по всему американскому континенту, кроме Канады и Чили.
Пути и механизмы передачи вирусной инфекции
Переносчиками вируса являются комары рода Aedes, а позвоночными носителями, как правило, приматы и люди. За 60 лет со дня открытия было описано лишь 15 случаев заболевания человека, и до начала пандемии в 2007 г. вирус редко вызывал клинически тяжёлые случаи заболевания.
Такое быстрое распространение Зика объясняется двумя основными причинами:
- Население Америки не было подвержено этому вирусу, вследствие чего отсутствует коллективный иммунитет.
- Комары Aedes – главный переносчик вируса – распространились по всему континенту, исключая Канаду и Чили.
Вирус Зика может передаваться через кровь от человека к человеку, но такой путь реализуется редко. Что касается передачи вируса от матери плоду, то 3 декабря 2015 года была опубликована статья, в которой говорилось о двух случаях обнаружения вируса Зика в околоплодных водах зародышей. А 20 января текущего года ученые из Бразилии подтвердили теорию о возможности вируса проникать через плаценту: генетический материал вируса был обнаружен в плаценте женщины, перенесшей аборт из-за микроцефалии плода. Тем не менее исследования о возможности реализации вертикального пути передачи (то есть от матери – плоду) всё ещё необходимы.
Доказательств того, что вирус может передаваться младенцам через грудное молоко матери – нет. Поэтому для матерей, находящихся в районах распространения вируса Зика, ограничений по грудному вскармливанию не существует.
До недавнего времени лихорадка Зика считалась лёгким заболеванием: симптомы проявлялись у одного из пяти человек, смертность отсутствовала. Но несмотря на кажущуюся безобидность вируса, его последствия для человечества до сих пор под вопросом.
Симптомы лихорадки Зика
Лихорадка начинается с головной боли, затем следует сыпь, повышение температуры и боль в спине. Сыпь исчезает за два дня, на третий день спадает жар. Но мягкость симптомов обманчива, истинные последствия болезни изучаются по сей день и, возможно, они гораздо серьёзнее, чем сама лихорадка Зика.
Опасные последствия вируса Зика: синдром Гийена-Барре и микроцефалия
На сегодняшний день существует гипотеза о связи вируса Зика с синдромом Гийена-Барре (СГБ). В районах с документально подтвержденными эпидемиями вируса (например, во Французской Полинезии и Бразилии), наблюдалось увеличение случаев синдрома Гийена-Барре. СГБ развивается, когда иммунная система человека атакует собственный организм, влияя на клетки нервной системы. Этот процесс может быть инициирован посредством бактериальных или вирусных инфекций. Основными симптомами являются мышечная слабость и покалывание (парестезии) верхних и нижних конечностей, но опасность болезни в поражении дыхательной мускулатуры. Поэтому даже лёгкая форма синдрома в острой фазе является неотложным состоянием ввиду возможного развития дыхательной недостаточности или нарушения сердечного ритма.
Но существует более настораживающее последствие вируса: матери, инфицированные им, вынашивают детей с микроцефалией. Микроцефалия – это уменьшение размеров черепа и головного мозга при нормальных пропорциях остального тела. Такое заболевание сопровождается умственной недостаточностью: от имбецильности до идиотии. Некоторые из синдромов микроцефалии несовместимы с жизнью. Именно поэтому беременным женщинам следует воздержаться от посещения стран, подверженных эпидемии, а тем, кто проживает там, принять усиленные меры защиты от укусов насекомых.
Кто подвержен риску заражения вирусом Зика
Любой человек, ранее не подвергавшийся инфицированию вирусом и проживающий в районах, где обитают комары Aedes, имеет риск заболеть. Также это касается туристов, выезжающих в эндемичные страны.
На основании чего врач выставляет диагноз
Большинству пациентов диагноз ставят на основании клинических симптомов и эпидемиологического анамнеза (например, вспышки заболеваемости лихорадкой Зика в районе проживания или выезд пациента в такие страны). Подтверждается диагноз вирусологическими тестами: методом ПЦР в первые 5 дней заболевания и серологическими тестами после 5 дня заболевания.
Как отличить между собой вирусы Зика, Чикугуньи и денге
Все эти заболевания в настоящее время имеют аналогичные симптомы, но есть признаки, указывающие на определенный вирус. Так, лихорадка денге обычно протекает с более высокой температурой и выраженной мышечной болью, а в качестве осложнений могут возникать кровотечения (геморрагический синдром). Чикугунья также протекает на фоне высокой температуры, но сопровождается интенсивной болезненностью суставов верхних и нижних конечностей (вплоть до того, что пациент не может открыть бутылку воды). При инфицировании вирусом Зика в качестве характерных симптомов могут выступать кожные высыпания и конъюнктивит.
Профилактические меры и лечение вируса Зика
Вакцины против вируса на сегодняшний день не существует, поэтому Всемирная Организация Здравоохранения не рекомендует посещать регионы, в которых распространен вирус. Индивидуальные меры профилактики укусов включают в себя использование репеллентов и одежды, защищающей открытые участки тела. В странах, где обитают комары Aedes, необходимы москитные сетки на окнах и дверях, чтобы не допускать проникновения насекомых в жилище. Следует избегать скопления стоячей воды в вазах, горшках и других ёмкостях, так как это создаёт условия для размножения комаров.
Специфического лечения лихорадки Зика не предусмотрено, поэтому терапия направлена на устранение симптомов. Как правило, используются нестероидные противовоспалительные средства.
Потенциал вируса Зика
Несмотря на обманчивую мягкость течения лихорадки, её отдалённые последствия могут быть куда опаснее, чем мы себе представляем. Активизация вируса и его распространение создают необходимость детального изучения этой инфекции и создания вакцины для предупреждения заболеваемости.
Перед началом применения любого препарата посоветуйтесь со специалистом и ознакомьтесь с инструкцией по применению.
Читайте также:

