Ботулизм у взрослых клинические рекомендации по
Обновлено: 26.04.2024
Ботулизм является острой пищевой токсикоинфекцией, развивающейся в результате попадания в организм человека ботулотоксина. Заражение происходит алиментарным путем, наиболее часто при употреблении в пищу содержащих споры ботулизма консервов. Ботулизм характеризуется поражением нервной системы в результате блокирования ботулотоксином ацетилхолиновых рецепторов нервных волокон, проявляется в виде мышечных параличей и парезов. Основная опасность ботулизма состоит в развитии таких осложнений, как острая дыхательная недостаточность и нарушения сердечного ритма. Диагностика ботулизма строится в основном на данных анамнеза заболевания и результатах неврологического осмотра.
МКБ-10
Общие сведения
Ботулизм является острой пищевой токсикоинфекцией, развивающейся в результате попадания в организм человека ботулотоксина. Ботулизм характеризуется поражением нервной системы в результате блокирования ботулотоксином ацетилхолиновых рецепторов нервных волокон, проявляется в виде мышечных параличей и парезов.
Характеристика возбудителя
Ботулотоксин вырабатывает бактерия Clostridium botulinum – грамположительная спорообразующая палочка, облигатный анаэроб. Неблагоприятные условия внешней среды переживает в виде спор. Споры клостридий могут сохраняться в высушенном состоянии многие годы и десятилетия, развиваясь в вегетативные формы при попадании в оптимальные для жизнедеятельности условия: температура 35 С, отсутствие доступа кислорода. Кипячение убивает вегетативные формы возбудителя через пять минут, температуру в 80 С бактерии выдерживают в течение получаса. Споры могут сохранять жизнеспособность в кипящей воде более получаса и инактивируются только в автоклаве. Ботулотоксин легко разрушается во время кипячения, но способен хорошо сохраняться в рассолах, консервах и пищевых продуктах, богатых различными специями. При этом наличие ботулотоксина не изменяет вкуса продуктов. Ботулотоксин относится к наиболее сильным ядовитым биологическим веществам.
Резервуаром и источником клостридий ботулизма является почва, а также дикие и некоторые домашние (свиньи, лошади) животные, птицы (преимущественно водоплавающие), грызуны. Животным-носителям клостридии обычно не вредят, выделение возбудителя происходит с калом, бактерии попадают в почву и воду, корм животных. Обсеменение объектов окружающей среды клостридиями также возможно при разложении трупов больных ботулизмом животных и птиц.
Заболевание передается по фекально-оральному механизму пищевым путем. Чаще всего причиной ботулизма становится употребление консервированных в домашних условиях загрязненных спорами возбудителя продуктов: овощей, грибов, мясных изделий и соленой рыбы. Обязательным условием для размножения клостридий в продуктах и накопления ботулотоксина является отсутствие доступа воздуха (плотно закрытые консервы). В некоторых случаях вероятно заражение спорами ран и гнойников, что способствует развитию раневого ботулизма. Ботулотоксин может всасываться в кровь, как из пищеварительной системы, так и со слизистых оболочек дыхательный путей, глаз.
У людей отмечается высокая восприимчивость к ботулизму, даже небольшие дозы токсина способствуют развертыванию клинической картины, однако чаще всего концентрация его недостаточна для формирования антитоксической иммунной реакции. При отравлении ботулотоксином из консервированных продуктов нередки случаи семейного поражения. В настоящее время случаи заболевания становятся более частыми ввиду распространения домашнего консервирования. Чаще всего ботулизмом заболевают лица из возрастной группы 20-25 лет.
Симптомы ботулизма
Инкубационный период ботулизма редко превышает сутки, чаще всего, составляя несколько часов (4-6). Однако иногда может затягиваться до недели и 10 дней. Поэтому наблюдение за всеми людьми, употреблявшими одну пищу с больным, продолжается до 10 суток. В начальном периоде заболевания может отмечаться неспецифическая продромальная симптоматика. В зависимости от преимущественного синдрома различают гастроэнтерологический, глазной варианты, а также - клиническую форму в виде острой дыхательной недостаточности.
Клиническая картина ботулизма в разгар заболевания достаточно специфична и характеризуется развитием парезов и параличей различных групп мышц. У больных отмечается симметричная офтальмоплегия (зрачок стабильно расширен, имеет место косоглазие, обычно сходящееся, вертикальный нистагм, опущение века). Дисфагия (расстройство глотания) связана с прогрессирующим парезом мышц глотки. Если первоначально больные испытывают дискомфорт и затруднения глотания твердой пищи, то с развитием заболевания становится невозможным и проглатывание жидкости.
Ботулотоксин способствует параличам и парезам мимической мускулатуры, вызывая асимметрию лица, дисмимию. В целом отмечается общая слабость, неустойчивость походки. Ввиду пареза кишечной мускулатуры развиваются запоры. Лихорадка для ботулизма не характерна, в редких случаях возможен субфебрилитет. Состояние сердечной деятельности характеризуется учащением пульса, некоторым повышением периферического артериального давления. Расстройства чувствительности, потеря сознания не характерны.
Осложнения ботулизма
Самое опасное осложнение ботулизма – развитие острой дыхательной недостаточности, остановка дыхания вследствие паралича дыхательной мускулатуры или асфиксия дыхательных путей. Такие осложнения могут привести к летальному исходу. Ввиду развития застойных явлений в легких, ботулизм может спровоцировать вторичную пневмонию. В настоящее время есть данные о вероятности осложнения инфекции миокардитом.
Диагностика ботулизма
В связи с развитием неврологической симптоматики больной бутулизмом нуждается в осмотре невролога. Специфическая лабораторная диагностика ботулизма на ранних сроках развития инфекции не разработана. Основанием для постановки диагноза служит клиническая картина и данные эпидемиологического анамнеза. Токсин выделяют и идентифицируют с помощью биологической пробы на лабораторных животных. В разгар заболевания возможно определить присутствие токсина в крови с помощью HGUF с антительным диагностикумом.
Антигены возбудителей выявляются с помощью иммунофлуоресцентного анализа (ИФА), а также - РИА и ПЦР. Выделение возбудителя путем посева каловых масс не несет значимой диагностической информации, поскольку может иметь место развитие из спор вегетативной формы клостридий в кишечнике здорового человека.
Лечение ботулизма
При подозрении на ботулизм производится обязательная госпитализация в отделение с возможностью подключения аппарата ИВЛ, с целью предупреждения и своевременной помощи в случае развития опасных для жизни осложнений. Первейшим лечебным мероприятием, производимым в первые сутки заболевания, является промывание желудка при помощи толстого зонда.
Ботулотоксин, циркулирующий в крови пациентов, нейтрализуют с помощью разового введения поливалентных противоботулинических сывороток по методу Безредки (после осуществления десенсибилизации организма). В случае, если однократное введение сыворотки не было достаточно эффективным и спустя 12-24 часа у пациента отмечается прогрессирование нейрологической симптоматики, введение сыворотки повторяют.
Довольно эффективно введение противоботулинической человеческой плазмы, однако этот препарат довольно редок ввиду малого срока хранения (не более 4-6 месяцев). В настоящее время в лечении ботулизма находит применение противоботулинический иммуноглобулин. В комплекс мероприятий этиотропной терапии включаются антибиотики, назначаемые с целью подавления вероятного развития вегетативных форм возбудителя, а также тиаминпирофосфат и АТФ. Положительный эффект оказывает гипербарическая оксигенация.
В остальном лечение назначают исходя из тяжести течения и симптоматики. В случае формирования острой дыхательной недостаточности больных переводят на искусственную вентиляцию легких. Кормление больных в случае формирования стойкой дисфагии производят жидкой пищей через тонкий зонд, либо переводят на парентеральное питание. В период выздоровления хороший эффект в плане скорейшего восстановления функций мышечной системы имеет физиотерапия.
Прогноз при ботулизме
Прогноз при высокой дозе полученного токсина и отсутствии своевременной медицинской помощи может быть крайне неблагоприятным, летальность таких случаев достигает 30-60%. Применение этиотропного лечения и методов интенсивной терапии при развитии грозных осложнений значительно снижают риск летального исхода (до 3-4%). В случае своевременного лечения заболевание заканчивается выздоровлением с полным восстановлением функций через несколько месяцев.
Профилактика ботулизма
Профилактические меры против ботулизма подразумевают строгое следование санитарно-гигиеническим нормам при изготовлении консервов, стерилизации посуды для заготовления продуктов длительного хранения. Рыбные и мясные продукты должны консервироваться исключительно в свежем и тщательно очищенном от частиц почвы виде. Консервация перезрелых плодов недопустима. Консервирование в домашних условиях должно осуществляться в строгом соответствии с рецептурой при достаточной концентрации соли и кислоты в открытой для доступа кислорода посуде.
Ботулизм – острая инфекционная болезнь из группы сапрозоонозов преимущественно с фекально-оральным механизмом передачи, развивающаяся в результате употребления пищевых продуктов, в которых произошло накопление токсина возбудителя, блокирующего передачу нервных импульсов [1].
Название протокола: Ботулизм
Код протокола:
Код МКБ-10:
A 05.1- Ботулизм
Сокращения, используемые в протоколе:
ОАК - общий анализ крови
ОАМ - общий анализ мочи
ОЦК - объем циркулирующей крови
ОНМК - острое нарушение мозгового кровообращения
Дата разработки протокола: 2015 год.
Категория пациентов: взрослые.
Пользователи протокола: терапевты, врачи общей практики, врачи/фельдшеры скорой медицинской помощи, инфекционисты, анестезиологи-реаниматологи, невропатологи, организаторы здравоохранения.
Примечание: в данном протоколе используются следующие классы рекомендаций и уровни доказательств:
Классы рекомендаций:
Класс I - польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс II - противоречивые данные и/или расхождение мнений по поводу пользы/эффективности лечения
Класс II а - имеющиеся данные свидетельствуют о пользе/эффективности лечебного воздействия
Класс II b – польза / эффективность менее убедительны
Класс III - имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Классификация
Клиническая классификация [1,2,3,4]
По механизму:
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне: не проводятся.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне: не проводятся.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: не проводится.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне [1,2]:
• кровь на реакцию нейтрализации (РН) ботулотоксинов антитоксическими сыворотками путём биопробы на белых мышах (обнаружение ботулинического токсина в крови служит абсолютным подтверждением диагноза);
• бактериологические исследования промывных вод желудка, рвотных масс, испражнений больного, остатков подозрительного продукта;
• в случае раневого ботулизма – отделяемое из раны, кусочки отторгающейся омертвевшей ткани, тампоны из раны;
• в случае ботулизма грудных детей – определение ботулотоксинов в крови и/или возбудителя в испражнениях.
• затруднение при глотании твердой, сухой пищи, по мере прогрессирования болезни – нарушение глотания мягкой, жидкой пищи; при тяжелых формах – полная невозможность глотания;
• в тяжелых случаях – парез дыхательной мускулатуры с резким ограничением подвижности межреберных мышц и исчезновением кашлевого рефлекса; расстройства и остановка дыхания – основная причина смерти.
• острое начало заболевания с картины гастроэнтерита с последующим, в течение нескольких часов, присоединением неврологической симптоматики, либо второй вариант начала заболевания, при котором диспепсический синдром отсутствует и на первый план с самого начала выступает поражение ЦНС.
• употребление в пищу в период от нескольких часов до 7 суток до начала заболевания консервов (овощных, мясных, рыбных, грибных), копченой или вяленой рыбы, колбасы или окорока домашнего приготовления;
• температура тела нормальная или субфебрильная;
Специфическая лабораторная диагностика [1,2,5,6,7]:
• обнаружение ботулинического токсина в крови методом РН ботулотоксинов антитоксическими сыворотками с биопробой на белых мышах служит абсолютным подтверждением диагноза;
• выделение возбудителя ботулизма из содержимого желудка (рвотные массы и промывные воды), испражнений, подозрительных продуктов путем бакпосева на специальные питательные среды (Китта–Тароцци, казеиново-грибную, бульон Хоттингера и др.).
Инструментальные исследования:
УЗИ органов брюшной полости: возможна гепатомегалия;
ЭКГ: при тяжёлом течении болезни и выраженном поражении миокарда – нарушения проводимости, вплоть до полной АВ-блокады, электрическая нестабильность миокарда, вплоть до фибрилляции желудочков, нарушение сократительной способности миокарда с развитием сердечной недостаточности по большому кругу кровообращения [1,4,5,6];
Рентгенография органов грудной клетки: наличие призаков пневмонии при осложнении.
• консультация невропатолога – при присоединении явлений парезов черепных нервов, периферических полинейропатий;
• консультация анестезиолога-реаниматолога – при дыхательных нарушениях, полиорганной недостаточности;
Дифференциальный диагноз
Алгоритм дифференциальной диагностики при ботулизме

Лечение
Тактика лечения
Немедикаментозное лечение6:
Режим постельный или полупостельный.
Диета: стол №10, зондовое или парентеральное питание в зависимости от состояния больного.
• введение назогастрального зонда для эвакуации застойного содержимого и фракционного промывания желудка 5% раствором натрия гидрокарбоната с целью инактивации токсина 1-2 раза в сутки в течение 3-4 дней до полной ликвидации застоя;
• энтеральное питание через назогастральный зонд, инфузией в течение 16 ч. питательными смесями с высокой энергетической плотностью. Объём белка в сутки из расчёта 25 ккал/кг массы тела и 1,5 г/кг массы тела;
• при застойном отделяемом из желудка - парентеральное питание концентрированными растворами глюкозы (10–40%), смесями аминокислот и жировыми эмульсиями, с обязательным частичным энтеральным питанием из расчёта 2000–2500 ккал в сутки на взрослого больного.
Медикаментозное лечение [1-6,10]
Медикаментозное лечение, оказываемое на амбулаторном уровне: не проводится.
• инфузионно-дезинтоксикационная терапия кристаллоидами, декстранами, растворами глюкозы.
• при неизвестном типе токсина вводят смесь моновалентных сывороток или поливалентную сыворотку (10 тыс. МЕ анатоксина типов А и Е и 5 тыс. МЕ типа В).
• независимо от тяжести течения внутривенно вводят одну лечебную дозу сыворотки, разведённую в 200 мл подогретого изотонического раствора натрия хлорида; скорость введения – 60-90 капель в 1 мин.; сыворотку вводят однократно;
• в исключительных случаях, при невозможности осуществления капельной инфузии, допускается медленное струйное введение лечебной дозы сыворотки шприцем без разведения [5];
• наличие аллергической реакции при постановке пробы служит относительным противопоказанием к введению лечебной дозы сыворотки; в этих случаях предварительную дозу преднизолона увеличивают до 240 мг.
Подавление жизнедеятельности возбудителей ботулизма в ЖКТ и предупреждение возможного образования токсина – хлорамфеникол по 0,5 г х 4 раза в сутки в течение 5 дней, при нарушениях глотания – внутримышечно по 1 г х 3 раза в сутки в течение 5 дней. Вместо хлорамфеникола можно применять ампициллин по 0,5–1 г х 4 раза в сутки внутрь.
Перечень основных лекарственных средств:
• хлорамфеникол – таблетки 250 мг, 500 мг; порошок для приготовления раствора для инъекций 500 мг, 1000 мг;
• гидроксиэтилкрахмал 6% и 10% растворы для инфузий во флаконах по 250 и 500 мл.
• при высоком риске аспирации длительная интубация с постоянно раздутой манжеткой (25 см вод.ст. — максимальное давление, не приводящее к повреждению трахеи);
• препараты, уменьшающие кислотность желудочного сока (ранитидин, фамотидин), блокаторы протонного насоса (омепразол, эзомепразол, пантопразол);
• препараты, улучшающие моторную функцию ЖКТ (домперидон, метоклопрамид).
• утомляемость больного при дыхании, минимальное ощущение нехватки воздуха, повышение рСО2 ≥53 мм рт.ст. служат показанием к переводу пациента на вспомогательную вентиляцию (даже если нет одышки, участия вспомогательной мускулатуры, цианоза и других симптомов ОДН). Примеры: СРАР (постоянное положительное давление в дыхательных путях), уменьшает работу дыхания; MMV (гарантированный минутный объём). Больному устанавливают стабильный минутный объём — допустимо 6 л/мин. Если объём спонтанной вентиляции 4 л/мин, остальные 2 л/мин больной получит с помощью респиратора. PS (поддержка давлением): на каждую попытку вдоха больного респиратор доводит дыхательный объём до установленного давления (допустимо 20 см вод.ст.).
• тщательная санация трахеобронхиального дерева (не реже, чем каждые 30 мин. – 1ч.) и использование полноценно стерилизуемой дыхательной аппаратуры для профилактики и предотвращения пневмонии;
• согревание и увлажнение дыхательной смеси, стимуляция движения мокроты (перкуссия грудной клетки, вибрационный, вакуумный массаж), удаление мокроты (постуральный дренаж, её аспирация), оксигенация.
• тесный психологический контакт персонала с больным для выработки его активной позиции в отношении лечебных мероприятий;
• нормализация кислотно-щелочного равновесия, уровня гемоглобина, объёма циркулирующей крови, сердечного выброса, температуры тела, электролитного состава плазмы.
Миокардиальные цитопротекторы – при поражении миокарда: триметазидин, мельдоний.
Антибактериальная терапия - при развитии бактериальных осложнений: полусинтетические пенициллины, цефалоспорины III-IV поколения (с учетом чувствительности возбудителя): Рекомендуется монотерапия одно нижеследующих препаратов:
Показано введение иммуноглобулинов (иммуноглобулин человека нормальный: октагам, пентаглобин) во все сроки болезни.
Перечень дополнительных лекарственных средств
Рекомендуется монотерапия одно нижеследующих препаратов:
• фамотидин таблетки 10 мг, 20 мг, 40 мг; лиофилизированный порошок для инъекционных растворов в ампулах по 0,02 г в комплекте с растворителем;
• эзомепразол - таблетки, покрытые оболочкой, 20, 40 мг; лиофилизат для приготовления раствора для внутривенного введения 40 мг;
• пантопразол - таблетки, покрытые кишечнорастворимой оболочкой, 20, 40 мг; порошок, лиофилизат для приготовления раствора для инъекций 40 мг;
• домперидон - таблетки 10 мг; таблетки для рассасывания 10 мг; сироп; капли для приема внутрь; суспензия 1мг/мл;
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи: не проводится.
Другие виды лечения, оказываемые на амбулаторном уровне:
• промывание желудка кипяченой водой с целью нейтрализации токсина.
В случаях раневого ботулизма – соответствующая хирургическая обработка раны, применяют повышенные дозы (до 12–16 млн. ЕД/сут) пенициллина.
• промывание желудка вначале кипяченой водой для получения материала для лабораторного исследования, а затем 2–5%-ным раствором натрия гидрокарбоната с целью нейтрализации токсина.
Хирургическое вмешательство
Хирургическое вмешательство, оказываемое в амбулаторных условиях: не проводится.
Хирургическое вмешательство, оказываемое в стационарных условиях: не проводится.
Профилактические (противоэпидемические) мероприятия:
При установлении факта употребления инфицированных продуктов питания проводится специфическая профилактика – введение внутримышечно ПБС в дозах 1000-2000 МЕ каждого типа сыворотки (А, В, Е) однократно.
Дальнейшее ведение:
Правила выписки: Выписку больных проводят после клинического выздоровления при удовлетворительном состоянии больного, отсутствии осложнений. Примерные сроки нетрудоспособности после выписки определяются индивидуально.
Диспансерное наблюдение не регламентировано. Целесообразно наблюдение не менее 6 мес. с участием невропатолога, офтальмолога и кардиолога.
• обильное питьё (настой шиповника, щёлочные минеральные воды, отвары трав с мочегонными свойствами);
• соблюдение физического режима с исключением тяжёлой физической работы, переохлаждения, посещения бани, сауны, занятий спортом (в течение 6-12 месяцев);
• приём общеукрепляющих лекарственных средств, адаптогенов, поливитаминов.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
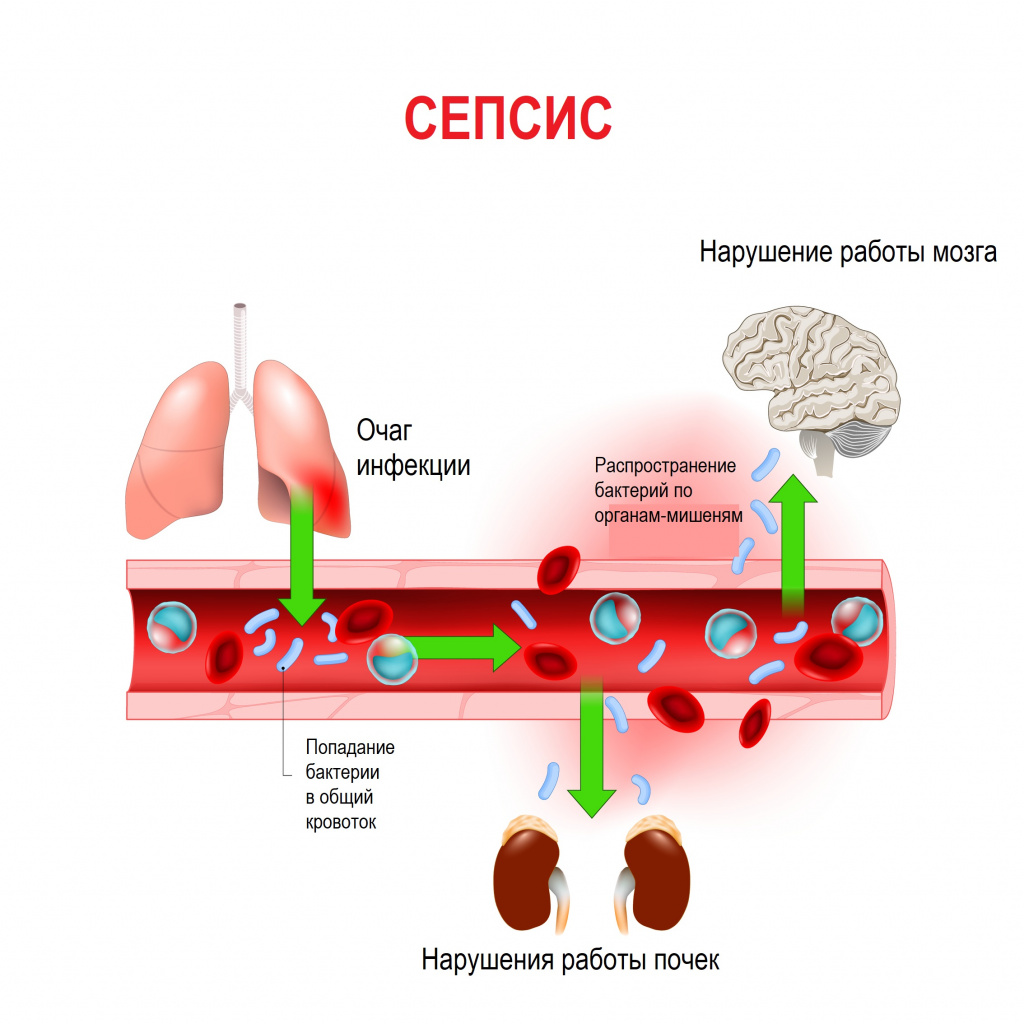
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
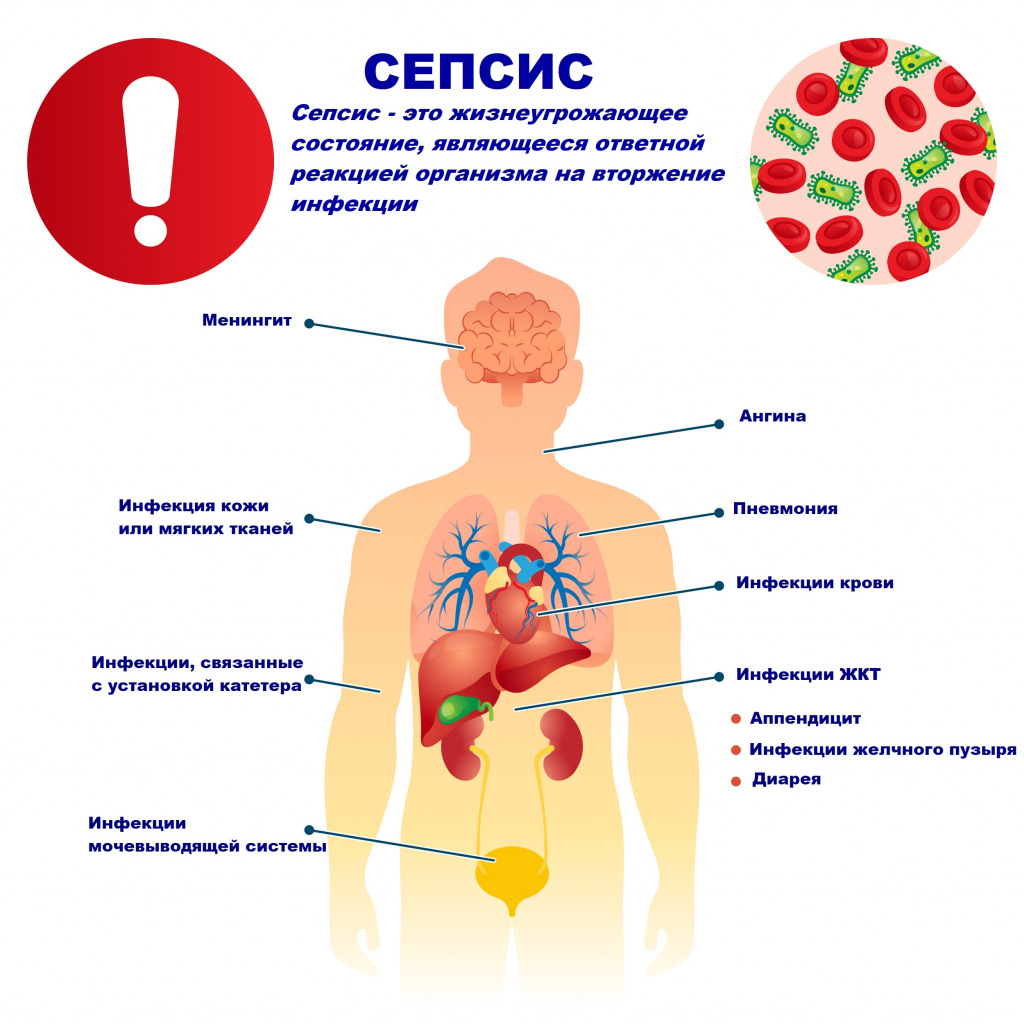
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Мышечная слабость - причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Задумывались ли вы когда-нибудь, сколько мышц в нашем теле? Каким образом происходит их сокращение? Какие функции, помимо перемещения тела в пространстве, выполняют мышцы? Что произойдет, если мышечные волокна утратят способность к сокращению, и разовьется мышечная слабость? На эти и другие вопросы мы постараемся ответить в этой статье.
Выделяют два вида мышечной ткани: поперечно-полосатую, из которой состоят сердечная мышца и скелетная мускулатура, позволяющая нам двигаться, и гладкую, выстилающую поверхность внутренних органов и сосудов.
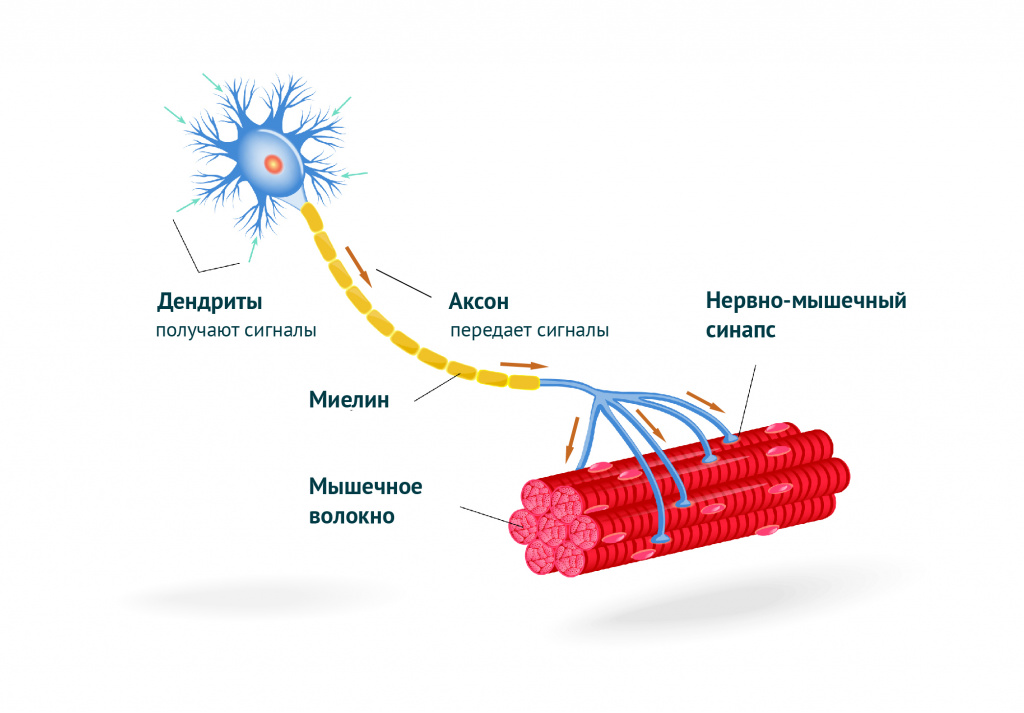
В теле человека насчитывается более шестисот скелетных мышц. Мышца – это орган, в котором осуществляется интенсивное кровоснабжение, что обеспечивает высокий уровень обмена веществ. Сокращение мышечных волокон происходит под действием нервных импульсов, исходящих из соответствующих центров нервной системы. Нервный импульс проходит через нервно-мышечный синапс (место соединения нервного окончания с мышцей) и вызывает сокращение мышцы.
Мышечная ткань выполняет не только двигательную функцию, но и функцию защиты, теплообмена, активно участвует в работе всех внутренних органов.
Сердечная мышца обеспечивает постоянную циркуляцию крови по организму, благодаря чему осуществляется транспорт веществ.
Мышечная слабость (миопатия, миастения) – состояние, для которого характерна быстрая утомляемость мышц. Мышечное утомление не всегда зависит от физической нагрузки и может быть симптомом многих хронических заболеваний.
Сила мышечного сокращения определяется интенсивностью нервного импульса, поступающего в мышцу, и строением мышечного волокна. Поэтому все заболевания, основным симптомом которых является мышечная слабость, делятся на две большие группы: миопатии и миастении.
К миопатиям относятся болезни, в основе которых лежит первичное поражение мышечных волокон. Миастении – заболевания, развивающиеся в результате расстройства нервно-мышечной передачи импульса.
Отдельно выделяют парезы и параличи, возникающие при первичном поражении нервной системы, когда к нервно-мышечному синапсу приходит импульс недостаточной силы, или импульс не доходит вообще.
Заболевания, вызывающие мышечную слабость, могут быть наследственными и приобретенными. Мышечная слабость бывает тотальная, поражающая большую часть мускулатуры тела, или избирательная с поражением отдельных групп мышц; симметричная (слабость одноименных мышц с двух сторон: справа и слева) или асимметричная.
Среди механизмов, приводящих к недостаточной силе сокращения и быстрой утомляемости мышц, можно выделить следующие.
Во-первых, это первичные поражения нервной системы, такие как повреждение головного или спинного мозга, а также нервных волокон в результате травм, нарушения кровоснабжения, воспалительных процессов и др.
Здесь же стоит сказать о ботулизме – токсикоинфекционном заболевании, при котором ботулотоксин, вырабатываемый бактериями Clostridium botulinum, блокирует проведение нервного импульса.
Во-вторых, изменения в нервно-мышечном соединении (синапсе). Например, выработка аутоантител к структурам синапса приводит к нарушению передачи нервного импульса с нервного волокна на мышечное.
Наконец, существует множество причин поражения непосредственно мышечного волокна при относительной сохранности нервных структур. Например, обширная группа наследственных заболеваний, в основе которых лежат мутации генов, определяющих структуру белков мышечных волокон, а также аутоиммунные заболевания, при которых неправильное функционирование иммунной системы приводит к выработке антител или размножению иммунных клеток, поражающих собственные ткани организма.
К заболеваниям, основным или второстепенным проявлением которых является мышечная слабость, относятся:
- наследственные мышечные дистрофии: дистрофия Дюшенна-Беккера, наследственная дилатационная кардиомиопатия и др.;
- наследственные миотонии, проявляющиеся нарушением расслабления мышц: миотония Томсена, миотония Беккера, периодические параличи;
- наследственные особенности нарушения биохимических процессов, протекающих в мышцах: болезни накопления липидов (нарушения липидного обмена), митохондриальные болезни (связанные с дефектами в функционировании митохондрий);
- воспалительные изменения, вызванные инфекциями и аутоиммунными заболеваниями (дерматомиозит, коллагенозы, саркоидоз);
- эндокринные заболевания, среди которых болезни щитовидной железы (гипо- и гипертиреоз), паращитовидных желез (гипо- и гиперпаратиреоз), гипофиза (болезнь Кушинга, акромегалия), надпочечников (синдром Кушинга, болезнь Аддисона, синдром Конна);
- побочное действие лекарственных средств, алкоголя, наркотиков;
- несбалансированная диета и дефицит витаминов и минералов, длительная рвота или диарея при кишечных инфекциях, приводящая к недостатку калия в организме;
- влияние факторов окружающей среды (хроническое воздействие на организм человека паров бензина, толуола);
- ботулизм;
- травматическое повреждение мышц, нервных стволов, головного и спинного мозга;
- нарушения кровоснабжения мышц при атеросклерозе, сердечно-сосудистой недостаточности;
- злокачественные опухоли и др.
- терапевт ;
- невролог ;
- эндокринолог ;
- ревматолог;
- инфекционист;
- генетик.
Первоначально стоит обратиться к врачу широкого профиля – терапевту, который сможет предположить поражение той или иной системы органов и направит вас к врачу-специалисту.
Диагностика синдрома мышечной слабости начинается с подробного опроса пациента, в ходе которого выясняют, в каких мышцах ощущается слабость, время ее появления, остроту, возможные провоцирующие факторы, сопутствующие признаки заболевания (боль, мышечные спазмы, нарушение дыхания, глотания, нарушения чувствительности и др.), наличие подобных симптомов у родственников пациента и т. д. Далее врач проводит тщательный осмотр и анализ двигательной активности при помощи различных диагностических упражнений и проверки рефлексов.
В связи с широчайшим спектром заболеваний, приводящих к развитию мышечной слабости, диагностика требует многих лабораторных и инструментальных обследований. Это:
- определение уровня мышечных ферментов, к которым относятся креатинфосфокиназа (КФК),
Синонимы: Анализ крови на креатинкиназу. CK; Creatine Phosphokinase (CPK). Краткая характеристика определяемого вещества Креатинкиназа Креатинкиназа катализирует обратимый перенос фосфорильного остатка с АТФ на креатин и с креатинфосфата на АДФ. Содержится преимущественно в скелетной мускулатуре.
Синонимы: Глутамино-щавелевоуксусная трансаминаза; Глутамат-оксалоацетат-трансаминаза сыворотки крови (СГОТ); L-аспартат 2-оксоглутарат аминотрансфераза; ГЩТ. Aspartateaminotransferase; Serum Glutamicoxaloacetic Transaminase; SGOT; GOT. Краткая характеристика определяемого вещества АсАТ .
Аланинаминотрансфераза − внутриклеточный фермент, участвующий в метаболизме аминокислот. Тест используют в диагностике поражений печени, сердечной и скелетных мышц. Синонимы: Глутамат-пируват-трансаминаза; Глутамат-пируват-трансаминаза в сыворотке; СГПТ. Alanine aminotransferase; S.
Синонимы: Анализ крови на ЛДГ; Лактатдегидрогеназа; L-лактат; НАД+Оксидоредуктаза; Дегидрогеназа молочной кислоты. Lactate dehydrogenase, Total; Lactic dehydrogenase; LDH; LD. Краткая характеристика определяемого вещества Лактатдегидрогеназа ЛДГ – цитоплазматический.
- определение концентрации электролитов в крови (кальция, калия), дисбаланс которых приводит к периодической или стойкой мышечной слабости;
Синонимы: Анализ крови на электролиты; Электролиты в сыворотке крови. Electrolyte Panel; Serum electrolyte test; Sodium, Potassium, Chloride; Na/K/Cl. Краткая характеристика определяемых веществ (Калий, Натрий, Хлор) Калий (К+) Основной внутриклеточный катион. Кал.
- иммунологическое исследование крови, цель которого – выявление антител (иммунных белков) как причины повреждения нервно-мышечных структур – антитела к ацетилхолиновому рецептору; антитела к скелетным мышцам IgG;
Серологический тест для диагностики миастении. Миастения представляет собой классическое аутоиммунное заболевание, обусловленное иммунной блокадой нервно-мышечного проведения, которое проявляется быстрой утомляемостью и мышечной слабостью. Заболевание имеет два возрастных пика, .
Серологический тест для диагностики паранеопластической миастении. Миастения является аутоиммунным неврологическим заболеванием, обусловленным иммунной блокадой нервно-мышечного проведения, которое проявляется быстрой утомляемостью и мышечной слабостью. У 20-40% пациентов с миастени.
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Безопасное и информативное сканирование структур головного мозга для диагностики его патологий.
- анализ ДНК на наличие специфических мутаций, который проводится после обязательной консультации генетика.
В основе лечения мышечной слабости лежит терапия основного заболевания, вызвавшего появление данного симптома.
Терапия заключается в устранении причинного фактора, а при невозможности (в случае наследственных заболеваний) – в коррекции и компенсации нарушения работы мышц и внутренних органов.
В случае аутоиммунных заболеваний, являющихся причиной хронической мышечной слабости, пациенту назначают гормональные и цитостатические препараты, подавляющие выработку антител и клеточную агрессию к тканям собственного организма. При инфекционно-воспалительных процессах в мышцах проводят антибактериальную, противовирусную, противогрибковую или противопротозойную терапию в зависимости от возбудителя.
При миастении, вызванной действием аутоантител на нервно-мышечный синапс, применяют препараты, способствующие улучшению проведения нервного импульса к мышце, возможно удаление тимуса (вилочковой железы) – тимэктомия, при необходимости назначают терапию кортикостероидами и иммуносупрессорами.
Если причиной развития мышечной слабости являются нарушения функционирования эндокринных желез, то пациенту назначают препараты, возмещающие недостаток того или иного гормона или, наоборот, подавляющие избыточную активность эндокринной железы.
При врожденных миопатиях и миотониях, радикальное лечение которых пока невозможно, значительная роль отводится физиотерапии, лечебной гимнастике, ортопедическим приспособлениям. Из медикаментозных средств пациенту назначают препараты, увеличивающие силу мышц и нормализующие обмен веществ в мышечной ткани. При сопутствующих поражениях внутренних органов (в первую очередь сердечной мышцы) проводят коррекцию нарушений при помощи лекарственных средств, установки кардиостимулятора и т. д. Если это необходимо, то медикаментозно и при помощи диеты корректируют дисбаланс электролитов и других веществ.
В случае появления периодически возникающей или стойкой хронической мышечной слабости не стоит откладывать визит к врачу. Не стоит экспериментировать с самолечением, поскольку это может нанести непоправимый вред здоровью. Проанализируйте, какие изменения со стороны других органов предшествовали мышечной слабости, какие изменения в вашем образе жизни и диете произошли в последнее время.
При резко нарастающей мышечной слабости, зачастую начинающейся с мышц лица, нарушения зрения, глотания, затруднения дыхания в сочетании с признаками отравления (тошнота, рвота, боли в животе) после употребления консервированных в домашних условиях продуктов (особенно грибов) не исключено заражение ботулизмом.

Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Читайте также:

