Для общей терапии микозов используются
Обновлено: 25.04.2024
О нихомикозы – грибковые инфекции ногтей – представляют давнюю проблему с неубывающей актуальностью. Заболеваемость населения России составляет не менее 5–15% и определяется различными факторами, включая экологические и социальные, а также индивидуальные особенности организма, такие как пол и возраст, состояние сосудистой, иммунной и эндокринной систем, а также наличие других патологических состояний.
Заболеваемость онихомикозами увеличивается с возрастом: грибковые инфекции ногтей казуистически редко встречаются у детей и широко распространены у лиц зрелого возраста, достигая почти 50% у больных в возрасте от 70 лет и выше. Мужчины страдают онихомикозом в 1,3 раза чаще, чем женщины. Немалую роль в развитии онихомикоза играют сосудистые заболевания (особенно сосудов нижних конечностей), ожирение, плоскостопие и другие деформации стоп. Особенно часто грибковые поражения ногтей возникают у больных сахарным диабетом, при котором создаются особенно благоприятные условия, связанные с повышенным содержанием в крови глюкозы, используемой грибами для метаболических процессов, а также изменениями крупных и мелких сосудов (диабетическая ангиопатия), приводящие к снижению трофики тканей и ослаблению защитных сил организма.
Известных возбудителей онихомикозов принято делить на три группы: дерматофиты, дрожжевые грибы рода Candida и плесневые грибы–недерматофиты. Актуальность проблемы онихомикоза обусловлена не только чрезвычайно широкой распространенностью заболевания среди населения, но и в немалой степени связана со сложностями его терапии, что в определенной мере обусловлено анатомо–физиологическими особенностями ногтя. Ногтевая пластинка интимно связана с ногтевым ложем и матриксом и представляет собой полностью кератинизированный слой роговых клеток, плотно прилегающих к ногтевому ложу.
Эпителий ногтевого ложа состоит из нескольких клеточных слоев и имеет протяженность от лунки до гипонихиума. Ногтевое ложе кератинизируется в отсутствие гранулированного слоя и фактически включает внутренний слой ногтевой пластинки. Ногтевое ложе может составлять около одной трети толщины окончательной ногтевой пластинки. Дорсальная и промежуточная части ногтевой пластинки происходят от ногтевого матрикса. Матрикс состоит из быстроразмножающихся клеток – кератоцитов, из которых строятся ногтевая пластинка и ногтевое ложе. За счет постоянного образования в матриксе кератоцитов идет рост ногтя от проксимального конца к дистальному.
В структуре грибковых инфекций внутренних органов за последние 15 лет наметилась четкая тенденция к увеличению доли плесневых микозов с 1,5% до 17% .
Особенно часто плесневыми грибами поражается бронхо–легочная система. Это обстоятельство обусловлено особенностями возбудителя, а именно, размером канидий (спор) гриба. Споры диаметром 2,0–3,0 мкм при экзогенном проникновении через верхние дыхательные пути легко попадают в терминальные отделы и альвеолярные пространства легких.
У больных хроническими пневмопатиями плесневые микозы присоединяются в 10–15% случаев, у пациентов с бронхиальной астмой – до 35%, а после трансплантации легких – у 19% больных. Как правило, плесневые микозы, развиваются у лиц с нейтропенией, онкопатологией, туберкулезом, эндокринопатиями, хронических неспецифических заболеваний легких и др.
Клинические проявления
Клинические проявления онихомикоза определяются как путем внедрения грибковой инфекции, так и свойствами самого гриба. Основным фактором, способствующим внедрению грибковой инфекции, является нарушение целостности ногтя и окружающих его тканей, например, травма во время маникюра, спортивные травмы, ношение неудобной обуви. Главные факторы патогенности грибов: выживаемость в среде макроорганизма, способность к инвазивному росту и выработке литических ферментов.
В настоящее время выделяют следующие клинические формы онихомикоза (N. Zaias, 1972):
– поверхностная (поверхностная белая) – поражение верхних слоев ногтевой пластинки без вовлечения матрикса;
– дистальная (дистально–латеральная) подногтевая – поражение ногтевого ложа, ногтевой пластики и реже – матрикса, часто сопровождающееся развитием подногтевого гиперкератоза (реакция ногтевого ложа на присутствие гриба);
– проксимальная подногтевая – начало заболевания с поражения зоны матрикса, не сопровождается гиперкератозом.
Одна из групп поражения легких от воздействия плесневых грибов характеризуется развитием синдрома гиперчувствительности и микогенной аллергии (экзогенная астма, экзогенный аллергический альвеолит, аллергический пневмомикоз) и требует проведения адекватной десенсибилизирующей и дезинтоксикационной терапии.
Другую группу составляют инвазивные плесневые микозы (острый и язвенный трахеобронхит, хронический некротический аспергиллез, аспергиллезный обструктивный бронхит, гнойно–некротический бронхит, пневмония, плеврит, острая аспергиллома и др).
Лечение онихомикозов представляет сложную проблему. Необходимо объяснить пациенту, что лечение будет длительным и потребует от него максимум усилий. Главной задачей лечения онихомикоза является удаление этиологического фактора – патогенного гриба из пораженных ногтей. В зависимости от пути воздействия на патогенный агент выделяют следующие виды этиотропного лечения:
а) местное (наружное) – когда противогрибковый препарат наносится непосредственно на пораженный ноготь;
б) системное – в случае назначения противогрибкового препарата внутрь, когда он попадает в ткани ногтя с током крови;
в) комбинированное – сочетание системного и местного лечения.
Выбор той или иной тактики лечения определяется клинической характеристикой онихомикоза: клинической формой, распространенностью поражения ногтя и выраженностью подногтевого гиперкератоза.
Местное лечение показано при поверхностной форме онихомикоза, когда поражаются только верхние слои ногтевой пластинки, нет угрозы вовлечения матрикса и подногтевого гиперкератоза, и при дистально–латеральной форме, в случаях, когда имеется поражение до 1/3 глубины с отсутствующим и умеренным гиперкератозом или до 2/3 глубины ногтя с отсутствующим или умеренным гиперкератозом.
В местной терапии используются вспомогательные методы, позволяющие удалить поврежденный ноготь. Это может быть механическое воздействие – спиливание поврежденной части ногтя одноразовой пилкой, хирургическое удаление ногтя, или воздействие химическими веществами, например, наложение уреапласта с последующей чисткой ногтевого ложа. Затем на ногтевое ложе наносятся крема, растворы, лаки.
Системная терапия показана при проксимальной и дистально–латеральной формах онихомикоза с поражением до 2/3 глубины ногтя с умеренным или выраженным гиперкератозом или более 2/3 глубины ногтя с отсутствующим или умеренным гиперкератозом.
Комбинированная терапия показана при дистально–латеральной форме с поражением более 2/3 глубины с выраженным гиперкератозом.
Объем лечения зависит от того, какие ногти поражены – при вовлечении ногтей на стопах потребуется схема наибольшей продолжительности. Особенность онихомикоза в России – большой удельный вес пожилых пациентов – заставляет чаще учитывать и возрастной фактор. У пожилых лиц скорость роста ногтей снижается в среднем на 25% по сравнению с молодыми. На фоне патологии сосудов и трофических нарушений замедление роста может быть еще более выраженным. Почему следует учитывать скорость отрастания ногтя перед началом лечения? Дело в том, что современные противогрибковые препараты в терапевтических дозах не способны к радикальной элиминации возбудителя в ногте. Механизм действия таких препаратов при онихомикозе сводится к подавлению роста гриба на время роста ногтевой пластинки. Иными словами, пока действует противогрибковый препарат, рост ногтевой пластинки опережает встречный (приостановленный) рост гриба, смещая его кнаружи. Однако если ногти растут медленно, то для достижения перевеса в скорости требуется большая сила воздействия, определяемая концентрацией и дозой препарата.
Выбрав подход к терапии, врачу остается предложить своему пациенту препарат для осуществления намеченной программы лечения. Современный выбор средств лечения онихомикоза достаточно широк – пять системных и не менее десяти местных противогрибковых препаратов.
При системном лечении могут быть использованы препараты содержащие флуконазол – является бис–триазолом, селективно ингибируя синтез стеролов в клетке гриба, он оказывает противогрибковое действие, основное его действие направлено на фермент 14 a–деметилазу, входящий в систему цитохрома Р–450, с этим связана высокая специфичность флуконазола к зависимым от цитохрома Р–450 ферментам гриба.
При этой патологии в комплексное лечение, наряду с общеукрепляющей и симптоматической терапией, включают и этиотропное средство. Существует несколько противогрибковых препаратов, воздействующих на плесневую флору.
Амфотерицин Б часто применяется для лечения плесневых микозов. Но, обладая широким спектром фунгистатического действия против грибов, к сожалению, параллельно оказывает иногда нежелательное пирогенное и токсическое влияние на организм человека. При внутривенном введении антимикотика нередко возникают ознобы, подъем температуры, головная боль, боль в суставах и мышцах, диарея, высыпания на коже, нарушение функции печени и почек. Амфотерицин иногда комбинируют с 5–флюороцитозином, но миелосупрессивный эффект последнего не позволяет применять его у пациентов с иммуносупрессией.
Тербинафин – представляет собой аллиламин и обладает широким спектром противогрибкового действия. Тербинафин специфическим образом изменяет ранний этап биосинтеза стеролов, поисходящего в грибах. Это ведет к дефециту эргостерола и внутриклеточному накоплению сквалена, что вызывает гибель клетки гриба. Действие тербинафина осуществляется путем ингибирования фермента скваленэпоксидазы, расположенного на клеточной мембране гриба. Этот фермент не относится к системе цитохрома Р–450.
Итраконазол является производным триазола и воздействует на фермент 14 a–деметилазу, входящий в систему цитохрома Р–450, нарушая синтез эргостерола и приводя к разрушению клеточной мембраны гриба. В последние годы на российском фармацевтическом рынке появился новый отечественный итраконазол под торговой маркой Ирунин (фармацевтическая компания Верофарм), по цене доступный большому количеству пациентов.
При выборе препарата в зависимости от необходимой продолжительности лечения учитывают известные сроки, в течение которых этот препарат задерживается в ногте. При использовании Ирунина в распространенной схеме пульс–терапии (см. ниже) эти сроки известны и составляют от 3 до 4 месяцев в зависимости от числа пульсов. Этот период является наибольшим среди современных системных антимикотиков, поэтому подробнее остановимся на данном препарате. Ирунин (итраконазол) активен в отношении дерматофитов (Trichophyton, Microsporum, Epidermophyton), дрожжевых и дрожжеподобных грибов (Cryptococcus neoformans, Pitysporum, Candida), а также Aspergillus, Histoplasma, Fonsecaea, Cladosporium, Paracoccidioides brasiliensis, Sporothrix schenckii, Blastomyces dermatitidis. Эффективность Ирунина клинически подтверждена в многочисленных исследованиях в различных городах России, включая Москву, Санкт–Петербург, Красноярск, Нижний Новгород, Волгоград, Омск, Кемерово, Новосибирск, Уфу.
Максимальная биодоступность Ирунина отмечается в том случае, если препарат принимают сразу же после плотной еды. После однократного приема препарата Смах итраконазола в плазме достигается через 3–4 часа. Связывание с белками плазмы составляет 99,8%. Ирунин распределяется в различных тканях. Терапевтическая концентрация в кератине ногтей достигается через одну неделю после начала лечения и сохраняется, по крайней мере, в течение 6 месяцев после завершения 3–месячного курса лечения. Ирунин метаболизируется в печени, с образованием большого числа метаболитов. Выводится из организма почками в виде метаболитов и с калом в неизмененном виде.
При онихомикозе препарат назначают в виде пульс–терапии или в виде непрерывного лечения. Один курс пульс–терапии заключается в назначении итраконазола по 200 мг 2 раза в сутки в течение 7 дней.
При поражении ногтевых пластинок стоп (вне зависимости от того, имеется или нет поражение ногтей на руках) проводят 3 курса лечения (1 неделя приема препарата, 3 недели – перерыв). При повреждении ногтевых пластинок кистей проводят 2 курса лечения (1 неделя приема препарата, 3 недели – перерыв). При непрерывном лечении аспергиллеза, системного кандидоза итраконазол назначают по 200 мг 1 раз в сутки в течение 3 недель – 7 месяцев, при необходимости возможно повышение дозы до 200 мг 2 раза в сутки.
У пациентов с циррозом печени и/или с нарушением функции почек препарат применяют под контролем уровня итраконазола в плазме и при необходимости корригируют дозу итраконазола.
В случае проведения терапии в течение более 1 месяца, необходим контроль показателей функции печени. Контроль показателей функции печени необходим также в тех случаях, когда у пациента, принимающего препарат, развивается анорексия, тошнота, рвота, боли в животе или темный цвет мочи. При обнаружении нарушений функций печени препарат отменяют.
Под наблюдением С.А. Буровой находилось 32 больных, в возрасте от 28 до 52 лет, из них 11 аспергиллезным трахеобронхитом, 8 аспергиллезным обструктивным бронхитом, 2 аспергилломой, 1 мукорозом придаточных пазух носа, 1 аспергиллезным поражением кожи и мягких тканей, 5 – плесневым отомикозом, 4 – пенициллиозом легких. У 7 больных аспергиллезный трахеобронхит протекал на фоне бронхиальной астмы легкой и средней тяжести.
Аспергиллома легких локализовалась у обоих больных в верхней доле. На рентгенограммах она имела округлую форму с характерным серповидным просветлением вокруг и значительной зоной перифокального воспаления. У одного больного аспергиллома дренировалась в бронх.
Пенициллиоз легких по клинической симптоматике соответствовал пневмонии. На рентгенограммах были видны инфильтративные тени, фиброзные прикорневые узлы. Предшествующая антибиотикотерапия вполне закономерно, не давала положительного эффекта.
Отомикоз проявлялся снижением слуха, болевыми ощущениями, выделениями из слуховых проходов, налетами белого, желтоватого или черного цвета.
Мукороз придаточных пазух носа был диагностирован на основании микробиологического исследования материала из пазух, характерного затемнения на рентгенограмме, заложенности носа, головных болей и др.
Аспергиллез мягких тканей плечевого пояса развился после травмы пациентки с иммуносупрессией и внешне напоминал вяло текущую гнойную рану, с индуративной инфильтрацией в основании и рыхлыми желто–белыми наслоениями на поверхности.
В исследовании Ирунин играл роль этиотропного средства и входил в схему комплексного лечения каждого конкретного больного наряду с общеукрепляющей, симптоматической, наружной и физиотерапией. Изучали эффективность лечения и переносимость препарата.
Полное клиническое и микологическое излечение хронических грибковых заболеваний наблюдалось у 14 (43,7%) больных, улучшение у 17 (53,1%), отсутствие эффекта – у 1 (3,2%). Общая эффективность составила 96,8%.
Профилактические мероприятия при онихомикозе сводятся к тому, чтобы не допустить развитие инфекции у еще не болевших (первичная профилактика), а у болевших и получивших лечение предотвратить ее рецидив или повторное возникновение (вторичная профилактика). Соответственно уровню профилактических мероприятий мы выделяем личную (индивидуальную) профилактику и общественную, ставящую целью предотвратить распространение инфекции среди групп населения.
Меры первичной личной профилактики включают личную гигиену, уход за ногтями, устранение или компенсацию факторов риска, профилактическое использование местных антимикотических средств при посещении мест общего пользования, а также своевременное выявление и излечение микоза стоп.
Первичная общественная профилактика во многом обеспечивается санитарно–гигиеническим просвещением населения. Его задачи включают не только рекомендации о том, как избежать заражения, но и объяснение необходимости лечения для уже болеющих онихомикозом, то есть своевременным выявлением и санацией источника инфекции на уровне популяции.
В последние десятилетия отмечается значительный рост грибковых заболеваний. Это связано со многими факторами и, в частности, с широким применением в медицинской практике антибиотиков широкого спектра действия, иммунодепрессантов и других групп ЛС.
В связи с тенденцией к росту грибковых заболеваний (как поверхностных, так и тяжелых висцеральных микозов, ассоциированных с ВИЧ-инфекцией, онкогематологическими заболеваниями), развитием устойчивости возбудителей к имеющимся ЛС, выявлением видов грибов, ранее считавшихся непатогенными (в настоящее время потенциальными возбудителями микозов считаются около 400 видов грибов), возросла потребность в эффективных противогрибковых средствах.
Противогрибковые средства (антимикотики) — лекарственные средства, обладающие фунгицидным или фунгистатическим действием и применяемые для профилактики и лечения микозов.
Для лечения грибковых заболеваний используют ряд лекарственных средств, различных по происхождению (природные или синтетические), спектру и механизму действия, противогрибковому эффекту (фунгицидный или фунгистатический), показаниям к применению (местные или системные инфекции), способам назначения (внутрь, парентерально, наружно).
Существует несколько классификаций лекарственных средств, относящихся к группе антимикотиков: по химической структуре, механизму действия, спектру активности, фармакокинетике, переносимости, особенностям клинического применения и др.
В соответствии с химическим строением противогрибковые средства классифицируют следующим образом:
1. Полиеновые антибиотики: нистатин, леворин, натамицин, амфотерицин В, микогептин.
2. Производные имидазола: миконазол, кетоконазол, изоконазол, клотримазол, эконазол, бифоназол, оксиконазол.
3. Производные триазола: флуконазол, итраконазол, вориконазол.
4. Аллиламины (производные N-метилнафталина): тербинафин, нафтифин.
5. Эхинокандины: каспофунгин.
6. Препараты других групп: гризеофульвин, аморолфин, циклопирокс, флуцитозин.
Подразделение противогрибковых препаратов по основным показаниям к применению представлено в классификации Д.А. Харкевича (2006 г.):
I. Средства, применяемые при лечении заболеваний, вызванных патогенными грибами:
1. При системных или глубоких микозах (кокцидиоидомикоз, паракокцидиомикоз, гистоплазмоз, криптококкоз, бластомикоз):
- антибиотики (амфотерицин В, микогептин);
- производные имидазола (миконазол, кетоконазол);
- производные триазола (итраконазол, флуконазол).
2. При эпидермомикозах (дерматомикозах):
- производные N-метилнафталина (тербинафин);
- производные нитрофенола (хлорнитрофенол);
- препараты йода (раствор йода спиртовой, калия йодид).
II. Средства, применяемые при лечении заболеваний, вызванных условно-патогенными грибами (например при кандидамикозе):
- антибиотики (нистатин, леворин, амфотерицин В);
- производные имидазола (миконазол, клотримазол);
- бис-четвертичные аммониевые соли (деквалиния хлорид).
В клинической практике противогрибковые средства делят на 3 основные группы:
1. Препараты для лечения глубоких (системных) микозов.
2. Препараты для лечения эпидермофитий и трихофитий.
3. Препараты для лечения кандидозов.
Выбор ЛС при терапии микозов зависит от вида возбудителя и его чувствительности к ЛС (необходимо назначение ЛС с соответствующим спектром действия), особенностей фармакокинетики ЛС, токсичности препарата, клинического состояния пациента и др.
Грибковые заболевания известны очень давно, еще со времен античности. Однако возбудители дерматомикозов, кандидоза были выявлены только в середине XIX в., к началу XX в. были описаны возбудители многих висцеральных микозов. До появления в медицинской практике антимикотиков для лечения микозов использовали антисептики и калия йодид.
Полиеновые антибиотики — антимикотики природного происхождения, продуцируемые Streptomyces nodosum (амфотерицин В), Actinomyces levoris Krass (леворин), актиномицетом Streptoverticillium mycoheptinicum (микогептин), актиомицетом Streptomyces noursei (нистатин).
Механизм действия полиеновых антибиотиков достаточно изучен. Эти ЛС прочно связываются с эргостеролом клеточной мембраны грибов, нарушают ее целостность, что приводит к потере клеточных макромолекул и ионов и к лизису клетки.
Полиены имеют самый широкий спектр противогрибковой активности in vitro среди антимикотиков. Амфотерицин В при системном применении активен в отношении большинства дрожжеподобных, мицелиальных и диморфных грибов. При местном применении полиены (нистатин, натамицин, леворин) действуют преимущественно на Candida spp. Полиены активны в отношении некоторых простейших — трихомонад (натамицин), лейшманий и амеб (амфотерицин В). Малочувствительны к амфотерицину В возбудители зигомикоза. К полиенам устойчивы дерматомицеты (род Trichophyton, Microsporum и Epidermophyton), Pseudoallescheria boydi и др.Нистатин (крем, супп. ваг. и рект., табл.), леворин (табл., мазь, гран.д/р-ра для приема внутрь) и натамицин (крем, супп. ваг., табл.) применяют и местно, и внутрь при кандидозе, в т.ч. кандидозе кожи, слизистой оболочки ЖКТ, генитальном кандидозе; амфотерицин В (пор. д/инф., табл., мазь) используется преимущественно для лечения тяжелых системных микозов и является пока единственным полиеновым антибиотиком для в/в введения.
Все полиены практически не всасываются из ЖКТ при приеме внутрь, и с поверхности неповрежденной кожи и слизистых оболочек при местном применении.
Общими побочными системными эффектами полиенов при приеме внутрь являются: тошнота, рвота, диарея, боль в животе, а также аллергические реакции; при местном использовании — раздражение и ощущение жжения кожи.
В 80-е годы был разработан ряд новых ЛС на основе амфотерицина В — липид-ассоциированные формы амфотерицина В (липосомальный амфотерицин В — амбизом, липидный комплекс амфотерицина В — абелсет, коллоидная дисперсия амфотерицина В — амфоцил), которые в настоящее время внедряются в клиническую практику. Их отличает существенное снижение токсичности при сохранении противогрибкового действия амфотерицина В.
Липосомальный амфотерицин В (лиоф. пор. д/инф.) — современная лекарственная форма амфотерицина В, инкапсулированного в липосомы (везикулы, формирующиеся при диспергировании в воде фосфолипидов), отличается лучшей переносимостью.
Липосомы, находясь в крови, долгое время остаются интактными; высвобождение активного вещества происходит только при контакте с клетками гриба при попадании в ткани, пораженные грибковой инфекцией, при этом липосомы обеспечивают интактность ЛС по отношению к нормальным тканям.
В отличие от обычного амфотерицина В, липосомальный амфотерицин В создает более высокие концентрации в крови, чем обычный амфотерицин В, практически не проникает в ткань почек (менее нефротоксичен), обладает более выраженными кумулятивными свойствами, период полувыведения в среднем составляет 4–6 дней, при длительном использовании возможно увеличение до 49 дней. Нежелательные реакции (анемия, лихорадка, озноб, гипотензия), по сравнению со стандартным препаратом, возникают реже.
Показаниями к применению липосомального амфотерицина В являются тяжелые формы системных микозов у пациентов с почечной недостаточностью, при неэффективности стандартного препарата, при его нефротоксичности или некупируемых премедикацией выраженных реакциях на в/в инфузию.
Азолы (производные имидазола и триазола) — наиболее многочисленная группа синтетических противогрибковых средств.
Эта группа включает:
- азолы для системного применения — кетоконазол (капс., табл.), флуконазол (капс., табл., р-р в/в), итраконазол (капс., р-р для приема внутрь); вориконазол (табл., р-р в/в);
- азолы для местного применения — бифоназол, изоконазол, клотримазол, миконазол, оксиконазол, эконазол, кетоконазол (крем, мазь, супп. ваг., шампунь).
Первый из предложенных азолов системного действия — кетоконазол — в настоящее время из клинической практики вытесняют триазолы — итраконазол и флуконазол. Кетоконазол практически утратил свое значение ввиду высокой токсичности (гепатотоксичность) и используется преимущественно местно.
Противогрибковое действие азолов, как и полиеновых антибиотиков, обусловлено нарушением целостности мембраны клетки гриба, но механизм действия иной: азолы нарушают синтез эргостерола — основного структурного компонента клеточной мембраны грибов. Эффект связан с ингибированием цитохром P450-зависимых ферментов, в т.ч. 14-альфа-деметилазы (катализирует реакцию превращения ланостерола в эргостерол), что приводит к нарушению синтеза эргостерола клеточной мембраны грибов.
Азолы имеют широкий спектр противогрибкового действия, оказывают преимущественно фунгистатический эффект. Азолы для системного применения активны в отношении большинства возбудителей поверхностных и инвазивных микозов, в т.ч. Candida albicans, Cryptococcus neoformans, Coccidioides immitis, Histoplasma capsulatum, Blastomyces dermatitidis, Paraccoccidioides brasiliensis. Обычно к азолам резистентны Candida glabrata, Candida krucei, Aspergillus spp., Fusarium spp. и зигомицеты (класс Zygomycetes). Препараты для местного применения при создании высоких концентраций в месте действия могут действовать фунгицидно в отношении некоторых грибов.
Азолы для системного применения (кетоконазол, флуконазол, итраконазол, вориконазол) хорошо всасываются при приеме внутрь. Биодоступность кетоконазола и итраконазола может значительно варьировать в зависимости от уровня кислотности в желудке и приема пищи, тогда как абсорбция флуконазола не зависит ни от pH в желудке, ни от приема пищи.
Флуконазол и вориконазол применяют внутрь и в/в, кетоконазол и итраконазол — только внутрь. Фармакокинетика вориконазола, в отличие от других системных азолов, является нелинейной — при повышении дозы в 2 раза AUC увеличивается в 4 раза.
Флуконазол, кетоконазол, итраконазол и вориконазол распределяются в большинство тканей, органов и биологических жидкостей организма, создавая в них высокие концентрации. Итраконазол может накапливаться в коже и ногтевых пластинках, где его концентрации в несколько раз превышают плазменные. Итраконазол практически не проникает в слюну, внутриглазную и спинно-мозговую жидкость. Кетоконазол плохо проходит через ГЭБ и определяется в спинно-мозговой жидкости лишь в небольших количествах. Флуконазол хорошо проходит через ГЭБ (уровень его в ликворе может достигать 50–90% от уровня в плазме) и гематоофтальмический барьер.
Системные азолы отличаются длительностью периода полувыведения: T1/2 кетоконазола — около 8 ч, итраконазола и флуконазола — около 30 ч (20–50 ч). Все системные азолы (кроме флуконазола) метаболизируются в печени и выводятся преимущественно через ЖКТ. Флуконазол отличается от других антифунгальных средств тем, что выводится через почки (преимущественно в неизмененном виде — 80–90%).
Наиболее частые побочные эффекты азолов системного применения включают: боль в животе, тошноту, рвоту, диарею, головную боль, повышение активности трансаминаз, гематологические реакции (тромбоцитопения, агранулоцитоз), аллергические реакции — кожная сыпь и др.
Азолы для местного применения (клотримазол, миконазол и др.) плохо абсорбируются при приеме внутрь, в связи с чем используются для местного лечения. Эти ЛС создают высокие концентрации в эпидермисе и нижележащих слоях кожи. Наиболее длительный период полувыведения из кожи отмечается у бифоназола (19–32 ч).
Поскольку азолы ингибируют окислительные ферменты системы цитохрома Р450 (кетоконазол > итраконазол > флуконазол), эти ЛС могут изменять метаболизм других лекарств и синтез эндогенных соединений (стероиды, гормоны, простагландины, липиды и др.).
Аллиламины — синтетические ЛС. Оказывают преимущественно фунгицидное действие. В отличие от азолов, блокируют более ранние стадии синтеза эргостерола. Механизм действия обусловлен ингибированием фермента скваленэпоксидазы, катализирующей вместе со скваленциклазой превращение сквалена в ланостерол. Это приводит к дефициту эргостерина и к внутриклеточному накоплению сквалена, что вызывает гибель гриба. Аллиламины обладают широким спектром активности, однако клиническое значение имеет только их действие на возбудителей дерматомикозов, в связи с чем основными показаниями к назначению аллиламинов являются дерматомикозы. Тербинафин применяют местно (крем, гель, мазь, спрей) и внутрь (табл.), нафтифин — только местно (крем, р-р наружн.).
Каспофунгин применяется только парентерально, т.к. биодоступность при пероральном приеме составляет не более 1%. После в/в инфузии высокие концентрации наблюдаются в плазме, легких, печени, селезенке, кишечнике.
Применяют каспофунгин для лечения кандидоза пищевода, инвазивных кандидозов (в т.ч. кандидемии у пациентов с нейтропенией) и инвазивного аспергиллеза при неэффективности или непереносимости других видов терапии (амфотерицин В, амфотерицин В на липидных носителях и/или итраконазол).
ЛС других групп. К противогрибковым препаратам других групп относятся средства для системного (гризеофульвин, флуцитозин) и местного применения (аморолфин, циклопирокс).
Гризеофульвин — одно из первых противогрибковых средств природного происхождения — антибиотик, продуцируемый плесневым грибом Penicillium nigricans (griseofulvum). Гризеофульвин до сих пор остается одним из основных средств лечения дерматомикозов, применяется внутрь и местно.
Аморолфин — синтетический антимикотик широкого спектра действия для местного использования (в виде лака для ногтей).
Циклопирокс — синтетическое ЛС для местного применения.
В настоящее время в стадии разработки находятся антимикотики, являющиеся представителями уже известных групп противогрибковых средств, а также относящиеся к новым классам соединений: коринекандин, фузакандин, сордарины, циспентацин, азоксибациллин.
Литература
Антимикробные и противогрибковые лекарственные средства/ Под ред. Ю.В. Немытина.- М.: Ремедиум, 2002.- С. 57-59.
Базисная и клиническая фармакология/ Под ред. Б.Г. Катцунга; пер. с англ. под ред. Э.Э. Звартау: в 2 т.- М.-СПб.: Бином-Невский диалект, 1998.- Т. 2.- С. 290-297, 555-559.
Виноградов В.М., Каткова Е.Б., Мухин Е.А. Фармакология с рецептурой/ Под ред. В.М. Виноградова.- 4-е изд, испр.- СПб.: СпецЛит, 2006.- С. 221-232.
Коротяев А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология: Учебник для мед.вузов.- 3-е изд., испр. и доп.- СПб.: СпецЛит, 2002.- С. 491-511.
Климко Н.Н., Веселов А.В. Новые препараты для лечения инвазивных микозов// Клиническая микробиология и антимикробная терапия.- 2003.- Т. 5.- № 4.- С. 342-353.
Клиническая фармакология по Гудману и Гилману/ Под общей редакцией А.Г. Гилмана. Пер. с англ.- М.: Практика, 2006.- с 996-1010.
Машковский М.Д. Лекарства XX века.- М.: Новая Волна, 1998.- С. 159-161, 250.
Машковский М.Д. Лекарственные средства: в 2 т.- 14-е изд.- М.: Новая Волна, 2000.- Т. 2.- С. 352-366.
Михайлов И.Б. Настольная книга врача по клинической фармакологии: Руководство для врачей.- СПб.: Фолиант, 2001.- с. 119-126.
Митрофанов В.С. Системные антифунгальные препараты// Проблемы медицинской микологии.- 2001. -Т.3, №2. - С.6-14.
Практическое руководство по антиинфекционной химиотерапии/ Под ред. Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова.- М.: Боргес, 2002.- С. 129-144.
Рациональная фармакотерапия в стоматологии: Рук. для практикующих врачей/ Г.М. Барер, Е.В. Зорян, В.С. Агапов, В.В. Афанасьев и др.; под общ. ред. Г.М. Барера, Е.В. Зорян.- М.: Литтерра, 2006.- С. 74-78. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 11).
Рациональная фармакотерапия в офтальмологии: Рук. для практикующих врачей/ Е.А. Егоров, В.Н. Алексеев, Ю.С. Астахов и др.; под общ. ред. Е.А. Егорова.- М.: Литтерра, 2004.- С. 76-80. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 7).
Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем: Рук. для практикующих врачей/ А.А. Кубанова, В.И. Кисина, Л.А. Блатун, А.М. Вавилов и др.; под общ. ред. А.А. Кубановой, В.И. Кисиной.- М.: Литтерра, 2005.- С. 145-182. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 8).
Федеральное руководство по использованию лекарственных средств (формулярная система)/ Под ред. А.Г. Чучалина, Ю.Б. Белоусова, В.В. Яснецова.- Вып. VIII.- М.: ЭХО, 2007.- С. 705-713.
Харкевич Д.А. Фармакология: Учебник.- 9-е изд., перераб., доп. и испр.- М.: Гэотар-Медицина, 2006.- С. 653-659.
Харкевич Д.А. Фармакология: Учебник.- 9-е изд., перераб., доп. и испр.- М.: Гэотар-Медицина, 2006.- С. 653-659.
В последние десятилетия отмечается значительный рост грибковых заболеваний. Это связано со многими факторами и, в частности, с широким применением в медицинской практике антибиотиков широкого спектра действия, иммунодепрессантов и других групп ЛС.
В связи с тенденцией к росту грибковых заболеваний (как поверхностных, так и тяжелых висцеральных микозов, ассоциированных с ВИЧ-инфекцией, онкогематологическими заболеваниями), развитием устойчивости возбудителей к имеющимся ЛС, выявлением видов грибов, ранее считавшихся непатогенными (в настоящее время потенциальными возбудителями микозов считаются около 400 видов грибов), возросла потребность в эффективных противогрибковых средствах.
Противогрибковые средства (антимикотики) — лекарственные средства, обладающие фунгицидным или фунгистатическим действием и применяемые для профилактики и лечения микозов.
Для лечения грибковых заболеваний используют ряд лекарственных средств, различных по происхождению (природные или синтетические), спектру и механизму действия, противогрибковому эффекту (фунгицидный или фунгистатический), показаниям к применению (местные или системные инфекции), способам назначения (внутрь, парентерально, наружно).
Существует несколько классификаций лекарственных средств, относящихся к группе антимикотиков: по химической структуре, механизму действия, спектру активности, фармакокинетике, переносимости, особенностям клинического применения и др.
В соответствии с химическим строением противогрибковые средства классифицируются следующим образом:
1. Полиеновые антибиотики: нистатин, леворин, натамицин, амфотерицин В, микогептин.
2. Производные имидазола: миконазол, кетоконазол, изоконазол, клотримазол, эконазол, бифоназол, оксиконазол.
3. Производные триазола: флуконазол, итраконазол, вориконазол.
4. Аллиламины (производные N-метилнафталина): тербинафин, нафтифин.
5. Эхинокандины: каспофунгин.
6. Препараты других групп: гризеофульвин, аморолфин, циклопирокс, флуцитозин.
Подразделение противогрибковых препаратов по основным показаниям к применению представлено в классификации Д.А. Харкевича (2003 г.):
I. Средства, применяемые при лечении заболеваний, вызванных патогенными грибами:
1. При системных или глубоких микозах (кокцидиоидомикоз, паракокцидиомикоз, гистоплазмоз, криптококкоз, бластомикоз):
- антибиотики (амфотерицин В, микогептин);
- производные имидазола (миконазол, кетоконазол);
- производные триазола (итраконазол, флуконазол).
2. При эпидермомикозах (дерматомикозах):
- производные N-метилнафталина (тербинафин);
- производные нитрофенола (хлорнитрофенол);
- препараты йода (раствор йода спиртовой, калия йодид).
II. Средства, применяемые при лечении заболеваний, вызванных условно-патогенными грибами (например при кандидамикозе):
- антибиотики (нистатин, леворин, амфотерицин В);
- производные имидазола (миконазол, клотримазол);
- бис-четвертичные аммониевые соли (деквалиния хлорид).
В клинической практике противогрибковые средства делят на 3 основные группы:
1. Препараты для лечения глубоких (системных) микозов.
2. Препараты для лечения эпидермофитий и трихофитий.
3. Препараты для лечения кандидозов.
Выбор ЛС при терапии микозов зависит от вида возбудителя и его чувствительности к ЛС (необходимо назначение ЛС с соответствующим спектром действия), особенностей фармакокинетики ЛС, токсичности препарата, клинического состояния пациента и др.
Грибковые заболевания известны очень давно, еще со времен античности. Однако возбудители дерматомикозов, кандидоза были выявлены только в середине XIX в., к началу XX в. были описаны возбудители многих висцеральных микозов. До появления в медицинской практике антимикотиков для лечения микозов использовали антисептики и калия йодид.
Полиеновые антибиотики — антимикотики природного происхождения, продуцируемые Streptomyces nodosum (амфотерицин В), Actinomyces levoris Krass (леворин), актиномицетом Streptoverticillium mycoheptinicum (микогептин), актиомицетом Streptomyces noursei (нистатин).
Механизм действия полиеновых антибиотиков достаточно изучен. Эти ЛС прочно связываются с эргостеролом клеточной мембраны грибов, нарушают ее целостность, что приводит к потере клеточных макромолекул и ионов и к лизису клетки.
Полиены имеют самый широкий спектр противогрибковой активности in vitro среди антимикотиков. Амфотерицин В при системном применении активен в отношении большинства дрожжеподобных, мицелиальных и диморфных грибов. При местном применении полиены (нистатин, натамицин, леворин) действуют преимущественно на Candida spp. Полиены активны в отношении некоторых простейших — трихомонад (натамицин), лейшманий и амеб (амфотерицин В). Малочувствительны к амфотерицину В возбудители зигомикоза. К полиенам устойчивы дерматомицеты (род Trichophyton, Microsporum и Epidermophyton), Pseudoallescheria boydi и др.
Нистатин (крем, супп. ваг. и рект., табл.), леворин (табл., мазь, гран.д/р-ра для приема внутрь) и натамицин (крем, супп. ваг., табл.) применяют и местно, и внутрь при кандидозе, в т.ч. кандидозе кожи, слизистой оболочки ЖКТ, генитальном кандидозе; амфотерицин В (пор. д/инф., табл., мазь) используется преимущественно для лечения тяжелых системных микозов и является пока единственным полиеновым антибиотиком для в/в введения.
Все полиены практически не всасываются из ЖКТ при приеме внутрь, и с поверхности неповрежденной кожи и слизистых оболочек при местном применении.
Общими побочными системными эффектами полиенов при приеме внутрь являются: тошнота, рвота, диарея, боль в животе, а также аллергические реакции; при местном использовании — раздражение и ощущение жжения кожи.
В 80-е годы был разработан ряд новых ЛС на основе амфотерицина В — липид-ассоциированные формы амфотерицина В (липосомальный амфотерицин В — амбизом, липидный комплекс амфотерицина В — абелсет, коллоидная дисперсия амфотерицина В — амфоцил), которые в настоящее время внедряются в клиническую практику. Их отличает существенное снижение токсичности при сохранении противогрибкового действия амфотерицина В.
Липосомальный амфотерицин В (лиоф. пор. д/инф.) — современная лекарственная форма амфотерицина В, инкапсулированного в липосомы (везикулы, формирующиеся при диспергировании в воде фосфолипидов), отличается лучшей переносимостью. Липосомы, находясь в крови, долгое время остаются интактными; высвобождение активного вещества происходит только при контакте с клетками гриба при попадании в ткани, пораженные грибковой инфекцией, при этом липосомы обеспечивают интактность ЛС по отношению к нормальным тканям.
В отличие от обычного амфотерицина В, липосомальный амфотерицин В создает более высокие концентрации в крови, чем обычный амфотерицин В, практически не проникает в ткань почек (менее нефротоксичен), обладает более выраженными кумулятивными свойствами, период полувыведения в среднем составляет 4–6 дней, при длительном использовании возможно увеличение до 49 дней. Нежелательные реакции (анемия, лихорадка, озноб, гипотензия), по сравнению со стандартным препаратом, возникают реже.
Показаниями к применению липосомального амфотерицина В являются тяжелые формы системных микозов у пациентов с почечной недостаточностью, при неэффективности стандартного препарата, при его нефротоксичности или некупируемых премедикацией выраженных реакциях на в/в инфузию.
Азолы (производные имидазола и триазола) — наиболее многочисленная группа синтетических противогрибковых средств.
Эта группа включает:
- азолы для системного применения — кетоконазол (капс., табл.), флуконазол (капс., табл., р-р в/в), итраконазол (капс., р-р для приема внутрь); вориконазол (табл., р-р в/в);
- азолы для местного применения — бифоназол, изоконазол, клотримазол, миконазол, оксиконазол, эконазол, кетоконазол (крем, мазь, супп. ваг., шампунь).
Первый из предложенных азолов системного действия — кетоконазол — в настоящее время из клинической практики вытесняют триазолы — итраконазол и флуконазол. Кетоконазол практически утратил свое значение ввиду высокой токсичности (гепатотоксичность) и используется преимущественно местно.
Противогрибковое действие азолов, как и полиеновых антибиотиков, обусловлено нарушением целостности мембраны клетки гриба, но механизм действия иной: азолы нарушают синтез эргостерола — основного структурного компонента клеточной мембраны грибов. Эффект связан с ингибированием цитохром P450-зависимых ферментов, в т.ч. 14-альфа-деметилазы (катализирует реакцию превращения ланостерола в эргостерол), что приводит к нарушению синтеза эргостерола клеточной мембраны грибов.
Азолы имеют широкий спектр противогрибкового действия, оказывают преимущественно фунгистатический эффект. Азолы для системного применения активны в отношении большинства возбудителей поверхностных и инвазивных микозов, в т.ч. Candida albicans, Cryptococcus neoformans, Coccidioides immitis, Histoplasma capsulatum, Blastomyces dermatitidis, Paraccoccidioides brasiliensis. Обычно к азолам резистентны Candida glabrata, Candida krucei, Aspergillus spp., Fusarium spp. и зигомицеты (класс Zygomycetes). Препараты для местного применения при создании высоких концентраций в месте действия могут действовать фунгицидно в отношении некоторых грибов.
Азолы для системного применения (кетоконазол, флуконазол, итраконазол, вориконазол) хорошо всасываются при приеме внутрь. Биодоступность кетоконазола и итраконазола может значительно варьировать в зависимости от уровня кислотности в желудке и приема пищи, тогда как абсорбция флуконазола не зависит ни от pH в желудке, ни от приема пищи.
Флуконазол и вориконазол применяют внутрь и в/в, кетоконазол и итраконазол — только внутрь. Фармакокинетика вориконазола, в отличие от других системных азолов, является нелинейной — при повышении дозы в 2 раза AUC увеличивается в 4 раза.
Флуконазол, кетоконазол, итраконазол и вориконазол распределяются в большинство тканей, органов и биологических жидкостей организма, создавая в них высокие концентрации. Итраконазол может накапливаться в коже и ногтевых пластинках, где его концентрации в несколько раз превышают плазменные. Итраконазол практически не проникает в слюну, внутриглазную и спинно-мозговую жидкость. Кетоконазол плохо проходит через ГЭБ и определяется в спинно-мозговой жидкости лишь в небольших количествах. Флуконазол хорошо проходит через ГЭБ (уровень его в ликворе может достигать 50–90% от уровня в плазме) и гематоофтальмический барьер.
Системные азолы отличаются длительностью периода полувыведения: T1/2 кетоконазола — около 8 ч, итраконазола и флуконазола — около 30 ч (20–50 ч). Все системные азолы (кроме флуконазола) метаболизируются в печени и выводятся преимущественно через ЖКТ. Флуконазол отличается от других антифунгальных средств тем, что выводится через почки (преимущественно в неизмененном виде — 80–90%).
Наиболее частые побочные эффекты азолов системного применения включают: боль в животе, тошноту, рвоту, диарею, головную боль, повышение активности трансаминаз, гематологические реакции (тромбоцитопения, агранулоцитоз), аллергические реакции — кожная сыпь и др.
Азолы для местного применения (клотримазол, миконазол и др.) плохо абсорбируются при приеме внутрь, в связи с чем используются для местного лечения. Эти ЛС создают высокие концентрации в эпидермисе и нижележащих слоях кожи. Наиболее длительный период полувыведения из кожи отмечается у бифоназола (19–32 ч).
Поскольку азолы ингибируют окислительные ферменты системы цитохрома Р450 (кетоконазол > итраконазол > флуконазол), эти ЛС могут изменять метаболизм других лекарств и синтез эндогенных соединений (стероиды, гормоны, простагландины, липиды и др.).
Аллиламины — синтетические ЛС. Оказывают преимущественно фунгицидное действие. В отличие от азолов, блокируют более ранние стадии синтеза эргостерола. Механизм действия обусловлен ингибированием фермента скваленэпоксидазы, катализирующей вместе со скваленциклазой превращение сквалена в ланостерол. Это приводит к дефициту эргостерина и к внутриклеточному накоплению сквалена, что вызывает гибель гриба. Аллиламины обладают широким спектром активности, однако клиническое значение имеет только их действие на возбудителей дерматомикозов, в связи с чем основными показаниями к назначению аллиламинов являются дерматомикозы. Тербинафин применяют местно (крем, гель, мазь, спрей) и внутрь (табл.), нафтифин — только местно (крем, р-р наружн.).
Каспофунгин применяется только парентерально, т.к. биодоступность при пероральном приеме составляет не более 1%. После в/в инфузии высокие концентрации наблюдаются в плазме, легких, печени, селезенке, кишечнике.
Применяют каспофунгин для лечения кандидоза пищевода, инвазивных кандидозов (в т.ч. кандидемии у пациентов с нейтропенией) и инвазивного аспергиллеза при неэффективности или непереносимости других видов терапии (амфотерицин В, амфотерицин В на липидных носителях и/или итраконазол).
ЛС других групп. К противогрибковым препаратам других групп относятся средства для системного (гризеофульвин, флуцитозин) и местного применения (аморолфин, циклопирокс).
Гризеофульвин — одно из первых противогрибковых средств природного происхождения — антибиотик, продуцируемый плесневым грибом Penicillium nigricans (griseofulvum). Гризеофульвин до сих пор остается одним из основных средств лечения дерматомикозов, применяется внутрь и местно.
Аморолфин — синтетический антимикотик широкого спектра действия для местного использования (в виде лака для ногтей).
Циклопирокс — синтетическое ЛС для местного применения.
В настоящее время в стадии разработки находятся антимикотики, являющиеся представителями уже известных групп противогрибковых средств, а также относящиеся к новым классам соединений: коринекандин, фузакандин, сордарины, циспентацин, азоксибациллин.
Литература
Антимикробные и противогрибковые лекарственные средства/ Под ред. Ю.В. Немытина.- М.: Ремедиум, 2002.- С. 57-59.
Базисная и клиническая фармакология/ Под ред. Б.Г. Катцунга; пер. с англ. под ред. Э.Э. Звартау: в 2 т.- М.-СПб.: Бином-Невский диалект, 1998.- Т. 2.- С. 290-297.
Виноградов В.М., Каткова Е.Б., Мухин Е.А. Фармакология с рецептурой/ Под ред. В.М. Виноградова.- 4-е изд, испр.- СПб.: СпецЛит, 2006.- С. 221-232.
Коротяев А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология: Учебник для мед.вузов.- 3-е изд., испр. и доп.- СПб.: СпецЛит, 2002.- С. 491-511.
Климко Н.Н., Веселов А.В. Новые препараты для лечения инвазивных микозов// Клиническая микробиология и антимикробная терапия.- 2003.- Т. 5.- № 4.- С. 342-353.
Машковский М.Д. Лекарства XX века.- М.: Новая Волна, 1998.- С. 159-161, 250.
Машковский М.Д. Лекарственные средства: в 2 т.- 14-е изд.- М.: Новая Волна, 2000.- Т. 2.- С. 352-366.
Митрофанов В.С. Системные антифунгальные препараты// Проблемы медицинской микологии.- 2001. -Т.3, №2. - С.6-14.
Практическое руководство по антиинфекционной химиотерапии/ Под ред. Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова.- М.: Боргес, 2002.- С. 129-144.
Рациональная фармакотерапия в стоматологии: Рук. для практикующих врачей/ Г.М. Барер, Е.В. Зорян, В.С. Агапов, В.В. Афанасьев и др.; под общ. ред. Г.М. Барера, Е.В. Зорян.- М.: Литтерра, 2006.- С. 74-78. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 11).
Рациональная фармакотерапия в офтальмологии: Рук. для практикующих врачей/ Е.А. Егоров, В.Н. Алексеев, Ю.С. Астахов и др.; под общ. ред. Е.А. Егорова.- М.: Литтерра, 2004.- С. 76-80. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 7).
Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем: Рук. для практикующих врачей/ А.А. Кубанова, В.И. Кисина, Л.А. Блатун, А.М. Вавилов и др.; под общ. ред. А.А. Кубановой, В.И. Кисиной.- М.: Литтерра, 2005.- С. 145-182. (Рациональная фармакотерапия: Сер. руководство для практикующих врачей; Т. 8).
Федеральное руководство по использованию лекарственных средств (формулярная система)/ Под ред. А.Г. Чучалина, Ю.Б. Белоусова, В.В. Яснецова.- Вып. VIII.- М.: ЭХО, 2007.- С. 705-713.
Харкевич Д.А. Фармакология: Учебник.- 7-е изд., перераб. и доп.- М.: Гэотар-Медицина, 2003.- С. 631-636.
Энциклопедия клинической онкологии: Руководство для практикующих врачей/ М.И. Давыдов, Г.Л. Вышковский и др.; под общей ред. М.И. Давыдова, Г.Л. Вышковского.- М.: РЛС-2005, 2004.- 1536 с. (Серия Регистр лекарственных средств России РЛС).
Что такое отомикоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Саидовой Б. С., ЛОРа со стажем в 4 года.
Над статьей доктора Саидовой Б. С. работали литературный редактор Юлия Липовская , научный редактор Евгений Буданов и шеф-редактор Маргарита Тихонова

Определение болезни. Причины заболевания
Отомикоз — это заболевание наружного или среднего уха, вызванное грибами, чаще всего дрожжеподобными и плесневыми.
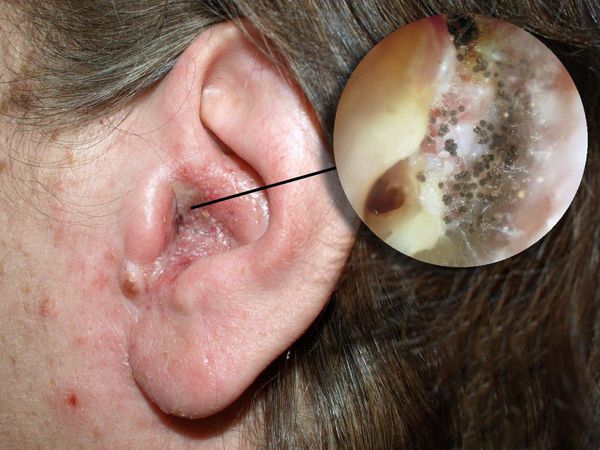
Болезнь развивается в наружном слуховом проходе, иногда процесс затрагивает кожу ушной раковины и барабанную перепонку. Также отомикоз может развиваться в барабанной и послеоперационной полости среднего уха, которая образуется в результате удаления патологически изменённых тканей среднего уха (например, при гнойном среднем отите с холестеатомой ) .
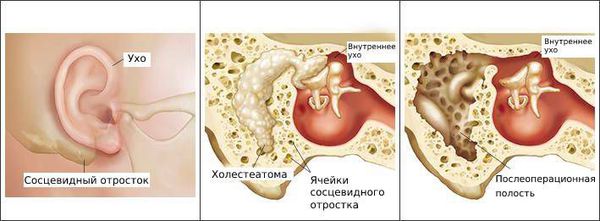
Чаще всего отомикоз начинается с зуда, возможно покалывание в ухе, а в дальнейшем появляются заложенность, ушной шум и выделения [7] .
В группу заболеваний, относящихся к отомикозам, включают [2] [4] :
- Наружный грибковый отит. Затрагивает кожу ушной раковины, стенки наружного слухового прохода и барабанную перепонку.
- Грибковый средний отит. Грибы развиваются в барабанной полости.
- Грибковый мирингит. Грибковое заболевание поражает барабанную перепонку.
- Микоз послеоперационной полости. Процесс развивается в послеоперационной полости среднего уха.
Распространённость
Среди взрослого населения частота развития отомикозов составляет 18,6 %. У детей распространённость заболевания 26,3 % [1] . Чаще всего отомикоз встречается в жарких и влажных климатических зонах, так как влажность и тепло благоприятно влияют на рост грибов. Также существует связь между заболеваемостью и временем года: в весенне-летний период она растёт [10] .
Среди отомикозов самым распространённым является наружный грибковый отит: 62 % от общего числа. Грибковый средний и послеоперационный отит составляют 20 % и 17 %, соответственно. На долю грибкового мирингита приходится 1 % случаев [2] [5] [10] [12] [15] .
Причины и факторы риска развития отомикоза
Причиной развития отомикозов являются грибы, которые входят в состав нормальной микрофлоры уха. В обычных условиях они себя никак не проявляют и не представляют опасности. Но когда появляются благоприятные для грибов условия, они начинают размножаться и приводят к развитию отомикоза. Возбудителями могут стать плесневые грибы рода Aspergillus или дрожжеподобные грибы рода Candida, иногда Mucor, Cladosporium, Alternaria, Penicillium, Geotrichum или Aspergillus и Candida в сочетании друг с другом [4] .
Предрасполагающими факторами, которые могут запускать развитие болезни, являются различные эндогенные (внутренние) и экзогенные (внешние) обстоятельства, а также их сочетания.
Основной экзогенный фактор — это механическая травма кожи наружного слухового прохода при слишком тщательной гигиене ушей с использованием ватных палочек и других подручных средств. Когда пациент слишком тщательно проводит эту процедуру, он не только травмирует кожу, но и удаляет главный фактор защиты — ушную серу. Это приводит к тому, что полезная микрофлора погибает и её место занимают грибы, для размножения которых имеются все условия: тёплая влажная среда и отсутствие защитного барьера — серы [8] .
- Лечение антибиотиками, что приводит к нарушению микрофлоры и размножению грибов.
- Цитостатическая и лучевая терапия, которые обладают иммуносупрессивным действием, т. е. подавляют работу иммунитета.
- Кожные заболевания в виде дерматитов и экземы.
- Длительный приём гормональных препаратов, например глюкокортикостероидов при аутоиммунных заболеваниях.
- Производственные и бытовые вредности: работа во влажных, сырых и пыльных помещениях.
- Гнойные отиты.
- Нарушенный обмен веществ: прежде всего сахарный диабет и гиперкортицизм (повышенное выделение корой надпочечников гормона кортизола), так как они способствуют росту грибов [2][7][11][19] .
- Гипо- и авитаминозы.
- Длительный воспалительный процесс в послеоперационной полости с повреждением эпителия. Образующийся при этом воспалительный экссудат выступает в роли хорошей питательной среды, богатой белками, углеводами, минеральными солями и другими веществами. В совокупности с постоянной температурой, влажностью, свободным доступом воздуха в послеоперационной полости среднего уха появляются благоприятные условия для размножения грибов.
- Послеоперационная травма уха, а также попадание нестерильной воды могут запускать процесс развития микоза послеоперационной полости среднего уха [11] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы отомикоза
Первый симптом отомикоза — зуд внутри уха. Сначала зуд ненавязчивый, возникает периодически и не доставляет сильного дискомфорта. Но потом становится постоянным, нестерпимо сильным и снижает качество жизни пациента [7] [9] [12] . По мере распространения инфекции и прорастания мицелия грибов в кожу возникает повышенная чувствительность и болезненность кожи наружного уха и слухового прохода [2] .
С первых дней заболевания пациенты отмечают появление патологических выделений из уха. Цвет может быть от светло-жёлтого до коричнего-чёрного, консистенция — от жидкой или кашицеобразной до плотной. Возможно образование себорейных корочек [10] .
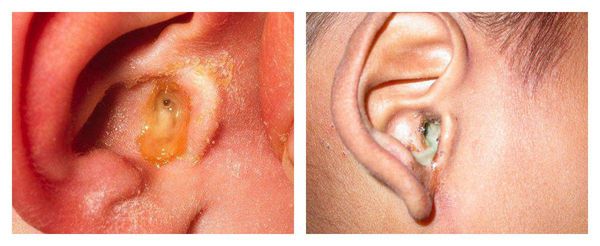
Выделения пациент может заметить на подушке после сна, если они достаточно жидкие и вытекают из наружного слухового прохода. Также их может заметить человек, стоящий рядом.
У некоторых пациентов снижается слух со стороны больного уха. Это возможно при поражении барабанной перепонки и полостей среднего уха, в редких случаях причиной становится повреждение наружного слухового прохода. Иногда отмечают появление шумов в ухе, заложенность, дискомфорт и ощущение полноты внутри уха. Часто имеются неспецифические симптомы, такие как повышение температуры тела и общее недомогание [2] [10] .
Патогенез отомикоза
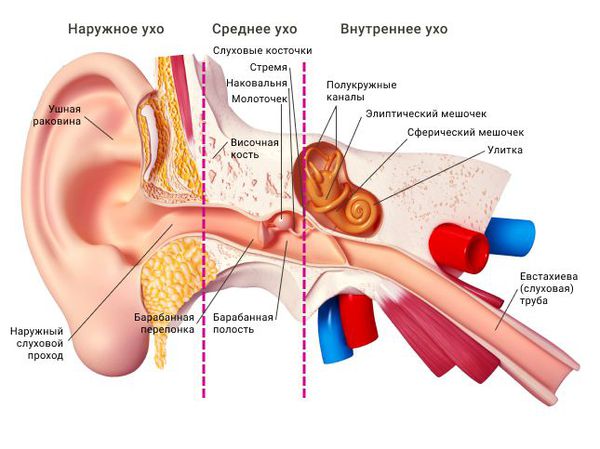
Ушная раковина представляет собой эластический хрящ, покрытый кожей. Полость ушной раковины воронкообразно углубляется и переходит в наружный слуховой проход. Функцией данной структуры является улавливание звуков, их концентрация и направление в наружный слуховой проход.
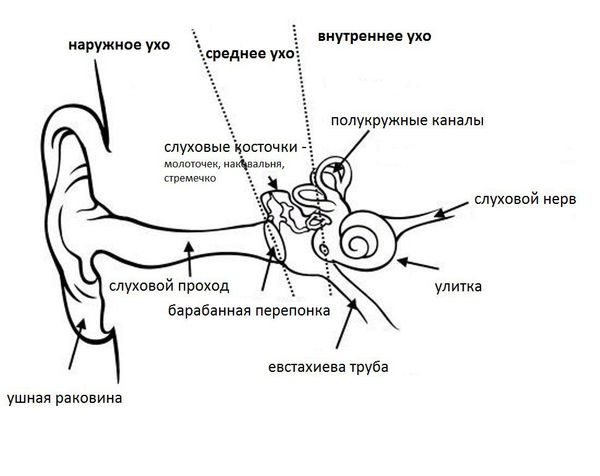
Наружный слуховой проход представляет собой полую трубку диаметром 0,3-1,0 см и длиной около 2,5 см у взрослых. Он состоит из хрящевой части, которая является продолжением хряща ушной раковины, и костной части, занимающей 2/3 наружного слухового прохода. Кожа в наружных отделах слухового прохода содержит волосы, сальные и серные железы [2] .
Барабанная перепонка проводит наружные колебания и является границей, которая отделяет наружное ухо от среднего. Среднее ухо состоит из центральной части, которая представлена барабанной полостью. Кпереди и книзу от барабанной полости находится слуховая труба (евстахиева труба). Кзади от барабанной полости находятся сосцевидные ячейки.
В норме полость среднего уха стерильна, т. е. грибков и других микробов в ней нет. Их попаданию препятствует изоляция от внешней среды за счёт барабанной перепонки, дренажной функции слуховой трубы и местного иммунитета. Тем не менее, грибы могут проникать в среднее ухо через слуховую трубу из глотки либо через систему крово- и лимфообращения.
Основными патогенетическими звеньями возникновения микоза являются адгезия грибов, т. е. прикрепление гриба к коже или раневой поверхности, колонизация гриба и инвазивный рост [7] . При тяжёлой форме микоза может произойти генерализация процесса, т. е. проникновение возбудителя в кровь с распространением по организму и появлением вторичных очагов грибковой инфекции в различных органах и тканях. Микозы могут выступать своеобразными "маркерами" нарушения иммунитета, так как иммунодефицит является одним из основных моментов в патогенезе грибковой инфекции.
Классификация и стадии развития отомикоза
По характеру возбудителя:
- дрожжеподобный — возбудителем выступают дрожжеподобные грибы рода Candida;
- плесневой — выделяют плесневые грибы рода Aspergillus;
- смешанный — присутствует сочетанное поражение грибами родов Aspergillus и Candida.
По локализации:
- наружный грибковый отит — процесс расположен в наружном слуховом проходе;
- грибковый мирингит — при поражении барабанной перепонки;
- грибковый средний отит и грибковый средний послеоперационный отит — при поражении среднего уха;
- сочетанное поражение наружного и среднего уха.
По стороне поражения:
По клиническому течению:
- Острый. Под острым отомикозом понимают впервые выявленный случай грибкового поражения, если речь идёт об острой фазе процесса продолжительностью до 3-4 недель. Пациент при этом жалуется на впервые возникшие симптомы, характерные для этой патологии: зуд в ушах, выделения из слухового прохода, болевой синдром и др.
- Хронический [18] . Этот диагноз пациенту уже ставили ранее и он получал лечение, но спустя какое-то время снова обратился с такими же жалобами. Характерно длительное и вялое течение свыше трёх месяцев с периодами улучшения и повторяющимися обострениями, при которых возобновляются боли в ухе и выделения.
Осложнения отомикоза
- Местное распространение. При вовремя начатом и адекватном лечении осложнения встречаются редко, но при отсутствии лечения отомикоз может приводить к обширному поражению всего слухового прохода, барабанной перепонки и окружающих ухо тканей [2] .
- Генерализация заболевания. Грибковая инфекция опасна тем, что быстро распространяется и угрожает поражением внутренних органов, особенно в послеоперационный период. При неблагоприятном течении отомикоз может являться причиной распространённого микоза внутренних органов и грибкового сепсиса. Такие осложнения возникают достаточно редко, обычно при сопутствующих патологиях: снижении общих иммунных сил организма, ВИЧ, аутоиммунных заболеваниях и т. д.
- Хронизация заболевания. При локализации патологического процесса в среднем ухе часто происходит хронизация процесса, выражающаяся в длительных и многократных обострениях.
- Рубцово-спаечный процесс. В течение времени могут образоваться спайки в полости среднего уха (адгезивный отит). Это будет затруднять нормальное звуковосприятие и приведёт к тугоухости, которая может носить необратимый характер [15] . Также из-за спаек возможно сужение (стеноз) наружного слухового прохода. Однако отомикоз не приводит к полной потере слуха.
Диагностика отомикоза
Опрос, сбор анамнеза
Диагностика начинается со сбора анамнеза. Врач задаёт ряд вопросов:
- Когда началась болезнь и как протекала.
- Был ли у пациента ранее средний отит.
- Было ли грибковое поражение других органов и систем, например урогенитального тракта.
- Как долго пациент болеет, с какой частотой, были ли обострения.
- Принимает ли пациент антибиотики, стероидные препараты, цитостатики (чаще всего используются при лечении онкозаболеваний) и химиотерапевтические препараты.
- Страдает ли пациент аллергией [2][3] .
- Есть ли неблагоприятные факторы в быту и производстве.
- Какими сопутствующими заболеваниями болел пациент.
- Есть ли хронические инфекции [6] .
Осмотр, оценка жалоб
Если речь идёт о кандидозе, пациенты жалуются на беловатые выделения из уха творожистой консистенции. При отоскопии наблюдается сужение слухового прохода в хрящевой части и гиперемия (покраснение) барабанной перепонки [6] [11] .
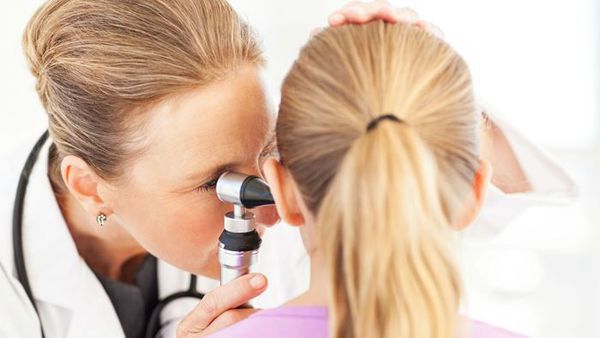
При аспергиллёзном поражении выделения тёмные, почти чёрные, имеют густую консистенцию. При отоскопии наблюдаются сужения в костной части слухового прохода, барабанная перепонка может выпирать и терять свои опознавательные знаки [13] [15] .
При пенициллиозе зуд более выражен, выделения напоминают жидкую ушную серу, хрящевой участок инфильтрирован, на барабанной перепонке может наблюдаться выпячивание, гиперемия или эрозия, что ложно указывает на перфорацию (сквозное повреждение).
Если говорить о поражении микозом среднего уха и послеоперационной полости, то основными жалобами являются снижение слуха, выделения из уха, периодический зуд, также может наблюдаться головокружение [9] .
Как правило, при любой форме грибкового поражения наружного уха слух не страдает или выявляются незначительные нарушения по типу звукопроводимости: ухудшается передача звуковой волны по слуховому проходу к среднему уху. В этом случае возникает ощущение заложенности уха. Такие симптомы, как боль и зуд, могут наблюдаться при любом типе грибкового поражения [3] [6] [20] .
Некоторые пациенты в остром периоде обращаются с жалобами на головную боль на стороне поражения, повышение температуры тела до 38 °C , гиперчувствительность ушной раковины, наружного слухового прохода и заушной области [6] .
Лабораторная диагностика
Из лабораторных методов исследования основным является взятие мазка из уха и его микологический посев на специальные питательные среды (Сабуро, Чапека и др.). Специалист берёт образцы с помощью аттикового зонда ATIC или ложки Фолькмана. Материал берётся под контролем зрения, чтобы не повредить барабанную перепонку, поскольку субстрат собирается из глубоких отделов слухового прохода [12] .
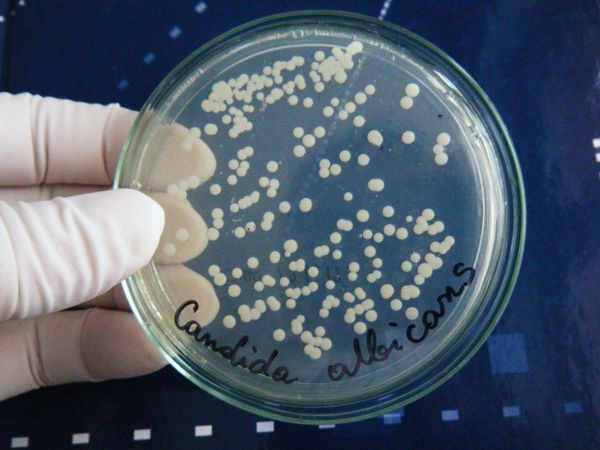
Помимо микологического посева собранного материала, проводится его микроскопия с использованием 10 % гидроксида калия, если это нативный материал. Иногда проводится окрашивание по Романовскому — Гимза. Эти 2 исследования вместе позволяют точно определить возбудителя процесса. Для диагностики микоза титр культуры (количество в 1 мл) должен быть не менее 10 4 КОЕ/мл.
Также проводится ряд общеклинических исследований, таких как клинический и биохимический анализы крови с определением уровня глюкозы, общего белка, АсАТ (аспартатаминотрансферазы), АлАТ (аланинаминотрансферазы) и креатинина. Выполняется анализ крови на сифилис, ВИЧ-инфекцию и гепатиты В и С с целью исключить эти заболевания и выявить сопутствующие патологии [9] .
Инструментальная диагностика
Из инструментальных методов исследования следует выделить отомикроскопию больного уха с использованием бинокулярных линз, микроскопической оптики или с помощью эндоскопа [12] [15] .
Дифференциальный диагноз
Дифференциальный диагноз необходимо проводить с воспалительными процессами наружного и среднего уха негрибовой этиологии (например, с бактериальным или вирусным средним и наружным отитом), с серными пробками и новообразованиями уха, такими как холестеатома.
Окончательный диагноз отомикоза может быть поставлен только при комплексном микологическом исследовании [9] [11] .
Лечение отомикоза
При выборе терапии врач учитывает эффективность ранее проведённого лечения, если оно имелось. Если у пациента есть хронические заболевания, то в первую очередь необходима их коррекция [2] . Например, при сахарном диабете важно контролировать уровень глюкозы, так как его повышение провоцирует развитие отомикоза [3] .
Лечение инфекции начинается с устранения возбудителя, при этом используется сочетание местных лекарственных форм и препаратов системного действия. Перед применением препаратов важно тщательно очистить ухо от патологических выделений, ведь даже небольшое количество грибковых масс может негативно сказаться на эффективности медикаментозной терапии [18] .
Если при отоскопии наблюдаются полипы или грануляции в слуховом проходе, то предварительно нужно обработать их 5-10 % раствором нитрата серебра и удалить [7] [15] .
Местное лечение
Препаратом выбора для местного лечения является хлорнитрофенол и 1 % раствор нафтифина. Препараты используются в качестве аппликаций на коже наружного слухового прохода в течение 10-14 дней. Лечение необходимо продолжать ещё 14 дней после исчезновения клинических признаков и/или до получения трёхкратного отрицательного лабораторного анализа [12] [17] [18] .
Если при микологическом посеве выделены грибы Candida, то назначаются аппликации комбинацией препаратов: 1 % раствор клотримазола и 1 % раствор нафтифина в течение 10-14 дней с продолжением терапии в течение 14 дней после исчезновения клинических признаков и/или до получения трёхкратного отрицательного результата лабораторного исследования [3] [18] .
Системное лечение
Если возбудителем являются грибы рода Candida, рекомендуется назначать флуконазол. При лечении грибкового среднего отита и микоза послеоперационной полости среднего уха, вызванного плесневыми грибами, применяется итраконазол [18] .
В период лечения и реабилитации пациенту необходимо ограничить контакт с источниками пыли и грязи, избегать повышенной влажности и попадания воды в ухо, чтобы не допустить рецидивов и возможных осложнений [7] .
Прогноз. Профилактика
Прогноз при впервые выявленном неосложнённом наружном грибковом отите благоприятный. Если лечение было своевременным и грамотным, то удаётся полностью уничтожить возбудителя.
При хроническом течении избавиться от грибка полностью сложно, поэтому случаются рецидивы. Из-за спаечных процессов возможно снижение слуха по типу звукопроведения. Чтобы избежать рецидивов, необходимо в течение 4 недель после клинического выздоровления аккуратно протирать кожу наружного уха противогрибковым средством или делать аппликации турундой, стараясь не травмировать кожу слухового прохода.
В качестве неспецифических методов профилактики можно рекомендовать соблюдение правил личной гигиены:
- тщательно и часто мыть руки;
- не трогать кожу ушей грязными руками и предметами;
- пользоваться только личным полотенцем;
- при любых заболеваниях уха проводить тщательный его туалет.
В осенне-зимний период особенно важно укреплять защитные силы организма и повышать иммунитет, избегать переохлаждений и заветриваний ушей. Если имеется сахарный диабет, необходима коррекция уровня глюкозы крови [6] [15] .
Читайте также:

