Гематогенный путь распространения инфекции что это
Обновлено: 13.05.2024
Причины и механизмы развития внутричерепных осложнений среднего отита
а) Факторы, влияющие на развитие осложнений. Внутричерепные осложнения возникают в результате многих факторов, часто действующих одновременно, вызывая распространение инфекции из уха в полость черепа. В общем, внутричерепные осложнения возникают, когда ушная инфекция является либо неконтролируемой, либо контролируется недостаточно.
Тенденция распространения инфекции из среднего уха за его пределы и за пределы смежных полостей зависит от ряда факторов, в том числе от вирулентности возбудителя и его чувствительности к антибиотикам, от резистентности организма, адекватности антибиотикотерапии, анатомических путей и препятствий для распространения, а также дренирования пневматических пространств, как природных, так и хирургических.
Микробиология инфекции среднего уха остается относительно постоянной в течение долгого времени. Наиболее острые инфекции вызывают Streptococcus pneumoniae, Haemophilus influenzae и Moraxella catarrhalis. По мере введения новых антибиотиков устойчивость к ним меняется и довольно значительно.
Микробиология хронической инфекции отличается от острого процесса. Такие организмы, как синегнойная палочка, встречаются гораздо чаще. Лечение синегнойной инфекции требует более высокой дозировки нерегулярно используемых антибиотиков. Доброкачественный тип хронической отореи со слизистыми выделениями из центральной перфорации сам по себе не поражает кость и не вызывает осложнения.
Тем не менее, ничто не мешает новому вирулентному микроорганизму проникнуть в такое ухо и вызывать обострение и осложнение по тому же механизму, что и в любом случае острого среднего отита. К сожалению, новый микроорганизм, вероятно, выводит значительную устойчивость к антибиотикам, так как пациент, скорее всего, получал лечение по поводу отореи.
Иммунокомпрометированные пациенты подвергаются риску развития не только среднего отита, но и его осложнений. Микроорганизмы, вызывающие инфекцию, чаще всего являются атипичными возбудителями. Отдельные лица могут принимать иммуносуппрессорные препараты, которые ослабляют иммунитет и делают их восприимчивыми к инфекции, или, возможно, имеют синдром приобретенного иммунодефицита (СПИД).
Внутричерепное распространение острого среднего отита происходит несколько чаще в плохо пневматизированных височных костях, чем в хорошо пневматизированных, даже если в анамнезе имелись случаи острого среднего отита. Вероятность осложнений, возникающих вследствие хронической инфекции среднего уха, зависит от патологического поражения, вызванного хронической отореей. Полость среднего уха имеет костные барьеры, которые препятствуют распространению инфекции из среднего уха в полость черепа.
Однако эти барьеры могут быть повреждены предшествующей инфекцией, грануляционной тканью, или холестеатомой, что позволяет инфекции распространяться в полость черепа из среднего уха. Травма с переломом также может создать пути, позволяющие инфекции обойти эту естественную защиту.
Естественный дренаж полостей сосцевидного отростка (примерно 5 см 3 в объеме) осуществляется в относительно меньшее пространство — в полость среднего уха (объемом около 0,9 см 3 ), а затем через слуховую трубу. Дренаж может быть недостаточным, что позволяет инфицированными выделениями накапливаться, а затем через поражение полости среднего уха распространяться интракраниально.
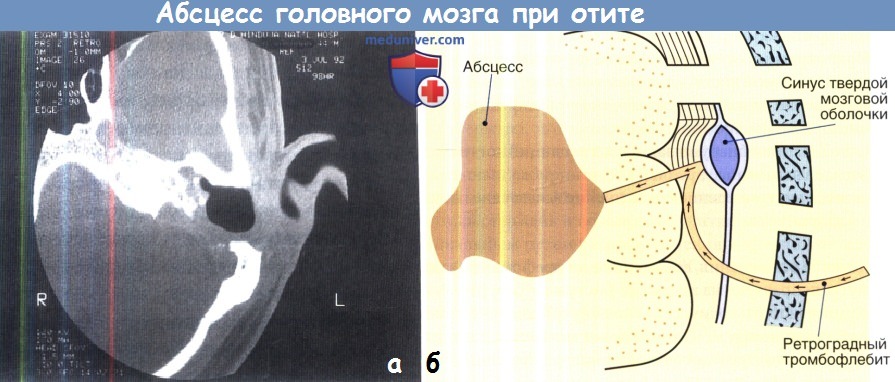
(А) Компьютерная томография височной кости, осевая проекция.
Визуализируется значительная эрозия височной кости и формируется высокая вероятность внутричерепного осложнения.
(Б) Схема развития абсцесса головного мозга вследствие среднего отита.
Развитие инфекции может происходить путем прямого распространения или ретроградного тромбофлебита.
б) Пути распространения при развитии гнойных осложнений. Как указано выше, инфекция распространяется за пределы уха, потому что она может быть неконтролируема или контролируется плохо. Инфекция из полости среднего уха может проникать в полость черепа любым из трех описанных ниже путей.
1. Разрушение кости. Экспансия путем разрушения кости является наиболее частым путем распространения и приводит к осложнениям в случаях острого среднего отита в хорошо пневматизированных височных костях, и почти всегда является путем распространения в случаях хронического гнойного среднего отита. При остром среднем отите разрушение кости является результатом мастоидита. При хроническом среднем отите эрозия кости обычно вызывается холестеатомой, реже хроническим остеомиелитом.
Процесс разрушения кости начинается с вовлечения соседних мягких тканей. Защитные грануляции формируют последний оборонительный рубеж. Затем, после некоторого периода времени, зависящего от вирулентности организма, гной под давлением проникает в стенку защитных грануляций путем некроза. Разрушение кости как путь распространения может быть распознан по следующим признакам:
• Осложнение возникает через несколько недель или более после случая острого среднего отита или при хроническом среднем отите большой продолжительности.
• Диффузному вовлечению часто предшествует продромальный период частичного вовлечения костной структуры. Таким образом, мягкая, интермиттирующая слабость лицевых мышц может предшествовать полному параличу лицевого нерва, рецидивирующее слабое головокружение — диффузному гнойному лабиринтиту, а очаговый менингизм — диффузному гнойному менингиту.
• При операции расхождение краев костного барьера находится между гнойным очагом и соседней структурой. Слой грануляций охватывает открытые мягкие ткани соседней структуры.
• Лечение эрозии кости направлено на осложнение и всегда включает в себя хирургическое удаление гнойного, костно-деструктивного очага в височной кости. Если пренебречь таким вмешательством, осложнение, скорее всего, повторится.
2. Прямое распространение по преформированному пути. Распространение по преформированному пути может произойти либо при обострении хронического среднего отита либо при остром среднем отите. Преформированный путь может являться нормальным анатомическим отверстием в костной стенке, например, овальное или круглое окно, внутренний слуховой проход, водопровод улитки или эндолимфатические проток и мешок.
Путь может представлять собой врожденную дегисценцию, например, шов или расхождение нижней стенки гипотимпанума над луковицей яремной вены. Преформированный путь может сформироваться в результате перелома черепа или предыдущей операции. В качестве пути также может служить перилимфатический свищ, врожденный или приобретенный. Иногда предшествующий средний отит с мастоидитом заживает, но оставляет полоску рубцовой ткани.
Эта полоска является преформированным путем для последующих инфекций. Распространение по преформированному пути не всегда легко диагностируется до операции. Диагноз можно предположить по следующим признакам:
• Неоднократные случаи менингита, перелом черепа, операции на височной кости, или пролеченный отит в анамнезе.
• Осложнение возникает в начале острой инфекции, напоминая развитие тромбофлебита.
• При операции обнаруживаются дегисценции костного барьера, не вызванные эрозией кости.
• Имеется внутричерепное осложнение вследствие гнойного лабиринтита.
Лечение осложнения, возникшего по преформированному пути, направлено на закрытие фистулы и хирургической эвакуации любого количества гноя внутри височной кости. В качестве примера можно привести менингит, развивающийся через внутренний слуховой проход при гнойном лабиринтите; лабиринт должен быть дренирован в то же время, проведения антибактериального лечения менингита.
3. Тромбофлебит. В 1902 году Кернер продемонстрировал возможность проникновения инфекции через слизистую оболочку среднего уха и сосцевидного отростка, а также через неповрежденную кость на фоне прогрессивного тромбофлебита небольших венул. Этот способ распространения может наблюдаться при острых инфекциях среднего уха или обострении хронической инфекции.
Инфекция распространяется по венам, смежным с инфицированными пневматизированными пространствами височной кости или ранее тромбированным венозным синусом твердой мозговой оболочки. Существует богатая сеть вен в височной кости, напрямую связанная с ней, и эта сеть, в свою очередь, находится в прямой связи с экстракраниальными, внутричерепными и черепными диплоическими венами. Экстракраниальные вены тесно связаны с артериальным руслом височной кости.
Экстракраниальные и внутричерепные венозные системы соединяются эмиссарными сосцевидными венами, впадающими в сигмовидный синус, отводя кровь в верхний и нижний каменистые синусы. Все венозные синусы твердой мозговой оболочки взаимосвязаны. Таким образом, тромбоз сигмовидного синуса может привести к тромбофлебиту других пазух.
Осложнение, вызванное тромбофлебитом, может быть распознано по следующим признакам:
• Осложнение возникает в начале острой инфекции, иногда в течение первых двух дней, но обычно в течение первых 10 дней.
• При некоторых осложнениях, таких как гнойный менингит, отсутствует продромальный период начинающейся инвазии с очаговым менингитом, обычно называемым менингизмом, как это наблюдается при эрозии кости.
• При операции костные стенки среднего уха и клеток сосцевидного отростка интактны. Кость и мукопериост, покрывающий клетки сосцевидного отростка, могут быть воспалены и легко кровоточат, но нет слитого абсцесса, и кость не повреждена.
• Гематогенный путь распространения инфекции, как правило, приводит к менингиту. В то время как венозный тромбофлебит обычно ведет к абсцессам мозжечка, артериальное распространение приводит к абсцессам височной доли и диффузной септицемии.
в) Специфические внутричерепные осложнения среднего отита. Довольно редко внутричерепное осложнение может возникать без первичного поражения височной кости. Общие симптомы грозящего внутричерепного осложнения заключаются в следующем:
• Стойкая оторея. Выделения из уха зловонные и становятся более вязкими. Гной густой и сливкообразный может иметь примесь крови. При угрожающем внутричерепном осложнении, выделения становятся скудными, что свидетельствует о плохом дренаже.
• Высокая лихорадка, измененная чувствительность, токсикоз, светобоязнь, и раздражительность являются признаками надвигающегося внутричерепного осложнения.
• Ригидность затылочных мышц и общее недомогание — признаки того, что микроорганизмы достигли спинномозговой жидкости (ликвора).
При этих осложнениях основные принципы хирургии уха неизменны:
• Ликвидация поражения
• Создание адекватного дренажа для накопленного содержимого
Борьба с заболеванием требует тщательной и полной мастоидэктомии. Все пораженные воздухоносные ячейки вскрываются. Везде, где встречается гной, он дренируется. Все пораженные или мертвые ткани удаляются. Создание адекватного дренажа обычно требует выполнения радикальной операции, с исключениями в определенных ситуациях. При наличии острого среднего отита, вызвавшего менингит, для обеспечения адекватного дренажа обычно достаточно антибиотикотерапии и миринготомии с установкой тимпаностомической трубки. При наличии упорного течения заболевания и холестеатомы, большинство авторов рекомендуют выполнение радикальной операции.
Не менее важна восстановительная операция на канале. Широкая полость дает возможность адекватного дренажа и позволяет легко осматривать и очищать мастоидальную полость.
Ниже определяется и обсуждается каждый диагноз внутричерепного заболевания. Диагнозы представлены в порядке убывания частоты. Менингит является наиболее распространенным осложнением в этой группе диагнозов в большинстве традиционных статей. Следующими по распространенности осложнениями являются абсцесс головного мозга и тромбоз латерального синуса. Наконец, рассмотрены другие состояния, в том числе отогенная гидроцефалия, субдуральный и эпидуральный абсцессы. Изложены патофизиология, в том числе микробиология, различные симптомы, специфические методы диагностики и лечения.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Пути инфицирования позвоночника. Классификация инфекций позвоночника
а) Вопросы лучевой диагностики с позиций анатомии. Возбудители инфекционных заболеваний могут проникать в органы и ткани человека различными путями, в т.ч. путем прямого контакта, лимфогенным путем, гематогенным путем или с током спинномозговой жидкости Контактный путь, как говорит само его название, предполагает прямое соприкосновение кости или мягких тканей с источником инфекции с развитием абсцесса мягких тканей или остеомиелита.
Если вести речь о позвоночнике, то такой путь инфицирования можно видеть, например, при развитии спондилита в области глубокого пролежня. Инфекционное поражение межпозвонкового диска может распространяться на окружающие паравертебральные мягкие ткани и приводить к формированию абсцессов поясничных мышц. Контактный путь также является механизмом развития эпидуральных абсцессов, расположенных краниальней или каудальней уровня поражения межпозвонкового диска. Этот путь инфицирования имеет место и при развитии интрамедуллярных абсцессов спинного мозга, при которых возбудитель проникает в спинной мозг через эпителиальный ход и дефект в задних элементах позвонка.
Лимфогенный путь имеет ограниченное значение, поскольку при инфекционных поражениях позвоночника намного чаще мы видим контактный или гематогенный пути инфицирования. Лимфогенный путь может быть актуален, например, при поражении забрюшинных лимфоузлов при первичных злокачественных новообразованиях брюшной полости и таза.
б) Гематогенный путь инфицирования. Гематогенный путь является одним из самых главных механизмов развития инфекционных поражений костей аксиального скелета. При этом вопрос о том, какой именно гематогенный путь (артериальный или венозный) имеет большее значение, остается спорным. Артериальный путь распространения инфекции в отношении позвоночника традиционно считается более актуальным. В телах позвонков существуют области, с физиологической точки зрения очень похожие на метафизы длинных трубчатых костей. Области эти расположены вблизи передней продольной связки и характеризуются наличием разветвленной сети конечных артериол, которая делает их восприимчивыми к развитию инфекционного процесса.
Дистальные сосуды в этих областях характеризуются отсутствием сети анастомозов и медленным кровотоком, тромбоз их ведет к аваскулярному некрозу кости. Сегментарные артерии обычно кровоснабжают тела двух смежных позвонков и расположенный между ними диск, в связи с чем и картина инфекционного поражения позвоночника бывает достаточно типична. Венозный путь инфицирования традиционно реализуется через сплетение Батсона, представляющее собой продольно ориентированную сеть бесклапанных вен, расположенных параллельно позвоночному столбу. Вены эти располагаются за пределами брюшной или плевральных полостей. Сплетение Батсона сообщается с различными другими венозными системами, в т. ч. с полой веной, системой воротной вены, системой непарной вены, межреберными венами, легочными и почечными венами.
Направление тока крови в сплетении меняется в зависимости от градиента давления в грудной и брюшной полостях. Аналогичную функцию на уровне шейного отдела позвоночника выполняет глоточно-позвоночное сплетение. Непрерывность ликворных пространств полости черепа и дурального мешка обеспечивает возможность прямого распространения возбудителей инфекций или метастазов опухолей стоком ликвора. Внутричерепные новообразования таким образом могут давать отсевы с развитием метастазов в шейном, грудном или поясничном отделах дурального мешка. Точно также новообразования, расположенные в самых дистальных отделах дурального мешка, могут метастазировать с током ликвора в полость черепа.
(Слева) На схеме сагиттального среза показаны признаки инфекционного поражения поясничного межпозвонкового диска с распространением процесса на тела позвонков с развитием спондилита, деструкцией замыкательных пластинок и отеком костного мозга. Отражено формирование дорзального и вентрального абсцессов.
(Справа) Сагиттальный срез, Т1-ВИ FS с КУ, пациент со спондилодисцитом: контрастное усиление сигнала тел L5 и S1 позвонков и межпозвонкового диска, флегмонозные изменения превертебральных и эпидуральных тканей. (Слева) Аксиальный срез, Т1-ВИ с КУ, пациент со спондилодисцитом: распространение инфекционного процесса в превертебральные ткани, поясничные мышцы и дорзальные мышцы позвоночника. Флегмона проникает в вентральный отдел эпидурального пространства и вызывает сдавление дурального мешка.
(Справа) Аксиальный срез, Т2-ВИ FS: распространение воспалительного процесса в превертебральное пространство, на поясничные мышцы и дорзальные мышцы позвоночника. (Слева) Аксиальный срез, Т1-ВИ с КУ: случай диссеминированного кокцидиомикоза с диффузным поражением костной и мягких тканей, распространением процесса в паравертебральные ткани и легкое.
(Справа) Сагиттальный срез, Т2-ВИ: пациенте кокцидиомикозом: массивные паравертебральные абсцессы. Дуральный мешок в спинномозговом канале деформирован за счет пора -жения межпозвонкового диска и тел позвонков.
в) Патологическая лучевая анатомия. Варианты инфекционного поражения позвоночника можно разделить на инфекцию межтелового пространства/остеомиелит позвонков, субдуральную эмпиему, менингит, интрамедуллярный абсцесс спинного мозга и септический артрит/поражение дугоотростчатых суставов. Инфекция межтелового пространства характеризуется типичной картиной снижения интенсивности сигнала в Т1 -режиме в области соответствующего межпозвонкового диска, распространяющейся на смежные замыкательные пластинки. Типичной характеристикой является неровность контура замыкательных пластинок. В Т2-режиме характерна гиперинтенсивность сигнала межпозвонкового диска, не повторяющая анатомию диска и распространяющаяся на смежные тела позвонков. При контрастировании наблюдается неравномерное усиление сигнала межпозвонкового диска и диффузное усиление, распространяющееся на пораженные тела позвонков.
Важным аспектом инфекционного поражения позвоночника является распространение процесса на паравертебральные ткани, признаки чего будут видны в режимах подавления сигнала жировой ткани, постконтрастныхЛ -ВИ, на которых мы ищем признаки контрастного усиления сигнала паравертебральных тканей и поясничных мышц, или Т2-ВИ, характеризующихся усилением Т2-сигнала соответствующих анатомических образований. В протоколе исследования важно описать не только уровень поражения, но также признаки нестабильности или изменения анатомии позвоночника, если таковые имеют место, признаки распространения инфекционного процесса на паравертебральные ткани, эпидуральное пространство и поясничные мышцы.
г) Эпидуральный абсцесс и менингит. Изолированные эпидуральные абсцессы могут возникать и в отсутствии сопутствующей инфекции межпозвонкового диска, а также могут быть связаны с постоянной катетеризацией эпидурального пространства или перенесенным стабилизирующим вмешательством на позвоночнике. Изредка эпидуральный абсцесс может быть следствием гематогенного заноса инфекции. Менингит обычно проявляется на постконтрастных Т1 -ВИ как линейное усиление сигнала вдоль мягкой мозговой оболочки спинного мозга или корешков конского хвоста. При грибковых инфекциях наблюдается узелковый характер усиления сигнала, что напоминает картину метастатического поражения. Субдуральная эмпиема позвоночника встречается редко и может развиваться при тяжелом течении инфекционного процесса межпозвонкового диска с его распространением на эпидуральное пространство. Эмпиема является результатом в первую очередь прямого распространения процесса через твердую мозговую оболочку в субдуральное пространство.
Интрамедуллярные абсцессы спинного мозга встречаются редко и могут возникать как вследствие гематогенного, так и прямого распространения инфекции. У взрослых более типичным механизмом является контактный путь, у детей-также контактный путь через функционирующий эпителиальный ход. Септический артрит/поражение дугоотростчатых суставов может развиваться как вследствие гематогенного, так и контактного распространения инфекции. Ранние стадии инфекционного поражения могут характеризоваться лишь некоторым усилением интенсивности Т2-сигнала субхондральных участков суставных отростков в сочетании с выпотом в полость суставов.
д) Особенности течения инфекционного процесса у взрослых и детей. В силу анатомических особенностей пути распространения инфекции у взрослых и детей отличаются друг от друга. У взрослых в первую очередь поражаются замыкательные пластинки, затем процесс распространяется на межпозвонковый диск, смежные участки тел позвонков, паравертебральные ткани и эпидуральное пространство. У детей через толщу ростковой зоны проходят сосуды, за счет которых первичный очаг инфекционного поражения развивается в межпозвонковом диске с последующим вторичным распространением в тело позвонка. Наиболее частой локализацией инфекции межпозвонкового диска является поясничный отдел позвоночника, за которым следует грудной и шейный отделы. Факторы риска развития инфекции многочисленны и включают возраст старше 50 лет, сахарный диабет, ревматоидный артрит, СПИД, прием глюкокортикоидов, инородные тела мочевыводящих путей, перенесенную травму позвоночника и параплегию. Наиболее распространенной этиологической причиной инфекции является Staphylococcus aureus.
У лиц, употребляющих внутривенные наркотики, возбудителем могут бактерии рода Pseudomonas. Для пациентов с серповидноклеточной анемией классикой считаются поражения, вызванные бактериями рода Salmonella, однако и у них наиболее распространенными остаются стафилококковые поражения.
е) Классификация. Классификация инфекционных поражений костей подразделяет эти поражения на четыре анатомических типа заболевания и три вида ответа организма-хозяина и включает, таким образом, 12 клинических стадий заболевания. Четыре анатомических типа: (1) ранний гематогенный или медуллярный остеомиелит, (2) поверхностный остеомиелит (контактное инфицирование), (3) локальная или полнослойная секвестрация и (4) диффузный остеомиелит. Классификация ответа организма: (А) нормальный физиологический ответ, (В) локальный или системный патологический ответ и (С) лечение остеомиелита будет более тяжелым, чем лечение собственно инфекции.
Классификация туберкулеза позвоночника Mehta (2001) подразделяет заболевания на четыре группы: (1) стабильное поражение передней колонны без кифотической деформации, при котором показан передний дебридмент и костная пластика опорным трансплантатом, (2) тотальное поражение с кифотической деформацией и нестабильностью, показана задняя стабилизация и передняя костная пластика опорным костным трансплантатом, (3) пациенты высокого риска трансторакальных вмешательств, которым показана задняя декомпрессия и стабилизация, (4) изолированные задние поражения, при которых показана задняя декомпрессия.
ж) Клинические вопросы. Инфекционные поражения позвоночника составляют 2-5% всех остеомиелитов. Наиболее распространенным симптомом является боль в спине. Болевой синдром прогрессирует, развиваясь постепенно, он становится постоянным, не уменьшаясь даже в состоянии покоя. Температурная реакция вариабельна и присутствует в
Интрамедуллярные абсцессы оканчиваются фатально в 8% случаев, более, чем у 70% этих пациентов остается стойкий неврологический дефицит. Более, чем у 90% пациентов отмечается повышение СОЭ. Также повышается и уровень С-реактивного белка. Бактериологическое исследование крови оказывается положительным у 25-60% пациентов с остеомиелитом позвоночника.
Показания к хирургической санации очага и спондилодезу при инфекционном поражении позвоночника включают необходимость забора материала для бактериологического исследования, дренирование абсцесса, сохраняющийся неврологический дефицит, деформацию и нестабильность позвоночника, и неэффективность консервативного лечения. Первой линий терапии при условии отсутствия острого или прогрессирующего неврологического дефицита остается продленная внутривенная антибактериальная терапия. Курс внутривенной терапии антибиотиками обычно продолжается 6 недель, по завершении антибактериальная терапия может быть продолжена перорально. Может быть показана наружная иммобилизация позвоночника. Рецидивы инфекции проявляются рецидивирующими эпизодами бактериемии, формированием паравертебральных абсцессов и хронических функционирующих свищей. Наиболее распространенным и благоприятным исходом консервативного лечения является формирование спонтанного костного блока пораженных позвонков.
(Слева) На схеме сагиттального среза показаны эпителиальный ход, соединяющий поверхность кожи с конусом спинного мозга, абсцесс конуса спинного мозга и распространенный отек спинного мозга.
(Справа) Сагиттальный срез, Т2-ВИ: пациент с абсцессом шейного отдела спинного мозга и стрептококковым эндокардитом отмечается диффузное расширение спинного мозга с формированием на уровне С4-С6 в его толще кольцевидной зоны низкоинтенсивного сигнала (капсула абсцесса). (Слева) Сагиттальный срез, Т1-ВИ с КУ и подавлением сигнала жировой ткани: распространенная субдуральная эмпиема с периферическим контрастным усилением сигнала на протяжении всего шейного отдела позвоночника и распространением вдоль поверхности ската.
(Справа) Случай септического артрита дугоотростчатого сустава. Аксиальный срез, Т1-ВИ с КУ на уровне L4-L5: распространение инфекционного процесса на правый дугоотростчатый сустав с диффузным усилением сигнала суставных отростков и поражением околосуставных мягких тканей. (Слева) Аксиальный срез Т1-ВИ с КУ: признаки прямого распространения инфекционного процесса (аневризма аорты на фоне грибкового поражения) от аорты в тело позвонка с формированием зоны деструкции и развитием спондилита. Инфекция также напрямую распространяется на поясничную мышцу.
(Справа) Аксиальный срез с КУ: признаки прямого распространения инфекционного процесса (аневризма аорты на фоне грибкового поражения) от аорты в тело позвонка и на левую поясничную мышцу.
з) Дифференциальный диагноз. Первичным методом диагностики эпидуральных абсцессов является МРТ, чувствительность которой в отношении диагностики инфекционного поражения эпидурального пространства аналогична КТ-миелографии, однако она в то же время позволяет исключить другую патологию, например, грыжу диска, кисту, опухоль и инфаркт спинного мозга. МР-картина эпидурального абсцесса включает мягкотканное образование эпидурального пространства с конусовидными краями, оттесняющее дуральный мешок и спинной мозг. В Т1 -режиме абсцесс характеризуется изоинтенсивностью сигнала, в Т2-режиме — усилением сигнала.
Для полноценного трактования наблюдаемых изменений как признаков эпидурального абсцесса необходимо исследование с контрастированием. Картина контрастного усиления при эпидуральном абсцессе включает: (1) диффузное и гомогенное усиление, (2) неоднородное усиление и (3) тонкий ободок периферического усиления сигнала. Контрастирование является очень полезным дополнительным инструментом исследования, позволяющим оценить протяженность поражения в случаях, когда стандартные режимы МР-томографии оказываются недостаточно информативными. Контрастное усиление сигнала свидетельствует об активности инфекционного процесса и позволяет рационально ограничить зону интереса для последующей игольной биопсии или хирургического вмешательства. Эффективное медикаментозное лечение должно приводить к прогрессирующему снижению выраженности контрастного усиления сигнала паравертебральных мягких тканей, дисков и тел позвонков. На ранних стадиях развития инфекционного процесса, когда межпозвонковые диски еще интактны, только с использованием МРТ инфекционный процесс сложно дифференцировать с опухолевым поражением, дегенеративными изменениями замыкательных пластинок I типа или компрессионным переломом.
Для окончательного определения природы наблюдаемых изменений необходимо исследование в динамике.
Boden et al. предположили, что признаком инфекции позвоночника в послеоперационном периоде будеттриада из контрастного усиления сигнала межпозвонкового диска, контрастного усиления сигнала фиброзного кольца и контрастного усиления сигнала костного мозга позвонков в сочетании с соответствующими лабораторными изменениями, например, увеличением СОЭ. Однако бывают пациенты с неосложненным течением послеоперационного периода и признаками контрастного усиления сигнала фиброзного кольца (в зоне вмешательства), межпозвонкового диска и замыкательных пластинок и без признаков инфекционного поражения. В послеоперационном периоде в норме контрастное усиление сигнала межпозвонкового диска обычно определяется в виде тонких полос, параллельных смежным замыкательным пластинкам, а усиление сигнала костного мозга тел позвонков связано с дегенеративными изменениями замыкательных пластинок I типа.
Подобную МР-картину следует отличать от аморфного усиления сигнала межпозвонкового диска при инфекционном поражении.
и) Список использованной литературы:
1. Duarte RM et al: Spinal infection: state of the art and management algorithm. Eur Spine J. 22(12):2787-99, 2013
2. Malghem J et al: Necrotizing fasciitis: Contribution and limitations of diagnostic imaging. Joint Bone Spine. 80(2): 146-54, 2013
3. Go JL et al: Spine infections. Neuroimaging Clin N Am. 22(4):755-72, 2012
4. DeSanto J et al: Spine infection/inflammation. Radiol Clin North Am. 49(1):105-27,2011
5. Celik AD et al: Spondylodiscitis due to an emergent fungal pathogen: Blastoschizomyces capitatus, a case report and review of the literature. Rheumatol Int. 29(10):1237-41,2009
6. Hong SH et al: MR imaging assessment of the spine: infection or an imitation? Radiographics. 29(2):599-612, 2009
7. Karikari IO et al: Management of a spontaneous spinal epidural abscess: a single-center 10-year experience. Neurosurgery. 65(5):919-23; discussion 923-4, 2009
8. Mylona E et al: Pyogenic vertebral osteomyelitis: a systematic review of clinical characteristics. Semin Arthritis Rheum. 39(1): 10-7, 2009
9. Petruzzi N et al: Recent trends in soft-tissue infection imaging. Semin Nucl Med. 39(2): 115-23, 2009
10. Posacioglu H et al: Rupture of a nonaneurysmal abdominal aorta due to spondylitis. Tex Heart Inst J. 36(1):65-8, 2009
11. Sobottke R et al: Treatment of spondylodiscitis in human immunodeficiency virus-infected patients: a comparison of conservative and operative therapy. Spine (Phila Pa 1976). 34(13):E452-8, 2009
12. Thwaites G et al: British Infection Society guidelines for the diagnosis and treatment of tuberculosis of the central nervous system in adults and children. J Infect. 59(3):167-87, 2009
13. Dai LY et al: Anterior instrumentation for the treatment of pyogenic vertebral osteomyelitis of thoracic and lumbar spine. EurSpineJ. 17(8):1027-34, 2008
14. Mehta JS et al: Tuberculosis of the thoracic spine. A classification based on the selection of surgical strategies. J Bone Joint Surg Br. 83(6):859-63, 2001
15. Mader JT et al: Staging and staging application in osteomyelitis. Clin Infect Dis. 25(6):1303-9, 1997
16. Boden SD et al: Postoperative diskitis: distinguishing early MR imaging findings from normal postoperative disk space changes. Radiology. 184(3):765-71, 1992
8.3. ПУТИ РАСПРОСТРАНЕНИЯ ИНФЕКЦИИ
В зарубежной и отечественной литературе описано пять основных пу-тей проникновения возбудителей инфекции в организм плода (Анкирская А.С., 1985; Радзинский В. Е, 1992; Кира Е.Ф., 1996; Левицкая С. К., 1991):
1) восходящий (через шейку матки и оболочки плодного яйца);
2) трансплацентарный, или гематогенный (через плацентарный барьер к плоду);
3) нисходящий (из воспалительно измененных придатков матки, аппен-дикса);
4) интранатальный (при прохождении плода через инфицированные ро-довые пути матери);
Антенатально инфекционный агент попадает к плоду гематогенно (трансплацентарно) или через инфицированные околоплодные воды. Чаще при антенатальном заражении возбудители поступают в организм плода ге-матогенно. Вначале они с кровью матери поступают в плаценту, где возмож-но размножение возбудителя и последующее развитие воспалительного про-цесса (плацентита). Преодолев маточно-плацентарный барьер, возбудитель проникает к плоду и может привести к развитию генерализованной инфекции с поражением печени, легких, почек, головного мозга и других органов (Ан-кирская А.С., 1989; Айламазян Э.К., 1995; Есаулова Н.Е., 1996; Сидельникова В.М., 1996; Сидорова И.С., 1999; Михайлов А.В., Лаврова Д.Б., Коляченко Е.С., 2003). Следует отметить, что распространение возбудителей может происходить и по вартонову студню пуповины, чему способствует внесосу-дистый ток жидкости от плаценты к плоду (Mindel A., 1995).
Околоплодные воды могут быть инфицированы восходящим (из влага-лища) и нисходящим (из маточных труб) путём, а также самим плодом, ин-фицированным гематогенно и выделяющим возбудителя с калом и мочой с последующим инфицированием околоплодных вод. При синдроме инфици-рования амниона может произойти преждевременный разрыв околоплодных оболочек с последующим развитием эндометрита, инфекционных осложне-ний новорожденного (Анкирская А.С., 1985). Учитывая ведущую роль трансплацентарного (гематогенного) инфицирования при антенатальной ВУИ, важно отметить, что состояние барьерной функции плаценты в значи-тельной мере определяет возможность развития инфекции и количество по-павшего к плоду инфекционного агента. Известно, что фетоплацентарная не-достаточность резко увеличивает риск развития генерализованной ВУИ при наличии хронического очага или остром заболевании у беременной.
Гематогенный путь передачи инфекции характерен для цитомегалови-русной, энтеровирусной инфекции, вируса простого герпеса, ветряной оспы, а также наблюдается при листериозе, микоплазмозе, некоторой бактериаль-ной инфекции и приводит к тяжёлым диссеминированным поражениям фе-топлацентарной системы, жизненно важных органов плода (мозга, печени, лёгких) (Девис П. А., 1987; Лозовская Л. С., 1995; Самохин П. А., 1987; Си-макова М. Г., 1995).
Восходящий путь инфицирования характерен для условно - патогенной микрофлоры, грибковой инфекции, а также наблюдается при хламидиозе, микоплазмозе, листериозе, других инфекциях. При восходящем пути инфи-цирования микроорганизмы проникают через плодные оболочки в около-плодные воды, где происходит размножение возбудителя. При этом плод оказывается в инфицированной среде. Заражение внутренних полостей плода происходит при заглатывании и аспирации инфицированных вод (Гуртовой Б. Л., Анкирская А. С., 1994; Цинзерлинг А. В., 1986).
Нисходящий путь инфицирования менее характерен для ВУИ, хотя его риск высок при персистенции возбудителей в эндометрии и маточных трубах (хламидии, микоплазмы, уреаплазмы) (Радзинский В. Е., 1996; Тареева Т. Г., 1994).
Интранатальный путь инфицирования (заражение плода во время родов путём аспирации или заглатывания содержимого родовых путей матери) наиболее характерен для бактериальной инфекции (стрептококк группы В, E.сoli, стафиллококк, Proteus, клебсиелла, анаэробная флора), но возможен и для вирусной (ВПГ, ЦМВ) инфекции, грибов рода Кандида. Причем передача инфекции возможна как при наличии симптомов поражения в области шейки матки и вульвы, так и при бессимптомном выделении возбудителя (Адаске-вич В. П., 1996; Барашнев Ю. И., 1994; Кудашев Н. И., 1991; Carmack M. A., 1993).
Таким образом, при наличии у беременной урогенитальной инфекции внутриутробное инфицирование плода и новорожденного может произойти любым из вышеперечисленных путей.
Гематогенные формы менингита. Механизмы возникновения гематогенного менингита
Гематогенная форма менингита обычно наблюдается тогда, когда инфекция переходит на мозговые оболочки по сосудам. Менингит возникает благодаря заносу бактерий и их токсинов в мозговые оболочки или вследствие поражения сосудов, соединяющих среднее ухо с твердой мозговой оболочкой.
Субстратом гематогенного пути являются мелкие костные вены сосцевидного отростка, а также капилляры (система гаверсовых сосудов) костной капсулы лабиринта, которые анастомозируют с сосудами среднего уха (Л. Н. Ямпольский).
Штейрер (Stcurer) большое значение в этом отношении также приписывает сосудистым связям, существующим между клетками сосцевидного отростка и твердой мозговой оболочкой, т. е. костным венам. Кроме того, инфекция из среднего уха может попасть в полость черепа по сосудистым тяжам, имеющимся на крыше барабанной полости.
Гематогенные формы менингита наблюдаются преимущественно при острых средних отитах. Они возникают в результате тромбоза вен, соединяющих среднее ухо с мозговыми оболочками. Менингит может также возникнуть при отогенном сепсисе или при другом гнойном процессе, который сопровождается генерализацией инфекции по организму. Известный интерес в этом отношении заслуживает описание случая менингита, опубликованное Маутнером (Mauthner). У больного, страдавшего острым средним гнойным отитом, почти в одно и то же время развились субдиафрагмальный абсцесс и гнойный менингит.
Автор считает, что менингит в данном случае развился метастатически. Подтверждением этому служит то, что в гнойных выделениях из среднего уха и абсцесса был обнаружен один и тот же вид стрептококка. Этот автор ссылается также на Руттина (Ruttin), приводящего историю болезни больного, у которого на почве острого среднего отита развился септический эндокардит и одновременно гнойный менингит. В литературе описано несколько случаев менингита с аналогичным патогенезом.
Гематогенная форма менингита отличается быстрым, нередко молниеносным развитием патологического процесса. Это объясняется тем, что инфекция быстро преодолевает защитные механизмы (слизистую оболочку, сосудистые стенки, твердую мозговую оболочку и т. п.) и попадает в полость черепа. Процесс сразу принимает диффузный характер. Гематогенные формы менингита наблюдаются, как уже сказано, при острых отитах, часто в их начальной стадии развития, т. е. в первые дни или даже часы. Иначе говоря, процесс развития менингита идет почти параллельно острому воспалительному процессу в ухе. Во время мастоидотомии кость в таких случаях оказывается макроскопически не измененной.
Нам кажется наиболее целесообразным деление отогенных менингитов на две формы: контактную и гематогенную. К первой относятся: а) случаи менингита, при которых патологический процесс переходит на мозговые оболочки непосредственно из кариозно измененной кости или из имеющегося уже в полости черепа гнойника (абсцесса мозга и т. д.); б) случаи, когда этот переход происходит по протяжению, например лабиринтогеyный менингит. Ко второй относится распространение инфекции по сосудам, соединяющим среднее ухо с мозговыми оболочками.
Говоря о гематогенном пути, мы, как уже сказано, различаем два вида заражения мозговых оболочек. Первый мы назвали бы сегментарно-васкулярным, исходя из тех соображений, что тут речь идет 6 поражении только сосудов уха, которые имеют связи с мозговыми оболочками. Инфекция в таких случаях не попадает в общее кровяное русло, т. е. она не генерализуется по организму, она только циркулирует от уха до мозговых оболочек. При метастатическом способе развитие менингита происходит вследствие генерализации инфекции по организму. Источником распространения инфекции может быть любой инфекционный процесс или гнойный очаг различной локализации (заболевания легких и бронхов и т. п.). Часто занос инфекции в полость черепа имеет место при сепсисе, в том числе сепсисе ушного происхождения.
При сегментарно-васкулярном способе реакции организма до поражения мозговых оболочек могут быть слабо выражены, так как процесс до определенной поры не выходит за пределы уха. При втором способе реакции организма резко выражены (высокая температура, ознобы) и они предшествуют воспалению мозговых оболочек. Метастазы при сепсисе возникают в различных органах и тканях малого и большого круга кровообращения. Метастазы в полости черепа выявляются в виде абсцессов мозга или менингита. Нередко метастазы возникают одновременно в различных местах, примером могут служить клинические наблюдения, приведенные нами выше.
На основании многочисленных клинических наблюдений, экспериментальных данных, а также гистологических исследований можно сказать, что отогенный менингит в большинстве случаев возникает в результате разрушения кости в области крыши барабанной полости и антрума. Этот путь наиболее частый. При нем патологический процесс из пораженной кости переходит на мозговые оболочки.
Для иллюстрации приведем данные наших наблюдений, касающихся 93 больных отогенным менингитом, находившихся на излечении в ЛОР-клинике Одесского медицинского института с 1947 до первой половины 1956 г.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

