Хронический цервицит как вич
Обновлено: 25.04.2024
Профессор В.Н. Прилепская, С.И. Роговская
ГУ Научный центр акушерства, гинекологии и перинатологии Росмедтехнологий, Москва
В динамике воспаления возникают взаимосвязанные нарушения местного иммунитета, кровоснабжения подлежащей стромы и клеточного обновления эпителиального пласта, способствующие рецидивирующему течению процесса, то есть хронизации.
Лечение хронических воспалительных процессов нижних отделов гениталий нередко малоэффективно и требует от врача и пациентки значительных усилий. Трудность этого обусловлена прежде всего тем, что этиология их различна и однозначно выявить причину удается не всегда, при этом роль вирусов может оставаться завуалированной. Хронические цервициты нередко играют важную роль в генезе рака шейки матки, частота которого, по данным Минздрава РФ, составляет 15,2 на 100 тыс. женского населения (2002) и на протяжении последних десятилетий меняется незначительно.
Инициирующую роль в развитии хронических воспалительных процессов шейки матки могут играть разные специфические и неспецифические микробные и вирусное агенты. Первые относятся к инфекциям, передаваемым половым путем (ИППП). В частности, ими могут быть трихомонады, способные вызывать многоочаговые длительные поражения урогенитального тракта как у женщин, так и у мужчин. Актуальной остается гонорея, которая также характеризуется многоочаговостью поражений и часто протекает в виде микст-инфекций, но самой распространенной формой поражения у женщин остается гонорейный цервицит.
Бактериальный вагиноз при превалировании анаэробной флоры способен вызывать полиморфные жалобы, чаще всего связанные с постоянными выделениями из влагалища, сопровождающимися неприятным запахом. Почти в половине случаев вагиноза имеются ассоциации с другими возбудителями, при этом у 80% женщин диагностируются воспалительные процессы экзоцервикса [Bhalla P, Kaushika A, 1998]. Грибы рода Candida, которые являются аэробами и обладают тропизмом к тканям, богатым гликогеном, часто сапрофитируют на слизистой оболочке влагалища и шейки матки и вызывают сочетанные поражения вульвы, влагалища и экзоцервикса.
Противоречивы данные о роли микоплазм в развитии хронических процессов половых органов у женщин, однако превалирует мнение о том, что данные возбудители в их различных формах представляют собой этиологический фактор развития хронических воспалительных процессов и осложнений течения беременности и родов [Кира Е.Ф., 1996, Скрипкин Ю.К., 1999]. Значительную долю среди ИППП занимает урогенитальный хламидиоз, вызываемый облигатным внутриклеточным паразитом, который часто ассоциируется с вирусом герпеса, уреаплазмой, грибами и т.д. Хламидиям отводится роль кофактора в развитии предраковых и раковых процессов шейки матки, их нередко определяют при цервицитах и другой доброкачественной патологии шейки матки.
За последние годы отмечено увеличение частоты поражений урогенитального тракта вирусом герпеса, при этом основным резервуаром считают слизистую оболочку шейку матки, поскольку вне клинических проявлений там этот вирус обнаруживают у 15% женщин [Скрипкин Ю.К., Мордовцев В.Н., 1999]. Диагностика и лечение герпесвирусных поражений экзоцервикса трудна, особенно если принять во внимание наличие его атипичных форм [Марченко Л.А., 2000].
В генезе хронических цервицитов важную роль может также играть неспецифическая банальная условно-патогенная флора. По данным В.И. Краснопольского (2001), частота вагинитов, обусловленных бактериальным инфицированием, составляет 40-50%, кандидозом -20-25%, трихомониазом -10-15%, у 15-20% - наблюдается смешанная инфекция. Реже ведущим фактором являются золотистый стафилококк, гемолитический стрептококк, встречаются также вагиниты, обусловленные недостатком эстрогенов и коллагеновыми болезнями. В последние годы этиология изменилась: чаще выявляются грамотрицательные аэробы (кишечная палочка, протей, клебсиелла, энтерококки) и неклостридиальные анаэробы (пептококки, бактероиды). Частота вирусных поражений, по данным разных авторов, колеблется в пределах от 7 до 80% ввиду трудностей в диагностике.
Несомненной на сегодняшний день представляется ведущая роль вируса папилломы человека (ВПЧ) в генезе рака шейки матки. ВПЧ также может инициировать и, по-видимому, поддерживать хронические воспалительные процессы нижнего отдела гениталий, поскольку при ВПЧ-индуцированном изменении структуры эпителия создаются предпосылки для манифестации вирусных, бактериальных, протозойных, грибковых и других инфекций. Роль данного вируса в генезе хронических цервицитов продолжает уточняться. Вирусом папилломы является ДНК-содержащий вирус, икосаэдрический по форме, который является строго эпителиотропным, то есть поражает только эпителий кожи и слизистых оболочек гениталий и других органов (гортань, ротовая полость, глаза и др.).
Вирус папилломы способен индуцировать экзофитные кондиломы (бородавки) и субклинические или эндофитные формы, при которых поражение эпителия не сопровождается наружными разрастаниями. Частота последних недооценивается, поскольку они могут маскироваться под личиной других инефкций. По нашим данным, разные формы папилломавирусной инфекции гениталий встречаются у 44,3% пациенток, обращающихся в гинекологическую клинику по различным причинам. По данным биопсий шейки матки субклинические формы инфекции выявляются у 8,1% женщин [Роговская С.И., Прилепская В.Н., Кондриков Н.И., Ежова Л.С., 2003].
Как известно, в основе патогенеза любого воспаления, как сосудисто-тканевой (мезенхимальной) защитно-приспособительной реакции организма, лежат несколько основных стадий:
- альтерация ткани с последующим выделением медиаторов;
- сосудистая реакция с последующей экссудацией, нарушением микроциркуляции, миграцией лейкоцитов, выработкой иммунных клеток, простагландинов, ферментов, различных ионов, кининов, изменения Ph тканей;
- пролиферация - репаративная стадия.
Нарушения в структуре соединительной ткани при хроническом вагините неизбежно ведут к появлению дистрофических изменений в клетках многослойного плоского эпителия с последующей вакуолизацией ядер и цитоплазмы и изменению ферментативных процессов, уменьшению и даже полному временному исчезновению гликогена в тканях. При хроническом процессе в большой мере поражается строма: происходит инфильтрация ее клетками, сосуды полнокровны и расширены.
При распространении процесса на подлежащие шеечные железы содержимое их становится гноевидным, на поверхности перерастянутых желез можно наблюдать выраженную сеть варикознорасширеннных сосудов. Пролиферация фиброзной ткани приводит к тому, что шейка при хроническом цервиците нередко выглядит гипертрофированной. Ввиду инфильтрации и утолщения соединительнотканых сосочков на обширных участках слизистой оболочки можно наблюдать мелкие точечные вкрапления и возвышения, продолжавшие существовать длительный период времени, что во многом определяет соответствующую картину при кольпоскопии, которая является одним из ведущих методов диагностики цервицитов.
Хронические цервициты нередко беспокоят женщину на протяжении месяцев и даже лет. Клинически они сопровождаются постоянными белями, кратковременным и неполным эффектом противовоспалительной терапии. Такие пациентки нередко обращаются к разным врачам, неоднократно получают антибактериальную терапию, при этом спектр выявляемых возбудителей может изменяться.
Диагностика хронических воспалительных процессов шейки матки сложна. Для этиологической верификации используются бактериоскопический метод (самый доступный и дешевый), микробиологический культуральный метод с подбором антибактериальных средств, серологический, ПЦР. В ряде ситуаций полезной может быть провокация различными методами, аминный тест при вагинозе, ИФА, методы прямой и непрямой флуоресценции, а также кольпоскопия, цитологический метод и другие.
Цитологический метод диагностики позволяет оценить клиническую ситуацию и дифференцировать воспалительный процесс от злокачественного. Цитологическое заключение при цервиците может быть разным в зависимости от интенсивности процесса. При слабовыраженном воспалении картина может не отличаться от таковой при норме, может также содержать клетки, отражающие картину некробиоза: клетки плоского эпителия с дистрофическими изменениями ядер, в т.ч. парабазальных (анизонуклеоз, пикноз, кариорексис), и цитоплазмы (слабая эозинофилия, вакуолизация, цитолиз). Могут определяться гистиоциты, лимфоциты, лейкоциты.
При воспалительном процессе большой давности ячеистые структуры цилиндрического эпителия приобретают расплывчатые контуры, границы клеток становятся нечеткими. Наличие парабазальных клеток с крупными ядрами и ядрышками в мазках и признаки дегенерации цитоплазмы не должны сразу рассматриваться, как неоплазия, поскольку после лечения воспаления клетки с псевдодискариозом исчезают, появляются метапластические клетки. Однако если после противовоспалительной терапии подобные изменения цитологически продолжают определяться, следует производить биопсию из участков с кольпоскопически наиболее выраженной картиной воспаления.
Многочисленными работами показано, что клинические проявления хронического цервицита, сопровождающегося наличием ВПЧ, характеризуются изменениями системного и локального иммунитета, что проявляется, например, снижением выработки фактора некроза опухоли и повышением интерлейкина-10 клетками эпителия, снижением индукции γ-интерферона и повышением сывороточного интерферона в периферической крови, а также менее понятными изменениями клеточного иммунитета. Более выраженные изменения наблюдаются при наличии высокоонкогенных типов ВПЧ. Это обусловливает целесообразность выявления последних, обследования системы иммунитета с возможным подбором иммуномодуляторов по чувствительности клеток крови.
Терапия хронических цервицитов должна быть комплексной, поэтапной и принимать во внимание возможность микст-инфекции. Но лечение следует назначать только после полноценной постановки диагноза. Деструктивное лечение эндофитных форм папилломавирусной инфекции шейки матки и влагалища нередко бывает малоэффективным и часто сопровождается рецидивами. В связи с этим поиски новых более эффективных средств лечения продолжаются.
Первоочередным методом терапии хронических цервицитов представляется этиотропное лечение, основаннное на данных обследования, стандартные схемы которых изложены во многих отечественных и зарубежных клинических рекомендациях. Безусловно, важное значение имеет коррекия биоценоза влагалища и лечение сопутствующих бактериальных инфекций с учетом данных микробиологических исследований. Различные методики коррекции микробиоценоза также широко публикуются. Среди них применяются бифидумбактерин, хилак, флорадофилюс, ацилакт, солкотриховак и другие. Однако при хронизации воспалительных процессов этих средств оказывается недостаточно. В частности, учитывая нарушение микроциркуляции в тканях, пораженных хроническим воспалительным процессом, предлагаются различные методики физитерапии. Поскольку дисбаланс гормонов приводит к выраженным нарушениям в дифференцировке клеточных пластов и дистрофии эпителия, хороший эффект может дать коррекция гормональных нарушений, на фоне которых процесс хронизируется.
Предлагаются методы комбинированного деструктивного лечения эндофитных папилломавирусных поражений шейки матки с одновременным назначением иммунопрепаратов, снижающих активность вируса и повышающих иммунитет. В настоящее время препаратов, избирательно воздействующих на вирус папилломы человека, не существует. Наиболее часто для лечения ВПЧ-инфекции применяют интерфероны и различные иммуномодуляторы. Однако даже длительная интерферонотерапия зачастую не приводит к излечению. Эффективность лечения напрямую зависит от уровня синтеза онкобелка Е7, который нейтрализует противовирусную активность интерферонов.
На российском аптечном рынке представлено множество препаратов-активаторов иммунитета. Мы имеем опыт использования препарата Изопринозин, противовирусного средства (активное вещество - инозиплекс - inosine pranobex), который подавляет репликацию ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Кроме противовирусного действия, препарат обладает и иммуномодулирующим свойством за счет комплекса инозина, что повышает его доступность для лимфоцитов. Препарат стимулирует неспецифический иммунитет, усиливает продукцию интерлейкинов, повышая синтез антител, стимулирует хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфно-ядерных клеток. Фармакокинетика препарата хорошо изучена. Максимальная концентрация Изопринозина достигается через 1 ч после приема 1,5 г препарата. Первый период полувыведения (50 мин) связан с образованием мочевой кислоты. Второй период полувыведения 3-5 ч, при этом метаболиты выводятся почками. Во время приема Изопринозина не рекомендуется применять иммунодепрессанты и аналогичные препараты, а также лекарственные средства, обладающие нефротоксическим действием.
Показаниями для применения Изопринозина являются вирусные инфекции у пациентов с нормальной и ослабленной иммунной системой, в т.ч. заболевания, вызванные вирусами Herpes simplex типов 1 и 2, Varicella zoster (включая ветряную оспу), вирусами кори, паротита, цитомегаловирусом, вирусом Эпштейна-Барра; вирусный бронхит; острые и хронические вирусные гепатиты B и C; заболевания, вызванные вирусом папилломы человека; подострый склерозирующий панэнцефалит; хронические инфекционные заболевания мочевыводящей и дыхательной систем; профилактика инфекций при стрессовых ситуациях и др. В литературе имеются данные о его успешном применении при лечении остроконечных кондилом, генитального герпеса, папилломавирусной инфекции шейки матки [Забелев А.В. с соавт, 2005], CIN и даже рака шейки матки. Так, Кедрова А.Г. с соавт, (2005) указывают, что на первом этапе лечения больные по поводу CIN и рака шейки матки должны по показаниям подвергаться электрокоагуляции, криодеструкции, лазеровапаризации, электроконизации. На втором этапе должно обязательно проводиться противовирусное лечение, так как персистенция вируса является ключевым фактором для возникновения рецидива заболевания. По их данным, применение противовирусного препарата Изопринозин до операции (1000 мг 3 раза в сутки в течение 10 дней) сопровождается значительным снижением активности вируса HPV 16 и 18 типов, определяемых при ПЦР-диагностике. Указывают, что уже после первого курса лечения тест на вирус отрицателен у 77,8% больных.
Эффективность комбинированного лечения (этиотропный препарат, Изопринозин и аблация) была изучена нами в поликлиническом отделении Центра на группе больных (n=64) с гистологически подтвержденными субклиническими формами ПВИ, CIN I (что трактуется в современной литературе, как плоскоклеточное интраэпителиальное поражение низкой степени - LSIL) на фоне хронического цервицита сочетанной этиологии. Кольпоскопическая картина у всех пациенток представляла собой низкоатипическую зону трансформации и хронический цервицит. У 8 пациенток был диагностирован хламидиоз, у 2 - гонорея, 19 - кандидоз, 37 - бактериальный вагиноз, микоплазмы были выявлены у 37 женщин, вирус герпеса - у 16, условно-патогенная флора в высоких концентрациях выявлялась у 22 женщин. Следует подчеркнуть, что у 100% женщин данные обследования продемонстрировали наличие микст-инфекции, то есть сочетания ВПЧ с другими инфекционными агентами. Этиотропная терапия базировалась на европейских рекомендациях по лечению ИППП и не различалась у двух групп пациенток.
Последующее наблюдение за пациентками и полученные нами данные свидетельствуют о том, что эффективность комбинированного лечения с применением Изопринозина была выше и составила 87,5%, в то время как при монодеструкции - 65,6%. Важно, что частота рецидивирования папилломавирусной инфекции к 6-му месяцу наблюдения составила 9,4 и 28,1% соответственно. Симптоматика воспалительного процесса на шейке матки наблюдалась только при рецидиве ВПЧ-инфекции. Кроме того, при комплексной схеме лечения выявили более высокую частоту очищения от ВПЧ через 6 месяцев (65,6 и 46,9% соответственно) и более качественную эпителизацию.
Представляется очевидным, что локальная деструкция очагов субклинического проявления ПВИ на фоне хронического цервицита позволяет воздействовать только на участок эпителия, где произошла клиническая манифестация инфекции. При этом в окружающих тканях остаются резервуары ВПЧ в латентном состоянии или других возбудителей, которые могут являться основой для дальнейшего рецидива цервицита и персистенции инфекции. Адекватная иммунотерапия способствует более полной элиминации возбудителей и полноценной эпителизации шейки матки, что и снижает частоту рецидивов и повышает эффективность терапии такой сложной патологии, как хронический цервицит.
Учитывая высокую стоимость деструктивного лечения шейки матки при LSIL и возможность их спонтанного регресса некоторые зарубежные стандарты ведения пациенток с данной патологией рекомендуют не деструктивное лечение, а наблюдение с регулярным цитологическим контролем. Возможно, в ряде случаев папилломавирусной инфекции это более правильная и менее дорогостоящая тактика. Однако при сочетании хронического цервицита и ВПЧ-инфекции больные, как правило, предъявляют жалобы на постоянные бели и настоятельно требуют помощи.
В связи с этим мы предприняли аналогичную консервативную терапию у 29 женщин с LSIL на фоне хронического цервицита без аблации. Всем пациенткам была рекомендована этиотропная терапия в соответствии с данными обследования в сочетании с Изопринозином по схеме 1000 мг 3 раза в сутки на протяжении 10 дней без аблации. У всех пациенток в анамнезе уже были курсы антибактериальной терапии с кратковременным эффектом не более 3 недель. Мы наблюдали данных женщин в течение 3-х и более месяцев и отметили, что после одного курса лечения Изопринозином бели исчезли у 21 больной (72,4%), а тест на ВПЧ стал отрицательным у 19 из них (65,5%). При этом клинически значимых побочных эффектов мы не наблюдали.
К настоящему времени нами накоплен значительный опыт использования Изопринозина в лечении неспецифических цервицитов и вагинитов, когда при наличии длительных белей при обследовании не представляется возможным выявить какую-либо специфическую патологию, а при посевах обнаруживается обычная условно-патогенная флора типа стафилококков, стрептококков, и т.д. В курс лечения антибиотиками и физиотерапевтическими средствами мы включали Изопринозин по схеме 1 г 2 раза в сутки в течение 10 дней. В сравнении с контрольной группой с аналогичной терапией без иммуномодуляторов эффективность излечения и в последующем частота рецидивов была меньше.
Таким образом, по нашему мнению, включение антивирусного иммуномодулирующего препарата Изопринозин в курс лечения больных хроническими цервицитами и вагинитами можно считать обоснованным и перспективным.
Увеличение частоты воспалительных заболеваний влагалища и шейки матки, в частности экзо- и эндоцервицитов, требует необходимости поиска новых методов и схем лечения данного заболевания. Раннее начало половой жизни, ИППП, наличие нескольких половых партнеров, бесконтрольное применение антибактериальных препаратов, приводящих к нарушению биоценоза влагалища, ведет к хронизации заболевания и частым обострениям. Высокая частота встречаемости хронических цервицитов обусловлена изменением общей реактивности организма в результате нарушения клеточных и гуморальных звеньев иммунной системы [2, 8, 10].
Несмотря на возможности и широкий спектр препаратов, применяемых в лечении цервицитов, не всегда удается добиться элиминации возбудителя, вызвавшего заболевание и ликвидации воспалительного процесса. По данным разных авторов частота рецидивов заболевания достигает 40% [8, 9].
На фоне хронического цервицита могут сформироваться дистрофические изменения шейки матки с дальнейшим развитием диспластических процессов. Ряд авторов относит больных с хроническим цервицитом специфической и неспецифической этиологии к группе риска в отношении развития рака шейки матки [5, 9]. Наличие цервицита имеет большое значение у беременных, поскольку при этом повышается риск инфицирования амниона, хориона, околоплодных вод и плода, преждевременного прерывания беременности, осложнений в родах, послеродовом периоде, высокой заболеваемости новорожденного [12].
Воспалительный процесс в цервикальном канале считают одним из этиологических факторов бесплодия [2, 11].
Основными повреждающими агентами при развитии воспалительного процесса являются возбудители инфекций. Механизм повреждения тканей может быть различным:
Проводимая на ранних этапах развития воспаления антибактериальная терапия, с учетом конкретной инфекции и чувствительности к антибиотикам, ликвидирует воздействие инфекционного агента на эпителий влагалища и шейки матки и нормализует состояние многослойного плоского эпителия. Однако при длительно текущих воспалительных процессах лечение не оказывает столь благотворного воздействия, т. к. воспаление – это полисистемное заболевание, которое поддерживается образованием провоспалительных медиаторов. Основными из них являются циклооксигеназы. Циклооксигеназа II (ЦОГ-2) в нормальных условиях во многих тканях отсутствует и образуется под действием цитокинов, индуцирующих воспалительную реакцию, участвуя в синтезе простагландинов при воспалении [1, 3, 5, 13].
Воспаление повреждает глубокие слои ткани шейки матки, нарушает физиологический процесс метаплазии, способствует появлению атипичных клеток. Кольпоскопически ткань экзоцервикса становится рыхлой, гиперемированной, отечной и за счет этого бугристой: кровоточивость выраженная, сосудистая сеть приобретает вид атипичной (крупные, легко травмирующиеся сосуды, плохо сокращаются на уксусной пробе), наблюдается гипертрофия шейки матки. На пробе Шиллера отмечаются йоднегативные участки с размытыми краями. Цитологически и гистологически может наблюдаться картина цервикальной интраэпителиальной неоплазии. Несмотря на отсутствие инфекционного агента во всех анализах, состояние шейки матки и слизистой оболочки влагалища не улучшается. Проведение на таком фоне коагуляции шейки матки тем или иным методом неэффективно, т. к. эпителизация практически не наступает и это способствует развитию различных осложнений [5]. В достижении эффективности лечения хронических цервицитов используются методики и препараты комплексного действия, лазеро- и рефлексотерапия, различные фитопрепараты, иммуномодуляторы [11].
Развитие хронических воспалительных процессов сопровождается изменениями иммунной системы организма, которые влияют не только на течение, но и исход заболевания. Это служит основанием для разработки и изыскания новых средств и методов, оказывающих эффективное терапевтическое воздействие, направленное на восстановление функции нарушенного иммунного статуса человека в целом или же на конкретное звено в иммунной системе.
Основным показанием к назначению иммуномодуляторов является индуцированная или спонтанная вторичная иммунная недостаточность, клинически проявляющаяся следующими особенностями:
Выбор иммуномодуляторов должен быть определен с учетом состояния иммунной системы пациента, цели иммунофармакотерапии, иммунофармакологических свойств, эффективности и безопасности применяемого препарата, особенностей взаимодействия с другими лекарственными средствами.
Ведущая функция в формировании иммунитета принадлежит интерферонам, являющимся важнейшим компонентом врождённой неспецифической защиты организма от инфекций. Интерфероны представляют собой семейство белков местной (аутокринной и паракринной) регуляции, которые способны активировать внутриклеточные процессы и межклеточные взаимодействия, обеспечивающие устойчивость к вирусным инфекциям, усиливающие врождённый и приобретённый иммунные ответы, модулирующие процессы развития и гибели нормальных и опухолевых клеток. Резистентность организма к инфекционным заболеваниям, в т. ч. к вирусным инфекциям, во многом зависит от активности группы генов системы интерферонов.
Является уникальным препаратом, обладающим не только иммуномодулирующим и противовоспалительным действием, но и мембранопротективным, антиоксидантным и репарационным действием.
Обладает рядом преимуществ:
Иммуномодулирующий эффект Галавита слагается из влияния как на клеточный так и на гуморальный звенья иммунитета.
Непосредственно воздействует на регуляцию фагоцитарной и пролиферативной активности:
Регулирует синтез эндогенных интерферонов (ИФН-α, γ). Опосредованно влияет на продукцию антител (IgM, IgG, IgA) и их функциональную активность.
Противовоспалительный эффект Галавита: обратимое (на 6-8 часов) ингибирование избыточного синтеза активированными макрофагами провоспалительных цитокинов (ИЛ-1, ФНО-α) индукция синтеза противовоспалительных цитокинов (ИЛ-10), приводящее к снижению степени интоксикации, продолжительности и выраженности воспалительного процесса.
Репарационный эффект выражается в увеличении выработки фагоцитарными клетками ростовых факторов; перенос макрофагами в очаг воспаления регенерационной информации и в результате – ускорение процессов репарации.
Антиоксидантный эффект обусловлен обратимым (на 6-8 часов) ингибированием избыточного синтеза активированными макрофагами активных форм кислорода и оксида азота приводящее к снижению степени оксидантного стресса в клетках и тканях, накопления продуктов перекисного окисления липидов.
Мембранопротективный эффект проявляется опосредовано, за счет снижения оксидантного стресса, вследствие ингибирования выработки активных форм кислорода фагоцитарными клетками, что приводит к повышению устойчивости клеточных мембран и уменьшению повреждающего действия продуктов перекисного окисления липидов.
Нами было проведено исследование, целью которого явилась возможность применения Галавита в комплексном лечении цервицитов, обусловленных хламидийной инфекцией.
В исследование были включены 30 пациенток в возрасте от 18 до 45 лет (средний возраст 26,2±1,2 года) с клиническими проявлениями и подтвержденным диагнозом урогенитального хламидиоза по данным клинико-лабораторных методов исследования.
Все пациентки были обследованы с применением клинических (анализ анамнестических данных, жалоб пациентки), гинекологических (осмотр вульвы, слизистых влагалища и шейки матки в зеркалах, бимануальное гинекологическое исследование, расширенная кольпоскопия) и лабораторных (ПЦР, ИФА) методов исследования.
83,3% пациенток предъявляли жалобы на обильные выделения из влагалища; тянущие боли внизу живота отмечались у 36,7% пациенток; зуд во влагалище и в области наружных половых органов отмечали 13,3% пациенток; жжение в области наружных половых органов отмечалось у 26,7%; 16,7% пациенток не предъявляли жалоб при обращении. При гинекологическом осмотре у всех пациенток отмечались гиперемия слизистой оболочки влагалища, шейки матки и вульвы той или иной степени выраженности. При лабораторном исследовании у 100% пациенток методом ПЦР была выявлена хламидийная инфекция.
Пациентки перед назначением терапии были разделены на две группы. В I группу включены 15 пациенток, которые принимали препарат Галавит в виде ректальных свечей (по 1 сумм 1 раз в день 5 дней, затем по 1 супп через день, курс 15 супп) в составе комплексной стандартной терапии. Во II группу включены 15 пациенток, которые для лечения УХ получали стандартную антибактериальную терапию.
До начала исследования в обеих группах среднее значение уровня специфических IgG и IgА были практически одинаковыми и составляли, соответственно, 1,76±0,15 и 0,48±0,1 оп.ед. в I группе и 1,39±0,13 и 0,59±0,12 оп.ед. во II группе. Также близкими по значению были у них уровни ИНФ-α и ИНФ-γ – соответственно, 20,6±0,4 и 3,1±0,9 в I группе и 20,7±0,5 и 3,2±0,7 во II группе. Эти данные говорят о равнозначности двух исследуемых групп по характеру течения хламидийной инфекции.
Контроль эффективности лечения проводился через 3 недели после окончания терапии. При оценке эффективности терапии клинические симптомы, которые отмечались до начала терапии и явления цервицита при расширенной кольпоскопии отсутствовали у 93,3% пациенток I группы и 80% пациенток II группы. У 6,7% пациенток I группы и 20% пациенток II группы отмечались незначительные клинические симптомы заболевания. (слабо выраженный цервицит). Отсутствие эффекта от проведенной терапии не отмечено ни у одной пациентки обеих групп. При двукратном контрольном исследовании соскоба из цервикального канала методом ПЦР у пациенток обеих групп хламидийная инфекция не обнаружена. При микроскопическом исследовании влагалищного отделяемого у всех пациенток отмечена I –II степень чистоты влагалища. После завершения лечения уровень специфических IgG в среднем по группам изменился незначительно. Содержание IgА в крови у всех пациентов обеих групп снизилось до уровня отрицательного контроля. При контрольном исследовании после лечения у пациенток II группы уровень ИФН-α и ИФН-γ существенно не изменялся. В то же время у пациенток I группы отмечено увеличение уровня ИФН-α почти в полтора раза (среднее значение до лечения – 20,6±0,4, после лечения – 29,2±1,6). Уровень ИФН-β у пациенток I группы, в среднем повысился почти в 3 раза – до лечения среднее значение в группе было 3,1±0,9, после лечения 8,1±0,9.
Таким образом, проведенное клинико-лабораторное исследование показало, что применение препарата Галавит в составе комплексной терапии цервицитов, обусловленных хламидийной инфекцией, приводит к выраженному положительному клиническому эффекту и способствует более быстрому исчезновению клинических симптомов урогенитального хламидиоза, нежели стандартная терапия антибактериальными препаратами.
Хронический эндоцервицит — это инфекционное воспалительное заболевание слизистой цервикального канала, длящееся от двух месяцев и более. Отличается скудной клинической симптоматикой: увеличением количества слизистых влагалищных выделений с появлением в них примеси гноя и тянущими болями внизу живота. Для диагностики эндоцервицита применяют осмотр в зеркалах, расширенную кольпоскопию, трансвагинальное УЗИ, лабораторные исследования. При лечении назначают этиотропные противомикробные средства, эубиотики, иммунокорректоры, физиотерапию. По показаниям проводят малоинвазивные хирургические вмешательства, трахелопластику и радиоконизацию.
МКБ-10
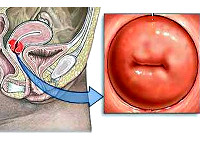
Общие сведения
Хронические цервициты — одни из самых частых гинекологических заболеваний. Из-за бессимптомного течения их истинную распространенность установить крайне сложно. Обычно воспаление эндоцервикса выявляют при плановых профосмотрах или при обращении по поводу других болезней репродуктивной сферы.
Наиболее подвержены заболеванию женщины детородного возраста (до 70% пациенток с установленным диагнозом), несколько реже цервицит встречается в перименопаузе и в исключительных случаях — у девочек до наступления менархе. Важность своевременной диагностики и лечения хронической воспалительной болезни шейки матки обусловлена повышенным риском распространения воспаления на матку с придатками и злокачественного перерождения пораженного эндоцервикса.

Причины
Заболевание развивается на фоне недолеченного или недиагностированного острого воспалительного процесса и вызывается различными микроорганизмами или их ассоциациями. Воспаление в эндоцервиксе возникает при участии следующих инфекционных агентов:
- Возбудители ИППП. По результатам исследований, хронический воспалительный процесс в цервикальном канале у половины пациенток вызван возбудителями хламидиоза. Причиной болезни также могут быть вирусы простого герпеса, папилломы человека (ВПЧ), гонококки, уреаплазмы, микоплазмы, бледные спирохеты.
- Условно-патогенная флора. Неспецифическое воспаление чаще возникает при патологической активации грамотрицательных аэробов (энтерококков, эшерихий, клебсиелл, протея) и неклостридильных анаэробов (бактероидов и пептококков). Из очага инфекции также высеивают стафилококков, стрептококков, клостридий, гарднерелл.
Факторы риска
Важную роль в переходе заболевания из острой в хроническую фазу играют предрасполагающие факторы. Хронизацию процесса провоцирует:
- ослабление иммунитета при длительных физических нагрузках, стрессах, переохлаждениях, различных заболеваниях и приеме иммуносупрессоров;
- гипоэстрогенемия;
- травмы шейки матки при инвазивных процедурах;
- постоянное раздражение внутриматочной спиралью, контрацептивными колпачками и диафрагмами; химическими агентами (кислыми растворами для спринцевания, спермицидами, некачественным латексом).
Группу риска составляют женщины с опущением шейки матки и влагалища, а также пациентки, ведущие беспорядочную сексуальную жизнь без барьерной контрацепции.
Патогенез
При хроническом течении эндоцервицита в очаге инфекции постоянно поддерживается вялотекущее воспаление, проникающее в парабазальный и базальный слой эпителия. При этом непосредственная повреждающая роль микроорганизмов уменьшается, а ведущими становятся снижение местного иммунитета и метапластические процессы. Это приводит к развитию сложной сосудисто-мезенхимальной реакции, замещению части цилиндрического эпителия плоским, инфильтрации и уплотнению мышечной и соединительной ткани.
Секреторная активность эпителиальных клеток остается повышенной, что при перекрытии устьев цервикальных желез способствует формированию наботовых кист. Отмечается ускоренное обновление эпителиоцитов с замедлением их дифференцировки, прогрессивным снижением апоптоза и нарастанием атипии. У некоторых пациенток процесс носит рецидивирующий характер с периодическим обострением.
Классификация
Формы хронического эндоцервицита являются такими же, как и при остром воспалительном процессе. Основными критериями классификации являются:
- Тип инфекционного агента. Воспалительный процесс может быть специфическим, возникшим в результате заражения ИППП, и неспецифическим, вызванным естественной микрофлорой при ее патологической активации.
- Распространенность воспаления. При очаговом (макулезном) эндоцервиците поражаются отдельные участки эндоцервикса, при диффузном — в процесс вовлекается весь эпителий. Хронический эндоцервицит обычно является диффузным.
Симптомы хронического эндоцервицита
Клиническая картина заболевания отличается крайне скудной симптоматикой. В большинстве случаев хронически протекающий эндоцервицит становится случайной находкой при плановом или внеплановом гинекологическом обследовании. Обычно пациентки отмечают незначительное увеличение объема влагалищных выделений и изменение их характера. Бели становятся мутными, густыми, иногда они имеют неприятный запах или в них появляются прожилки крови.
При обострении воспаления женщину могут беспокоить тупые, тянущие, ноющие боли в нижней части живота, зуд и жжение в области наружных половых органов. Иногда единственным признаком длительно существующего воспаления в шеечном канале становится бесплодие или привычный выкидыш.
Осложнения
Из-за снижения защитных свойств слизистой пробки и наличия постоянного очага воспаления повышается риск развития эндометрита, сальпингита, аднексита с отдаленными последствиями в виде бесплодия и невынашивания беременности. В двух третях случаев хронический эндоцервицит сопровождается эктопией шейки матки. По мнению специалистов в сфере гинекологии, при этом заболевании существенно возрастает вероятность малигнизации тканей. Воспаление эндоцервикса играет роль в развитии акушерской патологии с внутриутробным инфицированием плода и его оболочек, преждевременным излитием околоплодных вод, послеродовыми гнойно-септическими осложнениями.
Диагностика
Из-за неспецифичности симптоматики при постановке диагноза основное значение имеют данные физикальных, инструментальных и лабораторных исследований. Пациентке с подозрением на хронический эндоцервицит проводится:
- Осмотр на кресле. При исследовании в зеркалах наружный зев цервикального канала гиперемирован, шейка матки отечна. Могут выявляться участки повышенной кровоточивости, слизистые и гнойно-слизистые выделения.
- Расширенная кольпоскопия. Сосуды эпителиального слоя шейки матки расширены, выявляются очаги с сосудистыми петлями. Слизистая оболочка выглядит отечной. Могут определяться другие патологические процессы (псевдоэрозия, эрозия и др.).
- Лабораторные исследования. Для определения возбудителя заболевания проводят микроскопию и посев мазка (с антибиотикограммой), ПЦР-диагностику, специальные серологические методы (РИФ, ИФА).
- Цитология мазка из цервикального канала. Позволяет оценить степень вовлеченности в воспаление клеток эндоцервикса. Анализ эффективен для раннего выявления дистрофических, диспластических процессов, атипии и возможного озлокачествления.
- УЗИ шейки матки. Шейка матки увеличена в размерах, утолщена. В ее структуре присутствуют гипоэхогенные включения (наботовы кисты). Метод позволяет исключить или своевременно выявить сочетанный рак шейки матки.
Дифференциальная диагностика производится с эктопией и раком шейки матки, туберкулезным поражением. В сложных случаях назначают консультации онкогинеколога, фтизиатра.
Лечение хронического эндоцервицита
Медикаментозная терапия
При подтвержденном диагнозе хронического воспаления эндоцервикса рекомендован комплексный этиопатогенетический подход. Предпочтительна консервативная терапия, основными задачами которой являются:
- Ликвидация очага инфекции. С учетом чувствительности возбудителя заболевания назначают антибиотики, противогрибковые, противотрихомонадные, противохламидийные и другие средства. Обычно пероральный прием препаратов и их парентеральное введение дополняют местным воздействием (вагинальными свечами и т. п.).
- Восстановление влагалищного биоценоза. Вследствие хронического воспаления и использования антимикробных средств в вагине нарушается нормальный баланс микроорганизмов. Своевременное назначение эубиотических препаратов позволяет предупредить рецидивы эндоцервицита и активацию условно-патогенной флоры.
- Иммуннокоригирующая терапия. Поскольку фоном для развития заболевания часто становится иммунодефицит, пациенткам показаны витамино-минеральные комплексы и стимуляторы иммунитета. Их применение позволяет повысить общую и местную сопротивляемость инфекционным агентам, а также нормализовать иммунный ответ.
Физиотерапия
При лечении хронического эндоцервицита эффективно сочетание медикаментозной и физиотерапии. Физиотерапевтические методики усиливают противовоспалительный эффект антибактериальных средств и ускоряют процессы репарации. Пациенткам назначают:
- низкочастотную и высокочастотную магнитотерапию;
- электрофорез магния в маточной зоне;
- диадинамические токи;
- ДМВ;
- вагинальную лазеротерапию;
- дарсонвализацию через влагалищный электрод;
- грязевые тампоны.
Хирургическое лечение
В некоторых случаях консервативное лечение эндоцервицита дополняют хирургическими методами. При обнаружении большого количества наботовых кист, в которых может персистировать возбудитель, выполняют диатермопунктуру. При упорном течении показаны криодеструкция, лазерная вапоризация, радиокоагуляция. Если хроническое воспаление сочетается с деформацией шейки, дисплазией эпителия или элонгацией, возможно проведение радиоконизации и трахелопластики.
Прогноз и профилактика
Несмотря на необходимость длительного лечения, прогноз при хроническом эндоцервиците благоприятный. Рецидив заболевания возможен только при стойком снижении иммунитета и наличии воспаления в других отделах женской половой сферы. Для профилактики рекомендованы своевременное адекватное лечение острого эндоцервицита, регулярные осмотры у гинеколога, упорядоченная сексуальная жизнь, барьерные методы контрацепции (особенно при частой смене половых партнеров). Целями вторичной профилактики является предупреждение осложнений заболевания, в первую очередь — развития злокачественных неоплазий и бесплодия.
Что такое цервицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Батаршиной О. И., гинеколога со стажем в 18 лет.
Над статьей доктора Батаршиной О. И. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Цервицит — это воспалительное заболевание шейки матки, которое развивается под влиянием различных агентов (как инфекционных, так и неинфекционных) [2] .
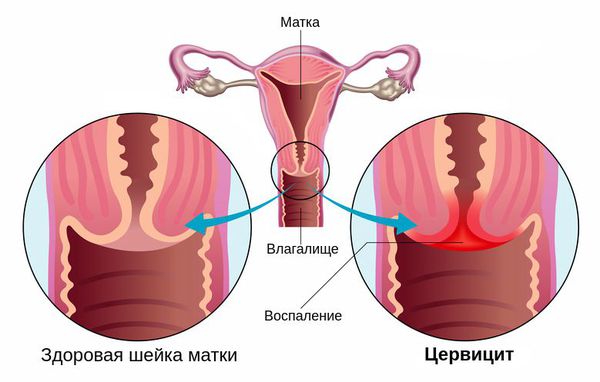
Распространённость цервицита у женщин достигает 10-45 %. Наиболее часто его вызывают возбудители, передаваемые половым путём, такие как гонокок, хламидия, трихомонада, вирус герпеса, бледная трепонема и др. [7] [8] [11] . Также причиной возникновения цервицита являются различные заболевания, аллергические реакции на противозачаточные спермициды, латекс в составе презервативов или продукты женской гигиены, такие как мыла, гели для душа или дезодоранты.
Длительный и вялотекущий дисбиоз влагалища (бактериальный вагиноз) также рассматривается как одна из возможных причин цервицита, поскольку на фоне изменения уровня кислотности влагалища меняется и соотношение видов влагалищной микрофлоры.
В зоне риска по возникновению цервицита находятся женщины, которые:
Также доказано, что фоном для развития воспаления шейки матки и его хронизации является местный иммунодефицит, связанный с нарушением защитной функции слизистой оболочки.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цервицита
Возможно как симптомное, так и бессимптомное течение заболевания [31] .
При бессимптомном процессе диагноз "цервицит" может быть поставлен:
- при неудовлетворительных результатах мазков — повышенном уровне лейкоцитов (клеток крови, отвечающих за иммунный ответ на внедрение инфекционных агентов);
- на основан ии визуального осмотра шейки матки врачом-гинекологом — покраснения и отёка шейки матки.
При симптомном течении заболевания женщину могут беспокоить:
- сероватые или бледно-жёлтые выделения из влагалища;
- аномальные кровянистые выделения во время или после полового контакта, а также в перерывах между менструациями [31] ;
- боль во время секса;
- затруднённое, болезненное или частое мочеиспускание;
- тазовая боль или, в редких случаях, лихорадка.
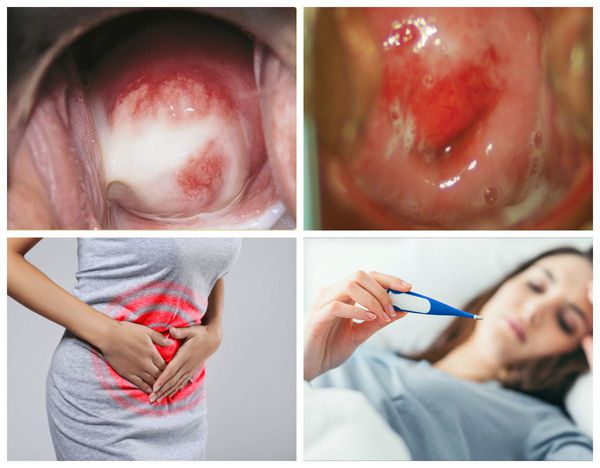
Патогенез цервицита
Когда речь идет о патогенезе цервицита, прежде всего необходимо обозначить понятия, о которых пойдёт речь.
Шейка матки представляет собой гладкомышечный орган длиной 2-3 см, образованный соединительной тканью. Основная функция данной части матки — барьерная. Она реализуется за счёт секрета (выделений) слизистой , которая препятствует попаданию патогенных возбудителей в матку, маточные трубы и малый таз. В состав секрета входят как иммуноглобулины всех классов ( IgG, IgM, IgA и др. ), так и вещества, обладающие высокой расщепляющей и бактерицидной активностью.
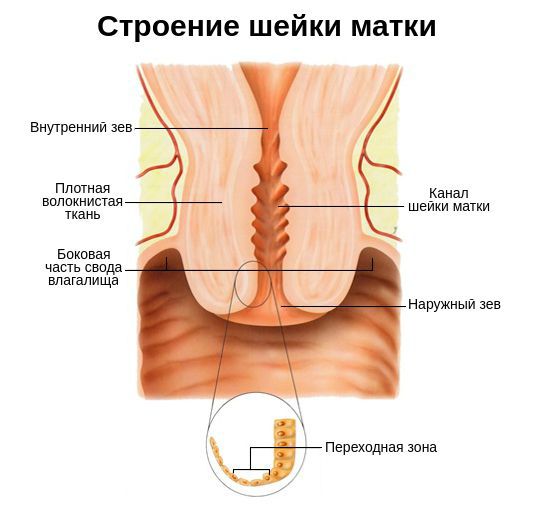
Также шейку матки защищает микрофлора влагалища . Она состоит из анаэробных и аэробных бактерий, причём первых в десять раз больше, чем вторых. Такое соотношение создаёт определённый уровень кислотности слизистой, который не позволяет патогенным микроорганизмам внедряться в полость матки [8] .
Циклическое воздействие половых гормонов на женский организм позволяет сохранять микрофлору влагалища в норме, тем самым защищать шейку матки:
- в первой фазе менструального цикла под воздействием эстрогенов синтезируется гликоген, стимулируется выработка слизистого секрета, выполняющего барьерную функцию [4][17][27] ;
- во второй фазе цикла под воздействием прогестерона происходит подкисление среды влагалища и размножение лактобактерий.
При снижении барьерных свойств микрофлоры влагалища и слизистой шейки матки в организм женщины проникают различные патогенные возбудители, которые приводят к развитию цервицита. Их активному проникновению и распространению в полости малого таза способствуют сперматозоиды в качестве клеток-переносчиков инфекционных агентов, а также трихомонады и установка внутриматочной спирали на фоне воспалительного процесса.
Острый цервицит
Чаще возникает при поражении шейки матки специфическими возбудителями (например, гонококком), а также после искусственного прерывания беременности, в осложнённом послеродовом периоде (возбудителями чаще становятся стафилококковая и стрептококковая инфекции) и при вирусном поражении шейки матки. На ранней стадии заболевания возникают:
- полнокровие сосудов;
- повышение уровня лейкоцитов (лейкоцитарная инфильтрация);
- просачивание крови сквозь стенки сосудов в зону воспаления (экссудация);
- дистрофические изменения с вакуолизацией цитоплазмы и ядер клеток.
В результате дистрофических изменений клеток на поверхности слизистой оболочки шейки матки появляется гнойный и серозно-гнойный экссудат — сероватые или бледно-жёлтые выделения.
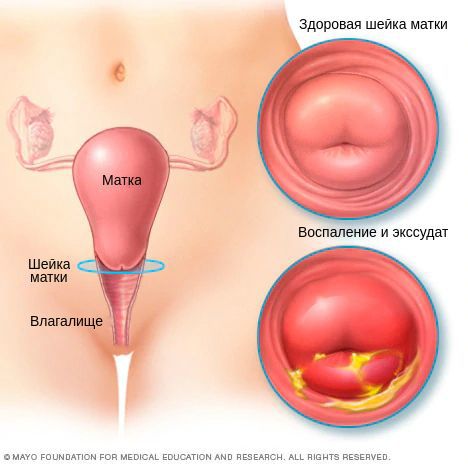
Хронический цервицит
При проникновении возбудителей в межклеточное пространство крипт шейки матки (небольших трубчатых углублений), труднодоступных для лечения, возникает хронический цервицит. Причиной хронизации заболевания нередко является поражение шейки матки хламидийной инфекцией. В 24-40 % случаев хронический цервицит возникает на фоне длительного и вялотекущего бактериального вагиноза. При осмотре гинекологом шейка матки выглядит покрасневшей, отёчной, легко травмируется. Микроскопически наблюдается инфильтрация подэпителиальной ткани лимфоцитами, плазмоцитами, полнокровие сосудов. Наряду с дистрофическими процессами в ткани преобладают процессы непрямого деления клеток, разрастания ткани и замещения одного вида клеток другим. Часто при хроническом цервиците нарушаются процессы ороговения клеток, что проявляется уплотнением тканей и изменением процесса гликогенизации клеток [6] [11] .
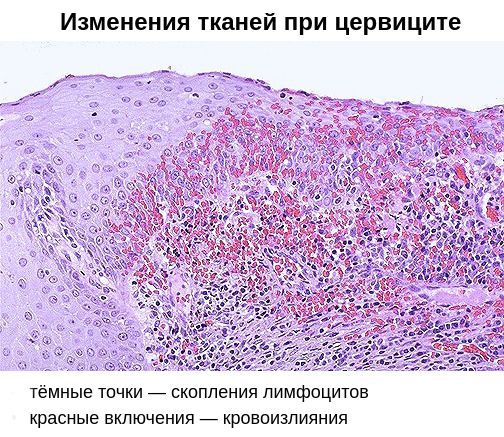
Помимо специфического возбудителя, немалую роль в возникновении хронического цервицита играет вторичный иммунодефицит. Он заключается в неполноценности клеточного и гуморального иммунитета. На клеточном уровне снижается количество Т- и В-лимфоцитов, а также нарушается фагоцитарная активности клеток, позволяющая им поглощать и переваривать патогенные микроорганизмы. В результате возбудители остаются в организме, снижается содержание антител IgG и IgM, увеличивается выработка антител IgA, что ведёт к изменению качества цервикальной слизи.
Послеродовой цервицит
Отдельно такую форму не выделяют, цервицит после родов ничем не отличается от обычного. Разница может быть лишь в лечении: не все антибиотики можно принимать при грудном вскармливании.
Классификация и стадии развития цервицита
Классификация цервицита зависит от типа возбудителей, локализации и давности патологических процессов. Так, в зависимости от типа возбудителя цервициты подразделяют на инфекционные и неинфекционные. Инфекционные цервициты бывают:
- гонококковыми;
- хламидийными;
- трихомонадными;
- кандидозными;
- вирусными.
Неинфекционные цервициты рассматриваются и классифицируется в зависимости от причины, вызвавшей воспаление. Они бывают аллергическими, атрофическими (сенильными) и др. [8] .
Кроме того, по локализации цервицит подразделяют на:
- экзоцервицит — протекает преимущественно на поверхности шейки матки;
- эндоцервицит — в основном затрагивает эпителий канала шейки матки (цервикальный канал).
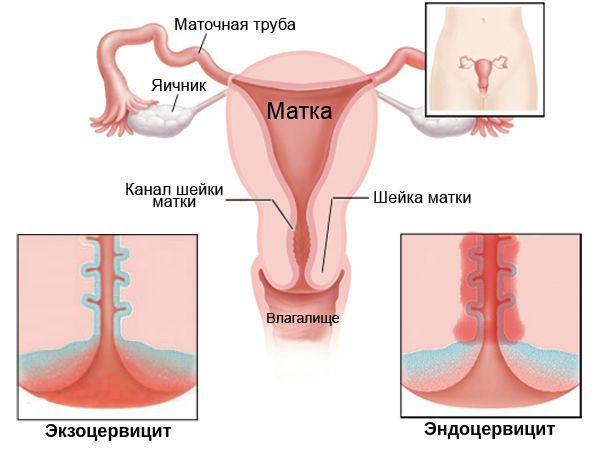
По длительности протекания процесса цервицит может быть:
- острым — процесс воспаления длится не более шести недель;
- хроническим — болезнь протекает с периодическими ремиссиями и обострениями.
Осложнения цервицита
Выявление причины цервицита имеет важное значение, поскольку при наличии инфекционного агента возбудитель способен распространяться за пределы шейк и матки и вызывать эндометрит , а также воспаление в теле матки, маточных трубах и малом тазе. В ряде случаев это приводит к бесплодию или препятствует вынашиванию плода [25] [27] .
Цервицит и беременность
Если беременность возникла на фоне цервицита, возбудитель заболевания может привести к преждевременному прерыванию беременности в связи с проникновением инфекции в водную оболочку, обращённую к плоду, затем в хорион (плаценту), околоплодные воды и сам плод.
При инфицировании ребёнка на ранних сроках беременности могут сформироваться врождённые пороки развития, возникает риск первичной плацентарной недостаточности и внутриутробной гибели плода. При позднем инфицировании наблюдаются следующие осложнения беременности:
- внутриутробная задержка развития плода;
- вторичная плацентарная недостаточность (часто на фоне плацентита — воспаления плаценты);
- локальные и генерализованные (распространённые) инфекционные поражения плода.
Генерализованные формы внутриутробной инфекции чаще развиваются в первом триместре беременности, так как плод ещё не может препятствовать распространению воспалительного процесса. В третьем триместре воспалительные изменения вызывают сужение или обтурацию (закрытие просвета) каналов и отверстий, что ведёт к аномальному развитию уже сформировавшегося органа — псевдоуродствам ( гидроцефалии , гидронефрозу и др.) [29] .
Длительное воспаление шейки матки становится фоном для развития злокачественных процессов . Это связано с нарушением регенерации слизистой оболочки шейки матки, которое наблюдается при хроническом цервиците. Наиболее значимыми факторами, влияющими на регенерацию, являются вирусы и хламидии [10] . Учёные доказали, что формирование рака шейки матки происходит только на фоне сохранившейся в криптах вирусной инфекции, которая активируется более чем через год после первичного обнаружения возбудителя [30] .
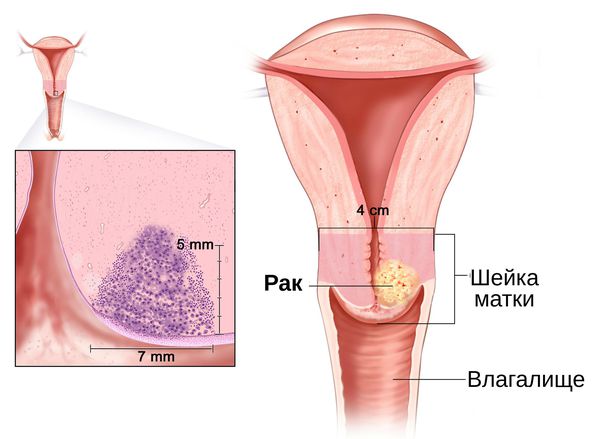
Диагностика цервицита
Диагностическими критериями цервицита при осмотре в зеркалах являются:
- покраснение слизистой, отёк;
- обильные выделения грязно-серого или зеленоватого цвета;
- творожистое отделяемое (при грибковом поражении шейки матки и влагалища).
При микроскопическом исследовании наблюдается увеличение количества лейкоцитов, также можно обнаружить возбудителей трихомониаза и гонореи.
Однозначными признаками цервицита при вульвоцервикоскопии служат:
- фолликулярный кольпит, "лунный ландшафт" — для хламидиоза;
- очаговый кольпит — для трихомониаза;
- диффузный кольпит — для неспецифической бактериальной инфекции;
- симптом "манной крупы" — для герпетической инфекции [17] .
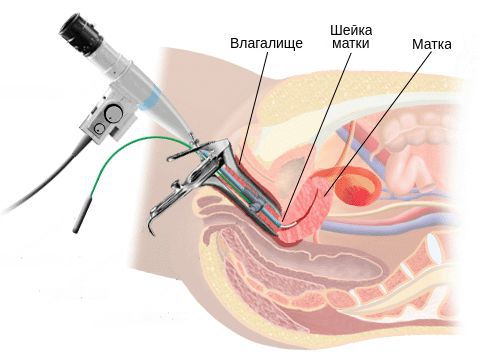
Бактериологическое исследование с поверхности шейки матки и заднего свода влагалища позволяет оценить не только соотношение лактофлоры, создающей нормальную кислотность влагалища, но и выявить рост условно-патогенных возбудител ей, таких как кишечные палочки, стрептококки, стафилококки, анаэробные кокки и др. Причём клинически значимым является рост микроорганизмов в колич естве более чем 10 4 КОЕ/мл.
ПЦР-диагностика позволяет обнаружить специфических возбудителей, вызвавших воспалительный процесс, таких как микоплаз мы, уреаплазмы, гарднереллы, хламидии, вирус герпеса и др. [31] . Для этого исследования врач-гинеколог должен взять мазок из шейки матки.
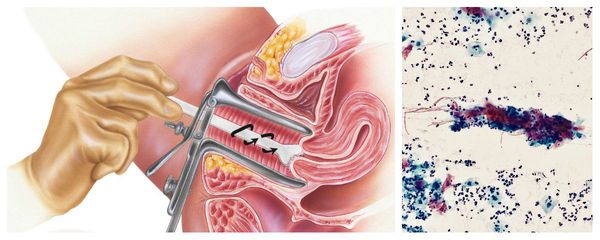
Цитологическое исследование клеточного материала позволяет оценить структуру клеток, характер и уровень их повреждения, а также эффективность лечения в динамике. При длительно текущем воспалении шейки матки в цитограмме преобладают гистиоциты, плазмациты, фибробласты и лимфоидные элементы. При продуктивном воспалении (защитной реакции организма) преобладают клеточные инфильтраты — макрофагальные, г игантоклеточные, плазмоклеточные, лимфоцитарно-моноцитарные. В 40 % случаев цитологическая диагностика позволяет выявить возбудителя заболевания (хламидии, кандиды, трихомонады, цитомегаловирус), более чем в 50 % случаев диагностируется папилломавирус и вирус простого герпеса.
При ультразвуковом исследовании признаками эндоцервицита являются увеличение толщины М-эхо шейки матки более 4 мм и реактивный отёк подэпителиальных о тделов УЗИ. рекомендуется выполнять на 5-7 день менструального цикла.
Следует помнить, что обследование гинекологом и взятие мазков проводятся перед началом менструации или через несколько дней после её окончания: оптимальный срок — пятый день, когда нет мажущих кровянистых выделений. Накануне и в день процедуры не следует использовать вагинальные свечи, тампоны, мази, средства интимной гигиены, поскольку это может стать причиной получения недостоверных данных. Кроме того, необходимо отказаться от спринцевания и воздержаться от половых контактов в течение одного-двух дней до сдачи анализа.
Лечение цервицита
Препараты для лечения цервицита
Определяющим звеном при выборе тактики лечения является природа возбудителя цервицита: вирусные воспаления шейки матки предполагают использование противовирусных препаратов, бактериальные воспаления — приём антибактериальных средств. При этом важно учитывать чувствительность выявленных инфекционных агентов к антибиотикам [1] [2] [3] .
Главной проблемой лечения цервицита шейки матки являются наличие нескольких возбудителей (микст-инфекции) и устойчивость возбудителей к антибактериальным препаратам. В таких случаях необходимо прибегнуть к приёму комбинации антибиотиков. Конкретные препараты назначает врач.
Иногда антибиотикотерапия сопровождается назначением фитопрепаратов, биологически активных добавок. Также рекомендуются общеукрепляющие физические нагрузки, нормализация режима труда и отдыха [9] [24] .
Помимо лечения пациентки параллельно в обязательном порядке проводится лечение её полового партнёра. Во время терапии необходимо пользоваться барьерной контрацепцией.
Нормали зация микробиоценоза влагалища с помощью пробиотиков [15] в сочетании с иммунокоррекцией (с учётом данных иммунограммы) [5] [16] [19] также целесообразны, поскольку изменённый уровень кислотности среды и возникающий дефицит иммунных факторов способствуют частым рецидивам воспалительного процесса [40] [43] [44] .
Физиотерапия
Кроме того, в ряде случаев назначается физиолечение:
- ДМВ-терапия — лечение дециметровыми волнами частотой от 300 МГц до 3 ГГц, проводится каждый день, предполагает 10-15 процедур продолжительностью 10 минут;
- магнитотерапия — воздействие магнитного поля низкой или высокой частоты, проводится каждый день, предполагает 10-20 процедур продолжительностью 10-20 минут;
- диадинамотерапия — лечение высокочастотным электрическим током, проводится каждый день до появления ощущения болезненной вибрации, предполагает 12-15 процедур;
- СМТ-терапия — лечение низкочастотным электрическим током, проводится каждый день, предполагает 12-15 процедур;
- электрофорез с солями магния — воздействует на область малого таза, проводится каждый день, предполагает 10-15 процедур продолжительностью 20 минут;
- дарсонвализация и лазеротерапия с использованием влагалищных датчиков — проводятся каждый день, предполагает 10-12 процедур [32] .
Деструктивные методы лечения цервицита
Цервицит — это воспалительный процесс, поэтому его лечат медикаментозно. Физические или химические методы применяются при атипии в клетках, покрывающих шейку матки или выстилающих цервикальный канал. Прижигание кислотами, жидким азотом, лазерная вапоризация, аргоноплазменная абляция, электрохирургическая эксцизия для лечения цервицита не используются .
Прогноз. Профилактика
Прогноз заболевания при своевременно начатом лечении благоприятный. При бессимптомном цервиците и отсутствии инфекций, передаваемых половым путём, у пациенток остаётся риск появления выраженных клинических признаков заболевания [30] .
Помимо основного лечения назначаются консультации других специалистов для коррекции различных нарушений (нейроэндокринных, гормональных, иммунных), выявления соматических заболеваний и факторов риска. Это позволит предотвратить повторное развитие цервицита [28] .
С целью профилактики воспаления шейки матки рекомендуется:
- один раз в шесть месяцев посещать гинеколога;
- использовать барьерные средства контрацепции;
- не допускать хронизации заболеваний мочеполовой системы.
Читайте также:

