Инфекционные осложнения в онкологии
Обновлено: 07.05.2024
Резюме
Актуальность Эпштейна - Барр вирусной инфекции объясняется широкой циркуляцией вируса Эпштейна - Барр среди детского и взрослого населения, его тропностью к иммунокомпетентным клеткам с пожизненной персистенцией после первичного инфицирования и полиморфизмом клинических проявлений от субклинических форм, инфекционного мононуклеоза до формирования онкологических, аутоиммунных гематологических заболеваний. Персистенция Эпштейна -Барр вируса приводит к подавлению клеточного звена иммунитета, снижению продукции интерферонов и факторов неспецифической защиты, что способствует реактивации персистирующей инфекции, чаще всего без мононуклеозоподобного синдрома, и появлению атипичных мононуклеаров в крови с формированием лимфопролиферативного, интоксикационного, астеновегетативного синдромов, длительного субфебрилитета, что диктует необходимость применения иммунокоррегирующей терапии. В статье приведен клинический случай, в котором изложены описание и анализ течения хронической Эпштейна - Барр вирусной инфекции у ребенка дошкольного возраста (5 лет 8 мес.) с отягощенным преморбидным фоном. Эпизоды реактивации хронической персистирующей инфекции протекали под маской острой респираторной инфекции с лимфопролиферативным синдромом, гнойного тонзиллита, гнойного аденоидита. Терапия, включавшая антибиотики, препараты с противовирусной активностью коротким курсом, бактериальные лизаты, физиотерапию, имела временный и непродолжительный эффект. В силу отсутствия полного мононуклеозоподобного синдрома в клинике и атипичных мононуклеаров в гемограмме обследование на Эпштейна - Барр вирусную инфекцию не проводилось до пятилетнего возраста, в связи с чем она не была верифицирована, и, соответственно, ребенок не получал адекватной иммунотропной терапии. Только в 5 лет 8 мес. при очередном эпизоде активации хронической Эпштейна - Барр вирусной инфекции в состав комплексной терапии был включен меглюмина акридонацетат, на фоне которого была достигнута хорошая клинико-лабораторная динамика. Описанный клинический случай демонстрирует эффективность включения в состав комплексного лечения Эпштейна - Барр вирусной инфекции меглюмина акридонацетата, обладающего противовирусным, иммуномодулирующим и противовоспалительным действиями, что позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем - и астеновегетативного синдрома и достигнуть перехода активной хронической Эпштейна - Барр вирусной инфекции в латентную форму.
Ключевые слова: острая респираторная инфекция, гнойный тонзиллит, гнойный аденоидит, лимфопролиферативный синдром, меглюмина акридонацетат, иммунотропная терапия.
Chronic Epstein-Barr viral infection in children: a clinical case
Svetlana P. Kokoreva, Veronika B. Kotlova®, Oleg A. Razuvaev
Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia
Abstract
The urgency of Epstein-Barr virus infection is explained by wide circulation of Epstein-Barr virus among children and adults, its tropism to immunocompetent cells with lifelong persistence after primary infection and polymorphism of clinical manifestations from subclinical forms, infectious mononucleosis to formation of oncological, autoimmune hematological diseases. Persistence of Epstein - Barr virus leads to suppression of cellular immunity, decreased production of interferons and nonspecific protection factors, which contributes to reactivation of persistent infection, most often without mononucleosis-like syndrome, and the appearance of atypical mononuclears in blood with the formation of lymphoproliferative, intoxication, astheno-vegetative syndrome, long-term subfebrile condition, which dictates the need for immunocorrective therapy. This article presents a clinical case describing and analyzing the course of a chronic Epstein-Barr virus infection in a preschool child (5 years 8 months) with a pre-morbid background. Episodes of reactivation of chronic persistent infection occurred under the mask of acute respiratory infection with lymphoproliferative syndrome, purulent tonsillitis, purulent adenoiditis. Therapy, including antibiotics, short-course antiviral agents, bacterial lysates, and physiotherapy, had a temporary and short-lived effect. meglumine acridonacetate. The described clinical case demonstrates the effectiveness of the inclusion of meglumine acridonacetate, which has antiviral, immunomodulatory and anti-inflammatory effects, in the complex treatment of Epstein-Barr virus infection, This allowed to obtain fairly rapid positive clinical dynamics of relieving intoxication and febrile and lymphoproliferative syndromes in the acute period, and subsequently - astheno-vegetative syndrome and achieve the transition of active chronic Epstein - Barr virus infection into a latent form.
Keywords: acute respiratory infection, purulent tonsillitis, purulent adenoiditis, lymphoproliferative syndrome, meglumine acridonacetate, immunotropic therapy.
Введение
Сегодня Эпштейна - Барр вирусная инфекция (ЭБВИ) представляет собой междисциплинарную проблему и активно изучается не только инфекционистами, но и врачами других специальностей: педиатрами, оториноларингологами, ревматологами, гематологами, онкологами, неврологами, иммунологами. Это объясняется тем, что вирус Эпштейна - Барр (ВЭБ) является одним из наиболее распространенных возбудителей, выявляемых как в детском возрасте, так и среди взрослого населения. По данным различных исследователей, инфицированность ВЭБ составляет 17,7% в периоде новорожденности и возрастает до 90% и выше у лиц старших возрастных групп 3. Являясь оппортунистической инфекцией, она в большинстве случаев протекает бессимптомно. Особенностью манифестных форм ЭБВИ является полиморфизм клинических симптомов, начиная от инфекционного мононуклеоза до фульминантных тяжелейших форм, аутоиммунных и онкологических заболеваний, реализующихся спустя годы после диагностированной ЭБВИ. Доказано, что манифестация клинических проявлений развивается при первичном инфицировании и реактивации персистирующей инфекции 4.
В случае адекватного иммунологического ответа первичное инфицирование приводит к формированию латентной формы инфекции - персистирующей неактивной ЭВБИ. Приравниваясь к здоровому носительству, она является естественным завершением иммунологических изменений. При снижении иммунитета происходит реактивация инфекции с манифестными проявлениями -активация персистирующей инфекции. При тяжелом течении могут формироваться органные поражения: менингоэнцефалит, миокардит, гепатит, гломерулонефрит и другие с возможным летальным исходом 7.
Но чаще в клинической практике встречаются варианты повторной реактивации ЭБВИ с неспецифической симптоматикой, когда при отсутствии остро развившегося полного мононуклеозоподобного синдрома и появления атипичных мононуклеаров в периферической крови, характерных для инфекционного мононуклеоза, возникают утомляемость, слабость, артралгии, головная боль, снижение памяти и внимания, депрессия, субфебрилитет. При этом принято говорить о хронической инфекции, если симптоматика сохраняется в течение полугода. Дети с хронической ЭБВИ имеют, как правило, отягощенный преморбидный фон, страдают хроническим тонзиллитом, хроническим аденоидитом; у них формируются различные варианты лимфопролиферативного синдрома, умеренно выраженный интоксикационный синдром, астенизация, может быть субфебрилитет; у этой категории больных отмечаются частые рекуррентные заболевания, что объясняется иммуносупрессивным воздействием ВЭБ 12.
Изучение форм ЭБВИ стало быстро развиваться благодаря возможностям современной лабораторной диагностики, которая позволяет оценить время инфицирования и активность инфекционного процесса [15, 16]. Для острой первичной инфекции типично появление ДНК вируса в крови и иммуноглобулинов М к капсидному антигену (аVCAJgM) и (или) иммуноглобулинов к раннему ЕА-антигену (аЕАIgG), которые циркулируют с третьей недели инфицирования, а также низкоавидных иммуноглобулинов к капсидному антигену (аVCAIgG). Со временем низкоавидные аVCAIgG трансформируются в высокоавидные, сохраняясь пожизненно. Начиная со второго месяца с момента заражения появляются антитела к ядерному антигену (аEBNAIgG). У части пациентов они сохраняются всю жизнь, у части -элиминируются. Положительный результат исследования полимеразной цепной реакции (ПЦР) крови не позволяет судить о форме инфекции, так как может регистрироваться как при первичном инфицировании, так и при реактивации персистирующей инфекции. На фоне высокоавидных аVCAIgG и (или) аEBNAIgG при реактивации персистирующей инфекции появляются капсидные антитела класса М и (или) ранние антитела. Давность инфицирования вне обострения инфекционного процесса подтверждается обнаружением высокоавидных аVCAIgG и аEBNAIgG. Положительные результаты ПЦР слюны могут быть у 15-25% здоровых серопозитивных людей. Это происходит в силу пожизненной персистенции вируса в В-лимфоцитах, которые, находясь в лимфоидной ткани миндалин при латентной инфекции или ее активации, дают положительный результат исследования [17].
Иммунокорригирующая терапия Эпштейна - Барр вирусной инфекции
На сегодняшний день общепринятых принципов этиотропного лечения ЭБВИ не разработано, так как препараты с противовирусной активностью не позволяют элиминировать возбудитель из организма, и основой лечения является симптоматическая и патогенетическая терапия. Однако длительная персистенция ВЭБ, приводящая к угнетению клеточного иммунитета, факторов неспецифической защиты, интерферон-продуцирующей функции лейкоцитов, свидетельствует о необходимости использования иммунокорригирующих препаратов [18, 23-26].
В педиатрической практике хорошо зарекомендовали себя индукторы эндогенного интерферона, в частности меглюмина акридонацетат (Циклоферон®), которые имеют ряд преимуществ по сравнению с экзогенными интерферонами. При их назначении не вырабатываются аутоантитела на собственный интерферон, время выработки стимулированных эндогенных интерферонов контролируется макроорганизмом, что не приводит к его передозировке. Кроме того, индукторы эндогенного интерферона имеют высокую биодоступность 31. Циклоферон® является низкомолекулярным индуктором интерферона и, соответственно, оказывает противовирусное, иммуномодулирующее, противовоспалительное действия, стимулируя синтез а- и у-интерферона, что способствует усилению Т-клеточного иммунитета - нормализации субпопуляций СD3-лимфоцитов, СD4-лимфо-цитов, NK-клеток и иммунорегуляторного индекса. Прямое действие меглюмина акридонацетата реализуется через нарушение репликации вируса, блокирование вирусной ДНК или РНК, увеличение дефектных вирусных частиц и снижение вирус-индуцированного синтеза белка [32, 33]. Его клиническая эффективность доказана у детей при острой респираторной вирусной инфекции (ОРВИ) и гриппе, так как на ранней стадии инфицирования он подавляет репликацию вируса, стимулирует и поддерживает уровень всех видов интерферона. Из всех индукторов интерферона Циклоферон является самым быстрым, вызывая продукцию интерферона через 2-72 ч после введения, реализуя таким образом противовирусный и иммуномодулирующий эффекты уже через 2-3 ч после приема 36. Наибольшую эффективность у детей препарат имеет при низком интерфероновом статусе 38. Доказано прямое противовирусное действие Циклоферона с подавлением размножения вируса на стадии репликации и вирусного потомства, его способность индуцировать синтез эндогенного интерферона в отношении герпетических вирусов, и показана его клиническая эффективность у детей при различных герпесвирусных инфекциях, в том числе и ЭБВИ 39. В качестве примера успешного использования иммуно-тропной терапии при герпесвирусной инфекции приводим клинической случай течения и исхода хронической ЭБВИ у ребенка дошкольного возраста.
Anamnesis vitae: ребенок от третьей беременности (в семье есть двое детей 8 и 10 лет), протекавшей с угрозой прерывания (терапия дюфастоном) на фоне хронической фетоплацентарной недостаточности, третьих срочных родов путем кесарева сечения. Вес при рождении -3260 г, оценка по Апгар - 7-8 баллов. По поводу конъюгационной гипербилирубинемии была переведена на второй этап выхаживания. С рождения находилась на искусственном вскармливании в связи с гипогалактией у матери. До года наблюдалась неврологом по поводу перинатального поражения нервной системы, профилактические прививки с 12 мес. Из перенесенных заболеваний мама отмечала нетяжелые ОРИ в 1,5 года и острую кишечную инфекцию в 2 года 4 мес.
Предварительный диагноз - острая респираторновирусная инфекция, осложненная аденоидитом. Синусит (?).
Динамика и исходы. В гемограмме лейкоцитоза нет -9,5 х 10 9 /л, абсолютный лимфомоноцитоз (п4%, с28%, л56%, м12%), СОЭ - 18 мм/час. Биохимические тесты без патологических изменений, СРБ - 3 мг (норма - 0-10). При рентгенологическом исследовании придаточных пазух носа данных по синуситу не выявлено. Получен отрицательный результат ПЦР-исследования мазков из носоглотки (респираторный скрин). Лор-врачом диагностирован гнойный аденоидит. По данным ультразвукового исследования органов брюшной полости выявлялись умеренная гепатомегалия, мезентериальная лимфаденопатия.
Терапия в отделении включала антибиотики (цефтриаксон парентерально), Виферон-1 per rectum 2 раза в сутки, симптоматические средства, физиолечение. На фоне проводимого лечения в течение трех суток состояние ребенка оставалось без убедительной клинической динамики: продолжала лихорадить, сохранялись интоксикационный и лимфопролиферативный синдромы. На четвертый день пребывания в стационаре результаты лабораторного обследования: ПЦР+ крови на ВЭБ, аVCAJgM+ и аVCAIgG+ авидность 100%, аEAIgG–, аEBNAIgG+, что позволило диагностировать реактивацию хронической ЭБВИ. К лечению добавлен Циклоферон в таблетках по схеме на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-е сутки. На третий день у девочки нормализовалась температура, восстановился аппетит, улучшилось самочувствие. Стал менее выраженным лимфопролиферативный синдром: носовое дыхание более свободное, уменьшился насморк. На 10-й день лечения ребенок жалоб не предъявлял. При объективном осмотре меньше выражены гипертрофия небных миндалин 1-й степени, шейная лимфаденопатия (размеры лимфоузлов уменьшились до 0,5 см), гепатомегалия 1,5 см. Выписана с клиническим улучшением с рекомендацией продолжить прием Циклоферона по схеме.
Клинический диагноз - хроническая Эпштейна - Барр вирусная инфекция, реактивация: лимфопролиферативный синдром, обострение хронического аденоидита, астеновегетативный синдром.
При объективном осмотре сохранялась умеренная гипертрофия небных миндалин, пальпировались мелкие, 0,3-0,5 см, безболезненные подчелюстные, передне-и заднешейные лимфоузлы, гепатомегалия отсутствовала, клинических проявлений астеновегетативного синдрома не отмечалось. Гемограмма соответствовала возрастной норме. В лабораторных тестах отсутствовали маркеры активной ЭБВИ: ПЦР крови - ДНК ВЭБ не обнаружено, аVCAJgM отрицательные, аEAIgG отрицательные, обнаружены аVCAIgG с авидностью 100% и аEBNAIgG.
Рисунок. Этапы формирования у пациентки хронической Эпштейна - Барр вирусной инфекции
Figure. Stages of chronic Epstein - Barr virus infection development in a patient
Заключение
Описанный клинический пример демонстрирует течение хронической ЭБВИ у больной в возрасте 5 лет 8 мес. с развитием лимфопролиферативного и астено-вегетативного синдромов. При реактивации хронической ЭБВИ, протекавшей с клиническими проявлениями ОРИ, гнойного тонзиллита, применялись антибиотики, препараты интерферона, глюкокортикостероиды интраназально, физиотерапия с временным эффектом. Назначение Циклоферона в составе комплексного лечения позволило получить достаточно быструю положительную клиническую динамику купирования интоксикационно-лихорадочного и лимфопролиферативного синдромов в острый период, а в дальнейшем -и астеновегетативного синдрома и достигнуть перехода активной хронической ЭБВИ в латентную форму, что подтверждается отсутствием маркеров активности хронической инфекции в течение года после использования Циклоферона.
Информация об авторах:
Кокорева Светлана Петровна, д.м.н., доцент, заведующая кафедрой инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Котлова Вероника Борисовна, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Разуваев Олег Александрович, к.м.н., доцент кафедры инфекционных болезней, Воронежский государственный медицинский университет имени Н.Н. Бурденко; 394036, Россия, Воронеж, ул. Студенческая, д. 10.
Information about the authors:
Svetlana P. Kokoreva, Dr. Sci. (Med.), Associate Professor, Head of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Veronika B. Kotlova, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Oleg A. Razuvaev, Cand. Sci. (Med.), Associate Professor of the Department of Infectious Diseases, Voronezh State Medical University named after N.N. Burdenko; 10, Studencheskaya St., Voronezh, 394036, Russia.
Особенности течения и терапии респираторного микоплазмоза у детей в эпидемический сезон 2020-2021 гг.
Список литературы
References
Онкологические больные являются группой риска в отношении развития инфекционных осложнений. Существуют множество механизмов защиты организма против инфекции. Их развитие – это результат длительного эволюционного пути. Они представляют собой мощный барьер, препятствующий проникновению патогенов внутрь организма, размножению их и, как следствие, развитию заболевания. Степень необычного повышения чувствительности больного к окружающей его микрофлоре зависит от того, какой из механизмов его иммунной защиты поврежден, насколько тяжелы имеющиеся расстройства и как они взаимодействуют между собой.
Выделяют специфические и неспецифические механизмы защиты. К неспецифическим относятся так называемые физические и химические барьеры: кислотность желудочного содержимого, эндогенная микрофлора, сфинктеры, морфологическая целостность кожных покровов, слизистых оболочек [7]. Специфические механизмы представлены клеточным и гуморальным иммунитетом.
Онкологические больные – особая группа больных. У этих пациентов всегда присутствуют дефекты иммунной системы, с чем связано, прежде всего, развитие самого онкологического заболевания. Дефекты Т-лимфоцитов или моноцитарно-фагоцитарной системы (клеточного иммунитета) имеют место при остром и хроническом лимфобластном лейкозе, лимфогранулематозе, после трансплантации костного мозга, трансплантации органов (почек, сердца). Дисфункция В-клеток может привести к развитию хронического лимфоцитарного лейкоза, множественной миеломы. Дефекты гуморального иммунитета, обычно, представлены нарушением выработки брадикининов, фибринолитической системы, системы арахидоновой кислоты и так далее. Кроме того, сама опухолевая ткань вырабатывает биологически активные вещества, обладающие имуносупрессивным действием. Все онкологические больные получают терапию кортикостероидами, химиолучевое лечение, имеют длительные эпизоды нейтропении. Все эти факторы в комплексе способствуют усугублению иммунодефицита, увеличению частоты различных инфекционных заболеваний.
Возбудителями инфекции, как правило, являются те микроорганизмы, которые колонизируют тот или иной орган, то есть являются его постоянными обитателями. Нормальная микрофлора присутствует на поверхности кожных покровов, слизистых оболочках мочевыделительных путей, желудочно-кишечного тракта, дыхательных путей. Это первая линия защиты, препятствующая инвазии патогенов внутрь организма. В норме поверхность кожи и слизистых колонизирована собственной эндогенной микрофлорой, которая представлена стафилококками, стрептококками, энтерококками, гемофильными палочками, коринебактериями, бактериями семейства Enterobacteriaceae. Так, например, слизистая оболочка пищевода колонизирована различными аэробными и анаэробными микроорганизмами, включая зеленящие стрептококки, энтерококки, дифтероиды, стафилококки, пневмококки, молочнокислые бактерии, микоплазмы, вибрионы, нейссерии, гемофильные палочки, дрожжеподобные грибы рода кандида, бактероиды, вейллонеллы, актиномицеты и др. На уровне пищевода, желудка концентрация микроорганизмов составляет от 100 до 100000 бактерий в 1 мл содержимого [6]. Микроорганизмы, представляющие нормальную микрофлору человека, различаются по вирулентности, т.е. способности вызывать инфекционный процесс. Например, бифидо- и лактобактерии никогда не вызывают заболеваний человека, тогда как E.coli, K. pneumoniae, H. influenzae являются частыми этиологическими агентами, их относят к условно-патогенным микроорганизмам. На поверхности кожи, дыхательных путей можно обнаружить Acinetobacter spp., а на слизистой желудочно-кишечного тракта – Pseudomonas aeruginosa. Эти микроорганизмы обладают выраженной патогенностью, возможностью развития резистентных форм за короткий период времени.
Нормальная секреторная функция кожных желез, быстрая регенерирующая активность эпителия, отшелушивание омертвевших эпителиальных клеток также обеспечивают защиту организма, уменьшая количество потенциальных патогенов на поверхности кожных покровов. В секрете слюны, слезной жидкости, секрете цервикального канала и других секреторных жидкостях организма присутствуют вещества, обладающие антимикробным эффектом. К ним относятся, например, лизоцим, N-ацетил мурамил-L-аланинамидаза, IgG, IgA [7]. Они способны агглютинировать (связывать) микроорганизмы, ингибировать их присоединение к рецепторам клеток или препятствовать их размножению.
В условиях нарушения целостности кожных покровов и слизистых оболочек нормальная микрофлора может стать патогенной и привести к развитию как локальных инфекций (фурункулез, стрептодермия, нагноение ран, формирование абсцессов и многое другое), так и системных.
Особенно важна целостность и функциональная активность кожных покровов и слизистых оболочек для иммунокомпрометированных больных, к которым собственно и относятся онкологические пациенты [9]. В следствие иммуносупрессивной терапии, которую получают все больные (кортикостероиды, химиотерапия, лучевая терапия), снижаются секреторная функция кожных желез и регенерирующая активность эпителия, повышается проницаемость кожных покровов для микроорганизмов. Могут возникать воспалительные изменения слизистых оболочек – мукозиты [11]. Например, при вовлечении в процесс слизистой оболочки полости рта развиваются стоматиты, слизистой желудочно-кишечного тракта – эзофагиты, гастриты. Особенно эта проблема актуальна для больных, длительно находящихся в глубокой нейтропении (после высокодозной химиотерапии, трансплантации костного мозга), у которых мукозиты могут представлять собой жизнеугрожающие ситуации [12]. Этиологическими агентами являются бактерии, грибы, вирусы. Чаще всего наблюдается комбинация возбудителей. Бактериальными патогенами будут являться те микроорганизмы, которые ранее являлись нормальной микрофлорой слизистых оболочек, грибы – чаще всего представлены Candida spp., вирусы – вирус простого герпеса 1 и 2 типа (ВПГ1 и ВПГ2). Клиническими проявлениями являются многочисленные эрозии, язвенные дефекты, возможно, наличие беловато-серого налета на их поверхностях. Кроме того, у пациентов с выраженной иммуносупрессией, с длительной глубокой нейтропенией возможна инвазия патогенов в кровь с развитием бактериемии, фунгемии, вирусемии [11].
Целостность кожных покровов нарушается при установке различных имплантируемых устройств (артериальные и венозные катеты, трахео-, холангио-, нефростомы). В настоящее время не существует материалов, используемых для создания этих устройств, которые были бы биологически инертны. Микроорганизмы связываются с их поверхностями (адгезия), формируют отдельные колонии, которые сравнительно быстро (в течение 24 ч) формируют сплошную биопленку. Большинство микроорганизмов, находящихся в составе биопленки, пребывают в состоянии покоя. Однако на отдельных участках периодически возникают очаги размножения, и вновь возникшие клетки выделяются в окружающую среду: кровь, желчь, мочевые органы и т.д. (в зависимости от локализации имплантируемого устройства), вызывая развитие инфекционного процесса.
Всем онкологическим больным в связи с длительным лечением устанавливают центральные венозные катетеры или порты. Внутрисосудистый катетер устраняет необходимость венепункции для взятия образцов крови, кровезаменителей, антибиотиков, цитостатиков. Инфекции являются основным осложнением, связанным с внутрисосудистыми катетерами, причем в 80% случаев они вызываются грамположительными бактериями, как правило, стафилококками. Встречается инфекция наружной части катетера, туннельная инфекция, катетер ассоциированная бактериемия или фунгемия. Возможно сочетание всех перечисленных вариантов. Микроорганизмы, образующие биопленку в просвете катетера, продуцируют гликокаликс (особенно это касается коагулазонегативных стафилококков). Это вещество защищает бактерии от фагоцитов хозяина и ингибирует действие антибиотиков. Наличие данных о подкожной туннельной или перипортальной инфекции, септические эмболы, гипотензия, связанная с использованием катетера, являются показанием для срочного его удаления одновременно с немедленным назначением антибиотиков. Для профилактики катетер ассоциированных инфекций ряд исследователей предлагает использование импрегнированных антибиотиками катетеров, ротацию доставки антибиотиков через многопросветные катетеры, использование антибиотик-содержащих гепариновых растворов.
Онкологические больные зачастую длительно получают антибактериальную терапию препаратами широкого спектра действия. Это связано с эпизодами панцитопении, расширенными и комбинированными оперативными вмешательствами, которые часто сочетаются с термоабляцией, интраоперационной химиотерапией. Встречается нерациональное использование антибактериальных препаратов: назначение антибиотиков при контаминациях тех или иных органов, длительная антимикробная терапия после операций при отсутствии инфекции [1]. Как следствие происходит гибель нормальной микрофлоры кожных покровов и слизистых, замещение ее патогенными штаммами. Инфекционные осложнения у этих больных, обычно, вызваны комбинацией госпитальных микроорганизмов. В результате лечение инфекции у больных становится непростой задачей, требующей слаженной работы микробиологов и клинических фармакологов.
Развитие инфекций у больных является следствием обструкции опухолью тех или иных органов: бронхиального дерева, пищеварительного тракта, мочевыводящих путей, желчевыводящих путей. Например, обструкция просвета бронха опухолевой массой или сдавление бронхиального дерева опухолью извне приводит к развитию воспалительных изменений в легочной ткани [16]. Обструкция просвета пищевода тканью опухоли может привести к развитию аспирационных пневмоний, возможно развитие эмпиемы плевры, медиастинитов [3].
Опухолевая ткань, особенно с распадом, представляет питательную среду для развития микроорганизмов, их количество возрастает многократно, и они, в свою очередь, становятся возбудителями инфекционных осложнений.
В процессе хирургического вмешательства микроорганизмы проникают в исходно стерильные или заселенные нормальной микрофлорой органы и ткани, вызывая их бактериальное загрязнение, происходит изменение местных и общих иммунных реакций организма, что может явиться предрасполагающим фактором развития инфекции в послеоперационном периоде [2].
Химиолучевое лечение часто предшествует хирургическому вмешательству. В процессе терапии происходит повреждение не только опухолевых клеток, но и здоровых клеток организма, в том числе и клеток, ответственных за уничтожение патогенов. В процессе полихимиотерапии происходит подавление ростков кроветворения. В результате развивается лейко-тромбоцитопения. При глубокой лейкопении количество нейтрофилов не превышает 100-500/мм³ Риск развития тех или иных инфекционных осложнений напрямую зависит от глубины нейтропении и ее длительности. Подсчитано, что за один день пребывания в больнице меняется приблизительно половина эндогенной флоры кожи и кишечника больного, находящегося в состоянии нейтропении, при этом обычные грамположительные аэробы и анаэробные бактерии замещаются аэробными грамотрицательными микроорганизмами. Инфекции больным с нейтропенией могут передаваться с пищей и водой, молочными продуктами, свежими овощами, недостаточно термически обработанными мясными и рыбными продуктами. Микроорганизмы (потенциальные возбудители инфекции) обнаруживаются на кранах в ванной, в туалете, в душе. Они представлены энтеробактериями, Pseudomonas spp, Klebsiella spp, Cryptosporidium, Aspergillus spp, Legionella spp. Велика опасность инфицирования энтеробактериями, Pseudomonas spp, Klebsiella spp, Listeria spp, Staphylococcus spp, Streptococcus spp, Salmonella spp, Campylobacter spp, Toxoplasma gondii, грибы [5]. Химиотерапия нарушает функцию реснитчатого эпителия дыхательных путей, сократительную способность желудочно-кишечного тракта, целостность слизистых оболочек, приводит к уничтожению естественной микрофлоры дыхательных, пищеварительных путей и других отделов организма и замещению собственных микроорганизмов госпитальными штаммами. Многие режимы полихимиотерапии включают кортикостероидные препараты. Данная группа лекарственных средств обладает выраженным иммуносупрессивным действием, поскольку, кортикостероиды ингибируют комплемент-индуцированную агрегацию гранулоцитов, повышая тем самым риск развития инфекции [6].
Таким образом, онкологические больные требуют тщательной разработки подходов к профилактике и лечению инфекционных осложнений.
Список литературы:
6. Mims C., Playfair J., Roitt I., Wakelin D., Williams R., Medical microbiology, Mosby, Edinburg, 2002, 584.
7. Tramont C.E., Hoover D.L., Innate (general or non-specific) host defense mechanisms. Basic Principles in the Diagnosis and Management of Infectious diseases. Vol.1, 5th ed. Philadelphia: Churchill-Livingstone, 2000:31.
8. Giamarellou H., Antoniadou A. Infections complications of febrile leukopenia. Infections in the compromised host. Inf. Dis. Clin. of N Am. 2001; 15(2):457-482.
9. Finberg R.W. Infection in cancer patients. Cancer Medicine and Hematology. Harvard Medical School Department of Continuing Education, October 26, 1999.
10. Serody J.S., Shea T.C. Prevention of infections in bone marrow transplant recipients. Nosocomial Infections. Inf. Dis. Clin. Of N Am. 1997 2(2):459-477.
11. Leather H.L., Wingard J.R. Infections following hematopoetic stem cell transplantation. Infections in the compromised host. Inf. Dis. Clin. of N Am. 2001; 15(2):487-520.
12. Ibrahim N.K., Sahin A.A., Dubrow R.A., Lynch P.M., Boehnke-Michaud L., Valero V., Busdar A.U., Hortobagyi G.N. Colitis associated with docetaxel-based chemotherapy in patients with metastatic breast cancer. Lancet 2000; 355(9200):281-283.
13. Segal H.B., Walsh T.J., Holland S.M. Infections in the cancer patient. In: De Vita VT Jr, Hellman S., Rosenberg S.A., eds. Cancer Principles and Practice of Oncology. 6th ed. Philadelphia: Lippincott Williams and Wilkins, 2001:32855-2858.
14. Ang B.S., Telenti A., King B., Steckelberg J.M., Wilson W.R. Candidemia from a urinary tract source; microbiological aspects and clinical significance. Clin. Infect. Dis.1991; 75: 391.
15. Koozeniowski O.M. Urinary tract infections in the impaired host. Med. Clin. N Am. 1991; 75:391.
Copyright © Российское общество клинической онкологии (RUSSCO).
Полное или частичное использование материалов возможно только с разрешения администрации портала.
Инфекции у больных раком при подавлении иммунитета
Инфекции — главные причины смерти при раке. Они не только часто встречаются, но нередко имеют более тяжелое течение, чем у других пациентов, менее подверженных действию терапии, и иногда вызываются организмами, которые не патогенны для здоровых людей. Такая восприимчивость является следствием подавления защитных механизмов больного, вызванного опухолью и ее лечением.
Кожа и слизистые оболочки служат барьером для инфекции. Опухолевая инфильтрация и местная лучевая радиотерапия могут привести к повреждению лимфатических или венозных сосудов, что приводит к увеличению восприимчивости к локальной инфекции. Воспроизводство эпителиальных клеток в желудочно-кишечном тракте подавляется химиотерапией, из-за чего повреждается и изъязвляется слизистая, что позволяет организмам из кишечника попасть в систему воротной вены.
Кожа повреждается внутривенными иглами и канюлями, особенно туннельными подкожными каналами. Это частые источники инфекции, которые вызываются такими кожными организмами, как Staphylococcus epidermidis. В носоглоточной полости возникают инфекции, вызванные Candida albicans.
Рак при запущенной стадии иногда связан с ухудшением функций и нейтрофилов, и моноцитов. Было описано подавление хемотаксической, фагоцитарной и бактерицидной активностей.
Ослабленная замедленная гиперчувствительность довольно распространена при запущенной болезни Ходжкина, но менее часта в других случаях злокачественных опухолей. Лимфопения неизменно вызывается действием алкилирующих агентов и массивной радиотерапией. Клеточный иммунитет особенно важен при защите организма хозяина от грибов, вирусов, туберкулеза и простейших.
Интенсивная цитотоксическая химиотерапия ведет к ухудшению образования антител к бактериальным и вирусным антигенам.
Циркулирующие бактерии удаляются фагоцитарными клетками, находящимися в синусах ретикулоэндотелиальной системы, особенно в печени и селезенке. Для этой чистки важны антитела и белки системы комплемента. Спленэкто-мия увеличивает риск серьезной бактериальной инфекции, особенно пневмококковый сепсис в детском возрасте и в меньшей степени во взрослом.
Возбудители сепсиса
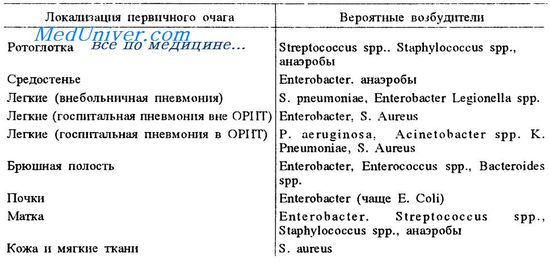
Бактериемия и септицемия у больных раком
Инфекции кровяного русла довольно часты у пациентов с гранулоцитопенией. Патогенами часто являются грамотрицательные бактерии (Escherichia coli, Pseudomonas aeruginosa), стафилококки и стрептококки. Увеличивается частота инфекций, вызванных грамположительными бактериями, особенно Staphylococcus epidermidis. Пациенты с тунельными подкожными каналами особенно подвержены поражениям этим организмом.
Жар у пациента с нейтропенией при раке — показатель присутствия бактерий в крови и под кожей. Если существует очевидный источник инфекции, например инфицированный порт для инфузий, следует взять культуру бактерий и удалить канюлю. Лечение не следует откладываеть для пациента с нейтропенией. Пациенты с лихорадочной нейтропенией с относительно низким риском развития серьезных осложнений относятся к тем, кого лечат короткими циклами химиотерапии для солидных опухолей.
Эти пациенты должны быть госпитализированы. Недавние исследования показали, что пероральный прием амоксициллина-клавуланата комбинированный с пероральным приемом ципрофлоксацина так же эффективен, как и внутривенная химиотерапия в этой группе (70% пациентов). Пациенты с высоким риском (с неконтролируемым раком или на стационарном лечении интенсивной терапией) лечатся внутривенными антибиотиками, в том числе b-лактамом и аминогликозидом или цефтазидимом.
Респираторные инфекции у больных раком
У пациента с серьезным подавлением иммунитета довольно часто возникает жар с легочным инфильтратом. Главные причины этого даны в таблице.
Осложнения в постановке диагноза могут быть значительны, поскольку тесты слюнных и кровеносных культур иногда отрицательны, а более инвазивные процедуры, такие как трансбронхиальная биопсия, невозможны из-за тромбоцитопении или общего состояния пациента.
Существуют некоторые клинические особенности, которые помогают при постановке диагноза. Кавитация наиболее часто сопровождает поражения анаэробными бактериями, стафилококками и микобактериями. Инфекции Pneumocystis вызывают заметную одышку, а на рентгенограмме грудной клетки видны билатеральные инфильтраты, обычно состоящие из хилуса. Болезнь, однако, может протекать вяло и вызвать долевое уплотнение. Цитомегаловирусные инфекции встречаются главным образом у пациентов с серьезным подавлением иммунитета, в частности в течение аллогенной ВМТ. Болезнь может также вызывать миокардит, невропатию или офтальмию.
Легочные инфильтраты обычно билатеральны. Инфекции Candida вызывают широкое разнообразие изменений в рентгенограмме. Инфекции Aspergillus обычно быстро прогрессируют. Тесты культур крови обычно отрицательны, а инфильтраты возможны в одном или двух легких.
При затруднениях в постановке диагноза можно следовать следующей схеме.
У пациентов без нейтропении или тромбоцитопении исследовать посевы крови, слюны, бронхоскопические промывания и трансбронхиальную биопсию там, где это возможно. Если кровяные и слюнные культуры отрицательны, лечить антибиотиками широкого антибактериального спектра действия (обычно в комбинации с аминогликозидом, пенициллином и метронидазолом или аналогичными соединениями). Если возможной причиной инфекции является Pneumocystis, следует давать высокие дозы котримоксазола. Если ответа нет, рассмотрите ацикловир для вируса простого герпеса и противогрибковую терапию с амфотерицином или кетоконазолом. Ацикловир не эффективен против цитомегаловирусов.
Если кровяные или слюнные тесты положительны, лечите соответствующе, но если ответа нет, рассмотрите смешанные инфекции.
Пациентам с нейтропенией или тромбоцитопенией проводят бронхоскопию, но биопсия не всегда возможна, и лечение продолжают без дальнейшего диагностического исследования. До и после бронхоскопии иногда необходимы антибиотики и переливание тромбоцитов.

Инфекции мочевыводящих путей у больных раком
Инфекции часты у пациентов с затрудненным мочеиспусканием. Затруднения могут быть вызваны опухолью или ослаблением мочевого пузыря у пациентов с компрессией спинного мозга и его корешков. Диагноз ставится после исследования уринокультуры, и лечение осуществляется антибиотиками и снятием осложнений, если это возможно.
Желудочно-кишечные инфекции у больных раком
Молочница ротовой полости (инфекция, вызываемая Candida albicans) — частое осложнение химиотерапии. Она особенно распространена у пациентов с подавленным иммунитетом, у пациентов, принимающих стероиды и тех, кого лечат антибиотиками с широким спектром действия. Рот и глотка становятся очень болезненными, а белые пятна грибков видны на эри-темной основе. У плохо питающихся пациентов инфекция может проникать глубже и распространяться по пищеводу, желудку и кишечнику. Обычно эффективен пероральный прием нистатина, амфотерицина или миконазола.
Проявление вируса простого герпеса на губах часто проблематично для пациентов с лейкопенией, и повреждения могут быть довольно обширными. В данном случае необходимо местное применение ацикловира для пациентов с подавленным иммунитетом или систематический прием ацикловира при более серьезных инфекциях.
Инфекции, вызванные Candida в пищеводе, необходимо лечить пероральным приемом суспензии нистатина, но если такое лечение неэффективно, то необходимо применение кетоко-назола или короткий курс амфотерицина. Кишечные инфекции, возникающие при поражении Candida, должны лечиться амфотерицином.
Перианальные инфекции распространены среди пациентов с нейтропенией. Всегда необходимо применять профилактические меры совместно с тщательной гигиеной промежности и смягчителями стула для предотвращения запора и анальных трещин. Распространяющиеся перинеальные (паховые) инфекции могут угрожать жизни пациента, и требуется срочное лечение внутривенными антибиотиками, действующими против грамотрицательных и анаэробных бацилл.
Менингит у больных раком
Инфекции центральной нервной системы (ЦНС) довольно редки, но у пациентов с лимфомой или лейкемией иногда развивается менингит из-за Cryptococcus neoformans. Начало заболевания индивидуально у каждого и сопровождается головной болью. Микроорганизм обнаруживают при окрашивании India ink спинномозговой жидкости (CSF).
Выявление антигенов Cryptococcus в крови и CSF возможно у большинства пациентов. Состояние многих пациентов улучшается при приеме амфотерицина, некоторые вылечиваются.
Кожные инфекции у больных раком
В отличие от инфекции, представленной на портах для вливания, наиболее частое кожное заболевание — опоясывающий лишай (varicella zoster). Возникает из-за реактивации вируса varicella zoster в ганглии дорсального корешка, вызывает кожную пузырчатую сыпь, которая особенно серьезна у людей с подорванным иммунитетом, может распространяться как ветряная оспа и вызывать фатальную пневмонию. Пациентов следует лечить ацикловиром как можно быстрее.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Осложнения у больного при онкологических заболеваниях.
В этой главе анализируются лихорадочные состояния и нарушения дыхания у больных со злокачественными новообразованиями; во второй части речь идет об осложнениях, связанных с гиперлейкоцитозом и неотложными неврологическими состояниями.
1. Решения о проведении любых лечебных вмешательств у онкологических больных в критическом состоянии должны приниматься с учетом целей основной лечебной тактики. Большое значение имеют характер течения основного заболевания, степень истощения больного, нарушения функции различных органов, а также наличие предшествующей химиотерапии. Не описанные в этих двух главах общие для онкологических больных состояния встречаются в других разделах (Кровотечения, Электролитные расстройства, Почечная недостаточность). Неотложные состояния, возникающие вследствие лечебных мероприятий, требуют устранения опасного фактора и симптоматической терапии. В числе осложнений химиотерапии нужно назвать застойную сердечную недостаточность при приеме антрациклинов (в зависимости от дозы), пневмониты, почечную недостаточность в результате приема метотрексата или цисплатины, тромбоз сосудов мозга, при лечении L-аспарагиназой либо блеомицином.
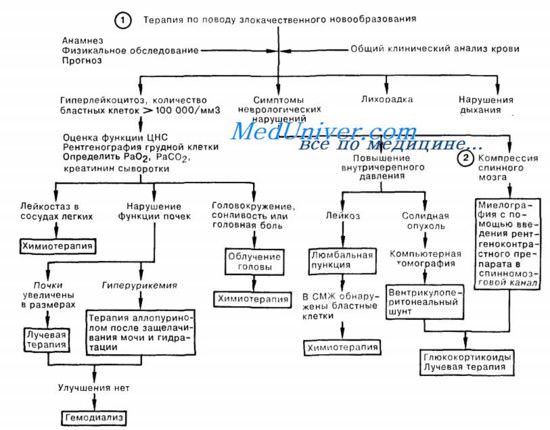
2. Часто встречающийся у онкологических больных иммунодефицит объясняет легкость возникновения оппортунистических инфекций и генерализованного бактериального сепсиса. Высокая вероятность серьезных инфекционных осложнений объясняется нарушением целостности естественных барьеров (например, изъязвление кожи или слизистой ЖКТ, перианальные трещины, катетеризация центральных вен), а также наличием нейтропении (количество нейтрофилов
3. Причиной появления паренхиматозных инфильтратов могут быть: инфекция, химиотерапия (препараты группы нитромочевины, миелосан, блеомицин, циклофосфан, метотрексат), лучевой пневмонит (обычно через 2—6 мес после облучения), либо кровотечения. При инфекции неизвестной этиологии назначают препараты, действующие как на обычные бактериальные, так и на оппортунистические возбудители; например, антибиотики широкого спектра действия в сочетании с амфотерицином; триметоприм/сульфаметоксазолом и эритромицином. Лечение возникшего в результате химиотерапии пневмонита заключается в исключении данного препарата из лекарственной схемы и в некоторых случаях назначения стероидных гормонов. Эмболия легочной артерии наблюдается главным образом при карциономах желудка и поджелудочной железы. Появление объемного образования в средостении с синдромом верхней полой вены чаще всего встречается при лимфомах, других лейкозах и бронхогенной карциноме, но может быть связано с раком пищевода, толстой кишки, молочной железы и яичка. В числе симптомов следует назвать диспноэ, отеки на лице, туловище, а также верхних конечностях. Диагностика основана на немедленной биопсии, если возможно, под местной анестезией; далее проводится неотложная лучевая или соответствующая химиотерапия.
Далее рассмотрены ситуации, в которых у больного с леченным ранее злокачественным новообразованием обнаруживают гиперлейкоцитоз, а также признаки и симптомы неврологического расстройства.
1. Гиперлейкоцитоз при лейкозе с числом бластных клеток более 100000/мкл может привести к фатальным осложнениям вследствие повышения вязкости крови с лейкостазом в сосудах ЦНС и легких, к внутричерепным кровоизлияниям, нарушениям функции почек из-за инфильтрации лейкозными клетками или гиперурикемии, а также к электролитным расстройствам при лизисе опухолевых клеток, сопровождающимся высвобождением внутриклеточного содержимого. По мере возникновения этих осложнений следует незамедлительно проводить соответствующее лечение. До начала терапии добиваются адекватной гидратации больного при щелочной реакции мочи на фоне приема аллопуринола и уровня мочевой кислоты в сыворотке крови менее 0,59 ммоль/л; затем начинают химиотерапию уменьшающимися дозами до снижения числа бластных клеток менее 100000/мкл.
2. Наиболее частыми симптомами сдавления спинного мозга являются боль, парестезии, слабость. Чтобы предотвратить необратимые повреждения, необходимо своевременно локализовать сдавление с помощью компьютерной томографии после введения рентгеноконтрастного препарата и немедленно начать прием глюкокортикоидов и лучевую терапию. Повышение внутричерепного давления вследствие роста первичной или метастатической опухоли требует введения кортикостероидов, неотложного наложения вентрикулоперитонеального шунта, а также начала лучевой терапии. Лейкозное поражение мозговых оболочек, лежащее в основе повышения внутричерепного давления, служит показанием к интратекальному введению противоопухолевых препаратов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Мы продолжаем публиковать главы из книги "Паллиативная помощь онкологическим больным" под редакцией Айрин Салмон (начало - см. "СД" №1'2000).
Слабость при онкологическом заболевании
От этого неприятного симптома страдают 64% раковых больных. При онкологическом заболевании в запущенной стадии слабость - самый распространенный симптом.
Сонливость, усталость, вялость, утомление и слабость переносятся каждым пациентом по-разному. В некоторых случаях ситуация может быть неконтролируемой. Однако причины слабости могут поддаваться лечению. Тщательное обследование пациента и оценка ситуации - первый шаг на пути к решению этой проблемы.
Прежде всего, следует выяснить, испытывает ли пациент локальную слабость или общую. Локальная слабость может быть вызвана церебральными неоплазмами (монопарез, гемипарез), компрессией спинного мозга (в основном билатеральной), повреждением плечевого сплетения, рецидивом рака в подмышечной области, повреждением пояснично-крестцового сплетения, латеральным подколенным нервным параличом; а также мускульной слабостью в проксимальной конечности (кортикостероидной миопатией, паранеопластической миопатией и/или невропатией, паранеопластическим полимиозитом и миастеническим синдромом Ламберта-Итона).
Миастенический синдром Ламберта-Итона (аутоиммунный синдром) - это паранеопластическое отклонение нервно-мускульного пути передачи, возникающее у 3% онкологических больных с мелкоклеточным раком легкого и в нескольких единичных случаях у пациентов с другими видами ракового заболевания, как, например, рак груди и лимфома. Среди клинических проявлений синдрома - слабость ног (у 25% пациентов может проявляться и слабость рук), временная диплопия (двоение в глазах), дизартрия, дисфония, дисфагия, сухость во рту, запор.
Общая прогрессирующая слабость может означать, что пациент близок к смерти. Но стоит принять во внимание и другие возможные причины. Причинами общей слабости могут быть анемия, гиперкальциемия, гиперфункция надпочечников, невропатия, миопатия и депрессия. Общая слабость может быть вызвана последствиями хирургического лечения, химиотерапией и лучевой терапией, а также применением медицинских препаратов (диуретиков, гипотензивных препаратов, гипогликемиков), гиперкалиемией, бессонницей, утомлением, болью, одышкой, общим недомоганием, инфекцией, дегидратацией, нарушением питания.
В зависимости от ситуации пациенту должно быть назначено соответствующее лечение.
Медсестра должна помогать пациенту в соблюдении правил личной гигиены, наблюдать за состоянием кожи и ротовой полости, чтобы исключить возможные осложнения.
Следует убеждать пациента в необходимости принимать пищу и питье (пища должна быть по возможности высококалорийной), а также помогать ему при приеме пищи, если пациент слишком ослаб. Нельзя оставлять ослабленного пациента без наблюдения при приеме горячей пищи или питья. Необходимо также оказывать ему помощь при посещении туалета, обеспечивая при этом достаточное уединение.
Медсестра должна оказывать пациенту психологическую поддержку, проявлять дружеское участие, чтобы повысить его самоуважение и способствовать проявлению интереса к жизни. Следует воодушевлять пациента, но не принуждать его.
Чувство слабости, неспособность совершать привычные действия могут вызвать у пациента стрессовое состояние. В этом случае помогает спокойное обсуждение создавшейся ситуации. Например, медсестра может сказать больному: "Да, вы сейчас не в состоянии делать многое из того, что могли делать раньше. Но если мы попробуем сделать это вместе или отложим до того момента, когда вы будете чувствовать себя немного лучше, то у нас все получится".
Сестринский уход должен быть направлен на то, чтобы предупредить возможные осложнения или неприятные ощущения, связанные с ограниченной подвижностью пациента. Так, чтобы предотвратить вызывающую болевые ощущения контрактуру, следует проводить массаж конечностей и рекомендовать пациенту пассивные упражнения, а правильно зафиксированное положение слабых конечностей поможет предотвратить повреждение суставов.
Компрессия спинного мозга
Данный симптом появляется у 3% пациентов с запущенным онкологическим заболеванием. При этом более чем 40% случаев компрессии спинного мозга встречаются у пациентов с раком груди, бронхов и простаты, остальные 60% случаев - у пациентов с раком почек, лимфомой, миеломой, саркомой, раком головы и шеи.
Компрессия спинного мозга в 85% случаев бывает вызвана распространением метастаз в тело позвонка или питающую ножку, в 10% - распространением опухоли через межпозвоночное отверстие (особенно при лимфоме), в 4% - интрамедуллярной первичной опухолью.
Чаще всего (в 90% случаев) компрессия спинного мозга приводит к возникновению болевых ощущений, в 75% случаев - к слабости, в половине случаев - к появлению сенсорной недостаточности и в 40% случаев - к нарушениям функции сфинктера.
Появление болевого синдрома обычно происходит за несколько недель или месяцев до появления других симптомов и признаков компрессии спинного мозга. Возникновение болевых ощущений может быть вызвано метастазами в спинной мозг, сдавливанием нервного корешка, компрессией длинного нервного пути спинного мозга.
Наиболее пессимистичный прогноз бывает у пациентов с быстро развивающейся полной параплегией (за 24-36 часов); это почти всегда вызвано инфарктом спинного мозга вследствие давления опухоли и тромбоза позвоночной артерии. Также плохой знак - потеря функции сфинктера. В лучшем положении находятся пациенты с парапарезом.
Основными терапевтическими мерами в случае возникновения компрессии спинного мозга является назначение кортикостероидов, которые позволяют быстро уменьшить околоопухолевое воспаление, и лучевой терапии, которая приводит к уменьшению опухоли, но за достаточно продолжительное время.
Хирургическое вмешательство показано в тех случаях, когда нет улучшений после стероидной и лучевой терапии, когда имеются единичные метастазы в позвоночник или если диагноз под сомнением.
Медицинская сестра при уходе за пациентом с компрессией спинного мозга должна оказывать ему психологическую поддержку, так как пациент, как правило, испытывает страх, беспокойство, подавленное состояние из-за вынужденной зависимости от других людей. Медсестра должна помочь пациенту адаптироваться к новому образу жизни, обеспечить его необходимым оборудованием.
Сестринский уход включает в себя также ряд мер по предотвращению осложнений (пролежни, проблемы с мочевой и пищеварительной системами и др.), обучение пациента приемам самопомощи, а членов его семьи - методам ухода; выбор и выдачу лекарственных препаратов, а также анализ их воздействия на организм больного.
Спутанность сознания
Спутанность сознания - состояние человека, которое характеризуется дезориентацией во времени, пространстве и окружающих его людях, вследствие чего больной запутан, смущен, его мысли беспорядочны, а действия нерешительны. Обычйо это состояние бывает вызвано какими-либо органическими нарушениями, а также может быть следствием сильного эмоционального стресса и различного рода психических и психиатрических отклонений.
При появлении спутанности сознания, прежде всего, необходимо проанализировать причины возникновения подобного состояния пациента.
Среди распространенных причин возникновения спутанности сознания отмечаются болезнь Альцгеймера, церебральный атеросклероз, неоплазмы, биохимические изменения, недостаточное функционирование какого-либо органа, СПИД, множественный склероз, применение определенных лекарственных препаратов, изменение окружающей обстановки, депрессия, утомление, боль, запоры, задержка мочеиспускания, инфицирование, дегидратация, авитаминоз, применение алкоголя или психотропных препаратов, курение.
Причин острой спутанности сознания на терминальной стадии онкологического заболевания достаточно много (см. таблицу). При этом две главные причины (острый и хронический мозговые синдромы) обычно проявляются в комбинации с второстепенными.
Необходимо также внимательно проанализировать историю болезни пациента, получить как можно больше информации от родственников больного. Следует установить, имеются ли у пациента какие-либо повреждения органов чувств, такие как глухота, потеря зрения, были ли в прошлом длительные периоды, когда пациент был не в полном сознании, каково было умственное состояние больного до появления симптома спутанного сознания, происходили ли какие-либо изменения в схеме приема медицинских препаратов. Необходимо также выяснить уровень знания пациента о своем диагнозе, имеются ли у него какие-либо сосудистые или инфекционные заболевания, состояние кишечника и мочевого пузыря, испытывает ли он болевые ощущения и т.д.
При уходе за онкологическим больным со спутанным сознанием следует особое внимание обратить на окружающую его обстановку. Комната такого пациента должна быть тихой и хорошо освещенной, из нее необходимо убрать все предметы, которые могут нарушить его покой. Следует сократить количество персонала, ухаживающего за таким пациентом до минимума, чтобы помочь ему быстрее освоиться и привыкнуть к окружающим его людям. Нужно также попросить кого-то из членов семьи больного остаться и помочь ухаживать за ним (это особенно важно в первую ночь после госпитализации).
К больному с нарушенным процессом мышления необходимо проявлять то же уважение и внимание, что и к остальным пациентам - он заслуживает этого не меньше их. Следует также учитывать, что возникновение спутанности сознания у пациента с тяжелым онкологическим заболеванием может нанести глубокую психологическую травму членам его семьи. Для них, уже смирившихся с мыслью, что близкий им человек умирает, бывает нестерпимо видеть, как он теряет свою личность, перестает быть тем, кого они знали и любили. В этой ситуации им также необходимы внимание и поддержка.
В действиях медсестры, ухаживающей за пациентом со спутанным сознанием, должны присутствовать уверенность и доброта. Ей необходимо использовать все свои знания, весь свой опыт, чтобы найти верную тактику общения с пациентом. Те пациенты, которые раньше занимали позицию лидера в обществе, часто лучше воспринимают информацию и легче идут на контакт, чем те, кто обладает нерешительным характером.
Медсестре следует ориентировать пациента во времени и пространстве, делиться с ним последними новостями, разговаривать, периодически напоминая ему свое имя, постоянно объяснять и комментировать свои действия. Будет полезно, если в комнате пациента будут находиться свежие газеты, часы и календарь. Медсестре следует как можно больше общаться с родственниками больного, чтобы лучше узнать и понять его.
Очень важно вести ежедневные записи наблюдений и оценки состояния пациента, которые должны максимально полно и подробно отражать все, что происходило с ним в течение дня.
Следует постоянно держать под контролем факторы, способные ухудшить ситуацию. Если организм больного обезвожен, ему нужно постоянно пить; следует изъять лекарства, которые оказывают отрицательное влияние на организм пациента, необходимо бороться с инфекцией, если это необходимо (по назначению врача и в зависимости от ситуации), лечить запоры, по возможности исправлять метаболические/биохимические отклонения.
При терминальном возбуждении/активации - редком состоянии, которое иногда предшествует смерти (за несколько дней или часов до нее), когда пациент проявляет нехарактерное для него беспокойство, которое он не может контролировать, так как находится без сознания, введение седативного средства часто бывает единственной возможностью помочь.
Читайте также:

