Интоксикация головного мозга после инсульта
Обновлено: 25.04.2024
Осложнения употребления кокаина со стороны нервной системы
Около 10—30 % инсультов у молодых пациентов вызвано употреблением наркотиков, причем у 30- и 40-летних пациентов эта цифра возрастает до 90 %. По этой причине диагностика молодых пациентов с инсультом включает анализ на содержание наркотиков в организме. Наркотики, наиболее часто вызывающие инсульт, являются симпатомиметическими агентами.
Это амфетамины, фенилпропаноламин, фенциклидин, метилфенидат, кокаин и опиаты, например героин. За прошедшие 10 лет кокаин стал наиболее распространенным веществом, вызывающим инсульт. Неврологические симптомы развиваются спустя 3—6 ч после употребления кокаина в большинстве случаев инсульта, обусловленного данным наркотиком.
Инсульты поражают как лиц, употребляющих кокаин впервые, так и тех, кто злоупотребляет наркотиком длительное время, независимо от пути попадания последнего в организм.
Алкалоидная форма кокаина способна вызвать как окклюзивный, так и геморрагический инсульт. Гидрохлоридная форма чаще всего обусловливает геморрагический инсульт. Употребление кокаина чревато как субарахноидальными, так и внутричерепными кровоизлияниями. Почти в 80 % случаев наблюдаются аневризма или артериовенозные злокачественные образования.
Ангиографическое исследование черепа рекомендуется в случаях внутричерепного кровоизлияния, вызванного употреблением кокаина, особенно при долевом или внутричерепном кровоизлиянии.
В настоящее время кокаин является наиболее распространенным нелегальным наркотиком, вызывающим черепно-мозговые заболевания у взрослых. У наркоманов, нюхающих "крэк", с одинаковой частотой отмечаются ишемические и геморрагические черепно-мозговые заболевания. Гидрохлорид кокаина (при интраназальном и внутривенном введении), как правило, вызывает геморрагический инсульт.
а) Кокаин как причина субарахноидального кровоизлияния. Пациенты с внезапными приступами сильной головной боли, возникающими спустя несколько минут или часов после употребления кокаина, особенно в сочетании с тошнотой, рвотой, онемением в шее и потерей сознания, должны быть обследованы на предмет возможного субарахноидального кровоизлияния.
Причиной осложнений являются патологические изменения (черепная аневризма или артериовенозные злокачественные образования) в анамнезе. Пациенты могут находиться в гипертензивном или нормотензивном состоянии.
б) Кокаин как причина внутричерепного кровотечения. Внутричерепные кровотечения, вызванные употреблением кокаина, могут сопровождаться головной болью, преходящей или постоянной потерей сознания, изменением сознания или неврологическими аномалиями с латеральными признаками. У отдельных пациентов отмечаются фоновые нарушения (аневризма, артериовенозные злокачественные образования, опухоли). Кровоизлияние обычно диагностируется посредством компьютерной томографии.

в) Кокаин как причина ишемического инсульта. Кокаин может вызывать ишемический инсульт у лиц, злоупотребляющих этим наркотиком, по-видимому, в результате гипертензии, развивающейся под воздействием наркотика с последующим образованием вазоспазма и ишемии. Кокаин блокирует поглощение серотонина и тем самым активно повышает его уровень. Серотонин является сильным сосудосуживающим веществом и может снижать поступление крови в мозг.
Церебральный васкулит также может привести к инсульту. Средствами диагностики являются артериограмма и биопсия. Васкулит бывает вызван курением "крэка". У пациентов могут наблюдаться гемиплегия, нарушение речи, парестезия и расстройство артикуляции. Компьютерная томография обычно выявляет область инфаркта, однако на первоначальном этапе она может дать негативный результат. Синдром передней спинномозговой артерии, а также латеральный медуллярный синдром также бывают связаны с употреблением кокаина. Употребление "крэка" может вызвать эмболию.
г) Кокаин как причина преходящего нарушения мозгового кровообращения. Употребление кокаина обусловливает преходящее нарушение мозгового кровообращения в системе среднецеребральной и вертебробазилярной артерий. При поступлении пациента в больницу неврологическое обследование может дать нормальные результаты. Результаты компьютерной томографии и исследования спинномозговой жидкости также могут быть в норме. Данное состояние, по-видимому, является следствием вазоспазма.
д) Кокаин как причина инфаркта мозга. В одном случае у новорожденного наблюдался инфаркт мозга вскоре после рождения. Мать употребляла 5 г кокаина за 3 сут до родов и 1 г за 15 ч до родов. Через 16 ч после рождения у ребенка развились удушье и цианоз, а также многоочаговые судороги и правосторонний гемипарез. Наличие инсульта было подтверждено компьютерной томографией. В течение 4 сут в моче ребенка выявляли бензоилэкгонин.
е) Припадки от кокаина. Припадки отмечаются у 2—10 % пациентов, поступающих в отделение "скорой помощи" по поводу кокаиновой интоксикации. По словам очевидца, припадки, вызванные кокаином, наблюдались спустя примерно 90 мин после употребления наркотика. Большой эпилептический припадок отмечался спустя 12 ч после употребления кокаина. У пациентов без припадков в анамнезе обычно наблюдается большой эпилептический припадок в результате внутривенного введения кокаина или употребления "крэка".
Результаты сканирования с помощью краниальной компьютерной томографии и ЭЭГ, как правило, в норме. У данной группы пациентов выздоровление обычно происходит без неврологических нарушений. В случае очаговых припадков у пациентов, как правило, наблюдаются инфаркт мозга, субарахноидальное или внутрипаренхиматозное кровоизлияние. Эпилептический статус типичен для кокаиновых наркоманов, без припадков в анамнезе и употребивших кокаин в большом количестве (2—8 г).
У пациентов с припадками в анамнезе, не связанными с употреблением кокаина, после приема наркотика отмечаются очаговые моторные припадки, обычно многократные. Они часто происходят после употребления наркотика через нос. У пациентов с большим эпилептическим припадком результаты краниального КТ-сканирования, ЭЭГ и неврологический исход нормальные.
У пациента с припадками, вызванными употреблением кокаина, могут быть припадки в анамнезе и нормальные результаты обследования либо послеприпадочное состояние. Припадки обычно имеют форму генерализованной тонико-клонической эпилепсии.
Дети, поступающие в городские отделения "скорой помощи" с необъяснимыми припадками, могут относиться к группе риска по кокаиновой интоксикации. Это состояние может служить показанием токсикологического скрининга. Во многих случаях припадок бывает первым в жизни пациента. Припадки также могут быть связаны с гиперадренергическим состоянием (гипертензия, гипертермия и ацидоз) и привести к остановке дыхания. Гиперадренергическое состояние чревато гипертензией и внутричерепным кровотечением, сердечной аритмией, ишемией миокарда и/или тяжелой гипертермией.
Факторы риска. К группе риска в плане развития судорог, связанных с употреблением кокаина, относятся:
(1) лица, у которых наблюдаются прямые судорожные эффекты, обычно в результате употребления больших доз (2—8 г);
(2) женщины с повышенным по сравнению с мужчинами риском припадков в связи с употреблением кокаина (однако связанная с кокаином боль в груди отмечается преимущественно у мужчин);
(3) лица с эпилепсией в анамнезе, у которых возможны местные судороги, вызванные кокаином (даже при интраназальном употреблении из-за снижения порога припадка);
(4) лица, хронически злоупотребляющие кокаином, что может привести к "химической" стимуляции эпилепсии.
Причины припадков, вызванных кокаином:
Адренергическая тяга к наркотику
Острые гипертензивные эпизоды
Церебральный вазоспазм
Гипертермия
Внутричерепное кровоизлияние, аневризма, артериовенозные нарушения Васкулит
"Режущие агенты" (эпилептогенные агенты: лидокаин, прокаин, фенциклидин, амфетамины, хинидин)
Метаболический ацидоз в результате интенсивной мышечной активности, гипоксемия, рабдомиолиз или лактат-ацидоз, который повышает чувствительность и усиливает эффект катехоламинов, что может привести к аритмии, гипотензии, церебральной гипоперфузии, аноксии и припадкам
Гипертермия в результате периферийной вазоконстрикции, повышенной активности скелетных мышц, повышенного минутного объема сердца и дисфункции центральной терморегуляции
Фармакологический эффект "воспламенения", когда вводятся повторные дозы кокаина
ж) Головная боль. Кокаин может служить причиной головной боли. Кокаиновая абстиненция также может вызвать головную боль, для снятия которой вновь употребляют кокаин. Кроме того, головная боль бывает связана с травмой головы, полученной во время кокаинового припадка, или травмой головы, полученной по причине употребления наркотиков. Также вероятны субдуральная или эпидуральная гематома или трещина в черепе. При внутривенном употреблении наркотика или у пациентов со СПИДом головная боль бывает вызвана инфекциями центральной нервной системы.
з) Носовая ликворея. Хроническое употребление кокаина приводит к вазоспазму, хроническим воспалительным изменениям и повреждению решетчатой кости. В этом случае необходимо хирургическое вмешательство.
и) Грибковый энцефалит. Внутривенное употребление кокаина иногда приводит к возникновению грибкового энцефалита, эти случаи обычно заканчиваются летальным исходом.
к) Нарушение движений. Злоупотребление кокаином связано со стереотипными движениями, такими как подергивания, поглаживания и тики, синдром Туретта, хорея и дистонические реакции, причем последние могут быть вызваны употреблением "крэка".
л) Абсцесс мозга. Вдыхание кокаина приводит к фронтальному синуситу, который чреват летальным абсцессом мозга. Первоначальные результаты сканирования компьютерным томографом могут быть негативными. Синусовая патология и внутричерепные симптомы у лиц, злоупотребляющих кокаином, должны навести клинициста на мысль о возможном абсцессе мозга.
м) Церебральная атрофия. У лиц, хронически злоупотребляющих кокаином, без скрытых признаков инфаркта мозга, а также без серьезной травмы головы, инфекции ВИЧ и других неврологических заболеваний в анамнезе компьютерная томография может выявить рассеянную лобно-височную церебральную атрофию.
н) Синдром кокаинового вымывания. У пациентов после многодневного наркотического эксцесса часто диагностируют пониженный уровень сознания. Они реагируют только на энергичные стимулы и даже после этого не могут говорить, назвать свое имя или выполнять простые команды. Они настолько истощены, что не способны ни говорить, ни двигаться. Глубокие сухожильные рефлексы, признак Бабинского, исследование черепного нерва, размер и реакции зрачка, и холодная колористическая проба обычно в норме. Результаты метаболических и структурных исследований также бывают в норме. У большинства пациентов токсикологические анализы не выявляют седативных препаратов. Состояние электролитов, формула крови, поясничная пункция и результаты сканирования компьютерным томографом также в норме. Через 12—18 ч такие пациенты становятся менее сонливыми и их отпускают домой.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Токсическая энцефалопатия представляет собой рассеянное органическое поражение головного мозга, которое может развиться как после тяжелых острых отравлений нейротропными ядами, так и при хронических профессиональных нейроинтоксикациях.
Ранними клиническими проявлениями различных хронических интоксикаций в большинстве случаев являются функциональные нарушения центральной нервной системы. При прогрессировании интоксикации происходит постепенное перерастание нейродинамических нарушений в стадию органических изменений - развивается картина токсической энцефалопатии. Органическая природа заболевания нередко может длительное время маскироваться астеническими или невротическими чертами, в связи с чем переход из функциональной стадии в органическую не всегда выявляется своевременно.
К веществам, которые способны вызывать рассеянные повреждения мозговых тканей, относятся:
- пестициды,
- продукты нефтеперегонки,
- соли тяжёлых металлов,
- химические составы бытового предназначения,
- нейротропные медицинские препараты (снотворные, транквилизаторы),
- угарный газ,
- пары ртути,
- свинец,
- мышьяк,
- марганец,
- спиртосодержащие жидкости,
- бактериальные токсины, образующиеся при ботулизме, кори, дифтерии.
Основные типы интоксикаций при энцефалопатии
Выделяют два основных типа интоксикаций: острую и хроническую:
- Острая токсическая энцефалопатия наступает в результате однократного, сильного воздействия отравляющего вещества на организм. Острое состояние требует срочной медицинской помощи и последующих реабилитационных мероприятий.
- В условиях систематического влияния отравления имеет место хроническая форма повреждения тканей мозга. Она наступает на поздних стадиях развития болезни, когда организм уже не способен противостоять длительному воздействию отравления. Больному требуется долгий курс лечения.
Клиническая картина
Для начальной формы токсической энцефалопатии характерна следующая симптоматика: жалобы на упорные головные боли, головокружение, снижение памяти, общую слабость, повышенную утомляемость, нарушение сна и др. На фоне резкой астенизации появляется рассеянная органическая симптоматика, которая не укладывается в картину какой-либо четко очерченной нозологической единицы (асимметрия лицевой иннервации, девиация языка, легкая гипомимия, рефлексы орального автоматизма, высокие сухожильные рефлексы, часто анизорефлексия, ослабление или исчезновение кожных рефлексов). Наряду с этим наблюдаются нарушения психоэмоциональной сферы: снижение памяти, внимания и умственной работоспособности, медлительность, заторможенность, апатия, немотивированная тревога, угнетенное настроение, выраженная эмоциональная лабильность.
Наиболее часто при токсических энцефалопатиях страдают стволовой и диэнцефальный отделы, нередко в процесс вовлекаются мозжечковая, оптико-вестибулярная и экстрапирамидная системы. Общей особенностью токсических энцефалопатий является рассеянность поражения. Однако каждое токсическое вещество придает заболеванию свои клинические особенности. Так, при марганцевой энцефалопатии на фоне диффузной патологии головного мозга начинают вырисовываться очаговые подкорковые симптомы. При энцефалопатиях, обусловленных хроническим воздействием окиси углерода, клинической особенностью является развитие церебрально-кардиальных ангиодистонических расстройств, протекающих на фоне органического диффузного поражения головного мозга. Нарушения координации движений, потливость, дрожание конечностей, галлюцинации, приступы раздражения и агрессии характерны для отравлений алкоголем.
Нарушения психики при различных энцефалопатиях также имеют некоторые особенности. Так, для сероуглеродной энцефалопатии характерны понижение активности, отсутствие инициативы, угнетенное настроение, тоска, равнодушие ко всем, прежде интересовавшим больного сторонам жизни. Такой же астенодепрессивный синдром часто возникает при энцефалопатиях, развившихся вследствие хронической интоксикации этилированным бензином. Ртутной энцефалопатии свойственно сочетание повышенной эмоциональной возбудимости с растерянностью, болезненной застенчивостью, нерешительностью и неуверенностью в себе.
Сроки развития токсических энцефалопатий различны. Так, при интоксикациях сероуглеродом и марганцем энцефалопатия развивается значительно быстрее, чем при хронической интоксикацией алкоголем, ртутью, свинцом или окисью углерода.
Течению токсических энцефалопатий свойственны стойкость патологических проявлений, наличие остаточных явлений в отдаленном периоде и наклонность к прогрессированию вне контакта с токсическим агентом. Патологоанатомические данные указывают, что в основе токсических энцефалопатий лежат сосудистые поражения головного мозга и рассеянные дегенеративные изменения мозговой ткани.
Лечение токсической энцефалопатии головного мозга
Устранение причин, давших толчок болезни, является безотлагательной мерой в тактике лечения токсических энцефалопатий. Контакт больного с ядовитой средой должен быть прекращён. В большинстве случаев пациенту предлагается госпитализация. Первичные назначения врача состоят в детоксикационных мерах. Пациенту назначаются антидоты, нейтрализующие действие ядов. Лекарство подбирается в соответствии с типом отравляющего вещества. Общие мероприятия по детоксикации заключаются в очистительных клизмах, стимуляции диуреза, проведении плазмафереза и гемодиализа.
Следующим этапом лечения являются меры по улучшению кровообращения в сосудах мозга и активизации метаболических процессов. Больному показаны внутривенные и внутримышечные вливания следующих препаратов:
- кавинтон,
- пирацетам,
- церебролизин,
- актовегин,
- цераксон,
- глиатилин.
Для внутримышечного введения назначаются витамины В, С, Р. Перорально пациент принимает биостимуляторы и адаптогены: экстракт женьшеня, лимонника, элеутерококка, препараты на основе алоэ.
По симптоматическим показаниям могут быть назначены транквилизаторы, миорелаксанты, противосудорожные и седативные средства, антидепрессанты:
- реланиум,
- карбамазепин,
- мидокалм,
- сирдалуд,
- амитриптилин,
- тералиджен,
- паксил,
- анафранил.
После стабилизации состояния в курс лечения включаются физиотерапевтические комплексы. Эффективными признаны массаж, иглорефлексотерапия, гидротерапия, грязелечение.
Последствия и прогноз токсических энцефалопатий
Успех лечения больных с поражением мозговых структур во многом зависит от степени тяжести состояния, при которой пациент стал получать медицинскую помощь.
Запущенные болезни не могут быть полностью излечены, а глубокие церебральные изменения не поддаются корректировке. Квалифицированная помощь будет наиболее действенной на ранних стадиях процесса.
Наличие остаточных явлений и прогрессирование болезни без контакта с ядовитыми агентами характерно для отравлений. Но это не означает, что больной лишается надежды на исцеление. Даже в случае инвалидизации самочувствие может стать вполне удовлетворительным при условии проведения полного курса лечебных процедур.
Регулярные реабилитационные мероприятия необходимо проводить на протяжении дальнейшей жизни. Эти меры позволят замедлить дегенеративные процессы в тканях мозга и восстановить многие утраченные функции.

Спирт является сильным ядом, разрушающим все ткани и системы организма. Алкогольный инсульт – это острое нарушение кровообращения из-за повышенного артериального давления, которое происходит на фоне постоянного отравления этанолом при длительном запое. Без оперативно оказанной помощи состояние приводит к инвалидизации или смерти.
Причины, виды, симптомы алкогольного инсульта
Токсины этанола при длительном злоупотреблении спиртным любой крепости разрушают эритроциты, что приводит к ухудшению кровоснабжения, свертываемости крови. Стенки сосудов теряют эластичность и не способны выдерживать повышенное давление. Происходит разрыв и кровоизлияния.
Алкогольный инсульт делится на два типа:
1. Ишемический. Встречается у 85 % алкоголиков. Случается вследствие закупорки артерий головного мозга тромбом, в результате чего к отдельным участкам перестает поступать кровь. Происходит кислородное голодание. Клетки мозга начинают погибать. При несвоевременном оказании помощи 25 % пациентов погибают. Еще 18 % больных умирают после повторного ишемического инсульта в ближайшие 1-5 лет.
2. Геморрагический инсульт. Встречается реже, но намного опаснее. Его причиной является разрыв стенок артерии головного мозга из-за резкого скачка артериального давления.
Первым признаком алкогольного инсульта является транзиторная ишемическая атака (ТИА), или микроинсульт. Это кратковременное нарушение мозгового питания, которое у непьющего человека может пройти самостоятельно. Так как в организме алкоголика истощены возможности и ресурсы для восстановления, после проявления ТИА максимум в течение суток наступает инсульт. ТИА можно распознать по таким симптомам:
- потеря равновесия, ориентации в пространстве, невозможность самостоятельного передвижения;
- помутнение или временная утрата зрения;
- нарушение речи;
- расстройство восприятия;
- резкая головная боль, которая может сопровождаться сильным головокружением, повышением температуры;
- онемение конечностей;
- возможна потеря сознания.
После появления первых признаков инсульта наблюдается улучшение самочувствия на небольшой период. Затем симптоматика нарастает, и состояние резко ухудшается. Опасность инсульта заключается в том, что его симптомы напоминают сильную абстиненцию и формируются обычно на ее фоне. На начальном этапе состояния легко перепутать. Именно поэтому при проявлении признаков абстиненции или похмелья у алкоголиков рекомендуется не заниматься самолечением, а сразу обращаться к врачу. Несвоевременное оказание помощи может стоить больному жизни.
Последствия алкогольного инсульта
Инсульт приводит к гибели клеток головного мозга, что в некоторых случаях вызывает необратимое нарушение его функций. Последствия зависят от степени поражения, типа инсульта и скорости оказания неотложной медицинской помощи:
- нарушение двигательных функций на несколько месяцев или даже лет;
- расстройство речи;
- депрессивное состояние, агрессивное поведение;
- психические расстройства;
- частичная или полная потеря памяти, которая может и не восстановиться;
- невозможность самостоятельно обслуживать себя, выполнять элементарные действия вроде причесывания и чистки зубов.
Риск частичной и полной инвалидизации, смертности у запойных алкоголиков в 2 раза выше, чем у непьющих людей. Чтобы предотвратить осложнения, многие из которых необратимы, стоит отказаться от вредной привычки.
При подозрении на алкогольный инсульт нужно немедленно вызвать скорую. Чем быстрее окажут помощь пациенту, тем больше шансов на восстановление и спасение жизни.
Лечение инсульта
Первичное лечение после инсульта проводится в стационарных условиях. Оно включает медикаментозную и восстановительную терапию. Основные препараты для стабилизации жизненных показателей вводятся врачами скорой. Первую помощь нужно оказать в течение 5-6 ч после приступа. Тогда шансы на восстановление значительно увеличиваются.
Медикаментозная терапия включает:
- препараты для понижения давления;
- медикаменты для разжижения крови и предотвращения дальнейшего тромбообразования;
- препараты для нормализации кровообращения;
- антиоксиданты.
После улучшения состояния проводится реабилитационная терапия:
- лечебная гимнастика с индивидуально подобранным комплексом упражнений для восстановления двигательной активности;
- занятия с логопедом-дефектологом для восстановления речевых функций;
- лечебный массаж, в том числе водный.
В течение всего восстановительного периода пациент принимает препараты для стабилизации деятельности нервной системы, антидепрессанты. Реабилитация – это длительный процесс, который зависит от стараний самого больного, выполнения врачебных предписаний, индивидуальных особенностей организма. Только 5-10 % пациентов восстанавливаются после алкогольного инсульта при условии, что поражение было незначительным, а помощь оказана оперативно и профессионально.
Можно ли пить алкоголь после инсульта
После инсульта и реабилитации образ жизни придется изменить раз и навсегда, чтобы исключить его повторения. Помимо соблюдения диеты и постоянной поддерживающей терапии, необходимо навсегда отказаться от алкоголя. Малейшая доза спиртного может вызвать новый приступ и смерть. Если человек после болезни все еще испытывает тягу к спиртному, которую не может преодолеть самостоятельно, нужно обратиться к врачу-наркологу. Кодирование после инсульта запрещено, так как может вызвать осложнения.
В клинике доктора Шорина проводится безопасное лечение алкогольной зависимости любой степени тяжести психотерапией. Есть групповые, индивидуальные сеансы, а также реабилитационный центр с санаторными условиями. Одновременно с основным лечением алкозависимости проводятся занятия умеренной физической активностью, йогой, прогулки, физиотерапия, что также способствует восстановлению после инсульта. При необходимости проводятся консультации узкоспециализированных врачей.
Алкогольный инсульт лучше предотвратить, чем проходить длительную восстановительную терапию или погибнуть от приступа. Поэтому при запойном алкоголизме лучше не медлить с лечением и обратиться в наркологическую клинику, чтобы избежать смертельно опасного осложнения.
Энцефалопатия – это собирательное название, включающее однотипные поражения головного мозга, возникающие под действием различных причин. Патологический процесс сопровождается гибелью отдельных нейронов и разрушением связей между ними. При отсутствии медицинской помощи приводит к прогрессирующему ухудшению состояния вплоть до полной деградации личности.
Общие сведения
Энцефалопатия возникает на фоне нарушения метаболизма в клетках головного мозга. Вне зависимости от причины, патология протекает по единому сценарию. Сначала происходит снижение активности нейронов, затем – постепенная их гибель. Очаги дистрофии располагаются по всему головному мозгу, что вызывает разнообразную симптоматику.
Повреждения носят необратимый характер, но при своевременном обращении к специалисту и качественном лечении состояние пациента может улучшиться. Оставшиеся неповрежденными нейроны частично берут на себя функцию погибших клеток, и работа головного мозга значительно улучшается. Если заболевание было застигнуто на ранней стадии, пациент сохраняет полную ясность ума.
Причины
Поражение нервных клеток может возникнуть на фоне воздействия разнообразных патологических факторов.
- перенесенная травма;
- острая или хроническая интоксикация солями тяжелых металлов, наркотическими веществами, алкоголем;
- нарушения кровоснабжения (атеросклероз, артериальная гипертония, амилоидоз и т.п.);
- инфекционные заболевания (дифтерия, ботулизм, столбняк и другие);
- нарушения работы печени или почек, сопровождающиеся накоплением токсинов в крови;
- нарушения обмена глюкозы;
- нехватка витаминов (особенно группы В);
- задержка воды, недостаток натрия в крови и спровоцированные этим отеки;
- иммунодефицитные состояния;
- воздействие ионизирующего излучения;
- гипоксия: недостаточное поступление кислорода к клеткам головного мозга.
Врачи выделяют врожденную и приобретенную энцефалопатию. Первая возникает на фоне неправильного течения беременности или родов и, зачастую, развивается еще во время пребывания плода в утробе матери. Ее признаки обнаруживаются сразу после родов или появляются в первые недели жизни. Диагностикой и лечением этого состояния занимаются неонатологи и педиатры.
Приобретенная энцефалопатия встречается уже во взрослом возрасте. Она подразделяется на несколько видов в зависимости от причины гибели нейронов:
В зависимости от скорости развития процесса выделяют энцефалопатию острую и хроническую. Первая может развиться в течение нескольких дней или часов, чаще возникает на фоне сильной интоксикации, травмы, инфекционного процесса. Хронический процесс может протекать годами и десятилетиями.
Степени
Границы между степенями тяжести энцефалопатии условны, но для удобства врачи пользуются следующей классификацией:
- 1 степень: клинические признаки отсутствуют, при детальном обследовании выявляются легкие изменения в структурах мозга;
- 2 степень: симптомы энцефалопатии выражены слабо или умеренно, нередко носят временный характер;
- 3 степень: тяжелые, необратимые изменения, сопровождающиеся грубой симптоматикой, пациент становится инвалидом.
Симптомы
Признаки энцефалоптии зависят от локализации очага разрушения, а также степени развития заболевания. Наиболее часто пациенты и их родственники сталкиваются со следующими симптомами:
- головная боль: может захватывать всю голову или концентрироваться в отдельных ее участках; интенсивность зависит от степени поражения и постепенно нарастает; болевые ощущения плохо купируются приемом анальгетиков;
- головокружение: возникает эпизодически, сопровождается потерей ориентации в пространстве; нередко человек вынужден пережидать это состояние в постели, поскольку малейшее движение способствует усилению симптома; состояние часто сопровождается постоянной тошнотой и рвотой;
- нарушения когнитивных функций: постепенное снижение способности адекватно мыслить является характерным признаком энцефалопатии; человек постепенно становится забывчивым, рассеянным, плохо концентрирует внимание на конкретном процессе и с трудом переключается между различными занятиями;
- эмоциональные и поведенческие нарушения: человек с трудом контролирует свои эмоции, становится раздражительным, плаксивым, быстро возбуждается; по мере прогрессирования заболевания возникает апатия, депрессия и полное нежелание делать что-либо;
- увеличение или уменьшение тонуса мышц; часто сопровождается гиперкинезами (дрожью в конечностях, навязчивыми движениями и т.п.);
- снижение зрения и слуха;
- повышенная метеочувствительность.
У одних пациентов преобладают расстройства поведения, другие перестают нормально владеть своим телом; у третьих страдают, в основном, органы чувств. В тяжелых случаях человек требует постоянного ухода и наблюдения окружающих.
Осложнения
Осложнения энцефалопатии связаны с сильным и необратимым поражением головного мозга и представляют собой предельную степень наблюдаемых симптомов:
- утрата способности к самообслуживанию вследствие двигательных или когнитивных нарушений;
- деменция: потеря знаний и навыков вплоть до полного распада личности;
- потеря зрения и слуха;
- тяжелые расстройства психики;
- судороги;
- нарушения сознания: сопор, кома;
- летальный исход.
Диагностика
Диагностикой и лечением энцефалопатии занимается врач невролог. Обследование пациента включает в себя:
- опрос: сбор жалоб и анамнеза; в обязательном порядке уточняются сведения о перенесенных заболеваниях, травмах, факторах риска, время появления первых нарушений, скорость развития и т.п.;
- неврологический осмотр: оценка рефлексов, чувствительности, мышечной силы, двигательной функции;
- электроэнцефалографию (ЭЭГ): оценка электрических импульсов, возникающих в процессе работы мозга; позволяет выявить признаки эпилепсии, воспаления, наличия опухолей и т.п.;
- УЗДГ сосудов головного мозга и шеи: оценивает качество кровотока в крупных сосудах, выявить участки сужения, оценить объем поступающей крови;
- реоэнцефалография: дополняет УЗДГ, позволяет оценить тонус и эластичность сосудов, обнаружить тромбы;
- ангиография: рентгенологическое исследование сосудов с помощью введения в них контрастного вещества;
- КТ и МРТ: позволяют обнаружить очаги склероза, опухоли, воспалительные очаги последствия инсульта и другие структурные изменении;
- анализы крови (общий, биохимический): дают возможность оценить работу почек, печени, поджелудочной железы, выявить токсины, которые могут повлиять на состояние головного мозга.
При необходимости могут быть назначены другие анализы и обследования, а также консультации специалистов для точного определения причины энцефалопатии.
Лечение
Чем раньше будет начато лечение энцефалопатии, тем больше шансов остановить прогрессирование патологии и восстановить полноценную работу головного мозга.
В первую очередь, необходимо устранить причину поражения нейронов:
- скорректировать уровень сахара в крови;
- стабилизировать артериальное давление;
- восстановить работу печени, почек, поджелудочной железы;
- снизить уровень холестерина в крови;
- вывести токсины;
- нормализовать уровень гормонов и т.п.
Лечение непосредственно энцефалопатии требует назначения препаратов, улучшающих кровоток в сосудах головного мозга и обмен веществ внутри клетки. В зависимости от причины и степени поражения, врачи могут назначить:
- ноотропы (церебролизин, пирацетам): направлены на усиление метаболизма;
- кроворазжижающие средства (аспирин, пентоксифиллин и т.п.): способствуют ускорению кровотока, препятствуют образованию тромбов;
- антиоксиданты: нейтрализуют токсины;
- ангиопротекторы (кавинтон, никотиновая кислота и другие): необходимы для ускорения кровообращения и обмена веществ;
- витаминно-минеральные комплексы, аминокислоты;
- симптоматические средства: успокоительные, противосудорожные препараты и т.п.
При энцефалопатии курсы лечения проводятся регулярно, минимум 2 раза в год. Это позволяет держать заболевание под контролем. Подбор конкретных препаратов и определение дозировки осуществляется только врачом. Единой схемы лечения для всех больных не существует.
Для усиления действия лекарственных препаратов используются немедикаментозные методы лечения:
- физиотерапия (рефлексотерапия, электрофорез, магнитотерапия, лазерная терапия);
- лечебная физкультура для улучшения состояния мышц, облегчения контроля за ними;
- массаж для расслабления и улучшения кровообращения;
- иглоукалывание.
В отдельных случаях (при сосудистой природе энцефалопатии) приходится прибегать к хирургическому лечению:
- устранение тромба из просвета сосудов;
- расширение суженных участков артерии с установкой стента, поддерживающего стенки в правильном положении;
- шунтирование: восстановление кровотока за счет создания альтернативного пути, обходящего пораженный участок.
Профилактика
Энцефалопатия – сложное заболевание. Не существует четкой методики, позволяющей предупредить ее появление и устранить все факторы риска. Врачи рекомендуют придерживаться следующих правил:
- обеспечить себе полноценный режим дня с чередованием труда и отдыха, полноценным ночным сном;
- минимизировать стрессы;
- правильно и сбалансировано питаться, не допускать переедания и избыточной массы тела;
- обеспечить достаточное поступление витаминов и микроэлементов;
- отказаться от курения, наркотиков, алкоголя;
- в умеренном количестве (не профессионально) заниматься спортом;
- своевременно выявлять и лечить хронические заболевания: гипертонию, сахарный диабет, атеросклероз;
- обращаться к врачу при первых признаках неблагополучия.
- назначим наиболее подходящую терапию, распишем курс лечения и частоту его повторения;
- проведем все необходимые манипуляции (постановка капельницы, внутривенные и внутримышечные инъекции) в комфортабельных условиях дневного стационара и манипуляционного кабинета;
- дополним терапию современными физиотерапевтическими процедурами;
- проведем курс массажа и назначим ЛФК для максимальной эффективности.
Наши неврологи будут контролировать состояние пациента и корректировать лечение при необходимости. Лечение энцефалопатии – это длительный и сложный процесс, но мы готовы за него взяться.
Преимущества клиники
- опытные специалисты, регулярно повышающие квалификацию, чтобы быть в курсе всех новых тенденций в мире медицины;
- современное диагностическое оборудование;
- все необходимое для проведения физиотерапии, массажа, ЛФК;
- собственный дневной стационар для медленного капельного введения лекарственных средств;
- доступные цены на все услуги.
Отек мозга. Определение отека мозга. Причины ( этиология ) отека мозга. Патогенез отека мозга.
Отеком мозга называется увеличение его объема вследствие накопления жидкости в межклеточном пространстве. Увеличение объема мозга за счет интрацеллюлярной жидкости называется набуханием. С точки зрения патофизиологии, данные состояния (отек и набухание) нередко могут развиваться одновременно и взаимно переходить друг в друга, поэтому с клинической точки зрения вполне допустимо оба эти понятия толковать как отек мозга.
Отек мозга относится к вторичным симптомам поражения. Он может быть местным (локальным, перифокальным) или генерализованным (диффузным).
Этиология отека мозга. Отек мозга возникает при многих заболеваниях, поражающих нервную систему: черепно-мозговая травма; инсульт; опухоли и абсцесс головного мозга; энцефалиты и менингиты; при гипоксии; при различных формах окклюзионной гидроцефалии; различных синдромах нарушения осмотического равновесия; общих интоксикациях; инфекциях; ожогах тела; злокачественной гипертонической болезни и др. В эксперименте и клинике доказано, что различные этиологические факторы вызывают патогенетически разные формы отека мозга, но механизмы его нарастания идентичны.
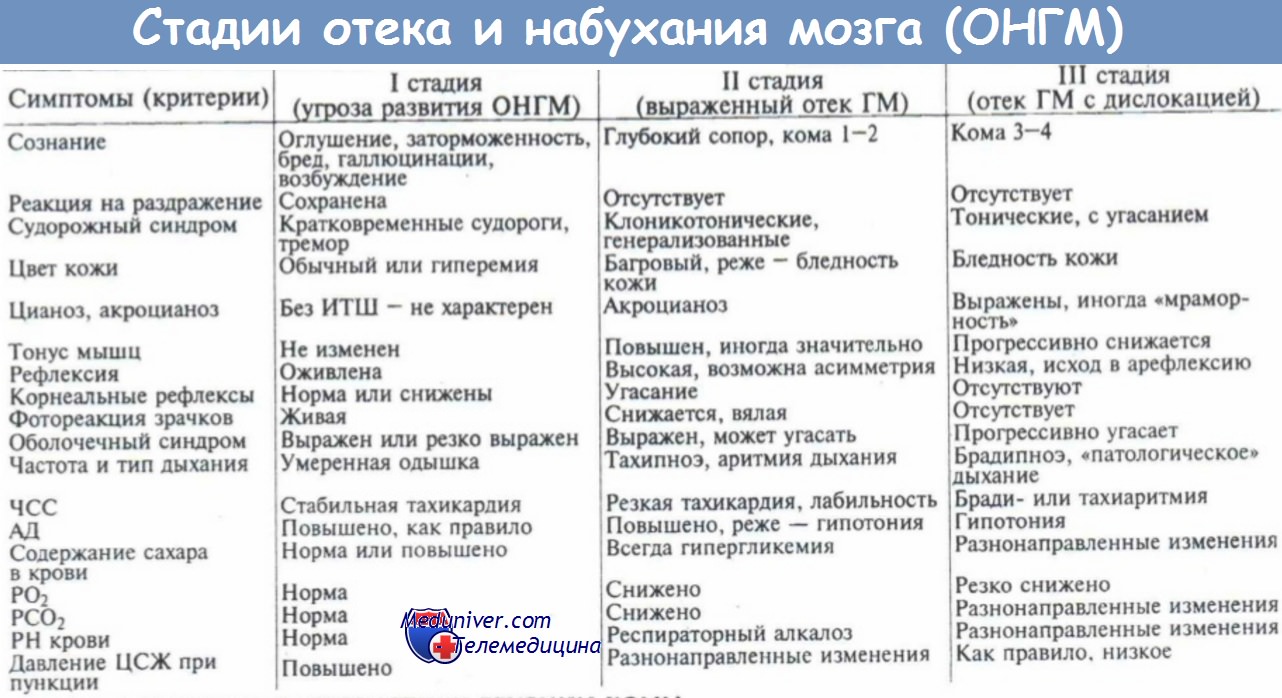
Патогенез отека мозга. Различают четыре типа отека мозга: вазогенный, цитотоксический, осмотический, гидростатический (А. Н. Коновалов, Б. А. Кодашев).
1. Вазогенный отек мозга связан с повышенной проницаемостью капилляров, вследствие чего жидкость из сосудов частично переходит в интерстициальное пространство (в толщу белого вещества), вызывая увеличение его объема. Вазогенные отеки обычно бывают перифокальными. Наиболее часто они наблюдаются при ЧМТ, опухолях мозга, инфекционно-аллергических поражениях ЦНС, геморрагических инсультах и др. (А. Н. Коновалов, Б. А. Кодашев, 1995).
2. Цитотоксический отек мозга возникает при токсическом (экзо- или эндогенном) воздействии на клетки головного мозга, в результате чего нарушается нормальный клеточный метаболизм и изменяется проницаемость клеточных мембран. Данный вид отека встречается при различных отравлениях и при ишемии мозга на фоне ишемического инсульта (А. Н. Коновалов, Б. А. Кодашев, 1995). Цитотоксический отек мозга обратим в течение 6—8 ч прежде всего за счет реактивации ионного насоса, которая может быть достигнута при восстановлении кровотока. Если это не происходит, отек приобретает вазогенный характер (Б. С. Виленский, 1986).
3. Осмотический отек развивается при нарушении существующего в норме небольшого осмотического градиента между осмо-лярностью ткани мозга (она выше) и осмолярностью плазмы. Данный вид развивается вследствие водной интоксикации ЦНС за счет гиперосмолярности мозговой ткани. Этот вид отека наблюдается при метаболических энцефалопатиях (почечная и печеночная недостаточность, гипергликемия и др.) (А. Н. Коновалов, Б. А. Кодашев, 1995).
4. Гидростатический отек обычно формируется при быстром повышении вентрикулярного давления. Накопление жидкости происходит в перивентрикулярной зоне, что четко выявляется при компьютерной томографии (А. Н. Коновалов, Б. А. Кодашев, 1995).
Читайте также:

