Интоксикация после обширной резекции кишечника
Обновлено: 12.05.2024
Осложнения формирования резервуаров после резекции толстой кишки. Питание
Наименее изучены возможности нутритивной поддержки у больных после хирургической коррекции уже возникших постколэктомических нарушений (в частности, при резервуаритах — наиболее частом осложнении в отдаленном периоде после проктоколэктомии с реконструкцией). Сам по себе резервуарит служит причиной илеоанальной дисфункции.
Симптомы: диарея (стул как минимум 4—8 раз в день), инконтиненция или подтекание кишечного содержимого, повышенное газообразование, отхождение слизи и крови. Вторичные симптомы: перианальный дерматит, перианальная боль, зуд и жжение. Системные проявления: лихорадка, внекишечные проявления, гриппоподобная симптоматика.
Резервуарит — морфологический диагноз, при котором выявляются воспаление слизистой, изъязвления.
Выделяют также синдром раздраженного резервуара (такие же симптомы, как при резервуарите, но при полном отсутствии морфовоспалительных изменений). При подборе сред для метаболической коррекции следует учитывать и возможность специфической инфекции в резервуаре (c.difficile, кандидоз, цитомегаловирус) и профилактически применять комбинированную терапию в комплексе нутриционной поддержки.
Клинически: выражены сухость кожных покровов, умеренная жажда, торможение психических процессов (симптомы дефицита водных разделов), урчание и боли в животе, снижение аппетита, жидкий стул с повышенным содержанием газов (дизбактериоз), непереносимость ряда пищевых продуктов, зловонный стул с примесью непереваренных компонентов (симптомы дисфункции поджелудочной железы), дефициты массы тела, натрия, общего белка, альбумина, астения, непостоянные отеки и анемия (показатели белково-энергетической недостаточности), остаточные явления проктита, выделение крови, слизи и гноя из культи прямой кишки (симптомы прогрессирования основного заболевания).
Некомпенсированные потери через желудочно-кишечный тракт после тотальной колэктомии прямо пропорциональны массе суточных испражнений и обратно пропорциональны объему диуреза.
Из хирургических осложнений, связанных с последствиями формирования резервуара, в литературе называют: пролапс резервуара, недостаточный его объем, стриктуру, образование десмоида, свищ, формирование патологической полости (синуса), полип резервуара, обструкцию отводящего сегмента резервуара, изъязвление проксимальнее сформированного резервуара (например, при болезни Крона).
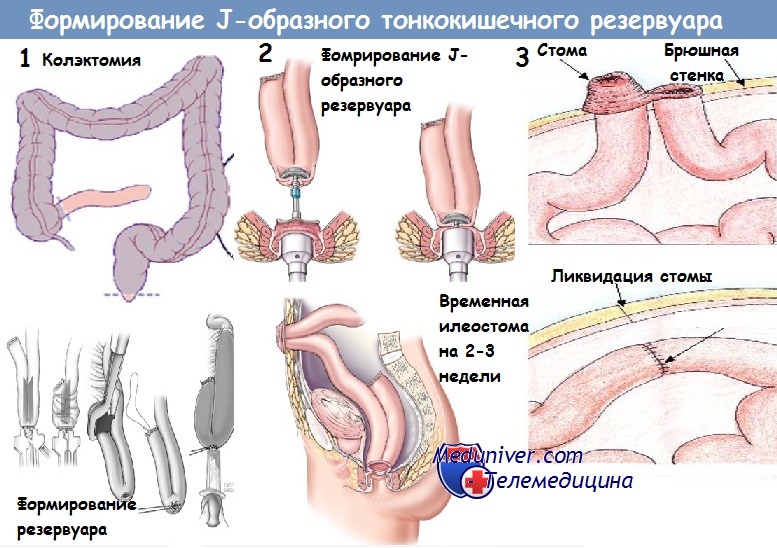
В зависимости от вида осложнения по показаниям проводят оперативное лечение (резервуаропексию, бужирование стриктуры, формирование резервуара заново, рассечение перегородки, мукозэктомию, марсупиализацию патологической полости, удаление резервуара с выведением различных типов стом).
Ведение больных с использованием технологий нутритивной коррекции в таких случаях начинают с новой оценки функциональных резервов лимитирующих органов (в первую очередь, кишечника, печени, почек).
Нутритивную поддержку назначают, опираясь как на синдромный подход, так и на функциональные возможности кишечной культи (в т.ч. ее резервуарных конструкций).
Их постколэктомическая трансформация — основная причина неблагоприятных отдаленных результатов, клинически проявляющихся диареей, колонизацией резервуарных илеоректальных анастомозов, энтеритом с рентгенологическими и эндоскопическими феноменами.
Даже на фоне задержки контраста в области тонкокишечного резервуара до 24 часов функция резервуара остается непредсказуемой. У многих больных резервуар не только не восстанавливает обменные нарушения, но может способствовать прогрессированию диареи (Г.К. Жерлов с соавт.).
В ряде случаев следует быть настороженным в отношении малигнизации резервуара или развития паучита (Н. Stern и соавт., L. Hulten и соавт. и др.), ректального рефлюкса.
Несмотря на то что в последние годы выполнение колэктомии чаще сопровождают формированием резервуарного илеоректального анастомоза со сдерживающим и арефлюксным механизмом, даже макроскопическая динамика стула не всегда восстанавливается в полной мере в течение года после колэктомии, что усугубляет метаболические (в т.ч. нутритивные) расстройства.
В копрограмме в зависимости от сроков, прошедших после оперативного вмешательства и состоятельности адаптивных процессов выявляются различные изменения.
Г.К. Жерлов, С.Р. Баширов, А.И. Рыжов приводят данные копрограммы при различных уровнях резервуарного илеоректального анастомоза.
Приводимые данные свидетельствуют о том, что даже после хирургической реабилитации больных, перенесших тотальную колэктомию или обширные резекции кишечника, остаются нарушения переваривающей функции, двигательные, гомеостатические сдвиги, транслокация микроорганизмов, в свою очередь, ведущая к нарушению межуточного обмена. Поэтому обеспечение нутритивной поддержки таким больным — весьма сложная задача.
Приступая к проведению нутриционной поддержки, нельзя не отметить, что применяя инфузионные среды (внутривенно или через кишку, желудок, даже через рот), мы вмешиваемся не только в белково-энергетический баланс больного организма, но и в другие виды обмена, т.к. невозможно себе представить введение растворов без дополнительного введения жидкости, введение аминокислот без сопутствующей энергетической составляющей, введение глюкозы без инсулина, обеспечивающего ее проникновение в клетку, трансинтестинальное введение растворов (в т.ч. поляризующего действия) без определенных соотношений солей, удовлетворяющих требования по осмотичности смесей, и, наконец, используя смеси натуральных продуктов (нутрихим, ренутрил, составы для сипинга и др.), следует понимать, что уже в самих исходных натуральных ингредиентах этих составов (мясо, морковь, яйца и т.д.) присутствуют в разных количествах (но всегда) и белки, и липиды, и углеводы, и витамины, и соли и т.д.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Высокий риск развития постоперациооных тошноты и рвоты отмечается у лиц, перенесших лапароскопическую операцию и после продолжительной операции, согласно результатам мета-анализов. Во многих исследованиях говорится о высоким риске тошноты и рвоты после перенесены урологических и билиарных вмешательств. В одном из недавних исследований говорится о 35% частоте тошноты и рвоты после резекции кишки.
У пациентов с послеоперационной тошнотой и рвотой отмечается снижение аппетита в послеоперационном периоде, что может приводить к более длительному пребыванию в стационаре.
Целью исследования было определись снижает ли риск тошноты и рвоты предоперационное назначение дексаметазона у пациентов, у которых планируется вмешательство на кишечнике.
Дизайн исследования
Проведено рандомизированное исследование с двумя параллельными группами сравнения в 45 медицинских центрах Великобритании.
В анализ были включены 1350 пациентов в возрасте 18 лет и старше, которым проводилась плановая открытая или лапароскопическая операция на кишечнике по поводу доброкачественной или злокачественной патологии.
Пациентам вводили внутривенно 8 мг дексаметазона перед началом введения анестетиков или проводили стандартную терапию.
В качестве первичной конечной точки было выбрано развитие рвоты в течение 24 часов после операции. В качестве вторичных конечных точек были выбраны: рвота в течение 72 и 120 часов, репортируемые пациентом или врачом, частота послеоперационной тошноты и рвоты в течение 24, 72 и 120 часов, усталость и качество жизни через 120 часов и через 30 дней, время возвращения к приему пищи, длительность госпитализации и частота нежелательных явлений.
Результаты
Из 1350 пациентов 674 были включены в группу дексаметазона и 676 в группу стандартной терапии.
- Рвота в течение 24 часов после операционного вмешательства имела место у 172 участников, получавших дексаметазон (25.5%) по сравнению с 223 из контрольной группы (33.0%), P=0.003. Число пациентов, которое необходимо пролечить, чтобы предотвратить рвоту у одного больного (NNT) составило 13.
- Антиеметические препараты были назначены по требованию 285 лицам из группы дексаметазона (39.3%) и 351 пациенту из группы контроля (51.9%). Показатель NNT составил 8 (95% CI, 5-11; P <0.001). В течение 72 часов сниженная потребность в назначении препаратов сохранялась. Не было отмечено повышения частоты осложнений.
Заключение
Добавление внутривенно однократно дексаметазона в дозе 8 мг в начале анестететической терапии ассоциировано с достоверным снижением риска послеоперационной тошноты и рвоты в течение 24 часов и уменьшением потребности в введении антиеметических препаратов в течение 72 часов у больных, которым проводится операция на кишечнике.
Источник: DREAMS Trial Collaborators and West Midlands Research Collaborative. BMJ 2017;357:j1455.
Обширные резекции толстой кишки. Последствия
Lennard-Jones и Nightingale высказали мнение, что средняя длина кишечника, оканчивающегося стомой (без парентеральной поддержки), должна составлять не менее 100 см. При этом, если по крайней мере половина толстой кишки остается связанной анастомозом с тонкой кишкой, пациент должен оставаться хотя бы с 50 см тонкой кишки.
При обширных резекциях толстой кишки, когда выключаются обе интероцептивные зоны (илеоцекальная и аноректальная), резко страдает моторно-эвакуаторная функция желудочно-кишечного тракта, в связи с чем наблюдаются весьма серьезные нарушения обменных процессов. В случае сохранности тонкой кишки постепенно наступает синхронизация моторной функции вследствие равномерного расширения дистальных участков тонкой кишки — это важный элемент компенсации (В.М. Величенко, И.Н. Сипаров, Н.И. Лобоцкий).
Для уточнения показаний к выбору путей коррекции (парентерального, энтерального, смешанного) при нутритивной поддержке в ЦНИИ гастроэнтерологии был использован метод электроэнтерографии, позволивший оценить функциональные возможности кишечника.
Обследованы больные в возрасте 64,5±5,3 лет в отдаленном периоде после колэктомии (58% из них перенесли левостороннюю гемиколэктомию или резекцию сигмовидной кишки по поводу травмы живота — 1-я группа). Намомент обследования они предъявляли жалобы на запоры, боли в животе, похудание.

Остальным 42% была выполнена правосторонняя гемиколэктомия по поводу диффузного семейного полипоза, карциноида терминального отдела подвздошной кишки, травмы (2-я группа). Эта группа больных на момент обследования жаловалась на диарею, боли в животе, похудание, метеоризм.
В лабораторных показателях пациентов обеих групп отмечался дефицит белка, нарушения электролитного баланса и КОС, снижение трофологического статуса.
По нарушению двигательной функции (по данным регистрации электрической активности — записи биопотенциалов в течение 20—30 минут с последующей статобработкой по программе аппаратно-программного комплекса CONAN-M) эти две группы, однако, различались. В группе с левосторонней гемиколэктомией или резекцией сигмовидной кишки превалировали гипомоторные нарушения. После правосторонней гемиколэктомии преобладали гипермоторные сдвиги. У части больных отмечалась выраженная гипермоторная дискинезия, сопровождающаяся усиленной спайковой активностью, что приводило к возникновению интенсивного болевого синдрома.
После лечения отмечалось снижение амплитудно-частотных показателей медленных волн ЭМА с последующим уменьшением спайковой активности.
Из 1-й группы наиболее тяжело в отдаленном пострезекционном периоде белково-энергетическая недостаточность протекала у пациентов старше 70 лет, что коррелировало с изменениями параметров электрической активности, дисбиотическими изменениями в кишечнике и проявлялось в виде запоров (65% случаев).
Выбор тактики инфузионно-нутриционной поддержки у данного контингента основывался также на четко выставляемом алиментационно-волемическом диагнозе, а параметры электрической активности служили маркером двигательных нарушений кишечника и использовались для уточнения показаний к выбору тактики парентерально-энтеральной коррекции белково-энергетической недостаточности.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Постколэктомический синдром. Патогенез
Последствия радикальных операций на толстой кишке резко снижают качество жизни пациентов. И если синдрому короткой тонкой кишки уделялось и уделяется достаточно много внимания, то последствия гемиколэктомий, проктоколэктомий с реконструкцией стали вновь привлекать внимание специалистов в последние годы. Тем не менее, радикализм колэктомии ставит перед хирургом, а в отдаленном периоде и перед терапевтом, гастроэнтерологом, нутрициологом сложную задачу обеспечения функциональной адаптации кишечника. Решение этой задачи базируется на физиологических и патофизиологических особенностях различных отделов толстого кишечника.
При этом слепая и восходящая кишки всасывают еще и жидкость, и электролиты, витамины, а также утилизируют случайно попавшие из тонкой кишки фрагменты белка, клетчатку.
Поперечно-ободочная кишка выполняет главным образом транспорт кишечного содержимого и лишь частично участвует в регуляции водно-электролитного обмена.
Однако большинство хирургов на основе анализа качества жизни пациентов при сохранении и удалении илеоцекального угла все же придерживаются позиции, что этот отдел функционально значим как регулятор моторной активности и как заслонка от транслокации кишечной микрофлоры в проксимальном направлении, что он принимает участие во всасывании и обмене прежде всего витамина В12.
Левая половина ободочной кишки, особенно сигмовидная кишка, выполняет резервуарную (накопительную) функцию.
Долгое время считалось, что это и есть все основные функции толстой кишки. Однако при анализе последствий обширных резекций толстой кишки и колэктомий, уровня резекций выявляются весьма специфические изменения как в культе толстой кишки, так и в других органах и системах, функционально взаимосвязанных с толстой кишкой (П.К. Климов). Качество жизни большинства пациентов, перенесших обширные резекции различных участков толстой кишки, существенно страдает не только от нарушений, связанных с калообразованием и дизэлектролитемиями, но и от патологических изменений в межуточном обмене, постепенно развивающихся в соответствующих органах.
Поэтому при уточнении программы метаболической (в т.ч. нутритивной) коррекции особое внимание следует уделять лимитирующим органам (печени с ее уникальной дезинтоксикационной функцией, почкам, возможностям верхних отделов пищеварительного канала по обеспечению достаточной перевариваемости и усвояемости вводимых трансинтестинально рационов и др.).
Определяющими же моментами в патогенезе возникающих метаболических нарушений, несомненно, служат выпадения функций отрезков толстой кишки или всей ее поверхности в целом.
Следует отметить, что одним из патогенетически значимых компонентов развития последствий после гемиколэктомий является транслокация микроорганизмов, которые в наиболее значительных количествах и разнообразии представлены в толстой кишке.
Кроме того, в толстой кишке микробная флора обеспечивает переваривание пищевых волокон, клетчатки, которая не усваивается в вышележащих отделах. Этот процесс напрямую участвует в дополнительном энергообеспечении за счет продуктов, синтезируемых толстокишечной микрофлорой (короткоцепочечных жирных кислот — КЦЖК) в процессе ее жизнедеятельности (усвоения ею клетчатки).
Он также принимает участие во всасывании воды, натрия, хлора, кальция, магния.
Адекватная дезинтоксикационная функция толстой кишки также в определенной степени связана с возможностями микробиоты. Другой механизм дезинтоксикации, связанный с микрофлорой толстой кишки, связан с преобразованием билирубина в уробилиноген, который частично всасывается и экскретируется с мочой, а частично тоже выводится с калом.
Локально КЦЖК принимают также участие в регуляции кишечной моторики, что видно на выполненных в ЦНИИГ электромиограммах желудочно-кишечного тракта, позволяющих не только оценить состояние двигательной функции различных отделов кишечника, но и сопоставить, в частности, моторику толстой кишки с сократительной активностью желчного пузыря у больных с право- и левосторонними гемиколэктомиями.
У больных с последствиями левосторонней гемиколэктомии, как правило, наблюдаются выраженное снижение массы тела, боли по ходу толстой кишки и запоры. Это сопоставимо с характеристиками электромиографических кривых холедоха и культи толстой кишки.
У больных с левосторонней гемиколэктомией, как правило, отмечается гипомоторная дискинезия толстой кишки (амплитуда 0,11±0,02 мВ, частота 4,0±0,6 в мин.). После лечения с применением корригирующей питательной смеси для энтерального введения электрическая и двигательная активность толстой кишки имеет тенденцию к восстановлению (амплитуда электрической волны возрастает примерно до 0,2 + 0,02 мВ, частота — до 6,3 + 0,6 отражений в мин.).
У больных с правосторонней гемиколэктомией чаще наблюдаются боли в параумбиликальной области, весьма значительное снижение массы тела, диарея.
У больных с правосторонней гемиколэктомией (выполненной по поводу осложненной болезни Крона) моторная активность гладких мышц билиарного тракта повышена, как, впрочем, и двигательная активность мускулатуры толстой кишки .
Электромиографически: гипермоторная дискинезия толстой кишки с частотой ритма 14,5 ± 1,5 в мин (58,6%) и амплитудой электромиографической кривой 0,17 ± 0,02 мВ.
Лечение пре- и пробиотиками в сочетании с мукофальком приводило к снижению частоты медленных волн электромиографической активности (ЭМА) до 6,0 ± 0,7 в минуту; амплитуда составляла 0,22 ± 0,04 мВ.
Таким образом, электромиографические изменения могут использоваться для уточнения особенностей моторики кишечника после обширных операций на толстой кишке и показаний к выбору тактики энтеральной коррекции ее двигательной активности и общей белково-энергетической недостаточности.
Поэтому роль толстокишечной микробиоты также отражается на липидном обмене, что при колэктомиях и обширных толстокишечных резекциях проявляется липидным дистресс-синдромом.
Иными словами, при нарушениях активности толстокишечной микробиоты можно ожидать:
- нарушения абсорбции холестерина из кишечника;
- нарушения транзита холестерина по желудочно-кишечному тракту;
- нарушения трансформации холестерина в нейтральные стерины и конечные продукты;
- нарушения трансформации холестерина в желчные кислоты и стероидные гормоны;
- повышения синтеза холестерина микроорганизмами;
- повышения синтеза холестерина клетками органов человека.
При выборе тактики сипинговой и парентерально-энтеральной коррекции у больных с обширными толстокишечными резекциями важно обратить внимание на возможный витаминный дефицит, т.к. другая важная метаболическая функция кишечной микрофлоры — синтез витаминов (особенно групп В и К).
Витамин К, как известно, необходим организму для кальцийсвязывающих белков, обеспечивающих функционирование свертывающей системы крови, нейромышечной передачи, структуры костей и др. Он представлен комплексом химических соединений, таких как витамин К1 — филохинон (растительного происхождения), витамин К2 — группа менахинонов, — синтезирующихся более тонкокишечной микрофлорой и др. Однако и при отсутствии значительных участков толстой кишки рядом авторов отмечены проявления недостаточности этих витаминов.
Дело в том, что для нормальной жизнедеятельности самих бактерий толстой кишки также нужны витамины, которые некоторые бактерии синтезируют сами.
Выбирая состав для алиментации рассматриваемого контингента, целесообразно обращать внимание на состояние микробиоты в толстокишечной культе, корригируя ее активность, например, пребиотиками (в т.ч. готовыми промышленными составами для нутритивной поддержки).
Таким образом, определяя тактику нутритивной поддержки при последствиях постколэктомического синдрома или последствиях обширных резекций толстой кишки, в первую очередь необходимо уточнить уровень и объем резекции, особенности клинических проявлений ее последствий, степень функциональной сохранности и выраженность приспособительных реакций.
Удаление всей ободочной кишки, как правило, клинически проявляется признаками некомпенсированных нарушений водно-электролитного, белково-энергетического балансов, выпадением функций регуляторных гормонов, источником которых служит в том числе ободочная кишка: энтероглюкагон, пептид YY, нейротензин, частично мотилин (Мо-клетки).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
На сервисе СпросиВрача доступна консультация онколога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте, Марина!
Не волнуйтесь!
Прикрепите пожалуйста выписку
И скажите : какие лекарства вообще в течение дня приримаете?

Сфотографируйте на камеру телефона документ и прикрепите из галереи- внизу вопроса есть ззачок- " скрепочка"

Спасибо
Хорошо что я запрросила выписки, и не стала сразу рекомендоввть противорвотные лекарства
Потому что они не помогут : у Вас имеется значительно нарушение минерального обмена- возможно как раз по причине плозого аппетита и недостатка питания
Вам необходимо госпитализироваться, и хорошо обследоваться- дома этого сделать не получится

Прикрепиие выписку и последнме анализы. На каком этапе появилась тошнота и рвота? Делали ли вам ЭГДС?

Причиной тошноты и рвоты могут быть разные факторы. В выписке видно у вас высокий калий (нарушена функция почек), это может приводить к тошноте и рвоте.
Также может быть заболевание желудка причиной ваших жалоб, надо делать ЭГДС.
Также это может быть патологическое состояние в животе с учетом недавней операции, у вас было лимфоцеле, вам его дренировали.
С учетом,что вы теряете вес , сложности ситуации (описана выше), в связи с тем что нужен диагностический поиск (здесь нельзя сказать, без обследования, что приводит к вашему плохому самочувствию) требуется госпитализация (смотреть креатинин, электролиты крови, делать эгдс и узи брюшной полости). Без выявленной причины, нельзя назначить лечение.

Здраствуйте. По всем данным может быть патологическое состояние в брюшной полости после проведённой операции. Нужно госпитализировать и начать диагностический поиск где идёт нарушение. Причин может быть много. Обычные противорвотные тут не помогут.
Читайте также:

