К осложнениям сепсиса относятся все перечисленные кроме
Обновлено: 26.04.2024
Сепсис представляет собой заражение крови продуктами гнилостного распада, имеющего место в организме вследствие воспалительного неадекватного леченого процесса. По сути, сепсис - это воспаление, распространившееся на весь организм. Это системный ответ на обильное пребывание в крови бактерий, независимо от места их проникновения и скопления.
Это достаточно опасное для организма состояние, стремительно идущее к летальному исходу и потому требующее немедленной и адекватной терапии.
Вопреки постоянно совершенствующимся медицинским технологиям сепсис сегодня, как и много лет назад остается актуальной проблемой. Для лечения сепсиса используются новые поколения антибактериальных препаратов, однако и это не устраняет болезнь из рейтинга причин смерти в отделениях интенсивной терапии. Примечательно, что 18% из тех, по отношению к кому применялась интенсивная терапия лечения в условиях медицинского учреждения, сталкивались с развитием сепсиса, еще в 63% случаев он сопровождал внутрибольничные инфекции.
К инфекциям, распространение которых по организму рискует завершиться сепсисом, относят:
- бактерии
- стафилококк,
- стрептококк,
- пневмококк,
- синегнойная палочка,
- клебсиелла,
- кандида,
- герпес,
- токсоплазмоз.
Для того чтобы инфекционный процесс в организме перерос в сепсис необходимо сочетание трех обстоятельств:
- наличие возбудителя инфекции;
- отрицательное состояние первичного очага инфекции;
- соответственная реактивность организма.
Риск развития сепсиса обуславливается не столько свойствами инфекции, сколько ее концентрацией в первичном очаге, распространением отсюда вглубь организма и ток крови. Непоследнюю роль играет и резистентность организма, которая легко подавляется под воздействием неблагоприятных факторов. Среди последних:
- любые заболевания
- эндокринные и обменные, в частности сахарный диабет,
- онкологические,
- гематологические,
- иммунологические,
- низкое содержание белка,
- хронические гиповитаминозы,
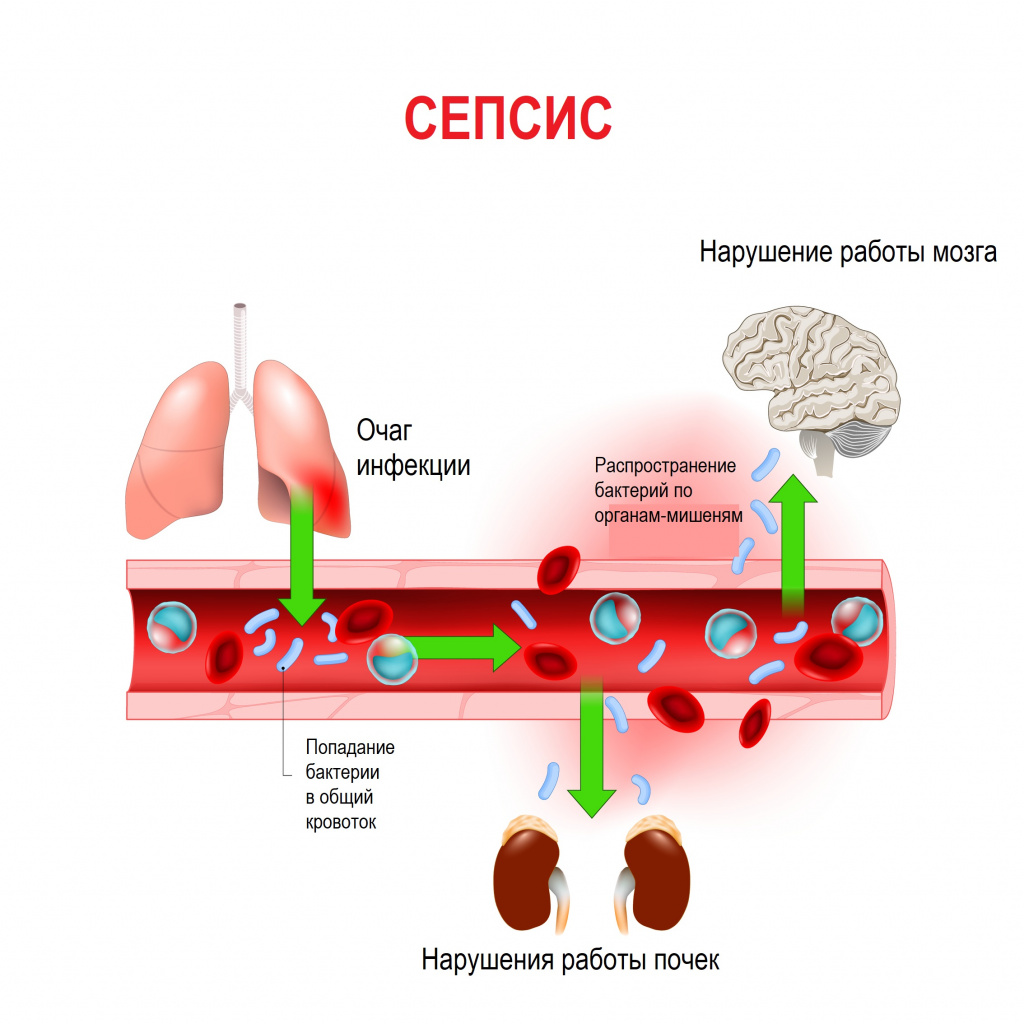
Механизм развития сепсиса берет начало с того, что из первичного очага инфицирования через кровеносные или лимфатические сосуды происходит, соответсвенно, гематогенная или лимфогенная диссеминация инфекции. Следственно, происходит образование вторичных септических очагов, так называемых метастазов, из которых инфекция также распространяется в кровь. Каковой будет локализация метастазов, зависит от типа возбудителя. Гнойники могут образовываться в любых внутренних органах.
![сепсис]()
При сепсисе случаются органно-системные повреждения, чем продолжается механизм заболевания. Это случается в силу отсутствия контроля над распространением провоспалительных медиаторов из первичного очага инфекции. Затем происходит их активация под влиянием макрофагов, нейтрофилов, лимфоцитов и других клеток в любых органах и тканях; повторно выделяются те же провоспалительные медиаторы и повреждается эндотелий.
Разновидности сепсиса
Чаще всего сепсис случается после воспалительного процесса конкретной локализации. Однако не менее распространен и раневой сепсис. И тот, и другой развивается на фоне сниженной резистентности макроорганизма к распространяющейся патогенной микрофлоре и на фоне ослабленного иммунитета. Упадок защитных способностей организма вследствие воспаления, раны, операционного вмешательства или тяжелого заболевания нередко дополняется крупной кровопотерей и недостаточным питанием.
Частыми источниками септической инфекции медики называются нагноения при выше описанных условиях. Нечто подобное способно развиться и при местных гнойных заболеваниях как то фурункул, карбункул, флегмона.
Зависимо от первичного очага сепсиса и его происхождения различают:
- хирургический сепсис - вследствие нагноения в ране, локализированных гнойниках;
- акушерско-гинекологический сепсис - вследствие родов или абортов, случившихся в нестерильных условиях, когда микротрещины или разрывы в родовых путях становятся "входными воротами" для инфекции;
- урологический сепсис - вследствие гнойных процессов и отяжеленных воспалений в мочеполовых органах, что обычно сопровождается и застоем, инфицированием мочи;
- риногенный, тонзилогенный, отогенный сепсис - редкие формы заражения крови, которые берут начало с локализации инфекции в полости рта, носу, околоносовых пазухах, носоглотке, ухе; для того чтобы течение инфекции обрело столь тяжелую форму необходимым условием становится тромбофлебит кавернозного синуса или тромбоз вен клетчатки глазницы, тромбофлебит сигмовидного и каменистого синусов.
Кроме того, выделяют септичемическую и септикопиемическую разновидность сепсиса:
- септицемическая - не сопровождается образованием метастатических очагов гнойной инфекции, однако склонная к перерастанию в септикопиемическую;
- септикопиемическую - характеризуется образованием метастатических очагов гнойной инфекции, откуда происходит все более глубокое распространению инфекции.
Заражение крови может протекать в четырех формах:
- молниеносная - несколько суток;
- острая - 5-7 суток;
- подострая - менее 6 недель;
- хроническая - более 6 недель.
Симптомы сепсиса
Коварство заболевания заключается в риске его симптомов оказаться размытыми. Объясняется это тем, что в разгар первичного заболевания свойства возбудителей поддаются изменениям из-за массивной антибиотикотерапии, несколько угнетаются, однако не всегда сам возбудитель уничтожается. Такое латентное его пребывание в организме чревато дальнейшим распространением даже при относительно невысокой температуре тела. Хотя именно устоявшаяся лихорадка гектического типа считается отличительным признаком сепсиса при наличии предпосылок к тому, то есть выше перечисленных факторов. Кроме нее возможны:
- обильное потоотделение при снижении температуры тела,
- в соответствии со скачками температуры скачкообразным становится и пульс,
- ознобы и головная боль, общая слабость,
- рвота и понос,
- утрата аппетита,
- обезвоживание и стремительная утрата веса,
- землистый цвет кожных покровов (если нарушается функция печени, кожа желтеет), утрата ими эластичности и упругости;
- образование флегмон и абсцессов различной локализации.
Возможны изменения психоэмоционального статуса вплоть до грубых общемозговых расстройств - коматозное состояние. В последующем присоединяются воспалительные изменения со стороны внутренних органов: почек, эндокарда, печени, кишечника, селезенки.
При сепсисе наблюдается тахикардия (более 90 ударов в минуту) и тахипноэ (более 20 вдохов в минуту).
Диагностика сепсиса
Заподозрить сепсис стоит если при инфекционно-воспалительном заболевании, вследствие ранения или операционного вмешательства лихорадка держится более 5 дней, и скачки температуры становятся немотивированными. Лабораторные анализы крови показывают:
- лейкоцитоз;
- лейкопению;
- палочко-ядерный сдвиг влево;
- тромбоцитопению.
Положительные результаты бактериологического исследования крови - обнаружение гемокультуры. Для получения достоверного результата необходим 3-кратный забор крови в объеме 20-30 мл. с интервалами 1 ч. во время подъема температуры по возможности до начала антибиотикотерапии.
При диагностике на предмет наличия сепсиса важно различить:
- синдром системного воспалительного ответа - системная реакция организма на воздействие различных сильных раздражителей (инфекция, травма, операция и т.д.);
- сепсис - та же совокупность изменений, что и при ССВО, но дополнительно обнаруживаются патогенны в одной или нескольких тканях, признаки перитонита, пурпуры, пневмонии и пр.;
- отяжеленный сепсис - клиническая картина сепсиса дополняется гипотензией и гипоперфузией, нарушением функций отдельных органов, например, печени или почек;
- септический шок - тяжелая форма заражения формы, когда нарушение функций не удается восстановить даже интенсивной терапией и реанимирующими мероприятиями; отличается высокой летальностью.
Лечение сепсиса
Лечение сепсиса представляет собой комплекс процедур, которые проводятся преимущественно в условиях медицинского учреждения. Так называемая интенсивная терапия состоит из мер, нацеленных на санацию очага инфекции, и дополняется антибиотикотерапией, призванной устранить инфекцию в крови. Отмечается, что сохранение жизни больного и устранение органных дисфункций не будет возможным без назначения интенсивной терапии.
Этиотропное лечение сепсиса должно быть не просто своевременным, а максимально ранним. Изначально препараты назначаются в столь высоких дозировках, чтобы обеспечить достаточную концентрацию действующего вещества в зараженной крови, а также в очагах инфекции. Этиотропная терапия может быть эффективной лишь при условии выявления возбудителя, конкретной инфекции, а также его чувствительности к выбираемым антибиотикам. Верный выбор антибиотика лежит в основе качественного лечения сепсиса.
Этиотропная терапия длится вплоть до достижения устойчивой положительной динамики состояния пациента и исчезновения основных симптомов инфекции. Если этого не происходит в течение первой недели лечения, необходимо провести дополнительное обследование для выявления осложнений или очага инфекции другой локализации.
Если установить первичный очаг инфекции не удается, равно как и выявить тип возбудителя, как минимум необходимо определить условия возникновения сепсиса - вследствие пребывания пациента в клинических условиях и развития инфекции на фоне определенной болезни (госпитальная форма) или внебольничная.
Как показывает практика, внебольничный сепсис поддается лечению:
- нефалоспоринами 3-го и 4-го поколения,
- фторхинолонами - благодаря широкому спектру действия являются препаратами выбора при лечении инфекций неизвестной этиологии
Госпитальная форма сепсиса лечится:
- карбапенемами - препаратами с широким спектром действия, к которым внутрибольничные штаммы грамнегативных бактерий низкорезистентны.
Лечение разных форм сепсиса определяется его происхождением:
- при анаэробном сепсисе применяются метронидазол, линкомицин, клиндамицин;
- для лечения сепсиса, вызванного грамотрицательными бактериями, уместен препарат с моноклональными антителами против эндотоксина грамотрицательных бактерий;
- сепсис вследствие распространения грибковой инфекции лечится амфотерными оксидами и флуконазолом;
- при стафилококковом сепсисе эффективен противостафилококковый иммуноглобулин, а также внутривенное введение противостафилококковой плазмы;
- когда инфекционный процесс достиг уровня генерализированной септической болезни, назначают ацикловир, ганцикловир, фамцикловир.
Параллельно с этиотропными средствами целесообразно использование пассивной иммунотерапии, среди разнообразия которых предпочтение отдается иммуноглобулину, идеально подходящему для внутривенного введения.
Ведущую роль в лечении сепсиса любой локализации играет инфузионная терапия. Она относится к первичным мероприятиям поддержания гемодинамики и сердечного выброса. Основными задачами, которые стоят перед врачом и которые удается решить посредством инфузионной терапии, оказываются:
- восстановление адекватной тканевой перфузии,
- нормализация клеточного метаболизма,
- коррекция расстройств гомеостаза,
- снижение концентрации медиаторов септического каскада и токсических метаболитов.
Использование этого алгоритма действий способствует выживаемости при септическом шоке и тяжелом сепсисе. Объем инфузионной терапии рекомендуют поддерживать на таком уровне, чтобы давление заклинивания в легочных капиллярах не превышало коллоидно-онкотическое давление плазмы. Это позволяет исключить риск отека легких и увеличить сердечный выброс.
Инфузионная терапия - это составляющая общей целенаправленной интенсивной терапии сепсиса. Для инфузий применяют кристаллоидные и коллоидные инфузионные растворы. Отмечается, что адекватная коррекция венозного возврата и уровня перенапряжения требует вдвое, а порой и вчетверо большего введения кристаллоидов, нежели коллоидов. Инфузия кристаллоидов более связана с риском отека тканей, а их гемодинамический эффект менее продолжителен, чем у коллоидов. Вместе с тем кристаллоиды не влияют на коагуляционный потенциал и не вызывают анафилактических реакций. В связи с этим выбор того или иного раствора диктуется особенностями течения сепсиса в конкретном случае:
- степенью гиповолемии,
- фазой ДВС-синдрома,
- наличием периферических отеков,
- уровнем альбумина крови,
- тяжестью острого легочного повреждения.
При выраженном дефиците объема циркуляционной крови показаны плазмозаменители:
- декстраны,
- гидроксиэтилкрохмал - имеет потенциальное преимущество перед декстранами вследствие низкого риска утечки через мембрану и отсутствия клинически значимого влияния на гемостаз.
В ранние сроки в связи с наличием тромбогеморрагического синдрома назначают гепарин, введение которого проводят под контролем клинических проявлений и коагулограммы.
В случае развития тяжелой степени сепсиса проноз неблагоприятен, оправданным становится гемодиализ. Для профилактики стрессовых язв в пищеварительном канале обязательны ингибиторы протонной помпы или блокаторы гистаминорецепторов. Назначают также препараты, ингибирующие протеолиз.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
![Сепсис_дисфункция.jpg]()
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
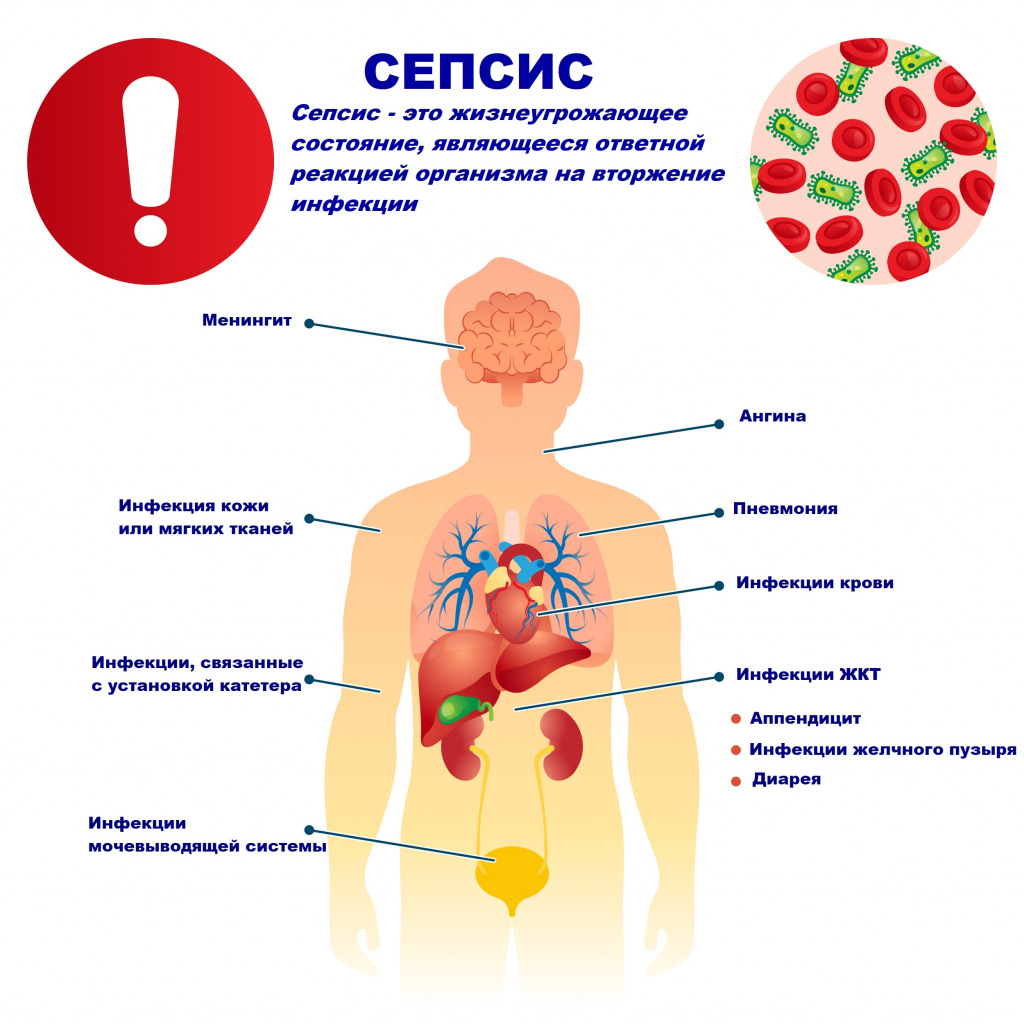
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
![Сепсис.jpg]()
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Столбняк: причины появления, симптомы, диагностика и способы лечения.
Определение
Столбняк представляет собой опасное инфекционное заболевание, вызванное столбнячной палочкой Clostridium tetani. Эта бактерия отличается крайней устойчивостью в окружающей среде: ее споры сохраняют жизнеспособность годами, а при температуре 90°С – около двух часов. Вегетативные формы клостридий погибают через несколько минут в кипящей воде и в течение 3-6 часов после обработки антисептическими и дезинфицирующими средствами. Попадая в рану, бактерии начинают вырабатывать токсин, который оказывает влияние нервную систему, приводя к тяжелым мышечным спазмам и судорогам.
По мере развития болезни спазм мышц вызывает серьезные проблемы с дыханием и в конечном итоге может привести к летальному исходу.
Столбняком можно заразиться в любом уголке земного шара, однако больше всего случаев заражения отмечается в жарких странах с плохой санитарно-гигиенической обстановкой. В странах с умеренным климатом пик заболеваемости приходится на летне-осенний период.
Причины появления столбняка
Огромную роль в распространении инфекции играет отсутствие профилактической вакцинации населения.Столбнячные палочки живут в почве. Путь заражения – контактный. Бактерии попадают в организм через раны, ссадины, при ожогах, обморожениях и т.д.
После попадания в рану бактерии начинают вырабатывать токсин, который проникает в отростки нервных клеток, вызывая спастические сокращения мышц и судороги.
В связи со способностью продолжительно существовать в виде спор в почве, водоемах, на предметах возбудитель столбняка может попасть с пылью и грязью в любые помещения и инфицировать любые поверхности, включая медицинские.
- раневой,
- послеоперационный,
- послеродовой,
- послеожоговый,
- после обморожения,
- постинъекционный,
- столбняк новорожденных.
- локальный (поражаются только близлежащие к ране мышцы),
- генерализованный (поражаются все мышцы организма).
По степени тяжести: легкая форма (от момента заражения до первых симптомов проходит около 3 недель), средняя форма (симптомы появляются спустя 2 недели с момента заражения), тяжелая (симптомы возникают через 9–15 дней с момента заражения), крайне тяжелая (инкубационный период длится всего 3-5 дней).
Симптомы столбняка
Первые симптомы появляются в среднем через 7–10 дней от момента заражения, в редких случаях заболевание может развиться и раньше.
Различают три классических симптома столбняка:
- боль в области раны и иногда подергивание близлежащих мышц;
- скованность мышц живота;
- болезненные спазмы тела, продолжающиеся в течение нескольких минут, как правило, вызванные незначительными явлениями - сквозняком, громким шумом, прикосновением, светом;
- головная боль;
- боль в спине и затылке;
- повышенная потливость.
При прогрессировании заболевания судороги распространяются на мышцы всего тела (опистотонус), больной для облегчения состояния принимает различные вынужденные позы - выгибается дугой, сгибается в сторону или застывает как столб (отсюда и произошло название болезни).
В тяжелых случаях судороги настолько сильны, что могут приводить к разрывам мышц и перелому костей.
Тяжелое течение заболевания сопровождается повышением температуры тела, снижением артериального давления, увеличением частоты сердечных сокращений.
Диагностика столбняка
Как правило, поставить точный диагноз удается на фоне клинической картины при наличии раны, указывающей на возможное заражение.Лабораторная диагностика не проводится, поскольку присутствие антител в крови может указывать на вакцинацию в детстве. При столбняке нарастания титров антител не происходит, так как даже летальные дозы экзотоксина не вызывают иммунного ответа. Ликвор (спинномозговая жидкость) также остается неизмененным, несмотря на поражение нервной системы.
В отдельных случаях применяют бактериологические методы (микроскопию мазков-отпечатков, гистологическое исследование тканей, иссекаемых при хирургической обработке ран, посевы раневого отделяемого на питательные среды в анаэробных условиях), позволяющие обнаружить возбудитель в месте расположения раны. Однако выделить культуру возбудителя из раны удается лишь у 30% больных.
К каким врачам обращаться
При травме с нарушением целостности кожных покровов, обморожении или ожоге следует обратиться к врачу-травматологу или врачу-хирургу, который после осмотра, сбора анамнеза и жалоб направит больного к узким специалистам: врачу-инфекционисту, врачу-неврологу.Лечение столбняка
Лечение больных столбняком проводится только в стационаре. При тяжелом течении заболевания больного госпитализируют в реанимационное отделение.
Для купирования судорог применяют миорелаксанты, нейролептики. В связи с нарушением глотания введение препаратов зачастую осуществляется внутримышечно или внутривенно.
При поражении дыхательных мышц может потребоваться искусственная вентиляция легких.
Обязательным является введение антистолбнячной сыворотки. Причем чем скорее она будет введена, тем больше вероятность нейтрализации токсина.
Хирургическое лечение заключается в обработке раны, удалении инородных тел, назначении антибактериальной терапии при подозрении на присоединение бактериальной инфекции и в целях предупреждения развития гнойного процесса. Зашивать рану нельзя, чтобы не допустить размножения противостолбнячной палочки, поскольку закрытая рана без доступа кислорода является благотворной средой для данной бактерии.
Особое внимание уделяется восполнению жидкости, обеспечению питания с достаточным количеством калорий, насыщенного витаминами и микроэлементами. При выраженном нарушении глотания питание осуществляется жидкими питательными смесями с помощью зонда - специальной тонкой трубки, которую вводят через нос в полость желудка.
Осложнения
Осложнения делятся на ранние, возникающие в самый разгар болезни, и поздние, которые могут оставаться после выздоровления.К ранним осложнениям относятся:
- Инфекции органов дыхания (бронхит, пневмония) - возникают в результате нарушения вентиляции легких, связанного с мышечным спазмом и длительным постельным режимом.
- Инфаркт миокарда – отмечается при тяжелом и крайне тяжелом течении столбняка, поскольку сердечная мышца, как и остальные мышцы организма, может подвергаться воздействию столбнячного токсина. Токсин особенно опасен для пожилых людей и пациентов с заболеваниями сердечно-сосудистой системы.
- Сепсис представляет собой системную воспалительную реакцию в ответ на попадание микроорганизмов в кровоток. Опасность сепсиса состоит в том, что воспалительный процесс затрагивает все органы и системы организма, нарушая их правильную работу, и в ряде случаев может привести к летальному исходу. Лечение сепсиса требует одновременного назначения нескольких внутривенных антибиотиков, постоянного контроля лабораторных показателей крови, пульса, артериального давления, температуры тела, мочеиспускания.
- Переломы костей, вывихи, разрывы мышц характерны для крайне тяжелого течения столбняка.
- Деформация позвоночника.
- Контрактуры мышц и суставов - состояние, при котором мышца или сустав сохраняют ограничение, скованность в движении даже после излечения от основного заболевания.
- Нарушение ритма сердца.
- Временный паралич черепных нервов, самым частым проявлением которого является нарушение функции глотания, двоение в глазах, птоз (опущение) века.
Плановая профилактики включает вакцинацию, которая проводится с рождения ребенка.
В России курс вакцинации против столбняка состоит из 3 прививок АКДС (в возрасте 3, 4,5 и 6 месяцев) и однократной ревакцинации в возрасте 18 месяцев. Далее ревакцинация проводится в 6–7 лет и в 14 лет вакциной АДС-М анатоксином. Последующие ревакцинации проводятся через каждые 10 лет.
Все прививки должны быть внесены в прививочные сертификаты. Полный курс прививок обеспечивает защиту у 95–100% привитого населения.
Экстренную профилактику необходимо проводить у непривитых или неправильно привитых людей при получении любых механических повреждений кожных покровов. Для этого как можно раньше (допустимо до 20 дня с момента травмы) вводят противостолбнячную сыворотку. Перед ее введением проводят пробу с разведенной сывороткой: если диаметр покраснения менее 1 см — проба отрицательная, если 1 см и более — положительная. При отрицательной пробе вводят сыворотку подкожно в наружную поверхность плеча или подлопаточную область. При положительной пробе введение сыворотки противопоказано. В этом случае вводят иммуноглобулин человека.
- Инфекционные болезни: национальное руководство / Под ред. Н.Д. Ющука, Ю.Я. Венгерова. - М.: ГЭОТАР-Медиа, 2009. С. 521–529.
- Рюмин А.М., Соболевская О.Л., Корочкина О.В., Волский Н.Е., Михайлова Е.А., Отмахова И.А., Собчак Д.М., Хряева О.Л. Случай столбняка легкого течения: тактические особенности ведения // Нижегородская государственная медицинская академия. 2017. С. 98–100.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Перитонит: причины появления, симптомы, диагностика и способы лечения.
Определение
Перитонит – это воспаление листков брюшины - ткани, которая выстилает внутреннюю поверхность живота (париетальный листок брюшины) и покрывает большую часть органов брюшной полости (висцеральный листок брюшины). Между двумя листками брюшины находится брюшинная полость, в которой содержится небольшое количество серозной жидкости, увлажняющей брюшину и обеспечивающей свободное движение органов. Брюшина выполняет ряд важных физиологических функций:
- всасывающая или резорбтивная – брюшина может всасывать в сутки до 70 литров содержимого брюшной полости (секретируемую жидкость, экссудат, продукты распада белков, форменных элементов крови, клетки некротических тканей, бактерии, токсины);
- выделительная, или экссудативная, заключающаяся в способности брюшины выделять жидкость и фибрин;
- защитная, или барьерная – брюшина осуществляет как механическую защиту органов брюшной полости, так и обладает гуморальными и клеточными механизмами защиты;
- пластическая – в ответ на раздражение брюшина способна выделять фибрин и образовывать спайки, тем самым ограничивая распространение воспалительного процесса.
Несмотря на развитие медицины, смертность от перитонита в мире колеблется от 4,5 до 58% и выше. Если развивается сепсис, септический шок и полиорганная недостаточность, то смертность увеличивается до 70%.
Причины появления перитонита
Основная причина развития перитонита - попадание в брюшную полость инфекции. Бактериальный перитонит чаще всего вызывает неспецифическая микрофлора желудочно-кишечного тракта, в 60-80% случаев это смешанная инфекция – кишечная палочка и стафилококк. Благодаря бактерицидным и иммунным свойствам брюшины для каждого микроорганизма существуют свои условия для возникновения перитонита.
Среди хирургических патологий к развитию перитонита может привести перфорация полого органа: у пациентов с травмой органов брюшной полости, перфоративной (прободной) язвой желудка или двенадцатиперстной кишки, при перфорации аппендикса или кишечника, в случае несостоятельности желудочно-кишечных и межкишечных анастомозов. Патологическое содержимое поступает в брюшную полость, бактерии в больших количествах производят токсины, которые затем поступают в кровеносную и лимфатическую систему. Вследствие попадания токсических продуктов в кровоток развивается интоксикация организма (эндотоксикоз). Резко угнетается перестальтика кишечника и развивается паралитическая кишечная непроходимость.
Токсины провоцируют выброс провоспалительных цитокинов, которые приводят к нарушениям работы жизненно важных органов и систем.
Классификация заболевания
На настоящий момент в России принята и утверждена классификация перитонита, согласно которой выделяют:Врачи и анатомы разделяют брюшную полость на 3 этажа и 9 областей – надчревную, правое и левое подреберья, пупочную, правую и левую боковые области, лобковую, правую и левую паховые области.
В зависимости от того, сколько областей захватывает перитонит, выделяют:
- местный перитонит (захватывает 1-2 анатомические области), который бывает отграниченным (абсцесс) и неотграниченным;
- распространенный перитонит, который делится на диффузный (3-5 анатомических областей) и разлитой (более 5 анатомических областей или 2 этажа брюшной полости).
Наконец, перитонит подразделяют по тяжести состояния в зависимости от выраженности системной воспалительной реакции (отсутствие сепсиса, сепсис, тяжелый сепсис, септический шок), и по наличию послеоперационных осложнений.
Симптомы перитонита
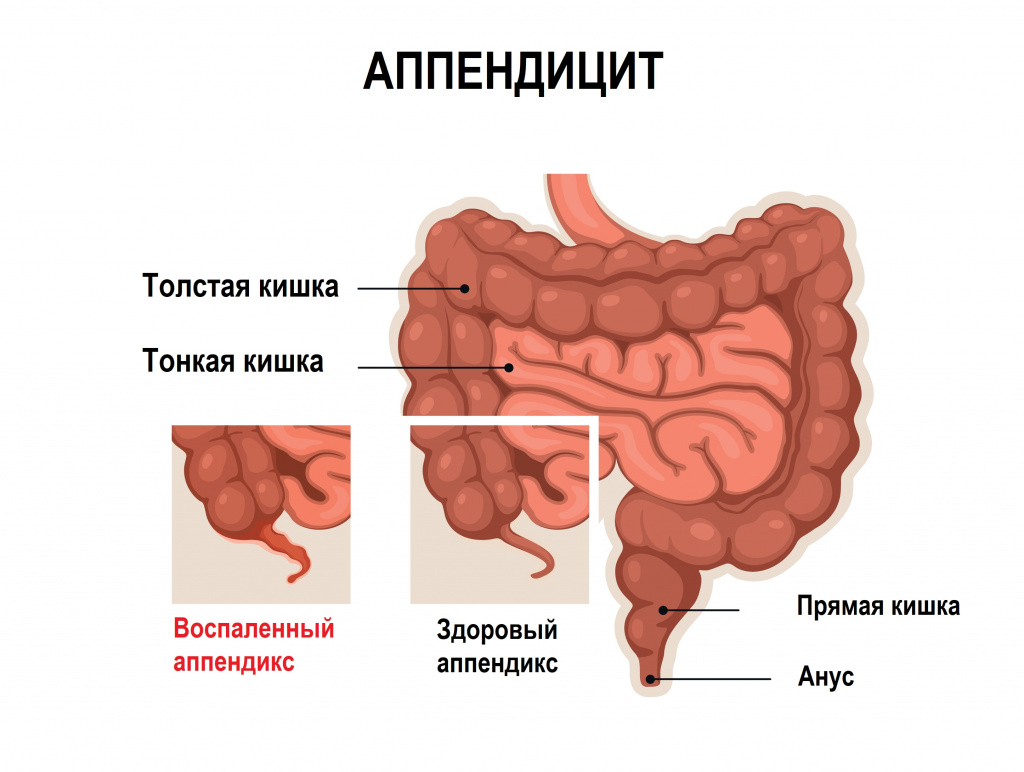
Симптомы перитонита обычно развиваются на фоне симптомов основного заболевания, ставшего причиной воспаления брюшины, например, аппендицита или язвенной болезни с перфорацией.![Аппендицит.jpg]()
Болезнь проходит три стадии – реактивную, токсическую и терминальную. В реактивной стадии боль локализуется в месте источника перитонита, постепенно распространяясь по всему животу, может отдавать в плечи и надключичные области (при перфорации полого органа). Мышцы передней брюшной стенки резко напряжены. Пациент может отмечать сухость во рту, тошноту и рвоту, отказывается от еды.
При распространенных формах перитонита пациент принимает вынужденное положение – на спине или на боку с приведенными к животу ногами.
Если пациент сидел, то при попытке лечь происходит усиление боли, заставляющее его вернуться в исходное положение.
Во время токсической фазы боль уменьшается, приобретает разлитой характер, напряжение и болезненность мышц живота снижаются. Падает артериальное давление, повышается пульс и температура тела, возникает одышка. Начинается вздутие живота, задержка стула и газов.При терминальной стадии преобладают явления паралитической кишечной непроходимости. Снова усиливаются боли в животе, появляется многократная рвота без облегчения, икота, резкое вздутие живота, черты лица заостряются, падают показатели гемодинамики, моча отходит с трудом, возникает желтуха и другие признаки полиорганной недостаточности.
Диагностика перитонита
Очень важно диагностировать перитонит как можно раньше. Перитонит – это, прежде всего клинический диагноз, но он всегда требует лабораторного и инструментального подтверждения.
Лабораторная диагностика включает:
Синонимы: Общий анализ крови (ОАК); Гемограмма; КАК; Развернутый анализ крови. Full blood count; FBC; Complete Blood Count (CBC); Hemogram; CBC with White Blood Cell Differential Count; Peripheral Blood Smear; Blood Film Examination; Complete blood count (CBC) with differential white blood cell coun.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
![Сепсис_дисфункция.jpg]()
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
![Сепсис.jpg]()
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также: