Как почистить организм от паразитов при псориазе
Обновлено: 25.04.2024
Описана связь псориаза и патологии печени, указано на опасность гепатотоксических воздействий в результате применения специфических дерматологических химиопрепаратов для лечения псориатического больного, рассмотрены возможности гепатопротекторов, препятст
Connection between psoriasis and hepatic pathology was described, danger of hepatotoxic impact as a result of application of specific dermatologic preparations for treatment of patients with psoriasis was shown, possibilities of hepatoprotectors, which prevent cellular membranes from destruction and stimulate regeneration of hepatocytes, were considered.
Несмотря на различную этиологию, хронические гепатиты характеризуются схожими морфологическими изменениями в виде диффузного воспалительно-дистрофического поражения печени с гистиолимфоплазматической инфильтрацией портальных полей, гиперплазией купферовских клеток, умеренным фиброзом в сочетании с дистрофией печеночных клеток при сохранении дольковой структуры. Гистологические изменения, как правило, зависят от тяжести поражения печени. Они также неспецифичны для различных этиологических факторов (алкогольного, вирусного, токсического и др.). Прогрессирование хронического гепатита ведет к усилению фиброза и перестройке архитектоники печени с развитием узлов. Это формирует цирроз печени с портальной гипертензией, нарастающей печеночной недостаточностью и другими нарушениями [3]. Одними из универсальных механизмов клеточного повреждения являются свободнорадикальные процессы. Под влиянием различных этиологических факторов, вызывающих хроническую патологию печени, происходит усиление процессов перекисного окисления липидов.
На практике, как показывают исследования, у молодых мужчин клинические симптомы хронических заболеваний печени в большинстве случаев немногочисленны, а у половины пациентов — отсутствуют. На наличие патологии печени часто указывают лишь повышенные показатели аланинаминотрансферазы, но и нормальные показатели ее еще не гарантируют отсутствия изменений в печени.
Среди многочисленных причин и механизмов, ведущих к повреждению и заболеваниям печени, ожирение, сахарный диабет 2-го типа и гиперлипидемия признаются наиболее частыми причинами развития, в частности, стеатоза и стеатогепатита и являются прогностическими факторами более выраженного гистологического поражения печени [4]. Но в то же время сопутствующие заболевания печени у таких пациентов имеют потенциально серьезное влияние на терапию ожирения, гипергликемии, гиперхолестеринемии и артериальной гипертензии. Наиболее частые причины неалкогольной жировой болезни печени и неалкогольного стеатогепатита могут быть представлены в двух группах.
1. Метаболические факторы:
- ожирение (особенно висцерального типа);
- сахарный диабет 2-го типа;
- гиперлипидемия (особенно гипертриглицеридемия);
- метаболический синдром.
2. Лекарственные препараты:
- метотрексат;
- амиодарон;
- тамоксифен;
- аналоги нуклеотидов;
- другие.
Таким образом, печень при метаболическом синдроме выступает в роли органа-мишени с развитием неалкогольной жировой болезни печени и сама обуславливает высокий атерогенный потенциал метаболического синдрома, активно участвуя в патогенезе атерогенной дислипидемии. Тесная связь между гиперлипидемией и жировой инфильтрацией печени определяет возрастающее значение медикаментозного лечения дислипидемий у пациентов с неалкогольной жировой болезнью печени.
По мнению ряда исследователей (Wenk и соавт., 2011) при псориазе имеется весьма высокий риск развития патологии печени. Известно, что у больных псориазом закономерно наблюдается высокий уровень ИЛ-1, что приводит к развитию инсулинорезистентности, которая, в свою очередь, лежит в основе системного воспаления с активацией провоспалительных адипокинов и развитием признаков метаболического синдрома, компонентом которого становится неалкогольный жировой гепатоз.
Надо сказать, сегодня существуют убедительные доказательства того, что среди многочисленных коморбидностей псориаза метаболический синдром является ведущим как по частоте, так и по риску развития кардиоваскулярных последствий, вплоть до инфаркта миокарда [8]. В силу этого обстоятельства обследование больного псориазом, направленное на выявление метаболического синдрома, сегодня представляется задачей именно дерматолога как ведущего специалиста любого псориатического больного [9].
Помимо значимого риска развития повреждений и заболеваний печени по причине метаболического синдрома и других коморбидных состояний при псориазе, существует опасность гепатотоксичных воздействий в результате применения специфических дерматологических химиопрепаратов для лечения псориатического больного по показаниям и в соответствии с существующими официальными рекомендациями и стандартами [10].
Давно известный факт, что опасность развития медикаментозного повреждения печени представляют фотосенсибилизаторы, применяющиеся при ПУВА-терапии у больных псориазом, которая, кстати, считается одним из самых эффективных терапевтических мероприятий при тяжелых распространенных формах псориаза. В связи с этим риском сопутствующие острые и хронические заболевания печени у больных псориазом являются противопоказанием для проведения ПУВА-терапии. Как следствие, перед началом такого лечения необходимо, как минимум, провести биохимическое исследование крови (трансаминазы, щелочная фосфатаза, триглицериды, холестерин) и при незначительных отклонениях в этих показателях фотохимиотерапию проводить можно, но с одновременным назначением максимально эффективного гепатопротектора.
Согласно отечественным и международным клиническим рекомендациям первой линией системной терапии тяжелых форм псориаза, особенно в сочетании с псориатическим артритом, является метотрексат, обладающий, как известно, прогнозируемой гепатотоксичностью. Повреждающее действие метотрексата на ткань печени давно доказано, в том числе с помощью описанных гистологических изменений при его применении [11]. Эти морфологические изменения включают сужение просвета печеночных протоков, уменьшение количества и разрушение микровилл, разрушение билиарных эпителиальных митохондрий, наличие фокусов внутриклеточного отека, изменения аппарата Гольджи с клеточной атрофией, расслоение базальной мембраны и др. Весь этот набор патоморфологических изменений неминуемо сказывается на функциональном состоянии печени, что естественно требует назначения гепатопротекторов при проведении терапии метотрексатом у больных псориазом.
Вообще гепатотоксическим действием среди наиболее часто применяемых системных дерматологических препаратов при других дерматозах, кроме метотрексата и фотосенсибилизаторов, обладают азатиоприн, часто применяемый при пузырчатке и лимфомах; синтетические ретиноиды, назначаемые при тяжелых угрях, дискератозах, псориазе; гризеофульвин, по-прежнему незаменимый при трихомикозах; циклоспорин А, показанный при упорных формах псориаза и атопического дерматита. И этим списком не ограничивается круг системных дерматологических химиопрепаратов с гепатотоксичческим эффектом, в том числе и при их комбинированном применении по механизму лекарственного взаимодействия, далеко не всегда достаточно хорошо известного.
Таким образом, как оказывается, едва ли не в большей части случаев назначения высокоэффективных на уровне доказательных исследований химиотерапевтических системных средств при тяжелых хронических, иногда жизнеугрожающих дерматозах, существует риск развития гепатотоксичности и повреждений печени, что является веским основанием для настоятельных рекомендаций одновременного применения препаратов с гепатопротективным эффектом. Гепатопротекторы — это фармакологическая группа разнородных лекарственных средств, которые препятствуют разрушению клеточных мембран и стимулируют регенерацию гепатоцитов [12].
К гепатопротекторным препаратам относят группу лекарственных средств с различными механизмами действия, направленными на нормализацию функциональной активности печени, потенцирование репаративно-регенеративных процессов, восстановление гомеостаза и повышение устойчивости органа к действию патогенных факторов [13]. К таким лекарственным средствам относятся биофлавоноидные препараты природного происхождения. Более 200 лет с этой целью применяют различные препараты, изготовленные из расторопши пятнистой (Silybum marianum). В последние годы из нее выделено много компонентов, обладающих гепатопротекторными свойствами. Силимарин — общее название химически связанных изомеров флавонолигнана из плодов расторопши. Основными биофлавоноидами в силимарине являются: силибинин, силидианин, силикристин, изосилибинин, среди которых силибинин обладает наибольшей биологической активностью.
Особое внимание стоит обратить на оригинальный гепатопротектор Легалон®. Он содержит в своем составе наибольшее количество силибинина (77%), поэтому считается наиболее эффективным гепатопротектором, имеющим широкий спектр воздействия на большую часть патогенетических механизмов хронических заболеваний печени. Многочисленные исследования доказали, что силибинин, содержащийся в препарате Легалон®, способствует значительному повышению содержания восстановленного глутатиона в печени, тем самым повышая защиту органа от окислительного стресса, поддерживая ее нормальную дезинтоксикационную функцию.
Противовоспалительный и иммунорегулирующий эффекты обуславливают антифиброзное действие силибинина. Легалон®, предотвращая действие фактора некроза опухолей (ФНО-α) на клетки Купфера, замедляет активацию звездчатых клеток, снижает коллагенообразование. Имеются данные о замедлении темпов прогрессирования фиброза печени на фоне длительного приема силибинина.
Легалон® целесообразно применять у больных с лекарственно-индуцированными заболеваниями печени с клиническими и биохимическими признаками активности, профилактическими курсами при необходимости длительного приема гепатотоксичных препаратов (например метотрексата, цитостатиков, нестероидных противовоспалительных средств, антиаритмических средств, антидепрессантов, контрацептивов и т. д.), при вынужденной полипрагмазии (особая группа риска — женщины после 40 лет). Лекарственную терапию пациентам, с указанием в анамнезе на диффузные заболевания печени любой этиологии или страдающим алкогольной и никотиновой зависимостью, следует также проводить под прикрытием препарата Легалон®.
Доказательство антифибротического эффекта силимарина было получено в результате специально проведенного клинического исследования, в которое было вовлечено 998 больных с хроническими заболеваниями печени (стеатоз печени, стеатогепатит и цирроз печени различной этиологии) [14]. На протяжении 12 недель больные получали силимарин по 140 мг 3 раза в день. В результате терапии у 96% больных были достигнуты клиническое улучшение или ремиссия заболевания, при этом нормализация показателей индикатора фиброза произошла у 47% больных стеатозом, у 41% — стеатогепатитом и у 26% — циррозом печени. У значительной части больных после терапии наблюдалась нормализация количества проколлагена как маркера фиброза.
Известно, что глутатион способствует выведению токсинов печени, является мощным естественным антиоксидантом и стимулирует обмен веществ. Как показано в исследованиях [15], силимарин связывает свободные радикалы, тормозит перекисное окисление липидов и стимулирует синтез глутатиона, что в целом лежит в основе антиоксидантного эффекта препарата Легалон®.
Кроме того, противовоспалительное действие силимарина продемонстрировано в работах [16], показывающих блокирующее влияние препарата на ферменты, продуцирующие медиаторы воспаления (лейкотриен В4 и простагландин Е2), а также путем взаимодействия с клетками Купфера, приводящего к подавлению воспалительного процесса.
Путем стимулирования синтеза рибосомальных РНК и синтеза белка силимарин приводит к восстановлению структурных единиц гепатоцитов, что составляет регенеративный эффект препарата, так необходимый при повреждениях печени различной природы [17].
Наконец, мембраностабилизирующий эффект силимарина осуществляется путем встраивания его в мембрану гепатоцита с последующим восстанавливающим биохимическим воздействием. Это находит подтверждение в клинических наблюдениях, демонстрирующих нормализацию уровней билирубина у 82% больных и АСТ у 60% после терапии силимарином [18].
Таким образом, возвращаясь к тяжелым хроническим дерматозам, необходимо помнить, что при подозрении или доказанном повреждении печени медикаментозного происхождения и жировом гепатозе метаболического характера во время проведения системной терапии больного рекомендуется сопровождать основное лечение назначением препарата Легалон® в дозе 140 мг трижды в сутки в качестве лечебного воздействия с переходом на поддерживающую дозу в 70 мг трижды в сутки как профилактическую терапию на протяжении последующих 3–4 мес.
В качестве заключения приводим табл. 2 и 3 с целью демонстрации достоинств и преимуществ оригинального препарата Легалон® перед другими гепатопротекторами.
Литература
- Степанов Ю. М., Залевский В. И. // Сучасна гастроентерологія, 2007, 6 (38), 14–21.
- Adams L. A., Lymp J. F., Sauver J. et al. The natural histori of non_alcogolic fatty liver discase: A population-based cohort study // Gastroenterology. 2005. № 129. Р. 113–121.
- Andersen T., Gluud C. Liver morphology in morbit obesity; a literature study // Int. J. Obes. 1984. Vol. 8. P. 107–115.
- Braillion A., Capron J. P., Herve M. A. et аl. Liver in obesity // Gut. 1985. Vol. 26. P. 133–139.
- Кочергин Н. Г., Смирнова Л. М., Потекаев Н. Н., Билалова У. В. Псориаз: коморбидности и комедикации // Врач. 2009, № 5, с. 15–20.
- Christophers E. Comorbidities in psoriasis // Clin. Dermatol. 2007; 25: 529–534.
- Abuabara K. et al. // BJD, 2010, v. 163, p. 585–592.
- Gisondi P., Tessari G., Conti A. et al. Prevalence of metabolic syndrome in patients with psoriasis // Br. J. Dermatol, 2007, v. 157, p. 68–73.
- Boehnke W. H. EADV Congress, 2014, D2 T11. 1 C.
- Farrell G. C. Liver disease caused by drags, anesthetics, and toxins / Feldman M., Scharschmidt B. E., Sleisenger M. H. (eds). Gastrointestinal disease. Philadelphia, PA$ WB Saunders, 2002. P. 1403–1447.
- Farreli G. C. Drag-induced liver disease. Edinburgh: Churchill Livingstone. 1994.
- Рук-во для практикующих врачей / Под общ. ред. В. Т. Ивашкина, А. О. Буеверова. М., 2009. 296 с.
- Журавлева Л. В., Кривоносова Е. М. // Сучасна гастроентерологія, 2013, 4 (72), 93–101.
- Schuppan. Z. // Allg. Med. 1998. 74, 577–584.
- Campos et al. // Planta Med. 1989. 55, 417–419.
- Dehmlow et al. // Life Sci. 1996. 58, 749–754.
- Sonnenbichler and Zeti in: Plant flavonoids in biology and medicine. 1986, 319–331.
- Kiesewetter E. et al. // Leber Magen Darm. 1977. V. 7, p. 318–323.
Н. Г. Кочергин, доктор медицинских наук, профессор
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва

Псориаз – хроническое заболевание, причины развития которого до сих пор точно неизвестны. В связи с этим его относят к неизлечимым хроническим болезням. В их течении выделяются периоды обострения и ремиссии. Они могут иметь разную длительность. Но в любом случае цель лечения – добиться стойкой ремиссии. Для начала стоит понять, что это такое – псориаз в стадии ремиссии, а уже затем рассмотреть способы и правила ее достижения.
Что такое ремиссия
Таким образом, ремиссия – не полное выздоровление, а период улучшения, который может длиться разное количество времени. Термин применяют только к хроническим рецидивирующим заболеваниям, к которым относят и псориаз. Его нельзя вылечить, но можно добиться ремиссии и поддерживать ее в течение длительного времени. Еще эту стадию развития псориаза называют регрессивной.
Описание ремиссии псориаза
Так, ремиссия псориаза – период облегчения или почти полного исчезновения признаков и симптомов. Необходимо сразу сказать, что единого способа нет, и кому-то это дается легко, а другим приходится проявить огромную силу воли. На сложность в достижении ремиссии влияют следующие факторы:
- степень выраженности заболевания;
- длительность лечения;
- на каком уровне находится общее здоровье человека;
- наличие сопутствующих заболеваний.
По этим причинам схему терапии всегда подбирают индивидуально, а лечение псориаза у детей отличается от лечения взрослых.

Ремиссия при псориазе имеет 2 формы:
От перечисленных факторов зависит и то, как долго длится ремиссия псориаза. В среднем период облегчения продолжается от 6 месяцев до 6 и более лет, но четких временных границ не существует. На длительность влияет то, насколько строго человек соблюдает предписания врача, проходит ли лечебные и профилактические курсы, а также их правильность и эффективность. Именно эти факторы становятся условием сохранения и продления состояния ремиссии.
Как добиться ремиссии при псориазе
Чтобы добиться стойкой ремиссии при псориазе, врач назначает поддерживающую терапию. Она может включать прием лекарств и применение специальной мази от псориаза. Дополнительно корректируется питание и назначаются витаминно-минеральные комплексы, даются рекомендации относительно образа жизни.
Самые важные советы:
- Постоянно наблюдаться у врача, приходить на профилактические приемы.
- Продолжать курс терапии еще некоторое время после исчезновения симптомов, но только по согласованию с врачом.
- Строго соблюдать диету, индивидуально составленную врачом.
- Исключить действие провоцирующих факторов.
- Придерживаться правильного распорядка дня с достаточным количеством сна, отдыха и физических нагрузок.
- Пройти лечение для устранения хронических очагов инфекций. Ухудшить состояние могут синусит, ринит, гайморит, тонзиллит, кариес и другие заболевания внутренних органов.
Исключить факторы риска
В первую очередь для достижения ремиссии необходимо исключить все, что может спровоцировать обострение. Многие пациенты отмечают, что рецидив произошел без видимых причин. Но на самом деле они просто остались незамеченными. Существует ряд факторов, способных спровоцировать прогрессирование псориаза:
- затяжная депрессия;
- сильное эмоциональное потрясение;
- перепады температуры или резкая смена климата;
- гормональные изменения (переходный возраст у детей и менопауза у женщин);
- курение и злоупотребление алкоголем;
- инфекционные заболевания.

Конкретные рекомендации по устранению негативных факторов зависят от локализации высыпаний. Например, при лечении псориаза на руках нужно обязательно исключить воздействие на кожу химических веществ. Не менее важно избегать повреждений (ссадин, царапин, порезов), поскольку на их месте могут появляться новые бляшки. При псориазе волосистой части головы ухудшить состояние может неправильно подобранный шампунь или неаккуратное расчесывание, а также окрашивание.
Соблюдать диету
Важным условием достижения и сохранения ремиссии выступает соблюдение диеты. Она исключает продукты, которые могут оказывать на организм неблагоприятное действие. К таким относятся:
- цитрусовые,
- орехи,
- пряности,
- свинина,
- алкоголь,
- жирная рыба,
- молоко,
- сладости.

Рацион при псориазе должен быть сбалансированным и разнообразным. Полезно употреблять сырые овощи и фрукты. Мясо должно быть постным, а рыба – нежирной (лосось, морской окунь). Из молочных продуктов хорошо переносятся обезжиренный творог, йогурт и кефир.
Принимать назначенные лекарства
Конкретный курс лекарственных препаратов назначает врач. Периодически специалисты рекомендуют проводить чистку организма с помощью сорбентов: Активированного угля, Энтеросгеля, Сорбекса, Смекты. В дополнение к ним могут применяться:
- антигистаминные для купирования аллергических приступов;
- фолиевая кислота, витаминные и поливитаминные комплексы;
- препараты для восстановления кишечной микрофлоры.

Поддерживать хороший настрой
Один из самых серьезных отпечатков на течение псориаза накладывает психологическое состояние человека. Если чрезмерно фиксировать внимание на симптомах, есть риск столкнуться с психологическими расстройствами и депрессией. А любой стресс может негативно повлиять на течение заболевания и вызвать рецидив.

В такой ситуации может потребоваться помощь психотерапевта. Улучшить психоэмоциональное состояние помогут занятия йогой. Они особенно рекомендованы тем, кто страдает от псориаза. Также полезно совершать пешие прогулки, заниматься спортом и принимать солнечные ванны (особенно при склонности к зимним обострениям псориаза).
Псориаз — распространенное дерматологическое заболевание, которое с древних времен и по сегодняшний день вызывает много вопросов. Болезнь не представляет угрозы для окружающих, она не имеет инфекционного компонента, но при этом может существенно испортить качество жизни самому больному. Важная задача, стоящая перед врачами, — донести до пациента информацию, что провоцирует псориаз, сформировать рекомендации, как максимально исключить эти факторы. Эффективное лечение псориаза всегда основано на взаимодействии врача и пациента, на систематическом выполнении всех рекомендаций и коррекции образа жизни.
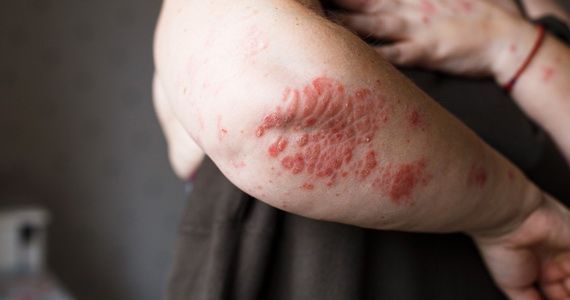
Проявляется псориаз розовыми приподнятыми пятнами на теле. Они вызывают зуд, склонны к слиянию и образованию обширных бляшек. Это очаги хронического воспаления, а чешуйки, которыми покрыты бляшки, говорят врачам о том, что в этом месте клетки эпителия делятся с бешеной скоростью, во много раз активней, чем это должно быть в норме.
Причины псориаза не ясны до конца. На данный момент предполагается аутоиммунная природа заболевания. Также врачи считают, что есть генетические факторы, предрасполагающие к появлению псориаза, потому что очень часто встречаются семейные случаи. Спровоцировать дебют могут инфекции, стресс, переохлаждение. При этом псориаз протекает волнообразно, эпизоды обострения сменяются ремиссией. И от правильно назначенного лечения и образа жизни пациента, от его систематического ухода за кожей напрямую зависит длительность спокойных периодов. В острые периоды улучшить состояние помогает мазь от псориаза.
Так как вылечить псориаз окончательно врачи пока не могут, основная цель — добиться стойкой длительной ремиссии, улучшить качество жизни пациента и максимально очистить от бляшек кожу. Мы расскажем, может ли острая пища вызвать псориаз, как влияют на рецидивы некоторые лекарственные препараты, какие факторы могут спровоцировать новое обострение.
Какие продукты провоцируют псориаз
Как ни странно, есть пища, провоцирующая псориаз. Под запретом любые острые, копченые и сильно соленые блюда, они нарушают процесс всасывания в кишечнике. Также спровоцировать рецидив могут цитрусовые, которые блокируют фолиевую кислоту из-за содержащегося в них колхицина. А фолиевая кислота важна для восстановления кожи. Нельзя употреблять в пищу консервированные продукты, которые могут послужить триггером к новому обострению.

Вот еще продукты, провоцирующие псориаз:
- торты, пирожные, газированные напитки, содержащие большое количество сахара;
- алкоголь;
- полуфабрикаты.
Желательно питаться блюдами, приготовленными дома, тогда можно контролировать состав и калорийность. Диета должна быть богата овощами и фруктами, медленными углеводами и белком, который легко усваивается.
Лекарства, вызывающие рецидивы болезни
Фармакологические препараты также могут влиять на течение болезни. Если говорить о том, какие лекарства провоцируют псориаз, то в первую очередь это антибиотики, нестероидные противовоспалительные препараты, бета-блокаторы. Существенное влияние оказывают вакцины и сыворотки, потому что они затрагивают напрямую иммунитет, некорректная работа которого и лежит в основе псориаза. Также провоцируют псориаз лекарства от повышенного давления, от психических заболеваний. Это не значит, что человек, страдающий от псориаза, не должен заниматься лечением других болезней, например, гипертонии, не вакцинироваться, но он должен сообщать врачам о наличии дерматологических проблем, не заниматься самолечением и не покупать в аптеке самостоятельно назначенные себе средства.
Какую роль играют паразиты в течении болезни
Существует паразитарная теория развития псориаза. Дело в том, что у людей, у которых уже установлен этот диагноз, часто обнаруживаются кишечные паразиты. Конечно, это не первопричина появления болезни, но не исключено, что паразиты влияют на иммунную систему человека, создают постоянную напряженность иммунитета, вырабатывают аллергичные токсины, могут вызывать эпизоды псориаза. Если говорить о том, какие паразиты провоцируют псориаз, то стоит выделить следующие:
- аскариды;
- острицы;
- лямблии;
- бычий цепень и другие.
У больных псориазом должна быть выявлена и вылечена любая паразитарная инвазия. Это поможет снизить вероятность обострений.
Профилактика рецидивов псориаза
Новый эпизод может быть вызван стрессом, переохлаждением, гормональными изменениями. Также провоцирует псориаз тесная синтетическая одежда, грубые швы, важно носить только свободную одежду из натуральных тканей — хлопка и льна. Летом нужно защищать кожу от ультрафиолетового излучения, использовать солнцезащитную косметику с фильтрами. Больные псориазом должны избегать ссадин и порезов, соблюдать гигиену, не допускать обезвоживания кожи и использовать регулярно эмоленты. Тогда можно будет добиться длительной и стойкой ремиссии.
А если вы хотите узнать об этой болезни больше, читайте статью "Все о псориазе во время беременности".
В статье приводятся данные о нарушениях функции гепатобилиарной системы у больных псориазом. Раскрываются результаты проведенных исследований зарубежных и отечественных авторов, показавшие значимые связи наличия и тяжести поражения печени, билиарного трак
The article provides information about disorders of the hepatobiliary system in patients with psoriasis. The research results of foreign and domestic authors, which showed a significant correlation with the presence and severity of liver damage, biliary tract severity and clinical forms of psoriasis are described.
Псориаз — это иммуноассоциированный, генетически детерминированный, органоспецифический хронический эритематозно-сквамозный дерматоз многофакториальной природы. Характеризуется гиперпролиферацией эпидермальных клеток, нарушением процесса кератинизации, воспалительной реакцией в дерме и изменениями в различных органах и системах [1, 2]. Псориаз приводит к эмоциональной, социальной дезадаптации, а в ряде случаев к инвалидизации. Показатель заболеваемости псориазом на территории Российской Федерации составляет у взрослых 65,9 на 100 тыс. населения. Частота встречаемости псориаза в мире достигает от 2% до 5% всего населения. Наиболее часто псориаз регистрируется в Скандинавии и странах Северной Европы (3-5% от популяции). Средний уровень выявляется в Европе, США и России (1-3%). Низкий уровень встречаемости псориаза наблюдается у коренных северо- и латиноамериканских индейцев, монголоидных и западных африканцев (0-0,3%). У 25% больных псориазом заболевание сопровождается потерей или временной утратой трудоспособности. Псориазом одинаково часто болеют как мужчины, так и женщины. В детском возрасте заболевание несколько чаще встречается у девочек. Дебют заболевания наблюдается в любом возрасте. В целом чаще в третьей декаде жизни, хотя в последние годы нередки случаи диагностики псориаза у детей и даже младенцев [1].
В настоящее время псориаз рассматривается как системное заболевание с поражением не только кожных покровов, но и функциональных и морфологических нарушений других органов. Важное значение в поддержании и рецидивировании дерматоза придают нарушениям функции гепатобилиарной системы, поскольку патология печени и желчных путей может инициировать и усугублять выраженность эндотоксикоза, воспаления, иммунный дисбаланс, поддерживает нарушения процессов регенерации во всех системах в целом, в коже в частности [3]. К причинам развития псориаза относят и иммунологические нарушения, которые, как правило, возникают у лиц с генетической предрасположенностью к их развитию под воздействием провоцирующих факторов. Гены (PSORS 1 — PSORS 9), по отдельности или в комбинации, под воздействием инициирующего фактора способствуют развитию временных или стойких псориатических изменений кожи самых разных видов, степени выраженности и локализации [1, 4, 5]. Провоцирующими факторами риска могут быть инфекционные процессы (особенно вызванные стрептококками), травматизация кожи (парезы, царапины, ушибы и т. д.), избыточная инсоляция, токсические факторы (алкоголь, курение, наркотики, некоторые лекарственные средства: β-блокаторы, аминохинолиновые препараты, препараты лития, пероральные контрацептивы, интерфероны и т. д.), синдром отмены кортикостероидной терапии. Изменения клеточного метаболизма кератиноцитов и их патологическая пролиферация являются результатом структурно-органических нарушений, таких как метаболические нарушения (абдоминальное ожирение, инсулинорезистентность, сахарный диабет 2-го типа, нарушение липидного спектра, атеросклероз, гипертоническая болезнь); психические расстройства; болезни сердечно-сосудистой системы, где общие генетические факторы определяют высокий кардиоваскулярный риск; заболевания пищеварительной и особенно гепатобилиарной системы [1, 2, 6].
В последние годы у больных псориазом значимое внимание уделяется сопутствующей патологии неалкогольной жировой болезни печени (НАЖБП). НАЖБП в анамнезе у больных псориазом определяется как избыточное накопление триглицеридов в печени пациентов при отсутствии сопутствующих заболеваний [8]. По данным Национальной образовательной программы по холестерину, пациент подвержен метаболическому синдрому, если он имеет по крайней мере три из следующих критериев [9]:
- абдоминальное ожирение, определяемое как окружность талии ≥ 102 см у мужчин и ≥ 88 см у женщин;
- триглицериды в сыворотке крови ≥ 150 мг/дл;
- липопротеиды высокой плотности холестерина в сыворотке крови не более 40 мг/дл у мужчин и 50 мг/дл у женщин;
- артериальное давление более 130 мм рт. ст. (систолическое) и 85 мм рт. ст. (диастолическое);
- уровень глюкозы в сыворотке крови натощак более чем 100 мг/дл.
Неалкогольная жировая болезнь печени в настоящее время является наиболее распространенным хроническим заболеванием печени, достигая 10-25%, особенно у тучных людей [10]. Известно, что метаболический синдром чаще связан с псориазом и НАЖБП, которые могут присутствовать у одного пациента одновременно [11]. НАЖБП может включать разнообразные поражения печени, начиная от относительно доброкачественного стеатоза, состоящего из жировой инфильтрации, безалкогольного стеатогепатита с жировой инфильтрацией, лобулярного воспаления до цирроза печени и гепатоцеллюлярной карциномы [12].
Наиболее часто встречаемые у больных псориазом неблагоприятные факторы, способствующие повреждению печени, включают окислительный стресс внутри клеток печени, инсулинорезистентность, выброс токсичных воспалительных белков тучными клетками и цитокинами. В жировой ткани инсулин способствует этерификации свободных жирных триглицеридов и хранению жира. Когда развивается инсулинорезистентность, свободные жирные кислоты смещаются в такие нежировые ткани, как печень. Кроме того, печеночный липогенез и активация профиброзных цитокинов опосредует гиперинсулинемия [13]. Накопление ТГ в печени приводит к развитию окислительного стресса, липотоксичности и, следовательно, к митохондриальной дисфункции, которые представляют собой дальнейшее повреждение печени [14].
Последние данные зарубежных исследователей показали, что НАЖБП может быть связана с повышенным риском сердечно-сосудистых заболеваний независимо от традиционных факторов риска [15]. Дислипидемический профиль предшествует развитию псориаза. Повышенные уровни липопротеидов низкой плотности и снижение уровня холестерина, липопротеидов высокой плотности коррелируют с ишемической болезнью сердца и смертностью от сердечно-сосудистых заболеваний [16]. Недавно проведенные исследования направлены на возможную связь между псориазом, ожирением и метаболическим синдромом, являющимися известными факторами риска для НАЖБП [17].
Известно, что в возрасте после 40 лет пациенты с псориазом имеют более высокую распространенность метаболического синдрома и повышенный риск для каждого из компонентов метаболического синдрома [11, 18]. Также по данным A. Campanati с соавт. (2013) у пациентов с псориазом и НАЖБП отмечается увеличение риска развития псориатического артрита, что отражает активность провоспалительных цитокинов при обоих заболеваниях. Пациенты с псориазом с НАЖБП имеют значительное увеличение концентрации АСТ/АЛТ и показателей фиброза по сравнению с контрольной группой больных НАЖБП, не связанных с псориазом. Показатели АСТ/АЛТ стали независимыми прогностическими факторами фиброза печени у пациентов с НАЖБП [13]. Проведенные исследования ряда авторов показали, что риск тяжелого фиброза печени выше у пациентов с НАЖБП, коморбидных с псориазом, чем только у пациентов с НАЖБП. Эти два параметра считаются независимыми прогностическими факторами фиброза печени у пациентов с НАЖБП [20].
E. A. van der Voort с соавт. в 2013 г. проведено большое проспективное популяционное когортное исследование пациентов в возрастной группе от 18 до 55 лет. Среди участников исследования регистрировались 2292 (5,1%) пациента с псориазом. Частота встречаемости НАЖБП составила 46,2% у пациентов с псориазом по сравнению с 33,3% пациентов без псориаза [21]. По данным P. Gisondi (2009) из 130 обследованных человек признаки НАЖБП были обнаружены у 47% больных псориазом, в то время как у 260 обследованных контрольной группы — только у 28%. Больные псориазом с признаками НАЖБП имеют более высокий индекс тяжести псориаза PASI (14,2 против 9,6), в сравнении с пациентами с псориазом без признаков НАЖБП [22]. Пациенты с псориазом, метаболическим синдромом и НАЖБП показали более высокий уровень С-реактивного белка. Следует также отметить, что проявление НАЖБП может быть связано с нарушением циркуляции и транспортировки желчных кислот. В связи с этим можно констатировать, что имеющиеся болезни печени усугубляют течение псориаза и осложняют его лечение [20]. Результаты многочисленных исследований показывают, что на уровне таких неблагоприятных факторов, как потребление алкоголя, статус курения, нарушения показателей метаболического эквивалента Mets и аланинаминотрансферазы, псориаз остается значимым прогностическим параметром НАЖБП [22, 23].
Патогенез НАЖБП, как и псориаза, многофакторный и сложный. Стойкое хроническое воспалительное состояние может быть первичной связью между НАЖБП и псориазом. Известно, что псориаз и ожирение значимо связаны (ожирение предрасполагает к развитию псориаза, и псориаз увеличивает риск ожирения). Псориаз и НАЖБП также связаны с ожирением, которое в результате может способствовать развитию дальнейшего изменения показателей метаболического эквивалента Mets и сопутствующих заболеваний [23]. Накопление жировой ткани может привести к гипертрофии и гиперплазии адипоцитов вследствие воспалительного процесса, высвобождения провоспалительных хемокинов, а также вовлечения макрофагов, которые усиливают распространение воспалительного процесса в соседние адипоциты. Избыток жировой ткани приводит к дисбалансу между про- и противовоспалительными цитокинами и увеличению воспалительных компонентов, отвечающих за запуск стойкого воспаления. Адипоцитокины являются биологически активными молекулами, способными модулировать энергетический баланс, иммунитет, чувствительность к инсулину, ангиогенез, кровяное давление и липидный метаболизм путем аутокринной, паракринной и эндокринной систем. Кроме того, они играют решающую роль в патогенезе метаболического синдрома. Адипоцитокины фактора некроза опухоли α (ФНО-α), лептина, висфатина, резистина оказывают провоспалительный эффект, тогда как адипонектин обладает противовоспалительными свойствами. Производство адипонектина тормозится ФНО-α. Положительная корреляция между ФНО-α и индексом массы тела, а также их более высокие сывороточные уровни наблюдаются у пациентов с НАЖБП. ФНО-α играет ключевую роль в патогенезе псориаза: у больных значимо повышенное содержание ФНО-α в сыворотке крови положительно коррелирует с индексом тяжести псориаза PASI и негативно коррелирует с уровнем сывороточного адипонектина. При псориазе ФНО-α повышает пролиферацию кератиноцитов, производство провоспалительных цитокинов, сосудистых эндотелиальных клеток молекул адгезии, ангиогенеза. Происходит высвобождение ФНО-α, непосредственно участвуют макрофаги и липолиз, создавая порочный круг [24, 25].
В проведенном исследовании А. А. Иблияминовой (2011) у пациентов вне зависимости от степени тяжести заболевания установлена прямая корреляционная взаимосвязь индекса тяжести псориаза PASI и концентрации общего билирубина, активности щелочной фосфатазы в сыворотке крови, степени выраженности холестаза (г = 0,56-0,64 при р < 0,01), а также повышения литогенности желчи, определяемой по снижению холатохолестеринового и фосфолипидно-холестеринового коэффициентов (г = -0,55-0,52 при р < 0,05) [26].
По мнению ряда российских авторов, обычный псориаз, коморбидный с некалькулезным холециститом, имеет особенности в клиническом течении, нарушении пигментного обмена, ферментов сыворотки крови и метаболизме холестерина, фосфолипидов и холевой кислоты на печеночном уровне, что проявляется холестазом, более высоким литогенным потенциалом желчи. При снижении показателей коэффициентов литогенности холато-холестеринового коэффициента и фосфолипидно-холестеринового коэффициента пузырной желчи прогнозируют возможность нарушения коллоидного состояния желчи, ухудшающего течение билиарной патологии, обострение которой оказывает отрицательное влияние на псориатический процесс [27].
По данным Матусевича с соавт. (2000) хроническая эндотоксинемия при псориазе может приводить к функциональным нарушениям в работе печени, тяжесть которых зависит от ее уровня и длительности, а также от наличия сопутствующих заболеваний [28]. Органическая патология билиарного тракта и/или его функциональные расстройства отягощают течение псориаза, а степень холестаза коррелирует с величиной индекса тяжести псориаза PASI [22, 26].
По данным полученных результатов Л. П. Розумбаевой с соавт. у пациентов с распространенными формами псориаза высока частота неалкогольной жировой болезни печени, начальных признаков фиброза печени в сочетании с патологией билиарной системы. Патология билиарной системы разнообразна и характеризуется признаками дисфункциональных расстройств, симптомами бескаменной и желчнокаменной болезни. Установлены значимые связи наличия и тяжести поражения печени и билиарного тракта с клинической формой псориаза: при распространенном поражении кожи достоверно чаще встречаются признаки не только стеатоза, стеатогепатита, но и признаки продвинутого фиброза печени. Указанные обстоятельства необходимо учитывать при назначении терапии обострения распространенного псориаза, особенно при применении препаратов с потенциальным гепатотоксическим эффектом [3].
Таким образом, учитывая высокую распространенность сопутствующих функциональных расстройств патологии печени у пациентов с псориазом, патогенетическая роль патологии печени при псориазе не вызывает сомнений, и углубленное комплексное обследование нарушений функционального состояния гепатобилиарной системы у больных псориазом (ультразвуковое и биохимическое) позволит лучше понять роль и место этих нарушений в механизме псориаза и, возможно, разработать новые персонализированные подходы к терапии дерматоза, что в конечном итоге будет способствовать повышению качества жизни этих больных.
Литература
Л. А. Юсупова, доктор медицинских наук, профессор
Резюме В патогенезе хронических рецидивирующих дерматозов, в частности псориаза определенное значение имеют кишечные и алиментарные нарушения, фокальные инфекции, гельминтозы и др. Гельминты являются одними из тригеррных факторов воспалительного процесса и аутоинтоксикации макроорганизма. Существует прямая корреляция между инвазией и тяжестью течения дерматозов, характеризующейся частотой и длительностью обострений, а также выраженностью клинических проявлений. Выявленная у больного псориазом паразитарная инфекция свидетельствует о необходимости включения в патогенетически обоснованную терапию комплекс антипаразитарных средств, энтеросорбентов, пре- и пробиотиков.
Ключевые слова глистная инвазия, лямблиоз, псориаз, антигельминтная терапия
Helminthic invasion in patients with psoriasis vulgaris (in the case of practice)
Kazakh National Medical university
Abstract In the pathogenesis of chronic recurrent dermatoses, particularly psoriasis have a definite value of intestinal and nutritional disorders, focal infection, helminth infections and other helminths are among the factors trigerrnyh inflammation and autointoxication microorganism. There is a direct correlation between infestation and severity of dermatitis, characterized by frequency and duration of exacerbations, as well as the severity of clinical manifestations. Detected in a patient with psoriasis parasitic infection evidenced by the inclusion of the need to pathogenetically substantiated therapy complex antiparasitic funds enterosorbents, pre-and probiotics.
Keywords helminthic invasion, giardiasis, psoriasis, anthelminthic therapy
Қабыршақты темереткімен ауыратын науқастағы құрт инвазиясы (тәжірибелік оқиға)
Түйін Қабыршақты теміреткінің патогенезінде алиментарлы және ішек бұзылыстары, фокальды жұқпалы аурулардың, құрттардың және т.б. маңызы үлкен. Құрттар макрорганизмінде қабыну үрдістерінің және аутоуланудың шешуші факторры болып есептеледі. Құрттар инвазиясы мен тері ауруларының арасында тығыз байланыс бар, олар өршу жиілігін, ұзақтығын және клиникалық белгілерінің анық болуына әсер етеді. Қабыршақты темереткімен ауыратын науқастағы құрт инвазиясы анықталу нәтижесінде патогентикалық кешенді еміне құрттарға қарсы, энтеросорбенттер, пре- және пробиотиктер қолдану қажет екендігі дәләлденді.
Түйінді сөздер құрт инвазиясы, лямблиоз, қабыршақты теміреткі, құрттарға қарсы ем
Псориаз — хронический рецидивирующий дерматоз, характеризующийся гиперпролиферацией эпидермальных клеток, нарушением процесса кератинизации и воспалительной реакцией в дерме, изменениями в различных органах и системах.
В мире около 3% человечества страдает псориазом. Заболевание распространено во всех широтах земного шара, среди населения разных национальностей и рас. Дерматоз часто возникает в 10-25 лет, однако впервые может проявиться в любом возрасте. В литературе имеются описания случаев псориаза у детей 4-5 и 7 мес. и у взрослых в возрасте 82 лет. Среди взрослых псориаз проявляется чаще у мужчин (60-65%), однако среди детей он чаще встречается у девочек [1].
В патогенезе псориаза определенное значение имеют генетическая обусловленность, кишечные и алиментарные нарушения, фокальные инфекции, нервные стрессы, сопутствующие соматические патологии, гельминтозы и др. факторы [2].
Паразитарными инфекциями сегодня в мире страдают около пяти миллиардов человек. По данным ВОЗ гельминтозы ежегодно отмечаются у 1 — 1,4 млрд. жителей Земли. Из них около 400 млн приходится на Китай, но при этом необходимо заметить, что диагностируется только меньшая часть гельминтозов и большой пласт остается за пределами диагностики. В России официально 1 млн случаев в год, реально — 11 — 20 млн. Число людей с аскаридозом составляет на данный момент 1 млрд 470 млн, с энтеробиозом — 1 млрд 50 млн. 80% зараженных гельминтозами приходится на развивающиеся страны и страны со слабой экономикой 4.
Наиболее распространены следующие виды гельминтозов: лямблиоз, трихоцефалез, аскаридоз, анкилостомидоз, стронгилоидоз, трематодоз, цистицеркоз ЦНС, токсокароз. В детских коллективах инфицированность лямблиями составляет 40%, среди взрослых — 10%. Этот показатель находится на уровне развивающихся стран Африки 6.
В связи вышеизложенным для демонстрации взаимосвязи псориаза и наличия глистной инвазии, а именно лямблиоза приводим случай из практического опыта.
Больной К., 7 лет, поступил на стационарное лечение в отделение аллергодерматозов и наследственных заболеваний кожи НИКВИ с жалобами на высыпания, шелушение и умеренный зуд, беспокойный сон. Давность заболевания 2 года. Начало заболевания ни с чем не связывает. Первые высыпания появились на коже шеи и груди, затем процесс распространился на кожу туловища, плеч и предплечий, бедер и голеней. Сезонности в течение кожного процесса не прослеживается. Был обследован по месту жительства и выставлен диагноз: Вульгарный псориаз. Неоднократно получал адекватное лечение в амбулаторных условиях: антигистаминные, мембраностабилизирующие, десенсибилизирующие, дезинтоксикационные препараты, витаминотерапию, сорбенты, местное лечение (кератолитические, рассасывающие, различные кортикостероидные мази, в том числе). Эффект от амбулаторного лечения был незначительным и кратковременным. В связи, с неэффективностью амбулаторного лечения больной был направлен на госпитализацию в НИКВИ,
Из анамнеза жизни: Со слов матери у ребенка часто наблюдаются диспепсические расстройства в виде тошноты, кишечной колики и частых запоров. В то же время мама отмечает при рецидиве диспепсических расстройств обострение кожного процесса, что выражалось в появлении новых высыпаний, окраска сыпи становилась ярче, шелушении обильнее, увеличивалась интенсивность зуда.
При объективном осмотре общее состояние больного среднетяжелое. Сознание ясное, положение. Самочувствие страдает. Сон и аппетит нарушены. Телосложение больного правильное, астеническое. На момент осмотра со стороны органов и систем патологии не выявлено.
Локальный статус: кожный процесс хронический, распространенный, локализован на коже шеи, груди, туловища, плеч и предплечий, бедер и голеней. Сыпь обильная, симметричная, мономорфная, представлена лентикулярными, нумулярными папулами, ярко-розового цвета. Местами папулы имеют тенденцию к слиянию с образованием бляшек. На поверхности, которых отмечаются обильные серебристо-белые, мелко- и среднепластинчатые чешуйки. По всему кожному покрову отмечаются точечные и линейные экскориации, геморрагические корочки. Дермографизм розовый, стойкий. Волосы и ногти не поражены.
Данные лабораторного исследования: ОАК – эозинофилы 8, остальные параметры соответствуют физиологической норме. ОАМ – параметры в норме, Результаты исследования крови на РВ, ВИЧ-инфекцию и HbS-антиген – отрицательны. Биохимические параметры крови в пределах физиологической нормы. Результат иммунологического исследования: относительное содержание Т- и В-лимфоцитов в норме. Аутоиммунная реакция. Коррекция не показана.
В связи с наличием жалоб на диспепсические расстройства ребенок был проконсультирован гастроэнтерологом и назначена сдача кала на обнаружение яйца глистов. Результат 3-х кратного (с интервалом 1 неделя) анализа сдачи кала на обнаружение яйца глистов – положительный, выявлены цисты лямблий. Исследование антител к лямблиям в сыворотке крови методом ИФА (определение диагностического титра) дало положительный результат.
Больной проконсультирован инфекционистом, по назначению которого получал 3 цикла специфического антигельминтозного лечения в комплексе с энтеросорбентов и пробиотиков.
В результате комплексного лечения, направленного на стабилизацию кожного процесса (антигистаминные, десенсибилизирующие, дезинтоксикационные, седативные препараты, витаминотерапия, энтеросорбенты, энзимы, пробиотики и местная симптоматическая терапия), и специфической антигельминтозной терапии получен значительный положительный клинический эффект.
Больной был выписан с клиническим выздоровлением. Кожный процесс регрессировал полностью, при выписке имели место лишь остаточные явления в виде гиперпигментированных пятен на месте бывших элементов сыпи.
Контрольное 3 кратное исследование (с интервалом 1 неделя) кала на наличие цист лямблий дало отрицательный результат. Больному при выписке рекомендовано наблюдение дерматолога по месту жительства, диспансерное наблюдение врача кабинета инфекционных заболеваний (КИЗ) до одного месяца с 3-кратным контролем кала на обнаружение яйца глистов с интервалом в 7-10дней.
Таким образом, кишечные инвазии, паразитирующие у больных хроническими дерматозами, являются одним из тригеррных факторов воспалительного процесса, дестабилизации микроценоза кишечника и аутоинтоксикации. Существует корреляция между инвазией и тяжестью течения дерматоза, характеризующейся частотой и длительностью периодов обострений, а также выраженностью клинических проявлений.
На фоне постоянной эндогенной паразитирующей интоксикации отмечаются дисбаланс окислительно-антиоксидантной системы, клеточного, гуморального и цитокинового звеньев иммунной системы, а также системы фагоцитоза, которые являются важными механизмами развития хронических дерматозов.
Выявленные у больных хроническими дерматозами паразитарная инвазия и повышение патогенного потенциала участников микроценоза свидетельствует о необходимости включения в лечебные мероприятия, для повышения их эффективности патогенетически обоснованную терапию хронических дерматозов, антипаразитарных средств, энтеросорбентов и пре- и пробиотиков.
Случай из практики приводится с целью напомнить врачам дерматовенерологам о возможности поражения кожного покрова у больных, страдающих глистными инвазиями, которым комбинированное лечение (антигельминтное и лечение кожного процесса) обеспечивает клиническое выздоровление.
4. Бельмер С.В. Лямблиоз у детей // Русский медицинский журнал. 2004. -Т. 12, №3. — С. 141-143.
6. Генис Д.Е. Медицинская паразитология // М.: Медицина. 1991. -240 с.
8. Almeida M.M., Arede C., Marta C.S., Pinto P.L., Daniel I., Peres I., Nogueira J.A., Pinto J.R. Atopy and enteroparasites // Allergie et Immunologic. 2001. -Vol.30, N9. -P.291-294.
9. Arienti H. Prevalence of enteroparasites in a residence for children in the Cordoba Province, Argentina // Eur. J. Epidemiol. 2000. — Vol. 16. — P.287-293.
10. Buslau M., Menzel I., Holzmann H. Fungal flora of human faeces in psoriasis and atopic dermatitis. // Mycoses. 1990. — Vol.33(2). — P.90-94.
Кабулбекова А.А.
Кафедра дерматовенерологии и эстетической медицины ЦНО, КазНМУ
Читайте также:

