Какие амебы относятся к факультативным паразитам человека
Обновлено: 25.04.2024
Возбудитель
На сегодняшний день общая распространенность носительства токсоплазмы в мире оценивается в пределах 40-70%; иногда приводятся и более высокие проценты. Однако статистика обнаруживает выраженную региональную зависимость, что отчасти обусловлено неравномерностью распределения самой токсоплазмы в земной экосистеме (в Южной Корее, например, ее почти совсем нет, а в Южной Америке очень много – в некоторых областях заражено до 90% населения). Частота встречаемости в России оценивается на уровне 20%, то есть каждый пятый из нас является, как минимум, носителем.
В течение активного, острого периода течения токсоплазмоза (2-3 недели) больная кошка с фекалиями выделяет порядка двух миллиардов цист.
Жизнеспособность их сохраняется, в зависимости от условий, до двух и более лет.
Заражение
Кроме того, возможно внутриутробное трансплацентарное заражение от первично инфицированной матери. Обратим на это особое внимание.
Патогенез
Опасность для человека, симптоматика
Крайне важно отметить: доля инфицированных токсоплазмой людей, у которых развивается клинически значимый токсоплазмоз, очень мала – по разным оценкам, она варьирует от долей процента до нескольких процентов. Животные и птицы болеют токсоплазмозом гораздо чаще (см. ниже). Человек же практически всегда переносит токсоплазменную инвазию бессимптомно, поскольку иммунная система мгновенно распознает этот микроорганизм как враждебный – и реагирует настолько мощно, что инфицированный обычно даже не узнаёт о том, что был чем-то заражен. Кроме того, исключена опасность заразиться от инфицированного, даже если он переживает острый период токсоплазмоза (как правило, не подозревая об этом).
Таким образом, нет никаких оснований создавать лепрозории для носителей, повсеместно истреблять диких кошек и избавляться от кошек домашних, а ребенка выпускать на улицу лишь в скафандре высшей эпидемиологической защиты. Можно сказать, что мы, взрослые люди, если и были когда-то инфицированы, то эта проблема давным-давно решена, причем раз и навсегда: к токсоплазме вырабатывается устойчивый пожизненный иммунитет, и даже если человек попадает в незначительный процент переболевших в клинически значимой степени (лихорадка, легкое общее недомогание, мышечные боли, лимфаденопатия, спленогепатомегалия), то это уже не повторяется ни при каких обстоятельствах.
Как показано выше, токсоплазма способна проникать через плаценту в организм плода. Единственный вариант и единственное стечение обстоятельств, при которых это представляет реальную угрозу, – первичное инфицирование токсоплазмой в период беременности, т.е. первое в жизни заражение женщины, у которой ранее не было иммунитета к возбудителю. В этом случае действуют следующие статистические риски и клинические закономерности.
Чем больше срок беременности, тем выше проницаемость плаценты и вероятность инфицирования плода: в зависимости от триместра, этот риск оценивается как 15%, 25% и 70%.
Если внутриутробное заражение все же произошло, то тяжесть последствий для плода тем больше, чем меньше срок беременности. Вероятности того, что внутриутробный токсоплазмоз в дальнейшем ничем себя не проявит, – не существует. Надеяться на то, что произойдет уникальное чудо и последствий удастся избежать, к несчастью, не приходится даже в том случае, когда инвазия сразу же диагностирована и подвергнута интенсивному квалифицированному лечению. На практике внутриутробный токсоплазмоз означает смерть плода со спонтанным абортом, рождение с гидро- либо микроцефалией, или же развитие, в дальнейшем, тяжелейших поражений центральной нервной, зрительной и других систем организма. Интеллектуальная недостаточность характеризуется глубокой степенью выраженности.
В подобной ситуации, – когда происходит первичное заражение беременной женщины, – приходится ставить вопрос об искусственном прерывании беременности.
На последующие беременности вышеописанные риски не распространяется: речь, повторим, идет лишь о ситуациях, когда первичная инвазия токсоплазмы приходится на гестационный период.
Частота врожденного токсоплазмоза на сегодняшний день варьирует в пределах от 1:1000 до 1:10000 новорожденных.
Диагностика
Стандартом диагностики токсоплазмоза, в том числе на этапе внутриутробного развития, является серологическое исследование: реакция непрямой флюоресценции или ИФА (иммуноферментный анализ). Дополнительно назначают УЗИ и другие исследования по показаниям.
Лечение
Профилактика
Учитывая вышесказанное, женщине при планировании или наступлении беременности чрезвычайно важно пройти все назначенные обследования, ни в коем случае не игнорируя какие бы то ни было анализы и процедуры. Если обнаружено отсутствие иммунитета к токсоплазме, или же имеет место выраженный иммунодефицит, необходимо принимать все меры предосторожности, особенно при наличии в доме кошки: животное не должно гулять на улице и питаться сырым мясом. Санитарную обработку туалетного лотка следует производить регулярно, и лучше бы к нему не прикасаться человеку, для которого токсоплазма представляет опасность. Кошку желательно обследовать в ветеринарной клинике и, если выявлен паразитоз, качественно пролечить. Возможно, наилучшим решением является, – как бы тяжело это ни было для большинства семей, – расстаться с домашним питомцем, по крайней мере временно, на период вынашивания беременности.
Овощи и фрукты необходимо тщательно отмывать; любые мясные продукты должны проходить достаточную термическую обработку, а столы и доски, на которых разделывается мясо, – очищаться с применением моющих средств. Все гигиенические процедуры, особенно после любого контакта с землей, овощами, фруктами, ягодами и т.д., лица из группы риска должны выполнять сразу же, с мылом, самым тщательным образом.
Странное дело: о мире простейших практически невозможно рассказать в двух словах – писать приходится много. Вопреки своему названию, эти микроорганизмы весьма сложны, разнообразны, неисчерпаемо интересны, а порой уникальны.
Некоторые смертельно опасны.
Но дело даже не в миграционных потоках. Сам мир изменился, став совсем маленьким, тесным и круглым. Расстояний больше нет. Приходится узнавать о болезнях, которые раньше не всякому-то специалисту были известны, и читать о возбудителях этих инфекций, уповая на всемогущество антибиотиков да на собственный иммунитет.
Иммунитет у Homo Sapiens хоть и силен, да не абсолютен; к тому же подрываем мы его сами, подрываем на каждом шагу, прекрасно зная, – чем. Жизнь у нас такая, и такая уж у нас цивилизация…
В подцарство простейших (protozoa) выделены одноклеточные эукариоты, т.е. микроорганизмы, имеющие в строении одно или несколько клеточных ядер. Этим они отличаются от бактерий (прокариотов, доядерных и безъядерных одноклеточных) и от вирусов, которые являются неклеточной формой органики (если считать органикой упакованные сгустки рибонуклеиновых молекул).
Большинство простейших отличается также:
- сложным многофазным жизненным циклом;
- способностью размножаться как бесполым делением с рекомбинацией ДНК (подобно бактериям), так и более совершенным, с генетической точки зрения, гаметогенезом (с образованием предзародышевых половых клеток-гамет);
- наличием органоидов (ложноножки-псевдоподии, жгутики, цитостомы, реснички, мембраны и т.д.);
- гетеротрофным питанием (могут паразитировать в макроорганизме, поглощая его клетки; или питаются детритными, разлагающимися органическими массами, т.е. ведут сапротрофный образ жизни; либо же охотятся и пожирают другие микроорганизмы);
- способностью как к одиночному, так и колониальному существованию;
- размерами (эта характеристика широко варьирует у всех мельчайших, но в среднем протозоа в тысячи раз больше вирусов и на порядок больше бактерий; некоторые простейшие видны невооруженным глазом, достигая нескольких миллиметров в размерах, а отдельные гигантские многоядерные виды вырастают до 10-15 см, оставаясь при этом одноклеточными и соответствуя всем критериям протозойного подцарства).
Впадать в тоскливо-обреченный ужас, конечно, не стоит. Все-таки Homo Sapiens неизмеримо сложнее (в этом его слабость), изобретательнее и умнее – в этом сила. Знать, понимать, соблюдать разумную осторожность и принимать адекватные меры – необходимо. Ниже перечислены и очень кратко описаны лишь самые распространенные протозойные паразитозы. Большинству из них на сайте Лахта Клиники посвящены также отдельные статьи; остальные заболевания этой категории, если понадобится, подробно рассмотрим в будущем.
Малярия, она же болотная лихорадка. Исторически первое заболевание, в отношении которого была установлена протозойная этиология. По уровню летальности занимает пятое место среди всех инфекционных болезней и первое место среди паразитарных (от малярии погибает примерно три миллиона человек в год). Вызывается плазмодиями класса Sporozoa; на сегодняшний день патогенность обнаружена у пяти видов из более чем двухсот.
Распространяется промежуточными хозяевами, – комарами-анофелесами; передается также через зараженный шприц, при переливании крови и трансплацентарно (плоду от инфицированной матери). Помимо собственно лихорадки, приводит к тяжелым, жизнеугрожающим полиорганным осложнениям. Иммунитет вырабатывается лишь частично. Вакцины и средства профилактики в настоящее время находятся на стадии разработки, лабораторных экспериментов и клинических испытаний.
Амебиаз. Вызывается несколькими видами внутритканных паразитов рода амеб. Встречается в тяжелых церебральных, легочных, печеночных, кожных и других клинических формах, однако наиболее распространенным является кишечный амебиаз (амебная дизентерия, амебный колит), вызываемый Entamoeba histolytica. Второе по летальности протозойное заболевание. Распространяется фекально-оральным путем, через зараженную воду и немытые руки. Иммунитет к амебным инвазиям не формируется. Инфицировано не менее полумиллиарда человек, у каждого десятого из заражаемых развивается клинически значимая симптоматика.
Токсоплазмоз. Вызывается единственным известным на сегодняшний день представителем рода токсоплазмы – Toxoplasma Gondii, мелким внутриклеточным паразитом. Окончательный хозяин, в организме которого токсоплазма размножается гаметогенезом и образует способные к активизации цисты, – семейство кошачьих. Человечество как один из промежуточных носителей инфицировано на 40-70%. Подавляющее большинство случаев острого токсоплазмоза протекает бессимптомно, с формированием стойкого пожизненного иммунитета. Вместе с тем, для лиц с выраженным иммунодефицитом токсоплазма смертельно опасна. Кроме того, при первичном заражении беременной женщины инфицируется и плод: в этом случае со стопроцентной вероятностью нарушается внутриутробное развитие, что приводит к тяжелейшим поражениям центральной нервной и других систем организма, – либо врожденным, либо проявляющимся в детском возрасте. Даже в случае своевременной диагностики на этапе гестации – лечение малоэффективно.
Трихомониаз. Вызывается видом Trichomonas vaginalis, урогенитальным паразитом из рода трихомонад класса жгутиковых. Реальная распространенность неизвестна, оценивается на уровне трехсот миллионов человек, однако с учетом пассивного носительства мужчинами доля инфицированных, по-видимому, гораздо больше. Передается половым путем или от беременной матери к плоду. Является наиболее частым ЗППП в мире, при этом наиболее контагиозным и наиболее вирулентным. Чаще всего обнаруживается в составе комбинированных инфекций, потенцирует патогенность папилломавируса и других вирусных инвазий. При хронизации и длительном течении вызывает ряд тяжелых осложнений со стороны репродуктивной системы. Повышает риск рака шейки матки, преждевременных родов и, даже если роды происходят в срок, дефицита массы тела у новорожденного.
Условным патогеном является также кишечная трихомонада, способная при определенных условиях вызывать соответствующую симптоматику.
Лямблиоз (гиардоз, жиардоз). Вызывается кишечным паразитом Giardia intestinalis из класса жгутиковых. Распространяется преимущественно фекально-оральным путем, а также бытовым и через воду, в том числе водопроводную (поскольку возбудитель устойчив к хлору). Инфицирована, как минимум, треть человечества, в большинстве бессимптомно или малосимптомно. Иммунитет не вырабатывается. Лямблии (жиардии) колонизируют тонкий кишечник, вызывая клинику гастроэнтерита, астенический синдром, снижение массы тела. Способы паразитирования изучены не полностью, равно как не до конца прояснены этиопатогенетические механизмы: способность вызывать осложнения в желчевыводящих путях опровергнута, риск осложнений со стороны кожи, иммунной системы и т.д. в настоящее время изучается и обсуждается.
Бабезиоз (бабезиеллёз). Вызывается внутриклеточным паразитом Babesia из отряда пироплазмид (в той или иной степени патогенны более 100 видов). Клинически проявляется лихорадочным симптомокомплексом, нарушениями состава крови, поражением печени. Инфицируется, в основном, крупный рогатый скот, однако во второй половине ХХ века стали регистрироваться случаи заболевания у человека. Точная распространенность неизвестна, этиопатогенез изучен недостаточно. Распространяется через укусы клещей.
Лейшманиоз. Эндемичное (регионально-зависимое) протозойное заболевание, распространенное в тропиках и субтропиках. Вызывается более чем 20 видами внутриклеточного паразита Leishmania, передается, в основном, через укусы москитов. Инфицировано не менее 12 млн человек. Встречается в кожной, кожно-слизистой и висцеральной (поражение внутренних органов) формах; при осложненном хроническом или тяжелом остром течении заболевание результирует фатально.
Амебиаз – паразитарное заболевание, вызываемое гистолитической амебой и протекающее с кишечными и внекишечными проявлениями. Кишечный амебиаз характеризуется обильным слизистым стулом с примесью крови, болью в животе, тенезмами, похуданием, анемией; внекишечный – формированием абсцессов печени, легких, головного мозга и пр. Диагноз амебиаза основан на данных клинической картины, ректороманоскопии, колоноскопии, микроскопии мазков содержимого абсцессов, серологического исследования, рентгенографии. В лечении амебиаза применяются медикаментозные средства (просветные и системные тканевые амебоциды, антибиотики), хирургические методы (вскрытие и дренирование абсцессов, резекция кишки).
МКБ-10
Общие сведения
Амебиаз – протозойная инфекция, проявляющаяся язвенным процессом в толстом кишечнике и поражением внутренних органов с образованием абсцессов. Амебиаз наиболее широко распространен в регионах с тропическим и субтропическим климатом; по уровню смертности среди паразитарных инфекций он занимает второе место в мире после малярии. В последние годы в связи со значительным ростом миграции и зарубежного туризма увеличилось число завозных случаев амебиаза в России. Амебиаз регистрируется в виде спорадических случаев, эпидемические вспышки редки. Амебиазом преимущественно поражаются пациенты среднего возраста.

Причины амебиаза
Возбудитель амебиаза - гистолитическая амеба (Entamoeba histolytica) относится к патогенным простейшим и имеет две стадии жизненного цикла: стадию покоя (цисту) и вегетативную (трофозоит), сменяющие друг друга в зависимости от условий существования. Вегетативные формы амебы (предцистная, просветная, большая вегетативная и тканевая) очень чувствительны к изменению температуры, влажности, рН, поэтому быстро погибают во внешней среде. Цисты проявляют значительную устойчивость вне организма человека (в почве сохраняются до 1 месяца, в воде - до 8 месяцев).
Зрелые цисты, попав в нижние отделы ЖКТ, трансформируются в непатогенную просветную форму, обитающую в просвете толстой кишки, питающуюся детритом и бактериями. Это стадия бессимптомного носительства амеб. В дальнейшем просветная форма либо инцистируется, либо превращается в большую вегетативную форму, которая за счет наличия протеолитических ферментов и специфических протеинов внедряется в эпителий кишечной стенки, переходя в тканевую форму. Большая вегетативная и тканевая формы патогенны, обнаруживаются при остром амебиазе. Тканевая форма паразитирует в слизистом и подслизистом слоях стенки толстой кишки, вызывая разрушение эпителия, нарушение микроциркуляции, образование микроабсцессов с дальнейшим некрозом тканей и множественными язвенными поражениями. Патологический процесс в кишечнике при амебиазе распространяется чаще всего на слепую и восходящую части толстой кишки, реже на сигмовидную и прямую кишку. Гистолитические амебы в результате гематогенной диссеминации способны попадать в печень, легкие, головной мозг, почки, поджелудочную железу с образованием в них абсцессов.
Основной источник заражения амебой - больные хронической формой амебиаза в период ремиссии, а также реконвалесценты и носители цист. Переносчиками цист амеб могут быть мухи. Пациенты с острой формой или с рецидивом хронического амебиаза не представляют эпидемической опасности, так как выделяют нестойкие во внешней среде вегетативные формы амеб. Заражение происходит фекально-оральным путем при попадании в ЖКТ здорового человека инфицированных зрелыми цистами пищевых продуктов и воды, а также бытовым путем через загрязненные руки. Кроме этого, возможна передача амебиаза при анальных половых сношениях, главным образом, среди гомосексуалистов.
Факторами риска заражения амебиазом служат несоблюдение личной гигиены, низкий социально-экономический статус, проживание в районах с жарким климатом. Развитие амебиаза может быть спровоцировано иммунодефицитным состоянием, дисбактериозом, несбалансированным питанием, стрессом.
Симптомы амебиаза
Инкубационный период амебиаза продолжается от 1 недели до 3-х месяцев (обычно 3-6 недель). По выраженности симптомов амебиаз может быть бессимптомным (до 90% случаев) или манифестным; по длительности заболевания - острым и хроническим (непрерывным или рецидивирующим); по тяжести течения - легким, средней тяжести, тяжелым. В зависимости от клинической картины выделяют 2 формы амебиаза: кишечную и внекишечную (амебные абсцессы печени, легких, мозга; мочеполовой и кожный амебиаз). Амебиаз может проявляться в виде микст-инфекции с другими протозойными или бактериальными кишечными инфекциями (например, дизентерией), гельминтозами.
Кишечный амебиаз является основной, наиболее распространенной формой заболевания. Ведущим симптомом кишечного амебиаза становится диарея. Стул обильный, жидкий, сначала калового характера с примесью слизи до 5-6 раз в сутки; затем испражнения приобретают вид желеобразной массы с примесью крови, а частота дефекации увеличивается до 10-20 раз в сутки. Характерны постоянные нарастающие боли в животе, в подвздошной области, больше справа. При поражении прямой кишки беспокоят мучительные тенезмы, при поражении червеобразного отростка – возникают симптомы аппендицита. Может отмечаться умеренное повышение температуры, астеновегетативный синдром. Острота процесса при кишечном амебиазе стихает через 4-6 недель, после чего наступает продолжительная ремиссия (несколько недель или месяцев).
Самопроизвольное выздоровление происходит крайне редко. Без лечения вновь развивается обострение, и кишечный амебиаз приобретает хроническое рецидивирующее или непрерывное течение (длительностью до 10 и более лет). Хронический кишечный амебиаз сопровождается расстройствами всех видов обмена: гиповитаминозом, истощением, вплоть до кахексии, отеками, гипохромной анемией, эндокринопатиями. У ослабленных больных, детей раннего возраста и беременных может развиться молниеносная форма кишечного амебиаза с обширными изъязвлениями толстой кишки, токсическим синдромом и летальным исходом.
Из внекишечных проявлений амебиаза наиболее частым является амебный абсцесс печени. Для него характерны одиночные или множественные гнойники без пиогенной оболочки, локализующиеся чаще всего в правой доле печени. Заболевание начинается остро - с озноба, гектической лихорадки, обильного потоотделения, болей в правом подреберье, усиливающихся при кашле, перемене положения тела. Состояние больных тяжелое, печень резко увеличена и болезненна, кожные покровы землистого оттенка, иногда развивается желтуха. Амебиаз легких протекает в виде плевропневмонии или абсцесса легкого с лихорадкой, болью в грудной клетке, кашлем, кровохарканьем. При амебном абсцессе головного мозга (амебном менингоэнцефалите) наблюдается очаговая и общемозговая неврологическая симптоматика, выраженная интоксикация. Кожный амебиаз возникает вторично у ослабленных больных, проявляется образованием малоболезненных эрозий и язв с неприятным запахом в перианальной области, на ягодицах, в зоне промежности, на животе, вокруг свищевых отверстий и послеоперационных ран.
Кишечный амебиаз может протекать с различными осложнениями: перфорацией кишечной язвы, кровотечением, некротическим колитом, амебным аппендицитом, гнойным перитонитом, стриктурой кишки. При внекишечной локализации не исключается прорыв абсцесса в окружающие ткани с развитием гнойного перитонита, эмпиемы плевры, перикардита или формированием свищей. При хроническом амебиазе в стенке кишки вокруг язвы формируется специфическое опухолевидное образование из грануляционной ткани – амебома, приводящая к обтурационной кишечной непроходимости.
Диагностика амебиаза
При диагностике кишечного амебиаза учитываются клинические признаки, эпидемиологические данные, результаты серологических исследований (РНГА, РИФ, ИФА), ректороманоскопии и колоноскопии. Эндоскопически при амебиазе обнаруживаются характерные язвы слизистой оболочки кишечника на разных стадиях развития, при хронических формах - рубцовые стриктуры толстой кишки. Лабораторным подтверждением кишечного амебиаза служит выявление тканевой и большой вегетативной форм амебы в испражнениях больного и отделяемом дна язв. Присутствие цист, просветных и прецистных форм возбудителя свидетельствует об амебном носительстве. Серологические реакции показывают наличие специфических антител в сыворотке крови больных амебиазом.
Внекишечные амебные абсцессы помогает визуализировать комплексное инструментальное обследование, включающее УЗИ органов брюшной полости, радиоизотопное сканирование, обзорную рентгенографию грудной клетки, КТ головного мозга, лапароскопию. Обнаружение в содержимом абсцессов патогенных форм возбудителя является доказательством его амебного происхождения. Дифференциальную диагностику амебиаза проводят с дизентерией, кампилобактериозом, балантидиазом, шистосомозом, болезнью Крона, неспецифическим язвенным колитом, псевдомембранозным колитом, новообразованиями толстой кишки; у женщин – с эндометриозом толстой кишки. Амебные абсцессы внекишечной локализации дифференцируют от абсцессов другой этиологии (эхинококкоза, лейшманиоза, туберкулеза).
Лечение амебиаза
Лечение амебиаза проводится амбулаторно, госпитализация необходима при тяжелом течении и внекишечных проявлениях. Для лечения бессимптомного носительства и профилактики рецидивов применяются просветные амебоциды прямого действия (этофамид, дилоксанида фуроат, препараты йода, мономицин). В терапии кишечного амебиаза и абсцессов различной локализации эффективны системные тканевые амебоциды (метронидазол, тинидазол, орнидазол). Для купирования колитического синдрома, ускорения репаративных процессов и элиминации патогенных форм амеб назначают йодхлороксихинолин. При непереносимости метронидазола показано использование антибиотиков (доксициклина, эритромицина). Сочетание препаратов, их дозы и длительность терапии определяется формой и тяжестью заболевания.
В отсутствие эффекта от консервативной тактики и угрозе прорыва абсцесса может потребоваться хирургическое вмешательство. При мелких амебных абсцессах возможно проведение пункции под контролем УЗИ с аспирацией содержимого или вскрытие с дренированием абсцесса и последующим введением в его полость антибактериальных и амебоцидных препаратов. При выраженных некротических изменениях вокруг амебной язвы или кишечной непроходимости выполняют резекцию кишки с наложением колостомы.
Прогноз и профилактика амебиаза
При своевременном специфическом лечении в большинстве случаев прогноз кишечного амебиаза благоприятный. В случае поздней диагностики амебных абсцессов других органов имеется риск летального исхода. Профилактика амебиаза включает раннее выявление и полноценное лечение больных и амебоносителей, соблюдение санитарно-гигиенического режима в быту, обеспечение качественного водоснабжения и очистки сточных вод, контроль безопасности пищевых продуктов, санитарное просвещение.
В 1965 г. в Австралии впервые были выявлены случаи заболеваний, вызываемых свободноживущими почвенными амебами, и с тех пор они регистрируются во многих странах. В большинстве случаев эти заболевания диагностируются только после смерти больных на основе гистологического исследования тканей, в которых обнаруживаются эти простейшие.
Крайняя тяжесть заболеваний, вызываемых этими амебами, объясняется тем, что паразитический образ жизни для них не является обязательным. Поэтому как у амеб, так и у человека на протяжении эволюции не возникло взаимных адаптации, в связи с чем система паразит — хозяин не является устойчивой.
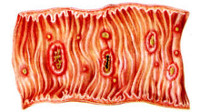
Среди амеб этой группы наиболее известны представители родов Naegieria и Acanthamoeba (рис. 19.12).

Рис. 19.12. Факультативные паразиты человека. А — Naegieria sp.; Б — Acanthamoeba sp.:
1, 2 — вегетативные стадии, 3 — цисты
Амебы р. Naegieria в организм человека попадают при купании в грязной воде через носовую полость и проникают в мозговые оболочки. Здесь амебы размножаются и вызывают острый менингоэнцефалит, который почти всегда заканчивается смертью. Наиболее часто поражаются дети.
Амебы р. Acanthamoeba образуют устойчивые цисты, которые попадают в организм человека не только через носоглотку и пищеварительную систему, но и при вдыхании, а также через травмированную кожу и роговицу. Заболевание проявляется по-разному в зависимости от путей попадания возбудителя в организм. Характерным является образование гранулем, содержащих амеб. У ослабленных больных и детей заболевание заканчивается менингоэнцефалитом и смертью.
Глава 20 медицинская гельминтология
Медицинская гельминтология изучает паразитов человека из группы червей. Черви— это многоклеточные, трехслойные, первичноротые, двусторонне-симметричные животные. Их тело имеет удлиненную форму, а кожно-мускульный мешок состоит из гладких или поперечно-полосатых мышц и покровных тканей.
Черви — паразиты человека, относятся к типам Плоские и Круглые черви. Заболевания, вызываемые гельминтами, называют гельминтозами. В большинстве случаев при одноразовой инвазии нарастания численности гельминтов в организме хозяина не. происходит: для успешного протекания циклов их развития необходима смена сред обитания. Из этого следует, что продолжительность заболевания часто определяется продолжительностью жизни паразита и колеблется от нескольких недель при энтеробиозе до нескольких десятков лет при шистосоматозах. Тяжесть заболевания зависит от количества паразитов, попавших в организм хозяина, и его индивидуальной чувствительности.
Гельминты могут обитать у человека практически во всех органах. В соответствии с этим различны пути проникновения их в организм человека, симптоматика заболеваний и методы диагностики.
На протяжении длительной эволюции при переходе к паразитизму у гельминтов возникли не только признаки общей дегенерации и адаптации к паразитическому образу жизни общего значения (особые покровы, мощная половая система), но и конкретные приспособления к обитанию в определенных органах. Хозяева, в свою очередь, приобрели соответствующие адаптации, обеспечивающие стабильное существование системы хозяин — паразит. Однако во многих случаях для попадания в определенный орган гельминты осуществляют миграцию по кровеносным сосудам или непосредственно через ткани и могут попасть в другие органы. Тогда говорят об атипичной, или эктопической, локализации. Заболевание при этом протекает тяжелее, диагностируется с трудом и часто может заканчиваться гибелью одного из компонентов системы: паразита или хозяина. Сказанное в полной мере относится и к видовой специфичности системы паразит — хозяин: гельминты, адаптированные только к человеческому организму, обусловливают более легкое течение заболевания у него, чем специфические паразиты животных, попадающие к человеку случайно.
Читайте также:

